行政院國家科學委員會補助專題研究計畫成果報告
※※※※※※※※※※※※※※※※※※※※※※※※※
※ ※
※ 二氧化鈦觸媒光催化還原二氧化碳 ※
※
※
※※※※※※※※※※※※※※※※※※※※※※※※※
計畫類別:V個別型計畫 □整合型計畫
計畫編號:NSC90-2214-E-002-038
執行期間:90年 8月 1日至 91年 7月 31日
計畫主持人:吳紀聖
共同主持人:
本成果報告包括以下應繳交之附件:
□赴國外出差或研習心得報告一份
□赴大陸地區出差或研習心得報告一份
□出席國際學術會議心得報告及發表之論文各一份
□國際合作研究計畫國外研究報告書一份
執行單位:台灣大學化學工程研究所
中
華
民
國 91年 8月 29日
二氧化鈦觸媒光催化還原二氧化碳
Photocatalytic Reduction of Carbon Dioxide Using Titania Catalysts
計畫編號:NSC90-2214-E-002-038
執行期限:90年8月1日至91年7月31日
主持人:吳紀聖 台灣大學化學工程研究所
計畫參與人員:周欣穎 曾怡享 台灣大學化學工程研究所
一、中文捎耍 本研究的主要目的為以光觸媒催化反應還原 二氧化碳,達到二氧化碳減量的效果,並嘗 試利用長波之紫外光 (365nm),希望能達到 有效利用光源的目的。 關鍵詞:光催化,二氧化碳,Cu/TiO2,, Ag/TiO2 Abstr actThe objective of the project is to investigate the photocatalytic reduction of CO2 using TiO2
photocatalyst. The wavelength of UV source (365 nm) was applied so that we could utilize the solar energy to decrease the CO2
concentration in the atmosphere.
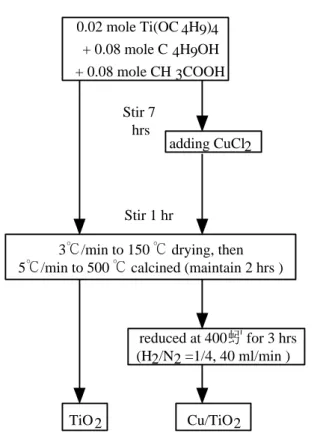
Keywords: Photocatalysis, carbon dioxide, Cu/TiO2, Ag/TiO2 二、緣由與目的 以光觸媒用光誘導的方式還原二氧化碳是這 個世紀開始的新興研究。採用不同的觸媒、 溶劑、製備觸媒的溫度、觸媒含金屬量的多 寡,粒子大小等… 皆會影響二氧化碳還原的 效率及產物種類。到目前為止,我們了解在 間、觸媒製備的方法、不同波長的光源… 等,以期能得到最佳的產率並進而了解反應 機制。 Fig. 1 簡示觸媒製備。觸媒製備過程為加入 Ti(OC4H9)4、n-C4H9OH、CH3COOH、CuCl2
或Cu(CH3COO)2、AgNO3為前驅物,採改良
式溶凝膠法並經150℃乾燥、500℃煆燒,製 備出一系列不同之Cu/TiO2觸媒及Ag/TiO2觸 媒;再利用UV光源(波長=254nm或365nm) 進行二氧化碳飽和水溶液之光催化還原反 應,產物分析得甲醇及微量之溶氧[1]。 進行實驗時,先以超高純度99.9999v% 的二 氧化碳通入含氫氧化鈉之光觸媒懸浮水溶液 中,待二氧化碳飽和後,再以紫外光照射以 進行二氧化碳 之光還原反應,最後 以GC-FID分析液相產物為甲醇,並且以溶氧偵測 器測得少量氧氣。 四、結果與討論 為探討進行二氧化碳光還原反應之最佳觸 媒,首先根據之前之實驗結果[1]發現,銅含 量2%的Cu/TiO2觸媒有最佳之反應結果,因 此 本 實 驗 之 觸 媒 皆 製 備 銅 含 量 為 2% 之 Cu/TiO2觸媒,單純就不同之Cu前驅物及前 驅物加入時間不同所製備觸媒進行反應結果 之比較,實驗結果發現,在零小時即加入前
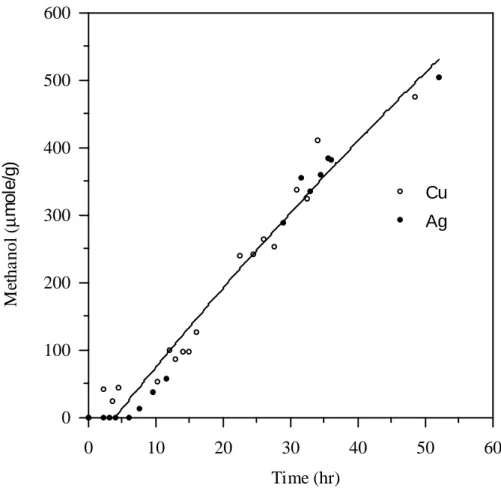
展,本研究亦選擇長波(λ=365nm)之紫 外燈管進行光還原二氧化碳反應,結果發 現,經由長波紫外燈照射之反應產量明顯比 短波紫外燈照射之反應產量減少許多;在短 波紫外光照射下,2%Cu/TiO2與2%Ag/TiO2 之反應結果趨勢幾近一致,兩者在50小時之 產量約達500μmole/g,如Fig. 4所示。 但在長波紫外光照射下,Cu/TiO2在50小時 之產量約達35μmole/g,Ag/TiO2的產量約 只有20μmole/g,如Fig. 5所示,推測可能因 為 Ag 之 螢 光 光 譜 所 對 應 的 激 發 波 長 (220nm)[2]較Cu之螢光光譜所對應的激發 波長(270-300nm)短[3],故Cu/TiO2在長波 紫外光照射下之反應結果較Ag/TiO2之反應 結果好。 五、參考文獻
1. I-H. Tseng, W.-C. Chang, J. C.-S. Wu,
Applied Catalysis B 37, 37 (2002)
2. M. Anpo, S. Zhang, H. Moshima, M. Matsuoka and H.Yamashita, Catalysis Today, 39, 159 (1997).
3. M. Anpo, M. Matsuoka, K. Hanou, H. Mishima and H. Yamashita, Coordination Chemistry Reviews, 171, 175 (1998). 0.02 mole Ti(OC 4H9)4 + 0.08 mole C 4H9OH + 0.08 mole CH 3COOH Stir 7 hrs adding CuCl2 Stir 1 hr
3℃/min to 150 ℃ drying, then 5℃/min to 500 ℃ calcined (maintain 2 hrs )
reduced at 400蚓 for 3 hrs (H2/N2 =1/4, 40 ml/min )
TiO 2 Cu/TiO2
0 10 20 30 40 0 200 400 600 800 Time (hr) M et h an o l ( µm o le /g ) CuCl2 (8 hrs) Cu(CH3COO)2 (0 hr) CuCl2 (0 hr) Cu(CH3COO)2 (8 hrs) P-25 Figure 2: 銅前驅物種類及加入時間對反應之影響 8 12 16 20 io n R a te ( µm o le /g -c at -h r)
0 10 20 30 40 50 60 0 100 200 300 400 500 600 Time (hr) M et h a n o l ( µ m o le /g ) Cu Ag
Figure 4: 在254nm紫外燈照射下之2%Cu/TiO2與2%Ag/TiO2觸媒反應之比較
0 10 20 30 40 50 0 10 20 30 40 50 Time (hr) M et h a n ol ( µm o le /g ) Cu Ag P25