天麻錠劑之配方研究; Formulation study of Gastrodia Rhizoma tablets
全文
(2) 目錄 目錄...................................................................................................................Ⅰ. 附圖目錄……………………………………………………………………...Ⅴ. 附表目錄……………………………………………………………………...Ⅶ. 英文摘要…………………………………………………………………….ⅩⅢ. 中文摘要…………………………………………………………………….ⅩⅣ. 內文目錄 第一章 緒言…………………………………………………………………...1 第二章 總論……………………………………………………………….......4 第一節 中藥劑型的現代化………………………………………………….4 第二節 天麻的化學成分…………………………………………………….5 第三節 天麻的藥理研究…………………………………………………….8 第四節 天麻素的定量分析方法…………………………………………...11 第五節 中藥錠劑的製劑設計……………………………………………...14 第六節 中藥的抽提技術…………………………………………………...17 第七節 中藥產品的乾燥理論與技術……………………………………...19 第八節 中藥製劑的安定性………………………………………………...22 第九節 研究動機與目的…………………………………………………...23 第三章 實驗藥材及研究方法……………………………………………….25 第一節 實驗藥材…………………………………………………………...25 一、藥材……………………………………………………………….25 I.
(3) 二、藥品及試劑……………………………………………………….25 三、儀器及材料……………………………………………………….25 四、溶液及賦型劑製備………………………………………………27 第二節 研究方法…………………………………………………………...29 一、天麻成分之基本理化性質分析…………………………………29 (一)實驗條件波長之選擇………………………………………..29 (二)不同波長下紫外光譜分析…………………………………..29 (三)標準溶液檢量線之製作……………………………………..29 (四)不同 pH 值下紫外光譜分析…………………………………29 (五)賦型劑對紫外光譜分析之影響……………………………..30 (六)標準溶液安定性試驗………………………………………..30 二、天麻藥材乾粉、天麻濃縮液和天麻浸膏之含量測定…………….30 三、天麻浸膏顆粒之製備……………………………………………31 四、天麻浸膏顆粒之物性測定………………………………………33 (一)安息角 (angle of repose) 之測定………………………….33 (二)顆粒密度 (particle density) 之測定……………………….33 (三)顆粒粒徑 (particle size distribution) 之測定……………34 (四)顆粒吸收水分(moisture sorption) 之測定……………….34 (五)含水量 (moisture content) 之測定…………………….......35 五、天麻浸膏錠劑之製備……………………………………………35 六、天麻浸膏錠劑的物性測定………………………………………35 (一)硬度試驗 (Hardness test)…………………………………..36 (二)厚度試驗 (Thickness test)………………………………….36 (三)重量差異試驗 (Weight variation test)……………………..36 (四)含量均一度試驗 (Content uniformity test)………………..36 (五)脆度試驗 (Friability test)…………………………………..37 (六)崩散度試驗 (Disintegration test)…………………………..37. II.
(4) (七)溶離試驗 (Dissolution test)………………………………...37 (八)溶離度均一性試驗 (Dissolution uniformity test)…………40 (九)天麻濃縮液錠劑之安定性試驗(Stability test)……………..40 第四章 結果與討論………………………………………………………….41 第一節 天麻成分之基本理化性質分析…………………………………...41 一、實驗條件波長之選擇…………………………………………….41 二、不同波長下紫外光譜分析……………………………………….41 三、標準溶液檢量線之製作………………………………………….41 四、不同 pH 值下紫外光譜分析……………………………………..41 五、賦型劑紫外光譜分析之影響…………………………………….42 六、標準溶液安定性試驗…………………………………………….42 第二節 天麻藥材乾粉、天麻濃縮液和天麻浸膏的含量測定…………….43 第三節 天麻浸膏顆粒之製備……………………………………………...44 第四節 天麻浸膏顆粒之物性測定………………………………………...45 一、安息角 (angle of repose) 之測定………………………………..45 二、顆粒密度 (particle density) 之測定……………………………..45 三、顆粒粒徑 (particle size distribution) 之測定……………………46 四、顆粒吸收水分(moisture sorption) 之測定………………………46 五、含水量 (moisture content) 之測定……………………………….47 第五節 天麻浸膏錠劑的物性測定………………………………………...48 一、硬度試驗 (Hardness test)…………………………………………48 二、厚度試驗 (Thickness test)………………………………………..48 三、重量差異試驗 (Weight variation test)……………………………49 四、含量均一度試驗 (Content uniformity test)………………………49 五、脆度試驗 (Friability test)…………………………………………49 六、崩散度試驗 (Disintegration test)…………………………………49 七、溶離試驗 (Dissolution test)………………………………………50. III.
(5) 八、溶離度均一性試驗 (Dissolution uniformity test)……………….52 九、天麻浸膏錠劑之安定性試驗 (Stability test)…………………….53 第五章 結論………………………………………………………………….54 參考文獻…………………………………………………………………….154. IV.
(6) 附圖目錄 Figure 1. 天麻浸膏及錠劑製造流程圖…………………………………...56. Figure 2. 天麻素 (Gastrodin, GA) 紫外吸收光譜圖…………………….57. Figure 3. GA 標準溶液檢量線之製作……………………………………57. Figure 4. 空白溶液及內標乙醯胺酚 (Acetaminophen, ASA) 之 HPLC 圖. …………………………………………………………….....58. Figure 5. 空白溶液中之 GA、天麻苷元 (p-Hydroxybenzyl alcohol, HBA) 及內標 ASA 之 HPLC 圖……………………………………….58. Figure 6. 天麻浸膏之 GA、HBA 及內標 ASA 之 HPLC 圖…………….58. Figure 7. 配方 R1 之 GA、HBA 及內標 ASA 之 HPLC 圖………………59. Figure 8. 配方 R2 之 GA、HBA 及內標 ASA 之 HPLC 圖………………59. Figure 9. 配方 R3 之 GA、HBA 及內標 ASA 之 HPLC 圖………………59. Figure 10 配方 R4 之 GA、HBA 及內標 ASA 之 HPLC 圖………………59 Figure 11 配方 R5 之 GA、HBA 及內標 ASA 之 HPLC 圖………………59 Figure 12 配方 R6 之 GA、HBA 及內標 ASA 之 HPLC 圖………………59 Figure 13 配方 R7 之 GA、HBA 及內標 ASA 之 HPLC 圖………………60 Figure 14 配方 R8 之 GA、HBA 及內標 ASA 之 HPLC 圖………………60 Figure 15 配方 R9 之 GA、HBA 及內標 ASA 之 HPLC 圖………………60 Figure 16 配方 R10 之 GA、HBA 及內標 ASA 之 HPLC 圖………………60 Figure 17 配方 RA 之 GA、HBA 及內標 ASA 之 HPLC 圖………………60 Figure 18 配方 RB 之 GA、HBA 及內標 ASA 之 HPLC 圖………………60 Figure 19 配方 R1 顆粒的粒徑分佈……………………………………….61 Figure 20 配方 R2 顆粒的粒徑分佈……………………………………….61 Figure 21 配方 R3 顆粒的粒徑分佈……………………………………….61 Figure 22 配方 R4 顆粒的粒徑分佈……………………………………….61 Figure 23 配方 R5 顆粒的粒徑分佈……………………………………….61 Figure 24 配方 R6 顆粒的粒徑分佈……………………………………….61 V.
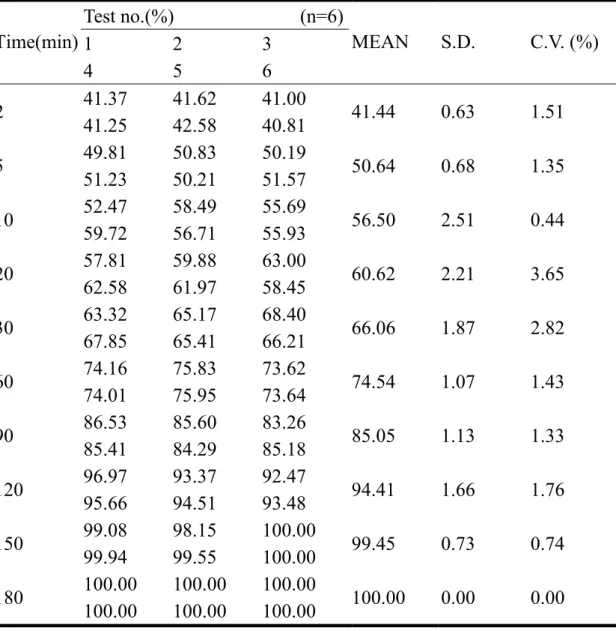
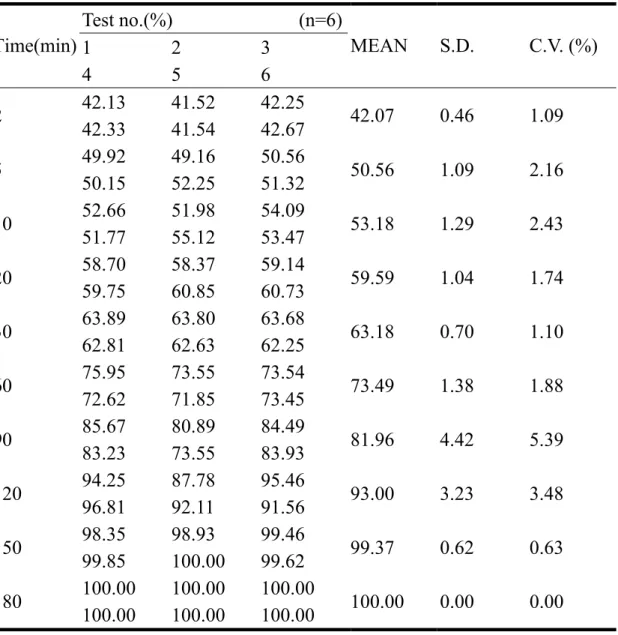
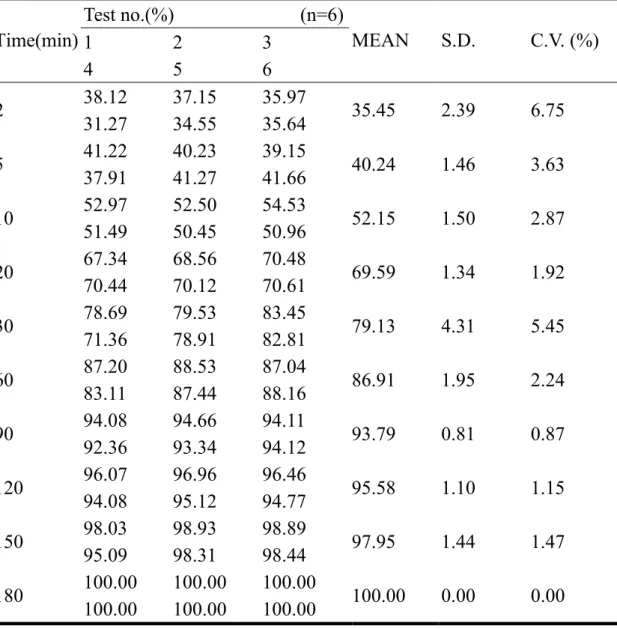
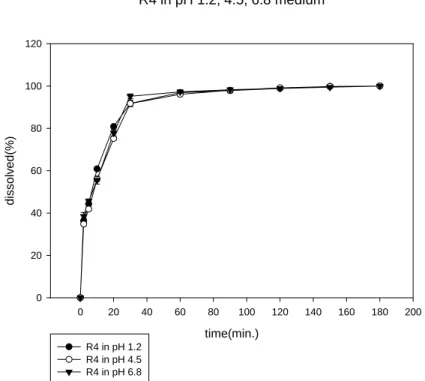
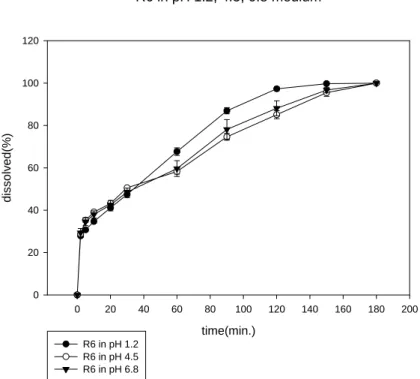
(7) Figure 25 配方 R7 顆粒的粒徑分佈……………………………………….62 Figure 26 配方 R8 顆粒的粒徑分佈……………………………………….62 Figure 27 配方 R9 顆粒的粒徑分佈………………………………………..62 Figure 28 配方 R10 顆粒的粒徑之分佈……………………………………62 Figure 29 配方 RA 顆粒的粒徑分佈……………………………………….62 Figure 30 配方 RB 顆粒的粒徑分佈……………………………………….62 Figure 31 配方 R1~R10 顆粒的粒徑分佈柱狀圖………………………….63 Figure 32 配方 R1~R10 顆粒的吸溼試驗…………………………………64 Figure 33 配方 R1~R10 含水量之測定…………………………………….64 Figure 34 配方 R1~R10 和 RA、RB 的錠劑成品外觀攝影………………65 Figure 35 dissolution profile of GA from R1 formulation in pH 1.2, 4.5 and 6.8 media……................................................................................66 Figure 36 dissolution profile of GA from R2 formulation in pH 1.2, 4.5 and 6.8 media……................................................................................66 Figure 37 dissolution profile of GA from R3 formulation in pH 1.2, 4.5 and 6.8 media………………………………………………………....67 Figure 38 dissolution profile of GA from R4 formulation in pH 1.2, 4.5 and 6.8 media……................................................................................67 Figure 39 dissolution profile of GA from R5 formulation in pH 1.2, 4.5 and 6.8 media………………………………………………………....68 Figure 40 dissolution profile of GA from R6 formulation in pH 1.2, 4.5 and 6.8 media………………………………………………………....68 Figure 41 dissolution profile of GA from R7 formulation in pH 1.2, 4.5 and 6.8 media………………………………………………………....69 Figure 42 dissolution profile of GA from R8 formulation in pH 1.2, 4.5 and 6.8 media………………………………………………………....69 Figure 43 dissolution profile of GA from R9 formulation in pH 1.2, 4.5 and. VI.
(8) 6.8 media………………………………………………………....70 Figure 44 dissolution profile of GA from R10 formulation in pH 1.2, 4.5 and 6.8 media………………………………………………………....70 Figure 45 dissolution profile of GA from R1 ~ R10 formulations in pH 1.2 media……………………………………………………………..71 Figure 46 dissolution profile of GA from R1 ~ R10 formulations in pH 4.5 media………………………………………………………….….72 Figure 47 dissolution profile of GA from R1 ~ R10 formulations in pH 6.8 media……………………………………………………………..73 Figure 48 dissolution profile of GA from RA and RB formulations in pH 1.2, 4.5 and 6.8 media………………………………………………...74 Figure 49 配方 R1~R10 加溫一個月安定性試驗………………………….75 Figure 50 配方 R1~R10 加溫二個月安定性試驗………………………….75 Figure 51 配方 R1~R10 加溫三個月安定性試驗………………………….76 Figure 52 配方 R1~R10 水中安定性試驗………………………………….76. VII.
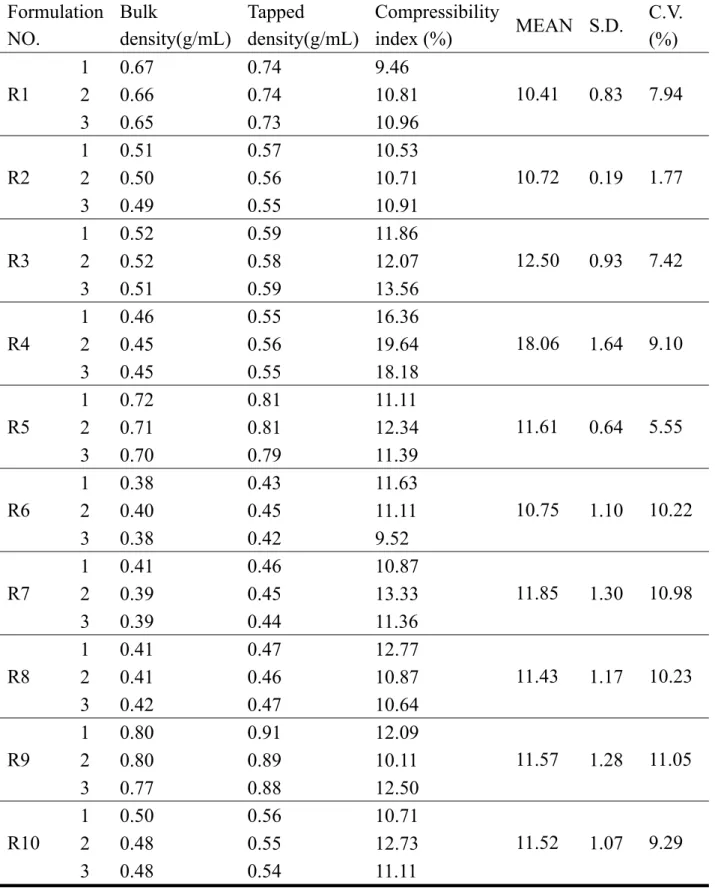
(9) 附表目錄 Table 1. GA 之 HPLC 定量法文獻整理………………………………….12. Table 2. 天麻錠劑配方 R1~R10 和 RA、RB 之組成………………………32. Table 3. 顆粒流動性與壓縮指數的關係………………………………….34. Table 4. 各種錠劑崩解時限表…………………………………………….50. Table 5. 不同濃度的 GA 溶液在不同波長下的紫外光譜分析…………..77. Table 6. 不同 pH 值的 GA 溶液之紫外光譜分析…………………………78. Table 7. 賦型劑對紫外光譜分析的影響………………………………….78. Table 8. GA (2 µg/mL) 標準溶液的安定性試驗結果……………………79. Table 9. GA (32 µg/mL) 標準溶液的安定性試驗結果…………………..79. Table 10 GA (64 µg/mL) 標準溶液的安定性試驗結果…………………..79 Table 11 天麻藥材乾粉 GA 與 HBA 的含量測定結果………………….80 Table 12 天麻濃縮液 GA 與 HBA 的含量測定結果………………………80 Table 13 天麻浸膏 GA 與 HBA 的含量測定結果………………………...81 Table 14 天麻浸膏 經流動床乾燥之顆粒中 GA 與 HBA 的含量 測定結 果…………………………………………………………….……81 Table 15 配方 R1~R10 安息角之測定結果………………………………..82 Table 16 配方 RA、RB 安息角之測定結果………………………………82 Table 17 配方 R1~R10 顆粒密度測定結果………………………………..83 Table 18 配方 RA、RB 顆粒密度測定結果……………………………….84 Table 19 配方 R1~R10 顆粒粒徑之測定結果……………………………..85 Table 20 配方 RA、RB 顆粒粒徑之測定結果…………………………….85 Table 21 配方 R1 顆粒的吸溼試驗結果…………………………………...86 Table 22 配方 R2 顆粒的吸溼試驗結果…………………………………...86 Table 23 配方 R3 顆粒的吸溼試驗結果…………………………………...86 Table 24 配方 R4 顆粒的吸溼試驗結果…………………………………...87 Table 25 配方 R5 顆粒的吸溼試驗結果…………………………………...87 VIII.
(10) Table 26 配方 R6 顆粒的吸溼試驗結果…………………………………...87 Table 27 配方 R7 顆粒的吸溼試驗結果…………………………………...88 Table 28 配方 R8 顆粒的吸溼試驗結果…………………………………...88 Table 29 配方 R9 顆粒的吸溼試驗結果…………………………………...88 Table 30 配方 R10 顆粒的吸溼試驗結果………………………………….89 Table 31 配方 R1~R10 顆粒的含水量之測定結果………………………..90 Table 32 配方 R1~R10 錠劑的硬度試驗結果……………………………..91 Table 33 配方 RA、RB 錠劑的硬度試驗結果…………………………….91 Table 34 配方 R1~R10 錠劑的厚度試驗結果……………………………..92 Table 35 配方 RA、RB 錠劑的厚度試驗結果…………………………….92 Table 36 配方 R1~R10 錠劑之 Tensile strength…………………………...93 Table 37 配方 RA、RB 錠劑之 Tensile strength……………………………93 Table 38 配方 R1~R10 錠劑的重量差異試驗結果………………………..94 Table 39 配方 RA、RB 錠劑的重量差異試驗結果……………………….94 Table 40 配方 R1~R10 天麻錠劑的 GA 含量測定結果………………….95 Table 41 配方 RA、RB 天麻錠劑的 GA 含量測定結果………………….95 Table 42 配方 R1~R10 天麻錠劑的 HBA 含量測定結果………………..96 Table 43 配方 RA、RB 天麻錠劑的 HBA 含量測定結果……………….96 Table 44 配方 R1~R10 錠劑的脆度試驗結果……………………………..97 Table 45 配方 RA、RB 錠劑的脆度試驗結果…………………………….97 Table 46 配方 R1~R10 錠劑的崩散度試驗結果…………………………..98 Table 47 配方 RA、RB 錠劑的崩散度試驗結果………………………….98 Table 48 The dissolution data of GA from R1 in pH 1.2 medium………….99 Table 49 The dissolution data of GA from R1 in pH 4.5 medium………...100 Table 50 The dissolution data of GA from R1 in pH 6.8 medium………...101 Table 51 The dissolution data of GA from R2 in pH 1.2 medium………...102 Table 52 The dissolution data of GA from R2 in pH 4.5 medium ………..103. IX.
(11) Table 53 The dissolution data of GA from R2 in pH 6.8 medium………...104 Table 54 The dissolution data of GA from R3 in pH 1.2 medium………...105 Table 55 The dissolution data of GA from R3 in pH 4.5 medium………...106 Table 56 The dissolution data of GA from R3 in pH 6.8 medium………...107 Table 57 The dissolution data of GA from R4 in pH 1.2 medium………...108 Table 58 The dissolution data of GA from R4 in pH 4.5 medium………...109 Table 59 The dissolution data of GA from R4 in pH 6.8 medium………...110 Table 60 The dissolution data of GA from R5 in pH 1.2 medium………...111 Table 61 The dissolution data of GA from R5 in pH 4.5 medium………...112 Table 62 The dissolution data of GA from R5 in pH 6.8 medium………...113 Table 63 The dissolution data of GA from R6 in pH 1.2 medium………...114 Table 64 The dissolution data of GA from R6 in pH 4.5 medium………...115 Table 65 The dissolution data of GA from R6 in pH 6.8 medium………...116 Table 66 The dissolution data of GA from R7 in pH 1.2 medium………...117 Table 67 The dissolution data of GA from R7 in pH 4.5 medium………...118 Table 68 The dissolution data of GA from R7 in pH 6.8 medium………...119 Table 69 The dissolution data of GA from R8 in pH 1.2 medium………...120 Table 70 The dissolution data of GA from R8 in pH 4.5 medium………...121 Table 71 The dissolution data of GA from R8 in pH 6.8 medium………...122 Table 72 The dissolution data of GA from R9 in pH 1.2 medium………...123 Table 73 The dissolution data of GA from R9 in pH 4.5 medium………...124 Table 74 The dissolution data of GA from R9 in pH 6.8 medium………...125 Table 75 The dissolution data of GA from R10 in pH 1.2 medium……….126 Table 76 The dissolution data of GA from R10 in pH 4.5 medium…….…127 Table 77 The dissolution data of GA from R10 in pH 6.8 medium……….128 Table 78 The dissolution data of GA from RA in pH 1.2 medium ………..129 Table 79 The dissolution data of GA from RA in pH 4.5 medium………...130. X.
(12) Table 80 The dissolution data of GA from RA in pH 6.8 medium………...131 Table 81 The dissolution data of GA from RB in pH 1.2 medium………...132 Table 82 The dissolution data of GA from RB in pH 4.5 medium………...133 Table 83 The dissolution data of GA from RB in pH 6.8 medium………...134 Table 84 配方 R1~R10 錠劑待溶量(%)半對數作圖…………………..…135 Table 85 配方 R1~R10 錠劑 in pH 1.2 medium 溶離參數……………….136 Table 86 配方 R1~R10 錠劑 in pH 4.5 medium 溶離參數……………….136 Table 87 配方 R1~R10 錠劑 in pH 6.8 medium 溶離參數……………….137 Table 88 配方 R1 錠劑之安定性試驗結果………………………………138 Table 89 配方 R2 錠劑之安定性試驗結果………………………………139 Table 90 配方 R4 錠劑之安定性試驗結果………………………………140 Table 91 配方 R3 錠劑之安定性試驗結果………………………………141 Table 92 配方 R5 錠劑之安定性試驗結果……………………………....142 Table 93 配方 R6 錠劑之安定性試驗結果……………………………....143 Table 94 配方 R7 錠劑之安定性試驗結果………………………………144 Table 95 配方 R8 錠劑之安定性試驗結果………………………………145 Table 96 配方 R9 錠劑之安定性試驗結果………………………………146 Table 97 配方 R10 錠劑之安定性試驗結果……………………………..147 Table 98 配方 R1~R10 和 RA、RB 錠劑之溶離度均一性試驗…………148 Table 99 配方 R1 錠劑在水中安定性測試結果…………………………149 Table 100 配方 R2 錠劑在水中安定性測試結果………………………....149 Table 101 配方 R3 錠劑在水中安定性測試結果…………………………150 Table 102 配方 R4 錠劑在水中安定性測試結果…………………………150 Table 103 配方 R5 錠劑在水中安定性測試結果…………………………151 Table 104 配方 R6 錠劑在水中安定性測試結果…………………………151 Table 105 配方 R7 錠劑在水中安定性測試結果…………………………152 Table 106 配方 R8 錠劑在水中安定性測試結果…………………………152. XI.
(13) Table 107 配方 R9 錠劑在水中安定性測試結果…………………………153 Table 108 配方 R10 錠劑在水中安定性測試結果………………………...153. XII.
(14) Abstrate Traditional chinese medicine (TCM) has been received increasingly as an alternative source for the treatment of human diseases. Gastrodiae elata Blume is a notable TCM. Recently, it is used for the treatment of patients with hypertension and Alzheimer’s disease. Gastrodin (GA) and p-Hydroxybenzyl alcohol (HBA) are active ingredients of Gastrodiae elata Blume. In this study, the curde extracts from Gastrodiae elata Blume were used to prepare the Gastrodiae tablets. The aim of formulation studies is to develop a useful tablet formulation and manufacturing process.Ten test formulations consist of different ratio of excipients, included. avicel 102, starch, lactose, dicalcium phosphate were evaluated. These tablet formulations were prepared by wet granulation method. Physical properties such as tablet hardness, thickness, weight variation, friability and compressibility were examined. Tablet disintegration, dissolution and content uniformity were evaluated by official methods. The dissolution of gastrodin from Gastrodiae tablets were tested by the paddle method using pH 1.2, 4.5 and 6.8 media. It was found that the R4 formulation dissolved gastrodin more rapidly and completely than others. By comparing the physical properties and dissolution data, as a rapid-released Gastrodiae tablets the best formulation is composed of Gastrodiae elata Blume extracts (260 mg)、avicel (150 mg)、 dicalcium phosphate (5 mg)、 lactose (5 mg)、starch (80 mg). By comparing different drying method fluid-bed drying and tray drying method on granulation process, which tested by R4 formulation, it showed that the fluid-bed drying was enhancing the crushing strength, disintegration times, therefore, increase the dissolution rate.. XIII.
(15) 中文摘要. 找尋傳統中藥來治療疾病慢慢受到重視。天麻就是一種著名的傳統中 藥,主要成分為天麻素 (Gastrodin) 和非糖基天麻苷元 (p-Hydroxybenyl alcohol ),藥理可用於高血壓和阿茲海默症等。在研究過程中,先萃取天 麻萃取液,再減壓濃縮成天麻浸膏,測天麻素 (Gastrodin) 的含量,以製 備所需含天麻素 (Gastrodin) 25 mg 的天麻錠劑。經由配方研究及不同製 程,比較配方間的差異和找尋簡單、快速、低成本的製造方式。錠劑是以 濕式造粒法製粒,經由加入不同比例賦型劑,包含微晶纖維素、澱粉、磷 酸鈣、乳糖、硬脂酸鎂等製成十種錠劑配方產品作評估。評估項目包括比 較處方間不同的物性,像錠劑的硬度、厚度、脆度、重量差異、壓縮性, 以及法定的崩散度、溶離度和含量均一性試驗等。天麻素 (Gastrodin) 的 溶離試驗在 pH 1.2、 4.5 和 6.8 溶媒中進行。由溶離數據得知,以 R4 處 方含有天麻浸膏 (260 mg)、微晶纖維素 (150 mg)、磷酸鈣 (5 mg)、乳糖 (5 mg)、澱粉 (80 mg) 為賦型劑製成的 R4 配方產品結果較佳。比較不同的 顆粒乾燥方法,流動床乾燥法與盤式乾燥法。以 R4 配方進行測試,發現 流動床乾燥,可改善錠劑的一些特性,如增加錠劑的硬度、縮短崩散時間 和增加溶離速度等。. XIV.
(16) 天麻錠劑之製劑學研究. 第一章 緒言. 隨著科學技術的發展,人類社會的進步、生活節奏的加快,世界人口 的老年化,要求生活品質的提升,從以前營養不良和細菌感染為主的疾 病,逐漸被諸如惡性腫瘤、心腦血管疾病、內分泌功能失調,神經精神系 統疾病等“現代文明病”所取代,人類的疾病也因此發生重大的變革。整體 醫學的快速崛起,主張人類生命健康的自然與整體和諧,與傳統中醫理論 講求的天人合一又不謀而合。回歸自然和綠色消費浪潮的興起,植物藥在 消費者心中的地位不斷提升,尤其對化學藥物的毒副作用與抗藥性,以及 藥源性疾病的增加,生態環境逐步惡化的憂慮,使人們寄於厚望於天然藥 物或非藥物治療來解決問題。中醫藥研究成果的日益豐富,特別是已經成 功地從天然藥物中提取出新藥,或設計出身體可用率高的劑型,使其備受 矚目,從而掀起一股“中藥熱”。世界各國也紛紛放寬對中藥的限制,為中 藥的國際化進程提供有利的的時機。 天麻. (Rhizoma Gastrodiae) 為 蘭 科. (Orchidaceae) 植 物 天 麻. (Gastrodiae elata Blume) 的乾燥塊莖。又名赤箭、定風草、獨搖芝,是種 名貴中草藥之一。兩千年前的《神農本草經》就將其列為上品,李時珍在. 1.
(17) 《本草綱目》中有較系統的概述,天麻能“主諸封痹,久服益氣,輕身長年”, 治療“語多恍惚,善驚失忘”等症。中醫臨床用於治療驚風抽搐、肢體麻木、 頭痛暈眩、冠心病、面肌痙攣等疾病(1)。現代的藥理學研究,則用於治療 高血壓及老年癡呆症的療效較為顯著。 眾所皆知,任何藥物用於臨床,必須給予一定的物態形式,即將原料 藥經由一定的製造過程製成物態形式,而此形式即為劑型(2)。過去人們認 為藥物的來源、化學結構、配方組成是決定藥效的唯一因素。隨著生物藥 劑學的發展,人們逐步認識到劑型因素在一定條件下對藥物的藥效有決定 性的影響,改變劑型可以調整藥物的作用速度,甚至降低或消除毒性及副 作用,也能達到靶向給藥的目的(3)。這方面的認知,已成為藥物研究或生 產時考慮的重要問題。如果以科學的角度來說明中藥製劑,就是所謂中藥 劑型的產生是為了發揮中藥的最好療效,減少毒性及副作用,以便於臨床 應用及儲藏、運輸和使用(4),因此可以根據中藥的基源、萃取方法、化學 成分、化學結構、理化性質、用藥目的、臨床需要、給藥途徑、給予對象、 投予劑量等,作為設計及生產出合適的劑型的科學依據。中藥製劑的創始 很早,歷代中醫典籍及本草藥書中有關方劑的製備有很多的記述。而傳統 上以丸、散、膏、丹、湯液及酒劑為中藥製劑的代表。近數十年來,由於 科技的進步,中藥製劑的開發已朝向更方便且更安全的現代劑型發展,是 結合中藥的抽提技術及現代劑型設計觀念,使中藥製劑往現代化發展。 經由系統性的研究和試驗來決定所需要的劑型,且能充分發揮各類中 藥劑型的特點。在條件許可的情況下,盡可能採用新劑型開發。已知現在 常用的中藥現代劑型有濃縮散劑、顆粒劑、錠劑、沖劑、膠囊、微囊、乳 劑、脂質體劑、滴丸、栓劑、噴霧劑、注射劑,經皮給藥貼佈等。現在天 麻的製劑已開發了天麻精膠囊、天麻素片、天麻丸、天麻注射液等。. 由於錠劑是現代给藥劑型中最廣用的口服劑型,主要是容易攜帶、貯 存及能夠很快的大量生產而便宜之優點。在選擇以錠劑當作天麻的劑型研. 2.
(18) 究時,首先需要考慮到藥材的前處理、中間製程、中藥製劑三大部分。藥 材的前處理包括天麻的基源鑑定、炮製及處理方式。中間製程則包括天麻 浸膏的萃取、成分定量分析。中藥製劑則以天麻劑型的設計,由賦型劑的 選擇及製程的相關評估,以確保劑型的安定、安全、有效。. 3.
(19) 第二章 總論 第一節 中藥劑型的現代化 我國中藥歷史悠久,從傳說中的神農嚐百草至今有 4700 餘年的歷史。 中藥來自植物、動物、礦物,並以植物來源為主,種類繁多,明•李時珍 《本草綱目》中就記載 1892 種,清•趙學敏《本草綱目拾遺》又補充了 716 種(5)。在傳承中形成了獨特的理論體系,並累積了豐富的臨床經驗, 使中草藥作為重要的天然資源的發展備受重視(6)。 隨著藥品專利化、智慧財產權保護法規的實行及化學合成藥物開發研 製資金龐大,所以從傳統中藥及其複方和天然藥物中篩選有價值的活性物 質(如治療老年疾病、愛滋病、癌症等)也日顯重要。美國 FDA 已批准對包 括中藥製劑在內的天然植物進行臨床評估,同時 USPⅩⅩⅣ版也增加了天 然藥物品種,日、韓、歐美諸國正加速研製和開發傳統醫藥產品等,這正 是中藥走向世界,佔領國際醫藥市場的良機(7)。正因如此,中藥製劑的現 代化是中藥現代化研究和中藥走向世界的關鍵,實質上就是中藥與現代科 技、現代學術思想,以及現代文化的結合,也是在繼承中醫藥傳統理論、 應用經驗和技術基礎上,使其擺脫傳統中藥製劑“粗、大、黑”的刻版印象, 以提高更有效的藥效品質為依歸,才能使中藥在國際醫藥市場上佔領一席 之地和尋求更卓越的醫療貢獻(6)。 由於傳統中藥成分複雜,藥材易受產地、天氣、土壤、養分等各種因 素影響,導致傳統製劑之質量標準難均一化且服用劑量偏大,療效不穩 定。因此,有賴含量測定、穩定性試驗、藥效學,藥動學等研究以協助中 藥製劑的現代化,才可保持中藥固有的特色和療效。將傳統劑型改製成新 劑型,還需進一步改善中藥劑型外觀、減小體積、提升劑型有效成分的含 量、增加藥物的有效成分的溶離及提高生體可用率等。 中藥的傳統劑型,近年來已逐漸應用現代化藥物製劑技術,提高製劑 科學化、機械化、標準化,朝向高效、速效、低毒、易攜帶、易服用、易 保存的方向發展。 4.
(20) 第二節 天麻的化學成分 天麻 (Gastrodiae elata Blume) 是主產於中國的名貴常用中藥,歷代本 草列為上品,但對天麻的化學成分過去則很少有人進ㄧ步探討。天麻的化 學成分研究始於 1936 年發現天麻中含有微量元素及為維生素 A 類物質。 根據文獻及伊利諾大學 Narpralet 資料庫之資料所做的統計,現在將以被分 離之鑑定之成分分述如下(8, 9):. 一、天麻成分 (1)Benzenoids 1. 3, 4-hydroxy benzaldehyde 2. 4-hydroxy benzaldehyde 3. 4, 4-dihydroxy dibezyl ether 4. 4, 4-dihydroxy diphenyl methane 5. 4-hydroxybenzyl alcohol 6. 4-hydroxy benzyl methyl ether 7. cis-(4- hydroxy benzyl)ether 8. 4-β-D-glucopyranosyloxy benzyl alcohol 9. 4-o-β-D-glucoside benzyl alcohol 10. gastrodin 11. gastrodigenin 12. 4-ethoxy methyl phenol 13. 4-ethoxy methyl phenol 4-hydroxy benzyl ether 14. trans [4-(β-D-glucopyranosyloxy)benzyl] citrate (parishin) 15. 1, 2-bis [4-(β-D-glucopyranosyloxy)benzyl] citrate (parishin B) 16. 1, 3-bis [4-(β-D-glucopyranosyloxy)benzyl] citrate (parishin C). 5.
(21) (2)Carbohydrates 1. glucose 2. sucrose. (3)Steroids 1.β-sitosterol 2. daucosterol. (4)Miscellaneous 1. citric acid 2. succine acid 3. palmitic acid 4. armillarine 二、天麻素及天麻苷元的結構式(10) 1.Gastrodin. 2.ρ-Hydroxybenzyl alcohol. 6.
(22) 三、天麻素及天麻苷元的理化性質 1.天麻素(Gasttrodin, GA) 化學名:4-(β-D-glucopyranosyloxy)benzyl alcohol 分子式分子量:C13H18O7 分子量:286.27 理化性質:m.p. 154~156℃ 由甲醇-乙酸乙酯再結晶為百色粉末,可溶於甲醇、乙醇。 2.天麻苷元(HBA) 化學名:ρ-Hydroxybenzyl alcohol 分子式分子量:C7H8O 分子量:122 理化性質:m.p. 116~117℃ 由氯仿-甲醇再結晶為無色針晶,可溶於甲醇、氯仿。. 7.
(23) 第三節 天麻的藥理研究 天麻為常用之中藥,國內、外近年來對其藥理都有進一步的研究和探 討,現將其概況做一統合性的敘述如下(11, 12):. 一、天麻對中樞神經系統的作用 1.抗驚厥作用 天麻抗驚厥有效成分是香莢蘭醛 (Vanillin) 、香夾蘭醇 (Vanillyl alcohol) 及天麻素,香莢蘭醛作用強於天麻水煎劑,但均不及苯妥英鈉(13)。 1979 年,鄧士賢(14)等人報導天麻浸膏有明顯對抗戊四氮陣攣性驚厥的潛伏 期。吳惠平. (15). 等人利用截肢術、機械刺激綜合法,造成豚鼠實驗性癲癇,. 分組觀察天麻對該模型治療前、後,中樞各腦區兒茶酚胺含量的變化,實 驗發現天麻治療豚鼠的 norepinephrine (NE) 和 dopamine (DA) 有明顯增 加,所以天麻的抗癲癇機轉可能是通過選擇性增加中樞兒茶酚胺神經細胞 內的兒茶酚胺含量,而影響中樞不同腦區兒茶酚胺類神經傳遞代謝有關。 2.鎮靜催眠作用 1985 年,黃正良(16)等人指出天麻注射液 5g/kg 亦可延長戊巴比妥鈉 (Amobarbital) 、 水 合 氯 醛 (Chloral hydrate) 及 硫 噴 妥 鈉 (Thiopentone sodium)等所引起的睡眠時間。鄧士賢(14)等人報導,正常人服用天麻素和天 麻苷元前、後,腦電圖實驗結果說明用藥後多數有嗜睡感、α 波指數減低, 且能減低咖啡因 (Caffeine) 引起的興奮,與硫噴妥鈉有協同作用,並延長 麻醉時間,有類似酸棗仁的安定作用(17)。對小鼠的自發性活動有明顯抑制 作用(18)。1993 年黃杉(19, 20)等人,對於天麻鎮靜催眠作用機轉利用天麻注射 液對大鼠大腦內 NA、DA 含量及釋放的影響。得到天麻的鎮靜催眠作用可 能與降低腦內 NA、DA 含量有關,而腦內 NA、DA 含量減少,可能與天 麻抑制中樞 NA、DA 神經末梢對它們的重攝取和儲存有關。. 8.
(24) 3.鎮痛作用 1980 年趙國舉(21)等人,用電擊鼠尾法,證明人栽天麻與野生天麻 5g/kg 均有明顯的鎮痛作用,且實驗證明野生天麻鎮痛作用強且止痛時間久。皮 下注射天麻製劑 5g/kg,能明顯對抗小鼠腹腔注射醋酸引起的扭體反應, 小鼠熱板法也證明出天麻製劑可提高疼痛閾值(22)。. 二、天麻對心血管的作用 1.對心臟的作用 從組織化學研究觀察到,天麻素能使培養細胞琥珀脫氫酶 (SDH)、 乳酸脫氫酶 (LDH)、三磷酸腺苷 (ATP) 活性增強,使糖原、DNA、RNA 增多,說明天麻具有促進細胞能量代謝的作用(23)。在此基礎上作一研究, 以絲霉素 (MCC) 形成的中毒性心肌損傷的細胞為病理模型,合成天麻素 可使心肌細胞變性減輕、壞死顯著減少,LDH、SDH 活性增加,且天麻濃 度越高保護作用越顯著,這可能與天麻素促進細胞能量下降,增強抗損傷 作用有密切關係。尚偉芬(1)等人報導,合成天麻素可使大鼠培養心肌細胞 搏動頻率加快,搏動範圍及強度增加而不影響心率,說明天麻增加心輸出 量作用為天麻使心肌細胞收縮增強所致。 2.對血管血壓的作用 天麻湯能對抗腎上腺素的收縮血管作用,對腎上腺素所至的大鼠循環 障礙有顯著的預防作用,還具有對抗大鼠血栓形成的作用,其機轉是在於 能抑制血小板黏聚功能,此項研究為天麻湯防治缺血性腦中風提供了理論 依據(24)。王正榮(25)等人通過實驗得知結論,天麻素是種能增加中央及外周 動脈血管順應性、降低外周阻力、具有溫和降壓作用的中藥有效成分。. 9.
(25) 三、天麻抗免疫的作用 1988 年陳怡敏(26)、1989 年于龍順. (27). 等人指出天麻注射液可增加鼷. 鼠之巨噬細胞吞噬能力及血清溶菌酵素之活性,所以得知天麻可增加鼷鼠 之細胞免疫及體液免疫系統,多次給藥後也可增加脾臟之重量,也顯示具 增強免疫系統的能力。. 四、天麻抗衰老及改善學習記憶的作用 1. 抗衰老作用 天麻可以提高 superoxide dismutase (SOD)、GSH-Px 活性,且有耐疲勞 作用,能縮短果蠅幼蟲發育的時間,延長成蟲的壽命(28, 29)。天麻還可提高 老年心藏血管患者血中 SOD 活性,降低血中 LOP 含量(30, 31)。1992 年 Liu. 及 Mori.指出天麻水抽液可抑制大白鼠大腦皮質部之脂過氧現象及增加粒 線體內 SOD 之活性,並具清除自由基之作用(32)。 2. 改善學習記憶作用 1997 年謝明村教授以 Sprague-Dawley 系雄性大白鼠,使用被動迴避 學習反應測定裝置實驗得知天麻具有改善大鼠學習障礙之效果(33, 34)。1996 年 周 本 宏 (35) 等 人 利 用 小 鼠 跳 台 法 實 驗 觀 察 了 天麻 提 取 物 對 東 莨 菪 鹼 (scopolamine)、亞硝酸鈉、乙醇所致的小鼠記憶損傷病理模型的影響,結 果顯示天麻提取物對小鼠學習記憶能力具有明顯改善作用。. 10.
(26) 第四節 天麻素定量分析方法 中華人民共合國藥典及許多天麻製劑皆以天麻素作為含量指標。天麻 素的定量分析方法包含顯微定量 (36)、薄層層析法(37)、紫外光分光光度法 (38). 、二階導數光譜法(39)、三階導數光譜法(40)、高效液相層析法(41-47)、毛細. 管電詠法(48),其中以高效液相層析法 (HPLC) 為最常使用之方法。 為了提高中藥製劑的質量,在文獻的研究報告上都會做成分含量的定 量分析,而天麻素這個成分分析,經文獻發表的方法,將整理於 Table 1 中。. 11.
(27) Table 1 天麻素 (GA) 之 HPLC 定量法文獻整理 作者:朴惠善等(41) 層析管柱:YWG-C18 波長 (nm):222 ,流速 (mL/min):1.2 移動相 (v/v):磷酸二氫鈉-乙腈= 97:3 (以磷酸調整為 pH 3 ~ 4) 檢品處理方法:藥品置圓底燒瓶中加甲醇 200、100、50 mL,回流 1、1、0.5 hr 3 次, 過濾,合倂濾液減壓濃縮,浸膏用 40 mL 蒸餾水溶解後,每次用 40 mL 石油醚萃取 3 次,取水層後在再用正丁醇 40、30、30 mL 萃取 3 次,正丁醇減壓濃縮回收,濃縮至 乾,乾燥物溶於蒸餾水中,通過 D101 大孔吸附樹脂柱,先用水洗,再分別用乙醇抽提 300、500、700 g/L,收集 700 g/L 乙醇抽提部分,回收乙醇,加甲醇溶解稀釋至 25 mL 容量瓶中,即得供試品溶液。. 作者:黃順爵(8) 層析管柱:Waters Nova-Pak C18 波長 (nm):270,流速 (mL/min):0.8 移動相 (v/v):乙腈-水=2.5:97.5 (加 1%醋酸) 檢品處理方法:取乾燥藥材 10 g,磨碎置於 50 mL 三角瓶內加入甲醇 35 mL,超聲振 盪 1 hr,吸出浸液,置於 100 mL 容量瓶內,重覆抽提 3 次加甲醇精確定容,混合均勻, 以 0.45μm 過濾,以作 HPLC 檢液。. 作者:謝敏等(42) 層析管柱:µ-Bondadpak C18 波長 (nm):220,流速 (mL/min):1.0 移動相 (v/v):甲醇-磷酸鹽溶液-水=3:3:94 檢品處理方法:取樣品 0.5 g,精密測定,加甲醇 100 mL,置索式抽提器加熱 2 hr,放 冷過濾,濾液濃縮至 2 mL,加至以處理好的中性氧化鋁柱上 (內徑 1.5 cm,長 10 cm), 用 80 %甲醇 100 mL 抽提,收集抽提液,蒸乾,用甲醇溶解並稀釋至刻度,搖均,過 0.45μm 濾模,測含量。. 作者:謝笑天等(43) 層析管柱:Shin-pack CLC-CN 波長 (nm):270,流速 (mL/min):1.0 移動相 (v/v):乙腈-水=10:90 檢品處理方法:天麻素片剝去糖衣,取 20 片,精密稱重,研細,加流動相超聲溶解定 溶,過慮。精密量取濾液配置成 0.5 mg /mL,測含量,膠囊測定同片劑。. 12.
(28) 作者:孫冬梅等(44) 層析管柱:LiChrospherR 100 波長 (nm):270,流速 (mL/min):1.0 移動相 (v/v):甲醇-磷酸鹽溶液-水=1.5:3:95.5 (柱溫 35℃) 檢品處理方法:天麻配方顆粒過 400 mesh,取 1 g 粉末置 50 mL 容量瓶,加入甲醇 25 mL,超聲處理 30 min.,靜置 24 h,振搖再超聲處理 15 min.,用甲醇補足減少重量, 取上清液離心即得。. 作者:莫志江等(45) 層析管柱:Nova-Pak RP18 波長 (nm):272,流速 (mL/min):0.7 移動相 (v/v):乙腈-水=6:94 檢品處理方法:精密稱取天麻粉 0.5 g,置 25 mL 錐形瓶,加甲醇 10 mL,超聲 30 min., 靜置 4 hr,再超聲提取 60 min.,置 25 mL 容量瓶中,用甲醇稀釋至刻度即得試液。. 作者:熊佐章等(46) 層析管柱:Shin-pack CLS-ODS 波長 (nm):221,流速 (mL/min):1.0 移動相 (v/v):甲醇-水-三乙胺=6:94:0.2 檢品處理方法:取天麻片樣品 20 片,除去糖衣精密測定,研細後取細粉 2 g,置三角 瓶中,加入無水乙醇-異丙醇 (1:1) 25 mL 混合液,密塞稱重,放置 30 min.後,超聲 處理 2 次,每次 25 min.,間隔 15 min.,放冷稱重,利用混合液補足重量,過濾,取濾 液 10 mL,80 ℃低溫蒸乾,加入甲醇 5 mL,超聲處理 2 min.,濾模過濾備用。. 作者:王興等(47) 層析管柱:Diamonsil C18 波長 (nm):221,流速 (mL/min):1.0 移動相 (v/v):乙腈-水-磷酸=2.64:97.36:0.2 檢品處理方法:用微量移液器精密吸取 0.5 mL 大鼠血漿於 5 mL 玻璃錐型離心試管, 加入 100μl GA 標準液、2 mL 無水乙醇,混均 30 s,低速離心 5 min.(3500 rpm),吸取 上清液,60℃水浴下以 N2 吹乾,再用 500μl Mini-Q 復溶,高速離心 5 min.,取上. 清液分析。. 13.
(29) 第五節 中藥錠劑製劑設計 中藥錠劑是一種或多種中藥藥物,經加工提取後,摻加賦型劑,壓製 成圓片狀之一種固體劑型。錠劑具有劑量準確、質量穩定、體積小攜帶運 輸方便。中藥打錠前需做成顆粒,原因是藥粉越細吸附力越大,凝集力也 越大,直接壓片會出現黏銃現象,且不能均勻填入銃膜,使製成的錠劑重 量和含量不準確,壓片困難。同時由於藥粉細、密度大或與賦形劑比重不 同,壓片時空氣不能即時地由銃模中逸出而造成錠劑鬆裂或分層現象。將 藥物製成顆粒,則可避免發生上述的問題。. 一、中藥錠劑種類 根據製作方法,中藥製顆粒的組成總類可分成以下兩大類(49),再經乾 燥後壓成錠劑。 1.全膏製粒 a.將中草藥全部製成稠膏,加入賦形劑,製粒。 b.將中草藥全部製成乾浸膏,粗磨成顆粒或磨成細粒,再以適宜濃 度的乙醇為濕潤劑,製粒。 2.粉膏製粒 a.將中草藥一部分磨成細粉,另一部分製成稠膏,混合,必要時加 入適量黏合劑或賦形劑,製粒。 b.將中草藥一部分磨成細粉,而另一部分製成乾浸膏粉,混合,加 入適宜的黏合劑或溼潤劑,製粒。. 二、賦型劑的選用 對於藥物物理性質和決定劑型後,接下來選擇適當賦型劑又稱輔料, 以製成處方。賦型劑包括稀釋劑、黏合劑、濕潤劑、吸收劑、崩散劑和潤 滑劑等,這些賦型劑都需具有化學性質的穩定性,如與主藥不發生物理或 化學作用、不影響藥效和片劑的含量測定且對人體無毒性(50),且賦型劑的 14.
(30) 選用,大多會影響藥物製劑的性質。 1.稀釋劑 稀釋劑又稱充填劑,主要用途是用來增加固體劑型的質量和體積。 2.吸收劑 中藥固體劑劑一般體積較大而不用稀釋劑。但以浸膏為原料壓錠,為 了降低浸膏黏度、預防引濕、增加可耐壓性,可加入一些中藥細粉或吸收 性賦型劑壓錠。如澱粉、乳糖、蔗糖、碳酸鈣、磷酸鈣等。 3.濕潤劑 為了將藥粉黏合製粒,必須加入黏合劑和濕潤劑。對於藥材有黏性 的,只要加入合適的液體如蒸餾水、乙醇等就可產生黏性,這類液體稱濕 潤劑。 4.黏合劑 對於本身無黏性的藥粉,要用有黏性的液體如糖漿、明膠溶液等,使 各成分彼此黏附在一起,這類液體稱黏合劑。黏合劑在製粒中的含量和混 合會影響顆粒的大小、鬆散、碎裂情形(51)。 5.崩散劑 錠劑服用後,再胃腸中應及時溶解或崩散,才能迅速吸收,產生療效, 所以加入崩散劑可增加崩散速度。崩散劑應具有親水性、性質穩定、經濕 潤或遇水迅速膨脹使錠劑崩散。如澱粉、微晶纖維素、海藻酸類、樹膠類 等。 6.潤滑劑 壓錠時可增加顆粒與顆粒或錠模間的摩擦,防止顆粒黏附於銃柱及銃 模表面和增加顆粒流動性,常用潤滑劑有滑石粉、硬酯酸鎂、硬酯酸鈣、 液態石蠟等。潤滑劑的加入雖可降低測表面邊緣與錠糢壁間的模擦力使錠 劑易被下銃糢推出,但會增加錠劑的硬度(52)。如潤滑劑硬酯酸鎂加入微晶 纖維素的粉末可增加流動性以便壓錠,但會在顆粒表面形成一層水不溶性 的薄膜,而減少微晶纖維素錠劑碎裂強度(53)。. 15.
(31) 7.著色劑與矯味劑 可使錠劑外型更美觀、易於服用及辨識,且保護有效成分對光線、潮 濕及空氣之安定,且掩飾不良味道。. 三、製粒方法 在製程中,造粒即〝Granulation〞 ,扮演一個重要角色,可以定義為是 一種 size enlargement(54)。一般在加入黏合劑後,可使粒子大小從 1-500 µm 增加至 2 µm-10 mm 的範圍(55)。廣泛使用在製藥技術、食品產業、肥料、 飼料、特殊化學工業上(56)。利用此法可製出我們所期望的顆粒,其中包含 顆粒大小、形狀、密度、分佈和流動性的設計,這些都和錠劑製造有關聯 性(57)。 1.溼式造粒法製粒 濕式造粒法現今仍是廣泛應用於製藥工業,在發展上受金錢和習慣上 的考量,一直是受矚目的技術,而未被直接壓錠法所取代。濕式造粒法對 於含藥成分高和含藥成分低的均一性與顆粒的壓縮性提供了較好的控制 性(58)。先將藥物和賦型劑稱量稱量、粉碎、過篩、混合成濕團塊,造粒、 乾燥,加潤滑劑準備壓錠。 2.乾式造粒法製粒 先將藥物和賦型劑稱量、粉碎、過篩、混合、預壓成較大得圓盤型餅 或塊、壓碎、整粒,再加潤滑劑混合,壓錠(59)。 3.直接壓錠法 藥物和賦型劑稱量,無須經過造粒就可直接壓錠,可減少製粒過程、 潤濕乾燥處理且製造過程迅速。像 acetaminophine(60)利用直接壓錠法,也 可提高藥物的含量,且錠劑的一些物理性質也不輸濕式造粒法。. 16.
(32) 第六節 中藥的抽提技術 對中藥製劑的提取技術的研究,首先應從傳統用藥的經驗出發,評估 藥材性質,結合現代,化學成分、藥理作用等方面研究資料,綜合考慮浸 提時所用的溶劑、方法和設備,並以臨床效果作為主要依據。 選擇有效的浸出方法,對於浸出的藥物質量、提高浸出效率、經濟效 益是十分重要的。藥材的浸出抽提技術可分為浸漬、煎煮、滲漉、回流、 水蒸氣蒸餾、超臨界流體萃取法(61)。 1.浸漬法 中藥生產的基本方法,在藥材抽提器上加適量溶劑,於一定溫度和時 間進行浸提,使有效成分浸出,並使固液分離。為了減少過程中成分的損 失,可利用多次浸漬法。適用於黏性、易膨脹、有效成分對熱不安定或易 揮發的藥材。 2. 煎煮法 以水作為浸出溶劑的水煎煮是常用的方式,將藥渣煎煮 2 至 3 次,收 集煎出液,離心分離或沉降過濾,低溫濃縮至規定濃度。適用於對濕、熱 安定的藥材。 3.滲漉法 滲漉法(50)是將適當的浸劑,慢慢經過置於滲漉器中粉末藥品所形成的 柱層,從底部流出滲漉液,而抽提出成分的方法。為求有效成分之提取完 全,並使無效成分減至最小限度,因此各種不同生藥,所需浸漬時間和滲 漉速率均不相同,須各別規定之,且生藥之量如有增減,應將規定浸漬時 間和滲漉速率,酌量的作變化。 4.回流法 加熱抽提時溶劑被蒸發,冷凝後又流回提取器,如此反複直到完成抽 提。適於對熱安定的藥材和低沸點的溶劑。. 17.
(33) 5.水蒸氣蒸餾法 將藥材浸潤後,加熱蒸餾,而藥材中的揮發成分隨蒸氣蒸餾帶出,冷 凝後分層,收集產物。適用於具揮發性難溶或不溶性成分之提取分離。 6.超臨界流體抽提法 超臨界流體抽提 (Supercritical fluid extraction, SFE) 就是利用超臨界 流體作為溶劑,從固體或液體中萃取出有效成分,進行分離技術。影響超 臨界流體萃取的主要因素為萃取的壓力、溫度、萃取物顆粒的大小和極性 的大小等。. 18.
(34) 第七節 中藥產品的乾燥理論與技術 現今所看到的中藥製劑大多為固體劑型,一般生產過程為中草藥經粉 碎後,再用水、醇或其他溶劑提取提取液,提取液經蒸發濃縮得到浸膏, 這些浸膏少數用於臨床,大多數要加工為固體製劑。浸膏一般經噴霧乾燥 製成粉狀產物,然後經由製粒製成所需要的劑型,像濃縮顆粒劑、錠劑、 丸劑、滴丸等。或將浸膏直接加進蔗糖、乳糖、澱粉、藥渣或其他賦型劑, 再乾燥製粒得到的各種形式的固體劑型。因此製造流程長,自動化程度 低,有的加工步驟程序是手工操作和開放式操作,所以藥品的質量難以控 制,並且不易達到 GMP 標準。所以中藥固體制劑製造加工的現代化是實 現中藥生產現代化的關鍵組成部分之一。 常見的需要乾燥、製粒的中藥種類很多,包括膏狀物、漿狀物、水溶 液或其他溶液、顆粒狀物、粉狀物等,另外存在中藥製劑中有的成分是對 熱不安定、有的是中藥為了符合生產小批量、多樣式的特點及達到設備易 清洗的要求,所以為了要克服這些特點,乾燥、製粒方法和設備也必然會 有多種形式,常見的乾燥設備有盤式乾燥、氣流式乾燥、冷凍乾燥、紅外 乾燥、微波乾燥、噴霧乾燥、流動床乾燥等。所以,隨著中藥新劑型的開 發,要提高藥物的利用率,必然需要具備一些較新的乾燥技術(62)。 乾燥時間根據藥物及賦形劑的性質,選擇適宜的溫度。一般以 60~80 ℃ 為宜,乾燥約 24 小時,顆粒乾燥溫度應逐漸升高,否則顆粒的表面乾燥 後,不僅會形成一層硬膜而影響內部水分的蒸發,要是顆粒中含糖粉會因 突遇高溫而熔化,使顆粒變堅硬而影響崩解。. 一、乾燥理論 由於固體原料內部結構複雜富多樣性,原料所含的水分結合方式也不 盡相同,因此就決定製劑除去水分的難易度。乾燥速度取決於水分自固體 製劑內部向表面的傳遞速率和原料本身的結構、形狀和顆粒大小等特性。 製劑中所含的水分性質大至可分成兩大類:(1) 平衡水與自由水(2) 結合水 19.
(35) 與非結合水。 (1)平衡水與自由水 平衡水與自由水是根據產物在一定乾燥條件下,所含水分能否利用乾 燥方法來除去所區分。如某種原料與某一狀態的空氣進行接觸,原料會除 去水分或吸收水分,最後達平衡,此時原料中所含的水分不會因接觸某一 狀態空氣的時間延長而發生變化,原料中所含的這部分水分稱平衡水分。 平衡水分會因原料種類的不同而有差異,也隨空氣狀態的不同而變化。不 吸潮的原料其平衡水分幾乎為零。而原料中大於平衡水的那一部分水分稱 自由水分,也就是在某一空氣狀態下可從吸濕原料中移除的水分。 (2)結合水與非結合水 結合水與非結合水是利用原料中移除水分難易度去區分的。非結合水 是存在於原料表面的濕潤水及孔隙中的水,以機械方式與物料結合,結合 力弱,易除去。結合水為原料藥、纖維管壁及毛細管中所含的水分,以物 化方式和原料結合結合力強,不易除去。. 二、乾燥技術 1.盤式乾燥 盤式乾燥器是間歇操作的設備,也可在真空條件下操作。小型叫烘 箱,大型叫烘房,需將被乾燥物料放在箱內的層疊盤內。盤式乾燥的缺點 是乾燥器各位置的原料受溫不同易導致乾燥不均勻;每乾燥一批原料,置 料盤要更換一次或原料接觸空氣先後不同,導致作用時間長、熱能損失 大、產品質量不均、消耗人力。因此,此類乾燥器多是用在小規模生產、 乾燥時間長、每批原料乾燥後要把設備清洗一次為主。 2. 氣流式乾燥 主體部分乾燥管為一個直立的圓管,熱氣流在其中通過,被乾燥的原 料由加料器送入到乾燥管底部,然後被熱空氣吹起在乾燥管中乾燥,氣流 中帶有較細的顆粒經過濾器過濾。氣流式乾燥的優點原料處於懸浮分散狀. 20.
(36) 態,可增加乾燥表面積使乾燥速度加快。 3.冷凍乾燥 冷凍乾燥是在低溫減壓的條件下,利用昇華的原理將冷凍溶液的水分 移去。通常用於怕熱或對水易產生不穩定的原料。 4.紅外乾燥 利用紅外線輻射能使被乾燥物料中的水分汽化乾燥,所需的時間短。 原理是利用紅外線的輻射能被藥物吸收,使被乾燥物原子、分子振動,轉 變成熱能,使物體溫度升高,進而達到乾燥目的。 5.微波乾燥 微波乾燥室指由微波能轉變為熱能使被乾燥物乾燥的方法。微波乾燥 的速度快、效率高、乾燥均勻,在乾燥過程中,還有滅菌的功能。 6.噴霧乾燥 噴霧乾燥包括液滴噴霧乾燥和流動床噴霧乾燥(63)。液滴噴霧乾燥一般 以溶液、漿狀物為原料。在一定條件下也可以用懸浮液和膏狀物作為起始 原料。噴霧乾燥、造粒包括四個基本過程,液體的霧化、液體和氣體的混 合、液滴的蒸發乾燥、被乾燥的產品與氣流分離。噴霧乾燥製粒適用於對 熱敏感且不能長時間暴露於空氣中。原料的乾燥、造粒,廣泛應用於無機、 有機、醫藥和食品等。張俊英. (64). 等人就是利用噴霧乾燥來製造天麻促智. 顆粒。流動床乾燥可在同一設備內同時完成蒸發、結晶、乾燥、冷卻、造 粒、包衣等過程,可實現生產過程的連續自動化,但如使用易燃燒有機溶 媒有引起爆炸的危險性。基本原理方法為,將液態原料噴在流動床內顆粒 的表面,經氣體的作用,液態物料蒸發、結晶、冷卻,使得顆粒表面形成 一新的薄膜,再慢慢使顆粒長大。特點是因液態原料的乾燥是在顆粒的表 面進行,以一種液膜的形式存在,所以具有大的蒸發表面積和速度,乾燥 過程中可在相對較低的溫度下完成,並保持藥品的活性。. 21.
(37) 第八節 中藥製劑的安定性 藥物的安定性是保證藥物有效性和安全性的重要因素。安定性種類包 含了化學安定性、物理安定性、微生物安定性、治療安定性、毒性定性。 藥物製劑在製造和貯存的過程當中,因外在環境溫度、水分、光線、 微生物等因素的影響,而使製劑容易發生變質問題,使得藥物製劑藥效的 降低,甚至有些藥品反而會增加毒性,使得藥品的效果和安全遭受質疑。 自 50 年代至今,人們對西藥製劑的安定性問題,已經有相當豐富的知識 和經驗,對某些製劑如抗生素、生物製品等都明確規訂了有效期限,但對 於中藥安定性的問題,則還須進一步的探討。到 80 年代後才慢慢被重視。 中藥製劑的固體劑型安定性,也會受到加入不同賦型劑而影響,因降 解可能發生在固體製劑中、賦型劑和藥物的交互作用、對主成分的降解產 生催化作用等(65)。 中藥製劑安定性研究範圍主要內容為: 1.測定處方中的活性成分及主要降解產物 2.比較實驗處方、包裝和貯存 3.決定用那些關鍵參數來篩選處方,了解有效期限。包括加溫的加速性實 驗、光照的加速性實驗等。 藥物在溶液中的降解一般符合一級化學動力學模式,而相同藥物製成 懸浮液,卻符合零級化學動力學模式,而大多數固體劑型中的藥物是在 固、液相的界面進行降解,探討固體劑型降解反應的液相環境有以下幾種 (65). :. 1.低溶點的藥物或賦型劑在高溫下溶化 2.濕式造粒法所殘留水分或溶劑 3.一些賦型劑的吸濕、固體製劑吸附空氣水分 4.隨著時間和溫度的改變,導致溶劑或水分含的改變. 22.
(38) 第九節 研究動機與目的 一、研究動機 現代中藥製劑,將很多傳統的丸劑、散劑、湯劑改成濃縮顆粒劑、膠 囊劑、錠劑、口服液等新劑型。但其中也存在不少問題,有的新產品劑型 選擇不當,或製程不合理以致療效下降。像錠劑是使用最廣的劑型,一般 產量高成本低,服用、攜帶、保存、運輸均方便,且可藉著包衣來掩飾不 良苦味,並減少空氣、溼度等對藥物的影響。由於同劑型、同藥材的製劑, 若因加入的賦形劑不同,製造過程條件的選擇不同,也會引起最終劑型的 品質與療效。主要的原因可歸納成兩大方向:一是在濃縮乾燥製粒的過程 中(特別是乾燥)需要長時在高溫環境下,使得不耐熱的有效成分受影響而 下降;二是錠劑的配方不同,可能延長崩散、溶離時間,因而影響藥物質 量的穩定性、有效成分的溶離、吸收及療效(66)。 而選擇天麻當作錠劑製劑的研究有四個原因,原因一是錠劑有諸多優 點包括方便且服合中藥選擇劑型原則、溶離速率及生體可用率較丸劑好、 劑量準確且錠劑內藥物含量差異小、質量穩定且錠劑為乾燥固體,某些易 氧化變質及潮解的藥物可藉包衣加以保護,所以光線、空氣、水分等對其 影響較少、成本低,產量大,機械化生產,攜帶、運輸、服用均方便,二 是天麻是我國著名的中藥材,有著兩千多年的老祖先的臨床應用經驗,對 於天麻的製劑研究有實質的意義,三是由於中藥中有效成分的複雜性,對 成分研究有一定的困難度,實際上複方的化學成分不等於組成複方的單味 藥化學成分之和;複方的有效成分也並非組成複方的單味藥有效成分的簡 單相加(6),所以只選擇單味藥,先作深入探討,四是本實驗室以對於天麻 的有效成分天麻素 (Gastrodin, GA)、天麻苷 (ρ-Hydroxybenzyl alcohol, HBA) 的含量測定條件之確效、基源鑑定、指紋圖譜,已做過詳細的論述 和分析,對於分析上可節省相當的時間和資源,基於上述四個原因,還希 望能再透過製劑學的研究過程中,找出高安全、高安定、高療效、低消費 的劑型,把傳統的中藥資訊、中藥劑型發揚光大、邁向現代化。 23.
(39) 二、研究目的 本實驗決定以天麻為藥用成分,以錠劑當作天麻的製劑,錠劑設計需 含 25mg GA,以相同製法、劑型,相同配方不同比例,來了解天麻在不同 比例配方的條件下,製成顆粒的物理性質及打錠後物理性質之間的相互關 聯性。實驗設計上參照中華藥典 (第五版) 對製劑的規定和藥劑學一般檢 測方法,透過一連串的實驗進一步探討比較不同配方,顆粒的分佈、密度、 流動性、含水量,錠劑的含量均一性、硬度、崩散、溶離等情況。而藥物 的安定性是保證藥物有效性和安全性的重要因素,中藥製劑安定性的研 究,如應用在中藥劑型的實驗設計當中,對於提高中藥製劑的質量有實質 的幫助。處方研究上,根據十種不同配方組成的錠劑,試著找出一種快速 溶離釋放的錠劑配方,獲得天麻錠劑製造之最適宜條件。 另外實驗設計上,是選用一個溶離釋放較佳的錠劑配方,利用兩種不 同乾燥方法,測其產物 GA 含量,並進一步比較兩種處方在製程上的差異 性。 綜合以上因素,盡可能充分利用現今科技,以新穎的並保持傳統中醫 藥的優秀特色,發揚創新並符合社會需求。. 24.
(40) 第三章 實驗藥材及研究方法 第一節 實驗藥材. 一、藥材 本實驗所使用之中藥材是購台中欣榮藥材行: 蘭科植物天麻 Gastrodiae elata Blume 之乾燥塊莖。. 二、藥品及試劑 天麻素 (Gastrodin, GA) 本所吳金濱教授研究室抽出品,純度 90 % 天麻苷元 (ρ-Hydroxybenzyl alcohol, HBA) Sigma 乙醯胺酚 (Acteaminophenol, ASA) Sigma 甲醇 (Methanol, CH3OH) Merck 乙腈 (Acetonitrile) Merck 鹽酸 (Hydrochloric acid, HCl) Merck 氫氧化鈉 (Sodium hydroxide, NaOH) 德國 R.D.H. 磷酸二氫鉀 (Potassium dihydrogen phosphate, KH2PO4) Merck. *使用於高效液相層析儀之水 (Mini-Q) 經 Millipore 公司之 Milli-RO-60 製造之純水,再經 Millipore 0.45µm 過濾膜過濾。. 三、儀器及材料 1. 高效液相層析儀之裝備 幫浦 (Pump):Jasco Model PU-980 偵測器 (Detector):Jasco Model UV-970 Intelligent UV/VIS 積分儀 (Integrator):Scientific Information Service Corporation Integrator 自動取樣機 (Auto Sampler):Jasco Model AS-950 印表機 (Printer):HP Laserjet 1200 25.
數據


Outline
相關文件
In the algorithm, the cell averages in the resulting slightly non-uniform grid is updated by employing a finite volume method based on a wave- propagation formulation, which is very
Al atoms are larger than N atoms because as you trace the path between N and Al on the periodic table, you move down a column (atomic size increases) and then to the left across
substance) is matter that has distinct properties and a composition that does not vary from sample
- Informants: Principal, Vice-principals, curriculum leaders, English teachers, content subject teachers, students, parents.. - 12 cases could be categorised into 3 types, based
Then, we tested the influence of θ for the rate of convergence of Algorithm 4.1, by using this algorithm with α = 15 and four different θ to solve a test ex- ample generated as
Particularly, combining the numerical results of the two papers, we may obtain such a conclusion that the merit function method based on ϕ p has a better a global convergence and
Then, it is easy to see that there are 9 problems for which the iterative numbers of the algorithm using ψ α,θ,p in the case of θ = 1 and p = 3 are less than the one of the
The CME drastically changes the time evolution of the chiral fluid in a B-field. - Chiral fluid is not stable against a small perturbation on v