第一章 前言
細胞凋亡是真核細胞自然死亡的方式,就個體而言,藉細胞凋亡可 以主動去除那些受傷、老化或不要的細胞,以維持生物體的發育和細胞 恆定。在一些人類重要疾病,如癌症、後天免疫缺乏症候群和神經退化 性疾病等,細胞凋亡也扮演著關鍵角色,因此成為當前國內外研究的熱 門課題。
惡性腫瘤已長年佔據台灣十大死亡原因的第一名,而肝癌則是僅次 於肺癌而為癌症十大死因的第二名。由於台灣屬於全球肝癌高發生率的 國家,罹患肝癌的高危險群以三十五歲以上至六十歲的成年男性居多,
對家庭影響很大,而且許多肝癌患者會尋求西醫治療以外的中醫治療或 服用以口相傳的偏方,加上西藥治癌藥物容易產生許多嚴重的副作用,
因此醫界便期待從傳統中草藥,尋找出較良好的取代或輔助藥物。
絞股藍是一種兼俱扶正補益與清熱解毒作用的抗癌中草藥,文獻顯 示其萃取物絞股藍總皂 有保肝、抗癌等廣泛功能,臨床上常用於治療 肝癌的中醫複方中。近年來的研究顯示,許多抗腫瘤藥物都可以誘導腫 瘤細胞凋亡,可能這些藥物具有抑制腫瘤細胞生長的功能,因此絞股藍 能否透過誘導細胞凋亡的機轉對抗肝癌細胞,來保護肝臟功能,是個令 人感興趣的議題。
中醫現代化是當今中醫學界推動的重點,由歷史發展亦可看出中醫
學的發展是不斷在時代學術衝擊與融合中求進步。因此本研究目的是希
望藉由細胞凋亡的相關實驗,來觀察絞股藍總皂 是否能誘導肝癌細胞
株 HA22T/VGH 和 HepG2 產生細胞凋亡作用,並體外培養周邊淋巴細胞 CD4
指標,觀察是否對此人體正常組織細胞有無毒害作用。
第二章 文獻探討
一、細胞凋亡背景
當細胞受到缺氧或外來毒素傷害時,最常發生的死亡形式為壞死,
此時細胞腫脹,膜完整性消失,細胞崩解且內容物釋出。但是在1960年 代Kerr及其同僚提出研究老鼠肝門靜脈結紮後的肝細胞變化時,觀察到 一種細胞縮小、胞膜完整、無發炎反應的另一種細胞死亡方式,在1972 年正式命名為細胞凋亡。由於細胞凋亡小體很快被吞噬掉,不易於體內 研究,且當時欠缺生化標記,因此沈寂了一陣子,直到1990年代以後得 力於線蟲類(nematode)及果蠅的遺傳知識,細胞凋亡的研究遂如成後春 筍般的興起。細胞凋亡是真核細胞自然死亡的方式,因為這種方式有別 於壞死模式,因此又有細胞計劃性死亡(programmed cell death)之稱。
就生理意義而言,生物個體藉細胞凋亡可以主動去除那些受傷、老化或 不要的細胞,以維持生物體的發育、細胞恆定。例如在胚胎發育過程,
差不多有一半的神經細胞與周邊組織細胞連接後,因得不到足夠周邊組 織分泌的特異性神經生長因子(specific neurotrophic factor)而死 亡。在病理意義上,一些人類重要疾病,如癌症、後天免疫缺乏症候群 和神經退化性疾病等,與細胞凋亡作用的過亢或不足扮演著關鍵角色,
因此細胞凋亡成為當前國內外研究的熱門課題
(1-3)。
二、細胞凋亡的研究方法
辨別細胞是否進行細胞凋亡,目前有幾種指標可以參考。首先就細 胞型態而言,由於細胞凋亡活化了許多內生性的蛋白質 (endogenous proteases),導致細胞骨架的破壞(cytoskeletal disruption)、細胞 萎縮(cell shrinkage)、細胞膜上會有泡狀物(membrance blebbing)的 產生,並且有染色質濃縮(chromatin condensation)的現象
(4,5)。
另 外 就 細 胞 核 的 變 化 而 言 , 由 於 活 化 了 細 胞 內 核 酸 分 解
(endonuclease),造成此酵素吸附到DNA的核間區域(internucleosomal
spacer DNA regions),使核內DNA斷裂成片段,此結果可藉由洋菜凝膠
電泳(agarose gel electrophoresis)觀察到DNA呈梯狀的排列
(6)。以往 的研究視DNA梯狀排列為細胞凋亡的正字標記,DNA斷裂過程可能分為二 期,第一期是把基因體以domain cleavage的方式切成200-300及30-50 kb的斷片,此期的內核酸分解 稱為domain nuclease;第二期則由 fragmentation nuclease,切位在nucleosome之間的連接處,而形成 180-200 bp的DNA梯狀排列規則斷片
(3)。
流式細胞儀(flow cytometry)的應用是另一項較新的技術,其配有 15微瓦的氬離子電射,發射出488 nm波長的藍光,細胞樣本附著能被488 nm藍光雷射激發的螢光染料後,會發散出或綠、或橙紅、或深紅色的螢 光 , 而 被 儀 器 所 分 析 。 常 用 來 定 量 DNA 的 染 劑 為 Propidium Iodide (PI),能嵌入雙鏈DNA及RNA的鹼基對中,由於PI不能進入細胞膜,因此 進行DNA分析時,需先在細胞膜上打孔,再除去細胞中的RNA,此法常用 來做DNA細胞周期分析
(7)。
正常人體的DNA是雙套的(2N),由於凋亡細胞DNA斷裂成小片斷,因 此會比正常G0/G1期細胞有較低的染色密度(stainability),經PI染色 後,可將凋亡細胞顯現出來,而在直方圖中形成sub G1 peak
(8,9,10)。同 樣 以 凋 亡 細 胞 的 DNA 受 內 核 酸 分 解 裂 解 現 象 , 運 用 細 胞 內 TdT (terminal deoxynucleotidyl transferase)的反應,將DNA斷裂切口的 3' 端 用 螢 光 標 記 過 的 特 殊 核 酸 BrDU 來 補 充 , 這 便 是 所 謂 的 TUNEL(TdT-mediated dUTP-dogoxigenin nick end labeling)分析法
(11)。
另外在活細胞的細胞膜只有內側含有phosphatidylserine,對淍亡 細胞而言,細胞膜尚未受到破壞,但會有phosphatidylserine移位到膜 外側面的現象,Annexin V是一種能與phosphatidylserine結合的蛋白 質,經FITC染劑可標示移位的胞膜外的phosphatidylserine,再合併以 PI對胞膜破損的壞死細胞進行染色,如此可區別活細胞、凋亡細胞及壞 死細胞三種細胞族群,可做為凋亡的早期變化之分析
(12)。
三、細胞凋亡相關因子
引發細胞凋亡需外源信號和內源性基因的調控,近年來的研究顯
示,許多抗腫瘤藥物都可以誘導腫瘤細胞凋亡,可能是這些藥物抑制腫
瘤細胞生長的機轉之一。實驗發現,在細胞凋亡過程中確有一些基因的 表現發生了改變,另一些基因則對凋亡起調控作用,以下即一些相關的 基因:
(一)細胞週期相關因子:cyclins、CDKs、CDKIs
在哺乳動物細胞周期進程中,從DNA複製到分裂期的轉變,存在一 系列的調節因子,例如調節G1期進到S期的cyclin 有cyclin D1-D3和E,
cyclin D1 會 與 細 胞 周 期 素 依 賴 性 激 (cyclin-dependent kinases, CDKs)之CDK4、CDK6結合,活化磷酸化激 ,調節細胞周期的中期G1期;
cyclin E與CDK2結合的複合物則是G1進展到S期的調節因子;至於一些 MTS/INK家族p15(INK4B)、p16(INK4A/MTS1/CDK4I)、p18、p19則是cyclin D-CDK複合物的抑制因子,而p21(WAF1)、p27(KIP1)則是cyclin D-CDK4 和cyclin E-CDK2的抑制因子
(13,14)。當細胞周期紊亂,出現異常失控傾 向,正常細胞會察覺此現象而產生凋亡反應,但若有其它致癌因子存在 下,有時會促進細胞的轉型與增殖
(11)。
(二)細胞凋亡的啟動者:Caspase蛋白脢家族
Caspase (Cystein-dependent ASPartase cleaving proteASE)為 一群能分解各重要結構如DNA與細胞結構體(cytoskeleton)之水解 總 稱
(15),目前被認為是起始程序死亡者。最早的元老caspase-1原稱為 IL-1b converting enzyme (簡稱ICE),是在尋找線蟲細胞凋亡重要基 因ced-3 在人類之同源基因時被鑑定出來
(16)。此家族目前至少已找到 十個成員,原來皆呈非活化狀態,待被切斷成小單位,重組後即成為具 活性之蛋白 ,可繼續分解其他之原形caspase或其他蛋白質,從而造 成一個連鎖反應。在此連鎖反應中,第一個出現不是caspase而被分解 的蛋白質是PARP (poly ADP-ribose polymerase),具DNA修補及遭逢壓 力下檢查基因體功能
(17,18)。接下來被分解蛋白質中有一類被稱為DNA裂解 因子(DFF),DFF受到caspase-3剪切後成為活化態,進而攻擊nucleosome 間之DNA,造成典型的梯形
(19)。
caspase-1與caspase-3分別代表此類 的兩大次集團。前者是在凋
亡決定點的上游,在線蟲有ced-4,人類則為caspase-1,4,5;後者則在 此決定點之下游作為執行處決者,在線蟲有ced-1,2,5,6,7,8,10,人類 則為caspase-2,3,6,7,8,10
(20)。有強烈證據支持這兩大事件的故事主要 發生在粒線體上
(21)。而生與死兩歸途的掌握,在線蟲則是由ced-9來裁 決,至於哺乳類動物則交在bcl-2家族上。
(三)生死路上之決定者:bcl-2家族
如前所述,bcl-2家族成員具有某些選擇生死之權力。這些路徑有 些與caspase有關(例如與Fas-L的結合),有些則無關(如DNA之破壞)。
bcl-2 (bcl: B cell lymphoma)是此家族第一個被發現的成員,可抑制 或阻斷多種因素引起的細胞凋亡,因而稱之為細胞凋亡抑制基因
(22)。同 源性研究證實bcl-2與線蟲ced-9基因為同源
(23)。隨著其餘成員的被發 現,現已知它們均具BH (Bcl Homology)結構,透過BH四個domain的排 列組合(每一成員帶一或多個BH domain),使它們分別具抑制或促進凋 亡功能。例如Bax在細胞內過度表現時,可形成bax-bax二聚體,此時與 p53基因產物一樣,促進細胞凋亡。bcl-2家族作用機制目前尚未明朗,
已知部份成員具穿膜區,很可能與粒線體、內質網等膜狀結構交換物質 有關。
(四)與免疫系統之互動:Fas/Fas-L
Fas (Apo-1; CD95)屬腫瘤壞死因子(Tumor Necrosis Factor,TNF) 家族及神經生長因子(Never Growth Factor, NGF)的一員,是一種貫穿 細胞膜的醣蛋白,以膜受體的形式存在,主要在胸腺、心、肺、肝、腎、
卵巢、活化的淋巴球等表達最多。其結合子Fas-L為一種Ⅱ型穿膜蛋白,
屬於TNF家族。Fas-L也可能分泌或脫落至細胞外,成為一種可溶性的功 能性活性分子
(24,25)。
當膜表面的Fas蛋白與其配體Fas L相結合後,可啟動細胞內一系列
導致凋亡的事件發生,對免疫反應的向下調控及T細胞毒殺作用扮演樞
紐的角色
(3)。bcl-2對生死的調控並非很完整,例如對於caspase上游的
訊號,就通常無法被bcl-2攔截。Fas/TNFR的訊號轉導系統因可直接作
用於下游之caspase,故可彌補此不足。生命體內多種組織和細胞均可 表現Fas,活化的成熟T細胞及HTLV-1,HIV及EBV等病毒轉化的T細胞可 大量表現Fas,某些腫瘤細胞也有Fas的表現。Fas-L的分布原只見於活 化的T細胞,最近在人睪丸、眼前房基底細胞及某些神經細胞中發現 Fas-L的表現。這些組織細胞可通過表現Fas-L來殺傷活化的Fas+的T細 胞,從而保護這些免疫赦免部位免遭T細胞的攻擊。最近發現,某些腫 瘤細胞也可表現Fas-L,在腫瘤的發生和免疫逃逸中具有重要意義
(2)。
(五)其它相關因子
p53:是一種分子量53kDa的轉錄因子,在正常的情況下,p53的表 現量很低,但當DNA異常時,p53蛋白及轉錄活動明顯增加,並刺激p21 蛋白的表現,使細胞停留在G0/G1期而不能進入S期,以進行DNA修補;
若DNA損傷嚴重無法修補時,則誘發細胞走向凋亡途徑,防止癌化。因 此p53有腫瘤抑制基因之稱,許多腫瘤細胞的p53基因多發生突變,使腫 瘤細胞具抗凋亡的能力,具較強的增毀及轉移能力。
myc:C-myc在一般的細胞屬於原致癌基因(proto-oncogene),對細 胞具有促進增殖及誘導凋亡的雙重作用,其機制與下游目標基因的調控 路徑不同,致使細胞走向不同的命運,而其它基因蛋白對C-myc的調控 也會導致不同反應,如活化C-myc會造成p53蛋白的累積,促進細胞凋 亡,但與Bcl-2同時存在於時,卻會讓C-myc致癌基因活化,表現細胞不 正常增殖現象
(22)。
四、肝癌簡介
惡性腫瘤已長年佔據台灣十大死亡原因的第一名,其中肝癌又是男 性癌症十大死因的榜首,女性癌症十大死因的第二位。肝癌分成由肝臟 本身長出來的原發性肝癌,以及由其他器官、組織轉移而來的轉移性肝 癌。原發性肝癌包括常見的肝細胞癌及肝內膽管演變的膽管癌,其他較 罕見的有肝臟胚細胞瘤、扁平上皮癌、類癌、膽道囊狀腺癌及血管肉瘤 管
(26)。
就全球肝癌盛行率而言,台灣屬於高發生率的國家,與肝癌相關的
危險因子包括肝炎病毒如 B 型和 C 型肝炎病毒、各種原因的肝硬化、黴 菌毒素如黃麴毒素、藥物及化學藥品毒品等。
依照肝癌細胞不同分化等級,可分為:
第一級:高度分化;癌細胞形態近似正常肝細胞。細胞體積較大,
胞漿豐富,嗜酸性染色;核圓形,具明顯核仁,有少數核分裂相,核漿 比例稍增大,腫瘤細胞呈小樑狀排列。
第二級:中度分化;癌細胞形態仍然與正常肝細胞相似。胞漿豐富,
嗜酸性;核增大,著色深,核仁明顯,核漿比例增大,核分裂相增多,
腫瘤細胞多排列成小樑狀結構,亦可見腺泡樣結構,腺腔內可見膽汁。
第三級:中度分化;癌細胞形態與正常肝細胞相距較遠。胞漿量減 少,嗜酸性增強;核大而不規則,染色質粗而不均勻,核仁大,核分裂 相多見,核漿比例明顯增大,見有多量的腫瘤巨細胞;腺泡樣結構和膽 汁少見。
第四級:低度分化;癌細胞形態變異甚大。胞漿少而嗜鹼;核大而 不規則,占據細胞大部,使核漿比例顯著增大。其細胞形態常顯多形性,
有圓形、奇異形、梭形和瘤巨細胞等。核仁不明顯或不見核仁。細胞間 失去連接性,排列紊亂,無一定結構
(27)。
西醫治療肝癌的方法,較常知的有開刀切除法、肝動脈栓塞術、局 部酒精或冰醋酸注射等,有些療法如全身性化學療法、放射線療法、微 波凝固壞死法、冷凍療法、免疫療法、肝臟移植等仍未普遍。另外在台 灣,許多肝癌患者會尋求西醫治療以外的中醫治療或服用以口相傳的偏 方治療
(28)。
傳統中醫學認為肝癌屬於「肝積」 、 「癥瘕」 、 「肥氣」 、 「膨脹」 、 「癖 黃」等範疇。 《靈樞.百病始生篇》說「積」症的成因是: 「外中於寒而 內傷憂怒」,而《醫宗必讀.積聚篇》則提到: 「積之成也,正氣不足,
而後邪氣踞之」,因此正氣虛損,邪氣乘襲,蘊結於肝,肝氣鬱結,氣 機受阻,血行不暢,痰瘀相互,形成痞塊,乃致肝癌。至於治療「積聚」,
《醫學心悟》提出:「治積聚者,當按初中末之三法焉。邪氣初容,積
聚未堅,宜真清之,而後和之;若積日久,邪盛正虛,法從中治,須以
補瀉相兼為用;若塊消積半,便以末治,即住攻擊之藥,但舌中養胃導
正經脈,俾榮衛流通,而塊自消矣。更有虛人患積者,必先補其虛,珍 其脾,增其飲食,然後用藥攻其積,斯為善治,此先攻後補之法也。」
(29)
依中醫藥辨證論治治療原則,常見的肝癌證型有瘀毒不化型、熱毒 蘊結型、正虛邪實型。
瘀毒不化型:主症見肝臟腫大,質地堅硬,包塊不平,肝區疼痛,
胃納著減,脘腹飽脹,面色失華,手見肝掌,頸項部或前胸及面部呈現 蜘蛛痣;舌有斑紫色,苔白厚,脈象沈弦。治法以化瘀解毒,消癥散結。
方用大黃蟅蟲丸加減。
熱毒蘊結型:主症見腹脹肝痛,肝脾腫大,腹壁靜脈怒張,胸悶痞 滿,飲食難下,不能平臥,坐臥不安,煩熱,噁心嘔吐,大便乾,小便 少,口乾渴,少津液;舌質燥,苔黃膩,脈沉細弦數。治法以清熱解毒,
消癥散結。方用龍膽瀉肝湯加減。
正虛邪實型:主症凡呈虛象,肝大腹脹,疲乏無力,少食懶言,精 神不振,腰酸腿軟,心悸氣短,呼吸無力,轉側艱難,面色晦暗,形體 消瘦,或有浮腫,尿少便溏;舌質艷紅或胖,少苔,脈沉細而弱。治法 以補虛袪邪,消癥散結。方用香砂六君子湯合理中湯加減
(30)。
臨床上隨醫者接觸觀察到的患者不同,另歸納為肝鬱脾虛型、氣滯 血瘀型、肝膽濕熱型和陰虛內熱型
(31)。
至於常用來治療肝癌的中藥,清熱解毒類的有牛黃、地龍、半枝蓮、
半邊蓮、蚤休、白花蛇舌草、龍葵、大黃、蟾蜍等;活血化瘀類的中藥 有丹參、莪朮、蜈蚣、水蛭、全蠍、麝香、斑蝥等;軟堅散結類有黃藥 子、澤漆等;扶正抗癌類有人參、黨參、黃耆、白朮、靈芝、龜板、甘 草、補骨脂、薏苡仁等。
五、絞股藍簡介
絞股藍,依本草學文獻
(32)的敘述,其別名有五葉參、七葉膽、小苦 藥、甘茶蔓、公羅鍋底等;來源為葫蘆科絞股藍屬植物絞股藍 Genostemma pentaphyllum (Thunb.) Makino,以根狀莖入藥。
形態特徵為多年生草質藤本,長約 1-1.5 米。根狀莖細長橫走,長
50-100 厘米,直徑粗長者可達 1 厘米,有分枝或不分枝,節上生鬚根。
莖細長,節部具疏生細毛。葉互生,通常由 5 小葉組成鳥趾狀複葉,有 時為 3 片或 7 片,小葉片卵狀長橢圓形或卵形,有小葉柄,中間小葉片 長 4-8 厘米,寬 2-3 厘米,先端圓鈍或短尖,基部楔形,下面脈上有短 毛,兩側小葉成對,著生方同一小柄上,較小。夏季開黃綠色花,圓錐 花序腋生,疏鬆,長 9-15 厘米;花單性,雌雄異株,花萼細小;花冠 裂片披針形,先端尾狀長尖,長約 2 毫米。漿果圓形,綠黑色,徑 6-8 毫米,上半部具一橫紋。種子長橢圓形,長約 4 毫米,有皺紋。
生境分布主要生於山間的陰濕環境,以山間林下陰濕而有亂石的環 境最為常見,分布於長江以南各省區。
采集一般是在秋季采集,洗淨,曬乾,研粉備用。
其化學成分自從 1976 年開始,日本學者報告從絞股藍中水解得到人 參二醇及 2α-羥人參二醇。以後報告從皂 中分離出多種達瑪烷皂 , 至目前為止,已報告分離得到 80 多種皂 ,分別命名為絞股藍 GypenosideⅠ-LⅩⅩⅨ,其中Ⅴ經 50%醋酸水解可得到人參皂 -Reg3,
Ⅰ、Ⅱ、Ⅴ、Ⅵ、Ⅶ、Ⅸ、Ⅹ、ⅩⅠ、ⅩⅢ、ⅩⅣ,經 水解可得到人 參皂 -F2,絞股藍皂 Ⅰ-ⅩⅦ經 水解後均可生成次級 20(S)-原人 參二醇-20-O-β-D 喃葡萄糖 ,該次級 與人參皂 中產生的次級
"化合物 K"的結構一樣。1981 年又從地上部分經醇提取分離得到的兩種 新的達瑪烷型皂 ,分別命名為 TN-1 和 TN-2。上述絞股藍 Ⅲ、Ⅳ、
Ⅷ、ⅩⅡ分別與人參皂 Rb1、Rb3、Rd、F2 結構相同。
其藥理作用,據現代研究發現有:
1. 絞股藍總皂 有明顯的降血脂作用,能使實驗性高血脂動物的血清 膽固醇和 油三酯明顯下降。
2. 有抗血小板聚集作用。
3. 其提取物對四氧嘧啶性糖尿病小鼠有明顯的降血糖作用,對老年大 鼠的糖耐量低下有明顯的改善作用。
4. 絞股藍總皂 靜脈註射 50mg/kg 對麻醉貓有顯著的降壓作用,對結
扎兔或大鼠冠狀動脈造成的心肌梗塞有保護作用,能增加離體家兔
心臟冠脈流量。
5. 有抗疲勞和抗寒作用,可提高常壓耐缺氧能力,並能增加應激狀態 下血漿 ACTH 含量。
6. 其總皂 對利卡因中毒有救治作用,可明顯延長小鼠存活時間。
7. 有明顯的鎮靜、催眠及鎮痛作用。
8. 對大鼠實驗性肝損傷有保護作用。
9. 對體外培養的肝癌、子宮癌、肺癌、黑色素肉瘤等癌細胞的增殖有 顯著的抑制作用,而對正常細胞無不良影響。
10. 有免疫增強作用。
11. 有抗衰老作用,能明顯延長果蠅壽命和體外培養的人皮膚細胞壽 命,能抑制血清及肝臟過氧化脂質的形成,提高過氧化物岐化酵素 活力。
12. 絞股藍有性激素樣作用,能使小鼠睪丸、精囊、前列腺和子宮的重 量增加。
13. 對大鼠實驗性胃潰瘍有保護作用。
14. 長期服用絞股藍可抑制實驗性膽石形成。
性味苦、寒。功能有清熱解毒,止咳祛痰、抗癌防老、降血脂等。常 用於治療慢性支氣管炎、傳染性肝炎、腎盂炎、胃腸炎、高血壓症等。
絞股藍最早文獻出處依清代《植物名實圖考》所述,是出自明代《救 荒本草》,作為饑荒時候充飢的食材,近世對它有「南方的人參」之稱
(33,34)
。由於絞股藍的臨床治療效果、藥理作用和化學成分都具有類似人 參的作用,具延緩衰老、抗疲勞、滋補強壯、養心安神、補腎溫陽等特 性,就中藥性能來說,一般寒性藥物的特性是具清熱、瀉火、解毒等作 用,因此有人認為應將絞股藍歸為微溫性中藥
(34)。
至於其成分除類似人參皂 之外,尚有多醣類,主要由木糖、鼠李 糖、半乳糖、葡萄糖等組成;黃酮類化合物有蘆丁(Rutin)、商陸素 (Ombiun)等;此外含有天冬氨酸、穀氨酸、甘氨酸、纈氨酸、異亮氨酸、
精氨酸、賴氨酸等 17 種氨基酸,以及鉀、鈉、鎂、鋅、錳、鈣、磷、
硅等無機元素,和葫蘿蔔素等維生素。臨床常應用於治療慢性氣管炎、
白細胞減少症、肝炎、高血脂症、銀屑病及癌症等
(35)。
絞股藍在抗癌的研究上,大陸的文獻已有一些相關研究報導。體內 實驗方面,觀察到絞股藍皂 對小鼠 S180 實體瘤的生長有抑制作用
(36); 以及大田絞股藍和新鮮絞股藍可使艾氏腹水癌小鼠生命延長率達 46.6%
和 40.7%
(37)。體外實驗方面,顯示絞股藍皂 對 S180 細胞株有直接滅殺
作用
(36);絞股藍總皂 在固定濃度下,對不同細胞株有不同的抑制作
用,其中對肺癌細胞株 A549、Calul、592/9 的抑制作用明顯強於子宮 頸癌 HeLa s3 及結腸癌 Colo205
(38)。絞股藍也被用在對癌前病變及抗誘
變的研究
(39,40),並以複方形式應用在臨床,顯示能使癌症患者的復發轉
移和死亡率皆降低
(41),及提高手術放療後的五年存活率
(42)。
第三章 材料與方法
一、細胞株培養
肝癌細胞株 HepG2 及 HA22T/VAH 自液態氮中取出解凍,培養 在 含 10% 小 牛 血 清 ( 購 自 JR 公 司 ) 、 0.02 mg/mL 慶 大 黴 素 (gentamycin) 、 0.1mM 非 必 需 胺 基 酸 、 2 mM L- 穀 胺 酸 (L-glutamine) 的 DMEM (Dulbecco ’ s Modified Eagle ’ s Medium)內 (皆購自 GIBCOBRL, USA)。以 75T 培養瓶培養,每隔 2-3 天作一次繼代培養。繼代培養時,先以 Trypsin-EDTA 緩衝液 (購自 GIBCO BRL, USA)處理細胞,使之自附著面脫離,繼以含血 清緩衝液終止 Trypsin-EDTA 的反應,整個過程在無菌操作檯操 作。處理後細胞置於 37
0C 恆溫,飽和濕度的培養箱,並供以 5% CO
2。
二、藥物配製
絞 股 藍 皂 的 萃 取 : 取 絞 股 藍 (Gynostemma pentaphyllum [Thunb.] Makino)莖葉,以 70%甲醇浸漬抽取,重覆六次,合併抽 出液,經減壓濃縮後,所得之粗抽出物用二氯甲醇萃取,去除低 極性物質,再以正丁醇萃取,所得正丁醇部分即為絞股藍皂
(43,44)
。再經冷凍乾燥法保存之。實驗時將絞股藍皂 溶於 PBS buffer 中,再以 0.2 ìm 濾膜過濾以達無菌狀態。
三、細胞生長抑制試驗
將 HepG2 和 HA22T/VGH 等肝癌細胞株細胞培養在 96 well
plate (購自 Corning 公司, USA),每個 well 含 1x10
6個細胞,隔
夜培養之,待細胞附著後,抽出原有培養基,加入含不同濃度的
測試藥品的培養基繼續培養,使之作用不同時間(6~72 小時)。吸
去 上 清 液 , 加 入 MTT (3-(4,5-dimethyl thiazol-2-yl)
2,5-diphenol tetrazolium bromide) proliferation kit (購自
Boehringer Mannheim, Germany)每個 well 加 10 ìL;4 小時後,
再加入清洗液(solubilization solution) 100 ìL;隔夜作用後,
再 以 免 疫 酵 素 螢 光 儀 (MRX microplate reader, Dynatech Laboratories, Germany)測量結果
(45)。(參考圖 3.1)
四、細胞存活率分析
比較經絞股藍總皂 處理與未用藥物處理,所存活細胞的比 率,即得絞股藍總皂 對肝癌細胞株 HepG2 和 HA22T/VGH 的影響,
其計算公式如下
(46):
藥物處理之測量值 - 背景值
細胞存活率 = ──────────────── X 100%
未經藥物處理之測量值 - 背景值 五、DNA 裂解與電泳分析
將約 1x10
7個細胞以 0.5 ml 溶解液(lysis buffer),於 4
0C 下作用約 20 分鐘,將細胞取至微離心管,離心使細胞沈澱;取上 清液,加 0.1 mg/mL proteinase K,於 50°C 水浴作用 24 小時後,
加入 RNase A 50 ìg/mL,再於 50°C 作用 1.5 小時;再以苯酚:
氯仿為 1:1 比例萃取細胞溶解液,混合均勻,13000 rpm 在 4
0C 下 離心 10 分鐘後,取上層溶液,加入 2-propanol 至最後濃度為 50%;
加入 20 mg 肝醣(glycogen) 1 ìL,於-20
0C 下靜置隔夜以沈澱 DNA。電泳分析前,取適量 DNA 溶於 TE buffer,置於 2% 洋菜凝 膠中進行電泳分析
(47,48)。(參考圖 3.2)
六、對細胞生長周期的影響
將約 1x10
6個細胞收集在 1.5 mL 的微離心管(Eppendorf tube),加 入 0.5 mL PI stain solution A (50
ìg/mL propidium iodide, 3%
polyethyleneglycol 6000, 0.1% Triton X-100, 1 mg/mL RNaseA, 4 mM
citrate buffer pH7.2) 混勻後置於 37
0C 作用 30 分鐘,再加入 0.5 mL
solution B (50
ìg/mL propidium iodide, 3% polyethyleneglycol 6000,
0.1% Triton X-100, 0.4 M NaCl, pH 7.2)(以上試劑購自 PharMingen,
USA),儲存於 4
0C 至少一小時,經 0.45
ìm 濾膜過濾後,以流式細胞儀 FACScan(Becton Dickinson, Germany) 進行分析
(49)。(參考圖 3.3)
七、分離周邊淋巴球
抽取受檢者的血液 10 mL,放入含 heparin 的綠頭試管。將血液分 兩管,沿管壁輕輕放入已含 5 mL Ficoll-paque 淋巴細胞分離液的試管 內,離心 2500 rpm,20 分鐘。沿管壁用吸管抽中層乳白色細胞層,加 入 PBS 10 mL,離心 1500 rpm,15 分鐘。倒掉上清液,加入 PBS 至 10 mL,
輕拍底部使沈澱散開,再清洗一次。離心 1000 rpm,10 分鐘。儘量倒 乾上清液。加入 RPMI 1640 細胞培養液,培養之。
八、Annexin Ⅴ染色
用 PBS 清洗細胞兩次,再加 1X binding buffer(0.1 M HEPES, pH 7.4; 1.4 M NaCl; 25 mM CaCl
2)於含周邊淋巴細胞的懸浮液,取出 100 ìL 的溶液,依比例加入 Annexin Ⅴ 和 Vital Dye 染劑,以及要觀察 的 CD marker 抗原,避光室溫靜置 15 分鐘,每個試管加入 400 ìL 的 1X binding buffer,在 1 小時內用流式細胞儀分析。再將分離的周邊淋 巴分空白對照組、絞股藍皂 處理組、HbsAg 處理組、HbsAg 加絞股藍 皂 處理組,培養 24 小時後,再以 Annexin Ⅴ染色及流式細胞儀分析
(12)
。(參考圖 3.4)
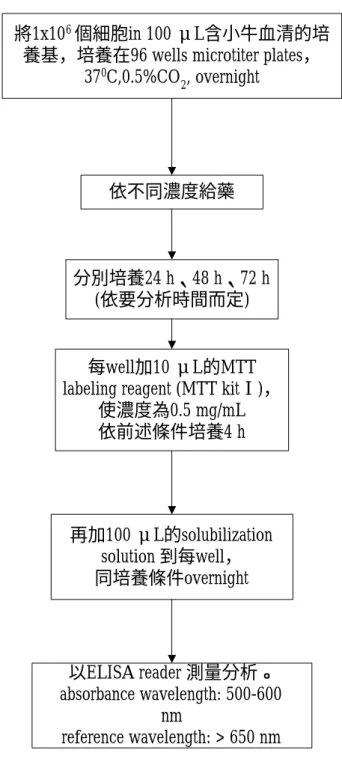
圖 3.1:細胞生長抑制試驗流程圖
將1x106 個細胞in 100 μL含小牛血清的培 養基,培養在96 wells microtiter plates,
370C,0.5%CO2, overnight
依不同濃度給藥
分別培養24 h、48 h、72 h (依要分析時間而定)
每well加10 μL的MTT labeling reagent (MTT kitⅠ),
使濃度為0.5 mg/mL 依前述條件培養4 h
再加100 μL的solubilization solution 到每well,
同培養條件overnight
以ELISA reader 測量分析。
absorbance wavelength: 500-600 nm
reference wavelength: > 650 nm
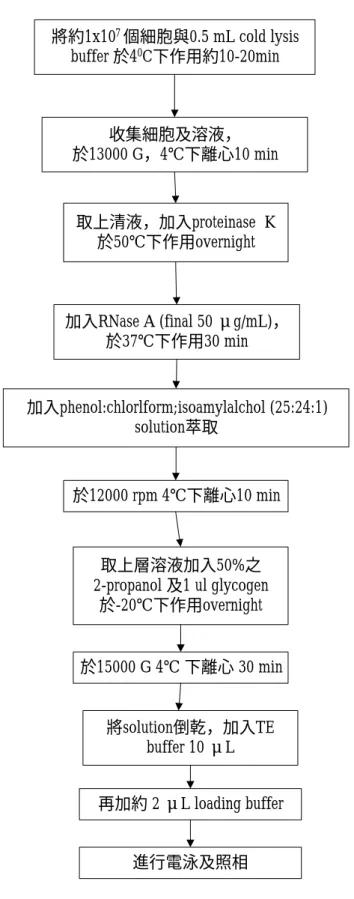
圖 3.2:DNA 裂解與電泳分析試驗流程圖
將約1x107 個細胞與0.5 mL cold lysis buffer 於40C下作用約10-20min
收集細胞及溶液,
於13000 G,4℃下離心10 min
取上清液,加入proteinase K 於50℃下作用overnight
加入RNase A (final 50 μg/mL),
於37℃下作用30 min
加入phenol:chlorlform;isoamylalchol (25:24:1) solution萃取
於12000 rpm 4℃下離心10 min
取上層溶液加入50%之 2-propanol 及1 ul glycogen
於-20℃下作用overnight
於15000 G 4℃ 下離心 30 min
將solution倒乾,加入TE buffer 10 μL
再加約 2 μL loading buffer
進行電泳及照相
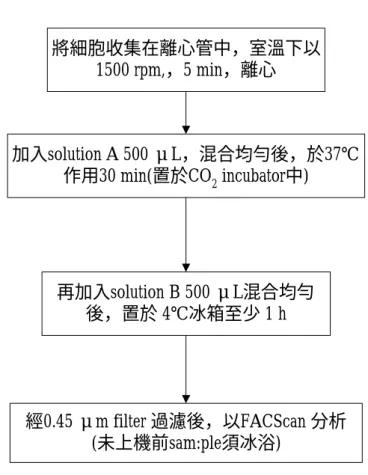
圖 3.3:細胞生長周期分析試驗流程圖
將細胞收集在離心管中,室溫下以 1500 rpm,,5 min,離心
加入solution A 500 μL,混合均勻後,於37℃
作用30 min(置於CO2 incubator中)
再加入solution B 500 μL混合均勻 後,置於 4℃冰箱至少 1 h
經0.45 μm filter 過濾後,以FACScan 分析 (未上機前sam:ple須冰浴)
圖 3.4:分離周邊淋巴球與 Annexin Ⅴ染色流程圖
PBMC↓抽取 10 mL 的血液,放入 Heparin tube (Green head)
↓加 5 mL Ficoll 至 10 mL 試管 (共 2 管)
↓將約 5 mL 血液沿管壁,小心放入含 5 mL Ficoll tube (共 2 管)
↓離心,2500 rpm ,20 min
↓抽中層 buffy-coat (2 tube) to 10ml tube
↓加入 PBS 至 10 mL (wash 1st)
↓mix
↓離心,1500 rpm,10 min
↓倒掉上清液
↓加入 PBS 至 10 mL (wash 2nd)輕拍底部使沉澱散開
↓mix
取 1 mL 至 Eppendorf tube 剩下 9 mL 放 15 mL 離心管
↓取 40 ìL 至 Eppendorf
↓加 40 ìL dye, mix
↓counting cells
↓取約 1x106 培養 24 hr 分不加藥組、
加絞股藍皂甘、
HbsAg+絞股藍皂甘組
↓剩餘放至 Eppendorf
↓離心
↓倒掉上清液,取 ppt
↓加 1 mL 1X binding buffer
↓1000 rpm, 10 min
↓倒掉上清液 加入 RPMI 1640
media culture
↓
避光下操作(單位 ìL)
1 2 3
CD4-FITC/CD8-PE 10
IgG-FITC/IgG-PE 5
Via-probe 10 10
Annexin V 5
CD maker Ab 5
Sample 100 100 100
Mix, 15min at RT in the dark
1X binding buffer 400 400 400
↓上 flow cytometry
第四章 結果
一、細胞生長抑制試驗
就 HepG2 細胞株而言,加入絞股藍總皂 0、100、200、300、400、
500、600、700、800、900、1000
ìg/mL 等不同的濃度,培養 48 及 72 小時後,藉由活細胞的胞膜才能與 MTT 染劑結合的特性來染色,經 ELISA reader 分析,顯示絞股藍總皂 濃度在 100 至 500
ìg/mL 時,對細胞生 長呈現部分抑制效應,而當濃度在 600
ìg/mL 以上,則細胞幾乎完全死 亡(表 4.1、圖 4.1)。
就 HA22T/VGH 細胞株而言,依次加入絞股藍總皂 濃度 0、100、200、
300、400、500、600、700、800、900、1000
ìg/ml 等不同的濃度,培 養時間分別為 6、12、24 及 48 小時,發現作用時間在 6 及 12 小時之後,
在濃度 500
ìg/mL 以上幾乎完全抑制效應;當作用 24 及 48 小時之後,
則在濃度 400
ìg/mL 即完全死亡。
為比較絞股藍皂 對不同細胞株的藥效,選用最高有效劑量之半 (50% effective dose; ED
50)為指標,發現此 ED
50隨藥物作用時間有所不 同。比較兩細胞株,絞股藍總皂 對 HepG2 作用 48 小時,其 ED
50值在 367
ìg/mL;對 HA22T/VGH 作用 48 小時,其 ED
50值在 300
ìg/mL。此外,
進一步實驗顯示在 50-150
ìg/mL 之較低濃度,培養 6、12、24 及 48 小
時後都出現刺激 HA22T/VGH 細胞株生長的現象(表 4.2、表 4.3、圖 4.2)。
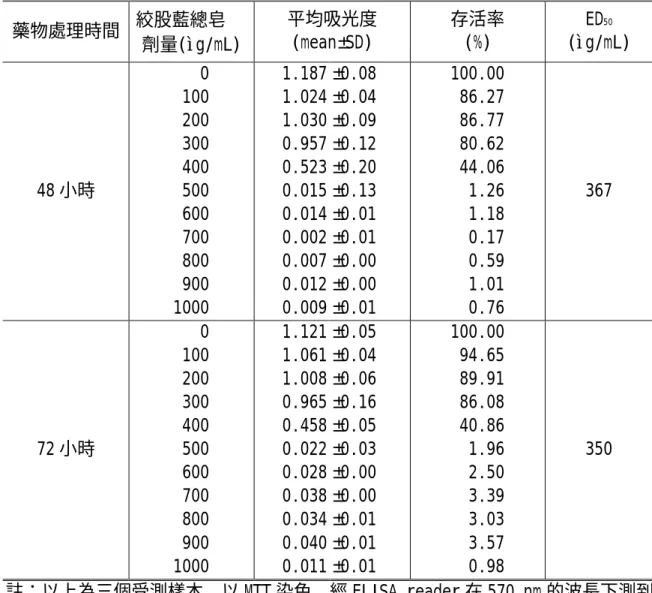
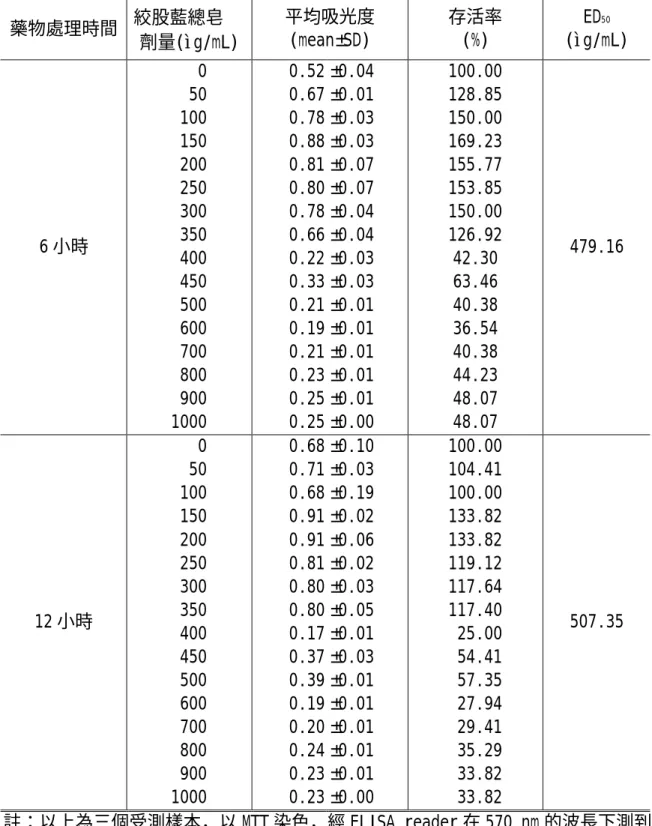
表 4.1:絞股藍總皂 作用 48 及 72 小時對 HepG2 細胞生長抑制試驗
藥物處理時間 絞股藍總皂
劑量(ìg/mL)
平均吸光度 (mean±SD)
存活率 (%)
ED50 (ìg/mL)
48 小時
0 100 200 300 400 500 600 700 800 900 1000
1.187 1.024 1.030 0.957 0.523 0.015 0.014 0.002 0.007 0.012 0.009
±0.08
±0.04
±0.09
±0.12
±0.20
±0.13
±0.01
±0.01
±0.00
±0.00
±0.01
100.00 86.27 86.77 80.62 44.06 1.26 1.18 0.17 0.59 1.01 0.76
367
72 小時
0 100 200 300 400 500 600 700 800 900 1000
1.121 1.061 1.008 0.965 0.458 0.022 0.028 0.038 0.034 0.040 0.011
±0.05
±0.04
±0.06
±0.16
±0.05
±0.03
±0.00
±0.00
±0.01
±0.01
±0.01
100.00 94.65 89.91 86.08 40.86 1.96 2.50 3.39 3.03 3.57 0.98
350
註:以上為三個受測樣本,以 MTT 染色,經 ELISA reader 在 570 nm 的波長下測到 其吸光度,並且消除在 650 nm 的背景波之吸光度。
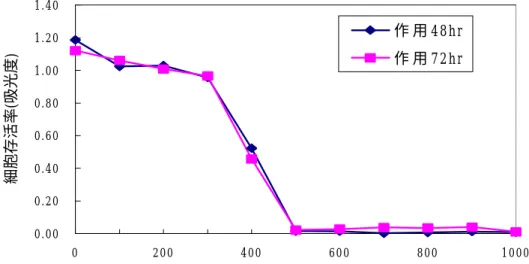
圖 4.1 :絞股藍總皂 對 HepG2 細胞生長抑制試驗 藥物處理後的 HepG2 細胞,繼續培養 48 及 72 小時後收集,以 MTT 染色處理,
經測光分析後的結果,顯示當絞股藍總皂 濃度超過 500
ìg/mL 時細胞完全死亡。作用 48 與 72 小時之 ED
50值分別為 367
ìg/mL 與 350
ìg/mL。
0.00 0.20 0.40 0.60 0.80 1.00 1.20 1.40
0 2 0 0 4 0 0 6 0 0 8 0 0 1 0 0 0
絞 股 藍 總 皂 甘 濃 度 (ì g / m L )
細胞存活率(吸光度)
作 用 4 8 h r 作 用 7 2 h r
表 4.2:絞股藍總皂 作用 6 及 12 小時對 HA22T/VGA 細胞生長抑制試驗
藥物處理時間 絞股藍總皂
劑量(ìg/mL)
平均吸光度 (mean±SD)
存活率 (%)
ED50 (ìg/mL)
6 小時
0 50 100 150 200 250 300 350 400 450 500 600 700 800 900 1000
0.52 0.67 0.78 0.88 0.81 0.80 0.78 0.66 0.22 0.33 0.21 0.19 0.21 0.23 0.25 0.25
±0.04
±0.01
±0.03
±0.03
±0.07
±0.07
±0.04
±0.04
±0.03
±0.03
±0.01
±0.01
±0.01
±0.01
±0.01
±0.00
100.00 128.85 150.00 169.23 155.77 153.85 150.00 126.92 42.30 63.46 40.38 36.54 40.38 44.23 48.07 48.07
479.16
12 小時
0 50 100 150 200 250 300 350 400 450 500 600 700 800 900 1000
0.68 0.71 0.68 0.91 0.91 0.81 0.80 0.80 0.17 0.37 0.39 0.19 0.20 0.24 0.23 0.23
±0.10
±0.03
±0.19
±0.02
±0.06
±0.02
±0.03
±0.05
±0.01
±0.03
±0.01
±0.01
±0.01
±0.01
±0.01
±0.00
100.00 104.41 100.00 133.82 133.82 119.12 117.64 117.40 25.00 54.41 57.35 27.94 29.41 35.29 33.82 33.82
507.35
註:以上為三個受測樣本,以 MTT 染色,經 ELISA reader 在 570 nm 的波長下測到 其吸光度,並且消除在 650 nm 的背景波之吸光度。
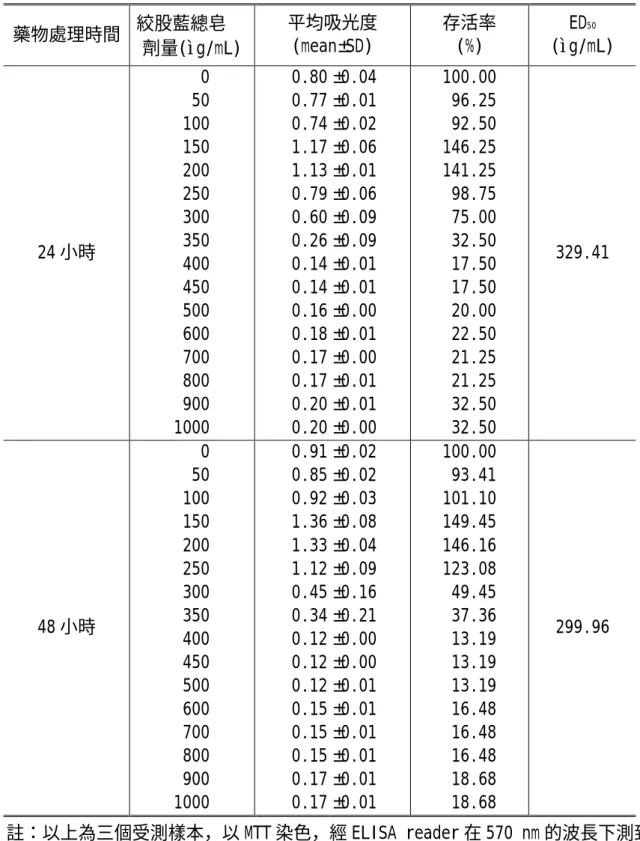
表 4.3:絞股藍總皂 作用 24 及 48 小時對 HA22T/VGA 生長抑制試驗
藥物處理時間 絞股藍總皂
劑量(ìg/mL)
平均吸光度 (mean±SD)
存活率 (%)
ED50 (ìg/mL)
24 小時
0 50 100 150 200 250 300 350 400 450 500 600 700 800 900 1000
0.80 0.77 0.74 1.17 1.13 0.79 0.60 0.26 0.14 0.14 0.16 0.18 0.17 0.17 0.20 0.20
±0.04
±0.01
±0.02
±0.06
±0.01
±0.06
±0.09
±0.09
±0.01
±0.01
±0.00
±0.01
±0.00
±0.01
±0.01
±0.00
100.00 96.25 92.50 146.25 141.25 98.75 75.00 32.50 17.50 17.50 20.00 22.50 21.25 21.25 32.50 32.50
329.41
48 小時
0 50 100 150 200 250 300 350 400 450 500 600 700 800 900 1000
0.91 0.85 0.92 1.36 1.33 1.12 0.45 0.34 0.12 0.12 0.12 0.15 0.15 0.15 0.17 0.17
±0.02
±0.02
±0.03
±0.08
±0.04
±0.09
±0.16
±0.21
±0.00
±0.00
±0.01
±0.01
±0.01
±0.01
±0.01
±0.01
100.00 93.41 101.10 149.45 146.16 123.08 49.45 37.36 13.19 13.19 13.19 16.48 16.48 16.48 18.68 18.68
299.96
註:以上為三個受測樣本,以 MTT 染色,經 ELISA reader 在 570 nm 的波長下測到 其吸光度,並且消除在 650 nm 的背景波之吸光度。
0.00 0.20 0.40 0.60 0.80 1.00 1.20 1.40
0 100 200 300 400 500 600 700 800 900 1000
絞股藍總皂甘濃度(μg/mL)
細胞存活率(吸光度OD值)
作用6小時 作用12小時 作用24小時 作用48小時
圖 4.2:絞股藍總皂 對 HA22T/VGH 細胞生長抑制試驗 以絞股藍總皂
藥物處理 HA22T/VGH 細胞株,培養 6、12、24 及 48 小時後
收集,以 MTT 染色處理,經 ELISA reader 分析後的結果。當藥
物處理時間為 6 及 12 小時之後,ED
50值約為 500
ìg/mL;藥物
作用 24 及 48 小時之後,當絞股藍總皂 濃度超過 400
ìg/mL
時,細胞生長完全死亡,而 ED
50值在 300 至 350
ìg/mL。
二、DNA 裂解與電泳分析
由 HA22T/VGA 細胞株生長抑制試驗所得結果,選擇最接近 ED
50值的 五個絞股藍皂 濃度 300、350、400、450、500
ìg/mL,分別培養 HA22T/VGH 細胞經 6、12、24、48 小時後收取細胞進行 DNA 裂解與電泳分析。發現 藥物濃度在 300
ìg/mL 時,培養 6 及 12 小時有出現 DNA 裂解片斷;藥物 濃度在 350
ìg/mL 時,培養 12 小時後電泳分析亦出現 DNA 裂解片斷;藥 物濃度在 400、450、500
ìg/mL 則培養 6、12、24 及 48 小時之後,則皆 未見到 DNA 裂解片斷(圖 4.3) 。
至於 G2 細胞株,則於上述 5 個藥物濃度及 6、12、24 及 48 小時四 個作用時間之後,均未見到 DNA 裂解片斷。
圖 4.3:絞股藍皂 處理 HA22T/VGA 的 DNA 裂解與電泳分析
三、對細胞生長周期的影響
對 HepG2 細胞株而言,分別加入濃度為 200、300、400、500
ìg/mL 的絞股藍皂 ,另外以無藥物處理組做對照組,經培養 48 小時之後,
以 PI 染色,經流式細胞分析儀來分析,對照組有完整的 G0/G1、M/G2 及 S 等生長期,當絞股藍皂 濃度增加到在 300、400
ìg/mL 對 HepG2 細胞株有顯著 G1 arrest 的現象,當藥物濃度增加到 500
ìg/mL 時,則 見 G0/G1 期的細胞亦減少,而凋亡的細胞增多(圖 4.4)。
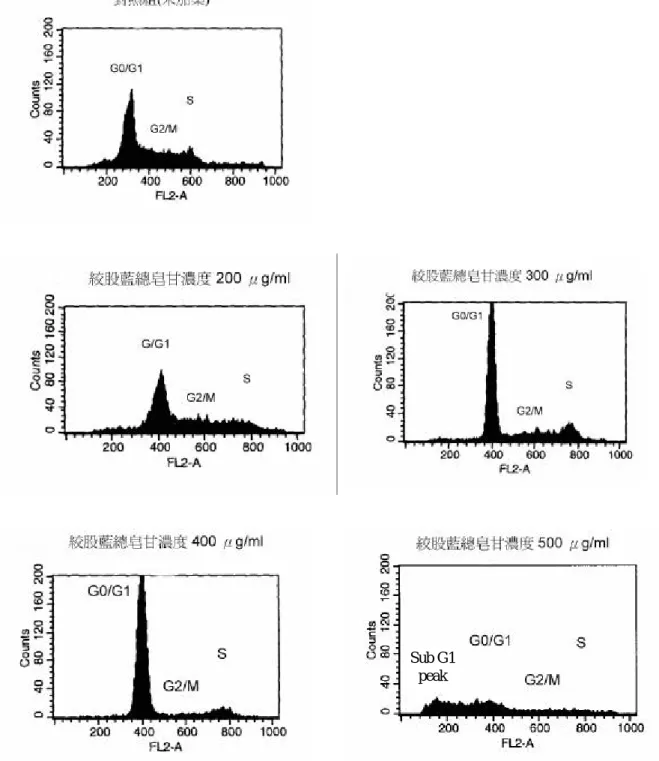
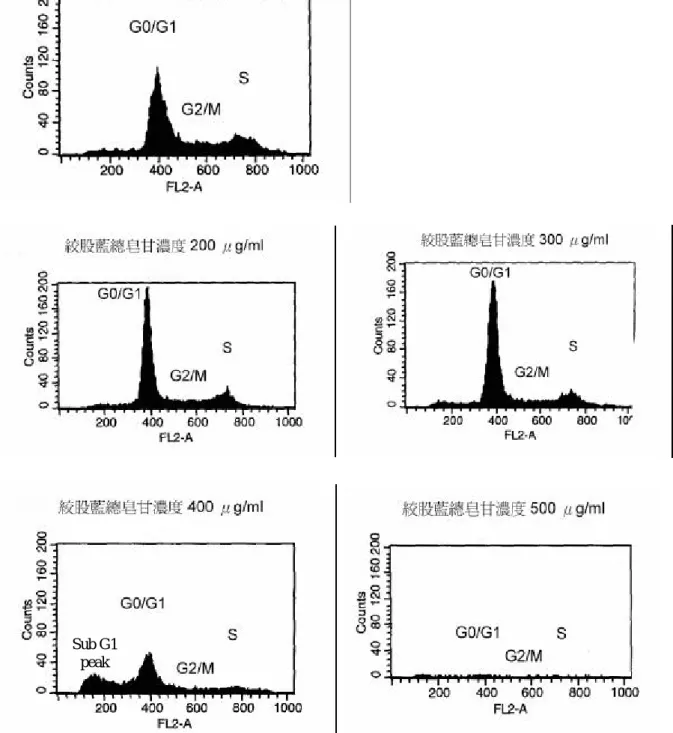
對 HA22T/VGH 細胞株而言,同樣加入濃度 200、300、400、500
ìg/mL 的絞股藍皂 ,並以無藥物處理組做為對照組,經培養 48 小時之後,
以 PI 染色,經流式細胞分析儀來分析,在藥物濃度 200 及 300
ìg/mL
有明顯的 G1 arrest 現象,當藥物濃度 400
ìg/mL 作用下,可見到凋亡
細胞增加,堆積形成 sub G0/G1 peak,而在濃度 500
ìg/mL 則見細胞大
量死亡(圖 4.5)。
圖 4.4:絞股藍皂 培養 48 小時對 HepG2 細胞生長周期的影響
Sub G1 peak
圖 4.5:絞股藍皂 培養 48 小時對 HA22T/VGH 細胞生長周期的影響
Sub G1 peak