國立宜蘭大學生物技術研究所 碩士論文
Institute of Biotechnology National Ilan University
Master Thesis
依據雙性螺旋胜肽之各項結構參數
設計開發具高度抗菌活性及選擇性之新穎抗菌胜肽 Rational design of novel antimicrobial peptides with enhanced
activity and selectivity based on structural parameters for amphipathic helical peptides
指導教授:陳威戎 博士
Wei-Jung Chen, Ph. D.
研究生:周宏達
Hung-Ta Chou
中華民國九十六年一月
I
致謝
本論文得以如期完成,首先要感謝指導教授-陳威戎博士,提供良好的學習環境,
並在實驗過程中不時給予指導解惑,在我最困惑的時候,適時的給予幫助,您給我的感 覺,更像是一位大哥,能在您的底下學習,使我受益良多。此外,也要感謝四位口試委 員,在公務繁忙之餘,還能對本論文詳加校閱釜正,使之更臻成熟,並在實驗期間所給 予的幫助,包括:台大醫學院生化所廖大修老師所提供之寶貴的意見及台大貴儀中心儀 器、郭村勇及林世斌老師對本實驗菌株的提供,而溫曉葳老師則幫助建立本實驗所需之 微脂體製備。另外,要感謝中研院臨海研究站的郭欽明主任及陳志毅老師,對我在抗菌 胜肽基礎知識方面的提供,對我之後的研究,有莫大的幫助。也要感謝國立宜蘭大學的 林佳靜所長及每一位老師們,經由你們的教導,使我更增廣了許多知識及見聞,為我未 來不管是就業還是再深造,立下良好的基礎。
此外也要感謝 PSF 實驗室中的各位學弟妹們,特別是 AMP 組的組員-愛玩蟲的阿 毛、把關東煮當主食的阿悳、最有"男人味"的惠君及貝貝,沒有你們的幫助,本論文就 無法順利的如期完成。另外,管家婆-小倩、電腦專家-明傑、電火球-阿春、愛耍任 性的元元、太陽神-伊翔、布袋戲狂-奶奶、有著濃厚高雄腔的妍君及三劍客-育袖、
淑婷及怡苓等學弟妹,使我在枯燥乏味的研究生生活中,添加一些樂趣。
在這研究生的九百多個日子當中,我也認識了一些同甘苦、共患難的好朋友,愛搞 笑的沖仔、森哥及洐煦,是我在籃球場上最好的搭擋、小安則是我在宜蘭的各名勝古蹟 中最好的嚮導及班上的每個同學,還有臨海研究站的明駿、捷玉、阿鏗、榮振、偉誠及 冠傑、台大張明富老師實驗室的魏文進學長及世斌老師研究室的怡君及小曼等,一起為 實驗鼓勵加油,為生活心事解憂,為我兩年半的研究生生活,增加了許多的色彩。其中,
特別要感謝嘉琦,每當實驗不順遂時總是能在我身邊激勵、鼓勵我,能陪我一起歡笑、
成長,希望在往後的日子中,能執子之手,攜手向前。
最後,要感謝的是我的爸媽及一路陪伴我的家人們,有你們的關心及支持,能使我 無後顧之憂的完成我的碩士學位,是支撐我走完全程的動力。
最終,將此論文獻給在我碩士生活中,每一位有給予我幫助的人,願你們與我共同 分享。
II
摘要
由於近年來抗生素過度的濫用,造成多種病原菌的抗藥性正迅速的增加當中,因此 許多科學家正致力於研究新型態的抗生素,以對抗這日益嚴重的抗藥性問題。目前有許 多的證據顯示最有潛力成為新型態抗生素的便屬於抗菌胜肽 (antimicrobial peptides;
AMPs) 了。
雙性陽離子抗菌胜肽屬於多種生物體的先天免疫系統及宿主防禦機制,它們造成細 胞死亡的機制可分為兩個階段 (1) 藉由本身所帶的正電,選擇性的結合上帶有負電的微 生物外膜,(2) 造成細胞膜滲透。大多數的抗菌胜肽在水溶液中是呈現鬆散的結構,但 和目標微生物作用時會褶疊形成雙性螺旋的結構並插入其膜內,導致破壞膜內外的電位 及離子梯度,造成細胞的洩漏,最後導致細胞死亡。
本實驗利用自行設計合成的人工抗菌胜肽當模型,固定長度為 20 個胺基酸,改變 其電荷、極性角度、疏水性及疏水性矩等四種結構特性,並利用其對各種不同病原菌之 抗菌活性 (MIC) 及對兔子紅血球細胞的溶血活性 (MHC) 來研究其結構特性的改變對 其抗菌活性、選擇性及微脂體膜的滲透性之影響,以期望改變結構參數能增加抗菌活性 及對原核的選擇性 (MIC/MHC)。
胜肽要扮演宿主免疫機制的一部分或要成為新型態的抗生素不僅要有強大的抗菌 活性還需要有高度的選擇性,由本實驗的結果發現,當抗菌胜肽的正電荷及極性角度增 加時,胜肽之抗菌活性會隨之增加,當抗菌胜肽的電荷為+4 而極性角度為 140° 時,
胜肽有最強之抗菌能力及膜滲透活性;而隨著胜肽疏水性以及疏水性矩的增加,會增加 溶血活性,結果反而降低了抗菌胜肽的選擇性。因此綜合以上結果,以人工抗菌胜肽-
GW-Q4 (Q=+4、θ=140°、H=-0.043、MH=0.344) 及 GW-H1 (Q=+4、θ=140°、H
=-0.115、MH=0.344),對革蘭氏陽性菌及革蘭氏陰性菌 (包括弧菌屬病原菌) 擁有最強 的抗菌效果及最佳的滲透能力和選擇性。基於此活體外分析結果,我們將進一步進行活 體內動物試驗,以驗證人工合成胜肽之臨床應用潛力。
關鍵字:抗菌胜肽、結構參數、微脂體
III
Abstract
The extensive use of classical antibiotics has led to the growing emergence of many resistant strains of pathogenic microorganisms. Therefore, the development of novel therapeutic agents that could overcome the resistance problem has become critical. Evidence suggested that antimicrobial peptides (AMPs) are of greatest potential to represent such a new class of antibiotics.
Cationic AMPs belong to the innate immune system and host defense mechanism of a wide range of living organisms. The largest group of AMPs comprises peptides which fold into an amphipathic α-helical conformation when interacting with the target. All of them exert their cell-lytic effect by a two-step mechanism consisting of (i) selectively binding to the negatively charged microbial surfaces with their cationic nature and (ii) membrane permeabilization. Largely unstructured in solution, linear peptides fold into an amphipathic helix upon binding and insert into the target membrane, leading to breakdown of the transmembranal potential and of ion gradients, thus causing leakage of cell contents, resulting finally in cell death.
In the current study, a series of cationic α-helical peptides of 20 a.a. were designed and synthesized based on four structural parameters, including charge, polar angle, hydrophobicity, and hydrophobic moment. Several methods were performed to describe the influence of these parameters on the antimicrobial (MIC) and hemolytic activity (MHC), and on the permeabilizing effect on model membranes (liposomes). The potential of these parameters to increase the antibacterial activity and to improve the prokaryotic selectivity (MIC/MHC) is assessed.
For a peptide to act as part of the host defense system or to be of pharmaceutical interest, high antimicrobial activity must be combined by low hemolytic activity. Our results indicated that the antimicrobial activity increased with increasing charge and polar angle, with charge of
+4 and polar angle of 140° exhibiting the highest antibacterial and membrane permeabilizing activity. Higher hydrophobicity and hydrophobic moment correlated with increased hemolytic activity, thus decreasing selectivity dramatically. Two of our de novo designed AMPs, GW-Q4 (Q=+4, θ=140°, H=-0.043, MH=0.344) and GW-H1 (Q=+4, θ=140°, H=-0.115, MH=0.344) exhibited highest antimicrobial activity and selectivity toward various Gram positive and negative bacteria, including several Vibrio strains. Based on these in vitro results, in vivo studies will be performed to further verify the clinical efficacy of our novel AMPs as potential antibiotics.
Key word: antimicrobial peptides (AMPs), structural parameters, liposome
IV
目錄
致謝………...………..I 中文摘要………...……….II 英文摘要………...…...……….III 目錄……….……….IV 表目錄………..………...……….VI 圖目錄……….VII 縮寫表………VIII
第一章 前言………...………1
1-1 抗菌胜肽簡介………...………..1
1-2 抗菌胜肽結構分類……….………2
1-2.1 雙性和疏水性螺旋胜肽 (amphipathic and hydrophobic α-helices)………..….3
1-2.2 β-褶板胜肽及較小的蛋白質 (β-Sheet peptides and small proteins)…………...5
1-2.3 擁有特殊胺基酸組成的抗菌胜肽………...6
1-3 抗菌活性機制………...……….……….7
1-3.1 抗菌胜肽目標特異性和選擇毒性的機制……….………7
1-3.2 膜的組成、疏水性作用力和極性………….………..8
1-3.3 抗菌胜肽作用機制……….……9
第二章 實驗目的……….………25
第三章 材料與方法……….………26
3-1 人工合成抗菌胜肽設計………...26
3-2 高效能液相層析試驗 (High Performance Liquid Chromatography;HPLC)…….28
V
3-3 最小抑制濃度測定 (Minimal Inhibitory Concentration;MIC)………..30
3-4 最小溶血活性濃度測定 (Minimal Hemolytic Concentration;MHC)………33
3-5 微脂粒 (liposomes) 的製備………34
3-6 磷脂質微粒 (liposome) 濃度定量……….………36
3-7 圓二色偏光光譜分析 (Circular Dichroism;CD)………...…39
3-8 Calcein leakage 試驗……….………..40
第四章 結果……….………43
4-1 抗菌胜肽之純度分析與分子量鑑定………43
4-2 抗菌活性試驗 (MIC)………...43
4-3 溶血活性試驗 (MHC)……….45
4-4 選擇性 (GM/MHC)……….………45
4-5 螺旋程度試驗………...46
4-6 Calcein leakage 試驗……….47
第五章 討論……….49
5-1 抗菌胜肽之抗菌活性……….………..49
5-2 抗菌胜肽之溶血活性………..…….51
5-3 抗菌胜肽之抗菌選擇性………..…….51
5-4 抗菌胜肽之二級結構與作用環境的關係………...52
5-5 抗菌胜肽與微脂體之交互作用………...53
第六章 結論與未來展望……….56
參考文獻……….………79
VI
表目錄
表1-1 由脊椎及無脊椎動物中所發現之螺旋型抗菌胜肽的結構特徵及抗菌活性……….4
表1-2 由脊椎動物與無脊椎動物中所發現之 β-褶板抗菌胜肽的結構特徵與抗菌活性,表 示抗菌胜肽擁有一至兩個雙硫鍵而形成 β-hairpin 的二級結構………6
表 1-3 胺基酸之疏水性值……….57
表 3-1 本研究之所使用抗菌胜肽之結構參數值及分子量……….58
表 4-1 疏水性組抗菌胜肽以 HPLC 分析時所得之滯留時間值………...59
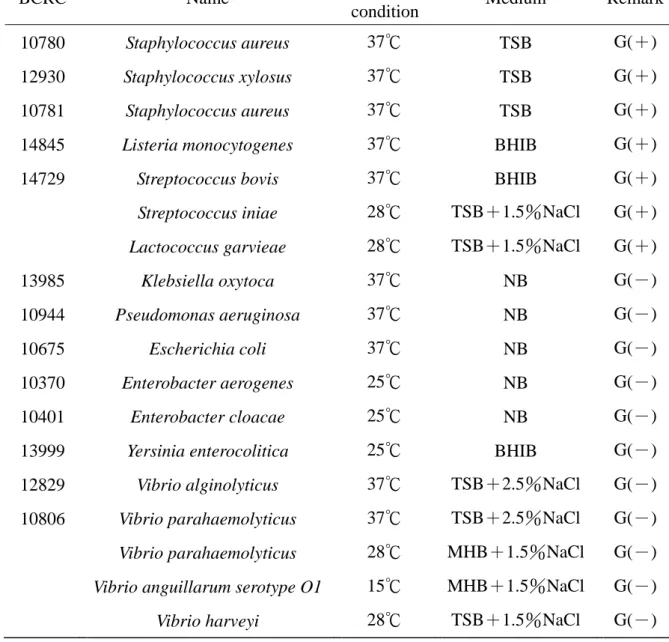
表 4-2 為本實驗中所研究之菌株……….60
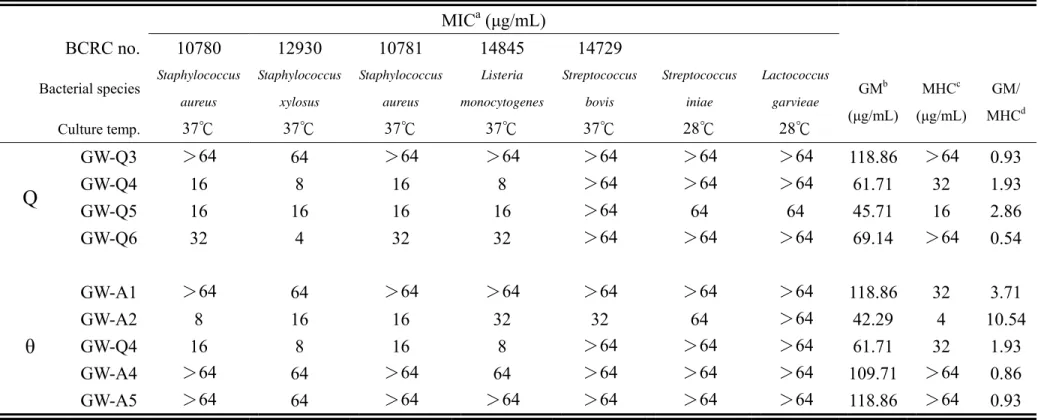
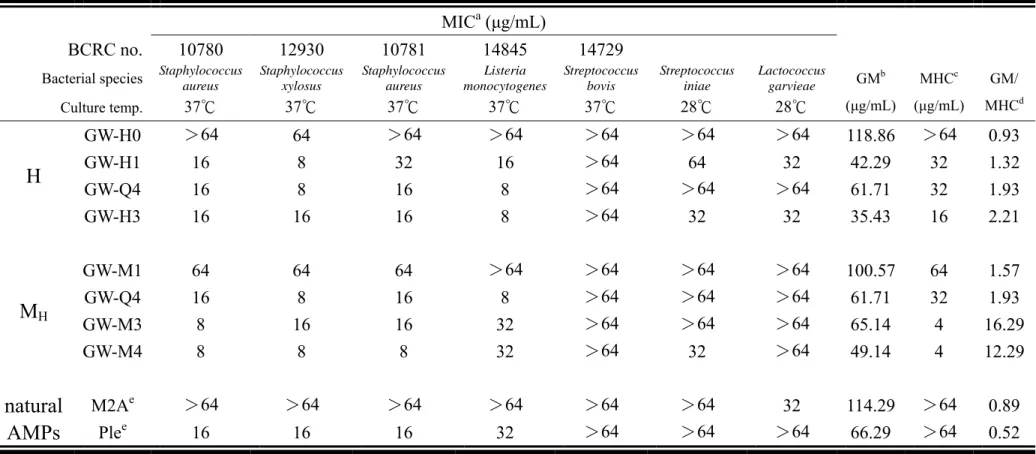
表 4-3 抗菌胜肽對革蘭氏陽性菌之抗菌活性 (MIC)、對兔子紅血球的溶血活性 (MHC) 及抗菌選擇性……….61
表 4-4 抗菌胜肽對革蘭氏陽性菌之抗菌活性 (MIC)、對兔子紅血球的溶血活性 (MHC) 及抗菌選擇性……….62
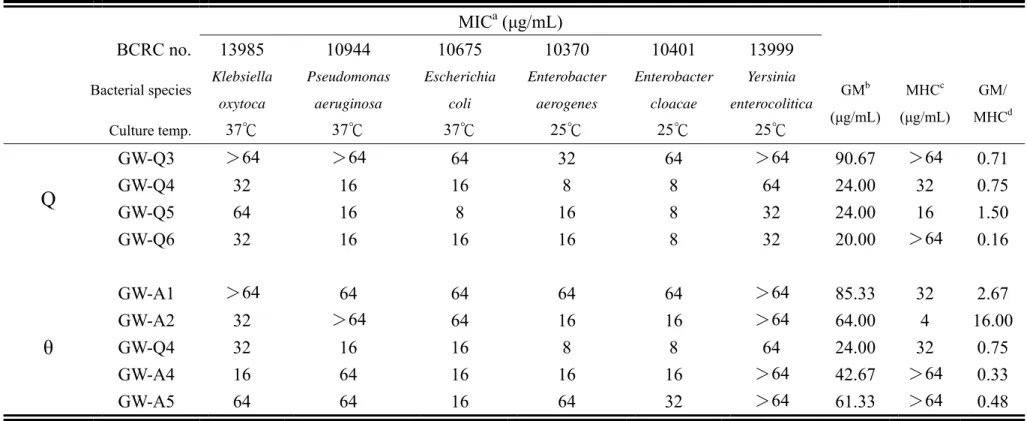
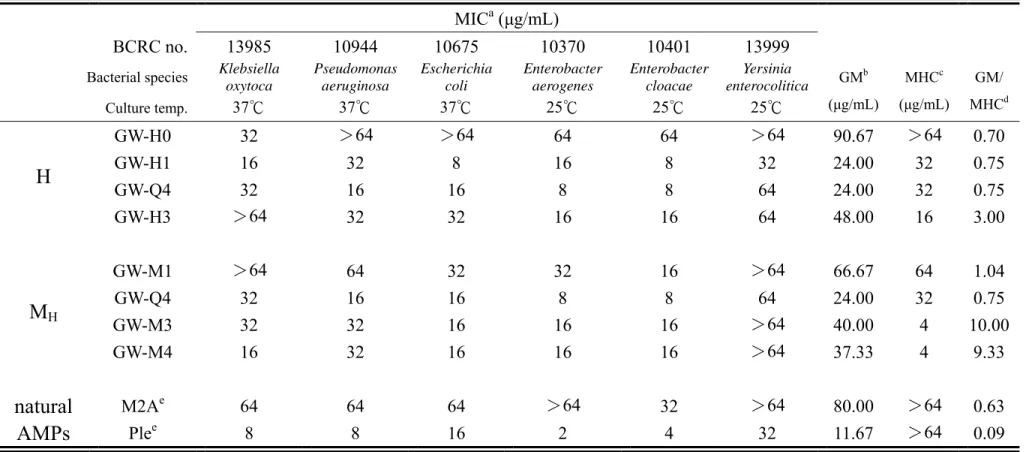
表 4-5 抗菌胜肽對革蘭氏陰性菌抗菌活性 (MIC)、對兔子紅血球的溶血活性 (MHC) 及抗菌選擇性……….………63
表 4-6 抗菌胜肽對革蘭氏陰性菌之抗菌活性 (MIC)、對兔子紅血球的溶血活性 (MHC) 及抗菌選擇性……….64
表 4-7 抗菌胜肽對弧菌屬革蘭氏陰性菌之抗菌活性 (MIC)、對兔子紅血球的溶血活性 (MHC) 及抗菌選擇性………...65
表 4-8 抗菌胜肽對弧菌屬革蘭氏陰性菌之抗菌活性 (MIC)、對兔子紅血球的溶血活性 (MHC) 及抗菌選擇性………...66
表 4-9 抗菌胜肽在不同溶液環境中之螺旋結構含量比例………...…67
表 4-10 抗菌胜肽造成各比例之微脂體中 calcein 滲透之最小濃度值 (LC50)…………68
VII
圖目錄
圖1-1 比較人類與微生物細胞膜的結構………...………..9
圖1-2 螺旋型抗菌胜肽和目標膜之間的作用………..……….10
圖1-3 螺旋型抗菌胜肽的膜滲透機制……….………..14
圖1-4 抗菌胜肽在細胞內的作用機制………..……….17
圖1-5 說明抗菌胜肽結構重要參數之間的相關性……….………..18
圖1-6 螺旋型抗菌胜肽-melittin 中每個胺基酸對螺旋疏水性矩的貢獻…………...……22
圖3-1 將自然界中所發現的螺旋抗菌胜肽,由其 N 端取 20 個胺基酸所做的胺基酸分佈 統計分析及序列模型……….27
圖 3-2 HPLC 溶液梯度流程………..30
圖 3-3 磷酸標準溶液曲線……….…………38
圖 3-4 螢光物質-calcein 自微脂體中洩漏之假想圖………42
圖 4-1 抗菌胜肽之 HPLC 分析圖譜 (各組擇一為例)……….……….69
圖 4-2 微脂體之粒徑分析圖……….………70
圖 4-3 各組抗菌胜肽在由 DOPC 所組成之微脂體中的 CD 光譜圖……….71
圖 4-4 各組抗菌胜肽在由 DOPC/DOPG 為 1:3 所組成之微脂體中的 CD 光譜圖...73
圖 4-5 不同濃度抗菌胜肽造成由 DOPC 所組成之微脂體中 calcein leakage 程度…….75
圖 4-6 不同濃度抗菌胜肽造成由 DOPC/DOPG 為 1:3 所組成之微脂體中 calcein leakage 程度………..77
VIII
縮寫表
abbreviation full text
△ψ electrochemical gradient θ polar angle
A amphipathicity AMPs antimicrobial peptides BHIB brain heart infusion broth
CD circular dichroism
CL cardiolipin DOPC 1,2-dioleoyl-sn-glycero-3-phosphocholine
DOPG 1,2-dioleoyl-sn-glycero-3-[phospho-rac-(1-glycerol)]
GM geometric mean of MIC values
H hydrophobicity HPLC high performance liquid chromatography LPS lipopolysaccharide M2A magainin
MH hydrophobic moment
MHB Mueller Hinton broth
MHC minimal hemolytic concentration MIC minimal inhibitory concentration
MW molecular weight
NB nutrient broth
NMR nuclear magnetic resonance PC phosphatidylcholine PE phosphatidylethanolamine PG phosphatidylglyceral Ple pleurocidin
SAR structure-activity relationships SM sphingomyelin
ST sterol
TFA trifluoroacetic acid TFE trifluoroethanol Tris tris(hydroxymethyl)aminomethane TSB tryptic soy broth
Q charge X conformation
1
第一章 前言
自從1928 年 英 國 科 學 家 弗 萊 明 (Alexander Fleming) 發 現 了 抗 生 素- 盤尼西林 (penicillin) ,至今已經有多種自然界的抗生素被發現,有些抗生素則是利用人為技術再 加以改良其化學結構以求增加療效,而這些抗生素也拯救了許多因病菌而感染的患者;
然而隨著這些藥物的大量使用,抗藥性的問題也隨之而來。由於近年來將抗生素廣泛使 用於醫藥、畜牧業及農業中,導致許多致病性微生物逐漸對已知抗生素產生抗藥性;雖 然到目前為止並不是所有的微生物都會對抗生素有抗藥性,但隨著時間的增加,微生物 所產生的抗藥性也在持續的增加當中 (McGahee & Lowy, 2000)。因此,對抗藥性沒有預 防的能力,而無法有效治療因細菌所引發的感染時,就必需早一步發現新的抗生素。換 言之,新型態抗生素的研究是非常迫切需要的!
在許多被提及的策略之中,研究自然界或人為產生作用在微生物細胞膜的抗菌胜肽 (antimicrobial peptides;AMPs) 是最有希望的。目前為止,有八百種以上這類型的胜肽 抗生素 (peptide antibiotics) 被純化分析出來,且其中一部份已進入臨床試驗 (Dubin et al., 2005)。如 Mak (2000) 等學者自血紅素 (hemoglobin) 及肌紅蛋白 (myoglobin) 中所 得到的抗菌胜肽-hemocidins,已分析到其擁有強大的抗菌活性,且 hemocidin 已成功地 應用在藥物方面,發展為新式的抗生素。因此抗菌胜肽的研究在目前醫學的發展及疾病 的控制中是刻不容緩的。
1-1 抗菌胜肽簡介
抗菌胜肽廣泛分布在許多的生物體中,不管是無脊椎動物 【如:Steiner (1981) 在 蜜蜂 (Apis melliferal) 刺裡的毒液中所發現的抗菌胜肽-melittins】、脊椎動物 【如:在 比目魚 (winter flounder) 中所發現的抗菌胜肽-pleurocidin (Cole et al., 1997)】、植物
【如:Fernandez (1972) 等學者在 wheat seeds 中所發現的抗菌胜肽-purothionins】甚 至在人類【如:Frohm (1997) 等學者在人類的嗜中性白血球 (neutrophils)、單核球細胞 (monocyte) 及 T 淋巴球細胞 (T lymphocyte) 中所發現的抗菌胜肽-LL-37】身上都可 以發現到抗菌胜肽的存在。生物體每天都暴露在會遭受到細菌及病原體感染的環境中,
為了保護自己而去抵抗這嚴苛的環境,便發展了”先天性”及”後天性”的免疫防禦機制 (Bulet et al., 2004)。在無脊椎動物中目前只發現到先天性的免疫防禦機制,但在脊椎動 物的免疫反應則需依賴先天性及後天性的免疫防禦機制共同運作 (Hoffmann et al., 1999)。所謂先天性免疫防禦機制主要指的是生物體中會產生一種主要由胜肽及多胜肽 鏈所組成的抗菌物質,它們最少由15到20個胺基酸所組成,並由不同類型的細胞及分泌
2
物製造出來。生物體相當依賴抗菌胜肽,它們主要存在分泌器官的細胞內或被感染時才 會被誘發產生 (Hancock & Diamond, 2000)。而合成抗菌胜肽的誘發過程已經在昆蟲,特 別是果蠅 (Drosophila melanogaster) 裡成功的研究出來 (Meister et al., 2000),在脊椎動 物或植物的組織中也曾經被發現。目前所發現的抗菌胜肽大多是帶有陽離子 (cation) 的,也就是說在生理的環境下它們是呈現正電性的,這是由於在胜肽中存在的帶正電胺 基酸 arginine 及 lysine 比帶負電的胺基酸 aspartic acid 和 glutamic acid 含量要高,且 如果C端修飾為醯胺基 (amide) 則更會加強胜肽之陽離子特性。除了這常見的陽離子特 性之外,抗菌胜肽通常會形成雙性 (amphipathic) 的結構,以一側為親水性區域,另一 側為疏水性區域的方式存在。因此這兼具陽離子及形成雙性的特性,會使得胜肽更容易 和帶有陰離子的細胞膜或微生物的磷脂膜產生交互作用甚至嵌入到膜中 (Oren & Shai, 1998)。已經有許多的機制可以用來說明胜肽作用的模式,如:桶狀式穿鑿 (barrel stave)、
地毯式吸附 (carpet) 或是超環面機制 (toroidal-pore) 等 (Castle et al., 1999;Kragol et al., 2001;Otvos et al., 2000)。
雖然無脊椎或脊椎動物所發現的抗菌胜肽其一級結構差異性非常大,但存在在類似 膜的環境中,大多會形成α-螺旋 (α-helix) 或是帶有一個或一個以上的分子內雙硫鍵的β- 褶板 (β-sheet) 等二級結構 (Dimarcq et al., 1998;Tossi et al., 2000)。而除了這兩個類型 外,抗菌胜肽還可以利用本身存在一種或多種以上的特殊胺基酸 如:arginine、
tryptophan、histidine 或 glycine 等來加以分類,例如由蜘蛛 (Acanthoscurria gomesiana) 身上所發現到的抗菌胜肽-acanthoscurins,擁有92個胺基酸,但其中73%皆是由 glycine 所組成 (Bulet et al., 1999),其中最常見的為帶有 proline 的抗菌胜肽 (如:Gennaro (1989) 等人由牛身上所發現的抗菌胜肽-bactenecin 7)。
抗菌胜肽的研究大約是由80年代開始興起。Hultmark (1980) 由天蠶 (Hyalophora cecropia) 中分離純化得到具有抗菌性的多胜肽鏈-cecropin 後,學者便相繼由細菌、昆 蟲、植物、哺乳動物甚至人類體內發現到抗菌胜肽的存在。目前所發現的抗菌胜肽已有 800多種。以下便就抗菌胜肽的結構及抗菌機制來加以分類及討論。
1-2 抗菌胜肽結構分類
目前所發現的抗菌胜肽不管是在胺基酸序列或特性方面都是獨特且具有多樣性 的,有鑑於此,學者只能利用其胺基酸的組成或二級結構將為數眾多的抗菌胜肽加以分 成以下幾大類 (Epand & Vogel, 1999)。
3
1 - 2.1 雙性和疏水性螺旋胜肽 (amphipathic and hydrophobic α-helices)
在許多的生物體中如:脊椎及無脊椎動物、植物甚至於微生物等都會發現線性螺旋 抗菌胜肽的存在 (如表 1-1),目前約有上百種抗菌胜肽都屬於此類型。這類抗菌胜肽的 胺基酸序列相當短 (大多小於40個胺基酸),缺乏 cysteine ,卻富含 lysine 及 arginine (使胜肽帶有大量的正電荷),且C端大都帶有醯胺基 (amide) (Bulet et al., 2004)。在水溶 液 中 , 胜 肽 多 呈 現 混 亂 (random) 的 二 級 結 構 , 但 如 果 存 在 於 三 氟 乙 醇 (trifluoroethanol)、磷脂微粒、脂質體或脂質雙層膜中,胜肽便會改變而形成螺旋的二級 結構 (Gennaro & Zanetti, 2000)。另有學者發現,產生螺旋的程度與抑制革蘭氏陰性及 陽性菌的活性有密切的關係;而增加螺旋的程度也會相對增加抗菌的活性。以脊椎動物為 例,科學家已在兩棲動物的皮膚分泌物、胃黏膜及腸的上皮組織中發現到相當強且作用 範圍廣泛的抗菌胜肽存在,且他們的活性並不僅限於病原體,如:對革蘭氏陰性菌及陽 性菌、真菌和原生動物 (protozoan) 的抑制,而有些螺旋抗菌胜肽也具有高度的溶血活 性 (hemolytic activity)。由於螺旋型抗菌胜肽長度較小,較有利於利用化學方法合成,
有鑑於此,許多的學者便利用圓二色偏極光譜儀 (circular dichroism;CD) 及核磁共振 (nuclear magnetic resonance;NMR) 來做結構特性的描述,並藉此判斷其結構及功能間 的相互關係 (structure-activity relationships;SAR)。有許多研究指出螺旋胜肽的效力和 活性由以下幾個要點共同決定,包括(1)有能力形成雙性結構、(2)帶正電荷、(3)整體而 言是呈現疏水性、 (4)大小、序列以及 (5)極性角度等,都和胜肽的抗菌活性有密切的 關係。而這些結構需求 (structural requirements) 彼此間是有關聯的,當改變其中某種結 構需求,即可能連帶改變其他的結構需求,造成胜肽在生物活性上的改變 (Bulet et al., 2004)。
在目前抑制細菌的胜肽 (bacteriostatic peptides) 研究中,研究的最透徹也最廣泛的 就屬會形成陽離子雙性螺旋的抗菌胜肽了 (Epand & Vogel, 1999)。然而,也還有某部 份的螺旋胜肽會形成疏水性的結構,甚至於會帶輕微的負電。但胜肽如果不是以帶有正 電荷的形式存在,則會顯示出對微生物和哺乳動物細胞具較低的選擇性 (selectivity)。以 帶有輕微負電且會形成疏水性結構的細胞毒素胜肽 (cytotoxic peptide)-alamethicin 為 例,此胜肽在穿越雙層膜時會先聚集,然後圍繞形成可運輸離子的孔洞。而 alamethicin 會被微生物利用非核醣體生合成 (ribosome synthesis) 的機制所合成。但由於其對微生 物的膜具較低的選擇性,在藥理上的效用有諸多限制。不過在自然界中大多數的雙性螺 旋細胞毒素胜肽都是帶有正電荷,且也顯示出對微生物有高度的選擇性及毒性 (Sansom, 1991)。
而在雙性陽離子螺旋抗菌胜肽中,最被學者所廣為研究的是 magainin。它是由23 個胺基酸所組成,在非洲爪蟾蜍 (Xenopus laevis) 的皮膚分泌物中所發現 (Zasloff,
4
1987)。此胜肽的特性在最近才被學者再仔細討論,認為此胜肽會形成促使細胞溶解的 孔洞 (lytic pore) (Matsuzaki, 1998;Matsuzaki, 1999);而此孔洞和一些螺旋型胜肽 (如:
alamethicin) 利用聚集形成孔洞的形式不同。就 magainin 來說,其形成的孔洞較大且在 開啟或關閉時不會分離,然而形成這類型的孔洞並不會造成膜完全的瓦解,例如:
magainin 不會容許 24kDa 的胰蛋白酶 (trypsin) 進入到膜中 (Matsuzaki et al., 1995)。
另外和 alamethicin 形成的孔洞相異的地方是 alamethicin 之孔洞只利用胜肽去排列形 成 (此即 barrel-stave 機制),而 magainin 所形成的孔洞外牆則包含了胜肽及脂質兩 種,這是由於胜肽會促使帶負電荷的雙層膜彎曲,使其更容易在所形成的孔洞外牆產生 胜肽及脂質的界線 (此即 toroidal pore 機制) (Matsuzaki et al., 1998;Wieprecht et al., 1997b)。
表1-1 由脊椎及無脊椎動物中所發現之螺旋型抗菌胜肽的結構特徵及抗菌活性。(Bulet et al., 2004)
活性表示:B:抗細菌;C:細胞毒素;F:抗真菌;H:溶血活性;I:殺蟲劑;L:胜 肽會和脂多醣結合;T:trypanolytic activity;Y:造成酵母細胞溶解。
*代表胜肽C端帶有醯胺基 (amide)
1、2、3及4分別代表6-bromotryptophan、dihydroxyresidues、3,4-dihydroxyphenylalanine 及 5-hydroxylysine,
在三維結構部份,是利用由刺蠅 (Stomoxys calcitrans) 及非洲爪蟾蜍 (Xenopus laevi) 身 上所發現到的抗菌胜肽 stomoxyn 及 magainin 來呈現其三級結構。
螺旋輪 (helical wheel) 是利用由蛾 (Hyalophora cecropia) 身上所發現的抗菌胜肽 -cecropins,來呈現其含有的雙性結構特性。
5
1 - 2.2 β-褶板胜肽及較小的蛋白質 (β-Sheet peptides and small proteins)
目前發現屬於此類的抗菌胜肽約有三百多種。此類的抗菌胜肽中包含數個成對的半 胱胺酸 (cysteine) 所氧化形成分子內雙硫鍵 (disulfide bridges),這些帶有雙硫鍵的胜肽 通常在水溶液中會形成β-褶板狀結構 (Brogden, 2005) (如表 1-2)。近年來,有學者在恆 河 猴 (rhesus monkey) 身 上 發 現 環 狀 且 帶 有 半 胱 胺 酸 的 抗 菌 胜 肽 (cyclic cysteine-containing antimicrobial peptide) 稱為, minidefensin 或 θ-defensin (Tang et al.,1999); minidefensin 利用本身的半胱胺酸 (序列中第2及第8個位置) 配對產生的雙 硫鍵去形成β-褶板狀結構。其他如 β-hairpin-like 結構 (例如:由節肢動物上所發現的 thanatin、androctonin、gomesin 及 tachyplesin等,而在兩棲動物上則發現到 brevinins 及 esculentins) 及常在無脊椎動物及植物 defensins 中所發現到的 mixed α-helix/β-sheet 結構等 (Garcia-Olmedo et al., 1998),都可利用本身的半胱胺酸來形成雙硫鍵;而雙硫鍵 會使得胜肽呈現環狀 (ring) 結構如:tachyplesins、protegrin 及 lactoferricin 等,或使得 整個胜肽骨架環化 (cyclization) 如:gramicidin S、polymyxin B 或 tyrocidines等。以 tachyplesin 為例,此抗菌胜肽利用兩個雙硫鍵連結形成環狀反平行β-褶板結構,不管是 對細菌或是人工膜都會使其產生滲透性 (permeability),這是由於此胜肽會結合而形成短 暫的孔洞並藉此改變位置 (translocate) 穿越脂質雙層膜 (Matsuzaki et al., 1997),有學者 認為此胜肽對細胞質外膜作用的方法和螺旋胜肽-magainin 相當類似。由此可知對β-褶 板式胜肽而言,會影響抗菌活性最重要的結構變數是維持雙性,也就是親水性和疏水性 間的平衡 (Rao, 1999)。
自然界中的雙性β-褶板胜肽類似物之雙性程度可利用逆相 HPLC 的滯留時間 (retention time) 來判斷,發現到如果胜肽擁有較高的雙性程度,其溶血活性 (hemolytic activity) 會相對的增加,但卻會降低其抗菌的活性;相對的如果胜肽的雙性程度較低時 顯示出有較高的抗菌選擇性 (Epand & Vogel, 1999)。
Defensins 是一群約為50個胺基酸擁有強大抗菌活性的小蛋白抗菌胜肽,它們產生 及儲存於嗜中性白血球中 (granules of neutrophils),可在動物、昆蟲及植物的組織中發 現,近年來被廣泛的通稱為 thionines。其擁有高量的雙硫鍵可幫助胜肽維持結構的完整 性並形成β-褶板性的結構,但在植物及昆蟲的 defensins 裡通常還包含一部分的螺旋結 構區域。而所有的 defensins 都擁有雙性的結構特性,可使抗菌胜肽能藉此對細菌的細 胞膜作用 (Cornet et al., 1995)。
6
表1-2 由脊椎動物與無脊椎動物中所發現之β-褶板抗菌胜肽的結構特徵與抗菌活性,表 示抗菌胜肽擁有一至兩個雙硫鍵而形成 β-hairpin 的二級結構。(Bulet et al., 2004) 在圖中以黑線表示雙硫鍵的配對
灰色部分代表 thanatin 及 brevinin-1 裡的 insect box 及 Rana box
活性表示:B:抗細菌;C:細胞毒素;F:抗真菌;H:溶血活性;I:殺蟲劑;L:胜 肽會和脂多醣結合;T:trypanolytic activity;Y:造成酵母細胞溶解。
*代表胜肽C端帶有醯胺鍵 (amide)
三 維 結 構 是 以 在 昆 蟲 (Podisus maculiventris) 及 猪 的 白 血 球 中 所 發 現 的 抗 菌 胜 肽 thanatin 及 protegrin-1 來表示其三級結構
1 - 2.3 擁有特殊胺基酸組成的抗菌胜肽
這類擁有特殊胺基酸組成的抗菌胜肽,在自然界中已發現約 40 多種,其結構特性 為:在其胺基酸序列中富含一種或多種的特殊胺基酸 (Otvos, 2002)。不過此類的胺基酸 大多缺少 cysteine 以形成 β-褶板結構,多是呈現線性的結構。例如在唾液中所發現的 抗菌胜肽-histatin,其胺基酸序列就富含大量的 histidine (Brewer et al., 1998;Helmerhorst et al., 1999;Tsai & Bobek, 1998)。其他像由猪的嗜中性白血球中所發現的胜肽-PR-39 及 prophenin,分別由富含大量的 proline 及 arginine 和 proline 及 phenylalanine 所組成 (Vunnam et al., 1997)。Tryptophan 通常在胜肽或蛋白質中並不會大量出現,但如果要觀 察抗菌胜肽是否會進入到膜中,便可藉由觀測 tryptophan 在螢光光譜上的特性來判斷 此胜肽是位於膜或水界面中 (Persson et al., 1998;Yau et al., 1998)。以含有大量 tryptophan 的抗菌胜肽 indolicidin (ILPWKWPWWPWRR-amide) 為例 (Selsted et al.,
7
1992),此胜肽擁有可造成膜滲透但不會造成細胞溶解的活性,這是由於此胜肽會自我 聚集 (self-associate) 而形成傳導的通道 (conductance channels) (Ahmad et al., 1995;Falla et al., 1996;Subbalakshmi & Sitaram, 1998)。
1-3 抗菌活性機制
抗菌胜肽代表生物體內持續進化的古老宿主防禦機制,作為抗菌胜肽目標的微生物 及動物細胞基本上存在著許多的差異。包括:膜的組成、結構及能量 (例如:穿越膜的 可 能 性 、 極 化 作 用 (polarization) 及 組 成 膜 的 特 性 【 如 : 固 醇 (sterols) 、 脂 多 醣 (lipopolysaccharide) 或肽聚醣 (peptidoglycan) 等】。這些差異會導致抗菌胜肽有不同程 度的選擇性毒性,亦關係到抗菌胜肽和目標細胞之間的作用。
雖然目前有數以百計的抗菌胜肽已經被純化、分離出來,且發現彼此的序列有非常 大的差異性,所以這些胜肽只能以結構特性來加以分類。因此,抗菌胜肽的結構和活性 之間的關聯性便開始被學者提出來討論。但還是有許多的抗菌胜肽,並不能歸類在這些 結構分類上,顯示出抗菌活性的機制是非常複雜且有許多的不一致性。此外,有新的證 據指出位於目標細胞內部的細胞質內膜在胜肽的抗菌機制上扮演著很重要的角色 (Yeaman & Yount, 2003)。因此,在抗菌胜肽目前初步已知的機制之下,進一步確認這些 複雜的結構與活性關聯性將有助于完整了解其在宿主防禦機制中所扮演的多重角色。
抗菌胜肽逐漸發展成宿主在遭受感染後的免疫戰略和調節機制中一個不可或缺的 成分。然而,微生物病原體並不是只處於被動的狀態,不論是原核或真核的病原體,都 會利用大部分的基因體 (genomes) 去表現抵抗抗菌胜肽作用和機制活性。
因此,有學者認為在抗菌胜肽的發展上,可大致分為兩個重點。首先,要真正了解 抗菌胜肽的作用機制,並進一步的來加以改善,以對抗病原體的感染;另外,則是要理 解病原體所形成的抗藥性,找尋新的機會去發現及發展藥劑以增強免疫的機制及抑制病 原體的能力 (Yeaman & Yount, 2003)。
1 - 3.1 抗菌胜肽目標特異性和選擇毒性的機制
在自然界生物體中已分離出許多擁有抗菌活性的多胜肽鏈,這也引起許多學者的興 趣去解釋關於這些在宿主抗菌防禦胜肽所潛藏的功能,這些的胜肽被證明會抑制或殺死 微生物,但卻對宿主的細胞影響甚少,因此,有學者認為抗菌胜肽在辨別微生物或宿主 細胞時有一個關鍵性因子存在。
8
所有生物體的細胞膜實際上大都是由流動的蛋白質及磷脂質所組成。在某些生物體 中,固醇和甘油脂 (glycerides) 也是組成生物膜的結構。然而,微生物和宿主細胞膜組 成份中所存在的基本差異極可能決定了抗菌胜肽的選擇性。(Yeaman & Yount, 2003)。
1 - 3.2 膜的組成、疏水性作用力和極性
所有生物膜基本上都是由雙層磷脂質所組成,不論是微生物或宿主細胞的雙層膜均 呈現雙性 (amphipathic) 【擁有疏水性 (hydrophobic) 及親水性 (hydrophilic) 區域】 的 結構。然而就組成成分及細胞動力學而言,真核及原核細胞的生物膜彼此之間有著很明 顯的差異 (如圖 1-1)。例如,磷酸膽鹼 (phosphatidylcholine;PC) 及磷脂醯乙醇胺 (phosphatidylethanolamine;PE) 是呈現無浄電荷;而神經鞘磷脂 (sphingomyelin;SM) 及 一些帶有棕梠酸 (palmitoyl) 的 PC 類似物,及固醇類 (sterol, ST;如膽固醇與麥角固 醇) 則是不帶著任何的電荷。這些不帶電或無靜電荷之成分大多出現在真核細胞的細胞 膜中,較少存在原核的細胞膜中。反之,帶負電的磷酯質 【如:PG (phosphatidylglyceral、
PS (phosphatidylserine) 及雙磷脂酸甘油 (cardiolipin;CL)】 ,則是大多出現在原核細 胞膜中,在真核細胞膜中幾乎不存在,由此觀點顯示,生物膜上的浄電荷大部分是由磷 酯質的化學計量 (stoichiometry) 及結構 (architecture) 而決定。
在許多的細菌病原體所發現的細胞膜大部分是由 PG、CL 或 PS 所組成,傾向帶 有高的負電荷,相反的,通常在哺乳動物的細胞膜多富有兩性離子的磷酯質 (如:PE、
PC 或 SM)。真核或原核細胞不同的電位梯度會組成不同的膜電位特性。例如:利用存 在在膜中的固醇類可以幫助抗菌胜肽分辨此真核細胞中是屬於哺乳類或真菌類細胞 (Tytler et al., 1995)。然而,值得注意的是某些帶有抗真菌活性的抗菌胜肽中富含中性胺 基酸,例如:由青豆 (lima bean) 所分離出的抗菌胜肽-lunatusin (Hancock & Chapple, 1999;Wong & Ng, 2005),較易對真核細胞造成影響。
人類細胞 (例如:紅血球) 的細胞膜帶有大量的 PC、PE 及 SM。相較之下,非人 類的哺乳類細胞的細胞膜通常包含較少量的 PE,但帶有較大量的 SM;細菌細胞質的 外膜通常帶有較多的陰電性,擁有較高比例帶有陰離子的 PG 及 CL,但 PG 及 CL 在 哺乳動物細胞的細胞膜是很難被找到,甚至不會出現的。
Koppelman (2001) 等學者便証明了大腸桿菌 (Escherichia coli) 的細胞膜比起其他 細菌的細胞膜還擁有更多的 CL。然而,增加了 CL 的量表示 PG 存在的比例相對的 下降,細胞膜則帶有更高的陰電性。從這觀點來看,細胞膜的組成確實可能提供抗菌胜 肽在判斷微生物或宿主細胞時一個重要的決定因素。
9
圖1-1 比較人類與微生物細胞膜的結構。(Yeaman & Yount., 2003)
比較細菌 (E. coli, S. aureus 或 B. subtilis) 及真菌 (C. albicans) 等病原體的細胞膜 和人類紅血球之間脂質的相對組成及在膜內外葉的分布情形。在圖中構成膜的脂質範圍 由帶負電荷 (左邊) 至帶著兩性離子或不帶電荷 (右邊) 的脂質依次為 CL、PG、PE、
PC、SM 和固醇類 (如:膽固醇或麥角固醇等)。由圖中結果可得知,微生物病原體和 人類紅血球之間的脂質組成有著很大的差異,這些差異說明了為何抗菌胜肽會優先地對 微生物具有高度的親和性。圖中白色柱狀是為 E. coli;水平線柱狀是為 S. aureus;灰色 柱狀是為 B. subtilis;方格柱狀是為 C. albicans 而黑色柱狀是為人類紅血球。
1 - 3.3 抗菌胜肽作用機制
以下是將抗菌胜肽如何造成微生物死亡的過程,就各家學者所提出的理論,加以分 析、討論,期能了解其造成微生物死亡的確切機制。
10
圖1-2 螺旋型抗菌胜肽和目標膜之間的作用。(Tossi et al., 2000)
(A) 對帶有陰離子細胞表面的靜電作用力 (B) 穿越外膜或肽聚醣 (C)對細胞膜中 陰離子磷脂質的靜電作用力 (D) 膜的聚集及插入 (E) 超環狀孔洞機制 (toroid pore mechanism) (F) 地毯式包覆 (carpet mechanism) (G) 孔洞式穿鑿 (barrel-stave mechanism) (H) 次要影響及細胞內作用
I. 靜電作用力 (electrostatic interactions)
許多學者普遍認為,抗菌胜肽和微生物作用的最初機制是需先利用靜電作用力。例 如,陽離子抗菌胜肽和帶負電荷的細胞膜會使彼此形成強烈的吸引力,已有許多的研究 可以證明胜肽極性和膜結合活性之間有強烈的關聯性 (Bessalle et al., 1990;Dathe et al., 2001;Matsuzaki et al., 1997;Vaz Gomes et al., 1993)。這結果也說明了為何許多由生物 體中所純化分離出來的抗菌胜肽都保存帶有正電荷這個特色。而事實上靜電力在分子間 距離較長時還是能作用,且 lysine 及 arginine 和脂質雙層膜的磷酸端之間的作用能力 特別強 (Mavri & Vogel, 1996),因此,靜電作用力在許多的抗菌胜肽中可能可以成為抗 菌胜肽和膜之間作用的最初吸引力。
11
而在胜肽和膜之間靜電作用力的明確機制已有許多的研究在加以探討 (Bessalle et al., 1992;Dathe et al., 2001;Matsuzaki et al., 1997;Vaz Gomes et al., 1993)。以革蘭氏 陰性菌為例,Hancock (1997) 把胜肽和膜之間的作用機制稱為自我促進 (self-promoted uptake),這和已知氨基糖類抗生素的作用機制相類似,認為抗菌胜肽最初的作用需要競 爭、取代結合在LPS上以穩定外膜的二價陽離子 (如:Ca2+),經過取代後的 LPS 更加 的適合和抗菌胜肽作用,胜肽和 LPS 的結合親合力 (binding affinity) 甚至比二價陽離 子還高約三倍。雖然革蘭氏陽性菌缺乏外膜及 LPS,但它們的細胞壁富含帶負電的磷璧 酸 (teichoic acid) 及 teichuronic acid,由以上結果得知細胞膜上的陰離子對陽離子抗菌 胜肽活性來說有重要的相關性,有學者利用突變 S. aureus 細胞壁上的 teichoic acid 來 證明,結果顯示增加表面的負電荷,會導致增加陽離子抗菌胜肽抑制 S. aureus 的活性 (Peschel et al., 1999)。
許多的細菌細胞膜帶有較高的電化學梯度 (electrochemical gradient;△ψ) 會促進陽 離子抗菌胜肽和目標細菌之間的作用。研究顯示,細胞膜電位如果低於 -20mV,會使 陽離子胜肽-tachyplesin 的結合常數增加約200倍 (Matsuzaki et al., 1997)。也有類似的實 驗可以證明,如 Breukink 及 Kruijff 這兩位學者在1999年證實了乳酸鏈球菌素 (nisin) 膜和細胞膜作用需要一定程度的電化學梯度,而其他的抗菌胜肽要有最適的活性也需要 電化學梯度 (Yeaman et al., 1998)。一般來說細菌比哺乳動物細胞帶有更高的電梯度,這 可能便是抗菌胜肽利用電荷調節宿主選擇性的重要因素之ㄧ。
II. 起始濃度 (threshold concentration)
在最初和細胞膜結合之後,便開始進入膜作用的第二階段即為起始濃度。在此階 段,抗菌胜肽開始經由一些可能的機制來進入及穿越脂質雙層膜。由於抗菌胜肽會聚集 在病原菌的細胞膜表面,因此也提供了我們”起始濃度”的想法,而有可能會影響這起始 濃度的變數包括:胜肽濃度、自我聚集的特性及磷脂膜的組成、流動性、頂端極性區域 的大小等,此外值得注意的是同一類型的抗菌胜肽會依據胜肽或膜模型的結構動力學 (conformation dynamics) 利用許多的機制來形成不同的胜肽和膜之間的交互作用力 (Yang et al., 2000)。
III. 構形過渡時期 (conformational phase transition)
在胜肽結合上細胞膜後,緊接著發生胜肽結構或構型階段的過渡時期。有許多利用 生物物理學方法的研究顯示,許多抗菌胜肽在水溶液環境中大多呈現延展 (extended) 或
12
混亂的結構 (Bello et al., 1982; Dathe & Wieprecht, 1999)。然而這些胜肽在模擬膜的環 境或和磷脂雙層膜交互作用時,卻很快的呈現雙性螺旋的構形,有些則需要帶有負電的 雙層膜才能產生這種過渡時期,例如:青蛙表皮的抗菌胜肽-PGLa,在由兩性離子 (zwitterionic) PC 及 SM 所組成的膜中其結構是呈現混亂的;但存在於帶負電的 PG 及 PE 所組成的膜中則是形成雙性螺旋的結構 (Latal et al., 1997)
另外有一種機制和促進胜肽依序結合上雙層膜裡的磷脂質有關,例如:胜肽和磷脂 質極性區域的交互作用會促進胜肽裡的極性胺基酸形成最理想的週期性環繞,進而促進 螺旋的摺疊。而如上述所討論的,構形上的改變也會改變胜肽的疏水性矩及極性角度。
構形過渡時期還有另一個重要的觀點,就是會防止抗菌胜肽在確認是否為目標物表面 時,並不會不加區別的產生破壞膜的活性 (membranolytic activity),因此便可以對非目 標物有最小的生物活性,也使得抗菌胜肽對宿主細胞的活性降到最小。
對照之下,β-褶板型抗菌胜肽由於受到雙硫鍵 (disulfide bonds) 及環形胜肽骨架 (cyclization of the peptide backbone) 的影響,所以在水溶液及膜環境中其構型是較整齊 的,例如:tachyplesin 的二級結構為擁有第二型 β-turn 的環式平板胜肽,當胜肽由水 溶液的環境移至類似膜的環境時,其結構並不會有重大的改變 (Oishi et al.,1997)。因此 有 cystine 穩定的β-褶板胜肽和目標細胞的細胞膜作用時,其二級結構相對的會較穩 定,亦即β-褶板胜肽比螺旋胜肽更容易對非目標細胞細胞膜有破壞的活性,其選擇性也 相對較低。
IV. 自我聚集及聚合 (self-association and multimerization)
許多研究指出抗菌胜肽在和目標細胞細胞膜作用後會自我聚集或聚合。在膜上胜肽 -胜肽及胜肽-脂質間的交互作用創造出複合的結構,然而,胜肽形成特定結構的能力與 其本身的組成有重大的關係,例如:胜肽擁有明確的疏水性及親水性區域的界線,會各 自朝向生物膜或擁有相同特性區域的胜肽作用。如此便會使雙性胜肽容易分開疏水性的 膜核心,而聚集的胜肽複合物便會形成穿越膜的孔洞 (transmembrane pore) 或通道 (channels) (Yeaman & Yount., 2003)。
有關於抗菌胜肽造成膜滲透的模型已經被提出,對於不同的微生物膜結構,抗菌胜 肽會使用不同的機制,以下的模型所描述的是個體的胜肽或類似物對抗人工膜系統的活 性,因此每個學者所提出的模型普遍來說並不一致,但分別代表特定結構之抗菌胜肽與 不同微生物細胞膜可能產生之作用機制 (如圖 1-4)。
13 A. 桶狀式穿鑿機制 (barrel-stave mechanism)
所謂的桶狀式是指當膜滲透時所形成的膜通道形狀。在此機制中,螺旋形胜肽會在 膜中圍繞著中心內腔 (central lumen) 形成束狀,當要形成穿鑿時,胜肽便會組成桶狀結 構。在此機制中,螺旋胜肽的疏水性面會朝向外側,向著膜中的脂肪酸醯基,而親水性 面則會朝向孔洞的內側 (Breukink & Kruijff, 1999;Yang et al., 2001)。桶狀式穿鑿形成 的步驟,首先胜肽要和膜的表面結合,在胜肽結合至膜後,胜肽會經過構形過渡時期,
迫使磷脂質前端的極性區域離開,而導致局部的膜變薄,此時,胜肽疏水性的部份會插 入膜內,其長度會和膜外葉的疏水性相一致,而胜肽中帶正電荷胺基酸的位置則會接近 磷脂質前端極性區域。當所結合的胜肽到達起始濃度,胜肽便會開始自我聚集且深深地 插入膜的疏水性中心,這聚集要考慮到當胜肽形成穿越膜的結構時,其親水性胺基酸暴 露在疏水性膜內部的最小程度。而在磷脂質改變位置後,胜肽便會插入至膜內側,導致 形 成 穿 越 膜 的 孔 洞 , 並 由 實 驗 得 知 , 要 四 個 或 四 個 以 上 的 穿 越 膜 胜 肽 (transmembrane-spanning peptides) 才會形成穿越膜的孔洞 (Beven et al., 1999;Sansom, 1991;Yang et al., 2001)。
B. 超環狀孔洞機制 (toroidal pore mechanism)
超環狀孔洞機制和桶狀式穿鑿之間最主要的差異,在於,前者中胜肽插入膜中時,
會使得膜的內外葉由於孔洞的形成導致連續彎曲,而所插入的胜肽及磷脂質極性區域的 界線會形成孔洞的水核心 (water core),而胜肽永遠只會和磷脂質的前端極性區域結 合。而超環狀孔洞機制大多是經由螺旋胜肽 (如:magainin 及 PGLa) 所研究推論所得 知,在此機制中,當胜肽在細胞外的環境裡和帶有負電荷及疏水性的細菌外膜互相作用 時,呈現螺旋性的結構,螺旋胜肽最初會和膜表面呈平行 (Hara et al., 2001a),接著胜 肽中的疏水性胺基酸會移開膜的前端極性區域,造成內部疏水性區域的破壞,導致膜表 面的彎曲 (Hara et al., 2001b),而膜的彎曲及變薄皆會促進膜表面更加不穩定,使得胜 肽更容易和膜作用。一旦達到胜肽的起始濃度,胜肽便會開始和膜形成垂直及自我聚集 造成超環狀孔洞。隨後孔洞即會瓦解,許多的胜肽便會進入到膜的內葉,進而造成膜的 破裂瓦解 (Uematsu & Matsuzaki, 2000)。
C. 地毯式包覆機制 (carpet mechanism)
由於此機制的胜肽會像地毯一樣包覆住細胞膜的表面,最終造成細胞膜的瓦解,因 此將此機制稱之為地毯式包覆。在此機制中,會有較高濃度的抗菌胜肽利用靜電作用力
14
聚集在目標膜表面,並和細胞模平行,包覆著磷脂質雙層膜 (Shai & Oren, 2001),當 達到起始濃度時,胜肽並不會插入膜的疏水性核心形成孔洞,而是直接使細胞膜像清潔 劑般分散瓦解。例如:由蛾的血淋巴 (moth hemolymph) 所發現到的 cecropin A (Holak et al., 1988) 及富含 tryptophan 的抗菌胜肽-indolicidin (Gennaro & Zanetti, 2000)等,都是 利用此方法來造成微生物細胞膜的破裂,進而造成微生物的死亡。
圖1-3 螺旋型抗菌胜肽的膜滲透機制。(Toke, 2005)
(A) 桶狀式穿鑿機制 (barrel-stave mechanism);(B) 地毯式包覆 (carpet mechanism);(C) 超環狀孔洞機制 (toroidal –pore mechanism)。而圖中黑色及灰色分別代表胜肽親水性及 疏水性區域,方框中的圖示代表桶狀式穿鑿機制及超環狀孔洞機制的上視圖。
15
V. 細胞死亡的機制 (mechanisms of cell death)
關於抗菌胜肽有另一個領域需要我們特別去注意,即為抗菌胜肽造成細胞死亡的原 因。抗菌胜肽會造成微生物的死亡是由於細菌膜有許多不能克服的缺陷,因此胜肽便藉 此 引 起 細 胞 膜 產 生 孔 洞 , 進 而 導 致 膜 中 離 子 及 代 謝 物 的 洩 漏 , 接 著 產 生 去 極 化 (depolarization) 、抑制生物高分子 (biopolymer) 的合成,最終造成細胞的死亡。但造成 微生物的死亡並不是單一的機制就可達成,以下便依細胞外 (extracellular) 及細胞內 (intracellular) 死亡機制來區分並探討抗菌胜肽造成細胞死亡的機制 (如圖 1-5)。
A. 細胞外死亡機制
細胞外機制大多屬於膜功能的障礙 (membrane dysfunction)。由於微生物的細胞膜 必須負責調節許多必須的功能,如滲透性的選擇、梯度的維持、電子的傳輸及氧化磷酸 化作用 (oxidative phosphorylation) 等。由此可知,當抗菌胜肽和膜相互作用時便有可能 直接或間接造成膜功能的障礙,進而導致細胞的死亡。由許多研究抗菌胜肽造成細胞死 亡的機制中可得知,某些胜肽在開始和微生物作用的2至3分鐘便會快速的造成微生物的 死亡 (Lehrer et al., 1989; Tossi et al., 1997),主要是由於胜肽會造成膜的去極化,使得離 子及代謝物梯度消失,進而阻斷其他生理必須功能 (如:呼吸作用) (Blondelle et al., 1999;Hancock & Chapple, 1999)。
B. 細胞內死亡模型
雖然形成離子通道、穿越膜孔洞及大規模的膜破裂最終都會導致微生物的死亡,但 有新的推測認為,這些結果並不是造成微生物死亡的唯一機制,有新的證據指出抗菌胜 肽有其他細胞內的目標物 (Brogden, 2005)。許多學者觀察到抗菌胜肽有另一種抗菌活性 在交替運用,例如:在抗菌胜肽 Bac 7 的 1~16、1~23 及 1~35 等三個片段並不會使 E.coli 產生滲透性,但卻會導致生物體死亡 (Gennaro & Zanetti, 2000)。
Bierbaum 及 Sahl (1987) 等學者就認為抗菌胜肽會使一些非膜表面目標物如:自溶 素 (autolysin) 及磷脂酶 (phospholipase) 活化,在 Staphylococcus simulans 中,加入陽 離子胜肽-Pep5 會活化自溶素-N-acetylmuramoyl-L-alanine amidase 去抑制細胞膜對 lipoteichoic 及 teichuronic acids 的利用,藉此可以說明抗菌胜肽除了會破壞細胞膜外,
還可使用其他方式造成細胞死亡。
抗菌胜肽要進入至細胞內和胞內物質作用,第一要務便是必須穿過細胞膜,因此胜
16
肽便發展一套獨特的機制去穿越膜進入到細胞質內。例如:Buforin Ⅱ 是一條有脯胺酸 樞紐 (proline hinge) 的線性螺旋抗菌胜肽,並不會使細胞膜產生滲透性,但會穿過細胞 質並在細胞質內累積 (Park et al., 2000);推測其機制是由於 Buforin Ⅱ中的脯胺酸樞紐 區域會和非細胞滲透性的胜肽 (non-cell-penetrating peptide) 融合,於是這混合型的胜肽 就可以直接進入到細菌細胞質內並伴隨著抗菌胜肽在細胞質內累積 (Park et al.,2000)。
在其他的實驗中,富含精胺酸 (arginine) 的胜肽類如:NLS 及 polyarginine 等可輕易 的穿過細胞及細胞核的外膜 (Futaki et al., 2001)。在真核細胞中,apidaecin 是一條短鏈 且 富 含 脯 胺 酸 的 抗 菌 胜 肽 , 會 藉 由 利 用 透 性 酶 / 轉 運 蛋 白 的 機 制 (permease/transporter-mediated mechanism) 進入到膜內 (Casteels et al., 1993)。
ㄧ旦進入到細胞質內,胜肽便會改變細胞質外膜間隔的組成、抑制細胞膜的形成、
抑制核酸的合成、抑制蛋白質的合成或抑制酵素活性。例如:indolicidin 會導致 E.coli 無 法正常分裂 (filamentation),且受到胜肽攻擊的細胞型態會變的非常修長,這就表示經 過胜肽作用的細胞沒有能力進行細胞分裂 (Subbalakshml & Sitaram, 1998)。
但這並無法解釋是否細胞無法分裂是由於抗菌胜肽阻礙了 DNA 複製或抑制跟膜 間隔組成有關的蛋白。因此,有學者發現到 Buforin Ⅱ 會和大腸桿菌的 DNA 及 RNA 結合,改變其於1%洋菜膠中電泳的移動性 (Park et al., 1998)。而螺旋抗菌胜肽 -plurocidin、ermaseptin 和一些富含 proline 及 arginine 之胜肽 (PR-39 及 indolicidin) 進入到大腸桿菌後,會結合胸腺嘧啶 (thymidine)、尿嘧啶 (uridine) 及白胺酸 (leucine),
這表示這些抗菌胜肽會抑制 DNA、RNA 及蛋白質的合成 (Boman et al., 1993;Lehrer et al., 1989 ; Patrzykat et al., 2002 ; Subbalakshml & Sitaram, 1998) 。 Pleurocidin 及 dermaseptin 在其最小抑制濃度 (minimal inhibitory concentration) 時會抑制核酸及蛋白 質 的 合 成 但 並 不 會 對 大 腸 桿 菌 的 細 胞 膜 造 成 危 害 (Patrzykat et al., 2002) 。 又 以 indolicidin 來說,其濃度達到100 μg ml-1 時就會完全的抑制大腸桿菌中 DNA 及 RNA 的 合 成 , 但 濃 度 要 達 到150 μg ml-1 以 上 才 會 對 蛋 白 質 的 合 成 造 成 明 顯 的 抑 制 (Subbalakshml & Sitaram, 1998)。以上結果證明了抗菌胜肽除了和細菌細胞膜作用,造 成細菌死亡外,還有一些細胞內的機制,如:抑制DNA、RNA及蛋白質的合成,也是造 成細菌死亡的原因之ㄧ。
17
圖1-4 抗菌胜肽在細胞內的作用機制。(Brogden, 2005)
利用大腸桿菌為目標微生物,模擬抗菌胜肽在細胞內的活性機制
VI. 結構參數
影響抗菌胜肽活性之結構因素
任何宿主之理想抗菌防禦機制必須具備只針對目標微生物有選擇性,而不對宿主產 生影響之必要條件。理論上, 抗菌胜肽可對單一或多種微生物具親和性,即具有較寬之 對抗微生物範圍。抗菌胜肽首先接觸目標微生物細胞上之作用標的, 再進而累積至發病 機轉之臨界濃度以上。
其中一類的抗菌胜肽具有雙性之特色,因此,微生物的細胞膜會和抗菌胜肽相互作 用,並利用較易攻擊之固有微生物結構作標的,例如細胞膜。除了雙性特性之外,尚有 許多與抗菌活性和選擇性相關之抗菌胜肽結構重要參數,如構形 (conformation;X)、帶 電性 (charge;Q)、極性角度 (polar angle;θ)、疏水性 (hydrophobicity;H) 及疏水性矩 (hydrophobic moment;MH) 等五項,是最值得探討的。這些結構參數是相互影響的 (如 圖1-5所示),換言之,改變其中一結構參數通常會導致其他參數之改變。以下,針對各 結構參數進行探討。
18
抗菌胜肽主要藉由本身所帶的大量正電荷,和病原菌細胞膜上的負電荷形成離子鍵 互相結合,造成維持細胞膜的力量遭受破壞,細胞膜不再緊密結合,使得抗菌胜肽能鑲 在細胞膜中形成孔洞,造成細胞滲透壓失調,胞內物質大量外漏,最後造成病原菌死亡 (Yeaman & Yount., 2003)。
圖1-5 說明抗菌胜肽結構重要參數之間的相關性。(Yeaman & Yount., 2003)
抗菌胜肽的基本組成及胺基酸序列不只對其生物特性有影響 【如:帶電性 (Q)、
雙性 (A) 及疏水性 (H)】,也會影響到其三級結構 【構形 (X) 及極性角度 (θ)】。因 此抗菌胜肽的胺基酸序列、基本組成及分子內鍵結的改變,會影響其在水溶液或結合至 微生物細胞膜時結構和活性的相關性 (structure-activity relationships;SAR)。並且任意 的改變其中一種結構參數,也會造成其他結構參數的改變。因此抗菌胜肽在不同的環境 中 (如宿主或微生物的細胞膜) 要適當調節其結構特性才能得到最適化效能。
1. 構形 (conformation;X)
抗菌胜肽具有高度特異性,包括序列、來源及三維結構等,以二級結構做分類時,
其中以形成螺旋及褶板等兩種構形的胜肽含量最多,而其餘之胜肽,則依其所富含一種 或多種的特殊胺基酸加以區分,如富含 proline-arginine,或 tryptophan 等 (Hancock, 1997)。此外,亦可以抗菌胜肽的來源 【如:嗜中性血球 (neutrophils)、 白血球 (leukocytes) 等】 或前驅物 (如cathelicidin 為 cathelin 之衍生物) 等來加以分類。
19
構形為螺旋之抗菌胜肽,廣泛存在於昆蟲及兩棲類細胞外的體液中,但其在水溶液 中卻是呈現延展的無特定構形,此類的胜肽只有在和雙性磷脂質膜交互作用時才會形成 螺旋的構形。構形為褶板之抗菌胜肽於一級結構上具有高度結構差異性,但仍可以發現 其共同特性 (如:都會形成雙性等結構特性)。但在其他富含某種特定胺基酸的抗菌胜肽 上,如富含 proline-arginine 及tryptophan 等抗菌胜肽上則較不易找到與結構相關的特 性。然而區別螺旋及平板之兩種標準構形差異是需要鑑定的,例如 certain 為富含 proline-arginine 抗菌胜肽,而 indolicidin 為富含 tryptophan 之抗菌胜肽,但都經實驗 證實為 polyproline helical type II 之結構 (Boman et al., 1993 ; Cabiaux et al., 1994),結果 證明抗菌胜肽可能具有一種或一種以上的結構特性。
2. 帶電性 (charge;Q)
多數抗菌胜肽顯示具有帶正電荷之特性,範圍由+2 到+9,並且含有較多帶正電之 胺基酸。帶正電荷之特性,對抗菌胜肽在起初與帶有負電的磷脂質膜之細菌或其他微生 物相互作用時所需的靜電作用力 (electrostatic attraction) 而言,扮演著相當重要的角 色;並且就靜電性親和力 (electroaffinity) 的選擇性來說,抗菌胜肽和微生物的作用明 顯要高於宿主細胞。這是由於微生物細胞膜具有許多帶有負電的磷脂質,如 PG、PS 和 CL ,皆會使細胞膜呈現帶負電荷。此外革蘭氏陰性菌及革蘭氏陽性菌位於細胞膜上的 LPS 及 teichoic 或 teichuronic acids 也提供細胞膜表面更多的負電荷。一般而言,原核 生物細胞的電化學梯度 (electrochemical gradient;△ψ) 比哺乳動物細胞高 50%。因此,
推論化學滲透能力是以微生物表面淨電 (electrophoretic) 的方式來集中帶有正電荷之抗 菌胜肽,也就是為何抗菌胜肽大多帶有正電荷的原因。實驗證實抗菌胜肽帶有的正電和 抗菌活性之間具有相當程度的關係 (Bessalle et al., 1992;Dathe et al., 1997;Matsuzaki et al., 1997),而此影響程度並非絕對相對的,對于不同的胜肽,皆有可能產生直接、間接 或相反的影響 (Bessalle et al., 1992 ; Blondelle & Houghten, 1992);但於一定的範圍 內,增加抗菌胜肽的陽離子通常亦可增加其抗菌的能力。以 magainin 2 的類似物為例,
當不改變其疏水性、疏水性矩之結構參數情況下,胜肽所帶的電荷由 +3 改變到 +5,
即可增加對抗革蘭氏陰性及革蘭氏陽性菌的能力 (Dathe et al., 2001)。然而,若此時所 帶的正電荷已達到極限,即使再增加所帶的正電荷,也不會增加抗菌的活性;相反的,
當正電荷達到 +6 或 +7,反而會增加其溶血的活性,並且造成抗菌的活性下降 (Dathe et al., 2001)。這主要是由於過度的增加正電荷,會導致抗菌胜肽與帶負電的細胞膜彼此 間的靜電力增強,導致胜肽結合過於緊密而阻礙其進入細胞內側之能力,因而降低其抗 菌活性。
經由研究螺旋抗菌胜肽中雙性及疏水性這兩個結構參數,在其抗菌及溶血活性中所 扮演的角色,可以發現胜肽和膜之間的交互作用容易受到靜電力和疏水性作用力的影
20
響。我們發現,藉由修改胜肽所攜帶的正電荷來增加靜電力,再加上適當的改變胜肽的 疏水性螺旋區域以得到強大的滲透能力,可預期此胜肽會擁有強大的抗菌活性,而對原 核生物細胞也會有更好的選擇性 (Dathe & Wieprecht, 1999)。
3. 疏水性 (Hydrophobicity;H)
胜肽的疏水性指的是在胜肽中胺基酸所含疏水性的程度,以 Eisenberg (1984) 利用 胺基酸的疏水性程度所設計出的數值作依據,此即以其他學者 (von Heijen、Janin、
Chothia 及 Wolfenden) 所設計出的四種不同的疏水性值來加以平均 (如表 1-3 所示) (Chothia, 1976;Janin, 1979;von Heijne & Blomberg, 1979;Wolfenden et al., 1981),所 得之 consensus 值,為本論文所研究之疏水性值。
胜肽中所含的疏水性程度會影響其分開脂質雙層膜的能力在抗菌胜肽和膜之間的 交互作用中扮演相當重要的角色。雖然疏水性對形成膜的滲透性而言是有其必要性,但 增加疏水性的程度會使抗菌胜肽和哺乳動物細胞的細胞膜間作用力太過於強大,也會降 低抗菌的選擇性。因此,許多抗菌胜肽只需擁有適度的疏水性,這樣對哺乳類細胞的毒 性才不至於太高。
胜肽的疏水性反映了胜肽本身如何由水相進入到疏水性相的能力。疏水性作用力再 加上其他額外的作用力如:靜電力及凡得瓦爾力等,在抗菌胜肽要進入到脂質雙層膜時 扮演著重要的角色,因此胜肽的疏水性在調節其活性的程度上,有著不可忽略的地位。
就疏水性來說,要形成宿主防禦系統裡的膜溶解胜肽必須滿足以下兩個必要條件:(1) 此 胜肽必須是可溶於水且可將高濃度的胜肽儲存起來,當遇到微生物、細菌等目標物時,
有快速運送的能力 (此時的胜肽必須有低的疏水性);(2) 而同時胜肽和雙層膜的疏水性 區域互相作用,進而破壞雙層膜的結構,使膜增加通透性 (此時胜肽需要較高的疏水 性)。然而,胜肽疏水性程度太高,會導致胜肽彼此間自我的結合 (self-association) 或使 得胜肽無法溶於水中而沉澱,如此便抑制了胜肽運輸至目標微生物的能力,但相反的,
如果胜肽的疏水性程度太低時,胜肽和膜之間的親和力便會不夠。
利用模型來研究胜肽疏水性對溶血及抗菌活性之間的影響,結果顯示疏水性的改變 對於胜肽造成電中性PC膜滲透的能力會有重大影響,然而減少了疏水性的胜肽類似物卻 會增加負電荷雙層膜的滲透能力,因此可以得知,胜肽會利用靜電作用力而在負電荷雙 層膜上累積,減少了疏水性作用力對膜滲透能力的影響 (Dathe & Wieprecht., 1999)。
Wieprect (1997a) 研究群針對胜肽疏水性和膜滲透性之間的關係進行探討,以只改 變 magainin 的疏水性並將極性、疏水性矩等結構參數維持不變所形成 magainin 的類 似物,研究結果顯示,增加疏水性對於完全由 PG 所組成的微脂體膜結合力及滲透性是 不具影響的;但胜肽疏水性卻對 PC:PG 比率為 3:1 的微脂體膜結合力及滲透性具
21
有顯著影響。具有高度疏水性的 magainin 類似物其對 PC/PG (3:1) 的微脂粒滲透活 性比起最小疏水性程度的類似物高約 60 倍;而對完全由 PC 所組成的微脂粒來說,帶 有最高程度疏水性類似物的活性則比最低程度的類似物還要高約300倍,此外,實驗結 果並利用表面結合常數 (apparent binding constants;Kapp) 再加以判斷,當在 PC/PG (3:
1) 的微脂粒中,擁有最高程度疏水性的類似物,結合到微脂粒的結合常數為 105000 M-1,而最小程度疏水性的類似物則為 7400 M-1。表面結合常數上的差異代表疏水性的 程度會影響膜結合的親和性及滲透性,即表示抗菌胜肽的疏水性越強,對膜的結合力相 對也增加,但對呈現電中性的哺乳動物細胞膜比帶有負電的微生物膜增加的結合力要大 的多,使得選擇性也會因此而下降。因此,對抗菌胜肽而言,維持適度的疏水性,才可 擁有較高的抗菌選擇性。
4. 疏水性矩 (hydrophobic moment;MH)
疏水性矩是一種用來測量胜肽雙性程度的方法,可利用胜肽中各個胺基酸疏水性向 量的總和來清楚的呈現。最初這觀念主要是用來研究蛋白質的摺疊,但最後學者普遍用 它來定義膜相關的蛋白質 (membrane-related protein) 及胜肽結構 (Eisenberg, 1982)。絕 大多數抗菌胜肽與細胞膜作用時,皆會形成雙性的結構,其中又以雙性螺旋最容易形成 (Finer-Moore & Stroud, 1984)。在螺旋的抗菌胜肽有一面大部分是呈現親水性的區域,
而相對的另一面則是呈現疏水性的區域。雙性螺旋主要依據 Eisenberg (1984) 所研究 出的公式來做為依據,他們將螺旋型的抗菌胜肽利用”螺旋輪 (helical wheel)” 的方式呈 現,並設計出每一個胺基酸方位所相對的螺旋軸線,再搭配查表所知與每個胺基酸之疏 水性值,即可得知疏水性矩的數值。以下便是所求的公式
MH
MH=疏水性矩 (hydrophobic moment;MH)
δ=胜肽裡依序出現的胺基酸週期性的角度;以螺旋型的胺基酸為例,δ=100°
n=胜肽中胺基酸之數量
H=胜肽裡依序出現的胺基酸之疏水性值
主要是依據所有胜肽中的胺基酸向量的總和,來判斷疏水性矩的程度,可以將幾何
22
學的方程式利用疏水性矩圖 (hydrophobic moment plot) 加以呈現。下圖 1-6 所示是由 蜜蜂毒液上所發現的抗菌胜肽-Melittin 中第 5 至 22 個胺基酸,圖示裡箭頭表示胜肽裡 胺基酸的疏水性值,而實線向量則代表每個胺基酸的疏水性矩,實線向量的總和即代表 胜肽整體疏水性矩。數值越小表示疏水性及親水性胺基酸平均的分布在整個胜肽裡,也 意味著雙性的程度越小;相對的,數值越大表示在胜肽一側有大量疏水性胺基酸,而相 對的另一側也有大量的親水性胺基酸,表示雙性的程度也越大。
圖 1-6 螺旋型抗菌胜肽-melittin 中每個胺基酸對螺旋疏水性矩的貢獻。(Eisenberg, 1984)
在圖 1-6 中疏水性胺基酸的疏水性值是正值,其疏水性矩以實線向量由軸中心向外 延伸;相對的親水性胺基酸的疏水性值是負值,其疏水性矩以虛線向量由軸中心向外延 伸。而所有疏水性向量的總和即為疏水性矩。
雙性螺旋胜肽是以三到四個胺基酸形成一個循環,同時也是與雙性的細胞膜相互作 用之最佳結構。雙性螺旋的程度不僅影響胜肽與帶負電的細胞膜相互作用之活性,亦可 導致胜肽的溶血性以及和兩性離子 (zwitterionic) 或中性 (neutral) 的膜之間相互作用 能力的改變。因此,雙性的程度越高會增加分離疏水性區域的能力,但是,同時也將增 加對中性膜的毒性 (Dathe & Wieprecht, 1999)。
當增加疏水性矩,會明顯的加強胜肽和細胞膜之間的相互作用力,導致膜的滲透性 及溶血活性增加。Pathak (1995) 認為” 雙性”比其他結構參數 (如疏水性等) 對抗菌活性 的影響更為重要。在 magainin 2 類似物上也有相似的研究結果,當測試疏水性矩在膜 的結合及滲透性上所扮演的角色 (Wieprecht et al., 1997c) 時,顯示當增加胜肽的疏水性
23
區域並不會使內含螢光物質 (如:calcein 等) 之帶負電磷脂質 PG 脂質體中的螢光物質 洩漏。但是,當增加疏水性矩時,則會使 PC : PG 比例為 3:1 的磷脂質所組成的膜裡 螢光物質洩漏增加。藉由圓二色偏極光譜 (circular dichroism;CD) 可測得 ”結合等溫 線 (binding isotherm)”,即表示當增加疏水性矩時可增加膜的親和性,相對的,疏水性 矩的增加亦會導致胜肽對人類紅血球的溶血活性增加八倍。因此,增加胜肽的疏水性矩 對帶有高負電性的膜作用影響不甚明顯,但對於較中性之細胞膜而言,由於胜肽與脂質 交互作用所需的靜電力較少,所以,疏水性作用力扮演著相當重要的角色。
褶板型的抗菌胜肽也有雙性的結構特性,此類的雙性結構包含有許多 β-strands;即 帶有較少量甚至沒有螺旋的區域,也會組成極性及非極性的表面。褶板型抗菌胜肽通常 會形成反平行 (antiparallel) 的構形,並利用連續的雙硫鍵【如:defensins (Sitaram &
Nagaraj, 1999) 及 mytilins (Dimarcq et al., 1997)】或將胜肽骨幹圍成圓形【如:
protegrins、gramicidin 或 θ-defensins】來達到穩定整體的構形。許多褶板型抗菌胜肽在 水溶液中觀察到的結構是較堅硬的,也因此可促使聚合 (multimerization) ,主要由於親 水性的區域會限制疏水性面的暴露,但在相同的溶液下,螺旋型胜肽的構形可展現高度 的自由。此外亦有褶板型的胜肽,在水溶液中會形成二聚體 (dimer) 的現象,如利用X 光繞射所發現的人類抗菌胜肽 defensin HNP-3,即有學者認為 defensin HNP-3 及某些 抗菌胜肽要擾亂細胞膜是需要雙性和疏水性矩等特性的。當胜肽的疏水性面要嵌入到脂 質雙層膜中,便會利用帶有極性的 arginine 側鏈和脂質的極性區域結合,以形成三維結 構來分離疏水性及極性區,一旦與膜結合後,雙性褶板胜肽會形成穿越膜的孔洞 (transmembrane channels)。因此,有許多的理論模型用以說明造成及穿越膜孔洞的機制。
然而,精確的構型是需要將胜肽在疏水性膜環境中測定 (Yeaman & Yount., 2003)。
5. 極性角度 (polar angle:θ)
由於螺旋抗菌胜肽必須利用雙性結構的疏水性面和脂質雙層膜的醯基鏈 (acyl chain) 區域結合,而胜肽親水性的區域則需和膜前端的極性區域及水環境接觸,才能使 胜肽結合至膜上,甚至具有穿透膜的能力。因此學者認為胜肽要結合及擾亂雙層膜必須 依賴螺旋核心中疏水性及親水性區域相對的大小,於是便設計出結構參數-極性角度來 表示雙性螺旋胜肽裡疏水性及親水性螺旋區域的散佈的情形。不同於疏水性和疏水性 矩,極性角度是被認為有可能會影響胜肽在膜上的位置及形成穿越膜孔洞的結構,而極 性及非極性胺基酸分布的區域會促進雙層膜正向或負向的彎曲,進而造成脂質雙層膜的 不穩定。
Brasseur (1997) 認為可利用簡單的分類區分抗菌胜肽結合在膜上的位置和疏水性/