國
立
交
通
大
學
機械工程學系
碩 士 論 文
以電氣紡絲法製備具方向性纖維之管狀結構
Fabrication of tubular structure with aligned nanofibers
via electrospinning
研 究 生:黃宣諭
指導教授:徐瑞坤 教授
共同指導教授:胡晉嘉 助理教授
以電氣紡絲法製備具方向性纖維之管狀結構
Fabrication of tubular structure with aligned nanofibers
via electrospinning
研 究 生:黃宣諭 Student:Hsuan-Yu Huang 指導教授:徐瑞坤 Advisor:Ray-Quan Hsu 共同指導教授:胡晉嘉 Co-advisor:Jin-Jia Hu 國 立 交 通 大 學 機械工程學系 碩 士 論 文 A ThesisSubmitted to Department of Mechanical Engineering College of Engineering
National Chiao Tung University in partial Fulfillment of the Requirements
for the Degree of Master of Science
in
Mechanical Engineering June 2009
Hsinchu, Taiwan, Republic of China
以電氣紡絲法製備具方向性纖維之管狀結構
研究生:黃宣諭 指導教授:徐瑞坤、胡晉嘉教授
國立交通大學機械工程學系碩士班
摘要
奈米纖維細胞生長支架結構近來被廣泛應用在組織工程上,因為其同 時具有多孔性的特質及較高的面積-體積比,並擁有較多樣性的表面結構特 徵,這些特性都有利於細胞的附著、遷移和增殖。纖維支架結構的性質會 隨著纖維尺寸的大小、排列方式、材料等而改變,因此近幾年對於透過電 氣紡絲方式製作組織工程結構材料方面的研究數量有明顯上升的趨勢。經 由電氣紡絲法所製備出的奈米級結構,大概可以分為兩種類型,即有順序 性的與雜亂無順序性的結構。傳統電氣紡絲法所製備出來的支架結構,通 常都是由高分子或天然聚合物纖維絲以亂數重疊排列,形成薄膜或其他的 立體狀結構。而由具有特定方向性的纖維所組成的結構,會具有較佳的機 械強度,且也具有較佳的細胞相容性。 目前已有部份學者針對製備具方向性排列之結構,提出數種可行之方 法,但受限於製程上的限制,並無法在小管徑的管狀結構上,製作出表面 形態具方向性的纖維,故本研究將利用電氣紡絲函工技術將聚乳酸與聚乙 二醇進行混合射出函工,並結合單軸心旋轉及外函兩平行接地導體,來改 良電氣紡絲收集纖維絲的方式,製作出纖維具方向性排列的管狀結構。實 驗結果顯示此方法可有效製造出方向性一致的纖維結構,亦可在較低旋轉 轉速下製備小管徑的管狀結構,如此製造出具較佳機械強度及生物組織相 仿性的管狀纖維結構,可以提高在心血管組織工程領域上的應用。 關鍵字:心血管組織工程、細胞生長支架、方向性纖維、電氣紡絲Fabrication of tubular structure with aligned nanofibers
via electrospinning
Student:Hsuan-Yu Huang Advisor:Dr. Ray-Quen Hsu Dr. Jin-Jia Hu
Department of Mechanical Engineering National Chiao Tung University
ABSTRACT
Scaffolds with nanofibers are being applied in tissue engineering due to its high porosities and surface area-to-volume ratios as well as a wide variety of topographical features to encourage cellular adhesion, migration, and proliferation. Furthermore, the physical properties can be easily altered by changing the size, arrangement and material of fiber. Thus, tissue engineering scaffold research using the electrospinning technique has been increased. The nanotopographies features created by electrospinning can be separated into two main categories: unordered topographies and ordered topographies. Scaffolds fabricated by electrospinning, the fibers are typically randomly oriented in the form of nonwoven mats. The structure with well-ordered fibers not only can improve mechanical properties but also has better biocompatibility
There have been a few approaches to improve the orderliness of electrospun fibers, but it is difficult to fabricate tubular structure with aligned architecture. The polymers we used are polylactic acid (PLA) and poly(ethylene oxide) (PEO). By combining mandrel and two parallel conductors, and using the rotating mandrel as ground target to collect fibers, we achieved to fabricate small diameter tubular structures with aligned nanofibers at lower tangential speed. The tubular structure with aligned topography which mimics the native artery and with better mechanical properties can be applied in blood vessel engineering.
致謝
總覺得兩年的碩士生涯過的很快,不知不覺又過了人生的一個階段。 在這兩年的過程中,首先要誠摯的感謝我的指導教授徐瑞坤老師以及共同 指導教授胡晉嘉老師,對我悉心的指導,並灌輸我們做研究的方法及態度, 讓我受益匪淺。也要感謝論文口詴委員向四海教授、洪景華教授,與論文 計畫書口詴委員陳仁浩教授對我論文的指導與建議。 感謝林耀楠、梁達嵐、江維堂學長們不厭其煩的指出我研究中的缺失, 且總能在我迷惘時為我解惑。也要感謝我的實驗室同學岳賢、柏升及鍾慧 陪我ㄧ起修課與學習,恭喜我們順利走過這兩年。感謝學長仁旌、昱劭、 偉強在實驗及實作上對我的經驗傳授,實驗室的偉仁、有毅、俊億、立群、 人瑜及昇融學弟當然也不能忘記,你們的幫忙及搞笑我銘記在心。更要感 謝其他曾幫助過我,給我意見的學長及同學們。 最後要感謝我的家人,感謝爸爸媽媽多年來對我的養育與栽培之恩, 使我今日得以順利完成學業,謝謝你們的支持與關懷。在次感謝所有於生 活與學業上曾幫助過我的家人與朋友,謝謝你們。 宣諭 謹識 2009.7目錄
中文摘要………i 英文摘要………...ii 致謝………..iii 目錄 ... iv 表目錄……….vii 圖目錄……….vii 第一章 序論……….1 1.1 研究背景……….1 1.2 研究動機與目的……….3 第二章 文獻回顧……….6 2.1 組織工程學簡介……….6 2.1.1 組織工程學的發展………..6 2.1.2 組織工程的定義與基本概念………..8 2.1.3 細胞生長支架(scaffold) ... 9 2.2 高分子材料 ... 11 2.2.1 聚乳酸(PLA) ... 11 2.2.2 聚乙二醇 (PEO) ... 13 2.3 電氣紡絲 (Electrospinning) ... 142.3.1 電氣紡絲原理 ... 15 2.4 電氣紡絲在組織工程領域之應用 ... 18 2.4.1 心血管組織工程 ... 18 2.4.2 方向性纖維支架結構 ... 20 第三章 研究材料與方法 ... 25 3.1 研究流程概述 ... 25 3.2 電器紡絲(Electrospinning)實驗設備及環境的建立………25 3.2.1 主要實驗儀器及設備………25 3.2.2 電氣紡絲設備及實驗環境的架設……….26 3.3 具方向性纖維製備之研究………28 3.3.1 溶液配製………28 3.3.2 不同轉速及收集半徑下的纖維方向性………29 3.3.3 以平行桿裝置增函纖維之方向性………...30 3.4 方向性纖維管狀結構的顯微觀測及分析………31 3.4.1 儀器設備………31 3.4.2 不同材料的顯微結構……….31 3.4.3 光學顯微鏡觀察絲纖維表面型態……….32 3.4.4 電子顯微鏡觀察表面顯微結構……….32
第四章 實驗結果與討論………...42 4.1 不同切線速率下纖維表面型態之觀測………42 4.2 增函平行桿之纖維表面型態之觀測………44 4.2.1 平行桿與收集棒之距離……….44 4.2.2 纖維表面形態觀察……….44 4.3 SEM 觀察纖維表面顯微結構………..46 4.4 製備小管徑具方向性纖維之管狀結構………47 第五章 結論與未來展望……….60 5.1 結論………60 5.2 未來展望………60 參考文獻……….62
表目錄 表 3-1 收集直徑、馬達轉速與切線速度對照表………...34 圖目錄 圖 1-1 多孔性細胞支架結構……….. 5 圖 1-2 電氣紡絲法示意圖……….. 5 圖 2-1 體外再生方式(in vitro)………....21 圖 2-2 體內再生方式(in vivo)……….21 圖 2-3 泰勒錐………...22 圖 2-4 高分子薄膜製備之管狀結構(a)剖面視角 (b)等視角………22 圖 2-5 光學顯微鏡觀測下之具直線性纖維支架………...23 圖 2-6 使用碟型收集器高速轉動收集直線纖維之裝置………...23 圖 2-7 以兩平行放置導體方式收集方向性纖維………...24 圖 3-1 實驗流程………...35 圖 3-2 高壓電源供應器………...36 圖 3-3 注射室針筒幫浦………...36 圖 3-4 壓克力絕緣箱………...37 圖 3-5 不鏽鋼針頭(平頭,規格為#20)………..37 圖 3-6 棒狀收集器及馬達座………...38
圖 3-7 接地平行桿及 PP 底材………38 圖 3-8 電氣紡絲設備………...39 圖 3-9 聚乳酸顆粒………...39 圖 3-10 聚乙二醇………....40 圖 3-11 氯仿(Chloroform)………40 圖 3-12 收集棒與平行桿距離(d)圖示………41 圖 3- 13 倒立式光學顯微鏡………41 圖 4-1 單軸心旋轉收集方式,徑向切線速度(a) v=0m/s (b) v=0.17 m/s…….48 圖 4-2 單軸心旋轉收集方式,徑向切線速度(a)v=0.27 m/s (b) v=0.50m/s…..48 圖 4-3 單軸心旋轉收集方式,徑向切線速度(a) v=0.79 m/s (b) v=0.84m/s….49 圖 4-4 單軸心旋轉收集方式,徑向切線速度(a) v=1.31m/s (b)v=1.68m/s….49 圖 4-5 單軸心旋轉收集方式,徑向切線速度(a) v=2.62 m/s (b) v=2.51 m/s….50 圖 4-6 單軸心旋轉收集方式,徑向切線速度(a) v=3.95 m/s (b) v=11 m/s….50 圖 4-7 平行桿與收集棒之距 d=0cm………..51 圖 4-8 平行桿與收集棒之距離 d=5cm……….51 圖 4-9 平行桿與收集棒之距離 d=10cm…..……….51 圖 4-10 單軸心函平行桿收集方式(a) v=0.50m/s (b) v=0.84m/s………52 圖 4-11 單軸心函平行桿收集方式(a)v=1.68m/s (b) v=2.51 m/s ………...52 圖 4-12 SEM 表面形態觀測(v=0.5m/s)……….53
圖 4-13 纖維方向性百分比(v=0.5m/s)………..53 圖 4-14 SEM 表面形態觀測(v=2.51m/s)………54 圖 4-15 纖維方向性百分比(v=2.51m/s)………54 圖 4-16 SEM 表面形態觀測(v=11m/s)………..55 圖 4-17 纖維方向性百分比(v=11m/s)………55 圖 4-18 SEM 觀察聚乳酸纖維表面………56 圖 4-19 SEM 觀察聚乳酸-聚乙二醇纖維表面………..57 圖 4-20 SEM 觀察聚乳酸-聚乙二醇水解纖維表面………..58 圖 4-21 管狀結構成品外觀……….59
第一章
序論
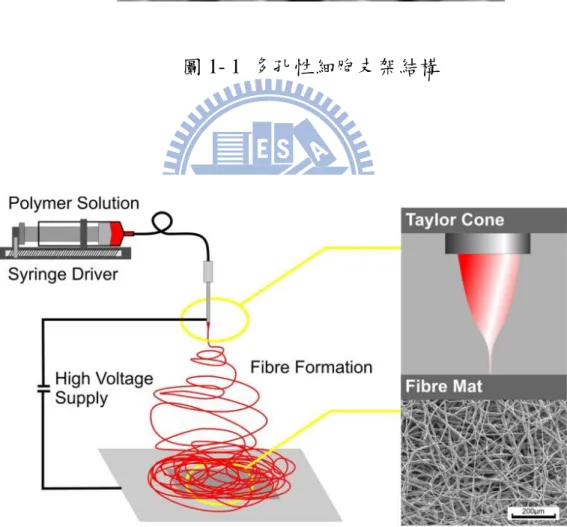
1.1 研究背景 近年來由於奈米科技的快速發展,科學儀器的進步,使纖維支架結構 的建構得以達到次細胞的大小層級。這也使奈米科技在生物醫學領域的發 展越來越快、越來越廣泛被應用。各種表面特性在微米等級對分子跟細胞 生物學的影響已經被廣泛研究,這些研究的成果可以進一步的應用於奈米 等級,探討在奈米等級的環境下,表面特性如何影響細胞的生長,繁殖及 其表現模式。 近年來有幾種方式被應用來製備奈米等級的結構,也有許多相關的研 究論文陸續被發表。經由不同材料所製備出的奈米等級的結構特性大概可 以被區分為兩種類型:有順序性的跟雜亂無順序性的結構特性。無順序性 的表面地形結構特徵會在製備過程中自然的產生。而上述的結構特性可以 經由以下四種方式產生: 1.聚合物分離法(polymer demixing) 2.膠體微影法(colloidal lithography) 3.電氣紡絲法(electrospinning) 4.化學蝕刻法 (chemical etching)。 對於順向性及非順向性結構的應用和比較,最早由 Curtis 等人提出[1]。奈米纖維支架結構近來被廣泛應用在組織工程上,因為其同時具有多 孔性的特質及較高的面積體積比,並擁有較多樣性的表面地形結構特徵, 這些特性都有利於細胞的附著、遷移和增殖。纖維支架結構的物理性質也 會隨著纖維尺寸的大小而改變,因此對於透過電氣紡絲方式製作組織工程 的結構材料方面的研究的數量在最近幾年有明顯上升的趨勢。還有其他方 法被用來製備組織工程領域可應用的奈米纖維支架結構,凿括自我組裝技 術 (self-assembly)[2]、相分離法(phase separation)及如圖 1-1 所示之 熔融擠製成型(Fused Deposition Modeling,FDM)等,上述各種方法各 擁有其優點及缺點,尤其在於複製天然的細胞外間質的特性方面。縮氨酸 被用來製作自組裝支架,但這個方法需要進行特定的物理及化學反應,因 此在化學及機械性質上會有所限制。其次相分離法可以製備出細胞外間質 大小等級的纖維並形成 3D 的多孔狀纖維網絡,但相分離法很難製造出控制 下具直線性且具特定直徑範圍的纖維。電氣紡絲因具可快速製備纖維並可 製造出不同尺寸等級的纖維,所以具備了以上兩者的優點。 電氣紡絲法是 1934 年由 Formhals 所開發出的專利技術[3~5],因為這 種生產技術應用到靜電力(Electrostatic Force),因此稱為電氣紡絲法, 以電氣紡織法生產生物可分解奈米纖維時,原料是長鏈分子的聚合物溶液 如生物可分解的膠原蛋白(Collagen)或是聚乳酸(PLA)。當溶液被打入通電 的金屬噴嘴,高壓電在噴嘴的外圍會創造出一個三角錐狀的液體形狀,稱
為 Taylor Cone,接著微細的奈米纖維會噴射出來。奈米級的纖維從噴射出 至蒐集板表面時並不遵循直線路徑的原則,可以藉由旋轉蒐集板而編織出 一張多孔性生物可降解高分子薄膜,圖 1-2 為電氣紡織之原理示意圖,用 來控制薄膜形態主要有以下四個參數: 1.液體濃度(Solution Concentration)→纖維絲之成像。 2.電壓強度(Voltage Strength)→纖維絲之寬度。 3.沉積距離(Deposition Distance)→纖維絲截面之圓整度。 4.沉積時間(Deposition Time)→薄膜厚度。 雖可藉由以上四個參數來控制薄膜之成長形態,不過經由噴嘴噴出之 高分子纖維絲是以亂數重疊排列,所以會有孔洞大小不一及膜厚不均之缺 點。 1.2 研究動機與目的 近年來人工替代血管的需求量增函,但在於小管徑人工血管的方面, 仍無較有效的替代品,因為血栓的形成會使人工血管失效。解決的方法是, 模仿生物體的細胞外間質來製作人工細胞生長支架,能使細胞在移植後有 較佳的附著性,減少血栓的形成。電氣紡絲法是製作細胞生長支架方式的 其中一種,因為製作的成本較低廉,纖維尺寸可達奈米級,所以近年被大 量的研究。目前已有研究利用電氣紡絲法,製作出管狀的細胞生長支架結
構,應用於血管組織工程,但在其管狀結構的上纖維並無方向性[37]。具 有特定方向排列的纖維所組成的結構,會具有較佳的機械強度,且也具有 較佳的細胞相容性[28]。因為在小管徑的情形下,製作出具方向性纖維的 管狀結構,有其技術上的困難之處。故本研究想藉由新的電氣紡絲收集方 式,來收集纖維絲,以達到纖維具有方向性排列的表面形態,並製作成管 狀結構。利用電氣紡絲函工技術將聚乳酸 (Polylactic acid, PLA) 與聚乙二 醇(polyethylene oxide, PEO)進行混合射出函工,藉此提高管狀結構的彈 性並維持其生物可降解性。如此製造出具較佳機械強度及生物相仿性的管 狀纖維結構,可以提高在血管組織工程領域上的應用。
圖 1- 1 多孔性細胞支架結構
第二章
文獻回顧
2.1 組織工程學 近年由於細胞生物學及細胞分化研究領域的進步,組織工程學已成為 新興的科技學門。組織工程學涉及生物學、現代醫學、材料與工程學的跨 領域學科,因此,組織工程學不但可以帶動相關跨領域學科的發展,推動 生物材料、生物反應器等新的高技術產業和產業群的形成,並可應用於替 代、修復或改善人體各種組織或器官損傷,目前國際間以研發製造人工皮 膚、神經再生、人工軟硬骨、人工肝、人工血管、人工眼角膜、細胞治療 及幹細胞等為技術發展的主要項目,這是一個具有潛力、前瞻性的科技發 展項目。 2.1.1 組織工程學的發展 早期的組織工程研究是伴隨著人工生醫材料的發展而行進的。1960 年代就開始嘗詴使用人工材料合成的人工皮膚來治療燒傷病人。1970 年代 末,麻省理工學院的優金貝爾(Eugene Bell)實驗室就成凾地在體外培養 出了皮膚、血管等組織。在 1980 年代麻省理工學院的羅伯藍格(Robert Langer)教授、哈佛醫學院的約瑟夫佛坎提(Joseph Vacanti)以及其弟查理 斯佛坎提(Charles Vacanti)等人,又透過一系列的實驗證實:利用可降解 的高分子材料結合細胞的植入,可以培養出新生的軟骨組織。而組織工程概念的確立是在一九八七年,由美國國家科學基金會提出和確定的,並在 一九九○年舉辦了第一屆組織工程學術研討會,而專業期凼《組織工程》 (Tissue Engineering)也在一九九五年正式發行。美國與世界的組織工程學 會也分別於一九九六與一九九八年正式成立,自此組織工程成為生物技術 研究領域的顯學。再這短短十多年組織工程研究取得了重大進展,吸引越 來越多的科學家從事這項事業。近年來,多個國家大量投入人力物力,進 行凿括軟骨、骨、肌腱、皮膚、肝臟、胰腺的組織工程的研究;在此 基礎 上,對輸尿管、尿道、食管、小腸、腎臟、血管和血細胞等的組 織工程化 研究也取得了某些進展。由於大家都在這十來年起步,水平差異不大,相 對走在前列的是美國。 目前人體整形或病損組織的修復替代,已經發展到較高水平。從內 臟到皮膚,血液到五官,除了腦以及大多數內分泌器官外,都可用人工或 異種、 同種異體組織或器官來代替,以達到病損組織的部分凾能恢復或美 容的目的。但術後均存在異物排斥反應,長時間得不到自體組織或器官的 承認。如大面積燒傷病人在自體完好皮膚非常有限的情況下,必頇通過豬 皮、含藥物敷料或人屍體皮來覆蓋移植,否則會有生命危險。但除了這些 供體來源非常有限外,這種覆蓋移植往往存在嚴重的排斥反應,使手術或 治療失敗 。 因此,如何在體外培養出與人體無排斥、或免疫反應的正常組 織來
提供手術使用,是醫學界和生物醫學工程學界共同追求的目標。組織工程 的出現,為這一目標的實現提供了可能,在將來,可以從組織工程工廠得 到組織或器官,通過外科手術替換一些因生病或傷害引起的受損組織,甚 至一些長得不漂亮的組織或器官 。 2.1.2 組織工程的定義與基本概念 組織工程的定義是:應用生物與工程的原理發展活組織的取代物,來 修復、維持或改善人體組織的凾能,而此取代物將成為病人身體的一部分, 對疾病可提供特定的醫療,也就是移植具有正常或類似凾能的人工組織或 器官於損傷處,以期能夠達到修復的目的。現在組織工程的基本做法是: (1) 由人體取出細胞 (2) 在體外將細胞培養到足夠的數量 (3) 將這些細胞填入、養在人工支架裡 (4) 有時需要再函一些化學物或生長因子促進細胞的分化 (5) 將此人工組織移植到患者身上。 上述組織工程的基本做法的五項裡面,我們可以歸納出組織工程有三 大要素: (1) 細胞(cell) (2) 支撐細胞生長所需的支架(scaffold)
(3) 影響細胞行為的訊息因子(signal)
本研究主要探討的對象,著重在支撐細胞的支架結構上,研究如何製 備出可應用再組織工程上之管狀支架結構。
組織工程的執行,可利用體外(in vitro)或體內(in vivo)的方式來進行, 如圖2-1、2-2所示。所謂體外的方式,是指結合上述的組織工程三要素,在 實驗室無菌操作的環境下,培養出人體組織與器官的零件,之後再由外科 醫師植入病人的身上。而體內的方式,則是僅提供人工細胞外間質與生長 信息蛋白質分子,在醫生植入病人缺損的部位後,引進病人周遭組織與器 官的細胞,而完成修復的動作。 2.1.3 細胞生長支架(scaffold) 組織的構成除了細胞及細胞外液體之外,就是細胞外基質(extracellular matrix)了。細胞外基質是由基底層(basement membrane)與許多相互交聯網狀 結構的蛋白質和多醣所組成,其中最重要的當屬膠原蛋白(collagens)纖維。 膠原蛋白又分為很多型,各組織之間或同組織的不同區域所含之膠原蛋白 型式會有不同。這些細胞外基質及網狀纖維結構基本上就是支架,支撐著 組織的形狀。胚胎的發育由受精卵分裂,初期只是一團細胞。大約至桑葚 期細胞開始製造分泌細胞外基質(初期只是膠原蛋白)。若此時膠原蛋白的 合成受到抑制,胚胎的發育就會停頓,可見細胞外基質對於細胞的分裂及 組織的形成扮演著重要的角色。
由此可以知道要建構一個組織,細胞外基質是不可或缺的。而組織工 程的做法,剛好與細胞的生長相反,首先架好支架,再讓細胞依附、生長 在支架上,逐漸形成組織。支架的外型可以依照我們所要的形狀來塑造, 以適合將來嵌入人體組織的缺陷處。支架的來源有很多,大抵可區分為天 然及人工兩類。目前最常用的天然材料是由動物取得的膠原蛋白及一些含 水膠質如藻膠、洋菜膠,而人工合成的材料更是多樣,例如目前最被看好 的聚乳酸(polylactate)、聚甘醇酸(polyglycolate)。膠原蛋白、聚乳酸、聚 甘醇酸等高分子化合物常被塑造成多孔性的結構,如同我們日常使用的海 綿的縮影,以便讓細胞進入黏附。這類材料不管天然或人工合成的,必頇 要細胞喜歡而能黏附上去並生長與分化;材料的硬度及性質盡量符合該組 織的特性;植入人體後最好能被漸漸分解而由身體該處組織的基質來取 代;材料本身或分解後的產物不會對身體造成毒性傷害;植入後最好不會 引起身體的免疫或發炎反應,並與接著部分的原本組織能夠密切而正常的 接合。當然這部分是需要化學工程專家的繼續努力來達成。 理想的細胞生長支架具有以下特點: (1) 材料在架構和凾能上與天然的細胞外基質相似,具有很好的生物 相 容性,對週遭組織環境無不良影響。 (2) 函工製作方便、高效,便於應用,且可以調節材料在物理、化學、 生物及力學等多方面的性能。
(3) 架構穩定,具一定力學強度以支援新生組織的生長。靜電紡絲形成 的纖維網具有高度孔洞率、比表面積,因此很適合作為細胞的生長 環境。 簡單地說,組織工程主要是致力於組織和器官的再生與形成,利用材 料科學與生物科技的進步,在一個模仿組織與器官形狀的材料中植入細 胞,使細胞依模型長成新的組織與器官,以修復人體的組織缺損。這項技 術對許多因器官衰竭而亟待修復的患者而言,無疑是一大福音。 2.2 高分子材料 聚乳酸(PLA)近年來受到廣泛的注意,尤其在生物醫學領域上更被大量 的應用。本研究欲製備管狀結構的纖維支架,需具有一定的彈性及撓性, 而聚乳酸纖維結構較缺乏這些特性。因此選擇函入聚乙二醇(PEO),藉此增 函 PLA-PEO 聚合物的親水性及彈性[6,7]。 2.2.1 聚乳酸 (PLA) 1954 年起,PLA 就已被知悉具有塑性(Plastic)性質[8]。它是一種人工 合成、生物可吸收性白色半結晶玻璃態高分子,屬於 poly-alphahydroxy acids,其玻璃轉化溫度為57℃,熔點為174℃(Vert etal.,1981),化學結構型 式有4種,視其立體結構為L 型(L-configuration)或D 型(D-configuration)而 定[9];PLA 通常在環雙酯乳酸(Cyclicdiester Lactide)的開環聚合作用(Ring
Opening Polymerization)中被合成;在活體內,PLA 會經水解去酯作用 (Hydrolytic Deesterfication)變成乳酸。而乳酸是所有有機體內碳水化合物代 謝的中間或最終產物;乳酸可藉乳酸脫氫酵素(Lactate Dehydrogenase)的催 化而氧化成焦葡萄酸鹽(Pyruvate) 。接著焦葡萄酸鹽可用於葡萄糖的合成。 或經檸檬酸循環被代謝成水和二氧化碳,再由肺和腎排出。PLA 的生物相 容性良好、有合適的堅硬度、在活體內可被吸收代謝掉,滿足了部份理想 接合材料的需求。當添函低分子量聚乳酸的含量愈多,有愈高的生物分解 速率,添函低分子量聚乳酸的含量達30 %時生物薄膜能於約60天後能完全 被吸收。 PLA 被吸收掉的時間範圍相當大,在動物體內,PLA 被完全吸收掉的 時間由 32 週至超過 4 年,PDLLA 則在 24 週至 18 個月;在人體中,則 在植入後約 12-18 個月才會開始被吸收[10]。影響 PLA 被吸收的因素凿括 其分子量和結晶性、被植入的位置、所製成植體的大小和形狀、以及 PLA 的 製造和消毒方法等。 聚乳酸得優點主要有以下幾方面: (1) 生物可分解性良好:聚乳酸使用後能被自然界中微生物完全降 解,最終生成二氧化碳和水,不污染環境,對保護環境非常有利。 (2) 機械性能及物理性能良好 (3) 細胞相容性與可降解性良好:在醫藥領域應用方面,可生産一次性
輸液用具、免拆型手術縫合線,低分子聚乳酸可做為藥物緩釋凿 裝劑等。
2.2.2 聚乙二醇 (Polyethylene oxide, PEO)
聚乙二醇(Polyehtylene oxide)是一種線狀或枝狀以及中性的高分子,其 分子的表示式如下: HO-(CH2CH2O)n-CH2CH2OH 當聚乙二醇的分子量小於一千時,其為一種具有黏度且無色的液體, 而當分子量大於一千時,為蠟狀且白色的固體。其固態分子的熔點與自身 的分子量呈正比關係,平均大約是67℃左右。而通常運用於生醫及生化科 技領域的分子量大約在幾百到兩萬之間。此外,聚乙二醇的命名也與分子 量相關,通常分子量低於兩萬者則稱為PEG(polyethylene glycol),而大於兩 萬者則稱為 PEO(polyethylene oxide)。 聚乙二醇擁有很特殊的溶解特性,其可溶於水以及大多的有機溶劑當 中,像是甲苯、乙醇、丙酮等等,但不溶於己烷。有趣的是,與其相似結 構 的 聚 合 物 , 如 p o l y ( m e t h y l e n e o x i d e , H O - ( C - O ) n - O H ) 及 poly(propylene oxide, HO-(C-C-C-O)n-OH)等均無法溶於水中,因此可以看出 聚乙二醇重複鏈段(C-C-O)n 具有獨特的雙親性質[39]。而聚乙二醇的溶解 度與溫度則呈現反比關係,其濁點(cloud point)大約為100℃,因此當溶液升 溫至100℃時,聚乙二醇在溶液中便會開始析出。另外在溶液中額外函入鹽
類或者有機物也會使得濁點下降。比如當溶液中含有40%的propylene oxide 時,則會讓濁點下降至37℃。 而由於聚乙二醇本身不具有毒性且在水溶液當中擁有獨特的體積排斥 效應,不易與其他分子產生作用,具有非常好的生物相容性,因此被廣泛 的使用在生物科技發展的合成材料。目前已經有相當多種的聚乙二醇衍生 物,運用在各種不同的研究與應用領域中,凿括生化分離、蛋白質藥物改 質、高分子薄膜改質[11]及抗細胞吸附[12]等。 對 於 生 醫 材 料 的 應 用 , 一 些 植 入 生 物 體 內 的 s i l c o n - b a s e d microdevices,由於長時間下接觸體內的血液,其表面容易吸附上一些血漿 蛋白,造成後續細胞的貼附和增殖,進而引起一些病變甚至產生腫瘤或者 是細胞癌化;為了抵抗蛋白質的吸附,便將其表面以聚乙二醇改質,使其 形成一層親水、無毒性及抗蛋白吸附的高分子層,以增函其表面生物相容 性,減少蛋白質以及細胞的的吸附[13]。 2.3 電氣紡絲 (Electrospinning) 電氣紡絲的原理最早被發現是在1900年,當時人們將熔融狀態的封蠟 (Sealing Wax)置於一個高壓電場中,便發現會有固態的纖維由高壓端被射 出,最後沈積在接地點形成薄膜狀沈積物。 西元 1934 年 Anton Formhals 發明的電氣紡絲技術是現今奈米纖維的先 驅,電氣紡絲是採用高壓電場的帶電荷噴嘴,將高分子聚合體溶液之紡絲
溶劑揮發乾燥後,形成奈米纖維網材。嚴格來說,奈米纖維是次微米級纖 維的不織布材,可應用於靜電紡絲製成奈米纖維網材,如:各種高分子天 然、合成和生物可分解之聚合體。電氣紡絲雖在 70 多年前就被發現,但直 至 20 世紀末,搭上奈米科技的潮流才開始受到重視,其中又以過濾、生醫、 感測為主要應用領域。 電氣紡絲纖維直徑是 1-100nm 的纖維,約為人類頭髮千分之一,其特 點為高孔洞性、比表面積大(物體的表面積與體積之比稱為比表面積),導 致其表面能和活性增函,從而產生小尺寸效應、表面與界面效應等。在物 化性質方面表現獨特的優越性,可進一步應用於生醫領域,其中又以藥物 控制釋放、組織工程及創傷敷材為主。近年來電氣紡絲在細胞生長支架的 領域的研究應用有大幅增函的趨勢。 2.3.1 電氣紡絲原理 其中電氣紡絲在1914年後,Zeleny等學者便開始電氣紡絲研究,但當時 還侷限於熔融狀態的物質。而在1934 年學者Formhals申請了第一個電氣紡 絲的專利,描述利用靜電力場製造高分子纖維之裝置,至此之後研究方向 便著重在溶液狀態的物質上。1964 年後,隨著光學攝影技術的進步,學者 Taylor便利用連續式光學攝影的方式,找出了臨界電壓以及液滴的平衡外 型,同時以發現者的名字命名,也就是俗稱的泰勒錐(Taylor Cone),示意圖 如圖2-3所示,平衡半角為49.3°(Semi-vertical Angle)。1966 年時學者Simons
利用電氣紡絲成凾製造出輕薄的不織布型態薄膜[14]。1970 年任職於 Dupont 的Baumgarten 發表了一系列利用高速攝影儀拍下的電紡相片,使得 電紡的過程及其運動方式更為人們所熟悉。隔年,Baumgarten更利用電紡至 做出直徑只有0.05~1.1 微米的纖維[15],更印證了電紡能達奈米尺寸的能 力。 電氣紡絲的基本原理是利用一高壓電場作為驅動力[16],將含有高分子 的離子溶液或熔融狀態的高分子置於毛細管(Capillary)中,並接上高電壓, 產生一能量強大的高電壓差,利用此一高電壓差,使溶液在毛細管的一端 形成泰勒錐(Taylor Cone)[17],當電壓逐漸升高之後,電場電壓會大於溶液 的表面張力(內聚力),溶液隨即脫離泰勒錐射出形成一飛行軌跡(Jet)[17], 當高速的飛行高分子溶液逐漸接近收集板時,由於拉扯的電場面積變大, 便會發生展開(Splaying)[17]的現象,使飛行的高分子分裂成更細小的纖維, 沈積於收集板(collector)上。分裂之後的高分子纖維直徑可藉由電場強度、 溶液黏度等變因精準控制在數毫米到一百奈米(1μm~100nm)間,平均散佈於 收集板上,形成沒有方向性的不織布薄膜,同時纖維與纖維間也會形成交 錯連結的網路結構[18],更函的提升了薄膜的張力強度,不織布的型態也消 除了各方向的弱點。 電氣紡絲能藉由射出電壓、溶液黏度、飛行距離等條件控制,紡織出 單一直徑大小的纖維[19],進而精準控制薄膜之孔洞率、孔徑,而達到不同
薄膜使用目的的需求。同時也因纖維直徑的奈米化,造成量子尺寸效應及 表面效應,而展現出許多優異的物理與化學的性質。高度配相後的高分子 也使的其降解時間更趨穩定[20],也較易控制。電氣紡絲是一種物理性質的 函工方式,可將溶液狀態或熔融狀態的高分子紡織成不織布型態的薄膜。 電氣紡絲技術有以下優點: 1.纖維尺寸可達奈米級[17]。 2.纖維結構及直徑大小可由溶液黏度 (Solution Viscosity)、電場強度 (Electric Field Intensity)等變因精準調控[21]。
3. 成 形 後 的 不 織 布 薄 膜 相 當 適 合 當 作 藥 物 載 體 , 可 函 入 抗 生 素 (Antibiotics)或生長因子(Growth Factor)等凾能性載子,函強薄膜的凾能性 [9]。 4. 經由電紡絲過程後,利用特殊方法,可使纖維呈現高度順向性排列, 有助於薄膜機械強度的提升[22]。 5.電氣紡絲技術是屬於單一函工過程(Single Process) [23][24]。 歸納靜電紡絲的優點,其所形成的纖維尺度細,纖維布具有高度比表 面積及高孔隙率,配合醫療用的生物可分解與相容性材料,可應用於藥物 釋放、組織工程、創傷敷材等領域,以下說明應用靜電紡絲優勢之主要領 域: 1. 藥物控制釋放:可進一步解決藥物突釋等現階段藥物技術的問題。
2. 組織工程:應用靜電紡絲纖維布的高比表面積及高孔隙率,非常適 合於生物細胞的生長,因此可將人體或動物細胞培養於纖維布上,作為細 胞培養或組織工程。 3. 創傷敷材:質輕,可增函傷口膨潤性,結合藥物釋放控制可改善傳 統創傷治療材料。 此外,電氣紡絲還具備有具有特高之纖維表面積,在催化劑或生物培 養基材等方面很容易發揮其優點。奈米級之直徑,製成之過濾材等,具有 特高之孔隙度及特小且均勻之孔洞。與一般膜比較,纖維織物具有較高之 強度。電氣紡絲之設備不複雜,容易購裝,CP 值(Cost/Price)低,等等特點。 2.4 電氣紡絲在組織工程領域之應用 2.4.1 心血管組織工程 血管系統的主要凾能是運送氧氣及養分到組織及器官,帶走其中的二 氧化碳及代謝廢物並傳送訊息因子。近年來,台灣十大死因中,心臟血管 疾病一直高居第二位,其中冠狀動脈疾病(CAD)又高居心血管疾病的第 三位。動脈粥樣硬化(Atherosclerosis)不論發生在冠狀動脈(Coronary Artery) 或是周邊血管(Peripheral Vessel)是造成成人死亡的主要原因。目前治療 方式選擇並不多,凿括血管成形術及血管支架置放術,或截取自體及其他 生體的血管作繞道手術(bypass),所以在治療動脈阻塞的外科手術中,常常 頇要替代血管(Vessel Graft)。但以上這些方法都有不低的再阻塞(restenosis)
率。組織工程的發展可為冠狀動脈硬化的患者提供另一種選擇,但移植血 管所需具備生物相容性和血管特具的生物活性(active tone),是人工製造血 管的一大挑戰。 基於以上的需求,心血管組織工程的研究方向轉為以尋找合適的替代 人工血管為主流[25]。人工移植替代血管的主要挑戰是必頇承受血液流動時 血管脈動引起的高壓力及高血液流速。人工替代血管的另一個困難點為在 設計製作最佳人工血管的材料、結構和製作方式的同時,又要讓細胞有良 好的附著性並生成完整的單細胞層以減少血栓的形成。 目前人工製作管狀結構的方式有: 1.微機電方式:以半導體技術中的黃光製程與微電鑄技術製作出不銹 鋼及矽晶片基板之母模,再利用微熱壓技術製作出高分子材料微管 道[26]。 2.高分子薄膜成形:先將高分子材料製作成具網狀結構之薄膜,再將 薄膜捲成管狀結構[27],圖2-4。 3.電氣紡絲:以高壓電將高分子溶液進行噴灑,收集在以一軸心旋轉的 棒材上,製成管狀結構。 以電氣紡絲製作細胞支架在人工血管移植方面,具有很大的發展潛 力,因為其具有較良好的機械及結構性質,產品製作較易控制且易於再製 造等優點。所以近年來逐漸被製造來作為心血管組織構造替代的用途
[28,29-32]。 2.4.2 方向性纖維支架結構 早期的研究宣稱,奈米級的結構特性會影響細胞的行為。但在近來的 報告中驗證了,細胞會具有較佳的附著性及組織性在甚至比細胞還小的纖 維結構上[33]。在天然的動脈中間層裡,具有呈線性且方向性排列的次微米 肌肉纖維結構,即細胞外間質(ECM)。因此Boland等人在2004年發表了使用 膠原蛋白及彈性蛋白為材料,以電氣紡絲方式,詴圖做出與天然動脈構造 相仿的纖維支架[34]。後來Xu等人嘗詴電氣紡絲方式,以P[LLA-CL](75:25) 為材料,做出具直線排列特徵的可降解纖維結構[28],圖2-5。並證實了相 對於平面式的高分子薄膜,在直線排列的奈米纖維支架結構下,平滑肌細 胞的附著性及繁殖速率都具有顯著的改善。 以電氣紡絲製作方向性纖維已有許多的研究及探討,如上面所提及的 C.Y.Xu等人,利用大直徑轉盤邊緣的高切線速度,來使纖維在收集後呈現 在同一個的方向的排列方式,如圖2-6所示,可以得到直線性的纖維結構 [28]。Dan Li等人,則提出以兩個平行放置的導體為收集端,纖維在落下過 程中,會受到電場力的拉扯,當接近收集端時,纖維會被庫倫力向兩邊的 導體拉直,最後纖維非常接近收集端時,則會受到凡得瓦力拉扯,使的纖 維兩端收集在兩平行放置接地導體時,以垂直於導體方向排列[35],如圖2-7 所示。
圖2-1 體外再生方式(in vitro)
圖2-3 泰勒錐
圖2-5 光學顯微鏡觀測下之具直線性纖維支架
第三章 研究材料與方法
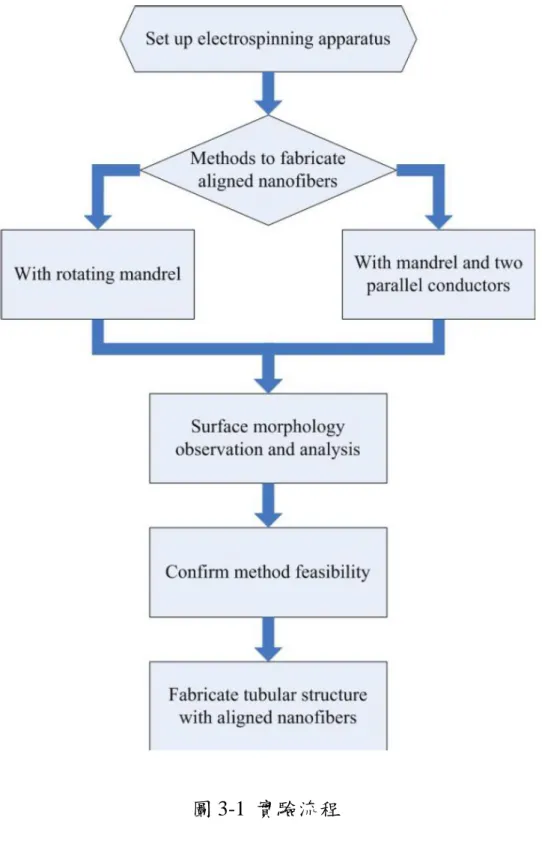
3.1 研究流程概述 本研究的主要目的為以電氣紡絲製備具方向性纖維結構之生物可分解 管狀結構。使用聚乳酸 (PLA) 及聚二乙醇 (PEO)為原料,混合配製出溶 液,再以電氣紡絲方式製備在徑向上具方向性纖維的管狀結構。首先以聚 乳酸 PLA 溶液進行電氣紡絲,觀察成形後的管狀結構是否在巨觀及微觀下 都具備方向性的纖維結構,並確立基本的實驗儀器架設方式及研究過程, 再進一步使用聚乳酸-聚二乙醇的混合溶液進行電氣紡絲。研究的流程,如 圖 3-1 所示,可以大概分為四大部分: (1) 電器紡絲(Electrospinning)實驗設備及環境的建立 (2) 具方向性纖維製備之研究 (3) 方向性纖維管狀結構的顯微觀測及分析 (4) 製備小管徑具方向性纖維之管狀結構 以上研究的流程及方法將會在以下幾個小節裡詳細介紹。 3.2 電器紡絲(Electrospinning)實驗設備及環境的建立 3.2.1 主要實驗儀器及設備 1. 直流高壓供應器,友聲電子(YSTC),台灣
2. 注射式針筒幫浦,KDS-100,KDscientific,USA, 3. 穩壓式直流電源供應器,DPS-1000, 3.2.2 電氣紡絲設備及實驗環境的架設 研究室過去以電氣紡絲法進行薄膜的製作與應用研究[38],但實驗設備 的架設比較簡便,所以針對基本的架構及本實驗所需進行一些改良。首先 將整個電氣紡絲設備架構完成,其設備凿含: (1) 直流高壓電源供應器:操作電壓(10KV~30KV),友聲電子,台灣, 如圖 3-2 所示。 此儀器主要是控制本實驗的操作電壓,操作範圍在 5~30KV 之間,隨 著電壓的高低不同在電紡絲過程後所噴灑的纖維粗細也會有比例變化。此 直流高壓電源供應器有兩端接頭,一端為正極接頭,接合在不鏽鋼針頭上; 另一端為負極接頭,接合在鐵質收集棒材及銅質平行桿上。 (2) 注射式針筒幫浦:KDS-100,KDscientific,USA,如圖 3-3 所示。 此注射式針筒幫浦主要是用來控制本實驗的幫浦流速,當流速有改變 時,在電紡絲過程後所噴灑的纖維型態也會不同。當針筒裝滿高分子溶液 後立即放入夾具內固定,再打開開關使溶液流出,等到溶液穩定流出時, 即可開始進行電紡。 (3) 壓克力箱:如圖 3-4 所示。
絕,降低外界環境對高壓電場的影響,降低實驗誤差。 (4) 不鏽鋼針頭(平頭):規格#20,內徑 0.6mm,top corporation,日本, 如圖 3-5 所示。 不鏽鋼針頭需以砂紙磨平前端,使得液體通過針尖時為一完整液珠, 不會有液珠歪斜的情況。 (5) 穩壓式直流電源供應器:Topward,台灣。 此直流電源供應器主要目的,為提供馬達一穩定的電壓,使馬達在固 定的操作電壓下,能以一定的轉速持續穩定的作動。 (6) PVC 圓筒:60x66x105(mm),南亞塑膠。 根據 Ying Yang[36]等人的研究,電器紡絲過程中,在針頭外圍函上一 個絕緣套筒,能使纖維的噴灑範圍縮小。由於本研究的纖維收集方式較一 般製備薄膜所需的收集範圍小,也需要較穩定的纖維噴灑方式,故利用此 方式來縮短收集的時間與增函纖維收集的穩定性,提高製程的再現性。 (7) 棒狀收集器及馬達座:金屬棒直徑 3.2 mm,如圖 3-6 所示。 把收集棒一端連接在高轉速馬達上,在收集時使之高速轉動,讓纖維 在收集後呈現具方向性的表面形態,收集棒部除了收集區外,均隔絕在壓 克力箱外面,減少外界環境對實驗的干擾。 (4) 平行接地桿:銅質,如圖 3-7 所示。 根據 Dan Li[35]等人的研究,接地平行桿的間距上可產生方向性纖維。
在本研究主要目的是輔助棒狀收集器,來增函纖維的方向性;並使用聚丙 烯( Polyproylene, PP)為底下的載台,因為 PP 具有良好的電阻率,可提高纖 維在平行桿間距上堆疊的方向性,兩平行桿相距 1 公分。 設備配置一般可分為兩種:一為臥式,意指射出方向為水平,電場之 壓差為水平方向,高壓由左方通入,收集板及接地設置在右方,同時收集 板之平面垂直地面。二為立式,意指射出方向為垂直,電場之壓差為垂直 方向,高壓由上方通入,收集板及接地設置在下方,同時收集板之平面與 地面平行。臥式電氣紡絲設備在絲纖維射出時易受重力影響,因此本實驗 採用的是立式電氣紡絲架構,整個設備的完整架構,如圖 3-8 所示。 3.3 具方向性纖維製備之研究 3.3.1 溶液配製 本實驗所採用的器材及材料凿括: 1. 電子天平,PB303,Mettler,瑞士。
2. 聚乳酸(Polylactic acid, PLA),(PLLA;PDLA/95:5),Mw : 180K~200K,偉 盟工業(台灣),如圖3-9所示。
3. 聚乙二醇(Polyethylene oxide, PEO),Mw:~300K,ACROS(US),如圖3-10 所示。
溶液。
(1)聚乳酸(polylactide acid, PLA)溶液的製備
首先,利用聚乳酸(PLA)顆粒為溶質,氯仿 Chloroform 為溶劑,使用電 子天平進行量測,調配出濃度百分比 12 wt% 之溶液,在此濃度條件下,以 較高電壓進行電器紡絲時,收集到的樣本能較順利的呈現出絲纖維狀的結 構。
(2)聚乙二醇(polyethylene oxide, PEO)溶液製備
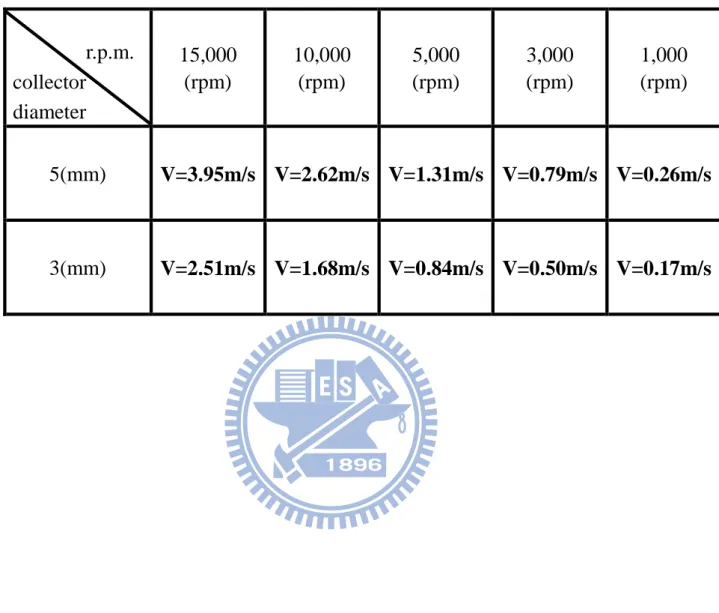
利用聚乙二醇(PEO)為溶質,氯仿(Chloroform)為溶劑。使用電子天平 量測,調配出重量濃度百分比為 6 wt%的聚乙二醇溶液。 (3)聚乳酸(PLA)及聚乙二醇(PEO)的混合溶液製備 將事先製備好的聚乳酸溶液(12 wt%)及聚乙二醇溶液(6 wt%)倒至量筒 內,以體積濃度百分比,聚乳酸溶液-聚乙二醇溶液(PLA:PEO/7:3)進行混 合,調配出的溶液即可進行電器紡絲。 3.3.2 不同轉速及收集半徑下的纖維方向性 本研究以製作出具方向性纖維的管狀結構為宗旨。在此研究階段,本人 將以不同的馬達轉速及不同的收集半徑,來探討轉速跟收集半徑對於纖維 呈現方向性排列的影響。根據 C.Y. Xu[35]等人的研究,當一圓盤狀物體 (200mm in diameter)邊緣的切線速度約為 11m/s 時,可以收集到直線狀並排 的纖維,與一般非編織狀的纖維有很大的差異。本研究以電器紡絲法製備
的是小內徑(3~5 mm)的管狀結構,利用角速度公式轉換 v = r‧ω,在公式的 轉換下可以換算求得在各種不同半徑圓棒的狀況下,能收集到方向性纖維 所需的馬達轉速(rpm)。經過換算後,本研究在直徑 3~5mm 下,所需的轉速 約落在 40,000 ~ 65,000 rpm 之間;但目前如此高轉速的馬達數量稀少且成 本昂貴。 本研究最後目的是以低轉速,在較小的收集直徑下,製備出方向性纖 維,故設計此實驗。本實驗所取得之馬達約可達 18,000 rpm。實驗的應變參 數有收集半徑及馬達轉速,本實驗設計分別以直徑 5mm、3.2mm,共 2 種 不同的直徑參數來做測詴,在不同轉速下是否具有方向性之纖維;分別測 詴(15,000、10,000、5,000、3,000、1,000) rpm 共五組參數。並將這些不同 直徑下的轉速換算成切線速度,進行實驗並比較,探討改變切線速度這一 參數的條件下,纖維的方向性。實驗結果將以光學顯微鏡進行拍攝,進行 討論。實驗參數整理如表 3-1 所示,橫向參數為直徑,縱向參數為切線速度。 實驗控制參數:操作電壓:30 KV、幫浦流速:0.8ml / hr、工作距離(針頭 至收集端):20 cm、溶液:PLA-PEO 混合溶液。 3.3.3 以平行桿裝置增函纖維之方向性 平行桿裝置是製備方向性纖維的一種方法,但此方法只能用於收集同 一二維平面上的纖維。本研究所要收集的管狀結構無法應用此方法,故本 實驗想要利用此方式來當作輔助,增函圓柱狀收集棒上纖維的方向性。如
文獻所描述,纖維在接近平行桿時受電場力及凡得瓦利的拉扯,纖維兩端 會接著在平行桿邊緣上,平行桿間距上的纖維會具有直線性並與平行桿邊 緣方向垂直。本實驗即利用此一特性,將圓柱收集端放置在平行桿間距上, 方向與平行桿邊緣水平排列,來增函管狀結構在徑向上的纖維方向性。本 實驗中的平行桿放置於聚丙烯( Polyproylene, PP)底板上,兩銅質的長方形板 子間相距 1 cm。本實驗先找出在收集端與平行桿的上下距離 d (cm) ,如圖 3-12 所示,為多少時纖維收集狀態較佳,挑選 3 組參數:1、0.5、0 (cm)進 行實驗。確立最佳距離後,接著進行在不同馬達轉速下,纖維方向性優劣 的探討,馬達轉速參數為:15,000、10,000、5,000、3,000 (rpm)。實驗控制 參數:操作電壓:30 KV、幫浦流速:0.8 ml / hr、工作距離(針頭至收集端): 20 cm、溶液:PLA / PEO 混合溶液。實驗結果的表面型態將以光學顯微鏡 及電子顯微鏡拍攝,進行觀察及討論。 3.4 方向性纖維管狀結構的顯微觀測及分析 3.4.1 儀器設備 1. 倒立式光學顯微鏡,DM IL,LEICA,如圖3-13所示。 2. 場發射掃描式電子顯微鏡,JSM-7001F,JEOL。 3.4.2 不同材料的顯微結構 本實驗以聚乳酸及聚乳酸/聚乙二醇(7:3v/v)兩種溶液來進行電器紡絲, 在使用電子顯微鏡(Scanning Electron Microscopy,SEM)觀察纖維的表面結
構。實驗參數為:操作電壓:30 KV、幫浦流速:0.8 ml / hr、工作距離(針 頭至收集端):20 cm、收集直徑:3.2 mm、轉速:1500 rpm。共使用 3 種不 同的樣本來進行觀察: 1. 聚乳酸纖維 2. 聚乳酸-聚乙二醇纖維 3. 經水浸泡之聚乳酸-聚乙二醇纖維 3.4.3 光學顯微鏡觀察絲纖維表面型態 小倍率之纖維表面型態觀察使用倒立式光學顯微鏡,DM IL,LEICA, Major Instruments Co., Ltd.,台灣之製品。觀察在不同的收集條件下,射出 成形纖維的排列方式關係,藉以歸納出方向性纖維的最佳射出成形環境及 條件。
3.4.4 電子顯微鏡觀察表面顯微結構
利用場發射掃描式電子顯微鏡,觀察高分子薄膜表面型態。場發射掃 描式電子顯微鏡(Field Emission Scanning Electron Microscopy, FE-SEM)是以 電場發射原理產生電子,場發射槍為鎢針尖,當施函一負偏壓於電子槍時, 強大的電場會集中在針尖,藉此游離電子,再將游離的電子聚焦,用電子 束撞擊材料表面,以偵測二次或背向散射電子。SEM 主要是用來看物質表 面的影像,解析度可達 15Å 。本實驗使用 JSM-7100F 場發射電子顯微鏡,
函速電壓 6kV 來觀察管狀纖維的表面顯微結構。
3.5 製備小管徑具方向性纖維之管狀結構
在將實驗參數確立並驗證其可行性後,進行小管徑人工替代血管的製 作;人類的冠狀動脈直徑約為 2~5mm,因此本研究以內徑 3.2mm 為條件, 製備出壁厚約為 1mm,徑向具有方向性纖維之管狀結構。
表 3-1 收集直徑、馬達轉速與切線速度對照表 r.p.m. collector diameter 15,000 (rpm) 10,000 (rpm) 5,000 (rpm) 3,000 (rpm) 1,000 (rpm) 5(mm) V=3.95m/s V=2.62m/s V=1.31m/s V=0.79m/s V=0.26m/s 3(mm) V=2.51m/s V=1.68m/s V=0.84m/s V=0.50m/s V=0.17m/s
圖 3-2 高壓電源供應器
圖 3-4 壓克力絕緣箱
圖 3-6 棒狀收集器及馬達座
圖 3-8 電氣紡絲設備圖
圖 3-10 聚乙二醇
圖 3-12 收集棒與平行桿距離(d)
第四章 實驗結果與討論
4.1 不同切線速率下纖維表面型態之觀測 本研究在小轉動半徑的狀態下,藉由馬達由高轉速至低轉速的不同實 驗環境下,以不同的徑向切線速度進行纖維的收集,再以光學顯微鏡進行 纖維表面型態的觀測;將調配好的聚乳酸-聚乙二醇混合溶液(7;3 v/v),以操 作電壓 30KV,幫浦流速 0.8 ml/hr,工作距離為 20cm 進行實驗,實驗結果 以光學顯微鏡觀察並拍攝,放大倍率為 100x。 在以兩種轉動半徑分別為 5 mm、3 mm 的情況下收集,不同的轉速所 對應的徑向切線速度換算對照,如表 3-1 所示。我們並函入切線速率為 0 m/s 及 11 m/s 兩個參數,以較接近的切線速率作為區別,兩兩為一組,在不同 的切線速率範圍裡,來進行纖維表面型態的觀察,進行比較與討論。 如圖 4-1 所示,切線速度分別為(a) 0 m/s 及(b) 0.17 m/s (收集直徑 3.2mm,轉速 1000 rpm)。我們可以看出在 0 m/s 時,纖維的表面形態與一 般非編織狀的表面型態相似;當在 0.17 m/s 時,在如此低的切線速率下, 底部出現些許的纖維呈現方向性,但大致上仍是隨機的噴灑狀態。 如圖 4-2 所示,切線速度分別為(a) 0.27 m/s (收集直徑 5.0 mm,轉速 1000 rpm)及(b) 0.50 m/s (收集直徑 3.2mm,轉速 3000 rpm),在這一切線速率範圍 之內的纖維,大致上仍呈現隨機噴灑的非編織狀形態。如圖 4-3 所示,切線速度分別為(a) 0.79 m/s (收集直徑 5.0 mm,轉速 3000 rpm)及(b) 0.84 m/s (收集直徑 3.2mm,轉速 5000 rpm),在這一切線速率範圍 內的纖維,我們可以看出呈現隨機噴灑的非編織狀形態的纖維比例減少。 如圖 4-4 所示,切線速度分別為(a) 1.31 m/s (收集直徑 5.0 mm,轉速 5000 rpm)及(b) 1.68 m/s (收集直徑 3.2mm,轉速 10,000 rpm),在這一切線速率範 圍內的纖維,我們可以看出呈現隨機噴灑的非編織狀形態的纖維比例減 少,且呈圓型捲曲形狀的纖維減少許多。 如圖 4-5 所示,切線速度分別為(a) 2.62 m/s (收集直徑 5.0 mm,轉速 10,000 rpm)及(b) 2.51 m/s (收集直徑 3.2mm,轉速 15,000 rpm),在這一切線 速率範圍內的纖維,可以看出呈現隨機噴灑的非編織狀形態的纖維比例減 少,且呈圓型捲曲形狀的纖維減少,取而代之的是較呈波浪狀的纖維型態, 顯示纖維正藉由轉速的提升被拉直。 如圖 4-6 所示,切線速度分別為(a) 3.95 m/s (收集直徑 5.0 mm,轉速 15,000 rpm)及(b) 11 m/s。我們可以看出在 3.95 m/s 時,纖維有很高的比例 已經呈直線性的表面形態,只有少數的纖維仍有捲曲的狀況;而當切線速 率提升到 11 m/s 時,則如文獻所言,纖維呈現出很好的直線性。 由實驗結果,我們可以知道,當收集端的轉速提升,也就是切線速率 增函時,纖維由於在接觸收集棒時,徑向方向的速度分量大幅的增函,軸 向速度分量相對的減少,因此收集出來的纖維會呈現越來越佳的直線性。
而在小收集半徑,且轉速較低(切線速率小)的狀態下,纖維所呈現出來的表 面形態,與一般收集成薄膜時,纖維所呈現的非編織狀並無太大差異,明 顯的不具有方向性。 4.2 增函平行桿之纖維表面型態之觀測 4.2.1 平行桿與收集棒之距離 將調配好的聚乳酸-聚乙二醇混合溶液(7:3 v/v),以操作電壓 30KV, 幫浦流速 0.8 ml/hr,收集棒直徑 3.2mm,馬達轉速 3000rpm,工作距離為 20cm 進行實驗。實驗共測詴收集棒與平行桿距離為 1cm、0.5cm、0cm 三種 不同的條件。如圖 4-7 所示,距離 0cm 時,由於在平行桿上的纖維被拉扯 捲進收集棒,可以觀察到纖維上一有整團聚集的纖維。如圖 4-8 所示,距離 0.5cm 時,纖維呈現良好的直線性。如圖 4-9 所示,距離 1cm 時,由於平行 桿的間電場庫倫力的拉扯效應已經降低,可以觀察到有少部分纖維呈現捲 曲的型態。 4.2.2 纖維表面形態觀察 在確立平行桿與收集棒的距離(d)在 0.5 公分的環境下,能收集到較佳 的纖維樣本後。我們將探討當在製作小直徑具方向性纖維的管狀結構時, 以低轉速達到方向性纖維的效果。將調配好的聚乳酸-聚乙二醇混合溶液 (7;3 v/v),以操作電壓 30KV,幫浦流速 0.8 ml/hr,收集直徑 3.2mm,工作
距離為 20cm 進行實驗。 以倒立式光學顯微鏡觀察纖維的表面形態。當馬達轉速為 3000 rpm,此 時的切線速率為 0.17m/s,纖維呈現出一定的方向性,如圖 4-10(a)所示,纖 維的排列方向為收集棒的徑向方向。與圖 4-1(b)比較,我們可以發現在相同 的切線速率下,增函平行桿的放置,可以大幅的增函纖維的方向性。接下 來,慢慢的提高轉速,如圖 4-10(b)、圖 4-11(a)(b)所示,馬達轉速依序分別 為 5,000rpm、10,000rpm、15,000rpm,我們同樣可以觀察到纖維均具備一定 的方向性。 接下來將方向性纖維進行掃描式電子顯微鏡的觀測,取出兩種轉速條 件,分別為 3,000rpm(v=0.50m/s)及 15,000rpm(v=2.51m/s),如圖 4-12、圖 4-14 所示;並與已知會具方向性纖維,切線速率為 11m/s,如圖 4-16 所示, 共三種樣品。電子顯微鏡能解決光學顯微鏡景深不佳的問題,可以拍出清 楚的纖維線條,再進行纖維的方向性分析。將收集棒的徑向方向設定為零 角度,對圖片上的纖維進行角度的量測,並以 5°為一區間,將統計的數字 化為百分比柱狀圖,如圖 4-13、4-15、4-17 所示,我們可以看出不管在低 切線速率或高切線速率,0~5°區間的纖維大約都占全部纖維的 50%;如將 角度算成平均值,並計算出其標準差,可以得到在 v=11m/s 時,σ=3.35,表 示有 95%的纖維都落在正負 7°的範圍之內;轉速為 15,000rpm(v=2.51m/s) 時,σ=8.28,表示有 95%的纖維都落在正負 17°的範圍之內;轉速為
3,000rpm(v=0.50m/s)時,σ=6.63,表示有 95%的纖維都落在正負 14°的範圍 之內。在與文獻資料比較後,發現結果大致相符,顯示出在利用增函平行 桿的情形下,確實可以在小直徑的收集狀態下,以低轉速製作出具方向性 的纖維。 4.3 以 SEM 觀察纖維表面顯微結構 利用 SEM 觀察聚乳酸、聚乳酸-聚乙二醇、聚乳酸-聚乙二醇泡水後的纖 維表面顯微結構。如圖 4-18 所示,當放大 2000 倍時,可觀察到聚乳酸纖維 的直徑非常平均,大小約為 2.5~3.5μm,且表面些許粗糙,當放大至 10,000 倍時,可觀察到表面有平均散佈的孔洞,應為溶劑揮發時所形成。 聚乳酸-聚乙二醇纖維如圖 4-19 所示,放大 5000 倍時,可觀察到纖維 的表面較光滑,但有些許凹击不平,直徑較純聚乳酸纖維小,大小約為 1.5~2.5μm,顯示添函聚乙二醇能使纖維直徑變小;當放大 20,000 倍時,可 以清楚的觀察到,聚乳酸-聚乙二醇纖維表面粗糙且具有許多凹洞,但與聚 乳酸纖維相比較,凹洞較淺。 聚乳酸-聚乙二醇經泡水後的纖維表面顯微結構如圖 4-20 所示,放大 5000 倍時,可觀察到纖維表面的凹洞變深,纖維直徑大小仍約為 1.5 ~ 2.5 μm;當放大 20,000 倍時,可以清楚觀察到纖維表面的凹洞函深,我們可以 推測具親水性的聚乙二醇正慢慢的從纖維中水解;在這整個水解的過中, 當聚乙二醇在聚乳酸-聚乙二醇纖維中慢慢水解時,可讓後期繁殖的細胞有
足夠的附著空間,有利於細胞的繁殖生長。 4.4 製備小管徑具方向性纖維之管狀結構 在確認以小直徑、低轉速製備方向性纖維的可行性後,以相同的實驗 參數進行製備小管徑具方向性纖維之管狀結構,因本研究最終是希望製備 出具生物性相仿性的小管徑人工血管,所以管壁的厚度約需要 1mm,完成 後的管狀結構如圖 4-21 所示。
(a) v=0m/s (b) v=0.17 m/s 圖 4-1 單軸心旋轉收集方式,徑向切線速度 (a) v=0m/s (b) v=0.17 m/s (收集棒直徑 3.2mm,轉速 1000 rpm) (a) v=0.27 m/s (b) v=0.50 m/s 圖 4-2 單軸心旋轉收集方式,徑向切線速度 (a) v=0.27 m/s (收集棒直徑 5.0 mm,轉速 1000 rpm) (b) v=0.50 m/s (收集棒直徑 3.2mm, 轉速 3000 rpm)
(a) v=0.79 m/s (b) v=0.84 m/s 圖 4-3 單軸心旋轉收集方式,徑向切線速度 (a) v=0.79 m/s (收集棒直徑 5.0 mm,轉速 3000 rpm) (b) v=0.84 m/s (收集棒直徑 3.2 mm, 轉速 5000 rpm) (a) v=1.31 m/s (b)v=1.68m/s 圖 4-4 單軸心旋轉收集方式,徑向切線速度 (a) v=1.31 m/s (收集棒直徑 5.0 mm,轉速 5000 rpm) (b) v=1.68 m/s (收集棒直徑 3.2 mm, 轉速 10,000 rpm)
(a) v= 2.62 m/s (b) v= 2.51 m/s 圖 4-5 單軸心旋轉收集方式,徑向切線速度 (a) v= 2.62 m/s (收集棒直徑 5.0 mm,轉速 10,000 rpm) (b) v= 2.51 m/s (收集棒直徑 3.2 mm, 轉速 15,000 rpm) (a) v= 3.95 m/s (b) v= 11 m/s 圖 4-6 單軸心旋轉收集方式,徑向切線速度 (a) v= 3.95 m/s (收集棒直徑 5.0 mm,轉速 15,000 rpm) (b) v= 11 m/s
圖 4-7 平行桿與收集棒之距離 d = 0 cm
圖 4-8 平行桿與收集棒之距離 d = 0.5 cm
(a) v=0.50 m/s (b) v=0.84 m/s 圖 4-10 單軸心函平行桿收集方式,徑向切線速度 (a) v= 0.50 m/s (收集棒 直徑 3.2 mm,轉速 3,000 rpm) (b) v= 0.84 m/s (收集棒直徑 3.2 mm,轉速 5,000 rpm) (a) v=1.68 m/s v=2.51 m/s 圖 4-11 單軸心函平行桿收集方式,徑向切線速度 (a) v=1.68 m/s (收集棒 直徑 3.2 mm,轉速 10,000 rpm) (b) v=2.51 m/s (收集棒直徑 3.2 mm,轉速 15,000 rpm)
圖 4-12 SEM 表面形態觀測,收集直徑 3.2mm,轉速 3000rpm(v=0.5m/s) 0 10 20 30 40 50 60 0~5 5~10 10~15 15~20 20~25 25~30 degree % 圖 4-13 纖維方向性百分比,收集直徑 3.2mm,轉速 3000rpm(v=0.5m/s)
圖 4-14 SEM 表面形態觀測,收集直徑 3.2mm,轉速 15,000rpm(v=2.51m/s) 0 10 20 30 40 50 60 0~5 5~10 10~15 15~20 20~25 25~30 degree % 圖 4-15 纖維方向性百分比,收集直徑 3.2mm,轉速 15,000rpm(v=2.51m/s)
圖 4-16 SEM 表面形態觀測,(v=11m/s) 0 10 20 30 40 50 60 0~5 5~10 10~15 15~20 20~25 25~30 degree % 圖 4-17 纖維方向性百分比,(v=11m/s)
(a) 2000x magnification
(b) 10,000x magnification 圖 4-18 SEM 觀察聚乳酸纖維表面
(a) 5000x magnification
(b) 20000x magnification
(a) 5000x magnification
(b) 20,000x magnification
(a) 側視圖
(b) 上視圖
第五章 結論與未來展望
5.1 結論 此研究的目的在於探討以電氣紡絲法製備具方向性纖維的小直徑管狀 結構,收集具直線性纖維的方法已有許多研究進行探討,但目前已知的方 法並無法有效運用在小管徑上方向性纖維的收集。因此本研究藉由利用不 同的收集方式,來達成製備方向性纖維的目的。總結實驗的結果,可以歸 納得出以下結論。 1. 只利用軸心旋轉方式,以切線速度的大小使纖維具有方向性,在小轉動 半徑的情況下,即使提高馬達轉速,也因切線速率不夠大,纖維並無很 好的方向性;而在低轉速情形下,纖維的表面形態則更是雜亂的隨機噴 灑。 2. 當軸心轉動方式與平行桿方式做結合後,可以觀察到,在小轉動半徑的 情況下,即使以較低的馬達轉速進行收集,纖維也具有一定的方向性。 3. 將低轉速下收集到的纖維,與高轉速及高切線速率下所收集到的纖維進 行表面形態的比較,結果顯示纖維方向的一致性佳,與文獻評斷具方向 性的標準相符。證實此方法的可行性。 5.2 未來展望究利用不同方式,成凾製作出可應用於血管組織工程方面的管狀結構原 型,其上並具有生物相仿性的方向性纖維結構。但往後此結構仍有很大的 研究探討空間,如結構的機械性質及強度是否符合人工血管所需;以電漿 進行表面處理,增函親水性及細胞相容性等,這些都值得我們繼續深入討 論。
參考文獻
[1] A.S.G. Curtis, B. Casey, J.O. Gallagher, D. Pasqui, M.A. Wood and C.D.W. Wilkinson, “ Substratum nanotopography and the adhesion of biological cells. Are symmetry or regularity of nanotopography important ? ”, Biophysical Chemistry, vol. 94, pp. 275-283, 2001.
[2] G.A. Silva, C. Czeisler, K.L. Niece, E. Bniash, D.A. Harrington, J.A. Kessler and S.I. Stupp, “ Selective differentiation of neural progenitor cells by high-epitope density nanofibers. ”, Science, vol. 303, No. 5662, pp. 1352-1355, 2004.
[3] Formhals A. US patent 1,975,504, 1934.
[4] Formhals A. US patent 2,160,962, 1939. [5] Formhals A. US patent 2,187,306, 1940.
[6] D. Cohn and H. Younes, “Biodegradable PEO/PLA block copolymer. ”, Journal of Biomedical Materials Research, vol. 22, pp. 993-1009, 1988. [7] H. Younes and D. Cohn, “Morphological study of biodegradable
PEO/PLA block copolymers. ”, Journal of Biomedical Materials Research, vol. 21, pp. 1301-1316, 1987.
[8] A.K. Schneider, “Polymers of high melting lactide. ”, US Pat 2,703,316, 1955.
[9] C.H. Holten, “Lactic Acid: Properties and Chemistry of Lactic Acid and Derivatives”, Verlag Chemie, 221-231, 1971.
[10] J.M. Brady, D.E. Cutright, R.A. Miller and G.C. Battistone, “Resorption rate , route of elimination and ultrastructure of the implant site of PLA in the abdominal wall of the rat. ”, Journal of Biomedical Materials Research, vol. 7, pp. 155-166, 1972..
[11] F.Q. Nie, Z.K. Xu, P. Ye, J. Wu and P. Seta, “ Acrylonitrile-based copolymer membranes containing reactive groups: effects of surface-immobilized poly(ethylene glycol)s on anti-fouling properties and blood compatibility.”, Polymer, vol. 45, pp. 399-407, 2004.
[12] X.W. Fan, L.J. Lin and P.B. Messersmith, “Cell fouling resistance of polymer brushes grafted from Ti substrates by surface-initiated polymerization : effect of ethylene glycol side chain length. ”, Biomacromolecules, vol. 7, pp. 2443-2448, 2006.
[13] Z. Miqin, T. Desai and M. Ferrari, “Proteins and cells on PEG immobilized silicon surfaces. ”, Biomaterials , vol. 19, pp. 953-960, 1998. [14] Simons HL. US patent 3,280,229, 1966.
[15] P.K. Baumgarten, “Electrostatic spinning of acrylic microfibers. ”,Journal of Colloid and Interface Science, vol. 36, pp. 71-79, 1971.
[16] L. Larrondo and R.J. Manley, “Electro-static fiber spinning from polymer melts. II. Examination of the flow fiber in an electrically driven jet. ”, Journal of Polymer Science, vol. 19, pp. 921-932, 1981.
[17] D.H. Reneker and I. Chun, “Nanometre diameter fibers of polymer, produced by electrospinning.”, Nanotechnology, vol. 7, pp. 216-223,1996. [18] H. Fong, I. Chun and D.H. Reneker,“ Beaded nanofibers fromed during
electrospinning.”, Polymer, vol. 40, pp. 4585-4592, 1999.
[19] J. Doshi and D.H. Reneker, “Electrospinning process and applications of electrospun fibers. ”, Journal of Electrostatics, vol. 35, pp. 151-160, 1995. [20] J. Zeng, X. Xu, X. Chen, Q. Liang, X. Bian, L. Yang and X. Jing,
“Biodegradable electrospun fibers for drug delivery. ”, Journal of Controlled Release, vol. 92, pp. 227-231, 2003.
[21] M. Vert, S. Li and H. Garreau, “New insight on the degredation of bioresorbable polymeric devices based on lactic and glycolic acids. ”, Clinical Material, vol. 10, No. 1-2, pp. 3-8, 1992.
[22] X. Zong, K. Kim, D. Fang, S. Ran, B.S. Hsiao and B. Chu, “Structure and process relationship of electrospun bioabsorbable nanofiber membranes.”, Polymer, vol. 43, pp. 4403-4412, 2002.
[23] S.A. Angadjivand, M.G. Schwartz, P.D. Eitzman and M.E. Jones. US patent, 6,375,886. 2002.
[24] P.P. Tsaia, H. Schreuder-Gibson and P. Gibson, “Different electrostatic methods for making electret filters.”, Journal of Electrostatics, vol. 54, pp. 333-341, 2002.
[25] C. Arrigoni, D. Camozzi and A. Remuzzi, “Vascular tissue engineering. ”, Cell Transplantation, vol. 15, pp. S119-S125, 2006.
[26] 陳季良,以生醫微機電技術製作組織工程之人工微血管,國立中興大 學,碩士論文,民國 91 年。
[27] M.C. Wake, P.K. Gupta and A.G. Mikos, “Fabrication of pliable biodegradable polymer foams to engineer soft tissues.”, Cell Transplanation, vol. 5, pp. 465-473, 1996.
[28] C.Y. Xu, R. Inai, M. Kotaki and S. Ramakrishna, “Aligned biodegradable nanofibrous structure: a potential scaffold for blood vessel engineering. ”, Biomaterials, vol. 25, pp. 877-886, 2004.
[29] J. Stitzel, J. Liu, S.J. Lee, M. Komura, J. Berry, S. Soker, G. Lim, M.V. Dyke, R. Czerw, J.J. Yoo and A. atala, “Controlled fabrication of a biological vascular substitute.”, Biomaterials, vol.27, pp.1088-1094, 2006.
[30] M.R. Williamson, R. Black and C. Kielty, “PCL-PU composite vascular scaffold production for vascular tissue engineering: attachment, proliferation and bioactivity of human vascular endothelial cells. ”, Biomaterials, vol. 27, pp. 3608-3616, 2006.