微生物產業生物危害調查
吳俊德
1張靜文
3陳振和
1于台珊
2洪其璧
1 1 長榮大學職業安全與衛生學系 2 行政院勞工委員會勞工安全衛生研究所 3 台灣大學公共衛生學院環境衛生研究所摘 要
由於現代生物科技快速發展,利用微生物於生產製程並經由生物程序來生產製造產品,或是改良 微生物及其相關產品的產業日益蓬勃,這類產業統稱為「微生物產業」。因為某些特定微生物已被證實 或懷疑和人類一些特定的不良健康效應有關聯,微生物產業工作人員因使用操作微生物,所造成的微 生物暴露狀況及其可能引發的生物危害問題必須加以正視。在本研究中,我們對國內現今微生物產業 在研究實驗和生產製造所可能造成的微生物暴露狀況,以郵寄問卷和電話訪問方式,調查廠商所使用 的微生物的菌種名稱、生產製程使用微生物的情形、並對含微生物的原料和產品資料進行收集。此 外,並針對 30 家廠商實施現場訪視評估,實地了解其作業人員可能的微生物暴露的可能性,及現有的 暴露控制預防措施。結果發現:國內的微生物產業大體上可分為傳統食品釀造及新興的生物科技。新 興的微生物產業依其產品適用對象,可大致上分為:菌體肥料或生物肥料、動物飼料添加物、農業或 環保生物製劑、生技製藥、檢驗試劑、人體和動物疫苗和保健或健康食品等七大類。傳統食品釀造使 用食用菌或是對人體無害的菌種,且未涉及基因改造的問題。新興的生物科技產業確有基因改造微生 物的使用,但尚未使用於疫苗的製造。微生物產業作業人員的微生物暴露狀況,未來應加以重視並實 施監測的產業項目包括:疫苗製造和檢驗試劑製造;並針對涉及醱酵製程,進一步評估作業環境中非 致病性微生物種類與濃度,以評估用於醱酵製程的微生物是否有引發作業員工過敏反應的健康風險。 關鍵詞:生物性危害、微生物產業、生物科技產業、基因改造、現場訪視緒 言
廣義的生物技術指利用生物體來製造產品 的技術[1],根據此定義生物技術包括人類利用 酵母菌發酵製造食品,利用微生物製造抗生素 治療疾病,及近年來分子生物學在基因操作技 術上的突破,開創生物科技新領域,應用層面 也因而從傳統農業及食品製造,擴展至醫藥開 發、診斷試劑,廢棄物處理等方向,成為二十 一世紀產業發展的新潮流。我國從民國 71 年行 政院頒布「科學技術發展方案」中,將「生物 技術」明定為八大重點科技之一,自此透過產 官學的合作,帶動國內生物科技產業積極發 展;民國八十六年行政院跨部會的「生物技術 產業指導小組」的成立,執行將生物技術推動 為國家重要產業的工作[2]。 依據生物技術的廣義定義,生物技術可進 一步詮釋為「利用生物細胞(包括動物、植物 民國 90 年 1 月 15 日收稿,92 年 8 月 22 日修訂,民國 93 年 5 月 27 日接受 通訊作者:吳俊德,長榮大學職業安全與衛生學系,台南縣歸仁鄉長榮路一段 396 號及微生物等)或其代謝物質,並經由生物程序 來生產製造產品或改良動物、植物或微生物及 其相關產品,以增加人類生活品質與福祉的科 學技術」[3]。因此,對於利用微生物於其製程 中,並經由生物程序來生產製造產品,或是改 良微生物及其相關產品的產業,在本研究中統 稱為「微生物產業」,例如:利用微生物發酵製 造醬油、啤酒、檸檬酸等食品;利用基因工 程、細胞融合與蛋白質工程技術開發新藥或疫 苗等。 由於利用微生物於生產製造過程中,如: 製備生物培養液、在醱酵槽中大量繁殖微生 物、微生物菌株分離及產物純化、處理製程所 產生的廢棄物,工作人員均有可能暴露於所使 用的微生物及其產物(如:細菌內毒素、細菌 外毒素、細菌與真菌酵素、抗生素或其他代謝 物、真菌孢子等),而造成工作人員健康上的潛 在危害。有關暴露於微生物本身或它所衍生的 分泌物或毒素所造成的健康危害,近年來國外 的研究已有一些疾病病例報告,主要包括微生 物感染、中毒或過敏症狀的出現[4, 5];在細胞 與真菌中生產酵素的工作人員出現氣喘與類似 感冒的症狀,血液中對 Bacillus subtilis 抗體效 價明顯上升,並有肺功能受損情形[6]。在生物 科技工廠工作的工人,因暴露於製程中所使用 的 Aspergillus niger,從菌種培養液所逸散的孢 子與抗原物質,而出現過敏症狀[7]。類似因使 用 Aspergillus niger 於製程中,導致員工發生過 敏 和 呼 吸 道 不 適 的 現 象 , 也 發 生 在 以 糖 蜜 (molasses)為原料醱酵生產檸檬酸的工廠中; 經 過 測 定 發 現 此 工 作 環 境 空 氣 中 Aspergillus niger濃度為 490 CFU/m3[8]。在以理論方式探討 利用基因重組衍生的基因改造生物(genetically modified organisms)的產業所可能造成的健康 危害研究中,研究者認為其風險不高,但仍需 繼續進行長期的追蹤觀察來證實這樣的結論; 無論如何,研究者建議此產業仍應注意並採行 完善的生物危害控制防範措施[9]。 目前有關國內生物科技廠商名錄已逐步建 立[10],但仍缺乏詳細的製程資料及所使用的生 物技術和微生物種類的描述。而國內對於微生 物產業,如: 醱酵工業、製藥工業、農產或農藥 工業從業員工的生物危害尚無詳細的調查。為 了評估相關產業的職業性生物危害,有必要藉 由系統性的資料庫搜尋,取得國內相關產業與 產品資料。並對應用微生物於製程的各種產業 進行實地現場調查,以了解與微生物有關的製 程、所使用微生物的種類與可能含微生物的產 物、以及工作人員的微生物暴露方式,更進而 評估於產業製程所使用微生物及其產物的潛在 健康危害。 本研究的目的主要為:1.建立國內使用微生 物於研發及生產製程的事業單位(簡稱微生物 產業)資料,2.透過問卷調查、現場訪視及文獻 回顧方式,建立微生物產業工作人員微生物暴 露型態、生物危害程度與現階段暴露控制與管 理情形等資料。
研究方法
1. 建立國內相關微生物產業的基本資料 透過財團法人生物技術開發中心的「生技/ 醫藥廠商名錄」與財團法人食品工業發展研究 所「食品產業資料庫」的查詢,建立國內微生 物產業相關廠商基本資料庫。其中「生技/醫藥 廠商名錄」共分為西藥製藥、中藥製藥、生技 藥品、藥物研發、農業、食品加工、診斷技 術、臨床前實驗、毒理、委託研究、委託製 造、儀器供應、材料供應、環保以及其他等類 別,本研究開始之初,由此名錄登錄 160 家廠 商資料。由於生技開發中心的資料庫,主要針 對以分子生物和基因工程等科技廠商為主,較 少涵蓋傳統生物技術產業(如:食品醱酵等產 業)的廠商資料。為補齊此不足,另外使用財 團法人食品工業發展研究所「食品產業資料 庫」,以「與微生物或其產物相關之食品種類」 且排除「僅屬進口之經銷商」進行搜尋,共計 取得 201 家廠商資料。廠商資料主要包括:事 業單位名稱、通訊資料、資本額以及微生物相 關產品。考量生物技術亦應用於生物農藥的製 造,傳統農藥製造廠可能因應潮流做企業轉 型,而投入生物農藥的研發與製造,故將勞委 會勞工安全衛生研究所「IOSH87-A301 農藥工 廠勞工暴露評估技術先驅計畫(I)」所建立的農 藥工廠資料庫所登錄的 51 家廠商,也納入本研 究中。此外亦從報章媒體與網路上工會名錄等來源搜尋新興廠商資料。 2. 建立微生物產業其微生物相關製程資料 為收集國內微生物產業及其生產製程所使 用微生物的相關資料,首先以問卷查詢各事業 單位從民國 88 年到訪視進行期間,在生產製程 中使用微生物的情形。問卷內容除依據本研究 目的而設計外,另外參考國外生物科技產業微 生物暴露偵測狀況調查所提列的詢問項目[11]。 其具體內容包括:基本資料、研究及檢驗實驗 室微生物使用操作情形、生產製程步驟和生產 製程微生物使用操作情形、微生物暴露的環境 監測狀況、和含微生物的廢棄物處理等五大部 分。問卷的初稿經學者及微生物產業工廠管理 者審閱,並於研究執行期間時,邀集國內工業 衛生和微生物產業有關的專家和學者審查評 估,針對問卷內容提出修正意見。整個問卷依 專家審查意見修改和調整內容,而完成微生物 產業生物危害調查訪視問卷。 基於成本效益的考量,首先將問卷以郵寄 方式送達微生物產業有關的事業單位,請該單 位研究及試驗實驗室負責人、工業安全衛生人 員、製程工程師或工廠負責人據實填寫。並於 問卷郵寄出一個月後,對未回應的事業單位逐 一以電話訪問進行追蹤調查,以收集事業單所 使用微生物、生產製程和人員暴露相關資料, 以提高調查資料的完整性。 3. 進行事業單位現場訪視 除了以問卷調查收集資料外,本研究亦選 擇具代表性的事業單位,在徵求對方同意及約 定訪視時間後,對其生產現場實地進行訪視。 此現場訪視除了可以驗證問卷調查的資料的可 靠性,也可以由訪視中記錄一些在問卷調查中 所無法獲得的訊息。在進行現場訪視評估前, 我們設計一份現場訪視評估紀錄表,使得現場 訪視有其一致的評量依據。此現場訪視評估紀 錄表,內容設計重點主要包括: (1) 微生物相關製程描述─依各不同製程逐一 記錄 (2) 製程使用微生物及其產物之名稱─包括學 名和商品名 (3) 是否使用或生產基因改造微生物 (4) 中間微生物相關產物 (5) 是否有中間產物為基因改造微生物 (6) 微生物製程的最終產品名稱 (7) 微生物製程相關員工人數和配置狀況 (8) 微生物暴露員工人數 (9) 有無微生物暴露環境監測及其監測方式與 時間間隔 (10) 微生物暴露環境監測目的 (11) 微生物暴露防護措施 (12) 有無微生物暴露防護訓練計畫 (13) 微生物暴露控制設備型式和維護狀況 (14) 微生物廢棄物處理方式 4. 問卷資料分析 問卷調查資料以 Microsoft Access 設計和 問卷格式一致的資料庫檔案,所有問卷資料的 鍵入及儲存,均在此格式中進行。問卷訪視及 現場訪視資料以統計套裝軟體 S-plus 進行分 析,以適當的統計指標描述問卷和現場訪視調 查結果,並解釋這些統計結果所顯示的意義。 統計分析的重點包括:基本資料分析、使用微 生物種類、暴露途徑和時間分析,暴露控制設 施和暴露管理狀況。由於問卷所能收集的資料 有限,此暴露危害分析主要著眼在定性的風險 描述,也就是說,依據問卷調查所收集的微生 物製程資料,進行微生物暴露可能危害分析, 定量的風險評估和分析在本研究中並未進行。
結 果
1. 問卷訪視 在本研究中列入郵寄名單的微生物產業廠 商名錄,主要包括經濟部產業資訊服務網中生 物科技開發中心生技醫藥速報中的廠商名錄, 食品工業發展研究所的食品釀造廠商名錄,國 內農藥工廠名錄,以及搜尋網站上的工會名錄 所得相關廠商名錄。由於過去對微生物產業的 分類方式,如醫藥產業、食品產業、特定化學 品和其他[1],或財團法人生物技術開發中心的 生技醫藥速報中的分類方式,對本研究中問卷 資料和現場訪視所涵蓋的微生物產業廠商,都 無法做適合的分類,所以在此我們依所獲得廠 商的特性分類為:(1)傳統食品釀造(2)菌體肥料(或稱生物肥料)(3)動物飼料添加(4)農業或環 保生物製劑(5)生技製藥(6)檢驗試劑(7)人體及動 物疫苗(8)保健及健康食品等八大類,問卷訪視 廠家數依此分類整理於表 1。 本研究一共完成 410 份問卷,由於有很多 廠商回覆製程中未使用任何微生物(98 家)及 所填的資料並不齊全(240 家),因此資料完整 能進一步分析的問卷份數只有 72 份。表 2 表列 微生物產業中屬於生物科技產品的適用對象, 在 57 家中用於人體的百分比約為 63%。表 3 為 微生物產業所生產的生物科技物產品的種類, 59 家中以食品佔 46%最高,其次依序為化妝品 (34%)、肥料(15%)、藥品(12%)、檢驗試 劑(10%)和飼料(10%)。 在 72 份回收問卷中設有研究或試驗用實驗 室佔 58%(42 家),有研究或試驗實驗室的公司 67%有微生物操作用途的通風櫥。有 4 家公司有 生物安全等級第二級(biosafety level 2)的通風 櫥,有 5 個公司有病原菌專用設施(其等級為 P-1級有 2 家,P-2 級有 2 家和 P-3 級有 1 家)。 在此所謂 P-1、P-2 和 P-3 等級的意義為物理性 表 1 訪視廠商依產業特性分類一覽表 產業特性 訪視家數 傳統食品釀造 174 菌體肥料 3 動物飼料添加物 8 農業或環保生物製劑 16 生技製藥 44 檢驗試劑 29 人體及動物疫苗 4 保健或健康食品 30 其他 102 總數 410 表 2 微生物產業中生物科技產品的適用對象 (n=57) 項 目 家 數 回答百分比 動物 12 21 植物 11 19 人類 36 63 環境 28 49 其他 14 25 防護(Physical Containment)等級,區分為 P-1、P-2、P-3 和 P-4 四個等級。物理性防護的目 的依據行政院國家科學委員會所頒定的”基因 重組實驗守則”中所作的描述為”將重組體 (recombinant)隔離在設施或設備內,防止實 驗人員和其他物品受到污染,並且防止其向外 界擴散”[13]。 在 49 家回答廠家中,研究及試驗實驗室內 最經常使用的滅菌方法為高壓蒸氣法、紫外光 法和火焰法(表 4)。49 家中有回答執行微生物 環境測定者共 25 家,其測定實施時間主要採不 定期測定(36%),其次為每月測定(24%),約 有 24%(12/49)的廠商在每半年內進行作業環 境檢測(表 5)。42 家設有實驗室的廠商會提供 工作人員預防暴露的個人防護設備,防護設備 的種類主要為防護手套(59%)、可拋棄式防護 口罩(67%)和防護衣(41%)(表 6)。 表 3 微 生 物 產 業 中 生 物 科 技 產 品 的 種 類 (n=59) 種 類 家 數 回答百分比 檢驗試劑 6 10 疫苗 1 2 藥品 7 12 合成胜 2 3 食品 27 46 酵素 5 8 環境污染控制 4 7 肥料 9 15 飼料 6 10 化粧品 20 34 其他 27 46 表 4 研究及試驗實驗室所使用的滅菌方法 (n=49) 種 類 家 數 回答百分比 高壓蒸氣滅菌法 46 94 紫外光法 27 55 火焰法 25 51 高溫法 6 12 製劑消毒法 6 12 輻射法 2 4 過濾法 13 27 其他 1 2
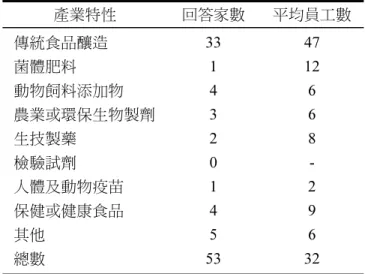
表 5 研究及試驗實驗室環境測定實施時間 (n=25) 測定實施時間 家數 回答百分比 每天 0 0 每週 2 8 每月 6 24 每兩個月 0 0 每季 1 4 每半年 3 12 每年 3 12 不定期 9 36 其他 1 4 表 6 研究及試驗實驗室操作使用微生物時所 使用的個人防護設備(n=42) 種 類 家 數 回答百分比 防護手套 29 59 可拋棄式防護口罩 33 67 防護眼罩 13 27 防護面具 10 20 防護衣 20 41 全面式防護具 1 2 關於生產製程部份,72 家回收問卷中, 56%有產品開始量產,其中僅有 1 家公司回答於 生產製程中使用基因改造微生物。參與使用微 生物生產製程的員工人數如表 7,其中以食品釀 造產業平均員工人數為 47 人最多,而菌體肥 料、生技製藥和保健或健康食品的平均員工人 數約 10 人。生產製程中有微生物逸散或洩漏到 空氣或工作環境地面的情形的佔 25%(10/40), 逸散或洩漏微生物的暴露途徑主要為皮膚接觸 (25%),其次為吸入(18%),食入的情況並不 顯著。僅有 4 家工廠對生產製程的特定微生物 實施暴露採樣監測。對於使用微生物的工作環 境約 60%工廠裝設有通風排氣設備,其中三分 之二的通風排氣設備型式為之部排氣,另三分 之一為整體換氣。有 50%的公司提供生產製程 工作人員個人防護具,可拋棄式防護口罩為最 常 使 用 的 防 護 具 ( 8 5 % ), 防 護 手 套 居 次 表 7 參與使用微生物生產製程的員工人數 產業特性 回答家數 平均員工數 傳統食品釀造 33 47 菌體肥料 1 12 動物飼料添加物 4 6 農業或環保生物製劑 3 6 生技製藥 2 8 檢驗試劑 0 - 人體及動物疫苗 1 2 保健或健康食品 4 9 其他 5 6 總數 53 32 (61%)。個人防護具每次操作都使用的約佔 60%,防護具主要由使用者本人保管,絕大部份 廠商認為保管防護具的場所清潔,僅有 30%有 個人防護具書面化配合計劃。 表 8 為微生物產業所使用的微生物種類, 經查閱國家科學委員會基因重組守則與美國 Center for Disease Control and Prevention 的 Department of Health and Human Services所制定 的生物安全守則(Biosafety Manual)[14]所表列 的微生物生物安全等級後發現,生技製藥、人 體疫苗和檢驗試劑製造三項產業涉及生物安全 等級第二級微生物的使用,這些微生物大體上 為致病性微生物,其所需物理防護等級為 P-2 或 以上。此外,檢驗試劑製造有使用基因改造微 生物的情形。有關含微生物的廢棄物處理,由 廢棄物代處理公司清運處理和自行處理的百分 比差不多。負責廢棄物清運處理的人員主要為 製程工作人員(35%),其次為工安環保人員 ( 29% ), 再 其 次 為 廢 棄 物 處 理 公 司 的 人 員 (19%)。有 39% 的廠商會提供個人防護具給 廢棄物清運人員,所提供的防護具主要為防護 手套和可拋棄式防護口罩,有 3 家廠商擬定使 用個人防護具的書面配合計畫。各工廠處理含 微生物廢棄物的費用差異很大,費用範圍在每 年 1.2 萬到 1.1 億元之間,年平均廢棄物的處理 費用約為九百多萬,可見微生物產業廠商每年 用於處理廢棄物的費用並不低。
表 8 微生物產業所使用的微生物物種 產 業 特 性 微 生 物 物 種 名 稱 生物安全等級 Aspergillus niger 1 Aspergillus oryzae 1 Bacillus subtilis 1 Bifidobacterium bifidum 1 Candida albican 1 Corynebacterum glutamicum 1 Lactobacillus acidophilus 1 Lactobacillus bulgaricus 1 Lactobacillus plantarum 1 Micrococcus luteus 1 Monascus anka 1 Pichia pastoris 1 Saccharomyces cerevisiae 1 Saccharomyces cerevisiae Hualien 1
Saccharomyces pake 1 Streptococcus thermophilus 1 Rhizopus delemar 1 Zygosaccharomyces rouxii 1 傳統食品釀造 毛黴菌屬 1 Actinomacor taiwanensis 1 Aspergillus oryzae 1 Aspergillus kawachii 1 Bifidobacterium longum 1 Canclida versatilis 1 Lactobacillus acidophilus 1 Lactobacillus spp. 1 Monascus purpureus 1 Rhizopus formosaensis 1 Rhizopus oryzae 1 Saccharomyces cerevisiae 1 菌體肥料或生物肥料 Streptomyces spp. 1
Aspergillus oryzae Fujita 1
Bacillus subtilis 1
Lactobacillus acidophilus 1 Lactobacillus coagulance-COOH 1 Super Bacillus subtilis Tiyoa Sp-HBT-k 1 Super Bacillus subtilis Tiyoa Sp-HBT-3L 1 動物飼料添加物
Super Bacillus subtilis Tiyoa Sp-HBT-R 1
Bacillus brevis 1 Bacillus stearothermophilus 1 Bacillus subtilis 1 Bacillus sp. 農業或環保生物製劑 Lactobacillus delbrueckii 1
Lactobacillus sp. Pichia farinosa 1 Rhodobactor capsulatus 1 Rhodospseudomonas palustris 1 Rhodospirillium sphaeroides 1 Rhodospirillium rubrum 1 Streptococcus sp. Streptomyces candidus 1 Streptomyces seraceticus 1 Aspergillus terrus 1 Bacillus subtilis 1 Bascillus sp. 1 Cordyces sinensis 1 Escherichia coli 1
Escherichia coli recombinant 1
Ganoderma sp. 1 Lactobacillus casei 1 Lactobacillus sp. 1 Minocycline luteus 1 Monascus ruber 1 Penicillium brevicompactum 1 Penicillium citrium 1 Pseudomonas sp. 1 Saccharomyces cerevisiae 1 Staphyllococcus aureus 2 Streptococcus sp. 1 Streptomyces faecium 1 生技製藥 Streptomyces hygroscopicus 1 Bacillus licheniformis 1 Bacillus subtilis 1
Enterovirus DNA sequence 1 Escherichia coli recombinant 1
Helicobacter pylori 1 Lactobacillus brevis 1 Lactobacillus casei 1 Lactobacillus sp. 1 Pseudomonas aeruginosa 1 Pseudomonas cepacia 1 Pseudomonas fluorescens 1 Pseudomonas aeruginosa 1 Rhodospirilloceae sp. 1 Saccharomyces cerevisiae 1 Salmonella typhimurium 2 Staphylococcus aureus 2 檢驗試劑 Staphylococcus epidermidis 1
Streptococcus agalactiae 2
Streptococcus bovis 1
Streptomyces candidus 1
Clostridium tetani 2
Haemophilus influenze type b 2 人體疫苗
Japenese encephalitis beiying strain 3
Agaricus blazei 1
Antrodia cinnamomea 1
Bifidobacterium bifidum 1
Bifidobacterium longum 1
Cordyceps sinensis(Berk) Sacc 1
Enterococcus faecalis 1 Enterococcus faecium 1 Grifola frondosa 1 Hericium erinaceus 1 Lactobacillus acidophilus 1 Lactobacillus brevis 1 Lactobacillus casei 1 Lactobacillus reuteri 1 Lactobacillus rhammosus 1
Plcurotus citrinipilcatus Sing 1 保健或健康食品 Sporolactobacillus inulinus 1 2. 現場訪視調查 本研究完成 30 家廠商現場訪視。從本研究 現場訪視觀察的結果,國內的微生物產業依產 業特性分類,大體上可分為:傳統食品釀造 (包括醬油製造、乳酸飲料製造、酒精醱酵和 食醋製造)及新興的生物科技二大類。新興的 微生物產業依其產品適用對象,在本研究實際 現場訪視觀察的結果,可大致上分為:菌體肥 料或生物肥料、動物飼料添加物、農業或環保 生物製劑、生技製藥、檢驗試劑、人體疫苗和 保健或健康食品等七個分類。延續前面問卷調 查資料分析的分類方式,以下就現場訪視所觀 察的結果,分別針對這八大產業分類就其所使 用菌種、生產製程狀況、可能微生物暴露狀況 和暴露防護情形作描述。 (1) 傳統食品釀造 這一類產業主要產品為醬油、酒精、味精 和食醋等民生用品,其生產過程所使用的微生 物為人類長久以來使用且認定為可食用或是對 人體無害的菌種,如黴菌、酵母菌等,此產業 主要使用的菌種表列於表 8,大體而言這些菌種 並不涉及基因改造問題。其主要製程流程為蒸 煮蛋白和澱粉原料、菌種培育、原料和菌種混 合醱酵、醱酵槽中醱酵、榨取或萃取汁液、調 味和包裝。以下是本訪視所見的酒精和醬油醱 酵的生產製程流程: 酒精醱酵生產流程: 菌種培養(在試管中)→麴汁(24 小時) →三角瓶培養(24 小時)→卡式罐(24 小 時)→第一酒母(酵母增殖,好氣培養) →第二酒母(酵母增殖,好氣培養)→發 酵槽(2~3 天),產量:8~10﹪酒精 80kg/ 天→蒸餾(15℃95﹪酒精)→檢定槽→酒 精儲槽 醬油醱酵生產流程: 蛋白原料:黃豆(脫脂豆片)蒸煮→冷卻↘ 澱粉原料:小麥炒熟→冷卻→磨碎→二種原料 混合並加種麴 →製麴(溫度<45℃,2 天)→成為麴豆+
鹽水→發酵(約 180 天) →通氣、攪拌→抽取醬汁和黃豆渣混合物 →以紗布過濾→壓榨 →調煮→滅菌→裝瓶→倉儲 在此生產製程中,菌種培育和原料與菌種 混合二個步驟可能造成含微生物本體或其衍生 物(如孢子)氣懸化,而導致工作人員微生物 或其孢子的暴露。由於產業長久的使用經驗, 認定製程中所使用的微生物為無害的菌種,因 此無論是研究試驗實驗室無菌操作台或是製程 的防護,主要考量是如何不會污染製程和培養 的微生物菌種和生產物質,而不是著眼在減少 人員暴露於微生物。如果未來有資料證實菌體 或孢子的暴露可能引發呼吸道過敏反應的問 題,則此產業作業員工的微生物暴露不容忽 視。 (2) 菌體肥料(或稱為生物肥料) 這 一 類 產 業 主 要 於 有 機 肥 料 中 添 加 微生 物,所添加的微生物並非單一菌種而是包含相 當多種類的微生物,通常有光合成菌、固氮 菌、乳酸菌、放線菌等(表 8)。這些微生物在 土壤中可促進肥料中有利植物生長的元素釋 放,幫助植物吸收利用這些生長所需的元素, 因而提高農作物抗病力、改善農產品質和增加 產量。目前此產業所使用的菌種大多從日本進 口,據業者所提供的訊息,這些菌種主要從自 然環境中經過實驗室篩選和純種培養而得的自 然原生菌種,並沒有經過任何基因改造。依他 們和出口國的使用經驗,不認為這些菌種的暴 露有任何健康危害的問題。這類產業的生產製 造過程如下: 有機原料(如豆渣、稻殼、椰子殼、麻油粕、 蓖麻粕或菜仔粕)混合 →有機原料醱酵(控制溫濕度和曝氣量) →醱酵腐熟達穩定狀態(溫度約 10℃和濕度 小於 40%) →添加微生物(混拌)→加壓射出成小條狀顆 粒→成品裝袋 在此製造過程中,作業員工的微生物暴露 主要發生在添加微生物於醱酵腐熟的有機肥料 的混拌,和將有機肥料填入機器加壓射出成小 條狀顆粒的過程中。在這二個操作中,由於含 有微生物菌體和孢子的粉末和已呈乾燥狀態的 有機肥料,在翻動和傳送過程中很容易變成氣 懸微粒而漂浮在空氣中,造成作業員工由呼吸 道吸入這些有機粉塵、微生物菌體和孢子。在 現場訪視中發現有雇主提供化學呼吸防護具給 作業員工使用而非防塵口罩,可見雇主意識到 粉塵暴露的問題,但卻不知如何正確選用適當 防護設備。因此,若日後懷疑此產業所使用的 微生物暴露可能有健康危害時,此產業的作業 員工的呼吸道氣懸微粒暴露測定評估,必須優 先考慮。 (3) 動物飼料添加物 這一類產業主要於水產、禽類及畜牧業養 殖使用的動物飼料中添加微生物,類似於菌體 肥料,飼料中所加入的微生物可能為單一或多 種菌種,目前此產業所使用的菌種包括:枯草 桿菌屬、乳酸菌屬、酵母菌屬等(表 8)。這些 的菌種除少數為國內業者自行分離培養的菌種 外,其他絕大部份的菌種從日本進口。訪視中 從業者所提供的資料和敘述中,確認這些菌種 純粹由自然界所分離培養的菌種,並未經過任 何基因改造。由於這些菌種均不是病原菌,業 者的使用經驗認為這些微生物的暴露應不致於 對人體健康產生危害。 此產業的生產製造過程的主要步驟如下: 菌種養分原料(包括蛋白質、澱粉、醣類 和特殊原料) →高溫殺菌→冷卻→加糖蜜及種菌 →液體或固體醱酵(若為固體醱酵,則過 程中需經過數次翻動以散熱) →冷卻→乾燥(→磨粉)→包裝 需特別說明,少數業者的製造過程在冷卻 前有一特殊高溫處理步驟,將化工澱粉敷裹於 菌種表面。此生產製造過程中可能造成作業員 工微生物暴露的步驟為種菌、乾燥和包裝,暴 露途徑主要為呼吸道吸入。和菌體肥料製造的 情形類似,若有證據支持此產業所使用的微生 物暴露可能有健康危害時,作業員工的呼吸道 氣懸微粒暴露測定評估,必須進行。
(4) 農業或環保生物製劑 這一類產業主要利用特定微生物在自然環 境存在時,成為優勢菌種而抑制其他有害植物 生長的致病微生物或昆蟲如黴菌、細菌、病 毒、紅蜘蛛等的生長繁殖,達到保護植物的作 用。其原始構想期望能取代化學農藥的使用。 這類產業經常使用的菌種為枯草桿菌、放線菌 等(表 8)。此產業的生產製造過程可分為固體 培養和液體培養二類,其操作流程如下: A. 固體培養流程: 原料淨化滅菌→磨細→添加微生物混拌→乾式培養→乾燥→包裝 ↑╴╴╴╴╴╴╴╴╴╴╴╴╴↑ (密閉作業) B. 液體培養流程: 種菌培養(在三角瓶中進行)→50 公升醱 酵槽→500 公升醱酵槽→5 公噸醱酵槽→真 空濃縮→噴霧乾燥→添加增量劑和分散劑 →成為孢子狀態→包裝 無論是固體或液體培養,這些工廠製程都 是新近裝設,所以都採用全自動化控制,所需 操作人員的數目都不多,且大部份時間都是在 控制室中監控醱酵狀況。目前所使用微生物並 未經過任何基因改造,且這些菌株都是從自然 環境中分離培養而來。由於整個生產製程因自 動化控制,操作人員的微生物暴露減至最低, 而整個生產製程中最可能有微生物暴露的操作 步驟為包裝過程,其次為實驗室菌種培養和菌 株篩選操作步驟。 (5) 生技製藥 生技製藥廠主要利用培養特定微生物,在 其生長繁殖過程中衍生具有疾病療效的藥物, 這類工廠依其生產藥物的種類和特性上的差 異,會使用不同種類的微生物,在本研究所調 查和訪視的生技製藥廠所使用的微生物表列於 表 8 中。這些微生物中有可能經過基因改造, 例如使用 Escherichia coli 加入特定的基因片段 形成質體(plasmid),用以產生所要的蛋白或多 胜,而製造多胜類藥品。 這一類產業的生產製造前的實驗室操作培 養流程,依其所生產藥品的特性而有所差異, 以下實驗室操作培養流程中,流程 A 是和大型 醱酵生產製程有關的實驗室操作培養流程,流 程 B 則是和涉及基因改造微生物的生技製藥廠 的實驗室操作培養: 實驗室操作培養流程: A. 振盪培養(shaker incubator)→以酒精萃取 →過濾→HPLC 分析
B. DNA sequence 選定→植入 Escherichia coli 中製成 plasmid →選取特定形質的 Escherichia coli→誘發培 養 Escherichia coli 產生蛋白→以高壓破碎 菌體→以染料染色→蛋白純化→蛋白特性 檢驗→移交生產部門 在涉及大型醱酵的生技製藥廠的生產製造 流程如下: 中間工廠發酵槽(50L)培養成功的菌種引 入 大 型 發 酵 槽 + 培 養 原 料 → 中 型 發 酵槽 (500L)→大型發酵槽(5000L)→酸化處 理(使產物穩定及殺滅菌株,pH2.5)→沉 澱→萃取→濃縮→包裝 由於大型醱酵生產的製程已採用自動化控 制,在生產製程中的操作人員僅有數人,倘若 所使用的微生物有健康危害顧慮,則在正常的 生產醱酵過程下,主要的微生物暴露可能發生 在生產過程中為執行品管控制的醱酵物取樣步 驟。因為大型醱酵槽的設計和控制措施大體上 已相當成熟,且生產醱酵製程中所使用的原物 料,並未含有高揮發的易燃物質,因此在異常 操作狀況下,造成大型醱酵槽培養的菌體外洩 逸散,發生大規模高數量的微生物暴露的機會 不大。 實驗室操作過程中,小型菌種增殖培養和 菌種篩選步驟,為微生物暴露可能發生的操
作。對於操作微生物所需注意的安全衛生知識 及防護設備,大體上這些工廠均具備無菌操作 的通風櫥,其通常設計為內循環、正壓型態、 含紫外線燈的生物安全操作櫃(biological safety cabinet)。另外,高壓蒸氣滅菌鍋被用來做為處 理需丟棄的培養皿和用具的設備。使用超音波 細胞打碎機的實驗室,大體上為小型操作,不 過操作過程並未在安全氣櫃或通風櫥中進行, 可能有產生氣膠(或氣霧)的可能,在日後人 員暴露的評估測定研究中,應列為優先考慮對 象。 (6) 檢驗試劑 此類產業使用微生物本體或植入某一段基 因片段的載體微生物,經培養產生特定的蛋白 或反轉錄反酸,然後將此蛋白或反轉錄反酸錄 抹於 nitrocellulose 所製 成的 薄膜 或生 物晶片 上,而製成檢驗試紙或晶片,作為醫療檢驗上 快速檢定有無特定微生物感染的工具。 基 本 上 這 類 產 業 的 生 產 廠 房 乾 淨 、 低噪 音,且精細操作,令人有高科技產業的印象。 雖然不是所有廠商有自已的生產廠房,但只要 已設有廠房者,其廠房本身通常有研發實驗室 從事微生物菌株的培養選定和檢驗試劑的萃取 製造,及生產部門進行試劑的錄抹或填充、切 割、組合和包裝。研發實驗室的設備主要包括 微生物培養所需的基本玻璃器具、離心機、培 養箱、振盪機、冷凍冰箱及生物安全操作裝 置。生產部門的設備則包括特殊的精密機械和 包裝機器。整個研發生產製程中,微生物菌體 暴露主要發生在實驗室的研發人員,而微生物 衍生物的暴露則實驗室和生產裝配的人員均有 可能。本研究所調查訪視的工廠,現今有使用 致病微生物菌體者,仍屬於實驗室試驗研發階 段,其中絕大多數使用致病微生物的某一段 DNA 片段植入載體微生物如 Escherichia coli, 以產生所要的產物。受訪的研發人員表示對於 根據國家科學委員會「基因重組實驗守則」的 規定,對於操作實驗這類型基因改造的載體微 生物,目前不必向研究機構實驗安全委員會及 行政院國家科學委員會報備或申請反准。若從 安全衛生的觀點而言,由於各實驗室的安全衛 生防護和管理差異頗大,在對基因改造微生物 對人體健康危害仍未有清楚的了解且無實際的 暴露評估測定前,實在難以斷言這些實驗操作 的安全衛生問題的狀況。 對於實驗室所產生含有微生物的培養皿和 培養液或其他實驗過程所用的針頭、吸管、手 套等的處理,在訪視中所得知的現行處理方式 為自行以高壓蒸氣滅菌鍋處理後交由垃圾清運 公司處理,或未經高壓蒸氣滅菌鍋處理,直接 裝 入 標 示 為 生 物 性 危 害 物 ( biohazardous materials)的橘紅色塑膠袋中,然後交予感染性 事業廢棄物代處理業處理。 (7) 人體及動物疫苗 此類產業以注入病原微生物進動物體內, 待動物體產生所需的抗體、免疫血清或抗毒素 後,然後從這些動物體內抽取這些物質經純化 或滅毒處理,而製成疫苗。人體疫苗製造在國 內並非新興和普遍存在的產業,在本研究中所 訪視疫苗製造公司已存在有相當時日,現在主 要製造的疫苗為日本腦炎疫苗和破傷風類毒素 疫苗,從製造的疫苗知道其製程中所使用操作 的微生物為日本腦炎病毒(Japanese encephalitis virus)和破傷菌(Clostridium tetani),二者分屬 於生物安全等級第三級和第二級的病原微生 物,在製程中所使用的安全防護設備為物理性 防護等級 P2 級,為裝有高性能微塵去除裝置 (HEPA 過濾器)的生物安全操作櫃,其 HEPA 過濾器需定期更換,並於維修或搬動時以甲醛 燻蒸整個裝置。每天實驗室內使用的材料在丟 棄前先經過滅菌處理,實驗及生產製造用的動 物屍體以焚化爐焚燒處理。人員進入實驗及生 產區域均洗手並換穿消毒滅菌過的工作服,於 工作完成時工作服放置於指定區域內,防護用 手套及口罩丟棄於指定的桶內,以利滅菌及銷 毀。以下是日本腦炎疫苗和破傷風類毒素的製 造流程: A. 日本腦炎病毒→注入天竺鼠腦部→動物病 情發作→動物犧牲抽取腦組織→純化抗原 →製成針劑 B. 特殊培養基滅菌→加入破傷風菌→10L 液 體發酵筒(少量空氣流通)→毒素產生→ 離心或過濾→沉澱→精製毒素→甲醛處理 以安定和減毒→透析去除甲醛→調配濃度 製成疫苗
在此製造流程中,最可能造成人員暴露於 日本腦炎病毒的步驟為抽取動物腦組織,此工 廠已透過必要的防護措施和良好的管理以減低 暴露的發生,而處理動物腦組織的過程造成工 作檯面病毒污染的情況,有待環境測定進一步 評估。 (8) 保健或健康食品 此類產業主要利用微生物產生酵素或萃取 其特定化學成分,這些酵素或特定化學成分基 本上被認為有提昇免疫力、排除體內毒素和促 進抗癌作用的功效。屬於這一類的微生物包 括:酵母菌、乳酸菌、紅趜菌、真菌類(如靈 芝 、 冬 蟲 夏 草 、 姬 松 茸 、 樟 芝 、 猴 頭 菇 ( Hericium erinaceus )、 舞 菇 ( Grifola frondosa)等,如表 8 所列。由於此類產業隨其 所培養的菌體不同(可能為菌體本身、真菌類 的菌絲體或子實體),其生產製造過程可能有極 大的差異。大體上為由小型至大型醱酵逐步放 大,然後萃取或分離酵素和萃取特定成份,製 成液體,然後經冷凍或自然乾燥,磨成粉末或 製成膠囊,以做為保健或健康食品。另一種製 程則比較接近農業經營,也就是說沒有醱酵和 萃取成份的問題,而是直接栽培真菌的子實體 為料理食用或經乾燥作為沖劑飲用。以下是本 研究所訪視廠商的生產流程: 生產流程: A. 振盪培養(shaker incubator)→選取菌株→ 小型發酵→中間工廠醱酵槽(50L)培養成 功的菌種(或菌絲體)引入大型醱酵槽+ 培養原料→中型發酵槽(500L)→大型醱 酵槽(5000L)→沉澱→過濾→萃取→冷凍 濃縮乾燥→包裝 B. 真菌孢子→洋菜膠培養皿或培養液培養→ 太空包栽種量產 由於這些微生物均被列為食用級微生物, 因此在生產製造過程中並未考慮任何作業員工 暴露於這些微生物的健康危害,反倒擔心作業 員工或空氣所帶入的雜菌污染生產製程和產 品。對於此產業的作業員工的有害物質暴露, 除微生物和真菌所產生的大量孢子散布於空氣 中,引發短暫性的呼吸道黏膜刺激需注意外, 慢性效應仍難以評估。另外,若製程中涉及成 分萃取,則作業員工的有機溶劑暴露可能是需 要注意的職業暴露問題。
討 論
歐 洲 生 物 科 技 聯 邦 生 物 科 技 安 全 工 作組 (The Safety in Biotechnology Working Party of the European Federation of Biotechnology)針對 生物科技產業所使用微生物可能引發的安全及 衛生問題探討的文獻[15-21];在美國的生物科 技產業的職業安全衛生初步調查[22],從業員工 中 有 36.2% 參 與 和 生 物 安 全 等 級 ( biosafety level)第一、二和三級的微生物操作有關的工 作,68%的工作人員暴露於不具生物危害的微生 物,商業生產的生物科技公司的相關作業 80% 暴露於需生物安全等級第一級或不需考慮生物 安全等級的微生物。在英國的生物科技產業對 製程的微生物監測的問卷調查資料顯示:完成 問卷的公司中有 73% 使用基因改造微生物,而 其中 50% 的公司針對工作環境實施定期的監 測,而監測所採用的採樣設備並不一致[11]。本 研究發現國內微生物產業使用生物安全等級第 二級以上的百分比低於國外的狀況,但可預期 的在未來國內對生物科技產業增加時,這個百 分比會增加。在此研究中原先構想估計員工暴 露狀況,惟受限於低調查回收率,而難以執行 這樣的評估。 從現場訪視調查中發現,微生物產業的菌 種提供來源主要從食品工業發展研究所、財團 法人生物技術開發中心、外國進口及自行由國 外帶入。而依產業性質的差異,來源各不相 同。其中新興的生物科技產業的菌種來源主要 從食品工業發展研究所及財團法人生物技術開 發中心。至於生物肥料、動物飼料、農業生物 製劑和保健或健康食品有相當多廠商從國外進 口,及少數由國外自行攜帶微生物入境,這些 菌種均仍未有健康危害的評估報告或文獻報 導。因此要掌握作業員工可能的生物暴露,未 來應要求各事業單位建立所使用的微生物菌種 的生物安全資料庫,勞工安全衛生檢查單位應 考慮如何將微生物菌種所引發的生物性危害納 入檢查項目及管理,國外對生物科技產業的安全危害分析方法或許可提供一些參考[23, 24]。 除了對菌種來源與使用狀況進行檢查及管 理外,在基因改造微生物上,近年來 DNA 在細 胞外穩定度和在不同細菌間轉移的研究顯示, 以質體(plasmid)形式存在的 DNA 可能在土壤 和有水的環境中有相當的穩定性,不被其他微 生物的 DNA 分解脢所分解[25, 26],因此關於微 生物產業廢棄物的處理問題,尤其是製程中使 用基因改造微生物的含微生物的事業廢棄物, 已開始受到重視和注意[21]。一般認為由生產製 程中所產生的含基因改造微生物的廢棄物被視 為安全無生物危害,但若基因改造加強微生物 在生產製程外存活,或在特定地建構或條件中 有改變較高等的細胞的機率,如基因疫苗或基 因藥丸等,則這些廢棄物必須以適當的方法處 理,以保證基因不具活性。本研究證實國內生 物科技產業確有基因改造微生物的使用,但目 前尚未使用於疫苗的製造。雖然目前生物科技 產業研發實驗室所操作的菌種安全性較無問 題,但微生物暴露防護及管理狀況難免有所疏 失。另外,隨著技術水準的提昇,可預期未來 可能會使用較危險的菌株,為防患未然,有必 要隨時保持適當的登錄和監測。 為了解生物科技產業在研發實驗室操作或 生產製程中,有無微生物的逸散到工作檯面和 作業環境而造成人員的暴露,或評估現有暴露 控制措施和管理狀況足以保護工作人員免於此 類微生物的暴露,有必要實施環境監測。其中 環 境 採 樣 可 考 慮 實 施 表 面 採 樣 法 ( surface sampling method),以沉降試驗收集懸浮在空氣 中的微生物,或以動力捕集方式收集微生物。 再配合適當的分析方法量化微生物暴露狀況, 包括:微生物種類、濃度等,而後可針對其可 能導致的不良健康效應如:感染、過敏、中毒 等予以適當的評估。
結論與建議
就產業特性而言,在病原菌感染風險上, 未來應重視監測的產業為疫苗製造和檢驗試劑 製造,這二類產業所使用的微生物含有致病菌 或嵌有致病菌(或病毒)特定基因片段的基因 改造微生物。雖然產業界和研究實驗室的安全 防護設施和裝置大體上合乎標準,但管理上可 能的疏漏或鬆散及作業員工的配合程度不一的 情形下,仍可能造成作業環境中微生物的散 布。因此,未來如有可能應考慮對這二類產業 執行作業環境微生物暴露評估計劃與安全防護 措施與裝置的效能評估,以確定作業員工無健 康危害風險。其中生物安全操作櫃的分級制度 在國外已行之有年,而國內無論是產業界和學 術單位研究實驗室仍未能落實,建議未來應逐 步建立分級管理制度。 關於微生物可能導致的過敏或中毒等健康 問題,則應著重於使用醱酵製程的產業。從本 研究的問卷調查和現場訪視調查結果顯示,食 品醱酵如醬油、食醋方面所使用的微生物麴菌 被認為沒有感染的危害,其中採用手工製造的 小廠已淘汰到少數且少量經營,而大型工廠則 已完全自動化生產。對這些產業作業員工,微 生物的暴露主要在完成培麴豆類和其他原料混 合操作上。其他醱酵作業如生產菌體肥料、動 物飼料添加物、農業或環保生物製劑等,作業 員工亦有可能因固體醱酵作業在攪拌、分裝等 作業過程中暴露微生物或其產物。這些產業使 用的微生物多屬真菌類、未來需配合菌種快速 鑑定技術的建立予採樣技術的開發,針對涉及 醱酵製程者如:傳統食品釀造、菌體肥料、動 物飼料添加物、農業或環保生物製劑、生技製 藥和保健及健康食品等,進一步評估作業環境 中非致病性(non-pathogenic)微生物種類與濃 度。因為醱酵方式的差異可能影響逸散微生物 的分佈和特性,未來在對這些產業實施暴露測 定時,也應對這些因子予以描述,以評估用於 醱酵製程的微生物是否有引發作業員工過敏反 應的健康風險。 本研究發現工業安全衛生人員有關微生物 的知識和現有生物科技產業的研發實驗人員比 較,仍嫌不足,至於微生物安全衛生操作上的 認知及訓練,則各有其欠缺,例如工業安全衛 生人員對於微生物和微生物基因片段的致病能 力,可能沒有完整的知識,而產業界研發人員 則對於在操作過程中微生物和微生物基因片段 氣膠化或逸散的可能較無概念,在以後的研究 中,應尋求這二方面專業人員的合作,以互補 彼此的不足。工業衛生的教育有必要加強微生物安全衛生操作上的訓練及測定,以因應未來 產業的需要。政府各相關部會可能擬定的管制 措施,如:經濟部工業之在反可微生物和生技工 廠設立時,應知會環保署、衛生署、農委會和 勞委會,由這些部會提出對生產製程、原料、 產物和廢棄物所可能導致的生物危害提示意 見,建議所需的控制措施、設備和操作人員訓 練等,以確保該工廠的設立不會發生生物危 害。各部會內部則需有專門人員開始收集相關 生物危害資料外,環保署可能針對基因改造微 生物在環境中散布的影響進行評估。衛生署可 能需研擬因接觸生產製程微生物而感染疾病的 病例通報系統及治療方法,以其快速掌握狀況 避免爆發流行。農委會則需在管制外來微生物 菌種的輸入上,採取更周全的管理措施,並監 控基因改造菌種對植物、動物及生態的影響。 勞委會則需對有生物危害之虞的生產製程,規 範期環境監測項目和頻率,建立防護措施規 格,人員操作規範,並開發標準檢測方法等。 如此透過各部會的協調、管理和行政整合,必 能有效預防生物危害的發生。 本研究受限於低問卷回收率,對真實情況 的代表性可能有相當的差距及低估嚴重程度, 加以國內微生物產業的機動變化性相當高(新 興生物科技產業在微生物使用與產品開發上日 新月異,傳統醱酵產業則不斷調整規模和產 量),因此在某種程度上限制了本研究調查數據 未來的應用性。然透過大量的現場訪視,本研 究已經對此產業的生物危害特性提供相當的釐 清,可作為未來各相關產業預防生物危害的重 要參考依據。唯一美中不足之處,為在本研究 中未能現場訪視動物疫苗製造產業,考量動物 疫苗使用病原性微生物的風險,建議未來的研 究可將其列為重要的調查訪視對象。
誌 謝
本研究由行政院勞工委員會勞工安全衛生 研究所九十年度研究計畫(IOSH90-H303)經費 贊助下完成,並承蒙國光生物科技公司林文理 博士在訪視問卷設計上的協助;所有參與本計 畫現場訪視廠商的配合,誌上謝忱。對本計畫 審查委員台灣大學公共衛生學院環境衛生研究 所林嘉明教授、台灣大學農業化學系潘子明教 授和明生生物科技公司田蔚城董事長對本研究 報告上所給予的指導與建議,對本計畫的執行 方向、資料整理和問題闡述上,均提供本研究 成員思考與檢討的機會,特此致謝。參考文獻
[1] 田蔚城主編:生物產業與製藥產業(上下 冊)。一版,台灣省台北市, 九州圖書文物 有限公司;1998 和 1999。 [2] 蘇遠志:我國生物科技產業的發展策略與 措施。生物技術產業推展研討會論文集, 中國農業化學會;1998。 [3] 陳啟祥:產業界應有之認知與推展方向。 生物技術產業推展研討會論文集,中國農 業化學會;1998。[4] Duffus JH, Brown CM. Health aspects of biotechnology. Ann Occup Hyg 1985; 29(1):1-12.
[5] Martinez KF, et al. General considerations for work practices and personal protective equipment in biotechnology industries. In Hyer W.C., Jr., (ed.) Bioprocessing safety: worker and community safety and health considerations, American Society for Testing and Materials, Philadelphia, Pennsylvania, ASTM STP 1051; 1990:83-90.
[6] Biagnini RE. Hypersensitivity reactions and specific antibodies in workers exposed to industrial enzymes at a biotechnology plant. J App Toxicol 1996; 16(2):139-45.
[7] Topping MD, Scarisbrick DA, Luczynska CM, Clarke EC, Seaton A. Clinical and immunological reactions to Aspergillus niger among workers at a biotechnology plant. Brit J Ind Medicine 1985; 42:312-8.
[8] Seaton A, Wales D. Clinical reactions to Aspergillus niger in a biotechnology plant: an eight year follow up. Occup Environ Medicine 1994; 51:54-6.
[9] Andrup L, Nielsen BH, Kolvraa S. Biosafety considerations in industries with production methods based on the use of recombinant
deoxyribonucleic acid. Scand J Work Environ Health 1990; 16:85-95.
[10] 蔡逸君主編:Taiwan 生技產業名錄總覽。 台灣省台北市,生技時代股份有限公司; 2002。
[11] Crook B, Cottam AN. The current status of monitoring for process micro-organisms in biotechnology: results of an industry questionnaire. Ann Occup Hyg 1996; 40(2):223-32.
[12] 行政院國家科學委員會:基因重組實驗守
則;2000。
[13] National Center for Infectious Diseases Division of Vector-borne Infectious Diseases, Centers for Disease Control and Prevention. Biosafety Manual. Mulberry & Overland Trial/Foothills Campus, Fort Collins; 1994. [14] Frommer W, Archer L, Boon B, Brunius G,
Collins CH, Crooy P, et al. Safe Biotechnology 5: Recommendations for safe work with animal and human cell cultures concerning potential human pathogens. Applied Microbiology and Biotechnology 1993; 39:141-7.
[15] Lelieveld HL, Bachmayer H, Boon B, Brunius G, Burki K, Chmiel A, et al. Safe biotechnology. Part 6. Safety assessment, in respect of human health, of microorganisms used in biotechnology. Working Party “Safety in Biotechnology” of the European Federation Biotechnology. Applied Microbiology and Biotechnology, 1995; 43(3):389-93.
[16] Lelieveld HL, Boon B, Bennett A, Brunius G, Cantley M, Chmiel A, et al. Safe biotechnology. 7. Classification of microorganisms on the basis of hazard. Working Party “Safety in Biotechnology” of the European Federation Biotechnology. Applied Microbiology and Biotechnology 1996; 45(6):723-9.
[17] Lelieveld HL, Bachmayer H, Boon B, Bennett A, Brunius G, Burki K, et al. Safe biotechnology. 8. Transport of infectious and biological materials. Working Party Safety in
Biotechnology of the European Federation of Biotechnology. Applied Microbiology and Biotechnology 1997; 48(2):135-140.
[18] Doblhoff-Dier O, Bachmayer H, Bennett A, Brunius G, Burki K, Cantley M, et al. Safe biotechnology 9: Values in risk assessment for the environmental application of microorganisms. Working Party Safety in Biotechnology of the European Federation of Biotechnology. Trends in Biotechnology 1999; 17(8):307-311.
[19] Working Party Safety in Biotechnology of the European Federation Biotechnology. Safe biotechnology 9: Values in risk assessment for the environmental application of microorganisms. Trends in Biotechnology 1999; 17(4):307-10.
[20] Working Party Safety in Biotechnology of the European Federation Biotechnology. Safe biotechnology 10: DNA content of biotechnological process waste. Trends in Biotechnology 2000; 18(4):141-6.
[21] Lee SB, Ryan LJ Jr. Occupational health and safety in the biotechnology industry--a survey of practicing professionals. Am Ind Hyg Assoc J 1996; 7(4):381-6.
[22] Jank B, Haymerle H, Doblhoff-Dier O. Zurich hazard analysis in biotechnology. Nature Biotechnology 1996; 14:894-6.
[23] Pettauer O, Kappeli O, van den Eede G. Safety analysis of contained low-hazard biotechnology applications. Appl Microbiol Biotechnol 1998; 49:649-54.
[24] Romanowski G, Lorenz MG, Wackernagel W. Adsorption of plasmid DNA to mineral surfaces and protection against DNAase I. Appl Environ Microbiol 1991; 57(4):1057-61.
[25] Sikorski J, Graupner S, Lorenz MG, Wackernagel W. Natural genetic transformation of Pseudomonas stutzeri in a non-sterile soil. Microbiology 1998; 144: 569-76.
Jyun-De Wu
1, Ching-Wen Chang
2, Thomas J.H. Chen
1,
Tai-Shan Yu
2, Chi-Byi Horng
11 Department of Occupational Safety and Health, Chang Jung Christian University 2 Institute of Occupational Safety and Health, Council of Labor Affairs, Executive Yuan
Abstract
Because of the rapid development of modern biotechnology, the industry involving the application of microorganisms and bioprocesses to the manufacturing processes or the modification of microorganisms and the usage of these modified microorganisms in making products has grown tremendously. This type of industry is generally called “microbial industry”. Since some specific microorganisms have been confirmed or suspected to be associated with some adverse health effects, it is necessary to focus on the issues of biohazards relevant to workers’ exposure to microorganisms from the handling and manipulation of microorganisms. In this study, we searched for the literatures of adverse effects induced by exposure to microorganisms in microbial industry and the basic information of manufacturers of microbial products. We designed questionnaires to collect the information of process-used microorganisms and microorganism-containing products and the routes and frequency of exposure to microorganisms in these manufacturing processes. We also conducted telephone interviews and field investigations to gather more detailed information. Thirty manufactures were chosen for field investigations. From the results of this study, we found that in general microbial industry might be classified into traditional food fermentation and recently-developed biotechnology. According to the characteristics of product-applied subjects, the recently-developed biotechnology can be classified into seven categories: microorganism-containing fertilizers, animal feed additives, environmental or agricultural biological agents, biotechnical medicines, diagnostic test kits, human and animal vaccines, and healthy food products. The traditional food fermentation used the microorganisms which are not hazardous to human beings and not genetically modified. The recently-developed biotechnology industry used genetically modified microorganisms in the manufacturing processes, but not in the vaccine preparation. Monitoring workers’ exposures to microorganisms in microbial industry especially for vaccine preparation and diagnostic kit production should be conducted in further studies. In addition, for the manufacturing processes with fermentation, the characterization of the species and concentration of non-pathogenic microorganisms is necessary to assess the risk of allergy among workers.
Keywords: Biohazard, Microbial industry, Biotechnology industry, Genetically modified microorganism, Field investigation
Accepted 12 August 2003
* Correspondence to: Jyun-De Wu, Department of Occupational Safety and Health, Chang Jung Christian University, Tainan, Taiwan, 396 Chang Jung Rd., Sec. 1, Kway Jen, Tainan 711, Taiwan, R.O.C.