國立臺灣大學生物資源暨農學院農業化學系 碩士論文
Department of Agricultural Chemistry College of Bioresources and Agriculture
National Taiwan University Master Thesis
土壤中鐵錳結核對鉻的氧化還原反應之影響 The Effects of Fe-Mn Nodules in Soil on Oxidation and Reduction of Chromium
徐仲禹 Chung-Yu Hsu
指導教授:李達源 博士 Advisor: Dr. Dar-Yuan Lee
中華民國九十八年六月
June, 2009
誌 謝
能夠順利地完成一份研究,不可能只靠自己的力量,必然是受到了許許多多人的幫 助以及鼓勵。而如今得以完成我的論文,我由衷地感謝曾經幫助過、鼓勵過我的每一個 人,或是事、物。若有遺漏,請原諒我的愚笨與疏失。
首先要感謝的,莫屬我的指導教授 李達源博士,老師從不對學生嚴厲要求,而讓 學生學習獨立自主以及自我要求的態度,不管是課業、實驗,或是待人處事方面,都給 了學生最佳的身教典範。老師讓學生在學的兩年獲益良多,並進入一個有家庭般溫暖的 團隊,學生因此得以認識這裡的每一個好夥伴。也感謝老師您的處處包容,讓學生在學 時亦能兼顧親情、友情與愛情。如果要以一句話來形容這兩年與老師相處的情形,學生 會說:「身為老師的學生是一件很幸福的事情」。對您的感謝實在難以用短短的文字表 達,由衷感謝您的關心、照顧與拉拔!
此外,要感謝我的恩師 施養信博士,感謝您在學生大學時期對學生的細心培養,
讓學生對研究產生興趣,也幸運地增加很多美好的經歷,您對研究的熱誠與積極的態 度,都是學生努力的目標。也感謝您讓學生有機會到不同的實驗室增加不同的經驗,雖 不敢說專精,但至少接觸到各式各樣研究領域的大門,謝謝您對學生的栽培!
感謝國立中興大學土壤環境科學系鄒裕民教授,以及國立屏東科技大學環境工程與 科學系許正一教授,於百忙中擔任學生的口試委員,並細心替學生校閱論文,學生沒齒 難忘,有您們幫學生的論文把關,真是學生最大的福氣!感謝國立台灣大學農業化學系 陳尊賢教授與何聖賓教授擔任學生的口試委員,感謝陳老師如此細心地找出學生沒有發 現的錯誤,要是沒有您的細心閱讀,學生真不知該如何自信滿滿地交出論文,此外還有 在觀念上的釐清等,都讓學生茅塞頓開,而在課程中也得到許多寶貴的知識,學生真的 很喜歡老師資源共享的概念,還有努力培養國際觀,成為一個優秀的領導人才這樣大氣 的思想!感謝何老師對於學生論文中拙見的修正,以及許多觀念的導正,讓學生體驗到 學海無涯,尚有許多需要學習的地方!而在課程上學生也學到很多細微的概念,雖然目 前尚無法學以致用,但謝謝您讓學生得到通往這些研究的金鑰。此外還要感謝老師教導 學生如何使用許多儀器,如AA、ICP-OES 等研究的好夥伴,讓學生在研究的路上能夠 運用他們來成就實驗的完整。您學識之淵博是學生所望塵莫及的,感謝您帶給學生的種 種美好!另外要感謝鍾仁賜老師、王一雄老師、顏瑞泓老師等在課業上給予學生許多啟 發,撰寫論文時亦能同時運用課程中學習到的概念,在此感謝您們的教導與鼓勵。
感謝實驗室裡最善解人意、溫柔大方的紫慧學姐,你總是辛苦地幫助解決我們在研 究與生活上種種的困難,還有對我們的關心、鼓勵以及愛護,讓我們喜歡這個有你的團 體。實驗、論文雖不能說完美,但因為有你的加持,一切都非常順利、成功。謝謝你對 我的教導與包容,也很抱歉這段時間讓你操心了!因為有學姐,讓我在研究所的日子裡 體驗了許許多多未接觸過的新奇事物,請讓我抱著你說愛你吧!此外還要感謝我心中完 美的典範,佳容學姐,雖然相處才一年,但你讓我看到了人性的美好,還有說不完的(冷) 笑話!謝謝學姐總是叫我不要哭,也讓我跟嘿娜之間感情比姊妹還要好,學姐的功勞絕 對是最大的!還有一切都很完美的瑤瓊學姐,你的一切都是我所遵循的模範,不管是課
業、實驗方面的成就還有溫文儒雅的氣質,都讓我相當崇拜,謝謝你對我的好!此外還 要感謝實驗室裡把嘿娜帶給我的愷瑋學長、什麼都會的天麟學長、有著天籟般嗓音的秋 萍學姐、懂的東西多到數不清的雯婷學姐,以及健智學長、婉菁學姐等,還有最可愛的 學妹們小茜和淳淳,謝謝可愛的你們幫了我許多的忙,學姐不才,沒能給你們什麼,請 多包涵!I also would like to express my sincere gratitude to Prof. Dean Hesterberg in Depart.
of Soil Science of North Carolina University and Clint Miller from Texas A&M University.
You both helped me a lot, and made me have nice experiences of getting along with foreigners.
還要感謝前實驗室成員,侑宗、士閔、宗勳、博信、淳剛等學長,以及美雪、孟宜、
希瓴等學姐,還有柏均學長、乃樺學姐、文菁學姐在這兩年間仍不忘給我鼓勵與關心,
並在各方面都給予我相當多的幫助,讓我覺得很溫馨,謝謝你們!
而在這裡與我共生死共患難、如膠似漆的好夥伴,嘿娜(懿芳),絕對是我完成論文 的功臣之一。謝謝你總是和我一起修課,一起做實驗,一起去很多地方,一起拍照,一 起開心,一起難過,一起歡笑,一起耍笨,一起發瘋…。現在想起來,每一件事情都是 這麼美好,這麼讓我捨不得與你分離,也謝謝你對我的包容、關心和照顧,像你這麼貼 心的女孩,要拿多少燈籠才找得到?!有太多話想講,但是手要拿來擦眼淚而無法打字 了。謝謝你,在我的生命裡留下了這麼美麗的詩句。還要謝謝來到這之後成為我和嘿娜 的好姊妹的孟妤,你的善良與體貼讓我覺得自己真是幸運又幸福的人!也謝謝一直以來 都很照顧我的瓊文,雖然你遠在台中,卻還是時常能感受到你對我的關心,真的很高興 你一直都是我的好姊妹。還要謝謝陪我一路走來的興光幫成員們:總是能讓大家感染到 快樂氣息的珮真、總是幫我解救電腦方面問題的英雄-俊廷、總是給我許多好意見也是 我生命中的小老師-泊原、讓我媽咪印象深刻的好孩子-偉勝、其實很關心同學朋友的致 甫,以及永遠都樂觀開朗的品潔,謝謝你們總是熱情參與同學間的活動,並且互相鼓勵 與支持,讓我在這裡的日子真的很快樂。另外也要謝謝來到這裡認識的同學們,柱中、
依潔和筠婷,以及摯友慧婷和婉娸,有你們的加油和打氣,事情都會變得非常順利!
此外,還要感謝我生命中不可或缺的寶貝-立傑,謝謝你一直以來對我的支持、鼓 勵、關心、幫助、容忍以及稱讚,你對我來說是最重要的寶藏,也是最甜蜜的巧克力,
有你在我身邊真的讓我非常幸福!也謝謝鄭爸爸與鄭媽媽,把我當自己的孩子般疼愛,
讓我學習到很多學校沒有教的事。還有當我感到疲憊時的精神糧食與支柱們:牡蠣、喵 哩、橘子、葡萄,以及姊姊的小米、Miko 和點點,如果沒有你們相伴,我的壓力將無 從釋放,你們真是我生命中的天使。
最後要感謝一直支持我唸書的爸爸徐瑞生先生和媽媽王麗華女士,有您們辛勤的栽 培與照顧,我才能在無後顧之憂的狀況下完成學業,謝謝您們給女兒的一切!還要謝謝 我親愛的姊妹,家禹和幼禹,謝謝你們在生活、實驗、論文幫我這麼多,尤其是姊姊幫 我修改我的論文,讓文章看起來更加地學術,謝謝你們!有你們這兩個貼心又會照顧人 的姊妹,我真的很幸運!
摘 要
先前研究中已發現具鐵錳結核的土壤具有將Cr(III)氧化為 Cr(VI)之能力,本研 究欲探討於田間容水量下,鐵錳結核之含量與粒徑大小對其氧化Cr(III)能力之影 響。並利用土壤之易還原性錳含量預估鐵錳結核之氧化能力,並與純的二氧化錳 進行比較;另外亦探討鐵錳結核對有機資材復育Cr(VI)污染土壤之影響,觀察鐵 錳結核是否具將Cr(III)再氧化之能力。研究鐵錳結核含量對 Cr(III)氧化能力之影響 的實驗可發現隨鐵錳結核含量增加,總Cr(VI)含量明顯增加,產生 Cr(VI)之速率 亦較快,但與純二氧化錳的反應能力相較,土壤中鐵錳結核僅產生純二氧化錳可 氧化產生量約30 % 的 Cr(VI),表示土壤中鐵錳結核之氧化能力較純二氧化錳差,
且易還原性錳量無法有效代表土壤中鐵錳結核之氧化能力。隨時間增加,鉻被鐵 鋁氧化物吸附,其有效性Cr(VI)含量僅佔總 Cr(VI)產生量之 15 %。研究鐵錳結核 粒徑對Cr(III)氧化能力之影響的實驗中,發現鐵錳結核粒徑較小者 (0.2 mm) 相較 之下容易與Cr(III)反應產生 Cr(VI),推測是因鐵錳結核粒徑不同,使其具有不同之 比表面積,較小的顆粒具有較大的比表面積,而可使Cr(III)與鐵錳結核均勻反應。
但鐵錳結核粒徑較大之土壤 (4 mm) 在反應過程中最高仍可將 500 mg-Cr(III) kg-1 氧化產生27.6 % 之 Cr(VI)。本研究亦觀察鐵錳結核對添加 3 % 有機質 (大豆粕) 還原Cr(VI)之影響,反應第 20 天,高鐵錳結核含量之土壤比低鐵錳結核含量之土 壤多測得8 % Cr(VI),推測是因鐵錳結核將經有機質還原 Cr(VI)產生之 Cr(III)再氧 化,而使該土壤可測得之Cr(VI)含量較中、低鐵錳結核含量土壤高。經觀察得知 土壤原有有機質在不同鐵錳結核含量之土壤中還原Cr(VI)之能力不顯著,推測是 因即使土壤中之Cr(VI)被還原,所產生之 Cr(III)也可能被鐵錳結核氧化。高鐵錳結 核含量之土壤中低有機質添加量 (1、2 %) 還原 Cr(VI)的實驗中可發現添加少量有 機質對Cr(VI)之還原作用並不顯著,推測是因鐵錳結核對 Cr(III)之氧化作用所致。
Abstract
The previous study had found that the soil with high content of Fe-Mn nodules can oxidize Cr(III) into Cr(VI). The effects of content and size of Fe-Mn nodules on its ability of oxidizing Cr(III) were investigated in this research. Besides, we predicted the oxidizing ability of Fe-Mn nodules based on its content of easily reducible manganese (Mnr), and compared with that of pure manganese dioxide. Furthermore, the effects of Fe-Mn nodules on Cr(VI) reduction by organic amendment added to
Cr(VI)-contaminated soil was also studied to observe whether Fe-Mn nodules could re-oxidize Cr(III) or not.
The results showed the total Cr(VI) content increased with the Fe-Mn nodules content during the oxidation of 500 mg-Cr(III) kg-1 by different contents of Fe-Mn nodules. Compared with pure MnO2, Fe-Mn nodules could only produce 30 % Cr(VI) of pure MnO2 could. And we also knew that Mnr could not evaluate the oxidizing ability of Fe-Mn nodules. Cr would be adsorbed by soil particles and the available Cr(VI) was only 15 % of total Cr(VI). The results also showed the total Cr(VI) content increased with the Fe-Mn nodules content during the oxidation of 500 mg-Cr(III) kg-1 by different sizes of Fe-Mn nodules, the soil with smaller Fe-Mn nodules (0.2 mm) could produce more Cr(VI) than the larger one (4 mm), because of the well mixed soil and Cr(III) solution and the larger specific surface area. The larger one could still produce 27.6 %
Cr(VI) of oxidizing 500 mg-Cr(III) kg-1 during the reaction.
To study the effects of Fe-Mn nodules on the reduction of Cr(VI) by organic matter, we added the soybean meal, which has confirmed its high ability to reduce Cr(VI), into the studied soils to raise 3 % organic matter and to reduce Cr(VI)-contaminated soil which has high content of Fe-Mn nodules. We found the total Cr(VI) was decreased with time and higher Cr(VI) was detected in the soil with higher content of Fe-Mn nodules. It was probably because of the re-oxidation of Cr(III) from Cr(VI) reduced by organic matter by Fe-Mn nodules. We also observed that the soil organic matter has low ability to reduce Cr(VI)-contaminated soil which has high content of Fe-Mn nodules. If we used less amount of organic matter, we could not reduce Cr(VI) obviously.
Keywords: Fe-Mn nodules, chromium, oxidation, Soybean Meal, reduction
目 錄
摘要 I Abstract II 目錄 IV 表次 VIII
圖次 IX
第一章 緒論 1
1.1 鉻於自然狀態下之性質 1
1.2 鉻於生活之利用與污染 5
1.3 鉻污染之整治 6
1.4 鉻氧化之研究 7
1.5 鉻還原之研究 11
1.6 鐵錳結核 15
1.7 全量六價鉻之測定方法 18
1.8 錳抽出法比較 20
1.9 研究目的 21
第二章 材料與方法 22
2.1 試驗土壤選定、採集及製備 22
2.1.1 試驗土壤選定 22
2.1.2 試驗土壤採集 22
2.1.3 試驗土壤製備 22
2.1.4 試驗鐵錳結核製備 23
2.2 試驗土壤基本性質分析 24
2.2.1 土壤 pH 值:玻璃電極法 24
2.2.2 土壤水分含量:重量法 24
2.2.3 土壤質地:比重計法 25
2.2.4 土壤有機質含量 26
2.2.4.1 燒灼失重法 26
2.2.4.2 濕式氧化法 26
2.2.5 土壤中總鐵、錳、鉻、鋁之含量:王水消化法 28
2.2.6 土壤中游離性鐵、錳、鋁氧化物之含量:DCB 法 29
2.2.7 土壤中無定型鐵、錳、鋁氧化物之含量:草酸銨法 31
2.2.8 土壤易還原性錳:錳電子消耗測定法 33
2.3 鐵錳結核對氧化 Cr(III)之影響 35
2.3.1 不同鐵錳結核含量對氧化 Cr(III)之影響 35
2.3.1.1 試驗土壤之製備 35
2.3.1.2 不同鐵錳結核含量對氧化 Cr(III)之影響之模擬田間實驗 35
2.3.1.3 土壤總 Cr(VI)含量之測定 36
2.3.1.3.1 土壤總 Cr(VI)之抽出 36
2.3.1.3.2 Cr(VI)濃度之測定 36
2.3.1.4 KCl 可抽出 Mn、Cr 含量之測定 37
2.3.1.5 KH2PO4可抽出Cr(VI)含量之測定 37
2.3.2 不同鐵錳結核粒徑對氧化 Cr(III)之影響 40
2.3.2.1 試驗土壤之製備 40
2.3.2.2 不同鐵錳結核粒徑對氧化 Cr(III)之影響之模擬田間實驗 40
2.4 鐵錳結核對有機質還原 Cr(VI)之影響 42
2.4.1 鐵錳結核對 3 % 有機質還原 Cr(VI)之影響 42
2.4.1.1 試驗土壤與有機資材之製備 42
2.4.1.1.1 試驗土壤之製備 (同 2.3.1.1) 42
2.4.1.1.2 有機資材之製備 42
2.4.1.2 鐵錳結核對 3 % 有機質還原 Cr(VI)之影響之模擬田間實驗 43
2.4.2 鐵錳結核對土壤原有有機質還原 Cr(VI)之影響 45
2.4.2.1 試驗土壤之製備 (同 2.3.1.1) 45
2.4.2.2 鐵錳結核對土壤原有有機質還原 Cr(VI)之影響之模擬田間 實驗 45
2.4.3 不同有機質含量對還原受 Cr(VI)污染之高鐵錳結核含量土壤之 影響 46
2.4.3.1 試驗土壤與有機資材之製備 46
2.4.3.1.1 試驗土壤之製備 (同 2.3.1.1) 46
2.4.3.1.2 有機資材之製備 (同 2.4.1.1.2) 46
2.4.3.2 觀察不同有機質含量對還原受 Cr(VI)污染之高鐵錳結核 含量土壤的影響之模擬田間實驗 (實驗期為 10 天) 46
2.4.3.3 觀察不同有機質含量對還原受 Cr(VI)污染之高鐵錳結核 含量土壤的影響之模擬田間實驗 (實驗期為 30 天) 46
2.4.3.4 觀察添加有機資材對土壤中錳還原的影響之模擬田間實驗 47
2.5 統計分析 48
第三章 結果與討論 49
3.1 試驗土壤基本性質 49
3.2 鐵錳結核對氧化 Cr(III)之影響 55
3.2.1 不同鐵錳結核含量對氧化 Cr(III)之影響 55
3.2.2 不同鐵錳結核粒徑對氧化 Cr(III)之影響 68
3.3 鐵錳結核對有機質還原 Cr(VI)之影響 78
3.3.1 鐵錳結核對 3 % 有機質還原 Cr(VI)之影響 78
3.3.2 鐵錳結核對土壤原有有機質還原 Cr(VI)之影響 85
3.3.3 不同有機質含量對還原受 Cr(VI)污染之高鐵錳結核含量土壤之
影響 88 第四章 結論 97 第五章 參考文獻 98
表 次
表一、本國環境保護署公告與鉻相關標準。 4 表二、本實驗所使用之有機資材,大豆粕的基本性質 (邱,2007)。 44 表三、去除鐵錳結核之土壤與鐵錳結核之基本性質。 52 表四、去除鐵錳結核之土壤與鐵錳結核以各種抽出法測定其鐵、錳、鉻、
鋁之含量。 53 表五、以去除鐵錳結核之土壤與鐵錳結核混合得到之試驗土壤 (18 meq kg-1
Mnr),以各種抽出法測定之鐵、錳、鉻、鋁含量與理論值之比較。 54 表六、不同鐵錳結核含量之土壤與500 mg-Cr(III) kg-1反應後,於各反應時
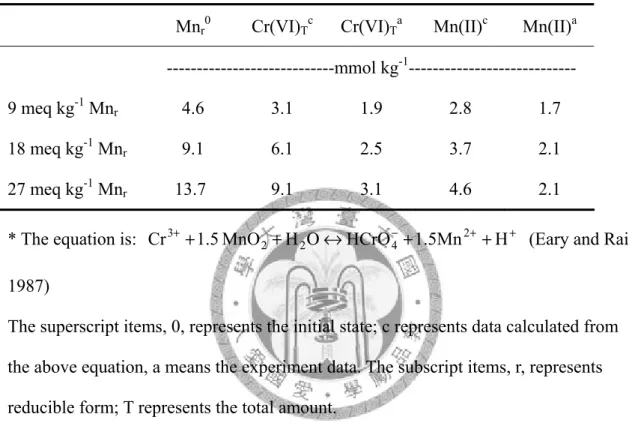
間點下,各土壤之總Cr(VI)產生量。 61 表七、不同鐵錳結核含量之土壤與500 mg-Cr(III) kg-1反應第20 天之總
Cr(VI)含量和可溶性錳,依據反應式計算之各項莫耳數比之比較。 62 表八、不同鐵錳結核粒徑之土壤與500 mg-Cr(III) kg-1反應後,於各反應時
間點下,各土壤之總Cr(VI)產生量。 72 表九、不同鐵錳結核粒徑之土壤與500 mg-Cr(III) kg-1反應第20 天之總
Cr(VI)含量和可溶性錳,依據反應式計算之各項莫耳數比之比較。 73
圖 次
圖一、鉻於水溶液系統中在不同pH 值與 Eh 值下物種之變化 (Palmer and Wittbrodt, 1991)。 3 圖二、具有鐵錳結瘤之土壤之顯微照片 (Manceau et al., 2003)。 17 圖三、鐵錳結核內部構造之掃描式電子顯微影像
(Gasparatos et al., 2005)。 17 圖四、Cr(VI)之鹼性消化法流程圖 (USEPA, 1996)。 19 圖五、由竹圍系土壤挑出之鐵錳結核;外圍紅色為鐵氧化物,中心黑色
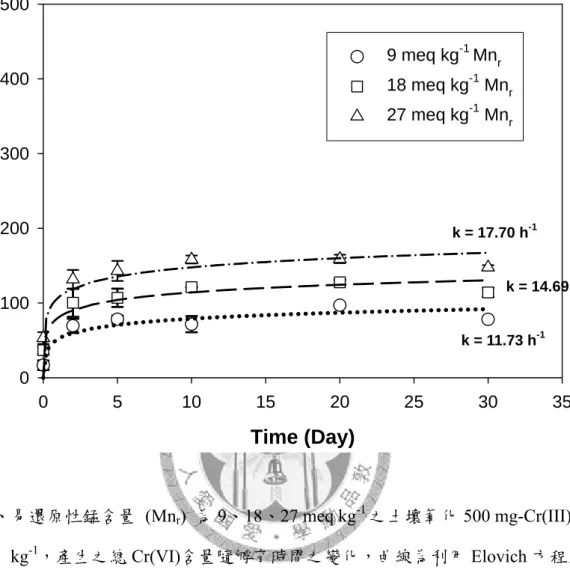
為錳核。 23 圖六、易還原性錳含量 (Mnr) 為 9、18、27 meq kg-1之土壤氧化500 mg-Cr(III)
kg-1,產生之總Cr(VI)含量隨孵育時間之變化,曲線為利用 Elovich
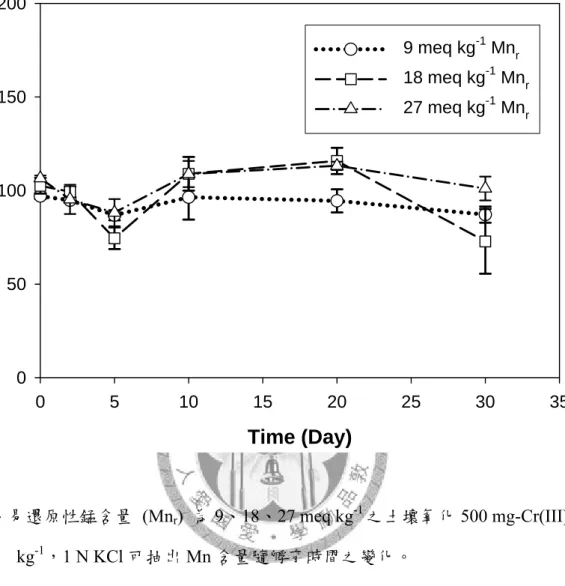
方程式進行套配之結果 63 圖七、易還原性錳含量 (Mnr) 為 9、18、27 meq kg-1之土壤氧化500 mg-Cr(III)
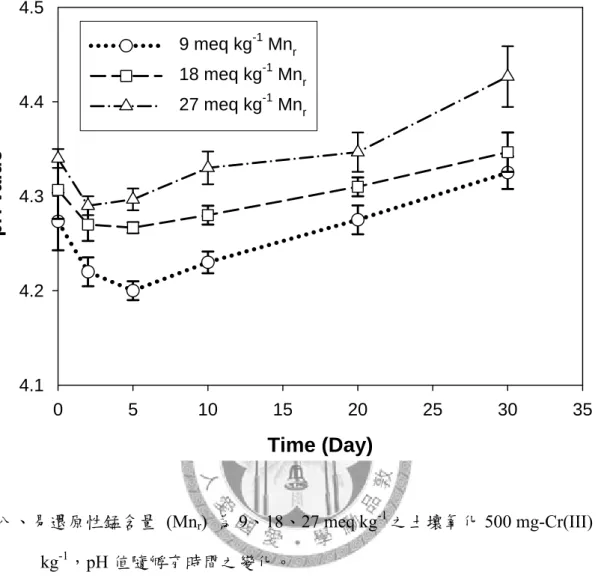
kg-1,1 N KCl 可抽出 Mn 含量隨孵育時間之變化。 64 圖八、易還原性錳含量 (Mnr) 為 9、18、27 meq kg-1之土壤氧化500 mg-Cr(III)
kg-1,pH 值隨孵育時間之變化。 65
圖九、易還原性錳含量 (Mnr) 為 9、18、27 meq kg-1之土壤氧化500 mg-Cr(III) kg-1,0.01 M KH2PO4可抽出Cr(VI)含量隨孵育時間之變化。 66 圖十、易還原性錳含量 (Mnr) 為 9、18、27 meq kg-1之土壤氧化500 mg-Cr(III)
kg-1,1 N KCl 可抽出 Cr 含量隨孵育時間之變化。 67 圖十一、鐵錳結核粒徑為0.2、4 mm 之土壤氧化 500 mg-Cr(III) kg-1,產生
之總Cr(VI)含量隨孵育時間之變化,曲線為利用 Elovich 方程式進 行套配之結果 74 圖十二、鐵錳結核粒徑為0.2、4 mm 之土壤氧化 500 mg-Cr(III) kg-1,1 N KCl
圖十三、鐵錳結核粒徑為0.2、4 mm 之土壤氧化 500 mg-Cr(III) kg-1,0.01 M KH2PO4可抽出Cr(VI)含量隨孵育時間之變化。 76 圖十四、鐵錳結核粒徑為0.2、4 mm 之土壤氧化 500 mg-Cr(III) kg-1,1 N KCl
可抽出Cr 含量隨孵育時間之變化。 77 圖十五、含500 mg-Cr(VI) kg-1且易還原性錳含量 (Mnr) 為 9、18、27 meq kg-1
之土壤被額外添加之3 % 有機質 (大豆粕) 還原期間,總 Cr(VI)含 量隨孵育時間之變化。 81 圖十六、含500 mg-Cr(VI) kg-1且易還原性錳含量 (Mnr) 為 9、18、27 meq kg-1
之土壤被額外添加之3 % 有機質 (大豆粕) 還原期間,0.01 M
KH2PO4可抽出Cr(VI)含量隨孵育時間之變化。 82 圖十七、含500 mg-Cr(VI) kg-1且易還原性錳含量 (Mnr) 為 9、18、27 meq kg-1
之土壤被額外添加之3 % 有機質 (大豆粕) 還原期間,1 N KCl 可 抽出Cr 含量隨孵育時間之變化。 83 圖十八、含500 mg-Cr(VI) kg-1且易還原性錳含量 (Mnr) 為 9、18、27 meq kg-1
之土壤被額外添加之3 % 有機質 (大豆粕) 還原期間,1 N KCl 可 抽出Mn 含量隨孵育時間之變化。 84 圖十九、含500 mg-Cr(VI) kg-1且易還原性錳含量 (Mnr) 為 9、18、27 meq kg-1
之土壤被土壤原有有機質還原期間,總Cr(VI)含量隨孵育時間之變 化。 86 圖二十、含500 mg-Cr(VI) kg-1且易還原性錳含量 (Mnr) 為 9、18、27 meq kg-1
之土壤被土壤原有有機質還原期間,0.01 M KH2PO4可抽出Cr(VI) 含量隨孵育時間之變化。 87 圖二十一、含500 mg-Cr(VI) kg-1且易還原性錳含量 (Mnr) 為 27 meq kg-1之
土壤被額外添加之1、2、4 % 有機質 (大豆粕) 還原期間,總
Cr(VI)含量隨孵育時間之變化。 90
圖二十二、易還原性錳含量 (Mnr) 為 27 meq kg-1之土壤被額外添加之1、2
% 有機質 (大豆粕) 還原期間,1 N KCl 可抽出 Mn 含量隨孵育 時間之變化。 91 圖二十三、含500 mg-Cr(VI) kg-1且易還原性錳含量 (Mnr) 為 27 meq kg-1之
土壤被額外添加之1、2、4 % 有機質 (大豆粕) 還原期間,1 N KCl 可抽出 Mn 含量隨孵育時間之變化。 92 圖二十四、含500 mg-Cr(VI) kg-1且易還原性錳含量 (Mnr) 為 18 meq kg-1之
土壤被額外添加之1.5 與 3 % 有機質 (大豆粕) 還原期間,總
Cr(VI)含量隨孵育時間之變化。 94 圖二十五、含500 mg-Cr(VI) kg-1且易還原性錳含量 (Mnr) 為 18 meq kg-1之
土壤被額外添加之1.5 與 3 % 有機質 (大豆粕) 還原期間,0.01 M KH2PO4可抽出Cr(VI)含量隨孵育時間之變化。 95 圖二十六、含500 mg-Cr(VI) kg-1且易還原性錳含量 (Mnr) 為 18 meq kg-1之
土壤被額外添加之1.5 與 3 % 有機質 (大豆粕) 還原期間,1 N KCl 可抽出 Mn 含量隨孵育時間之變化。 96
第一章 緒論
1.1 鉻於自然狀態下之性質
鉻 (chromium, Cr) 在自然環境中屬於常見過渡金屬元素之一。鉻在環境中有 兩種主要的氧化態,分別為三價鉻 (trivalent chromium, Cr(III)) 與六價鉻
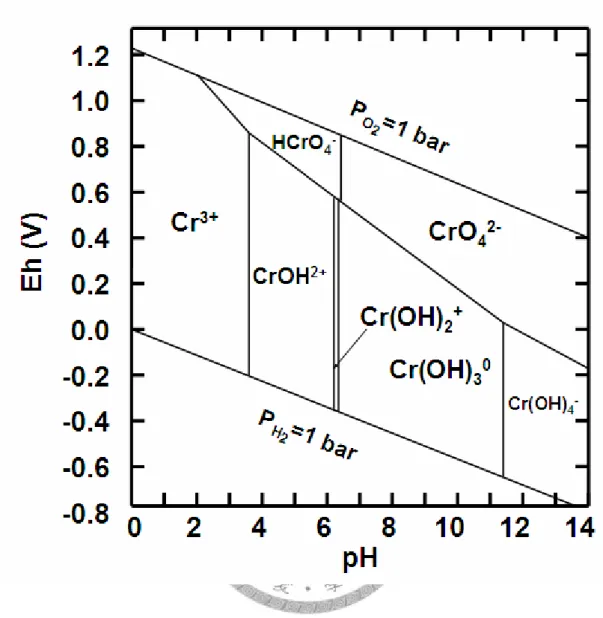
(hexavalent chromium, Cr(VI))。在不同的 pH 值與 Eh 值下,Cr(III)多以陽離子形態 存在,隨pH 值的增加分別為 Cr3+、CrOH2+、Cr(OH)2+、Cr(OH)3、Cr(OH)4-等形態 存在,而Cr(VI)則分別以 HCrO4-、CrO42-、Cr2O72-等陰離子形態存在 (如圖一) (Palmer and Wittbrodt, 1991),鉻在土壤中的移動性和分佈與其形態有相當密切的關 係。土壤顆粒表面多帶負電荷,因此Cr(VI)在土壤中的移動性較 Cr(III)來得佳。另 外,鉻會受到氧化還原 (oxidation- reduction)、沉澱溶解 (precipitation-
dissolution),與吸附脫附 (sorption- desorption) 等作用影響其於土壤中之移動性與 分佈。Cr(III)與 Cr(VI)間係經氧化還原作用轉換,移動性小與毒性低的 Cr(III)會經 氧化作用轉變為移動性大且毒性高的Cr(VI),反之 Cr(VI)亦可經還原作用轉變為 Cr(III)。
對生物體而言,Cr(III)與 Cr(VI)這兩種氧化態猶如一刀之兩刃,有研究證實當 鉻為Cr(III)這種氧化態時,對生物體有相當之必要性。1950 年代末期,Schwarz 與Mertz 證實大鼠體內的 Cr(III)對於葡萄糖的耐受性有一定的幫助 (Schwarz and Mertz, 1959)。Mertz 總結出鉻對於人體養分而言是必要的,他提出一些觀察來證明 之:(1) 鉻的缺乏會導致胰島素抗阻;(2) 胰島素抗阻可藉由補充鉻來改善;(3) 鉻 的缺乏會造成人體內立即的養分問題 (Mertz, 1993);相反地,當鉻為 Cr(VI)時,
則有研究指出其對人體具有危害性。自1950 年起,即有許多相關研究,如 Baetjer 提出暴露於具鉻酸鹽環境之工作者,其癌症之發生率較高 (Baetjer et al., 1950)。
1953 年,美國職業安全及健康研究院 (National Institute for Occupational Safety and Health, NIOSH) 證實了 CrO3致癌的可能,並於1975 年提出更多關於鉻酸鹽毒性 與致癌性的研究。鉻進入人體之可能途徑有:攝取、皮膚接觸、吸入等,其中以
吸入之途徑危害性最高,會導致癌症的發生,其他兩種途徑則不會導致癌症的發 生 (Zhang and Li, 1997)。另外,亦有研究指出 Cr(III)對植物體具有較 Cr(VI)更高 的毒性。
為避免生物體吸收過量的鉻,目前世界衛生組織 (World Health Organization, WHO) 訂定之飲用水 Cr(VI)濃度限制為 50 μg L-1或是960 nM。本國環境保護署亦 對鉻濃度有所限制,其相關標準如表一所示 (行政院環境保護署,2001;行政院環 境保護署,2003;行政院環境保護署,2007;行政院環境保護署,2008a;行政院 環境保護署,2008b;行政院環境保護署,2008c;行政院環境保護署,2009)。
圖一、鉻於水溶液系統中在不同pH 值與 Eh 值下物種之變化 (Palmer and Wittbrodt, 1991)。
Fig. 1. Eh-pH diagram for aqueous chromium species in a chromium-H2O system (Palmer and Wittbrodt, 1991).
表一、本國環境保護署公告與鉻相關標準。
Table 1. Regulation of chromium level in Taiwan announced by TWEPA.
適用範圍 Total Cr Cr(VI)
事業、污水下水道系統及建築物污水處理設施之放流水標準 2.0 0.5
廢(污)水以管線輸送排放於離開海岸之海洋之事業或污水下水道系統 2-5
(視施放海域而定) --
飲用水設備供應之飲用水及其他經中央主管機關指定之飲用水 0.05 --
第一類 0.025 --
地下水污染監測基準
第二類 0.25 --
第一類 0.05 --
地下水污染管制標準
第二類 0.5 --
土壤污染監測基準 175 --
土壤污染管制標準 250 --
單位:水體mg L-1;土壤mg kg-1
第一類:飲用水水源水質保護區內之地下水 第二類:第一類以外之地下水
1.2 鉻於生活之利用與污染
日常生活中鉻的使用相當廣泛,小如我們隨身攜帶的鑰匙,會利用鉻來電鍍 其表面;大如樹木砍伐後的木材防腐劑,木材防腐劑中有所謂CCA,即含有銅 (cooper, Cu)、鉻 (chromium, Cr)、砷 (arsenic, As) 等成份。其中鉻的比例以 47.5 % CrO3最高,其次砷 (As2O5) 佔 34 %,銅 (CuO) 則佔 18.5 %。CCA 中的鉻在土壤 中以吸附於鐵鋁氧化物的比例最高,可溶態與可交換態次之,這顯示鉻有極大的 可能會進入環境中其他環節,進而危害人體健康 (Balasoiu et al., 2001;Song et al., 2006)。此外,鉻亦可在化學上製備為無機藥品、金屬表面加工、製鋼、採礦、塗 料、釉料、石油提煉、製革等等,在在皆與我們的生活息息相關。
目前本國行政院環境保護署將鎘、鉻、銅、汞、鎳、鉛、鋅及砷列為八大重 金屬,且依據『台灣地區農地土壤重金屬監測結果』,重金屬因外來污染所致而列 為第五級 (鎘 10、鉻 16、銅 100、汞 20、鎳 100、鉛 120、鋅 80 及砷 60 mg kg-1 以上) 之地區有 1,027 公頃,造成污染之主因為灌溉水遭廢污水污染,其中污染面 積以546 公頃之彰化縣最高、121 公頃之桃園縣次之。其中鉻污染面積高達 219 公 頃係所有重金屬中排行第三 (行政院環境保護署,2002)。現今探討重金屬污染危 害及管制標準,大多以土壤中重金屬總量為基準。但,土壤中重金屬對生物體之 危害會受到重金屬本身氧化還原型態的影響,意即不同的氧化還原型態對環境與 生物造成的危害也會有所不同。對環境與生物體而言,除了毒性高的Cr(VI)之外,
Cr(III)也可能因氧化作用轉變為 Cr(VI)而對環境或生物體有所威脅。因此,應考量 鉻之氧化態與發生污染之土壤特性來訂定其污染管制標準。
1.3 鉻污染之整治
重金屬污染的整治方法很多,例如固定化/穩定化處理、玻璃化法…等等。本 國環境保護署考慮國內經驗、時間、效率等因素後,常是以「土壤翻土混合稀釋 法」及「土壤酸淋洗法」來改善土壤重金屬污染問題。現今亦有許多方法已應用 於去除Cr(VI)之污染,例如植生復育:利用如向日葵或其他特定樹種等對鉻的吸 收,來減少土壤中鉻的污染;或是生物復育:以具有還原Cr(VI)能力之微生物將 Cr(VI)還原為 Cr(III);亦有以化學法:以碳酸鈉與氫氧化鈉之混合物直接抽出 Cr(VI);其他還有如電解法、電動力法、活性碳吸附、零價鐵等都是目前常用於去 除或減少土壤中鉻污染的方法 (Memon et al., 2004;Wilkin et al., 2005;Graham et al., 2006;Wanze et al., 2007;Hoch et al., 2008;Buchireddy et al., 2009)。但這些方
法並非相當完善,本國常用之土壤翻土混合稀釋法改善重金屬污染,僅是將污染 物的濃度以未受污染的土壤稀釋之,並未真正將重金屬污染從土壤中移除。單純 就鉻污染而言,依健康危害風險評估,降低對生物體的危害即可;對生物體而言,
有危害之虞的鉻以Cr(VI)較具威脅性,Cr(VI)可利用各種還原物質來將其還原為 Cr(III),降低其移動性與毒性。
1.4 鉻氧化之研究
土壤中的氧化還原反應會影響鉻之氧化態,Cr(III)會經由氧化作用轉換為毒性 與移動性皆較高的Cr(VI)。在大部分的土壤以及廢棄物中僅有 O2與MnO2這兩種 無機氧化物能將Cr(III)氧化為 Cr(VI),其中 O2必須要在高溫下才能將Cr(III)氧化 為Cr(VI),或是需要其他條件輔助,自然界中這種狀況極少存在 (Eary and Rai, 1987;Apte et al., 2005;Apte et al., 2006;Panichev et al., 2008),因此土壤中最主 要能氧化Cr(III)的氧化物質為 MnO2。有關MnO2氧化Cr(III)的研究,最早有 Eary 與Rai 使用軟錳礦 (pyrolusite) 氧化 Cr(III),並探討各種因子如二氧化錳、氧氣存 在與否以及pH 值等對氧化作用之影響 (Eary and Rai, 1987)。有相當多種類之錳氧 化物用於將Cr(III)氧化為 Cr(VI),例如以構造區分有 α-MnO2、β-MnO2、
ramsdellite-MnO2、γ-MnO2、ε-MnO2、δ-MnO2、λ-MnO2、γ-MnOOH 等,或是天然 的氧化錳礦物如:水鈉錳礦 (birnessite)、軟錳礦 (pyrolusite)、鈣錳礦 (todorokite)、
鋰土礦 (lithiophorite)、黑錳礦 (hausmannite)、鉀錳氧礦 (cryptomelane)、鎂-水鈉 錳礦 (buserite)、水錳礦 (manganite) 等 (Eary and Rai, 1987;Fendorf and Zasoski, 1992;陳等人,1993;Yingxu et al., 1997;Chung, 1998;Kim et al., 2002;董等人,
2006;Feng et al., 2007)。
有許多研究提出純的二氧化錳將Cr(III)氧化為 Cr(VI)的反應式,不同的錳氧化 物之間有些許差異,但都大同小異。如Eary 與 Rai (1987) 研究利用 β-MnO2將Cr(III) 氧化為Cr(VI)的動力學實驗中,將 β-MnO2與Cr(III)的反應依不同 pH 值分為兩種 反應機制,在pH 值 3.0 至 4.7 之間為:
+
−
++ 2(s) → 4 + 2
2 1.5β-MnO HCrO 1.5Mn CrOH
但實驗結果往往會發現Cr(VI)與 Mn(II)的比例並非 1:1.5,而發現在較高的 pH 值 或Cr(III)濃度下,會有 MnOOH 生成,反應式如下:
+
−
++3β-MnO +3H O→HCrO +3MnOOH +3H
CrOH2 2(s) 2 4 (s)
Fendorf 與 Zasoski (1992) 則是以 δ-MnO2氧化Cr(III),提出了下式:
+ +
−
++1.5δ-MnO +H O→HCrO +1.5Mn +H
Cr3 2(s) 2 4 2
反應式中Cr(III)與 Mn(IV)或 Cr(VI)與 Mn(II)之間的莫耳數比皆為 1:1.5,這表示 純的MnO2與Cr(III)反應時,係以 1.5 mol Mn(IV)與 1 mol Cr(III)進行反應。
影響MnO2將Cr(III)氧化為 Cr(VI)的因子中,以 pH 值、溫度、離子強度、Cr(III) 濃度、MnO2用量、表面積、性質等研究較多。pH 值會影響鉻與錳顆粒在懸浮液 中的溶解度,Oze 等人 (2007) 利用水鈉錳礦氧化鉻鐵礦釋出之 Cr(III),發現 pH 值較低時Cr(VI)之產生量會比高 pH 值時多 (Oze et al., 2007)。而 pH 值的影響也 和錳氧化物的零電點有關,在零電點以上MnO2表面帶有負電荷,可以吸附存在於 溶液中的Cr(III),但是當 pH 值達到 7 左右,會有 Cr(OH)3的沉澱,使得Cr(III)無 法與MnO2發生反應;反之,在零電點以下MnO2表面帶有正電荷,無法吸附 Cr(III)。因此 MnO2的零電點高低會影響其氧化Cr(III)的能力 (Feng et al., 2006)。
溫度的增加則會加速反應的進行,溫度的增加會提升MnO2表面電位與電荷密度,
使帶負電荷的MnO2,負電位升高,負電荷密度增加,有利於MnO2表面吸附Cr(III) 以及對Cr(VI)的脫附 (劉等人,2003b)。另外,離子強度則是會增加 MnO2礦物表 面對Cr(III)的專一性吸附,於是 Cr(III)氧化的量及還原的 Mn 量皆會增加,此外也 易將氧化而來的Cr(VI)脫附至溶液中 (劉等人,2003b)。Cr(III)初始濃度亦限制了 Cr(III)被氧化的量,有研究指出在 Cr(III)濃度小於 1 mM 時,Cr(III)被鐵錳結核氧 化產生Cr(VI)的量隨其濃度增加而快速增加;Cr(III)濃度介於 1 至 2 mM 之間時,
其增加速度較為緩慢;當Cr(III)濃度大於 2 mM 時 Cr(VI)的產生量達到最大值 (Tan et al., 2005)。
MnO2本身之性質對其氧化Cr(III)的能力具有更為重要的影響。曾被探討的因 子有:表面積、結晶度、晶體構造、Mn 價數、用量、Mn 之形態等。以同一種 MnO2
而言,表面積愈大 (即用量愈大) 其可供反應之位置愈多,可氧化 Cr(III)的量愈
是與其所能提供之有效反應位置有關。前人研究中提出各種氧化錳礦物氧化Cr(III) 的能力與其表面積無關,該研究顯示不同氧化錳礦物之氧化能力大小依序為水鈉 錳礦I (48.3 m2 g-1) > 水鈉錳礦 II (35.8 m2 g-1) > 鈣錳礦 (98.5 m2 g-1) (Feng et al., 2006)。劉等人 (2003a) 之研究結果顯示 MnO2之結晶性愈差則氧化Cr(III)的能力 愈佳 (劉等人,2003a)。
晶體構造亦為影響MnO2氧化Cr(III)能力的因子之一,劉等人 (2003a) 探討不 同土壤鐵錳結核氧化Cr(III)能力的研究中指出,鈣錳礦 (todorokite) 屬於兩個三鏈 Mn-O 八面體共角頂形成之隧道構造,水鈉錳礦 (birnessite) 與鋰土礦 (lithiophorite) 則是由Mn-O 八面體通過共稜形成八面體片,就穩定性而言,前者較後者穩定,
表示前者之活性較後者差,氧化還原過程中,得失電子的能力較弱,造成鈣錳礦 氧化Cr(III)的量會少於構造相對不穩定的水鈉錳礦與鋰土礦 (劉等人,2003a)。錳 氧化物中Mn 的價數對其氧化 Cr(III)的能力大小有直接的關係,除了純的 MnO2 的 錳為Mn(IV)之外,天然的氧化錳礦物的錳都是由價數混合的錳組成。Oze 等人 (2007) 研究中所使用的水鈉錳礦,其化學式為 K0.16MnIII0.16MnIV0.8O2 (Oze et al., 2007),或是有研究利用實驗求得錳氧化物的平均氧化數 (average oxidation state, AOS),而這個數值愈高,表示其可接受的電子數較多,該研究中使用三種氧化錳 礦物氧化Cr(III),分別為水鈉錳礦 I、水鈉錳礦 II、鈣錳礦,其氧化 Cr(III)的能力 大小依序為:水鈉錳礦 I (3.96) > 水鈉錳礦 II (3.89) > 鈣錳礦 (3.82),與平均氧化 數有關 (Feng et al., 2006)。雖然錳氧化物可能具有將 Cr(III)氧化為 Cr(VI)的能力,
但並非Mn 的量愈高愈好,而是與 Mn 之形態有關。目前有許多研究是利用錳氧化 物中易還原性錳的量比較各個錳氧化物之間氧化Cr(III)的能力,但錳氧化物之氧化 能力大小還牽涉其他性質,故劉等人的研究 (2003) 中發現氧化 Cr(III)的能力與其 易還原性錳含量不一致 (劉等人,2003a)。Chon 等人 (2008) 的研究中利用不同還 原劑定義Mn 之形態,其中以 DCB (dithionite-citrate-bicarbonate, DCB) 抽出的 Mn 定義為Mnd,以HAHC (hydroxylamine hydrochloride, HAHC) 抽出的 Mn 定義為
Mnh,以NH4OAc 及 hydroquinone 抽出的 Mn 定義為 Mnr,再將不同形態的Mn 與 其氧化能力進行相關比較。這些抽出劑為還原物質,試圖將Mn(III)與 Mn(IV)還原 為Mn(II),各種抽出劑之還原能力不同,因此其抽出液測得的 Mn(II)量皆不同。
而結果發現Mnd與Mnh較能代表錳氧化物可氧化Cr(III)之能力。因此,在研究特 定錳氧化物能否氧化Cr(III)時,可測定 DCB 可抽出 Mn 或是 HAHC 可抽出 Mn 推 估其氧化Cr(III)的能力大小 (Chon et al., 2008)。
1.5 鉻還原之研究
環境中的鉻污染,首要考量Cr(III)是否會經環境中可能的氧化過程形成 Cr(VI) 及避免其對生物體造成危害。因此需藉由各種方法將Cr(VI)去除或還原為 Cr(III),
以降低危害。移除Cr(VI)之方法有:利用活性碳對水體中 Cr(VI)進行吸附 (Demirbas et al., 2004);利用高嶺石、伊萊石等礦物或土壤吸附 Cr(VI) (朱,1982)。本國鉻管
制污染標準 (表一) 係測定鉻之總量以區分有否受到污染,因此需利用上述吸附或 其他方法將鉻由污染廠址移除,但實際上將Cr(VI)還原為 Cr(III)同樣可降低其對生 物體造成的危害。過去數十年來有許多關於還原Cr(VI)的研究,不管是利用生物 或非生物方法皆不勝枚舉。利用生物的方法多是找出可還原Cr(VI)的菌種,如 Vibrio fischeri (Fulladosa et al., 2006)。而非生物的方法,便是添加可還原 Cr(VI)的
物質到水體或土壤中。可還原Cr(VI)的物質相當多,2005 年,Su 與 Ludwig 利用 硫酸亞鐵與連二亞硫酸鈉處理固體廢棄物之Cr(VI)的研究中,將常用於將還原 Cr(VI)之還原劑分為三大類。第一類為含硫化合物,如 H2S、FeS、Na2SO3、Na2S2O5、 Na2S2O4等等;第二類為含鐵的還原劑,如Fe0、溶解性Fe(II)、赤鐵礦、白水雲母、
磁鐵礦等含鐵礦物之Fe(II);第三類為有機化合物,如羥胺、抗壞血酸、草酸鹽、
檸檬酸鹽、有機酸以及土壤有機物 (Eary and Rai, 1988;Su and Ludwig, 2005;
Graham et al., 2006;Wanze et al., 2007;Hoch et al., 2008)。
儘管可用於還原Cr(VI)的方法很多,若欲處理土壤中的 Cr(VI),使用化學物 質對土壤可能會造成破壞或其他負面的影響,故若能以添加天然的有機物質還原 土壤中的Cr(VI),一方面可以將土壤中的 Cr(VI)還原為 Cr(III),另一方面不會對土 壤性質造成破壞,在進行污染復育之後,土壤可以較快被再次利用。早在1976 年 Bartlett 與 Kimble 兩人研究土壤中 Cr(VI)的行為時,即利用牛糞廄肥與土壤有機質 還原Cr(VI),兩者相較之下土壤有機質比牛糞廄肥更能有效地還原 Cr(VI)。其反 應式如下:
O 5H 2CrCl COOK
- R - KOOC 6HCl
O Cr K CHOH -
R -
HOHC + 2 2 7+ ↔ + 3+ 2
有機質扮演著電子捐贈者的角色,將Cr(VI)還原為 Cr(III),且其在酸性土壤中較鹼 性土壤中易發生還原作用 (Bartlett and Kimble, 1976)。
1994 年,Losi 等人研究土壤中 Cr(VI)還原的化學與生物效應之實驗中,有機 質還原Cr(VI)係以牛糞廄肥 (cattle manure) 作為還原劑,反應式如下:
−
++ ⇔ +
+
+ 2- 2 3 3
4
2O(organicmatter) 4CrO 5H 2H O 4Cr(OH) 3HCO 3CH
反應式中有機質的碳為電子的來源,有機質氧化後,Cr(VI)為最終電子接受者。廄 肥的添加在有生物與無生物的狀況下都可以增加Cr(VI)的還原,其中有生物的狀 況下更能增進Cr(VI)的還原 (Losi et al., 1994)。
2001 年 Bolan 與 Thiagarajan 利用兩種石灰資材與有機資材觀察其對兩種土壤 中鉻滯留的影響,並分別進行批次與管柱實驗。石灰資材的添加有利於降低Cr(III) 的植物毒性,而有機資材則有利於降低Cr(VI)的植物毒性。受鉻污染土壤中,石 灰資材與有機添加物的添加皆會降低植物吸收鉻的有效性,或減少淋洗到地下水 的量 (Bolan and Thiagarajan, 2001)。而後 Bolan 等人在 2003 年的研究中使用污泥 堆肥 (biosolid compost)、農家堆肥 (farmyard manure)、魚肥 (fish manure)、馬糞 堆肥 (horse manure)、腐熟之香菇太空包堆肥 (spent mushroom)、豬糞堆肥 (pig manure)、家禽堆肥 (poultry manure) 等七種有機資材還原一有機質含量低的土壤 中的Cr(VI)。並提出有機質的有機碳含量才是影響一有機質還原 Cr(VI)能力的主 要因子,由於有機資材的添加可以增加微生物的活性,提供碳源,因此有機資材 添加的狀況下可增進Cr(VI)的還原,結果與 Losi 等人 (1994) 的研究結果相符,即 有機資材的添加促進微生物活性而增進其還原Cr(VI)的量,其反應式如下:
O 11H 3CO
4Cr 16H
O 2Cr matter) (organic
O
3CH2 + 2 7+ +→ 3++ 2+ 2
(Losi et al., 1994;Bolan et al., 2003) 除上述文獻中使用之有機資材外,尚有許多有機資材使用於還原Cr(VI),且 具有良好的效果,如 (1) 榛果殼 (hazelnut shell) 不僅可有效地移除金屬離子並還
kg-1 (Cimino et al., 2000);(2) 豆渣餅 (soya cake) 可在 pH 值小於 1 的情況下有效 地將Cr(VI)還原為 Cr(III),在體積為 75 mL 濃度為 50 mg L-1的Cr(VI)溶液中,最 佳處理時間為5 小時。豆渣餅的最佳使用量為每 75 mL 的溶液使用 0.7 g 豆渣餅,
即可移除溶液中90 % 以上的 Cr(VI) (Daneshvar et al., 2002);(3) 小麥麩 (wheat bran) 中的木質纖維素 (lignocellulosic) 可移除 Cr(VI),在酸性基質中 Cr(VI)最大 吸附量為35 mg g-1。該實驗亦利用EXAFS (延伸 X 光吸收精細結構,extended X-ray absorption for fine structure) 證明 Cr(VI)還原後 Cr(III)之產生 (Dupont and Guillon, 2003);(4) 水生植物的殘體可固定 Cr(VI),該實驗以 N. graminea、P. stratiotes 的 葉片以及 P. stratiotes 的根吸附溶液中的 Cr(VI)。這些植物殘體可進一步將 Cr(VI) 還原為Cr(III),其中有 53 至 67 % Cr(III)為有機態,其餘為 Cr(OH)3沉澱物 (Hu et al., 2003);(5) 稻殼 (rice husk) 因富含矽酸且具有高孔隙率而成為廢水中良好的重
金屬吸附劑,實驗首先利用稻殼吸附Cr(VI),接著再以 XANES (X 光近緣結構,
X-ray absorption near edge structure) 分析發現反應 12 與 48 小時後,分別有 70 % 及 90 % Cr(VI)被稻殼吸附。經 12 小時反應後,鉻的物種分佈為 41 % 有機態 Cr(III) + 27 % Cr(OH)3 + 32 % CrO3;經48 小時反應後,鉻的物種分佈為 57 % 有機態 Cr(III) + 31 % Cr(OH)3 + 12 % CrO3 (Hu et al., 2004);(6) 東方櫸樹 (Fagus orientialis L.) 的木屑等低成本的吸附劑常用於吸附溶液中的重金屬,該實驗中發現其吸附量取 決於溶液之pH 值,pH 值為 1 時具有最大 Cr(VI)吸附量。而 Cr(VI)初始濃度愈低 則該吸附劑可吸附愈高比例的Cr(VI) (Acar and Malkoc, 2004);(7) 甘蔗渣
(bagasse)、炭化稻殼 (charred rice husk)、活性碳 (activated charcoal) 以及尤加利樹 的樹皮 (eucalyptus bark) 可用於移除工業廢棄物中的 Cr(VI)。實驗發現這些吸附 劑中以尤加利樹的樹皮移除Cr(VI)的效果最佳。pH 值為 2、Cr(VI)濃度 250 mg L-1 時吸附量最大可吸附45 mg-Cr(VI) g-1。廢水中若具有多種金屬如Cr(VI)、Cr(III)、
Mg 與 Ca 離子時,這些吸附劑會優先吸附 Cr(VI) (Sarin and Pant, 2006);(8) 葡萄 藤 (grape stalks) 與育亨賓樹皮 (yohimbe bark) 可吸附並還原 Cr(VI),結果發現育
亨賓樹皮比葡萄藤更能有效地移除Cr(VI),兩者反應 24 小時後,加入育亨賓樹皮 的溶液中有大約65 % 的鉻被吸附;而加入葡萄藤的溶液則吸附 55 % 的鉻 (Fiol et al., 2008)。
1.6 鐵錳結核
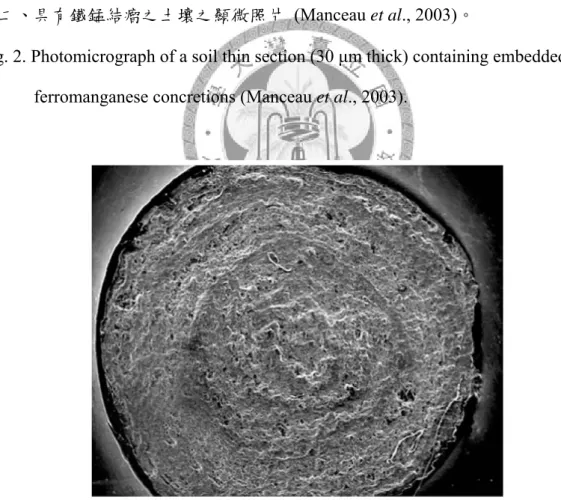
所謂鐵錳結核 (Fe-Mn nodules) 意指為中心為錳,外圍以鐵氧化物等裹覆的結 核,其形成的原因為土壤中中等還原狀況以及地下水位頻繁之變動。首先在還原 狀態中,受還原的錳先移動至土壤微孔隙中或不易風化之礦物表面上沉澱,形成 結晶性較差之錳核。由於地下水位變動或表面灌溉水之淋洗,導致還原的鐵隨著 黏粒或獨自洗入至一開始的錳核表面或該裂隙中再氧化而沉澱。經過長期乾溼交 替的水文變動,鐵錳結核逐漸氧化累積增大 (圖二) (Manceau et al., 2003)。因此會 由一開始小粒徑之鐵錳結核為核心逐漸增大,並可由其微形態觀察之,證實鐵錳 結核是現地生成的 (簡,2006)。Gasparatos 等人 (2005) 發現鐵錳結核的內部構造 是相當緊密的 (圖三) (Gasparatos et al., 2005)。
早在1960 年代左右即有關於鐵錳結核之研究,1965 年發現在海底有鐵與錳氧 化物形成的結瘤 (concretion) 與硬塊 (crust),當時觀察到該結瘤與硬塊中間有黑 色的斑紋,經分析後發現其為錳氧化物 (Bonatti and Nayudu, 1965)。這些錳氧化物 中的錳礦物種類相當多樣,有水鈉錳礦 (birnessite)、鈣錳礦 (todorokite)、水錳礦 (manganite) 等 (Crerar and Barnes, 1974),表示即使同為鐵錳結核,其中的錳氧化 物的種類仍可能不同,這也造成不同來源的鐵錳結核之間性質的差異。
關於鐵錳結核之詳細元素組成,Dawson 等人 (1985) 的研究中提及鐵錳結核 可分為三層,外層的鐵與錳含量低,愈往中心其鐵錳含量愈高,其中亦含有V、
Co、Ni、Cu、Zn、Na、Mg、K、Ca、Rb、Sr、Cd、Cs、Ba、La、Ce、Pb 等元素,
其中Si、Al、Ti 這三個元素在錳含量高的部分含量較少 (Dawson et al., 1985;
Palumbo et al., 2001)。然而,另有研究指出每個地方發現的鐵錳結核之鐵錳比例都 不盡相同,可分為鐵含量高、錳含量高以及鐵錳含量皆高等三種情形。結核中可 發現針鐵礦 (goethite) 與結晶性差的鐵氧化物,以及水鈉錳礦 (birnessite) 與複水 錳礦 (vernadite) 等錳氧化物之存在。但未發現含碳酸鹽之系統中易因氧化還原波 動而生成的礦物如:菱鐵礦 (siderite) 與菱錳礦 (rhodochrosite) (Sanz et al., 1996)。
雖然研究鐵錳結核生成、型態、成分等研究相當多,但對於鐵錳結核在土壤 中的作用,自2000 年始有較完整的研究。譚等人 (2001) 研究鐵錳結核之組成與 其化學性質的研究中,利用鐵錳結核中的氧化錳氧化Cr(III),試比較不同鐵錳結核 之氧化能力大小及pH 值、離子強度、競爭離子與氧化錳的結晶程度等因子對氧化 過程的影響。鐵錳結核氧化Cr(III)的過程僅發生在鐵錳結核中氧化錳的部分,首先 是Cr(III)吸附在氧化錳礦物的 Stern 層,並直接與氧化錳礦物表面的 O 與 OH 基產 生鍵結,此時Cr(III)之外圈電子與氧化錳礦物接觸,發生電子轉移,Mn4+/Mn3+還 原為Mn2+,Cr(III)氧化為 Cr(VI)。其中吸附於氧化錳之擴散層的 Cr(III)則不易發生 氧化還原反應 (譚,2000;譚等人,2001;劉等人,2002;劉等人,2003a;Tan et al., 2005)。
圖二、具有鐵錳結瘤之土壤之顯微照片 (Manceau et al., 2003)。
Fig. 2. Photomicrograph of a soil thin section (30 μm thick) containing embedded ferromanganese concretions (Manceau et al., 2003).
圖三、鐵錳結核內部構造之掃描式電子顯微影像 (Gasparatos et al., 2005)。
Fig. 3. Representative scanning electron photomicrograph image showing the internal structure of a Fe-Mn nodule (Gasparatos et al., 2005).
1.7 全量六價鉻之測定方法
受到環境中pH 值與氧化還原電位的影響,土壤中 Cr(VI)大多以陰離子存在,
如CrO42-、HCrO4-、Cr2O72-等形態。探討氧化錳氧化Cr(III)後產生 Cr(VI)的研究,
大多僅考慮有效性的Cr(VI),對於總量的 Cr(VI)鮮少討論,因而忽略了氧化錳真 正可氧化Cr(III)的量。
美國環境保護署 (United States Environmental Protection Agency, USEPA) 於 1996 年提出全量 Cr(VI)的鹼性消化法,在三個條件下,該鹼性消化法才適用於 Cr(VI)的分析,為:(1) 萃取液必須可完全溶解所有的 Cr(VI);(2) 萃取液不會將 Cr(VI)還原為 Cr(III);(3) 該方法並不會使 Cr(III)氧化為 Cr(VI)。在鹼性的環境中,
Cr(VI)不易受還原物質如亞鐵離子、硫化物、有機質等影響而轉變為 Cr(III),因此 不需要擔心會有高估或低估的情形。
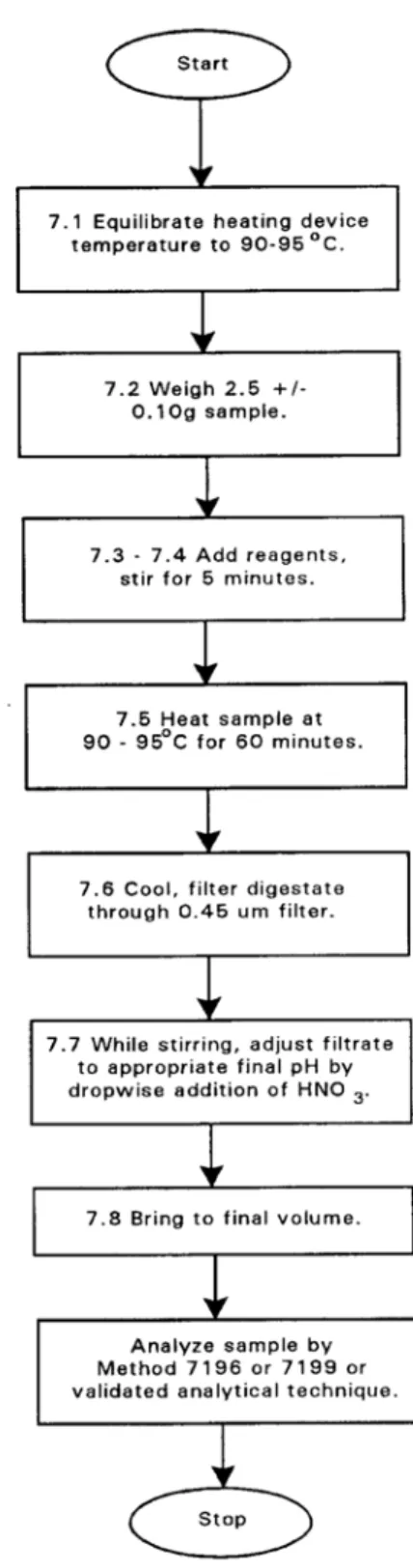
該方法是利用鹼性萃取液與待分析固體樣品進行消化,將溶解態、吸附態以 及沉澱態的含鉻化合物中的Cr(VI)溶出 (圖四)。如此一來便可比較總 Cr(VI)含量 與有效性Cr(VI)的差異。
圖四、Cr(VI)之鹼性消化法流程圖 (USEPA, 1996)。
Fig. 4. Flowchart of alkaline digestion for hexavalent chromium (USEPA, 1996).
1.8 錳抽出法比較
許多研究指出土壤中的氧化錳礦物將Cr(III)氧化為 Cr(VI)的能力大小與錳的 總量無絕對的相關,因此何種方法抽出的錳與土壤中氧化錳礦物之氧化能力具有 直接相關性,便為許多研究之焦點。例如依抽出劑之不同,可分為:水溶性錳 (water-soluble Mn)、可交換性錳 (exchangeable Mn)、雙酸 (鹽酸與硫酸) 可抽出的 錳 (double acid extractable Mn)、二乙烯三胺五乙酸可抽出的錳
(diethylenetriaminepentaacetic acid)、易還原性錳 (easily reducible Mn)、選擇性溶解 的錳 (selective dissolution of Mn-oxide) 等 (Gambrell, 1996)。
Chon 等人 (2008) 即用不同抽出劑抽出的錳與氧化錳氧化 Cr(III)的能力大小 進行比較,結果發現以DCB 可抽出性錳 (extracted with dithionite-citrate-bicarbonate) 或是HAHC 可抽出性錳 (extracted with 0.1M NH2OH.HCl in 0.01M HNO3) 之大小 可代表其氧化Cr(III)的能力 (Chon et al., 2008)。以上所用於抽出土壤中錳的方法 中的抽出劑,大致上為還原劑,將土壤中的錳以不同還原能力的還原劑抽出,使 其還原為Mn(II)而可被測得。
1.9 研究目的
鉻之於我們生活息息相關,其移動性與毒性受其氧化態之影響。而鉻氧化態 可分為Cr(III)與 Cr(VI),Cr(III)多以陽離子形態存在於土壤中,因此會被土壤顆粒 表面負電荷吸附住,不易移動;而Cr(VI)多以陰離子形態存在於土壤中,移動性 較Cr(III)高得許多 (Palmer and Wittbrodt, 1991)。根據 Baetjer 之研究此兩種氧化態 對人體之影響,發現Cr(VI)具有致癌性 (Baetjer, 1950),而 Cr(III)則相對無害,亦 為對人體有益之元素 (Schwarz and Mertz, 1959;Mertz, 1993)。當環境中有 Cr(VI) 污染時,將威脅人體的健康安全,因此必須要進行污染的整治以降低Cr(VI)的危 害性。雖然本國於各種管制標準中都是以總鉻為基準來考量其對生物體的危害 性,但實際上僅需降低Cr(VI)的量,即可降低其危害生物體之風險。
目前已知可用於將土壤中Cr(VI)還原為 Cr(III)的有機資材與化學物質相當 多,例如堆肥、豆渣餅 (Bolan and Thiagarajan, 2001;Daneshvar et al., 2002) 等。
但研究亦指出將Cr(VI)還原為 Cr(III)後,倘若與土壤中的氧化錳、鐵錳結核等具有 氧化能力之物質接觸,亦有可能再被氧化為Cr(VI) (Eary and Rai, 1987;陳等人,
1993;Yingxu et al., 1997),如此一來,則復育之努力徒勞無功。因此為降低土壤 中之Cr(VI)濃度,必須考量到土壤中的錳對整個還原過程的影響,進而評估還原 Cr(VI)所需使用之有機資材及其用量。
本研究之目的係利用富含鐵錳結核的土壤與Cr(III)進行反應,觀察鐵錳結核含 量與粒徑對其氧化Cr(III)能力之影響。利用錳電子消耗測定法 (manganese electron demand measuring method) 測得之土壤易還原性錳含量預估其氧化能力,並比較其 與純二氧化錳之氧化能力差異。此外,利用已知具有還原Cr(VI)能力的有機資材 復育含鐵錳結核之Cr(VI)污染土壤,藉此檢視鐵錳結核對有機質還原 Cr(VI)之影 響,並觀察有機質還原Cr(VI)而來的 Cr(III)會否被土壤中鐵錳結核再氧化。
第二章 材料與方法
2.1 試驗土壤選定、採集及製備 2.1.1 試驗土壤選定
為研究鐵錳結核氧化Cr(III)之情形,選擇具鐵錳結核的土壤。簡 (2006) 的研 究指出,桃園中壢臺地內之湖口土系、竹圍土系、蘆竹土系等土壤因地下水位之 變動而有鐵錳結核之生成,其中竹圍系土壤已證實其鐵錳結核具有氧化Cr(III)之能 力 (簡,2006;陳,2008),因此本研究中利用竹圍系土壤進行實驗。
2.1.2 試驗土壤採集
竹圍系土壤 (Chuwei Series, Cw),採樣地點為桃園縣新屋鄉;採樣深度為 40- 60 cm,採樣日期為 2007 年 12 月 5 日。該地點於春夏季種植西瓜,秋冬季種植水 稻,兩種作物輪流耕種會造成暫棲水位的變動,土壤原屬紅壤,因氧化還原的作 用,土壤中有鐵錳結核 (iron-manganese nodules, Fe-Mn nodules) 的形成。觀察其 中的鐵錳結核,可發現其為以錳核為中心,鐵氧化物包裹在外的顆粒 (圖五),形 成良好的鐵錳結核具有較為堅固的錳核。
2.1.3 試驗土壤製備
採集試驗土壤後,在風乾前將土壤中顆粒明顯之鐵錳結核取出,分裝到塑膠 盆中。試驗土壤的部份直接置於通風良好處風乾,以研缽式研磨儀 (Retsch, RM200) 研磨後通過10 mesh 篩網 (通過者粒徑小於 2 mm),接著以四分法將土壤充分混合 均勻,保存於塑膠罐中備用。實驗前土壤皆經研磨至可過80 mesh 篩網 (粒徑小於 0.2 mm),同樣以四分法將土壤充分混合均勻,保存於另一塑膠罐中備用。
2.1.4 試驗鐵錳結核製備
取出的鐵錳結核以蒸餾水將其外層裹覆的土壤黏粒盡量沖洗乾淨,確保顆粒 大部分為鐵錳結核而非一般土塊。沖洗完畢後將鐵錳結核置於通風良好處風乾,
再研磨通過5 mesh 篩網 (通過者粒徑約為 4 mm),接著以四分法將鐵錳結核充分 混合均勻,保存於塑膠罐中備用。最後在實驗前依需求研磨至通過5、80 mesh 篩 網 (粒徑分別小於 4、0.2 mm),各粒徑鐵錳結核皆以四分法將其充分混合均勻,
分別保存於塑膠罐中備用。實驗為研究鐵錳結核粒徑對其氧化Cr(III)能力之影響,
除了選擇與實驗中土壤相同之粒徑外,另選定與實驗土壤粒徑差異較大的大小,
即4 mm。
圖五、由竹圍系土壤挑出之鐵錳結核;外圍紅色為鐵氧化物,中心黑色為錳核。
Fig. 5. The Fe-Mn nodules selected from Chuwei series soil. The core with black color is Mn concretions, and the red periphery is composed of Fe-oxides.
2.2 試驗土壤基本性質分析
2.2.1 土壤 pH 值:玻璃電極法 (McLean, 1982)
a. 秤取 10 g 經研磨並通過 10 mesh 篩網的試驗土壤,置入乾淨的塑膠燒杯中。
b. 加入相同重量的蒸餾水,使得土壤與蒸餾水的重量比為 1:1。
c. 以玻璃棒攪拌使土壤與蒸餾水混合均勻,接著靜置 1 小時,使土壤沉降。
d. 以 pH 計 (Orion, 3STAR) 測定土壤 pH 值,並紀錄之。
e. 本實驗為三重複。
2.2.2 土壤水分含量:重量法 (行政院環境保護署環境檢驗所,2002)
a. 準備附蓋秤量瓶數個,以去離子水洗淨後,放入烘箱 (YIH DER, DN-600) 以 105 ℃烘 4 小時。
b. 將各秤量瓶與瓶蓋個別標上編號,再烘 30 分鐘,接著放入乾燥皿進行冷卻。
c. 冷卻後快速秤取瓶重,並紀錄之,記為 Wb。
d. 加入約 5 g 經研磨並通過 10 mesh 篩網的試驗土壤之後,再度秤重並紀錄之,
記為Wt。
e. 以 105 ℃烘 24 小時至恆重,以除去土壤中的水分,烘乾後蓋上瓶蓋後取出,
再放入乾燥皿進行冷卻。
f. 冷卻後秤取總重,並紀錄之,記為 Wd。 g. 計算土壤水分含量。
風乾土壤重量含水量 (%) = 100 W W
W W
b d
d
t ×
−
−
Wt:瓶重+風乾土重 (g),即總重,total weight。
Wb:瓶重 (g),weight of weighing bottle。
Wd:瓶重+烘乾土重 (g),weight of dry soil。
h. 本實驗為三重複。
2.2.3 土壤質地:比重計法 (Bouyoucos, 1936)
a. 秤取 50 g 經研磨並通過 10 mesh 篩網之試驗土壤,置入 500 mL 玻璃燒杯中,
加入200 mL 蒸餾水。
b. 將土壤與水攪拌混合後倒入金屬攪拌杯中,加入 10 mL 5 % Na(PO3)n (n
>3)c,將溶液體積加至距離金屬攪拌杯杯口2/3 處,於攪拌器 (Eijkelkamp, S1211) 內在第一階段轉速下攪拌 10 分鐘。
c. 攪拌完畢後將全部土壤懸浮液移入 1000 mL 量筒中,定量至 1000 mL,用攪 拌槳以相同頻率攪拌20 次。
d. 取出攪拌槳,開始計時。20 秒後放入比重計,於 40 秒時紀錄比重計讀數 (Ps),
此為坋粒與黏粒之含量。
e. 再以攪拌槳以相同頻率攪拌 20 次,靜置 2 小時後,放入比重計,並紀錄比 重計讀數 (Pc),此為黏粒之含量。
f. 計算砂粒、坋粒與黏粒含量。
砂粒 (%) = 100 % - ( Ps 100% 烘乾土重× ) 黏粒 (%) = ( Pc 100%
烘乾土重× )
坋粒 (%) = 100 % - (砂粒% + 黏粒%)
g. 以美國農部土壤調查手冊土壤質地分類三角圖判斷各土壤質地。
h. 本實驗為三重複,同時進行空白試驗與溫度校正。溫度校正係以 19.4 ℃為 基準。每增加1 ℃,比重計讀數應加 0.3,每減少 1 ℃,比重計讀數應減 0.3。
◎ 5 % Na(PO3)n配製-
秤取5 g Na(PO3)n先溶於少許蒸餾水中,完全溶解後倒入100 mL 定量 瓶中,以蒸餾水沖洗燒杯內殘餘溶液後,定量至刻線。
○1 Na(PO3)n (n >3):偏磷酸鈉 (sodium hexametaphosphate),Nacalai Tesque,試藥級。
2.2.4 土壤有機質含量
2.2.4.1 燒灼失重法 (Ball, 1964;Davies, 1974;Rabenhorst, 1988;Soon and Abbound, 1991)
a. 取附蓋坩堝數個,洗淨後以 105 ℃烘 24 小時。
b. 烘乾後,蓋上坩堝蓋取出,放入乾燥皿使其冷卻。
c. 冷卻後秤取坩堝重,並紀錄之,記為 Wb。
d. 取通過 80 mesh 之試驗土壤置於坩堝內,並將樣品以 105 ℃烘 24 小時,除 去水分。
e. 105 ℃烘乾過程結束後,蓋上坩堝蓋取出,放入乾燥皿使其冷卻。
f. 冷卻後秤取其重量,並紀錄之,記為 Wd1。
g. 之後置於灰化爐 (Nabertherm, R-L3),以 250 ℃烘 2 小時,之後升溫至 375 ℃ 烘16 小時。
h. 375 ℃烘乾過程結束後,蓋上坩堝蓋取出,放入乾燥皿使其冷卻。
i. 冷卻後秤取其重量,並紀錄之,記為 Wd2。 j. 計算土壤有機質含量。
土壤有機質含量 (%) = 100 W
W W W
b d1
d2
d1 ×
−
−
Wb:瓶重 (g),weight of weighing bottle。
Wd1:瓶重+烘乾土重 (g),weight of dry soil。
Wd2:瓶重+已去除有機質之土重 (g),weight of soil without organic matter。
k. 本實驗為三重複。
2.2.4.2 濕式氧化法 (Nelson and Sommers, 1982)
a. 秤取 0.5 g 且經研磨並通過 80 mesh 篩網之試驗土壤,置於 500 mL 三角錐瓶 中,加入10 mL 1N K2Cr2O7c,搖晃使其均勻後快速加入20 mL 濃 H2SO4d,
b. 加入約 200 mL 蒸餾水及 10 mL 85 % H3PO4e,放冷,再加入3-4 滴 o-phenanthroline 指示劑f。
c. 以 0.5 N Fe(II)滴定土壤溶液,至溶液顏色為棕紅色,為滴定終點。滴定過程 顏色變化如下:暗褐色→濁藍色→鮮明藍色→深綠色→紅棕色 (終點)。
d. 計算土壤有機質含量。
土壤有機質含量 (%) =
d B
S
W 100 77 . 0
724 . 1 1000
1 4 0 12 . 1 V ) 1 V (
10× − × × × × × 10:1N K2Cr2O7使用量 (mL),volume of K2Cr2O7。
1.0:K2Cr2O7的濃度 (meq L-1),concentration of K2Cr2O7。 12:碳的原子量 (g mol-1),atomic weight of carbon。
4:碳的價數 (eq),valence of carbon。
1.724:有機碳與有機質轉換係數,Van Bemmelen factor。
0.77:經無數次實驗求得本方法的回收率,recovery。
VS:以0.5 N Fe(II)滴定樣品溶液所需體積 (mL)。
VB:以0.5 N Fe(II)滴定控制組所需體積 (mL)。
Wd:烘乾土重 (g),weight of dry soil。
e. 本實驗為三重複,同時進行空白試驗。
◎ 1N K2Cr2O7配製-
秤取4.903 g K2Cr2O7溶於少許蒸餾水中,完全溶解後倒入100 mL 定量瓶 中,以蒸餾水沖洗燒杯內殘餘溶液後,定量至刻線。
◎ o-phenanthroline 指示劑配製-
濃度為0.025M,取 3.7125 g o-phenanthroline (monohydrate) 及 1.7375 g FeSO4.7H2O 溶於約 150 mL 蒸餾水完全溶解後倒入 250 mL 定量瓶中,以蒸 餾水沖洗燒杯內殘餘溶液後,定量至刻線。
◎ 0.5 N Fe(II)配製-
秤取70 g Fe(NH4)2(SO4)2,溶於300 mL 蒸餾水中,完全溶解後倒入 500 mL 定量瓶中,以蒸餾水沖洗燒杯內殘餘溶液後,加入濃硫酸7.5 mL,待其冷卻 後加水至刻線。
○1 K2Cr2O7:重鉻酸鉀 (Potassium dichromate),J. T. Baker,試藥級。
○2 H2SO4:硫酸 (Sulfuric acid),Fluka,試藥級。
○3 H3PO4:磷酸 (Phosphoric acid),85 %,merck,試藥級。
○4 C12H8N2.H2O:啡林指示劑 (o-phenanthroline),Riedel-deHaën,試藥級。
○5 Fe(NH4)2(SO4)2:硫酸亞鐵銨 (Ferrous ammonium sulfate),J. T. Baker,試藥級。
2.2.5 土壤中總鐵、錳、鉻、鋁之含量:王水消化法 (修改自行政院環境保護署環 境檢驗所之方法-NIEA S321.63B)
a. 秤取 0.5 g 經研磨且已過 100 mesh 篩網之試驗土壤,精秤至 1 mg。接著將土 壤樣品倒入消化管中,並以少許蒸餾水沿管壁沖下,潤濕土壤。
b. 以下於抽氣櫃中進行操作-每個消化管中先後加入 7.5 mL 濃 HClc與2.5mL 濃HNO3d,搖盪充分混合均勻。在室溫下靜置16 小時,並適時將消化管搖 晃使其充分反應。
c. 靜置結束後將樣品移至加熱板中 (FIRSTECK SCIENTIFIC, AT-480),開始加 熱至140 ℃,採階段式加熱、迴流 2 小時。
d. 加熱結束後將消化管移出加熱板,冷卻樣品至室溫後,以約 10 mL 0.5 N HNO3d沿消化管沖洗,收集於100 mL 定量瓶中,消化管內殘餘物以 0.5 N HNO3溶液盡量洗出,再定量至標線,以石蠟膜封住後搖勻。
e. 接著以 Whatman no.42 濾紙將定量瓶中溶液過濾至樣品瓶中。
f. 以感應耦合發射電漿光譜儀 (Perkin Elmer, Optima 2000 DV) 分析樣品液中 待測元素之濃度,於波長259.939 nm 下測定 Fe 濃度、於波長 257.610 nm 下