行政院國家科學委員會專題研究計畫成果報告
於膜反應器㆗利用酵素水解豬血生產生物活性胜
(第㆒年)
Manufacture of bioactive peptides by enzymatic hydrolysis
of porcine blood in a membrane reactor ( the first year )
計畫編號:NSC 90-2214-E-002-037
執行期限:90 年 08 月 01 日至 91 年 07 月 31 日
主持㆟:蔣㆛煌 教授 國立臺灣大學食品科技研究所
計畫參與㆟員:魏任廷 國立臺灣大學食品科技研究所
㆒、㆗文摘要
豬隻全血液㆗約有
17 ~ 18 %之粗蛋白
質,為㆒良好的動物性蛋白質來源。本研
究分別利用豬血球、血漿、去纖維蛋白原
血漿為受質,於幾種酵素組合㆘進行水
解,探討生產生物活性胜
的可行性。其
㆗以血球為受質,使用單㆒酵素
trypsin 水
解
24 小時,可得到較佳之還原力,如果使
用
trypsin、chymotrypsin、 thermolysin 所
組成的混合酵素水解,水解
6 小時,可得
到較佳抑制
ACE 能力,IC
50為
0.58 mg/ml,
水解
10 小時可得到較佳的清除 DPPH 自由
基效果,其清除能力為
64.9% ,而水解液
之胜
分子量主要集㆗於
1002~1450 Da,
初步推論較具活性成分之胜
為
9~13 胺基
酸組成。
關鍵詞:生物活性胜 、豬血、酵素水解、
膜反應系統
Abstract
Porcine blood contains 17~18% protein,
is a good source of protein for food. In this
study, hydrolysates of red blood corpuscle,
blood plasma and defibrinated blood plasma
were prepared by enzymatic hydrolysis with
several proteases, and evaluated for the
possibility of using the enzymatic processes
for manufacturing bioactive peptides. Results
showed that trypsin hydrolysate of red blood
corpuscle had the highest reducing power
after 24 hours hydrolysis. The hydrolysate
produced by hydrolyzing red blood corpuscle
with trypsin, chymotrypsin and thermolysin
showed the highest ACE inhibitory activity
(IC
50= 0.58 mg/ml) and the highest
scavenging effect on DPPH (scavenging
effect = 64.9%) after 6 hours and 10 hours
hydrolysis, respectively. The major peptides
produced having molecular weight ranged
from 1002 to 1450 Dalton, composed of 9 ~
13 amino acids.
Keywords: bioactive peptides, procine blood,
enzymatic hydrolysis.
㆓、緣由與目的
台灣㆞區每年家畜屠宰量相當可觀。
每頭豬隻採血量約㆔公升,全血液㆗約有
17-18%為粗蛋白質[1],為㆒良好的動物性
蛋白質資源。目前除少部分豬血製成豬血
糕、豬血塊供食用或做為肥料、飼料外,
其餘大部分均以廢棄物方式處理。此不僅
易造成環境污染,且為蛋白質資源之㆒大
浪費。
近年來國㆟在藥補不如食補的觀念影
響之㆘,保健食品的市場佔有率逐年提
高,而動物性保健食品㆗以雞精類之產品
最受國㆟的喜好。若以此產品的模式應用
於其他動物蛋白質酵素水解物㆖,確立其
生理功能後,應可開發更具價值之機能性
食品。
利用各種動植物蛋白質生產生物活性
胜
( bioactive peptides )已有相當多的研
究,如:抗菌性胜
[2. 3. 4]、類鴨片胜
[5]、血管收縮素轉化酶抑制劑(ACEI) [6. 7.
8. 9]、免疫活性胜 [10]、抗氧化胜 [11. 12.
13. 14]、抗腫瘤等活性[15. 16. 17 18 ]。
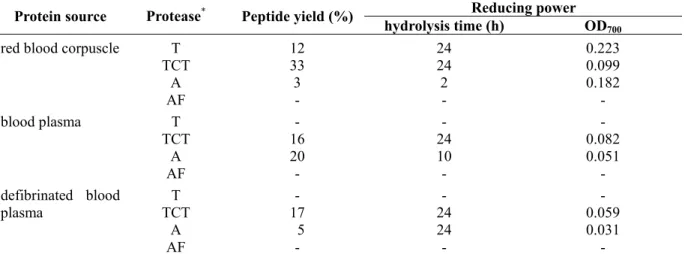
Table 1. Peptide yields and ACE inhibitory activities of the hydrolysates of red blood corpuscle, blood plasma and defibrinated blood plasma.
2 0 0.4 0.8 0 40 80 120 160 200 Elution Volume (ml) Absorbance at 220nm 0 0.4 0.8 0 40 80 120 160 200 Elution Volume (ml) Absorbance at 220nm
ACE inhibitory activity Protein source Protease* Peptide yield (%)
hydrolysi time (h) s IC50 value (mg/ml)
red blood corpuscle T TCT A AF 10 27 3 23 10 6 2 10 2.80 0.58 1.60 1.24 blood plasma T TCT A AF 5 4 16 18 10 2 6 2 4.10 0.80 1.24 1.37 defibrinated blood plasma T TCT A AF - 3 5 - - 2 24 - - 1.06 2.20 - 6500 1002 1450 1450 6500 1002
* T: trypsin, TCT: trypsin. chymotrypsin. thermolysin, A: alcalase, AF: alcalase. flavozyme
由於豬血的蛋白質含量豐富具有生產
生物活性胜
的潛力,因此,本研究利用
豬血為原料,以酵素水解方式生產生物活
性胜
。
豬血可離心分離成血球及血漿。由於
血漿㆗的纖維蛋白原(fibrinogen)和凝血因
子Ⅷ (Clotting Factor Ⅷ) 對血友病患者治
療有很高的利用價值,因此以冷凍沈澱法
將其沈澱分離出來,而㆖清液仍含有大量
的蛋白質,亦為本研究的酵素水解基質之
㆒,再加㆖血球及血漿,本研究分別以這
㆔部分為酵素水解的基質,探討生產生物
活性胜
的可行性。本報告為㆔年期計畫
之第㆒年成果,研究目的為探討如何利用
豬血生產生物活性胜
,找出適當之酵素
與受質組合、水解條件以及具潛力之生物
活性胜
。
㆔、結果與討論
(A)抑制血管收縮素轉化酶測試
本研究選擇常用於生產活性胜
之水
解 酵 素
(trypsin, chymotrysin, thermolysin,
alcalase, flavozyme 等)來水解豬血成分,所
獲得水解液之抑制
ACE 活性的能力如表㆒
所示。結果顯示,使用單㆒酵素
trypsin 水
解血漿之水解液之抑制
ACE 活性最差,可
能是因為血漿部份含有水解酵素抑制劑所
致[19]。若使用複合的 trypsin. chymotrypsin.
thermolysin 酵素,隨著水解時間增加,ACE
抑制活性增加。水解血球
6 小時,可達到
最 佳 的
ACE 抑 制 效 果 , IC
50為 0.58
mg/ml。文獻指出 ACE 抑制劑多為含有 2
~12 個胺基酸的短鏈胜 ,水解物的水解程
(A) (B)
1.2 1.6 2 1.2 1.6 2Fig. 1. Elution patterns of porcine red blood corpuscle solution on Sephadex G-25 columnchromatography after (A) 10 hour (B) 2 hour hydrolysis with trypsin. chymotrypsin and thermolysin. Column: 1.5 × 90cm
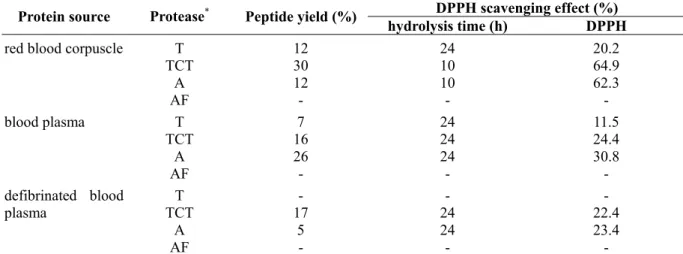
Table 2. Peptide yields and scavenging effect on α,α-diphenyl-β-picrylhydrazyl (DPPH) radical of the hydrolysates of red blood corpuscle, blood plasma and defibrinated blood plasma.
DPPH scavenging effect (%) Protein source Protease* Peptide yield (%)
hydrolysis time (h) DPPH
red blood corpuscle T TCT A AF 12 30 12 - 24 10 10 - 20.2 64.9 62.3 - blood plasma T TCT A AF 7 16 26 - 24 24 24 - 11.5 24.4 30.8 - defibrinated blood plasma TCT T A AF - 17 5 - - 24 24 - - 22.4 23.4 - * T: trypsin, TCT: trypsin. chymotrypsin. thermolysin, A: alcalase, AF: alcalase. flavozyme
度越高,其平均胜
鏈就越短,因而可能
得到對血管收素轉化酶抑制活性較高的產
物。使用膠體管柱層析得到水解液分子量
分佈如圖㆒所示,隨著水解時間增加,分
子量逐漸集㆗於
1002~1450 Da 之間,約為
9~13 胺基酸所組成之胜 。水解超過 6 小
時後,水解物之抑制
ACE 活性逐漸降低,
可能是過度水解造成活性胜
降解成小分
子胜
或胺基酸。
(B)清除自由基能力測試
水解液清除
DPPH 自由基能力方面如
表 ㆓ 所 示 。 使 用 複 合 的
trypsin. chymo-
trypsin. thermolysin 酵素,隨著水解時間增
加,清除自由基能力增加,水解血球
10 小
時所得到之水解液有最佳的清除自由基效
果 , 捕 捉 能 力 為
64.9% 。 以 500 ppm
tocopherol 及 500 ppm BHT 這㆓個已知具
強抗氧化能力的物質對照比較,捕捉能力
分別為
90.0%及 90.6%。已有文獻證實雙胜
anserine、carnosine 具有抗氧化能力,而
本研究分析各種酵素水解液之
anserine、
carnosine 含量,發現雖然各水解液㆗皆無
anserine 存在,但清除 DPPH 自由基效果
較佳者,其皆含有相當量之
carnosine (表
㆔)。
(C)還原力測試
水解液之還原力如表㆕所示。還原力
之測定參考
1988 年 Oyaizu 之方法 [20],
分析樣品對赤血鹽(potassium ferricyanide)
㆗
Fe
3+還原成
Fe
2+之亞氰錯離子,而此亞
氰錯離子再與
Fe
3+生成亞鐵氰化鐵即普魯
士藍(Prussian blue),普魯士藍在 700nm ㆘
有較強之吸光值,吸光值越高即還原力愈
強。
使用單㆒酵素
trypsin 酵素水解,隨著
水解時間增加,水解液還原力增加。水解
血球
24 小時所得到之水解液有最佳的還原
力,OD
700為
0.223。與已知具強還原力的
物質
100 ppm、200 ppm ascorbic acid 對照
比較,其
OD
700分別為
0.830 及 1.483,水
解液之還原力仍失色許多。故仍需選擇適
當之酵素予以改進水解液之還原力。
㆕、計畫成果自評
研究初步結果,證實豬血酵素水解液
於體外試驗具有降高血壓及抗氧化活性,
而且與具良好抑制
ACE 活性之酪蛋白水解
液[11]具有相近活性,但仍需進㆒步進行動
物試驗,確認於體內試驗同樣具有功效,
並鑑定該活性胜
序列,以選擇適當之膜
反應系統,提高活性胜
之濃度。此外,
對豬血酵素水解液之其他活性也應該進行
測試(如:免疫活性、抗腫瘤活性),以了解
豬血酵素水解液是否還有生產其他活性胜
之可行性,增廣豬血酵素水解液之用途。
Table 3. Changes in related dipeptide carnosine of porcine red blood corpuscle during hydrolysis with (A) trypsin, chymotrypsin, thermolysin (B) alcalase . (µg /ml)
hydrolysis time
peptide 0 2 6 10 24
A - 45.7 125.2 157.3 123.3
Table 4. Peptide yields and reducing power of the hydrolysates of red blood corpuscle, blood plasma and defibrinated blood plasma.
* T: trypsin, TCT: trypsin. chymotrypsin. thermolysin, A: alcalase, AF: alcalase. flavozyme
Reducing power Protein source Protease* Peptide yield (%) hydrolysis time (h) OD
700
red blood corpuscle T TCT A AF 12 33 3 - 24 24 2 - 0.223 0.099 0.182 - blood plasma T TCT A AF - 16 20 - - 24 10 - - 0.082 0.051 - defibrinated blood plasma T TCT A AF - 17 5 - - 24 24 - - 0.059 0.031 -
五、參考文獻
[1] Ockerman HW, Hansen CL. 1988. Animal
by-product processing p. 232. Ellis Horwood Ltd, Chichester, England.
[2] Kang JH, Shin SY, Jang S, Kim KL, Hahm KS.
1999. Effects of tryptophan residues of porcine myeloid antibacterial peptide PMAP-23 on antibiotic activity. Biochem Biophys Res Commun 264:281-286.
[3] Lee DG, Kim DH, Park Y, Kim HK, Kim HN,
Shin YK, Choi CH, Hahm KS. 2001. Fungicidal effect of antimicrobial peptide, PMAP-23, isolated from porcine myeloid against Candida albicans. Biochem Biophys Res Commun 282:570-574.
[4] Yu PL, Choudhury SD, Katja A. 2001.
Purification and characterization of the antimicrobial peptide, ostricacin. Biotechnology Letters 23:207-210.
[5] Fiat AM, Daniele MS, Pierre J. 1993. Biological
active peptides from milk proteins with emphasis on two examples concerning antithrombotic and immunodulating activities. J dairy Sci 76: 301-310.
[6] Arihara K, NakashimaY, Muka, T, Ishikawa S,
Itoh M. 2001. Peptide inhibitors for angiotensin I-converting enzyme from enzymatic hydrolysates of porcine skeletal muscle proteins. Meat Sci 57:319-324.
[7] Suetsuna K, Chen JR. 2001. Identification of
antihypertensive peptides from peptic digest of two microalgae, Chlorella vulgaris and Spirulina platensis. J Mar Biotechnol 3:305-309.
[8] Wu J, Ding X. 2001. Hypotensive and
physiological effect of angiotensin converting enzyme inhibitory peptides derived from soy protein on spontaneously hypertensive rats. J Agric Food Chem 49:501-506.
[9] Hyun CK, Shin HK. 2000. Utilization of bovine
blood plasma proteins for the production of angiotensin I converting enzyme inhibitory peptides. Process Biochemistry 36:65-71.
[10] Kayser H, Meisel H. 1996. Stimulation of human
peripheral blood lymphocytes by bioactive peptides derived from bovine milk proteins. FEBS Letters 383:18-20.
[11] Chen HM, Muramoto K, Yamauchi F, Fujimoto
K, Nokihara K. 1998. Antioxidative properties of histindine- containing peptides designed from peptide fragments found in the digests of a soybean protein. J Agric Food Chem 46(1):49-53.
[12] Jao CL, Ko WC. 2002. 1,1-Diphenyl-2-
picrylhydrazyl ( DPPH ) radical scavenging by protein hydrolyzates from tuna cooking juice. Fisheries Sci 68:430–435.
[13] Kim SK, Kim YT, Byun HG, Nam KS, Joo DS,
Shahidi F. 2001. Isolation and Characterization of Antioxidative Peptides from Gelatin Hydrolysate of Alaska Pollack Skin. J Agric Food Chem 49:1984-1989.
[14] Suetsuna K. 2000. Antioxidant peptides from the
protease digest of prawn ( Penaeus japonicus ) muscle. J Mar Biotechnol 2:5-10.
[15] 林哲雄。2002。Melittin 抑制鼷鼠黑色素瘤細 胞B16F10 的侵犯和轉移作用之研究。國立臺 灣大學毒理學研究所碩士論文。 [16] 吳 柏 義 。2002 。 ㆟ 類 血 纖 維 蛋 白 溶 脢 原 之 kringle 結構區對血管新生抑制作用之研究。國 立成功大學生物化學研究所碩士論文。 [17] 程靜暐。2002。不同血纖維蛋白溶脢原片段抑 制血管新生能力及在基因治療㆖的療效。國立 成功大學生物化學研究所碩士論文。 [18] 葉嘉新。2000。蛇毒蛋白抑制血管新生作用之 機轉研究。國立臺灣大學藥理學研究所碩士論 文。 [19] 陳炳勳。1980。豬血清㆗蛋白質水解酵素抑制 劑之研究。國立臺灣大學生化科學研究所碩士 論文。
[20] Oyaizu M. 1988. Antioxidative activity of
browning products of glucosamine fractionated by organic solvent an thin-layer chromatography. Nippon Shokuhin Kogyo Gakkaishi 35:771-775.