國
立
交
通
大
學
物理研究所
碩
士
論
文
不需標定、即時的液態 放電紡絲纖維一氧化氮感測器
Real-time and indicator-free detection of aqueous nitric
oxide with electrospun fibrous membrane
研 究 生:吳孟哲
指導教授:孟心飛 教授
洪勝富 教授
不需標定、即時的液態 放電紡絲纖維一氧化氮感測器
國立交通大學物理研究所碩士班 學生:吳孟哲 指導教授:孟心飛教授 洪勝富教授摘要
一氧化氮(NO)是一種在人體中扮演重要腳色的自由基,可以使血管周圍的平滑 肌舒張、控制血壓、抑制血小板聚集,並且在神經系統中扮演著訊息分子的角色。 而發展一種可以在細胞外、直接、即時的一氧化氮(NO)感測器是必要的,該感測 器可以幫助我們了解一氧化氮(NO)釋放的機制。 放電紡絲(electrospinning)在 20 世紀初就已經被發展出來了,那是一種可以製造 出精細纖維的方法,可以製造出小於微米,甚至奈米尺寸的連續纖維。 我們利用放電紡絲(electrospinning)製造一種在一氧化氮(NO)感測器上的奈米纖維 感測層,該感測層在液態環境下可以即時感測且不需標定。這種奈米纖維是由 NO probe ZnC1 (11,16-Bisphenyl-6,6,21,21-tetramethyl-m-benzi-6,21porphodimetheno-chloro-Zinc(II))和 高分子材料PAN(polyacrylonitrile) 組成的 ,它的直徑大約在 550 奈米左右。由於 奈米纖維感測層的表面積相當大,反應時間也相對快及敏感,反應時間只需要 6 秒鐘。最低可以偵測到濃度10-9莫耳的一氧化氮(NO)。而且奈米纖維感測層也顯 示出它具有重複利用性、單一選擇性以及在不同PH值中的穩定性。Real-time and indicator-free detection of aqueous
nitric oxide with electrospun fibrous membrane
Student:Meng-Che Wu Advisors:Prof. Hsin-Fei Meng Prof. Sheng-Fu Horng Institute of Physics
National Chiao Tung University
Abstract
Nitric oxide (NO) is a free radical playing important roles in the human body. NO relaxes the smooth muscle in the walls of the arterioles, regulates the blood pressure, and inhibits the aggregation of platelets.1–4 It also serves as a signaling molecule in the nervous system.5 Direct and real-time detection of NO outside the cell helps to unveil how NO relates to certain physiological function.
Since the beginning of 20 century, electrospinning had been developed
Electrospinning is a process, which produces superfine fibers. Electrospinning is able to produce continuous fibres from the submicron diameter down to the nanometre diameter.
A sensing fibrous membrane prepared by electrospinning is demonstrated for real-time and indicator-free detection of nitric oxide (NO) in aqueous solution. The fibers with diameters of 550 nm are composed of NO probe
11,16-Bisphenyl-6,6,21,21-tetramethyl-m-benzi-6,21-porphodimetheno-chloro-Zinc(I I) and host polymer polyacrylonitrile. The high surface area of the sensing fibrous membrane gives rapid response in 6 seconds and high sensitivity, and NO
concentration detection limit is estimated to be 10−9 M. The sensing fibrous membrane also shows good reversibility, selectivity, and stability in various pH values.
致謝
時間過的很快兩年的實驗室生涯一下子就過去了,我也從剛進實驗室的菜鳥到 現在再寫畢業論文了,在這兩年內除了學習到很多知識外,我也學到很多做人的 道理。 首先要感謝的是我們實驗室的大家長孟心飛教授和洪勝富教授,孟心飛教授是 一個相當帥氣的教授,我永遠都記得我第一次進去教授辦公室的時候,整個被嚇 到不敢相信有這麼帥的教授,而洪勝富教授是一個學問相當淵博的人,常常在他 的身上學習到很多不知道的領域,感謝他們給我這個學習的機會。 再來我要感謝的是實驗室的學長姐,感謝強哥,您總是給我很多建議給我很多 方向,讓我的實驗可以順順利利的,感謝俊宇,俊宇在這兩年內給我我很多幫助, 實驗器材有問題找俊宇就對了!感謝韻如學姐,你除了是實驗室最正的女生外, 也給了我很多幫助,信榮學長、家銘學長、建成學長感謝你們那麼照顧我。 感謝怡成、吉米、牛哥在實驗室最後的一年,陪我最多的就是你們了,我們畢 業後還要一起打牌喔!XD還有要感謝振豪、輝哥、唐牛、正忠在這兩年的時間 裡我們互相學習,感謝你們告訴我很多我不知道的事情,我在你們身上學到很 多。感謝學弟小胖我不會忘記我們一起喝酒、一起做菜的日子。還有野人、季老 師很多事情沒有你們是作不到的。感謝一起打球的同伴,沒有球打的日子我無法 想像。 最後我要感謝我的好朋友們,冠偉每當我不知道該怎麼辦的時候我第一個想到 的一定是你,橘子皮陪我度過很多無聊的時光,弱智你總是挺我!李碧旋沒有妳 那個暑假我不會過的這麼快樂,小頡你知道的,那是我最快樂的一段時光你對我 來說永遠都是那麼重要。 要感謝的人這麼多,那就謝天吧。目錄
中文摘要 ………. i 英文摘要 ……….. i i 致謝 ……….. iii 目錄 ………... i v 圖目錄 ……… viChapter1 緒論
………. 1-1 前言……….. 2 1-2 研究分子…………... …………... …………... …………... ……… 4 1-2-1 發現過程與三大實驗... 5 1-2-2 NO 在體內扮演的生理功效………...………. 9 1-3 研究動機………. 11 1-4 論文架構………. 11Chapter2 實驗原理
……….. 12 2-1 發光原理……… 13 2-2 NO Probe 和 NO 的反應機制……… 14 2-3 放電紡絲(electrospinning)的原理……… 17Chapter3 實驗製程、量測與材料
……… 22 3-1 NO probe 固態薄膜製程……… 23 3-2 量測……… 25 3-3 材料介紹……… 283-4 微流管(Microfluidic system)的製作和量測……… 32
Chapter4 實驗設計與結果
……… 36 4-1 NO probe 之基本特性………... 37 4-1-1 ZnC1……….. 37 4-1-2 DAQ………... 42 4-2 放電紡絲(electrospinning)纖維膜之製作………. 46 4-2-1 放電紡絲(electrospinning)之使用……….. 46 4-2-2 放電紡絲(electrospinning)纖維膜和 NO Probe 的結合…….. 48 4-3 放電紡絲(electrospinning)纖維膜和旋轉塗佈膜(spin)之比較… 504-3-1 ZnC1 fibrous membrane 和 spin film 的比較……… 50
4-3-2 DAQ fibrous membrane 和 spin film 的比較………. 53
4-4 放電紡絲(electrospinning)纖維膜之基本特性………. 56 4-4-1 放電紡絲(electrospinning)纖維膜之濃度階梯量測………… 56 4-4-2 放電紡絲纖維膜之可逆性反應(reversibility)測試………… 58 4-4-3 放電紡絲纖維膜 PH 值及 NAP 測試……… 60 4-4-4 在生理環境下 ZnC1 對 NO 的反應……… 63 4-4-5 低濃度 SNAP 對 ZnC1 PL 的變化……… 65 4-5 濃度極限及時間解析……… 67 4-5-1 濃度極限………. 67 4-5-2 時間解析……… 69
4-6 微流管實驗……… 73
Chapter5 結論
……… 76Reference
………. 77圖目錄
圖 1-1 血糖檢測計和採血器……… 2 圖1-2 Biosensor 的基本原理……… 3 表 1-1,1998 年諾貝爾生理醫學獎三大得主……… 4 圖 1-3,Furchgott’s 三明治實驗……… 5 圖1-4,血管內皮 NO 作用機制……… 6 圖 1-5,Ignarro's Spectrophotometry……… 7 圖 1-6,NO 在體內負責的八大工作……… 8 圖 1-7,NO 在體內扮演的生理功效……… 8 圖 2-1 電子躍遷圖……… 13 圖 2-2 入射光吸收的可能情況……….. 14 圖 2-3能帶圖……….. 14 圖 2-4 半導體材料中能量對能態密度的關係圖……….. 16 圖 2-5 常見的o-phenylenediamine NO indicators………….……….. 17圖 2-6DAF-2 和 NO 反應形成DAF-2 triazole (DAF-2 T) …….……… 18
圖2-7 DAQ和NO反應變成DAQ-TZ………... 18 圖2-8 ZnC1中間的Zinc和NO產生弱鍵結或作用力而造成PL下降……... 18 圖 2-9 electrospinning 示意圖………... 19 圖 2-10 放電紡絲(electrospinning)的基本架構……….. 20 圖 2-11 使用固定集合器時,奈米纖維呈現隨機不規則排列之情形 21 圖 2-12 使用旋轉盤集合器時,奈米纖維呈現平行規則之排列…. 21
圖 3-1 Electrospinning 示意圖………. ………. 23 圖 3-2 待測物在 f4500 裡面的架構………. ……….. 25 圖 3-3 CCD 量測的架構………. ……….………. 26 圖 3-4 PD 量測架構………. ……….……….. 27 圖 3-5 Polyacrylonitrile. ……….………. 28 圖3-6 ZnC1……….………. 28
圖 3-7 ZnC1 之 UV、PL 圖(from Prof.Hung) ……… 29
圖 3-8 DAQ 以及其和 NO 反應後的 DADAQ-TZ……… 29 圖 3-9 DAQ 和 NO 反應……… 30 圖 3-10 SNAP………. 30 圖 3-11 NAP……… 30 圖 3-12 NoNoate……… 31 圖 3-13 Microfluidic system 圖案示意圖……… 32 圖 3-14 PDMS 通道示意圖……… 32 圖3-15 PDMS 通道………. 33 圖3-16 Microfluidic system 量測之架構……… 34 圖 3-17 Microfluidic system 改善示意圖……… 35 圖 3-18 Syringe pump 針筒式幫浦……… 35
圖 4-1 ZnC1 溶液之 UV、PL 圖(from Prof.Hung)... 37
圖 4-2 ZnC1 溶液加入 SNAP 造成其 UV 吸收光譜改變... 39
圖 4-3 ZnC1 溶液加入 SNAP 造成其 PL 有 shift 以及 decay 之現象 40
圖 4-4 以 NO 氣體直接灌進 ZnC1 溶液也會改變其 UV 吸收光譜 40
圖 4-5 以 NO 氣體灌進 ZnC1 溶液,亦造成其 PL 下降... 41
圖 4-6 DAQ@DMSO 溶液加入 SNAP 造成其 PL 下降... ... 42
圖 4-7 SNAP 造成 DAQ 在 550 左右的吸收消失... ... 43
圖 4-9 NO 氣體造成 DAQ 溶液 PL 下降(用 545nm 的光激發) . ... 44 圖 4-10 NO 氣體亦造成 DAQ 溶液 550nm 左右之吸收消失... ... 45 圖 4-11 electrospinning 的基本架構... 46 圖 4-12 其單一條絲直徑約為600-800nm 之間... 47 圖 4-13 圖4-13 添加 ZnC1 的纖維膜... ... .... 48 圖 4-14 其絲的直徑~800nm 左右... ... 48 圖 4-15 添加 DAQ 的纖維膜... ... 49 圖 4-16 其絲的直徑~~~800nm 左右... ... 49 圖 4-17 纖維狀結構使反應很快... ... 51 圖 4-18 非纖維狀結構需要較長時間才可達到平衡... 51 圖 4-19 DAQ 纖維膜和 NO 反應造成其 PL 下降(545nm 激發) ... 54 圖 4-20 DAQ 一般膜和 NO 反應造成其 PL 下降(545nm 激發) ... 54 圖 4-21 ZnC1 纖維膜的 PL 會隨著 SNAP 濃度增加而下降... 57 圖 4-22 ZnC1 纖維膜 Reversibility 測試... 59 圖 4-23 PH 值和 NAP 並不會影響 ZnC1 的 PL... 61 圖 4-24 PH 值和 NAP 並不會影響 DAQ 的 PL... 61
圖 4-25 在 culture medium 的環境下,ZnC1 亦可以偵測到 NO... 64
圖 4-26 濃度為 0.0001625M 的 SNAP,亦可以明顯的造成 ZnC1 的 PL 下降 66 圖 4-27 極限濃度測試... ... 68 圖 4-28 暗電流和未放 ZnC1 纖維膜的電流... ... 70 圖 4-29 在加入 0.05MSNAP 後 PD 的光電流下降非常快... 71 圖 4-30 纖維膜和一般膜的時間解析... ... 71 圖 4-31 纖維膜可以立即反映出 SNAP 濃度的改變,而一般膜不能 73
Chapter1
緒論
1-1 前言
1-2 研究分子
1-3 研究動機
1-4 論文架構
1-1 前言
什麼是biosensor? biosensor就是生物感測器[1、2]。生物感測器定義為"使 用固定化的生物分子(immobilized biomolecules)結合換能器,用來偵測生物體 內或生物體外的環境化學物質或與之起特異性交互作用後產生回應的一種裝 置"。這種裝置在現在這個世界所扮演的腳色越來越重要!其最明顯的例子就是 血糖檢測器。我們只要在家裡紮自己一針,在短短幾秒內即可得知自己的血糖值。 (a) (b) (c) (d) 圖1-1血糖檢測計和採血器 而生物感測器的發展可追朔到Clark 與Lyon 於1962 年提出酵素電極作為第 一代生物感測器的概念後,便掀起一陣漩風, 如Yellow Springs Instrument 公 司於1979 年開發的第一個血液葡萄糖檢測的生物感測器。MediScense 公司於 1987~1988 年起相繼推出家用型及攜帶式(信用卡型及筆型)的血糖檢測器。然而 1980 年代之後,開始投第二代生物感測器的開發,在概念上,以抗體或受體蛋 白作為固定化的生物分子以開發,而在訊號換能器方面朝向多元化,選擇以場效 半導體(FET) , 光纖式光學感測器(Fiber-Optic Sensor, FOS),壓電晶體 (PZT),表面聲波器(SAW)等作為訊號換能器。而第二代生物感測器多仍在實驗室階段,尚未達技術成熟的商品。第三世代的生物感測器定位在更具攜帶式,自動 化,與即時測定功能,預測在二十一世紀初期可以達到上市目標。至於第四世代 具偵測/信號輸出/控制/自我組合/自我修補與複製等功能的生物感測器將於何 時出現,則尚無法預估。 生物感測器的分類是依據感測器的固定化的生物分子、訊號換能器、固定化的 生物分子與待測生物樣本的結合方式而有三種分類。(一)依據固定化的生物分子 分類:分為抗體、抗原、酵素、核酸、組織部份或個體細胞。(二)依據訊號換能 器分類:(1)電化學生物感測器(Eletrochemical Biosensor) (2)離子選擇性 場效電晶體(ISFET, Ion Sensitive Field Effect Transistor) 3)壓電晶體生 物感測器(Piezoelectric quartz crystal biosensor) (4)光纖生物感測器 (Fiber-optic biosensor) (三)依據固定化的生物分子與待測生物樣本的結合方 式:(1)生物親和性感測器(Bioaffinity sensors) (2)代謝感測器(Metabolism sensor)或生物催化型感測器(Biocatalytic biosensors)
1-2 研究分子
在本論文所研究偵測的分子為一氧化氮(Nitric Oxide,NO)。
NO[3、4]是空氣污染的主要成分,也是酸雨形成的主要因子,但NO卻也 被發現可執行重要的生化功能。此發現是生物學上一項重要的新發現,發現者因 此也被獲頒 1998 年諾貝爾生理醫學獎,如表 1-1。與其他訊息傳導物質不同的 是,NO非常不穩定,以至於它在 10 秒之內即會被完全代謝分解掉。 是含一未配對電子的自由基,十分活躍不穩定,半衰期約為3~5秒, 約10秒即會被氧化成亞硝酸鹽(nitrite,NO2-)和硝酸鹽(nitrate,NO3-)。
名字 Robert F. Furchgott Ferid Murad Louis J Ignarro
出生 1916 USA 1941 USA 1936 USA
研究 部門
紐約布魯克林的 SUNY Health Science Center
藥理部門 德州大學基礎藥學研 究部門 UCLE School of Medicine 的分子及藥 理部門 貢獻 乙醯膽鹼於體外可藉由 內皮細胞分泌 EDRF 而 使血管平滑肌舒張 硝基化合物會釋放 NO 而使血管平滑肌 舒張 1986 年,與 Furchgott 同時提出 EDRF 即是 NO 表 1-1,1998 年諾貝爾生理醫學獎三大得主
發現過程與三大實驗 (A) Robert F. Furchgott
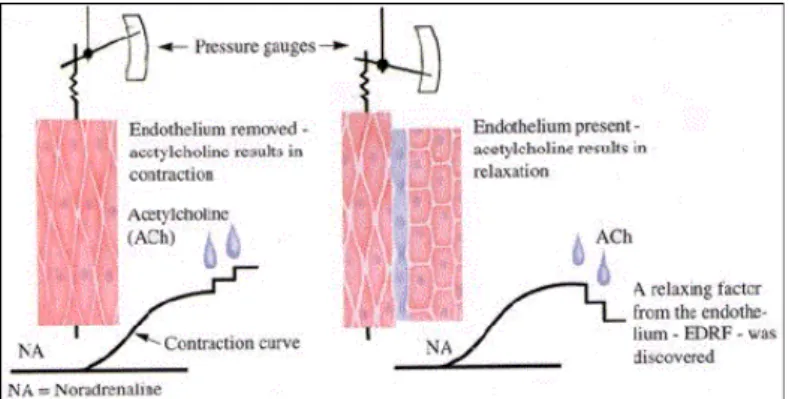
乙醯膽鹼(acetylcholine)在當時已經被證實在動物活體內可引發顯著的血管放 鬆;在離體血管實驗中,乙醯膽鹼有時候會造成血管平滑肌放鬆,但大部分卻是 造成血管肌肉收縮。Furchgott 於是開始懷疑"血管的「內皮細胞完整或損傷」 決定「血管壁收縮或擴張」"。 1978 年 5 月 7 號,Furchgott的技術員David Davidson利用血管環的方式以乙 醯膽鹼為刺激劑,測試藥物對血管的舒張反應。由於David Davidson不小心加錯 藥的順序,意外發現乙醯膽鹼可導致血管擴張。經過小心查證後,Furchgott發現 血管收縮是因為在血管處理過程中將血管內皮破壞造成的。當血管內皮完好無損 時,乙醯膽鹼只能擴張血管。 1980 年 11 月,Furchgott 在自然期刊 (Nature)提出「三明治(sandwitch)」實 驗,如圖 1-1 所示。他以兩組不同的動脈血管做實驗,一組(左圖)將血管內內皮 細胞移除,一組(右圖)維持原本的內皮細胞層。發現當受正腎上腺素(NA)刺激 時兩組動脈血管皆收縮,但在加入乙醯膽鹼(ACh)後,只有具有內皮細胞的血管 肌肉(右圖)舒張。因此 Furchgott 推斷血管內皮細胞可製造一個不明的訊息傳導 因子 --「內皮衍生放鬆因子」(EDRF=endothelium derived relaxing factor),而 使血管平滑肌細胞放鬆,造成血管擴張。
(B) Ferid Murad
Ferid Murad 本人是臨床醫生又是藥理學研究者,他主要研究工作是分析硝化
甘油與相關的血管擴張藥物是透過何種機制去發揮效果。
1970 年代,Ferid Murad 在維吉尼亞大學致力於一氧化氮 (NO,nitric oxide) 和 cGMP (環鳥嘌呤核甘單磷酸鹽) 當作訊息傳導 (signal transduction) 的研 究。 由於 guanylate cyclase 可將 GTP 轉化為 cGMP,因此他推測任何可以活化 guanylate cyclase 的酵素皆可調控細胞內 cGMP 含量,進而影響細胞功能。在分 離酵素的過程中,他發現酵素除了存在在細胞膜中,也存在於細胞漿中。細胞膜 中的酵素可藉由刺激物和受器結合而活化,那麼細胞漿中的酵素是如何受到活 化?
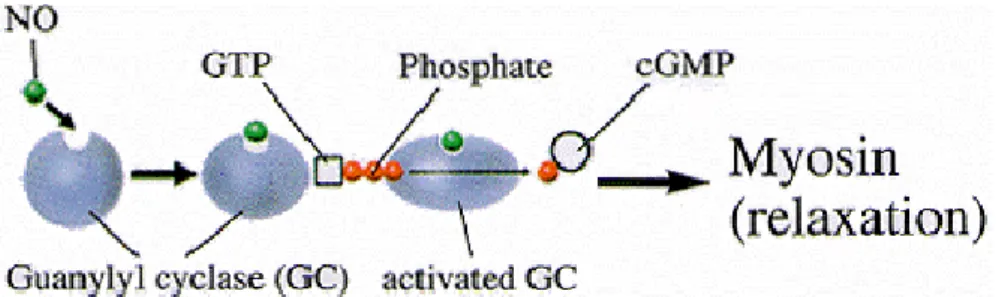
已知肌凝蛋白輕鍵(myosin light chain)之去磷酸化會導致平滑肌舒張。1977 年,Ferid Murad 經由實驗證明,含硝基之藥品(包括三酸甘油酯)會釋放 NO 使 細胞漿中的 guanylate cyclase 活化,促使 GTP 轉化生成 cGMP,cGMP 使肌凝蛋 白輕鍵去磷酸化,造成血管平滑肌舒張,如圖 1-2 所示。同時 Ferid Murad 也發 現乙醯膽鹼會刺激血管內皮細胞產生內生性 NO。
(C) Louis J Ignarro
在 Furchgott 和 Ferid Murad 陸續發表他們的理論後,Ignarro 也開始投入 EDRF 的研究。
Ignarro 收集了乙醯膽鹼刺激胸主動脈血管環後所遺留之培養液(含
EDRF),再觀察此一培養液對 guanylate cyclase 之活化作用。當這培養液加入各 式氧化、還原及抗氧化劑後,guanylate cyclase 的活化程度會被影響。Ignarro 進 一步測量此培養液的 NO,發現 NO 的產生量與 guanylate cyclase 活化量成正比, 此實驗證明了EDRF 即是 NO。
1986 年,Ignarro 藉由「分光術(spectrophotometry)」實驗(如圖 1-3 所示)提 出:
(1) 內皮衍生放鬆因子 EDRF 即是 NO。
(2) 人類首次發現一個氣體在生物體內可扮演一個訊息傳導因子的角色。
兩組實驗顯示出 EDRF 和 NO 的最大吸光值完全相同,證明 EDRF = NO。
血紅素中暴露在內皮細胞中 (內皮細胞受到刺激產生 EDRF)
血紅素
血紅素直接暴露於 NO 中
NO 在體內扮演的生理功效 NO 在人體負責的工作大約有八大項,如圖 1-6、圖 1-7 所示。 抗發炎 中樞神經系統 泌尿系統 心血管 呼吸系統 消化系統 主體防禦 其他
NO
圖 1-6,NO 在體內負責的八大工作 圖 1-7,NO在體內扮演的生理功效6(A) 心血管疾病(Cardiac Vascular Disease)的防止:
NO 可舒張血管,有利預防血脂肪沈澱物蓄積在血管內壁,造成動脈硬化或 阻塞、高血壓、中風、心絞痛等疾病。
(B) 中樞神經系統(Central Nerve System):
NO 可作為神經 胞間訊息,促進神經細胞之間的溝通, 與大腦學習、記憶、睡眠、協調等中樞有密切關聯性。 (C) 呼吸系統: 許多肺部疾病如氣喘、肺高壓及肺栓塞,經由吸入 NO 可以用來改善肺泡氣 體交換及局部血液循環功效。 (D)免疫系統(Anti-Inflammation): 當體內有 噬細胞殺死細菌、病毒、寄生蟲等感染,亦 可刺激胸腺產生 Killer T lls 免疫殺手細胞,提升抵抗力。 (E)消化系統: NO 可以促進腸胃蠕動及代謝。 (F) (cancer): 白血球會使用 NO 去對抗癌症細胞,因為 NO 會引起 Apoptosis(programmed cell death,計畫性細胞死亡)。 (Anti-Inflammation) NO 能舒緩發炎與風溼症,對於肌腱關節的發炎與疼痛,有很好的消炎緩解 作用。嗎啡的療效即是產生 NO,但 NO 本身不會使病人嗜癮,是藥物作用的有 效部份。 (G)陽萎:
NO 可以擴張陰莖內動脈管壁而引起勃起。PDE5 (phosphodiesterase type 5 第五型磷酸二脂酶) 會促進陰莖海綿體 cGMP cGMP 的量被消耗而不足時,陰莖將軟攤無法勃起。威而鋼藉著抑制 PDE5 來 傳導因子,傳遞神經細 感染時,NO 可協助巨 -ce 癌症 (F)抗發炎 : 的代謝消耗,當陰莖海綿體
減少陰莖海綿體 cGMP 的代謝消耗以增強 NO 的功能,而促進陰莖勃起。然而, 如果不能在陰莖海綿體製造足夠的 NO 或 cGMP,再多的威而鋼也無法使陰莖勃 起。
1-3 研究動機
一氧化氮(NO)在人體中扮演的腳色相當重要,人體中一氧化氮(NO)的含量往 康有著相當的關係。目前市面上還沒有偵測一氧化氮的生物感 於共軛高分子可大量合成材料和製程簡單優點,因此我們期待做出可 時偵測 NO 濃度變化、用完即丟的固態 NO sensor。此固態 NO Sensor 將是一 個將 前的研究中我們已經證明我們的 NO probe(ZnC1)固態膜會和 NO 反 應而降低其 PL。所以本論文討論的重點是如何改善我們既有的 NO probe(ZnC1) 固態 在第一章內先簡單介紹生物感測器的發展以及介紹一氧化氮的重要性,第二 章內介紹螢光分子發光原理以及放電紡絲(electrospinning)的基本原理,第三 章簡往跟一個人健不健 測器被發展出來,我們在測量NO濃度只能採用化學發光法(chemiluminescence), 即NO與O3結合後,會轉變為NO2和O2並釋放出光子,機器偵測吸收光強度,可算出
NO濃度。然而此方法無法做到即時量測細胞釋放NO濃度變化,而且它還需要龐大 的光學儀器。所以發展一種可以在體外,正確、即時的一氧化氮(NO)感測器是必 要的。 由 即 NO probe(會與 NO 分子反應的材料)、高分子有機發光二極體 PLED、共 軛高分子光偵測器 OPD 做在同一 substrate 上的整合型元件。並且可以應用在生 物實驗上。 在以 膜,進而增進我們的一氧化氮(NO)感測器性能,使其可以使用在生物實驗上。
1-4 論文架構:
單介紹實驗製程、量測架構和使用的材料,第四章則是實驗的設計和結果, 最後第五章是總結和未來的展望。Chapter2
實驗原理
2-1 發光原理
2-2 NO Probe 和 NO 反應的機制
2-1 發光原理:
在這裡我們討論的放光原理只有關於光激發光(photoluminescence) [5、6 ]。 光激發光(photoluminescence) 是指物質吸收光子(或電磁波)後重新幅射出光 子 (或電磁波)的過程。從量子力學理論上,這一過程可以描述為物質吸收光子 激發到較高能级的激發態後返回低能態,同時放出光子的過程。光激發光是多種 形式的螢光(Fluorescence)中的一種。 光激發螢光,牽涉到一個由電磁(Electro-Magnetic) 輻射激發的系統,在分 類上是屬於光學發光的技術。當入射光(電磁輻射) 照射在試片上時,導致電子 被升高至激發態,描繪如圖2-1,典型的能帶躍遷過程。當激態電子返回初始能 態時,它會產生一個光子(能量h PL),也可能產生許多的聲子(能量 h phonon)。由能量守恆,可將其表示為方程式(1)。圖2-1電子躍遷圖
發光可以當做是穩態的現象,試片受到激發源影響而連續地發出光來。在前述 的過程,首先是入射光的吸收,如圖2-2,這和激發光子的波長(能量) 有關,故 材料的吸收和激發光源的波長有關。圖 2-2 入射光吸收的可能情況 一旦吸收了入射光之後將電子激發到更高的能態,電子將會釋放到較低的能態。 在釋放中帶有不同的過程,可被分類為輻射過程(如光激發螢光),或非輻射過程 (如聲子放射,缺陷捕捉,或歐傑效應)。 圖2-3能帶圖:(a),(b)光吸收過程與(c),(d)光激發螢光。圖(b)中指光吸收過程需要光子 和聲子。圖(c)和(d)呈現除了光子放射外(PL),聲子的放射是會發生的,因為和光激發的長
度有關,另外,對間接能隙(d)而言,聲子的放射為了動量守衡。 一般而言,在發光產生之前,較高能量(較短波長) 激發的光子導致較多的聲 子射出。同樣地,較低的激發能量傾向導致較少的聲子射出。如果激發的能量小 於基態和第一激發態之間的能量差時,將沒有光被吸收,也就沒有光激發螢光。 前述的電子圖無法充分地解釋半導體結構中許多光激發螢光的特性。較好的解釋 是將吸收光想成價帶至導帶間的轉變。放射必需是電子從導帶的最小值移動到價 帶的最大值。對於直接能隙和間接能隙材料的光吸收情況如圖2-3(a,b) 所示。 導帶和價帶相關聯的自由載子,分別是電子和電洞。事實上,光激發螢光(如圖 2-3c,d) 可以想成是半導體中導帶的電子和價帶的電洞進行輻射復合所致。當激 發的能量小於能隙的能量時,光吸收情況將不會發生。圖2-4是典型半導體中導 帶和價帶的電子能態密度。在曲線(b) 中,一個價帶中的電子吸收一個光子後被 激發到導帶中。激發的光子可能經由聲子放射,部分釋放能量至導帶中較低能 態。之後,如曲線(a),導帶中的電子釋放回價帶後,放出一個光子。光激發螢 光光譜可以包含介於Eg,r 和Eg,o 間的光子能量,這是由於每一個發出的光子必 須來自佔滿電子能態層與導帶最低層之間。然而光吸收情況,由於能量可以大於 Eg,o。因此,由於電子和電洞在導帶和價帶分佈的關係,我們預期用比能隙Eg 更低波長的光激發可看見發光。
圖2-4半導體材料中能量對能態密度的關係圖。圖中呈現發光(a) 與吸
收(b) 的轉變過程。
2-2 NO Probe 和 NO 反應的機制
目前醫學上測量NO濃度是採用化學發光法(chemiluminescence), 即NO與O3結
合後,會轉變為NO2和O2並釋放出光子,機器偵測吸收光強度,可算出NO濃度。
然而此方法無法做到即時量測細胞釋放NO濃度變化,而且它還需要龐大的光學 儀器。
利用螢光顯微鏡來偵測NO是一種較新的技術,因為NO本身並不會發光,而使
用會和NO結合而改變其螢光特性的NO Probe就可以解決這個問題了。在這裡我們 將會說明一些NO Probe和NO反應的機制。
o-phenylenediamineNO Probe 是最常被使用的NO Probe。它就是使用
o-phenylenediamine 和NO作反應而命名,當o-phenylenediamine會改變其π鍵的共
振進而改變其發光特性[7-10
]。
圖2-6DAF-2和NO反應形成
DAF-2 triazole (DAF-2 T)
圖2-7 DAQ和NO反應變成DAQ-TZ
N N N Zn Cl而ZnC1和NO的反應機制,推測為NO 跟中心Zinc 產生弱鍵 結或作用力 造成被激發的電子以其他方式釋放能量而非螢 光方式,造成其PL的下降。 圖 2-8 ZnC1 中間的 Zinc 和 NO 產生弱鍵結或作用力 而造成 PL 下降
2-3 放電紡絲(electrospinning)的原理
放電紡絲(electrospinning)是一個在20世紀初就發展出來的技術,簡單的來 說就是一種利用靜電力製造出纖維的方法[11-14 ]。 放電紡絲(electrospinning)的基礎是在於兼具黏著性與伸縮性的溶液。如圖 2-9當電場強度逐漸增加後,其在毛細管尖端之半球形流體表面延伸形成圓錐狀 (Conical Shape)稱之為泰勒圓錐形(Taylor Cone);再增加電場強度,若達 到某臨界值,其靜電排斥力超過流體表面張力值時,Taylor Cone尖端之帶電荷 流體產生噴射現象,而此高分子溶液之放電噴射是一種掃塗行程,在這過程中須 使溶劑蒸發固化,留下無規則排列帶電荷之高分子奈米纖維在金屬集合器上。在 這裡黏著性與伸縮性扮演著重要的腳色,如果你的溶液並不存在著黏著性與伸縮 性的話,當排斥力大於溶液的表面張力的時候,就好像一直往氣球裡面充氣,而 使氣球爆開來一樣,只會胡亂噴出一些溶液。而如果你的溶液兼具黏著性與伸縮 性的話,就好像在輪胎扎一個洞一樣,裡面的氣體(溶液)就會連續的噴出。 圖 2-9 electrospinning 示意圖圖 2-10 放電紡絲(electrospinning)的基本架構,由溶液、power supply 和 Collector 組成。 如圖 2-9 所示,將高分子溶液或熔融體充填入玻璃量管(Pipette)內,一邊連 接喂入注射器(Syringe),而計量泵浦(Metering Pump)連結注射器之活塞 (Plunger),使之產生固定的壓力與流量。噴射驅動力來自高壓電源,其一端 線浸沉於流體中,而高壓電源可提昇至 30kV,且可變換正或負極之裝置。若調 整流量與電場強度大小,則可控制紡絲條件。 如圖 2-11 所示,為使用固定集合器時,奈米纖維呈現隨機不規則排列之情 形;如圖 2-12 所示,則為使用旋轉盤集合器時,奈米纖維呈現平行規則之排列。 因此,不同設備條件其所生成之纖維網膜亦異,尤其是如何快速大量地、穩定地 量化之設備乃是當務之急。
圖 2-11 使用固定集合器時,奈米纖維呈現隨機不規則排列之情形
Chapter3
實驗製程、量測與材料
3-1 NO
probe固態薄膜製程
3-2 量測
3-3 材料介紹
3-4 微流管(Microfluidic system)的製作和量測
3-1 NO
probe固態薄膜製程
NO probe 固態薄膜的製作發法分成兩種:一種是旋轉塗佈而另一種是放電紡絲 (electrospinning)。 I 溶液配置: 在這裡我們利用二甲基亞碸(Dimethyl sulfoxide或DMSO)作為我們的溶劑。其 為一無色液體,並為重要的極性非質子溶劑。它可與許多有機溶劑及水互溶。我 們利用它同時溶解PAN (polyacrylonitrile Sigma Aldrich, Mw = 150, 000)和NO probe (ZnC1、DAQ)。PAN溶在DMSO的重量百分比為 10%,而PAN和ZnC1 的重量比為 25 比 1。
II NO probe 固態成膜:
(A) 旋轉塗佈法(spin coating):
將泡好的溶液滴在欲成膜之乾淨白玻璃上,以旋轉塗佈法(spin coating)成膜,轉 速為 1000rpm 300sec,甩完後將之加熱 120℃約莫 60 秒。其膜後約為 10*10-6
m。 (B) electrospinning:
將溶液吸入玻璃針筒後加入電壓(~10KV),利用靜電利產生排斥力,當排斥力大 於表面張力時,溶液將會噴出成絲(polymer jet),然後在白玻璃上形成纖維膜 (randomly oriented nanofibers),其特性為表面積相當大。
electrospinning 的條件為: 溶液流速 1 ml/hr、針頭和白玻璃距離 5cm 、 電 壓 10KV。
3-2 量測
我們在這裡使用了很多不同方法去量測 ZnC1 PL 的變化,以下將會介紹各種量 測的架構。 (1) f4500 量測: 此量測法是直接利用 PL 量測機台 F4500 直接量測。其量測優點 在於穩定(整個量側物在一個黑色鐵箱子裡面)、操作方便、可以看到整個光 譜、可以使用不同波長的激發光,而且缺點為解析時間相對較長(1 分鐘)。PAN:ZnC1 film
石英槽
1ml DI water
Incident light
Emitted light
PAN:ZnC1 film
石英槽
1ml DI water
Incident light
Emitted light
圖 3-2 待測物在 f4500 裡面的架構(2) CCD 量測:此量測法是在光學桌上,利用雷射激發 ZnC1,在用 CCD 量測其 PL 變化。其優點在於時間解析時間相對較短(~10 秒)、可以看到整個光譜。 缺點在於架設時間長、較不穩定。 CCD
fiber
Quartz
Incident light
Laser 405nm
Emitted light
NO donor
Lens CCDfiber
CCDfiber
Quartz
Incident light
Laser 405nm
Emitted light
NO donor
Lens 圖 3-3 CCD 量測的架構(3) PD 量測: 此量測法是在光學桌上,利用雷射激發 ZnC1,在利用 PD 將 PL 光 訊號轉成電訊號。其優點在於時間解析最快(~1 秒)缺點是不能看到光譜、較 不穩定、由於其只會將光轉變成光電流(沒有選擇性),所以需要利用 P3HT filter 將激發光給濾掉。 PD
fiber
Quartz
Incident light
Laser 405nm
Emitted light
NO donor
P3HT Lens P3HT PDfiber
PDfiber
Quartz
Incident light
Laser 405nm
Emitted light
NO donor
P3HT P3HT Lens P3HT P3HT 圖 3-4 PD 量測架構3-3 材料介紹
(1) Polyacrylonitrile(PAN) 聚丙烯:其分子式為 ( 是一種碳纖維的材料,由於它可溶在 DMSO 且它溶解後黏 滯力相當大可用於 electrospinning,亦可增加 ZnC1 分子 離以減少其 self quench。 CH3N)n 間距 圖 3-5 Polyacrylonitrile 我們使用的是從 SIGMA 買的其性質為:mol wt average Mw 150,000 (Typical)
refractive index n20/D 1.514
transition temp Tm 317 °C
Tg 85 °C
density 1.184 g/mL at 25 °C(lit.)
(2)ZnC1(11,16-Bisphenyl-6,6,21,21-tetramethyl-m-benzi-6,21porphodimetheno-chloro-Zi nc(II): 由中研院化學所洪政雄老師實驗室所提供的NO probe。
N N N Zn Cl 說明:與 NO 分子反應後,Znc1 放出的 PL 相對 於材料本身的 PL 會有顯著的下降。此材料亦為本 論文研究之重點。 建議溶劑:為雙極性分子,除了水以外的溶劑幾乎都可以溶, 但在 ACN(acetonitrile)裡較為穩定。 圖 3-6 ZnC1 (3)ZnC2:也是 中研院化學所洪政雄老師實驗室所提供的NO probe。是在ZnC1 上 多長出羧基,未來可將它與某氧化物(如SiO2)作結合以增加材料與NO分子作用 表面積。 建議溶劑:DI water
w a v e le n g th (n m )
2 0 0 3 0 0 4 0 0 5 0 0 6 0 0 7 0 0 8 0 0 9 0 0 1 0 0 0 a b s o rp tio n e m is s io n
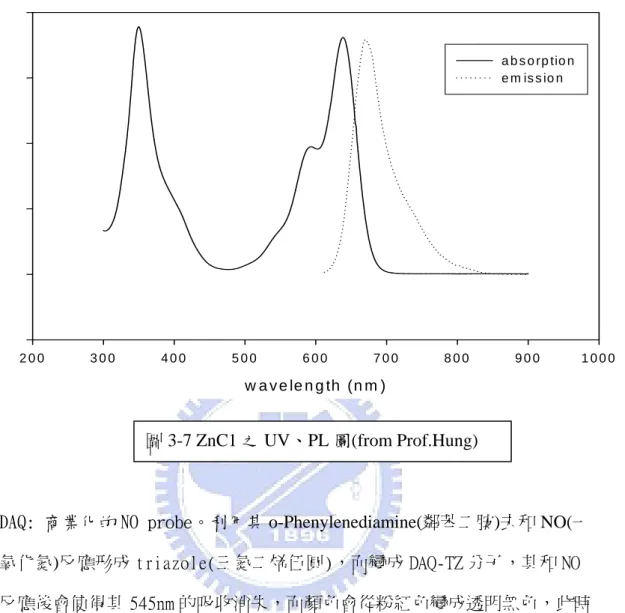
圖 3-7 ZnC1 之 UV、PL 圖(from Prof.Hung)
(4) DAQ: 商業化的 NO probe。利用其 o-Phenylenediamine(鄰苯二胺)去和 NO(一 氧化氮)反應形成 triazole(三氮二烯伍圓),而變成 DAQ-TZ 分子,其和 NO 反應後會使得其 545nm 的吸收消失,而顏色會從粉紅色變成透明無色,此時 如果以波長 350nm 左右的光去激發它會產生 PL。
圖 3-9 DAQ 和 NO 反應後其在 545nm 附近的吸收會消失使其顏色從粉紅變成透明 (5)SNAP:是一種 NO Donor (釋放 NO 分子的材料) 分子式:N-Acetyl-3-(nitrosothio)-DL-valine S-Nitroso-N-acetylpenicillamine 型號:Sigma 67776-06-1 分子量:220.25 儲存溫度:-20℃ 建議溶劑:DMSO(dimethyl sulfoxide) 圖 3-10 SNAP 半衰期(half-life) in solution:約 4~5 小時,視溶劑而定 說明:平均一個分子會釋放出 1 個 NO 分子 (6)NAP:SNAP 釋放 NO 後的殘留物。 和 SNAP 只差個 NO。
(7)NoNoate 分子式:3,3-Bis(aminoethyl)-1-hydroxy-2-oxo-1-triazene 型號:Sigma A5581 分子量:163.18 儲存溫度:-20℃ 建議溶劑:DI water 半衰期(half-life) in solution:3400 分鐘 說明:平均一個分子會釋放出 2 個 NO 分子 圖 3-12 NoNoate
3-4 微流管(Microfluidic system)的製作和量測
(1)微流管的基本設計:基於我們想要在液體系統中快速改變SNAP的濃度,所以我 們設計了以下的Microfluidic system[15、16 ]。SNAP 1
SNAP 2
DI water
output
5mm
35mm
圖 3-13 Microfluidic system 圖案示意圖z
通道太小會增加偵測上的困難所以 為了增加ZnC1的PL強度加寬通道, 增加 偵測面積但總體積不超過1cm3 (1cc) 1.通道寬 5mm 2.深為 100 μm 3.長寬=50mm x 25mm )通道的製作: 我們的通道是使用 PDMS 來製作,其優點為成本低 ,可大量生 產,缺點: 螢光背景值高,檢測靈敏度受限制。 圖 3-14 PDMS 通道示意圖 4.通道設計也使用垂直交叉 (2 PDMS 通道I 通道模具的製作 1. 先準備好 25mm*50mm 的白玻璃 帶(此膠帶一層約厚50um) 使白玻璃上只剩下所需之圖案 通道之製作 . 將 PDMS 主劑和硬化劑以 10 比 1 的比例調配好 PDMS 內的氣泡抽掉 璃上即完成所需之通道 2. 將白玻璃 clean 乾淨 3. 在白玻璃上貼上一層膠 4. 重複步驟 320 次使膠帶厚度達 1mm 5. 在膠帶上畫好所需之圖案 6. 用小刀將不要的交代裁掉, II 1 2. 用玻棒攪拌 PDMS(~10 分鐘) 3. 在模具上倒上混合好的 PDMS 4. 利用真空系統重複抽氣放氣,將 5. 放到 hot plate 上 以 120 度 C 烤 30 分鐘 6. 取下乾掉的 PDMS 7. 放在另一片乾淨的白玻 圖 3-15 PDMS 通道
(5) Microfluidic system 量測: 在主要通道下放置 ZnC1 纖維膜,再用 laser 激 ,在使用 CCD 或是 PD 來接收訊號。此量測可以快速改變 SNAP 濃度、而且少量溶液即可量測。 用 CCD 來量測其架構如下 發 ZnC1 使其發出 PL 利 PDMS ZnC1 CCD 中空 laser len 圖 3-16 Microfluidic system 量測之架構
Syringe pump
圖 3-18 Syringe pump 針筒式幫浦 Microfluidic system 之改善:一開始的設計直接用針筒注射不過針頭為金屬 (6) 會反光,影響 CCD 接收的訊號甚劇,所以就對此做一些改善 。input
訊號不穩定 接到 Syringe pumpinput
接到 Syringe pumpinput
圖 3-17 Microfluidic system 改善示意圖 ) Syringe pump: 針筒式幫浦,可以控制溶液注入速度、注入穩定可以減少雜 (7 訊。Chapter4
實驗設計與結果
4-1 NO probe 之基本特性
4-2 放電紡絲(electrospinning)纖維膜之製作
4-3 放電紡絲(electrospinning)纖維膜和旋轉塗佈膜(spin)之比較
4-4 放電紡絲(electrospinning)纖維膜之基本特性
4-5 濃度極限及時間解析
4-6 微流管實驗
4-1 NO probe 之基本特性
4-1-1 ZnC1:
實驗動機: 由於 ZnC1 是來自中研院化學所洪政雄老師實驗室,而非商用材料,因此在 使用前先對它做一些和 NO 反應的測試。 實驗經過: 我們使用 NO donor SNAP 以及直接吹 NO 氣體測試其對 NO 之反應。 實驗條件: 溶液: 我們將 ZnC1 溶在 DMSO 中 。 NO 釋放: NO donor SNAP 、 NO 氣體 。 實驗結果: ZnC1 和 NO 反應會造成其 PL 下降、以及其 UV 吸收光譜改變。 wavelength (nm) 200 300 400 500 600 700 800 900 1000 absorption emissionSNAP 釋放 NO 濃度估算: 在量測之前,我們先來大略估算不同時間點(SNAP 溶質一溶於水中即開始 計算) ,石英槽中存在的 NO 濃度約為多少? nSNAP(t)=nSNAP(0)e−K1⋅t (式 4-1) t K SNAP NO NO e n K t n K dt t dn = − − ⋅ − ( ) ( ) (0) 1 1 2 (式 4-2) 我們假設 SNAP 濃度隨時間成指數下降,如(式 4-1);不同時間點的 NO 濃度 衰變率會等於 NO 本身的衰變率減掉 SNAP 的 NO 釋放率,如(式 4-2)。我們去 解(式 4-2)一階非線性微分方程式,得到: ( ) (0)( 1 2 ) 1 2 1 K t K t SNAP NO n e e K K K t n − ⋅ − − ⋅ − = (式 4-3) 由於SNAP的半衰期為四小時,而NO的半衰期約為五秒從式 4-4 可以得出K1 = 4.813×10-5 而 K2 = 0.139 [A]e− tk⋅ → [ ] 2 1 A (式 4-4)
where t=half-life time
由於SNAP的半衰期為 4 小時,而量測時間相對SNAP的半衰期極短,我們 可以從式 4-3 換算出NO的濃度。例如:SNAP濃度 0.01667M時NO的濃度 5.77×10-6
M。
在估計完 SNAP 濃度轉換成 NO 濃度後,我們開始了實驗,首先將 ZnC1 溶在 DMSO 後加入也溶在 DMSO 的 SNAP 溶液,觀察其 UV 吸收光譜變化(如圖 4-2)我們 發現 ZnC1 在 600 多 nm 的吸收,在加入 SNAP 溶液後明顯的變小了。之後在用新 的 ZnC1 溶液,放在石英槽中,利用 F-4500 量測系統用波長 600nm 的光去激發 ZnC1 使它放出 PL,再加入 SNAP 溶液觀察其 PL 變化(如圖 4-3)。我們發現在加 入 SNAP 溶液後,ZnC1 的 PL 會隨著時間 Decay,並且會有藍移的現象。 為了確定這個實驗中和 ZnC1 反應的是一氧化氮(NO)我們亦做了另外一個 實驗,我們用一氧化氮氣體代替了 SNAP 溶液,如圖 4-4 我們直接吹入 NO 氣體亦 改變了 ZnC1 的 UV 吸收光譜,並且發現其結果和圖 4-2 一致。在圖 4-5 中我們也 可以看出,NO 氣體也會使 ZnC1 的 PL 隨著時間減弱並且也有著藍移的現象,這 個結果和圖 4-3 一致。從這幾個實驗的結果我們可以確定:ZnC1 會和 NO 反應造 成其 UV 吸收光譜改變並且造成其 PL 減弱。 300 400 500 600 700 800 900 -2 -1 0 1 2 3 4 Absorba n ce nm pure ZnC1 solution@DMSO blank ZnC1 solution+SNAP@DMSO may SNAP absorption
500 550 600 650 700 0.5 1.0 1.5 2.0 Absorbance nm pure ZnC1 solution@DMSO blank ZnC1 solution+SNAP@DMSO may SNAP absorption
ZnC1 solution
圖 4-3 ZnC1 溶液加入 SNAP 造成其 PL 有 shift 以及 decay 之現象 圖 4-4 以 NO 氣體直接灌進 ZnC1 溶液也會改變其 UV 吸收光譜 500 550 600 650 700 750 800 850 900 950 0 500 1000 1500 2000 2500 PL nm pure ZnC1 solution after 1min after 2mins after 3mins after 4mins add 0.5ml 0.05M SNAP after 1min after 2mins after 3mins after 4mins after 5mins after 6mins after 7mins after 8mins after 9mins after 10mins after 11mins after 13mins after 15mins after 17mins after 19mins after 21mins after 26mins after 31mins after 36mins after 41mins after 51mins after 61mins after 71mins after 76mins 650 675 700 1750 2000 2250 2500 pure ZnC1 solution after 1min after 2mins after 3mins after 4mins add 0.5ml 0.05M SNAP PL nm after 1min
PL shift
Decay with time
600 620 640 660 0.00 0.03 0.06 0.09 0.12 0.15 Ab sorban ce nm initial
bubbled NO for 1min for more 1min for more 1min 300 400 500 600 700 800 900 -0.05 0.00 0.05 0.10 0.15 0.20 0.25 Absorbance nm initial
bubbled NO for 1min for more 1min for more 1min
600
650
700
750
800
850
900
-50
0
50
100
150
200
250
300
350
PL
initial pure Zn complex solution bubbled NO for 10mins
bubbled NO for 1min bubbled NO for 1min more bubbled NO for 1min more
nm
4-1-2 DAQ:
驗動機:
測試買來的 NO probe DAQ 觀察 DAQ 和 NO 反應的結果。 實 實驗經過: 我們使用 NO donor SNAP 以及直接吹 NO 氣體測試其對 NO 之反應。 實驗條件: 溶液 我們將 DAQ 溶於 DMSO 中 體 : NO 釋放: NO donor SNAP 、 NO 氣 實驗結果: DAQ和 NO反應會造成其 PL 下降、以及其 UV 吸收光譜改變。 4-6 DAQ@DMSO 溶液加入 SNAP 造成其 PL 下降(用 545nm 的光激發)
500
600
700
800
900
圖0
20
40
60
80
100
120
0.001% wt DAQ/DMSO 0.001% wt DAQ/DMSO +1ml 0.01M SNAP 0min 1min 2min 3min 4min 5min 6minPL
wavelength(nm)
在測試完 ZnC1 後繼續測試另一個 NO probe DAQ。首先將 DAQ 溶在 DMSO 中 其重量百分比為 0.001% ,再加入 0.01M SNAP 溶液如圖 4-6,在這裏我們發現其 PL 隨著時間減弱,並且有藍移的現象。在觀察完其 PL 變化後,我們也觀察了其 UV 吸收光譜的變化,如圖 4-7 其在 545nm 左右的吸收峰再加入 SNAP 溶液後就消 失了,這個結果和 PAPER 一致(如圖 4-8)。在這裡我們也用 NO 氣體取代 SNAP 溶 液,亦得到一樣的結果(如圖 4-9 4-10),這些實驗可以證明 DAQ 和 NO 會反應造 成其 545nm 左右的吸收峰消失,也因為其 545nm 的吸收峰消失,所以造成其 PL 下降(用 545nm 的光去激發)。
4-7 SNAP 造成 DAQ 在 545nm 左右的吸收消失
500 600 700 800圖
DAQ+snap
-0.4
0.0
0.4
DAQ
ABS
nm
圖 4-8 其結果和 paper 的結果一致
500
600
700
800
900
0
20
40
60
80
100
120
140
160
PL
wavelength(nm)
0.001% wt DAQ/DMSO no bubble no bubble 1min圖 4-9 NO 氣體造成 DAQ 溶液 PL 下降(用 545nm 的光激發)
300
400
500
600
-1
0
1
2
ABS
nm
DAQ DAQ+no bubble圖 4-10 NO 氣體亦造成 DAQ 溶液 550nm 左右之吸收消失
實驗結果討論: 1. SNAP 會造成 ZnC1 溶液 PL 下降及 UV 吸收改變,其結果和 NO 氣體一致,可證 明 ZnC1 和 NO 確實會有反應。 2. NO 氣體和 DAQ 溶液反應會使得其 545nm 吸收峰消失,和 paper 一致。 3. 利用 SNAP 也會造成 DAQ 545nm 吸收峰消失。 4. 由於 545nm 的吸收消失,所以用 545nm 激發時,不管是 NO 氣體或是 SNAP 都 會造成 DAQ 的 PL 下降。4-2 放電紡絲(electrospinning)纖維膜之製作
4-2-1 放電紡絲(electrospinning)之使用
實驗動機: 使用放電紡絲(electrospinning)製造纖維膜,利用其表面機特大的特性我們 期望可以改善原有 ZnC1 固態膜的特性。 實驗經過: 利用 electrospinning 製造纖維膜,再用 SEM 去看其成膜的樣子。 實驗條件: 溶液: 我們將 PAN 溶於 DMSO 中重量百分比為 10%。 Electrospinning 製程條件:流量 1ml/hr 距離 5cm 電壓 10kv。 實驗結果: 利用 electrospinning 製造出來的膜,在 SEM 下呈現纖維狀,其單一條絲支直 徑約為 600-800nm 之間,有一些絲會特別粗,大約 2000nm 左右,很顯然其表 面積相當大。我們將 PAN 溶於 DMSO 中重量百分比為 10%後注入針筒內,並用流量控制器控 制其流量(如圖 4-11),之後在針頭上加上高電壓(~10KV),使溶液因靜電力而噴 出,在空氣中溶劑蒸發,而在收集器留下纖維膜。在這裡加上高電壓就好像在溶 液內灌進相同電荷,而相同電荷間會產生靜電排斥力,當排斥力大於溶液的表面 張力時會將溶液噴出,此即放電紡絲的基本原理。在這裡要特別注意的是容易需 兼具黏著性與伸縮性,如果在這裡溶液並不具黏著性與伸縮性的話,就會像在氣 球裡一直吹氣一樣破掉,並不會產生溶液噴發。 圖 4-12 其單一條絲直徑約為 600-800nm 之間 在收集纖維膜後,將纖維膜拿去照 SEM(如圖 4-12) ,其膜呈不規則排列,而其 單一條斯的直徑約為 600-800nm 之間 。
4-2-2 放電紡絲(electrospinning)纖維膜和 NO Probe 的結合
實驗動機: 將放電紡絲(electrospinning)纖維膜和 NO Probe(ZnC1、DAQ)結合 實驗經過: 在 PAN@DMSO 裡加入 NO Probe 其重量比都為 25 比 1,再利用 electrospinning 製造纖維膜,使用 SEM 去看其成膜的樣子。 實驗條件: 溶液: 我們將 PAN 溶於 DMSO 中重量百分比為 10%。 再分別添加 ZnC1 和 DAQ 這兩種 NO probe。 PAN 和 NO Probe 其重量比為 25 比 1 Electrospinning 製程條件:流量 1ml/hr 距離 5cm 電壓 10kv。 實驗結果: 其結果和只使用 PAN@DMSO 的溶液大致一致,不過添加 DAQ 的纖維膜呈粉紅色, 而添加 ZnC1 的纖維膜呈淡藍色。 圖 4-13 添加 ZnC1 的纖維膜 圖 4-14 其絲的直徑~800nm 左右在 PAN@DMSO 10%WT 的溶液中添加 ZnC1 和 DAQ 後,再利用放電紡絲製作成纖 維膜,PAN 和 NO Probe 其重量比為 25 比 1,這個比例為最佳比例可放出最大的 PL。將這些纖維膜拿去 SEM 可以發現其結構和一般纖維膜並沒有差別,而添加 DAQ 的纖維膜呈粉紅色,而添加 ZnC1 的纖維膜呈淡藍色。 可以證明這樣製作纖 維膜,可以在其表面上加入 NO probe。 ospinning)製造出纖維膜。 4. ZnC1、DAQ) 和纖維膜結合,且不會改變其性質,依然擁有很 添加 ZnC1 的纖維膜呈淡藍色,而添加 DAQ 的纖維膜呈粉紅色。 圖 4-15 添加 DAQ 的纖維膜 圖 4-16 其絲的直徑約 800nm 左右 實驗結果討論: 1. 可將 PAN@DMSO 溶液利用放電紡絲(electr 2. 製造出來的纖維膜其直徑~800nm 左右。 3. 製造出來的纖維膜有很大的表面積。 可將 NO probe( 大的表面積。 5.
4-3 放電紡絲(electrospinning)纖維膜和旋轉塗佈膜(spin)之比較
3-1 ZnC1 fibrous membrane 和 spin film 的比較
實驗動機: 比較 ZnC1 纖維膜和一般固態膜對 SNAP 的反應。
4-實驗經過: 分別製作好纖維膜和一般固態膜,分別加入 0.05M 的 SNAP(@DI water) ,利 其 PL 變化。 用 F4500 量測 實驗條件: Electrospinning 製程條件:流量 1ml/hr 距離 5cm 電壓 10kv。 PAN:ZnC1=25:1(重量比) Spin film 條件:轉速 1000rpm 300s 甩完後將之加熱 120℃約莫 60 秒。 其膜後約為 10*10-6m。PAN:ZnC1=25:1(重量比) 實驗結果: ‧ Electrospinning film 參與反應的面積大 加快反應時間 很快達到飽和 spin film 需要時間慢慢滲透。‧ Electrospinning film 32% > spin film 26% (1min) 纖維膜反應較為明顯 ‧ 絲狀的結構確實大大增加了反應面積並加快反應速率。 ‧ 纖維狀結構使反應很快 在小於一分鐘或更短的時間內達到飽和。 ‧ 一般膜(spin film)其反應時間超過 20 分鐘。 在這裡我們要比較不同結構的膜和 NO 反應會有什麼樣的結果,首先我們分別 製作了 ZnC1 的纖維膜和一般膜,在加入相同條件的 SNAP 溶液,觀察其 PL 變化 情形(如圖 4-17、4-18),在這裡我們發現纖維膜因為其表面積較大所以其反應 速度較快。
ZnC1:
PAN
1:25 (fibrous membrane)
600
650
700
750
0
500
1000
1500
2000
PL
wavelength(nm)
ZnC1 ele film+DI water 1ml DI water 1ml 0.05M snap 1ml 1min 2min 5min 10min 0.05M snap 1ml 1min 2min
1149 776 32.46%
add SNAP Add DI water
Add DI water
add SNAP
圖 4-18 非纖維狀結構需要較長時間才可達到平衡600
650
700
750
0
500
1000
1500
2000
2500
3000
PL
wavelength(nm)
DI water 1ml
1min
2min
0.05M snap1ml
1min
2min
5min
10min
15min
PAN:ZnC1 25:1 (spin film)
1. 所有實驗都在確認加入 DI WATER 不會改變 PL 後再開始。 2. 在纖維膜實驗中,加入 SNAP 一分鐘後再次量測其 PL,並沒有再下 降代表其環境已經穩定了,已經達到飽和了。 3. 而在一般膜中,雖未再加入 SNAP 但是其 PL 依然下降,代表還沒飽 和 ZnC1 依然還在和 NO 反應造成其 PL 下降。 4. 在纖維膜中,再次加入 SNAP 其 PL 未再下降,原因是在於可以和 NO 反應的 ZnC1 都和 NO 反應了,所以這時候加入在多的 NO 已經 沒有意義了。 5. 這兩個實驗比較可以得出:增大表面積可以讓 NO 和 ZnC1 反應速度加 快。
4-3-2 DAQ fibrous membrane 和 spin film 的比較
實驗動機: 比較 DAQ 纖維膜和一般固態膜對 SNAP 的反應。 實驗經過: 分別製作好纖維膜和一般固態膜,分別加入 0.0125M 的 SNAP(@DI water) , 利用 F4500 量測其 PL 變化。 實驗條件: Electrospinning 製程條件:流量 1ml/hr 距離 5cm 電壓 10kv。 PAN:DAQ=25:1(重量比) Spin film 條件:轉速 1000rpm 300s 甩完後將之加熱 120℃約莫 60 秒。 其膜後約為 10*10-6m。PAN:DAQ=25:1(重量比) 實驗結果: ‧ 可以發現其結果和 ZnC1 一樣,纖維膜反應速度較一般膜快。可以驗證我們 的想法。 在比較完 ZnC1 的纖維膜和一般膜後,我們也比較了 DAQ 的纖維膜和一般膜, 這個實驗是為了確定上面的結果並不會只出現在 ZnC1 上。在分別製作完 DAQ 的 纖維膜和一般膜後我們加入一樣條件的 SNAP 溶液後,去觀察 DAQ 的 PL 的變化, 在這裡我們發現結果和 ZnC1 一致,纖維膜可以加快反應速度(如圖 4-19、4-20)。560 580 600 620 640 660 680
1000
1500
2000
2500
3000
3500
4000
PL
wavelength(nm)
DAQ ele film DI water 1min 2min 5min 0.0125M snap 1ml 1min 2min 5min
PAN:DAQ 25:1 (fibrous membrane)
圖 4-19 DAQ 纖維膜和 NO 反應造成其 PL 下降(545nm 激發) 圖 4-20 DAQ 一般膜和 NO 反應造成其 PL 下降(545nm 激發) 600 620 640 660 100 150 200 250 300 350 400
PAN:DAQ 25:1 (spin)
spin film DI water 1min 2min 5min 0.0125M snap 1ml 1min 2min 5min 8minPL
wavelength(nm)
10min1. 在 PL 穩定後加入 SNAP。 2. 如圖 4-20 DAQ 纖維膜在 1 分鐘內完成反應,此後 PL 達到穩定。 3. 如圖 4-21DAQ 一般膜需要八分鐘才能完成反應使其 PL 穩定。 4. 用 DAQ 證明此結果不只適用於中研院研發的 NO Probe ZnC1,亦可 使用於商業化的 NO Probe。 實驗結果討論: 1.Electrospinning film 參與反應的面積大,加快反應時間很快達到飽和, spin film 需要時間慢慢滲透。
2.Electrospinning film 32% > spin film 26% (1min) 纖維膜反應較為明顯 3.絲狀的結構確實大大增加了反應面積並加快反應速率。
4.纖維狀結構使反應很快 在小於一分鐘或更短的時間內達到飽和。一般膜(spin film)其反應時間超過 20 分鐘。
5. Electrospinning 製作的纖維膜確實比一般膜好。 6.此結果並非特例,亦可使用於商業化的 NO Probe。
4-4 放電紡絲(electrospinning)纖維膜之基本特性
4-4-1 放電紡絲(electrospinning)纖維膜之濃度階梯量測:
實驗動機: 漸漸增加 SNAP 濃度,測試 ZnC1 纖維膜 PL 對 SNAP 濃度變化的反應。 實驗經過: 在 ZnC1 纖維膜加入 DI water 後等待使之穩定,之後加入較淡的 SNAP,當 PL 穩定後再增加 SNAP 濃度,觀察其 PL 變化。 實驗條件: ZnC1 纖維膜:Electrospinning 製程條件:流量 1ml/hr 距離 5cm 電壓 10kv。 PAN:ZnC1=25:1(重量比) 。 SNAP 濃度:0.000325M、 0.000625M、 0.025M (皆溶於 DI water) 。 實驗結果: ‧ 發現 ZnC1 纖維膜的 PL 會隨著 SNAP 濃度增加而下降,並且相當穩定。 ‧ 從 ZnC1 PL 的值,可以對應出 SNAP 的濃度。 在這裡我們想要知道我們製作的 ZnC1 纖維膜的一些基本性質,首先我們緩慢 增加 SANP 的濃度,觀察其 PL 是否會隨著 SANP 濃度增加而改變。如圖 4-21 我 們發現 ZnC1 纖維膜的 PL 會隨著 SNAP 濃度變濃而下降。這是很重要的一件事, 一個好的感測器一定要可以感測出不同濃度的變化,而我們的 ZnC1 纖維膜會隨 著不同濃度做出其 PL 的反應,這代表我們可以偵測出不同濃度的 NO。650
660
670
680
500
1000
1500
2000
PL
wavelength(nm)
ele film DI water 1ml 1min 2min +0.000325M snap 1ml 1min 5min +0.000625M snap 1ml 1min 2min 5min +0.025M snap 0.5ml 1min 5minPAN:ZnC1 25:1 (fibrous membrane)
濃度階梯
圖 4-21 ZnC1 纖維膜的 PL 會隨著 SNAP 濃度增加而下降
1. 由於 ZnC1 纖維膜和 NO 反應速度很快,改變 SNAP 濃度其 PL 就會跟 著改變。
4-4-2 放電紡絲纖維膜之可逆性反應(reversibility)測試:
實驗動機: 測試 ZnC1 放電紡絲纖維膜是否可以重複使用。 實驗經過: 將 ZnC1 放電紡絲纖維膜加入 SNAP 後等其穩定,拿起來沖水洗乾淨,在加入 一樣濃度的 SNAP 看其 PL 變化。 實驗條件: ZnC1 纖維膜:Electrospinning 製程條件:流量 1ml/hr 距離 5cm 電壓 10kv。 PAN:ZnC1=25:1(重量比) 。 SNAP 濃度:0.05M (溶於 DI water) 。 實驗結果: ‧ 發現 ZnC1 纖維膜的 PL 在洗乾淨後卻沒有回到原本亮度。 ‧ 在洗完後再次加入相同濃度 SNAP 其 PL 會減弱到和前面一樣。 ‧ 再次做同樣動作一次,其結果亦相同。 可逆性對於一個好的偵測器來說也是很重要的,一個可逆性的材料除了使偵 測器可以重複使用外,為了達到及時的量測可逆性是必要的,在及時的量測中我 們不只要偵測出濃度增加,也要能夠偵測出濃度減弱,如果不是可逆反應是做不 到這點的。在可逆性實驗中我們加入 SNAP 造成其 PL 改變後,將石英槽內的 ZnC1 纖維膜拿出清洗,再加入相同濃度的 SNAP 溶液,觀察其 PL 是否會回到相同位置。 如圖 4-22 我們發現在清洗完後再加入相同濃度 SNAP 後,其 PL 會回到相同位 置,這可以證明 NO 和 ZnC1 的反應是可逆的,而清洗後無法回到相同 PL 的原因 是會有些微的 SNAP 殘留。640
660
680
700
0
1000
2000
3000
4000
5000
6000
PL
wavelength(nm)
ele film DI water 1ml 1min 2min 0.05M snap 1ml 0.5min 1min 2min 7min clean+1mlDIwater 2min 0.05M snap 1mlclean 1ml DIwater 0min 1min
PAN:ZnC1 25:1(fibrous membrane)
Reversibility 測試
圖 4-22 ZnC1 纖維膜 Reversibility 測試 1. 加入 0.05MSNAP 後其 PL 掉到淡藍色位置,洗乾淨後其 PL 變成 紫色位置,沒有回到紅色位置,再加入一樣濃度 SNAP 變成綠色 位置,和淡藍色位置相符,可以知道相同濃度會減弱到相同位置。 2. 回到相同濃度時,其濃度會回到相同位置。 3. 其洗乾淨後未能回到相同 PL,推測原因為依然有些微 SNAP 殘留。 4. 清洗完後會將石英槽內的溶液倒掉並清洗石英槽。 5. 其結果顯示 ZnC1 纖維膜是可重複利用的,但是殘留的 SNAP 是 個問題。4-4-3 放電紡絲纖維膜 PH 值及 NAP 測試
實驗動機: 由於 NO 在水中會造成 PH 值上升,所以需要排除 PH 值影響。又 SNAP 放出 NO 後會有 NAP 產生,所以也要將 NAP 影響排除。 實驗經過: 在石英槽內放入 ZnC1 和 DAQ 的纖維膜,加入 DI water 待其穩定後,改變石 英槽內 PH 值由 7 到 1,再回到 7,再慢慢增加至 14,最後再加入 NAP,觀察其 PL 值的變化。 實驗條件: ZnC1 纖維膜:Electrospinning 製程條件:流量 1ml/hr 距離 5cm 電壓 10kv。 PAN:ZnC1=25:1(重量比) 。 DAQ 纖維膜:Electrospinning 製程條件:流量 1ml/hr 距離 5cm 電壓 10kv。 PAN:DAQ=25:1(重量比) 。 NAP 濃度:0.05M (溶於 DI water) 。 實驗結果: ‧ 發現 PH 值對於 ZnC1 和 DAQ 這兩種 NO probe 影響都不大,都在誤差範圍內, 所以可以排除 PH 值對於這兩種 NO probe 的影響。 ‧ ZnC1 和 DAQ 對 NAP 沒有反應。 ‧ 由這邊可是確定 ZnC1 和 DAQ 的 PL 變化,是因為和 NO 反應造成的。 由於 NO 會和水反應生成亞硝酸鹽和硝酸鹽改變 PH 值,所以在這裡的實驗一 定要排除 PH 值的影響,而我們加入 SNAP 溶液除了提供 NO 外也會產生 SNAP 殘留 物 NAP,所以我們也要確定 NAP 並不會和 ZnC1 或是 DAQ 反應。如圖 4-23、4-24 我們可以發現改變 PH 值並不會造成 ZnC1 或是 DAQ 的 PL 有 明顯的改變,而 NAP 也不會和 ZnC1 或是 DAQ 反應,所以我們可以確定之前的實 驗和 ZnC1、DAQ 反應的確實是 NO。
pH and NAP test
PAN:ZnC1 25:1 (fibrous membrane)
0
2
4
6
8
10
12
14
500
1000
1500
2000
2500
3000
3500
PL
PH
670nm(ZnC1)
NAP
圖 4-23PH 值和 NAP 並不會影響 ZnC1 的 PLpH and NAP test
0
2
4
6
8
10
12
14
500
1000
1500
2000
2500
3000
3500
PL
PH
620nm(DAQ)
NAP
PAN:DAQ 25:1(fibrous membrane)
1. PH 值和 SNAP 殘留物(NAP)並不會造成 ZnC1 纖維膜 PL 下降, 所以可以肯定是 NO 造成 ZnC1 纖維膜 PL 下降。
2. PH 值和 SNAP 殘留物(NAP)並不會造成 DAQ 纖維膜 PL 下降, 所以可以肯定是 NO 造成 DAQ 纖維膜 PL 下降。
4-4-4 在生理環境下 ZnC1 對 NO 的反應
實驗動機:
試試在仿生理環境下,ZnC1 是否一樣可以偵測到 NO。
實驗經過:
在石英槽內放入 ZnC1 纖維膜,加入 culture medium 待其穩定後,加入 0.02M SNAP(亦溶於 culture medium)1ml,觀察其 PL 變化是否和在 DI water 環境下一樣。 實驗條件:
ZnC1 纖維膜:Electrospinning 製程條件:流量 1ml/hr 距離 5cm 電壓 10kv。 PAN:ZnC1=25:1(重量比) 。
NAP 濃度:0.02M (溶於 culture medium) 。
實驗結果:
‧ 在生理環境下 ZnC1 亦可以偵測到 NO。
由於未來我們期望可以將我們的 NO 感測器應用在生物實驗上,所以我們要確
定在仿生理環境下,ZnC1 是否一樣可以偵測到 NO,所以我們將我們的環境從 DI water 改變成一種在生物實驗常用的溶液 culture medium,我們期望在這個環境 下 ZnC1 一樣可以偵測到 NO。
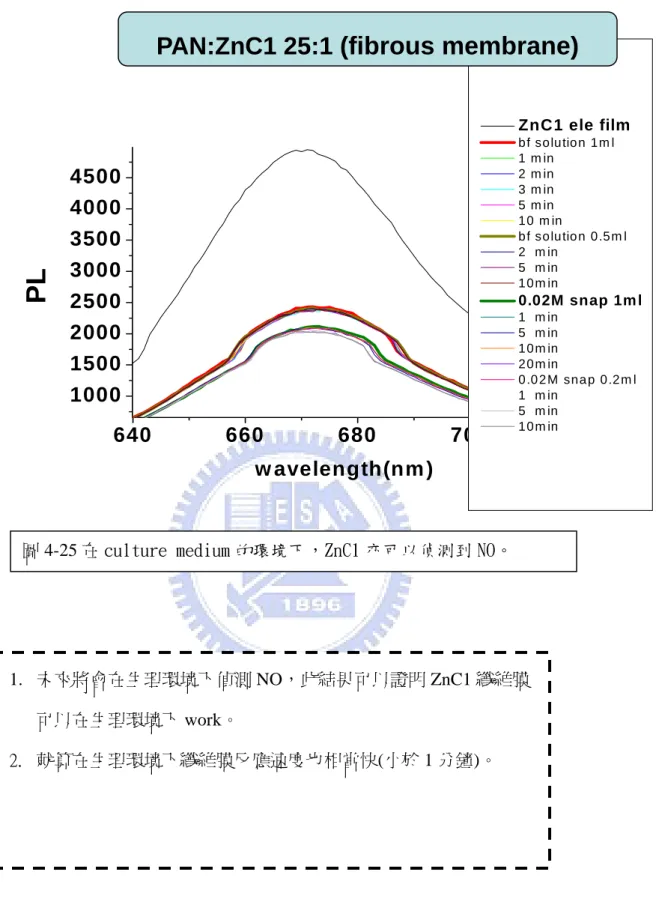
我們使用 culture medium 取代 DI water,再加入 SNAP 溶液觀察,ZnC1 是否 會和 NO 反應造成其 PL 下降,如圖 4-25 我們發現在 culture medium 的環境下, ZnC1 亦可以偵測到 NO。其性質和之前並無不同。
640
660
680
700
1000
1500
2000
2500
3000
3500
4000
4500
PL
w avelength(nm )
ZnC1 ele film bf solutio n 1m l 1 m in 2 m in 3 m in 5 m in 10 m in bf solutio n 0.5m l 2 m in 5 m in 10 m in 0.02M snap 1m l 1 m in 5 m in 10 m in 20 m in 0.0 2 M sna p 0 .2 m l 1 m in 5 m in 10 m inPAN:ZnC1 25:1
(fibrous membrane)
圖 4-25 在 culture medium 的環境下,ZnC1 亦可以偵測到 NO。
2. 就算在生理環境下纖維膜反應速度也相當快(小於 1 分鐘)。 1. 未來將會在生理環境下偵測 NO,此結果可以證明 ZnC1 纖維膜