國立交通大學
生物醫學研究所
碩士論文
以大腸桿菌
C41 與 C43 菌株表現登革熱病毒蛋白
NS1、NS2、NS4 與 E
Expression of Dengue Virus Proteins NS1, NS2, NS4 and E in E.coli
C41 and C43 Expression Strains
研究生:藍敏書
指導教授:楊昀良 博士
以大腸桿菌
C41 與 C43 菌株表現登革熱病毒蛋白 NS1、NS2、NS4
與
E
Expression of Dengue Virus Proteins NS1, NS2, NS4 and E in E.coli
C41 and C43 Expression Strains
研究生:藍敏書 Student:Min-Shu Lan
指導教授:楊昀良 博士 Advisor:Dr. Yun-Liang Yang
國 立 交 通 大 學 生 物 醫 學 研 究 所
碩 士 論 文
A Thesis
Submitted to Institute of Biomedical Science College of Biological Science and Technology
National Chiao Tung University in partial Fulfillment of the Requirements
for Degree of Master of Science in
Biomedical Science
June 2009
Hsinchu, Taiwan, Republic of China
以大腸桿菌C41 與 C43 菌株表現登革熱病毒蛋白 NS1、NS2、NS4 與 E
中文摘要
登革熱病毒屬黃熱病毒科(Flaviviridae)黃熱病毒屬(Flavivirus)。它會造 成登革熱(dengue fever)、登革出血熱(dengue hemorrhagic fever)及登革休克 症候群(dengue shock syndrome)等症狀。登革熱病毒產生蛋白質的過程中,
會先產生單一個蛋白質轉譯區,再切割成10 個獨立的蛋白質。包含 3 個結
構 性 蛋 白(structural proteins) 以 及 7 個 非 結 構 性 蛋 白 (non-structural
proteins),其中外膜蛋白(envelope protein)便屬於結構性蛋白,位於病毒雙 層膜的外側,是一種穿膜的蛋白質,被認為可和受體結合,與感染宿主細 胞有關。NS1 與 NS2A、NS2B、NS4A、NS4B 是較小的非結構性蛋白,具 有疏水的特性,皆是與膜有關的蛋白質。已知 NS2B 會參與蛋白切割酶切 割反應,而NS1、NS2A、NS4A、NS4B 則與病毒的複製有關。為研究蛋白 質的功能,首先必須建構質體並於大腸桿菌系統中表現蛋白質,本研究將 針對 NS1、NS2A、NS2B、NS4A、NS4B 與 E 蛋白等蛋白質做探討,由於 這些蛋白質皆具有疏水的特性,因此選用大腸桿菌C41(DE3)及 C43(DE3) 菌株以利其表現。將基因構築於修飾過pET-30(+)表現載體:pETΔ5T-HAHis 上 , 分 別 於 基 因 末 端 接 上 融 合 蛋 白 HA-His(influenza Hemagglutinin-
Hexahistidine protein)以利抗體偵測。將此建構質體送入大腸桿菌 C41(DE3)
或C43(DE3)菌株後,皆可採用西方點墨法(Western blot)偵測其表現,但
Expression of Dengue Virus Proteins NS1, NS2, NS4 and E in E.coli C41 and C43 Expression Strains
Abstract
Dengue virus is a member of family Flaviviridae, genus of Flavivirus. Dengue viruses cause dengue fever, dengue hemorrhagic fever and dengue shock syndrome. Dengue virus encodes 10 proteins in a single open reading frame, including 3 structural proteins and 7 non-structural proteins. Envelope protein is one of the structural proteins locates outside of the virus particle, which can bind to receptors on host cells and causes infection. NS2A, 2B, 4A and 4B are small non-structural proteins which are membrane-associated proteins exhibiting hydrophobic profiles. NS2B has been suggested to involve in protease activity. NS1, NS2A, NS4A and NS4B have been suggested to involve in virus replication. Individual expression plasmids were constructed and expressed in E.coli C41(DE3)and C43(DE3) strains due to their hydrophobic profiles. These genes were cloned individually into a modified pET-30(+) vector, pETΔ5T-HAHis. Their proteins were expressed as HA-His (influenza Hemagglutinin- Hexahistidine protein) fusion proteins for antibodies detection. Recombinant proteins fused with HA-His tag could be detected by Western blotting analysis, but not by Comassie blue staining.
致謝 在新竹兩年多的研究生活,除了學習到許多專業知識、也明白許多待 人處世的道理,很慶幸能遇到楊昀良老師的指導,開啟我充實的碩士生涯, 在此學生由衷的感謝您。 十分感謝口試委員林苕吟老師、黃兆棋老師、冷治湘老師給予論文上 的指導與建議,讓論文更加完整與充實,學生獲益良多。 在這裡,不僅擁有舒適的實驗環境,在實驗方面老師給予我們細心指 導與缺失的改進,做人做事方面老師也教導我們謙卑的態度,讓我們獲益 良多。研究生忙碌的日子中,朋友間的伴隨與幫助讓這段日子增添美麗豐 富的色彩,壞小孩旻秀生活玩樂有默契,淑貞做事認真努力,淑萍直來直 往有個性,同儕間的我們一同渡過許多時光;昶文生活好榜樣,小毛志豪 幽默很逗趣,秉博、晨圃、毓緯、欣彬照顧後輩很夠力,有學長姐們的提 拔讓我活力十足;大學姐惠菁總是幫大家送定序,正妹小倩聰穎伶俐,麻 麻阿毛笑嘻嘻很陶氣,阿彭毓駿率直有自信,為人師表佳真虧人有霸氣, 小Sunny 馨儀細心謹慎,妍寕禮貌周到,媚妹&重延簡報製作有創意,乖孩 子 Ubi 總愛玩遊戲,阿大人緣超好有魅力,武田幸璇小巨人有毅力,阿鋘 照顧愛貓有一套,志達催促進度有效率,新夥伴世宏與睿賢未來研究很順 利,有了大家的加入,實驗室彷彿像個大家庭般的快樂又美麗。 此外朝彥、小高、采婷、怡仁、茵嵐與孟鈴等好友的陪伴讓生活充滿 樂趣,感謝葉大哥全心全力呵護小楊實驗室不遺餘力,所辦工作團隊給我 許多工讀機會很感動,還有小胖吃喝玩樂揪團去,家煒活潑互動很有趣, 咏馨歌唱天后有實力,世勳提供居家生活好環境,若芬默默給予支持與鼓 勵,讓我在研究生涯中總是能夠樂觀進取的前進。 父母的栽培與弟弟的陪伴可以讓我在求學過程中平安順利,一路走來 受惠於許多人的幫忙與協助,感謝上天給了我許多學習成長的機會,研究生 涯的回憶點滴在心頭,未來的道路願你我都能平安順遂,期望我們都能保 持愉快的心去幫助更多的人,套句大家常說的話:「要感謝的人太多了,不 如就謝天吧。」,所有一切的祝福與感謝,盡在不言中。
目錄 中文摘要...I Abstract ...II 致謝... III 目錄... IV 表目錄...VII 圖目錄... VIII 附錄目錄... X 縮寫(Abbreviation)... XI 壹、緒 論... 1 1.1 登革熱病毒 ... 1 1.2 登革熱病毒的基因結構... 2 1.3 登革熱病毒基因轉譯... 2 1.4 外膜蛋白 E 之特性 ... 3 1.5 非結構蛋白 NS1 之特性... 4 1.6 非結構蛋白 NS2A 的特性... 5 1.7 非結構蛋白 NS2B 的特性 ... 6 1.8 非結構蛋白 NS4A 的特性... 6 1.9 非結構蛋白 NS4B 的特性 ... 7 1.10 表現登革熱蛋白質的系統-大腸桿菌 C41(DE3)與 C43(DE3)菌 株... 7 貳、材料與方法... 9 2.1 實驗材料 ... 9 2.1.1 菌株(Bacteria Strains)... 9 2.1.2 病毒(Viruses) ... 9 2.1.3 質體(Plasmids)... 9 2.1.4 引子(Primers)... 11 2.1.4.1 針對建構質體所設計的引子 ... 11 2.1.4.2 針對 Site-Directed Mutagenesis 所設計的引子 ... 13
2.1.5 藥品試劑 ... 14 2.1.5.1 藥品 ... 14 2.1.5.2 抗體 ... 15 2.1.5.3 Kit ... 16 2.1.6 溶劑及緩衝液之配方 ... 16 2.1.7 主要儀器 ... 17 2.2 實驗方法 ... 18 2.2.1 大腸桿菌勝任細胞(Competent cell)的製備 ... 18 2.2.2 大腸桿菌轉形作用(transformation) ... 18 2.2.3 建構質體 DNA ... 19 2.2.4 小量質體 DNA 萃取 ... 19 2.2.5 限制酵素反應 ... 20 2.2.6 萃取洋菜膠內之 DNA 片段 ... 20 2.2.7 重組蛋白在大腸桿菌之誘導表現... 20 2.2.8 大腸桿菌蛋白質之萃取 ... 21
2.2.9 以 SDS-PAGE 分析並以 Coomassie blue staining 及西方轉漬分 析(Western blot analysis)偵測蛋白質表現... 21
2.2.9.1 SDS-PAGE 電泳 ... 21
2.2.9.2 Coomassie blue staining ... 21
2.2.9.3 西方轉漬分析(Western blot analysis) ... 22
參、結果... 23
3.1 pET△5T-HAHis 質體之建構 ... 23
3.2 pET△5T-D2E-HAHis, pET△5T-D2NS1-HAHis, pET△5T-D2NS1(d) -HAHis pET-30a-D2NS1-HAHis 質體之建構 ... 23
3.3 pET△5T-D32A-HAHis, pET△5T-D32B-HAHis, pET△5T-D34A -HAHis, pET△5T-D34B-HAHis, pET△5T-D3E-HAHis 質體之建構24 3.4 利用限制酵素以確認所建構之質體... 24
3.6 登革熱病毒非結構蛋白以及外膜蛋白(E protein)在 E.coli C41(DE3) 和C43(DE3)中的表現... 27 3.6.1 登革熱病毒非結構蛋白 NS2 與 NS4 的表現... 27 3.6.1.1 pET△5T-D2NS2A-HAHis, pET△5T-D3NS2A-HAHis 蛋白質表現結果... 27 3.6.1.2 pET△5T-D2NS2B-HAHis, pET△5T-D3NS2B-HAHis 蛋 白質表現結果... 28 3.6.1.3 pET△5T-D2NS4A-HAHis, pET△5T-D3NS4A-HAHis 蛋白質表現結果... 29 3.6.1.4 pET△5T-D2NS4B-HAHis, pET△5T-D3NS4B-HAHis 蛋 白質表現結果... 30 3.6.2 登革熱病毒外膜蛋白的表現... 31 3.6.2.1 pET△5T-D2E-HAHis, pET△5T-D3E-HAHis 蛋白質表 現結果... 31 3.6.3 登革熱病毒非結構蛋白 NS1 的表現... 32 3.6.3.1 pET△5T-D2NS1-HAHis 蛋白質表現結果... 32 3.6.3.2 pET△5T-D2NS1(d)-HAHis 蛋白質表現結果 ... 33 3.6.3.3 pET30a-D2NS1-HAHis 蛋白質表現結果 ... 33 肆、討論... 35 4.1 質體建構與序列分析... 35 4.2 表現登革熱病毒非結構蛋白 NS2 與 NS4 與外膜蛋白在 Ecoli C41 (DE3)和 C43(DE3)表現系統 ... 35
4.3 表現登革熱病毒外膜蛋白在 E.coli C41(DE3)和 C43(DE3)表現 系統... 37
4.4 表現登革熱病毒非結構蛋白 NS1 在 E.coli C41(DE3)和 C43(DE3) 表現系統... 37
表目錄
表 1 Comparison of amino acid sequence of dengue virus type 2 and PL046 strain(Accession No. AJ968413)... 53 表 2 Comparison of amino acid sequence of dengue virus type 3 and
H87 strain(Accession No. M93130) ... 53 表 3 Result of Western blot ... 54
圖目錄 壹、 緒論圖 圖 1.1 Flavivirus 之 RNA 基因結構 ... 55 圖 1.2 Flavivirus Polyprotein 之結構與在 ER 膜上的分佈... 55 圖 1.3 登革熱病毒外膜蛋白結構圖... 56 圖 1.4 登革熱病毒 NS1 疏水性分布圖... 56 圖 1.5 登革熱病毒 NS2B 疏水性分布圖與 NS2B-NS3 protease 於膜 上之示意圖... 57 圖 1.6 登革熱病毒 NS2B-NS3 protease 立體結構圖 ... 58 圖 1.7 登革熱病毒 NS4A 於膜上之 Topology 示意圖 ... 59 參、結果圖 圖 3.1 pET△5T-HAHis 質體建構示意圖與 HA3His6 定序分析.. 60
圖 3.2 pET△5T-D2E-HAHis, pET△5T-D2NS1-HAHis, pET△ 5T-D2NS1(d)- HAHis 質體 ... 61
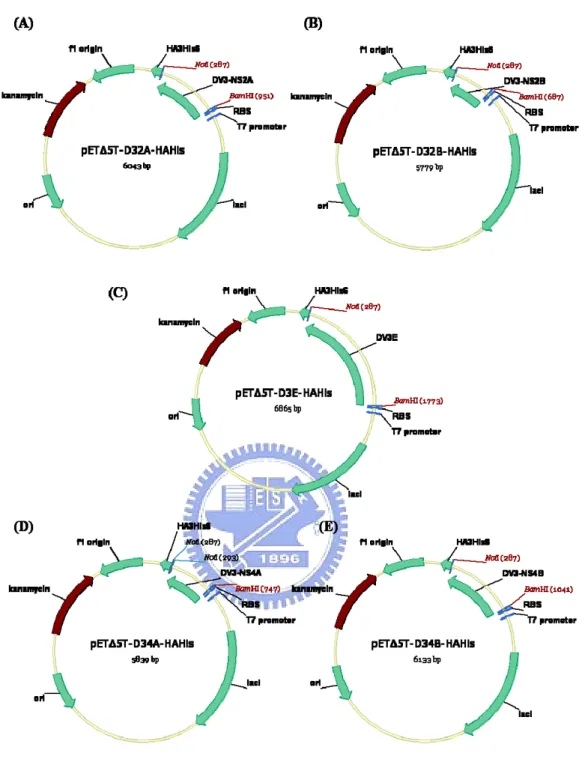
圖 3.3 pET△5T-D3NS2A-HAHis, pET△5T-D3NS2B-HAHis, pET △5T-D3NS4A-HAHis, pET△5T-D3NS4B-HAHis, pET△ 5T-D3E-HAHis 質體... 62 圖 3.4 限制酶酵素切割 pET△5T-HAHis ... 63 圖 3.5 限制酶酵素切割 pET△5T-D22A-HAHis, pET△5T-D22B-HAHis, pET△5T-D24A-HAHis, pET△5T-D24B-HAHis 質體 ... 64 圖 3.6 限制酶酵素切割 pET△5T-D32A-HAHis, pET△5T-D32B-HAHis, pET△5T-D34A-HAHis,
圖 3.7 限制酶酵素切割 pET△5T-D2E-HAHis,
pET△5T-D3E-HAHis, pET△5T-D2NS1-HAHis,
pET△5T-D2NS1(d)-HAHis 質體... 66 圖 3.8 限制酶酵素切割 pET-30a(+), pET-30a(+)-D2NS1-HAHis 質
體... 67 圖 3.9 DV2-NS2A 在 E.coli C41(DE3)與 C43(DE3)的蛋白質表現
... 68 圖 3.10 DV3-NS2A 在 E.coli C41(DE3)與 C43(DE3)的蛋白質表現
... 69 圖 3.11 DV2-NS2B 在 E.coli C41(DE3)與 C43(DE3)的蛋白質表現
... 70 圖 3.12 DV3-NS2B 在 E.coli C41(DE3)與 C43(DE3)的蛋白質表現
... 71 圖 3.13 DV2-NS4A 在 E.coli C41(DE3)與 C43(DE3)的蛋白質表現
... 72 圖 3.14 DV3-NS4A 在 E.coli C41(DE3)與 C43(DE3)的蛋白質表現
... 73 圖 3.15 DV2-NS4B 在 E.coli C41(DE3)與 C43(DE3)的蛋白質表現
... 74 圖 3.16 DV3-NS4B 在 E.coli C41(DE3)與 C43(DE3)的蛋白質表現
... 75 圖 3.17 DV2-E 在 E.coli C41(DE3)與 C43(DE3)的蛋白質表現 ... 76 圖 3.18 DV3-E 在 E.coli C41(DE3)與 C43(DE3)的蛋白質表現 ... 77 圖 3.19 DV2-NS1 在 E.coli C41(DE3)與 C43(DE3)的蛋白質表現
... 78 圖 3.20 DV2-NS1 在 E.coli B21(DE3)的蛋白質表現 ... 79 圖 3.21 DV2-NS1(d)在 E.coli C41(DE3)與 C43(DE3)的蛋白質表現
圖 3.22 DV2-NS1 在 E.coli C41(DE3)與 C43(DE3)的蛋白質表現
... 81
附錄目錄 附錄 1 Site-Directed Mutagenesis Kit ... 82
附錄 2 TA cloning Kit ... 83
附錄 3 pGEM-T 質體之 map ... 84
附錄 4 ExcelPureTM Plasmid Miniprep Purification Kit... 85
附錄 5 PCR Clean-up/Gel Extraction Kit ... 86
附錄 6 pET-30a(+)質體之 map... 88 附錄 7 pETΔ5T 質體之示意圖 ... 89 附錄 8 pETΔ5T-D22A-HAHis, pETΔ5T-D2B-HAHis, pETΔ5T-D24A-HAHis 與 pETΔ5T-D22A-HAHis 質體示意 圖... 90 附錄 9 pcDNA3-NCS/DV2FL-PL046-S 與 pcDNA3/DV3/1029-10696/fix5 示意圖 ... 91
縮寫(Abbreviation)
APS Ammonium Persulfate
C protein Capsid protein
CMV Cytomegalovirus
DENV Dengue virus
DF Dengue fever
DHF Dengue hemorrhagic fever
DNA Deoxyribonucleic acid
DSS Dengue shock syndrome
DTT 1,4-Dithiothreitol
E.coli Escherichia coli
EDTA Ethylenediaminetetraacetic acid
E protein Envelope protein
EtBr Ethidium bromide
HA-His Hemagglutinin-polyhistidine protein
HPR horseradish peroxidase
IPTG Isopropyl–β–D-thiogalactoside
KUNV Kunjin virus
LB broth Luria-Bertani broth
NS protein Non-structure protein
ORF Open reading frame
PCR Polymerase chain reaction
PMSF Phenyl methyl sulfonyl fluoride
prM protein Precursor membrane protein
RNA Ribonucleic acid
SDS Sodium dodecyl sulfate
SDS-PAGE Sodium dodecyl sulfate polyacrylamide gel electrophoresis
TAE Tris-acetate-EDTA
TBS Tris-buffered saline
TEMED N, N, N’, N’,-tetramethylenediamine
Tween-20 Polyoxyethene-sorbitan monolaurate
UTR Untranslated region
WNV West Nile virus
X-gal 5-bromo-4-chloro-3-indolyl-beta-D-galactopyranoside
壹、緒 論
1.1 登革熱病毒
登 革 熱 病 毒 (Dengue virus, DENV)在分類學上屬於黃質病毒科
(Flaviviridae)的黃質病毒屬(Flavivirus)。病毒直徑大小約為 50 nm (Henchal and Putnak, 1990)。黃質病毒屬的病毒的傳播影響人類的健康,主 要經由蚊蟲或壁蝨(tick)等節肢動物傳染,除了登革熱病毒(DENV), 黃熱病毒(yellow fever virus, YFV)、West Nile virus(WNV)、Kunjin virus (KUNV)、日本腦炎病毒(Japanese epcephalitis virus)與 Tick-borne epcephalitis virus 等也屬於 Flavivirus。
登革熱病毒可分為四種血清型(serotype)DENV-1~DENV-4,藉由埃 及斑蚊(Aedes aegypti)及白線斑蚊(Aedes albopictus)叮咬宿主的途徑進 而傳播給人類並引發疾病,臨床症狀可能為無症狀(asymptomatic),或依
其嚴重程度可區分為三種:登革熱(Dengue fever, DF)、登革出血熱(Dengue
hemorrhagic fever, DHF)以及登革休克(Dengue shock syndrome, DSS)等 (Clyde et al., 2006)。登革熱(DF)主要病徵類似流行性感冒,主要為發 燒、頭痛、眼窩疼痛、肌肉關節痠痛。登革出血熱(DHF)的病徵與登革 熱相同,並且會增加血管的通透性,導致血漿漏出(plasma leakage)、血 小板減少(thrombocytopenia)與紅血球濃縮(hemoconcentration)的症狀 發生,嚴重者將有休克性的現象(DSS),無妥善處理將導致死亡。 登革熱病毒於西元 1779~1780 年在主要擴及熱帶及亞熱帶地區爆發流 行,在1950 年代,由原本 9 個遭受登革熱病毒感染的國家,如今已經分布
超過100 多個國家,根據世界衛生組織(World Health Organization, WHO)
的統計數據顯示,全球約超過 25 億的人口曾經遭受登革熱病毒的感染,
DF/DHF 的感染率在西元 1950~1959 年之中,由每年平均增加 908 個病患;
到了西元 1990~1999 年,每年約有 50 萬 DHF/DSS 病患住院治療,約有 5
1.2 登革熱病毒的基因結構
登革熱病毒為正向單股的RNA 病毒(positive single stranded RNA virus)
且具外膜的病毒。基因體全長約 11 kb,在 5’端有 type I cap 結構-
m7GpppAmpN2,不同於一般的 mRNA,其 3’端則是缺乏 Poly A 序列
(polyadenylated tail)(Cleaves and Dubin, 1979; Wengler et al., 1978)。基
因體具有單一個 open reading frame(ORF),在 5’端以及 3’端各有一個
noncoding region(NCR),兩端之 NCR 含有 stem-loop(SL)可以協助 RNA 轉譯以及複製,3’端 SL 和許多蛋白質之間有交互作用,如病毒 replicase 相
關的蛋白質NS3 與 NS5,在 DENV-4 與 WNV 中的研究中,發現 elogation
factor 1A(EF1A)能與 3’端 SL 結合(Blackwell et al., 2004; De Nova-Ocampo et al., 2002)。【圖 1.1】
1.3 登革熱病毒基因轉譯
Flavivirus 運用許多機制去協助蛋白質轉譯的進行,如上述所提及的 5’
端與3’端 NCR 等特殊結構。轉譯的起始為 cap dependent,並能幫助 ribosomal
scanning,不過有研究發現 DENV 會運用未知的機制,在抑制 cap dependent
的情況下亦能進行蛋白質轉譯(Edgil et al., 2003)。以蚊子當媒介的
Flavivirus 因缺乏 Kozak motif 序列,對於起始密碼 AUG 的辨識缺乏專一性,
由於DENV 之 capsid coding region(cHP)上具有 RNA hairpin 的結構,協
助核醣體(ribosome)能從 first AUG 進行起始轉譯(Clyde and Harris, 2005)。
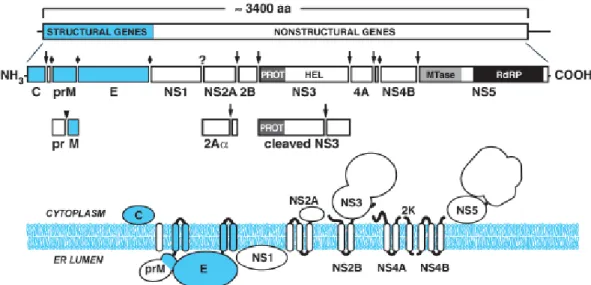
病毒的基因體擁有單一個 ORF,因此會轉譯出一個單一的 polyprotein,
經由轉譯後切割,成為10 個蛋白質。Polyprotein 的 N 端區域編碼三個結構
蛋白(structural protein)C- prM- E,分別為衣殼蛋白(capsid protein, C)、 前驅膜蛋白(precursor membrane protein, prM)以及外膜蛋白(envelope protein, E),其餘區域編碼非結構蛋白(nonstructural protein)NS1- NS2A- NS2B- NS3- NS4A- 2K- NS4B- NS5(Lindenbach et al., 2003; Miller et al.,
2007),其中 Transmembrane domain 2K 序列位於 NS4A 的 C 端。Polyprotein
內的peptidase 負責切割 C/prM、prM/E、E/NS1 與 2K/NS4B;病毒的 serine peptidase 負責切割 NS2A/NS2B、NS2B/NS3、NS3/NS4A、NS4A/2K 與 NS4B/NS5 的蛋白質連結。NS1/NS2A 的蛋白質切割所使用的酵素目前還未 知(Lindenbach et al., 2007)。【圖 1.2】
衣殼蛋白(C)會包住病毒的 RNA,形成雙體(dimer),其結構中包含 四個α-helixes(Dokland et al., 2004; Jones et al., 2003; Ma et al., 2004),衣殼
蛋白的雙體結構是如何組成nucleocapsids 的機制目前還不明確,RNA 與衣
殼蛋白間的交互作用有助於形成類似nucleocapsids 的結構(Kiermayr et al.,
2004)。前驅膜蛋白(prM)與外膜蛋白(E)同屬於醣蛋白(glycoprotein), 前驅膜蛋白會幫助外膜蛋白摺疊與組裝(Brock et al., 1992),前驅膜蛋白經 切割後會形成膜蛋白(M),膜蛋白和外膜蛋白同為鑲嵌在病毒外套上的蛋 白質(Mukhopadhyay et al., 2005)。 非結構性蛋白最主要的功能在於複製病毒RNA,NS3 是一個具有多功 能性的蛋白質,含有protease 以及 RNA 複製活性,其蛋白質 N 端約 1/3 的
大小含有 catalytic domain 將形成 NS2B-NS3 serine protease 以便進行
polyprotein 的修飾(Bazan et al., 1989; Chambers et al., 1990; Gorbalenya et al., 1989)。
NS5 擁有 7 個 motifs,C 端 2/3 的位置擁有 RNA-dependent RNA polymerase 活性,而 N 端的 2 個 motifs 則具有 methyltransferase(MTase) 活性(Koonin EV, 1993),為 S-adenosyl-methionine dependent MTase,研究
指出DENV-2 之 NS5 的 N 端能轉移 S-adenosyl-methionine 上的甲基(methyl
group)至受質 RNA 上,修飾 5’ cap 的功能(Egloff et al., 2002)。
1.4 外膜蛋白 E 之特性
E protein(約 53 kDa),是flavivirus 病毒顆粒表面主要的蛋白質,E 是
以膜蛋白 type I 的形式所合成,並且具有 12 個 cysteine 以利形成雙硫鍵
I 是 E proein 的中央區域並形成 β- barrel;domainⅡ含有和另外一個 E protein
形成雙體的區域,並且含有一個fusion peptide(fusion peptide 與病毒感染宿
主細胞有關); 而 domain I 的另一端則與 domain Ⅲ接合,domain Ⅲ含有 receptor-binding 的活性是一個 immunoglobulin(Ig)-like domain,可和宿主 細胞受體結合,能被抗體所辨識並且能抑制病毒的侵入(Lindenbach et al., 2007, Nybakken et al., 2005)。【圖 1.3】
E protein 於自然狀態下會形成雙體結構,在低 pH 值的環境下,E protein
的雙體結構(dimer)會分離成單體(monomer),之後形成三體結構(trimer)。
其機轉還不明確,但此三體的ectodomains 有助於與細胞膜融合(Bressanelli
et al., 2004; Modis et al., 2004)。
1.5 非結構蛋白 NS1 之特性
醣蛋白 NS1(約 45 kDa)主要位於 ER 的內部,共有三種表現形式:
位 於 replication complex 、 membrane-anchored 以 及 分 泌 於 胞 外 等 形 式
(Lindenbach et al., 2003)。利用宿主體內的 signal peptidase 使 NS1 與 E protein 分離,位於 ER 內部的酵素則可分離 NS1/2A 的鍵結(Falgout et al.,
1989; Falgout and Markoff, 1995)。NS1 會大量的存在於被感染的細胞中,並
且發現位於細胞表面的 NS1 將會被哺乳細胞緩慢的分泌出去(Lindenbach
and Rice, 2003)。
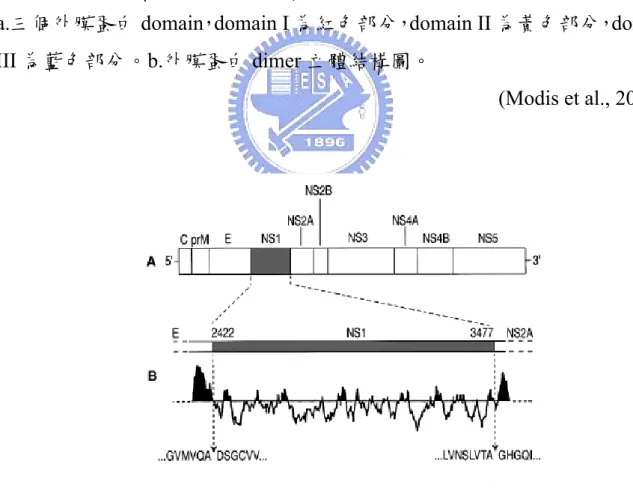
Flaviviruses 在 NS1 結構當中含有 2~3 個 N-linked glycosylation sites 與 12 個 conserved cysteine(Lee et al., 1989; Mason PW, 1989; Smith et al., 1970)。已知在 dengue virus 的 glycosylation sites 位於 N130 以及 N207,為 病毒複製所必須(Crabtree et al., 2005),而 NS1 參與 RNA 複製過程中的角
色並不明確,但有研究指出,若將NS1 之 N-linked glycosylation sites 做突
變,將抑制RNA 的複製以及病毒顆粒的產生(Crabtree et al., 2005; Muylaert
et al., 1996)。NS1 與 NS4A 之間的作用也是 replicase 運作所必須(Lindenbach
and Rice, 1999)。
傾向於附著於膜上(Winkler et al., 1988; Winkler et al., 1989)【圖 1.4】。NS1
具有高度的疏水性特質以及缺乏 transmembrane domains,但為何是和膜有
關的蛋白質,其機制目前還不明確。推測可能是dimerization 在蛋白質表面
創造出一個疏水性的區域以利於和膜產生疏水性鍵結的作用(Lindenbach et
al., 2007)。儘管前人的研究指出 NS1 為分泌到細胞外必須經由 dimerization
(Pryor and Wright, 1993),但也有研究指出,將 Kunjin virus(KUNV)之 NS1 做蛋白質突變,使其產生結構不穩定之 dimer 結構但仍然可以被細胞所 分泌到胞外(Hall et al., 1999)。被分泌到胞外的 NS1 將形成可溶性的 hexameric particles(約 11 nm),由三個具有 dimer 形式的 NS1 蛋白經由疏 水性鍵結(hydrophobic interaction)而成(Crooks et al., 2005; Flamand et al.,
1999)。此種形式的NS1 會被運送到 hepatocytes 以及 late endosome 中堆積,
並且會提高flavivirus 的感染性(Alcon-LePoder et al., 2005)。
1.6 非結構蛋白 NS2A 的特性
NS2A 是一個較小的疏水性蛋白質(約 22 kDa),其N 端與 NS1 相接,
透過宿主ER 內部未知的酵素分離 NS1-2A(Falgout and Markoff, 1995)。
NS2A/2B 暴露於細胞質中,會與 NS2B-NS3 serine protease 作用而分割, NS2A 之 C 端與 serine protease 作用後將形成 NS2Aα(Chambers et al, 1990; Nestorowicz et al., 1994)。在 Yellow Fever Virus(YFV)中,若將 NS2Aα
之cleavage site 做突變,將會影響之後病毒顆粒之組裝,但若在 NS3 helicase
domain 也進行突變,便會抵消突變 NS2A 所造成的效果(Kummerer and Rice, 2002)。KUNV 的 NS2A 亦會參與 RNA 的複製,並與 replicase 中的 NS3 與 NS5 有交互作用(Mackenzie et al., 1998)。
在免疫學上的研究指出 Interferon(IFN)可以抑制病毒的感染。在
Dengue virus type 2 中 , 發 現 NS2A 會 抑 制 IFN 在 細 胞 內 的 訊 號
(Munoz-Jordan et al., 2003),進一步研究指出,若將KUNV 以及 West Nile
將KUNV 之 NS2A 做突變,在 IFN 勝任細胞(IFN competent cell lines)的
實驗中,會提升KUNV 中複製子(replicon)的活性並且持續性地進行病毒
RNA 的複製(Liu et al., 2004)。
1.7 非結構蛋白 NS2B 的特性
NS2B是一個小分子量的膜蛋白(約14 kDa),會與NS3 serine protease
形成一個穩定的結構:NS2B-NS3 serine protease。NS2B同時也是NS3 serine
protease的cofactor,其角色與C型肝炎病毒(Hepatitis C virus)中的NS4A作 用相似(Falgout et al., 1991)。Cofactor的活性位置約位於整條peptide的中 心,由40個胺基酸所組成,一般稱為serine protease domain(或cofactor
domain),而其中具有疏水性的12個胺基酸(70 GSSPILSITISE 80)可能與NS3
的結合有關,(Brinkworth et al., 1999; Erbel et al., 2006)。進一步研究發現,
若將NS2B之conserve residue突變,將會造成蛋白質反切(transcleavage)的 活性,使NS2B/NS3分離(Chambers et al., 2005; Niyomrattanakit et al., 2004)。【圖1.5, 圖1.6】
1.8 非結構蛋白 NS4A 的特性
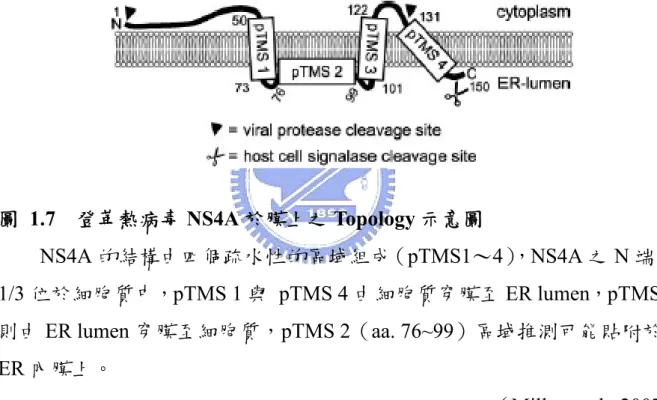
NS4A 是一個疏水性蛋白質(約 16 kDa),與NS1 交互作用並且與病毒
的RNA 複製有關(Lindenbach and Rice, 1999; Mackenzie et al., 1998)。NS4A
的結構由四個疏水性的區域組成(pTMS1~4)【圖1.7】,由於 Flavivirus 感
染細胞時會產生膜重排(cytoplasmic membrane rearrangement)的現象,以
提高病毒感染,而NS4A 其 C 端的 transmembrane domain 2K(圖 1.7 中之
pTMS4),被發現與膜重排有關。研究發現在 KUNV 中,NS4A/2K/NS4B
的連結經由 NS2B-NS3 serine protease 作用切割,可以切斷 2K/NS4B 的連
結,這將影響膜重排的起始,若是將NS4A 蛋白質 C 端的 2K 序列切除,將
會降低細胞膜重排的現象,而被切除2K 序列之 NS4A 則會被運送到高基氏
1.9 非結構蛋白 NS4B 的特性
NS4B亦是一個疏水性蛋白質(約27 kDa),其胺基酸序列在登革熱病毒
各個血清型間約有78~85%的相似度,研究發現NS4B、NS3與雙股RNA會一 同位於ER的膜上,推測NS4B與病毒的RNA複製有關(Miller et al., 2006; Westaway et al., 2002)。進一步研究指出,利用酵母菌雙雜交法(yeast two-hybrid assay)發現NS4B會與NS3的C端(aa 303~618)的helicase motif 結合,而NS3的C端的helicase motif也和RNA的結合有密切的關係,單一的 NS4B分子無法順利的與NS3和ssRNA結合,因此推測至少有兩個NS4B分子 構成oligomer後才能順利的與NS3和ssRNA結合。(Umareddy et al., 2006)。 如前面所述,NS2A 與 interferon(IFN)與細胞內的訊號抑制有關 (Munoz-Jprdan et al., 2003)。在 DENV 中 NS4B 同樣也能抑制 interferon (IFN)在細胞內的訊號,尤其對於 IFN-β 與 IFN-γ 具有強力的抑制作用 (Munoz-Jprdan et al., 2005)。
1.10 表現登革熱蛋白質的系統-大腸桿菌 C41(DE3)與 C43(DE3)菌株
為了研究登革熱蛋白質的功能,首先必須將蛋白質大量表現(over-
express),將DENV-2 PL046 strain 與 DENV-3 H87 strain 欲表現的結構與非
結構蛋白質基因建構成於適合的質體(plasmid),利用大腸桿菌(E.coli)
表現系統表現蛋白質,本實驗所運用的大腸桿菌為C41(DE3)與 C43(DE3)
菌株,可用來大量產生膜蛋白,從突變之大腸桿菌 E.coli BL21(DE3)而
來,在蛋白質表現方面,可以有效改善在BL21(DE3)中表現不佳的情形
(Miroux and Walker , 1996),此兩種菌株和一般 BL21(DE3)的不同點在
於在大量表現蛋白質(over-expression)的同時,於菌株體內會伴隨著增生
內膜(proliferation of intracellular membrane),所產生的蛋白質會附著於此
內膜上,並且降低inclusion body 的產生(Arechaga et al., 2000),此外,
此兩種菌株通常用於大量表現對宿主細胞有毒害的蛋白質並能避免宿主 細胞死亡,且有穩定質體的作用(Dumon- Seignovert et al., 2004),由於登
C41(DE3)與 C43(DE3)菌株表現登革熱病毒中具有疏水特性的蛋白質, 將蛋白質大量表現純化並製造專一性抗體,用於於病毒顆粒或感染細胞株 的偵測等功能性研究,以利於進一步探討蛋白質的生化功能。
貳、材料與方法
2.1 實驗材料
2.1.1 菌株(Bacteria Strains)
Escherichia coli DH5α (Yang laboratory collection) Escherichia coli BL21(DE3) (Yang laboratory collection) Escherichia coli C41(DE3)
(Yang laboratory collection; gift from Dr. Chin-Hsiang Leng) Escherichia coli C43(DE3)
(Yang laboratory collection; gift from Dr. Chin-Hsiang Leng)
2.1.2 病毒(Viruses)
PL046 strain(Dengue virus type 2 Taiwan local strain) H87 strain(Dengue virus type 3 strain)
2.1.3 質體(Plasmids) 質體名稱 特性 Reference pcDNA3 篩選標誌為Ampicillin,並含 T7 promoter 及 CMV promoter Invitrogen pET-30a(+) 篩選標誌為Kanamycin,並含 T7 promoter、His-tag 及 S-tag 序列 Novagen
pGEM-T Vector 本研究用於TA cloning Promega
pcDNA3-NCS/DV2FL-PL04 6-S pcDNA3 含有 PL046 strain 全長 的cDNA Yang laboratory collection
pcDNA3/DV3/1029-10696/ fix5 pcDNA3 含有 H87 strain 全長的 cDNA Yang laboratory collection pET△5T pET-30a(+)的 N-terminal His-tag
及S-tag 序列被切除 楊馥嘉, 2006 交大碩 士論文;Yang laboratory collection pET△5T-HAHis pET-30a(+)的 N-terminal His-tag
及S-tag 序列被切除,並含有 HA-tag 及 His-tag 序列 本研究 pET△5T-D22A-HAHis pET△5T-D22B-HAHis pET△5T-D24A-HAHis pET△5T-D24B-HAHis pET△5T 上含 PL046 strain 的 NS2A、2B、4A 以及 4B 基因, 3’端帶有 HAHis-tag,其 5’端及 3’ 端cloning site 為 Bam HI 及 Xba I
楊馥嘉, 2006 交大碩士論 文;Yang laboratory collection pET△5T-D2E-HAHis pET△5T-HAHis 上含 PL046 strain 的 E 基因,3’端帶有 HAHis -tag,其 5’端及 3’端 cloning site 為 Eco RV 及 Not I 本研究 pET△5T-D32A-HAHis pET△5T-D32B-HAHis pET△5T-D34A-HAHis pET△5T-D34B-HAHis pET△5T-D3E-HAHis pET△5T-HAHis 上含 H87 strain 的NS2A、2B、4A、4B 以及 E 基因,3’端帶有 HAHis-tag,其 5’
端及3’端 cloning site 為 Bam HI
及 Not I
pET△5T-D2NS1-HAHis
pET△5T-HAHis 上含 PL046 strain 的 NS1 基因,3’端帶有 HAHis-tag,其 5’端及 3’端 cloning site 為 Bam HI 及 Not I
本研究 pET△5T-D2NS1(d)-HAHis pET△5T-HAHis 上含 PL046 strain 的截短型 NS1 基因(a.a. 1~723),3’端帶有 HAHis-tag, 其5’端及 3’端 cloning site 為 Bam HI 及 Not I 本研究 pET-30a(+)-D2NS1-HAHis pET-30a(+)上含 PL046 strain 的 NS1 基因,3’端帶有 HAHis- tag,其 5’端及 3’端 cloning site 為 Bam HI 及 Xho I 本研究 2.1.4 引子(Primers) 2.1.4.1 針對建構質體所設計的引子 引子 序列5’~3’ 位置 HAHis-F’ TTTGCGGCCGCA{TACCCATACG A} HAHis gene(from pET△5T-D24B-HAHis) nucleotide:+5864~+5874 HAHis-R TTTCTCGAGTCACTA{GCCATG GTGA} HAHis gene(from pET△5T-D24B-HAHis) nucleotide:+5968~+5977 DV2-E-F TTTGCGGCCGC{GGCCTGCACC ACGACTCC} DV-2 (PL046; AJ968413) nucleotide:+2404~+2421 DV2-E-R TTTGATATC{ATGCGTTGCATAG GAATATC} DV-2 (PL046; AJ968413) Nucleotide:+937~+956
DV3-2A-F TTTGGATCCATG{GGGAGTGG AAAGG} DV-3 (H87; M93139) nucleotide: +3470~+3482 DV3-2A-R TTTGCGGCCGC{TCTCCTTTTG AGT} DV-3 (H87; M93139) nucleotide: +4111~+4123 DV3-2B-F TTTGGATCCATG{AGCTGGCC ACTGAAT} DV-3 (H87; M93139) nucleotide: +4124~+4138 DV3-2B-R TTTGCGGCCGC{TCTTTGGGTT TG} DV-3 (H87; M93139) nucleotide: +4502~+4513 DV3-4A-F TTTGGATCCATG{TCAATCGCC CTTGA} DV-3 (H87; M93139) nucleotide: +6371~+6384 DV3-4A-R TTTGCGGCCGC{GGCCGCTACT ATT} DV-3 (H87; M93139) nucleotide: +6808~+6820 DV3-4B-F TTTGGATCCATG{AATGAAATG GGACTG} DV-3 (H87; M93139) nucleotide: +6821~+6835 DV3-4B-R TTTGCGGCCGC{TCTCTTTCCT GTTC} DV-3 (H87; M93139) nucleotide: +7551~+7564 DV3-E-F TTTGGATCC{ATGAGATGTGTG GGAGTAG} DV-3 (H87; M93139) nucleotide: +935~+953 DV3-E-R TTTGCGGCCGC{AGCTTGCAC CACGA} DV-3 (H87; M93139) nucleotide: +2400~+2413 DV2-NS1-F TTTGGATCCATG{GATAGTGGT TGCGTTG} DV-2 (PL046; AJ968413) nucleotide: +2422~+2437 DV2-NS1-R TTTGCGGCCGC{GGCTGTGAC CAAG} DV-2 (PL046; AJ968413) nucleotide: +3465~+3477 DV2-NS1-R705 TTTGCGGCCGC{CTCACTTTCT AGCACTCC} DV-2 (PL046; AJ968413) nucleotide: +3112~+3240
註:DV-2 基因的引子是根據前人賴建斈定序結果所設計(賴建斈, 2006, 交 大碩士論文)。DV-3 基因的引子根據 NCBI 網站核酸序列編號(H87; M93139)所設計。{}內的序列為模板所具有的序列;{}外的序列為外加 的DNA 序列;畫單底線為外加的酵素切位;粗體字部份為起始密碼或終止 密碼。 2.1.4.2 針對 Site-Directed Mutagenesis 所設計的引子 DV3-2B-a {GGACTTGTGAGCATTC}TA{GCTA GTTCTCT} DV-3 (H87; M93139) nucleotide: +4157~+4185 DV3-2B-b {AGAGAACTAGC}TA{GAATGCTCA CAAGTCC} DV-3 (H87; M93139) nucleotide: +4185~+4157 DV3-4A-a {TGATGATCTTGTTA}A{CAGGTGG AGCAATG} DV-3 (H87; M93139) nucleotide: +6549~+6577 DV3-4A-b {CATTGCTCCACCTG}T{TAACAAG ATCATCA} DV-3 (H87; M93139) nucleotide: +6577~+6549 註: DV-3 基因的引子根據 NCBI 網站核酸序列編號(H87; M93139) 所設計。{}內的序列為模板所具有的序列;{}外的序列為外加的DNA 序列。
2.1.5 藥品試劑
2.1.5.1 藥品
藥品名稱 製造公司 目錄編號 應用
1kb DNA ladder SibEnzyme SEM11C001 DNA 電泳
2-propanol Sigma I 9516 SDS-PAGE
Acetic acid Fluka 33209 Western blot
Acryl/Bis 37.5:1 solution AMRESCO 0254 Western blot
Agarose VEGONIA 9201-05 核酸電泳
Ampicillin Applichem A0839 細菌培養
APS Bio-Rad 161-0700 SDS-PAGE
Coomassie Brilliant Blue R-250 J.T.Baker F792-01 蛋白質染色
Crystal Violet Sigma C-3886 DNA 染色
DTT(1,4-Dithiothreitol) Uni-region UR-DTT-15g 蛋白質製備
HRP substrate MILLIPORE WBKLS0500 Western blot
EtBr Sigma E-7637 DNA 染色
Ex Tag polymerase TaKaRa RR001B PCR
IPTG
(isopropyl–β–D-thiogalactoside)
MDBio,Inc. 105039 細菌培養
Kanamycin Sigma K4000 細菌培養
LB agar Alpha Biosciences L12-111 細菌培養
LB broth Scharlau 02-385 細菌培養
Methanol Mallinckrodt 3016-08 Western blot
NaCl AMRESCO 0241 緩衝液
NaOH Riedel-de Haën 30620 緩衝液
Nitrocellulose Transfer Membrane Schleicher&Schue ll
10401396 Western blot
Prestain Protein marker TBB 0901 SDS-PAGE
Restriction enzyme Biolab ─ 建構質體
SDS Riedel-de Haën 62862 Western blot
T4 DNA ligase Fermentas 1812 建構質體
Tris(base) AMRESCO 0826 Western blot
TEMED Sigma T-9281 Western blot
Tween-20 Sigma P-1379 Western blot
Urea Fluka SK-2644U 蛋白質製備
X-film Midwest Scientific
LA7111 Western blot
X-gal MDBio,Inc. 613049 細菌培養
β-mercaptoethanol MERCK 1.1543.0100 蛋白質製備
2.1.5.2 抗體
抗體名稱 製造公司 目錄編號
HA-probe(F-7)HRP Santa Cruz SC-7392
6xHis Monoclonal Antibody BD
Biosciences 8916-1
2.1.5.3 Kit
產品名稱 製造公司 目錄編號 應用
pGEM®-T and pGEM®-T Easy Vectors
Promega A3600 TA cloning
QuikChange® XL Site-Directed Mutagenesis Kit
STRATAGENE 200519 修補DNA
ExcelPureTM Plasmid Miniprep Purification Kit
Premier N-PM050 抽取小量質體
PCR Clean-up/Gel Extraction Kit
Premier N-DCE050 純化 DNA
2.1.6 溶劑及緩衝液之配方
z 0.25 % Coomassie blue stain solution
2.5 g Coomassie brilliant blue,50 % methanol,10 % acetic acid added ddH2O to 1000 ml
z 0.5 % crystal violet solution (500 ml)
2.5 g crystal violet,25 ml 37% formaldehyde,250 ml EtOH,4.25 g NaCl
z 10X SDS-PAGE running buffer
0.25 M Tris base,1.92 M Glycine,1 % SDS z 10X Transfer buffer
39 mM Glycine,48 mM Tris base,10 % SDS,20 % methanol z 2X SDS-PAGE loading buffer
0.5 % bromphenol blue,0.5 M Tris-HCl (pH 6.8) ,10 % SDS, 100 % glycerol
z 50X TAE buffer
48.4 g Tris base,0.5 M EDTA (pH 8.0) 20 ml,11.42 ml acetic acid added dd H2O to 200 ml
z LB (Luria-Bertani)/Ampicillin 培養基
1 % tryptone,0.5 % yeast extract,1 % NaCl,1.5 % agar,50 μg/ml Ampicillin
z TBS buffer (Tris-buffered saline) 10 mM Tris(pH 8.0),150 mM NaCl z TBST buffer
10 mM Tris(pH 8.0),150 mM NaCl,0.05% Tween 20
2.1.7 主要儀器 -20℃直立冷凍櫃 (WHITE-WESTINGHOUSE) 4℃三門冰藏櫃 KS-101-MS (MINI KINGKON) -80℃超低溫冷凍櫃 925/926 (FORMA SCIENTIFIC) 水平式電泳槽 MJ-105 (MEDCLUB) 水平式震盪器 S-101 (FIRSTEK) 加熱攪拌器 PC-420 (CORNING)
半乾式電泳轉印槽 TRANS-BLOT® SD CELL 221BR (BIO-RAD)
低溫培養箱701 (WISOOM)
往復式恆溫水槽 B206-T1 (FIRSTEK SCIENTIFIC) 直立式電泳槽(Bio-Rad)
恆溫式震盪培養箱 S300R (FIRSTEK SCIENTIFIC)
核酸計算儀 GeneQuant pro (AMERSHAM PHARMACIA BIOTECH )
桌上型低溫高速離心機Centrifuge 5415 R (eppendorf)
桌上型高速離心機5100 (KUBOTA CORPORATION)
程式溫度控制儀 PTC-100TM (MJ RESEARCH INC.)
微量離心機 MICRO 240A (DENVILLE SCIENTIFIC INC.)
落地型高速離心機 Avanti® J-E Centrifuge (BECKMAN)
電子天秤 PB153-S (METTLER TOLEDO) 電子防潮箱 DX106 (台灣防潮科技)
電泳影像處理系統 GEL DOC 2000 (BIO-RAD) 酸鹼值檢測計 Φ360 (BECKMAN)
震盪器 VORTEX-GENIE2 G560 (SCIENTIFIC INDUSTRICS)
2.2 實驗方法
2.2.1 大腸桿菌勝任細胞(Competent cell)的製備
首先取 Escherichia coli C41(DE3)與 C43(DE3)之單一菌落培養於 5 ml 的 LB 培養液,於 37℃下震盪培養(160 rpm/min)過夜後,取 2 ml 的菌液轉養於 50 ml 的 LB 培養液中,繼續於 37℃下震盪培養(160 rpm/min),直到OD600nm 介於 0.4 到 0.6 之間。將培養好的菌液轉移至 50 ml 離心管中,置於冰上 20 分鐘,之後在 4℃下以 1620 ×g 離心 10 分鐘 後倒去上清液,接著以25 ml 4℃預冷的 0.1 M CaCl2懸浮菌體,置於冰上 30 分鐘,在 4℃下以 720 ×g 離心 10 分鐘後去除上清液,以 5 ml 4 ℃預 冷的0.1 M CaCl2懸浮菌體,於4 ℃靜置 18 小時,在 4℃下以 720 ×g 離 心5 分鐘後去除上清液,以 5 ml 預冷的 0.05 M CaCl2(含15 % Glycerol) 懸浮菌體。將菌液以每管 100 μl 分裝至預冷好的微量離心管中,迅速儲 存於-80 ℃冰箱保存備用。 2.2.2 大腸桿菌轉形作用(transformation) 將儲存於-80 ℃的勝任細胞取出置於冰上解凍後,加入0.1~1 μg的質 體DNA充分混合,置於冰上25分鐘,再置於42 ℃水浴中進行熱休克(heat shock)1分鐘,之後加入 500 μl 的LB培養液於37 ℃震盪培養(160 rpm/min) 1小時,取100 μl 的菌液均勻塗布於含Ampicillin(50 μg/ml)
之LB培養基上,置於37 ℃恆溫箱中培養12~16小時。 2.2.3 建構質體 DNA 將所設計的引子(Primers)經由聚合酶連鎖反應(PCR , Polymerase Chain Reaction),透過每個引子 Tm 值的不同條件設計反應溫度,將欲得到 的 DNA 片 段 合 成 出 來 , 而 DV3-NS2B 與 DV3-NS4A 的 模 板 基 因 (pcDNA3/DV3/1029-10696/fix5 ) 因 含 有 deletion 的 現 象 , 因 此 利 用
Site-Directed Mutagenesis Kit 修補 deletion 的部分【附錄 1】,反應完成後利
用洋菜膠電泳確認PCR 產物片段大小是否正確,之後利用 PCR Clean- up Kit
(PREMIER)純化 DNA 以去除酵素及鹽類。
經 Clean-up 且確認 DNA 大小無誤之 PCR 產物,使用 pGEM-T Vector
Systems(Promega)進行 TA cloning 【附錄 2, 附錄 3】,使PCR 產物與 pGEM-T
Vector 接合(Ligation),以利於限制酵素作用,可用來進一步確認 PCR 產 物並加以保存。
2.2.4 小量質體 DNA 萃取
使用ExcelPureTM Plasmid Miniprep Purification Kit(PREMIER)抽取
並純化 E. coli 之質體 DNA。操作流程如下:將大腸桿菌接種於 5 ml 的 LB 培養液、於 37℃震盪培養箱中培養 12~16 小時之後,於室溫 1125 ×g 離心12 分鐘去除上清液,加入 200 μl Solution BufferⅠ 懸浮菌體並移置微 量離心管中,取200 μl Solution BufferⅡ 緩和地混合均勻後,加入200 μl Solution BufferⅢ 再次緩和地混合均勻,在室溫下以 16100 ×g 離心 5 分 鐘,取上清液至Mini-MTM Column,在室溫下以 16100 ×g 離心 1 分鐘, 倒掉收集管內液體,加入700 μl Washing buffer,在室溫下以 16100 ×g 離 心1 分鐘,倒掉收集管內液體,重複此步驟一次,再以室溫 16100 ×g 離 心2 分鐘,將 Mini-MTM Column 移至新微量離心管,置於 60 ℃的乾浴槽
於-20 ℃。【附錄 4】 2.2.5 限制酵素反應 為製備實驗所需的DNA 片段,取適量 DNA(約 0.5~10 μg)到適量 反應體積(約20 μl),以限制酵素切割(酵素的用量及反應溫度、時間都 依照廠商所提供的條件資料進行),原則上 1μg 的 DNA 是以 2U 的酵素 在適當的溫度作用2 小時至 3 小時,反應完成後,置於適當的溫度終止反 應(依廠商所提供的條件),利用洋菜膠體電泳分析。DNA 片段在經限制
酵素切割後,視需要以Gel Extraction Kit(PREMIER)或 PCR Clean-up Kit
(PREMIER)回收 DNA 並去除限制酵素及鹽類。【附錄 5】
2.2.6 萃取洋菜膠內之 DNA 片段
使用Gel Extraction Kit(PREMIER)萃取出洋菜膠內之 DNA 片段。
操作流程如下:將切下之洋菜膠 (約 50-200 mg),置於微量離心管內,加
入500 μl Binding Solution,60 ℃加熱至完全溶解後,將混合液移至 Gel-
MTM Column,以室溫 16100 ×g 離心 1 分鐘,倒掉收集管內液體,加入 700
μl Washing Buffer,以室溫 16100 ×g 離心 1 分鐘,倒掉收集管內液體,再
加入700 μl Washing Buffer,以室溫 16100 ×g 離心 1 分鐘,倒掉收集管內
液體,再以室溫16100 ×g 離心 3 分鐘,將 Gel-MTM Column 移至新微量離
心管,置於60 ℃的乾浴槽中 5 分鐘把多餘的酒精去除,再加入 30 μl Elution
solution 於 Gel-MTM Column 中,以室溫 16100 ×g 離心 1 分鐘後,將萃取
出之DNA 儲存於-20 ℃。【附錄 5】 2.2.7 重組蛋白在大腸桿菌之誘導表現 將質體轉形於大腸桿菌 BL21(DE3) 或 NovaBlue(DE3),隔天挑單一 菌落於含有Ampicillin(50 μg/ml)或 Kanamycin(50 μg/ml)之 LB 培養 液中於37 ℃培養箱震盪培養,隔夜後,取 1/100 之菌液轉養於 5 ml 的 LB 培養液中並於37 ℃培養箱震盪培養,至 OD 介於 0.6 到 0.8 之間時,
加入0.5 mM isopropyl-β-D- thiogalactoside(IPTG)誘導基因表現四小時。 2.2.8 大腸桿菌蛋白質之萃取 大腸桿菌經0.5 mM IPTG 誘導表現後,於室溫下以 1125 ×g 離心 12 分鐘後去除上清液,接著取200 μl 的 1M Tris-HCl(pH8.0)懸浮菌體並移 置微量離心管中,以16100 ×g 離心 3 分鐘後去除上清液,將此菌體之微 量離心管於液態氮及42 ℃恆溫水槽中來回反覆處理各 1 分鐘(共 6 次), 以打破細胞。然後再取150 μl 1M Tris-HCl(pH8.0, 含 1mM PMSF)懸浮, 在4 ℃下以 16100 ×g 離心 5 分鐘後,取上清液至另一微量離心管中。Pellet 則加入150 μl 1 M Tris-HCl(pH8.0, 含 1mM PMSF 與 8M Urea)再次懸 浮,冰浴1 小時,在 4 ℃下以 16100 ×g 離心 30 分鐘,取其 pellet 上清液 的部分至另一微量離心管中,最後再將所收集的pellet 與上清液各加入等
體積之2X SDS-PAGE loading dye(含 200 mM β-mercaptoethanol, 200mM
DTT 及 8M Urea)混合均勻,於室溫放置 30 分鐘以上後儲存於-20 ℃備 用。
2.2.9 以 SDS-PAGE 分析並以 Coomassie blue staining 及西方轉漬分析 (Western blot analysis)偵測蛋白質表現
2.2.9.1 SDS-PAGE 電泳
首先配製下層 14 % resolving gel,室溫靜置約 1 小時,膠凝後再配製上
層4% stacking gel,室溫靜置約 30 分鐘,待膠凝後移至 Mini-Protein 電泳槽
(Bio- Rad),加入 1X SDS-PAGE running buffer,接著將樣品以微量吸管置
入膠體之孔洞中,先以120 伏特跑膠直到樣品通過 stacking gel 成一直線後,
且以100 伏特電泳 2 小時直到適當位置。
2.2.9.2 Coomassie blue staining
30 分鐘,再以 Destain solution (30 % methanol,10 % acetic acid)褪染 膠體直到結果顯現後,以清水潤洗膠體,並取玻璃紙封膠並封乾保存。
2.2.9.3 西方轉漬分析(Western blot analysis)
SDS-PAGE 膠 體 電 泳 完 成 後 , 利 用 半 乾 式 ( semi-dry ) 轉 漬 槽
TRANS-BLOT® SD CELL 221BR(Bio-Rad)轉漬膠體上的蛋白質至硝基
纖維膜上(nitrocellulose membrane, PROTRAN, Schleicher& Schuell),以 0.09 安培進行 37 分鐘,之後把膜置入 20 ml Blocking buffer (5 % milk in 1X TBS buffer)於室溫下平面震盪 1 小時後,加入稀釋 1/1000 倍的之 6xHis 單株抗體(BD Bioscience)、HA-probe(F-7)HRP 抗體(Santa Cruz Biotechnology ) 或 NS1-monoclonal antibodies ( NS1-Mabs, abcan ) 於 Blocking buffer 中於室溫下平面震盪 1 小時以偵測有 HA-His 標誌的複合
蛋白,之後再以20 ml 之 1X TBST buffer 於室溫下平面震盪清洗 5 分鐘 3
次,(使用6xHis 單株抗體於 1X TBST buffer 清洗後加入稀釋 1/9000 倍之
Goat anti-mouse HRP(PIERCE),再以20 ml 之 1X TBST buffer 於室溫下
平面震盪清洗5 分鐘 3 次),最後將500 μl 之 HRP substrate (MILLIPORE) 均勻地加到硝基纖維膜上約 5 分鐘,在暗房內以 X 光底片進行壓片,取 出底片沖洗顯像。用夾子將底片浸入顯影液(Developer solution)中搖晃 約30 秒後,將底片換到清水中漂洗底片至底片中影像顯現完成,接著將 底片浸入定影液(Fixer solution)中約 1 分鐘直到底片定影完成,以水清 洗底片後晾乾保存。
參、結果
3.1 pET 5T△ -HAHis 質體之建構
pET 5T△ -HAHis 質體是由 pET-30a(+)質體而來,利用 NdeI 與 NcoI 將
pET-30a(+)的 N-terminal His-tag 及 S-tag 序列切除,接著進行 Klenow enzyme
fill-in 的方式將序列補齊接合,形成 pET 5T△ 質體(楊馥嘉, 2006, 交大碩
士論文)【附錄 7】。利用 PCR 反應方法以實驗室已有之 pET 5T△ -D24B-
HAHis 為模板得到 HA3His6 之基因片段(楊馥嘉, 2006, 國立交通大學碩士
論文),並分別在HA3 His6 基因之 5’端引入 Not I 切位、3’端引入 Xho I 切
位與轉譯終止密碼 TAGTGA,clone 入 pET 5T△ 質體中,所得到之質體命
名為 pET 5T△ -HAHis,此質體建構之示意圖於【圖 3.1】。利用 pET 5T△ -
HAHis 中的 Multiple cloning site 協助之後 DV-2 與 DV-3 的基因能建構於
pET 5T△ -HAHis 載體上,以利於蛋白質表現後的抗體的偵測。
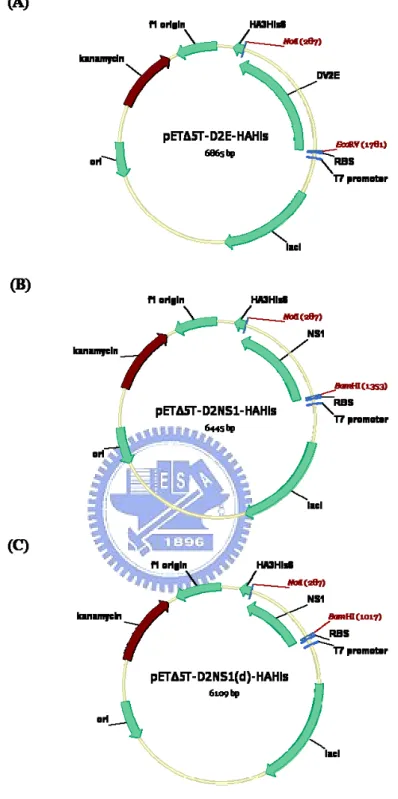
3.2 pET 5T△ -D2E-HAHis, pET 5T△ -D2NS1-HAHis, pET 5T△ -D2NS1(d) -HAHis pET-30a-D2NS1-HAHis 質體之建構
建構一pET△5T-HAHis 上分別含 PL046 strain 的 DV-2 E gene 以及 DV-2
NS1 gene 之質體,使其表達之 E protein 或 NS1 protein 的 C 端帶有 HAHis- tag。利用 PCR 方法以 pcDNA3 載體上含有 PL046 strain 全長的 cDNA 基因
之質體為模板(pcDNA3-NCS/DV2FL-PL046-S)【附錄9】,得到dengue virus
2(DV-2)之 E gene(nt.937 ~ 2421)以及 NS1(nt.2422~3477)片段,在 E gene 之 5’端引入 EcoR V 切位及在 3’端引入 Not I 切位,而 NS1 gene 與截短
型NS1(d) gene(nt.2422~3141, 由 NS1 全長基因 1056bp Æ 720bp)之 5’端
引入 BamHI 切位及在 3’端引入 Not I 切位,以協助之後能選殖於 pET 5T△ -
HAHis 載體,最後所得到之質體分別命名為 pET 5T△ -D2E-HAHis, pET 5T△ -
D2NS1-HAHis 以及 pET 5T△ -D2NS1(d)-HAHis,此質體建構之示意圖於【圖
3.3 pET△5T-D32A-HAHis, pET△5T-D32B-HAHis, pET△5T-D34A -HAHis, pET△5T-D34B-HAHis, pET△5T-D3E-HAHis 質體之建構
建構一pET△5T-HAHis 上含 H87 strain 的 DV-3 部分基因之質體,其
DV-3 部分基因包括 NS2A(nt.3470~4123), NS2B(nt.4124~4513), NS4A (nt.6371~ 6820), NS4B(nt.6821~7564), E gene(nt.935~2413)等。同樣
使其表達之基蛋白質的 C 端帶有 HAHis-tag。利用 PCR 反應方法以實驗室
已有之H87 strain cDNA clones 為模板(pcDNA3/DV3/1029-10696/fix5)【附
錄9】,得到 dengue virus 3(DV-3)之 NS 2、NS4 gene 以及 E gene 片段,
分別在 NS gene 之 5’端引入 BamH I 切位,E gene 在 5’端的切位則為
EcoRV,在 3’端引入 Not I 切位,以協助之後能選殖於 pET△5T-HAHis 載體,
最 後 所 得 到 之 質 體 分 別 命 名 為 pET 5T△ -D32A-HAHis, pET 5T△ -D32B-
HAHis,pET 5T△ -D34A-HAHis,pET 5T△ -D34B-HAHis,pET 5T△ -D3E-HAHis
,此質體建構之示意圖於【圖3.3】。
3.4 利用限制酵素以確認所建構之質體
【圖3.4.】為使用限制酵素切割 pET 5T△ -HAHis 質體所得之結果。Lane
1 為 MluI、NcoI 切割 pET 5T△ -HAHis 質體,可得到 4417 bp (圖中 A 所示)
和994 bp 之 band (圖中 B 所示)。
將實驗室已建構之質體加以確認 pET 5T△ -D22A-HAHis, pET 5T△ -
D22B-HAHis, pET 5T△ -D24A-HAHis, pET 5T△ -D24B-HAHis(楊馥嘉, 2006,
交大碩士論文)【圖3.5.】。
Lane 1 為 BamHI、NotI 切割 pET 5T△ -D22A-HAHis 質體,可得到 5260
bp (圖中 A 所示)、960 bp (圖中 B 所示); Lane 2 為 AflⅢ切割 pET 5T△ -D22A
-HAHis 質體,可得到 3123 bp (圖中 C 所示)、2101 bp (圖中 D 所示)及 996 bp
(圖中 E 所示)之 band; Lane 3 為 BamHI、NotI 切割 pET 5T△ -D22B- HAHis
質體,可得到5261 bp (圖中 F 所示)、696 bp (圖中 G 所示); Lane 4 為 MluI、
SpeI 切割 pET△5T-D22B-HAHis 質體,可得到 5008 bp (圖中 H 所示)、949 bp
質體,可得到5260 bp (圖中 J 所示)、756 bp (圖中 K 所示); Lane 6 為 BspHI
切割pET 5T△ -D24A-HAHis 質體,可得到 3423 bp (圖中 L 所示)、1417 bp (圖
中M 所示)、875 bp (圖中 N 所示) 及 301 bp (圖中 O 所示) 之 band; Lane
7 為 BamHI、NotI 切割 pET 5T△ -D24B-HAHis 質體,可得到 5260 bp (圖中 P
所示)、1050 bp (圖中 Q 所示); Lane 8 為 AflIII 切割 pET 5T△ - D24B-HAHis
質體,可得到 3168 bp (圖中 R 所示)、2101 bp (圖中 S 所示) 及 1041 bp (圖
中T 所示)之 band【附錄 8】。
【圖3.6】 Lane 1 為 BamHI、NotI 切割 pET 5T△ -D32A-HAHis 質體,
可得到5379 bp (圖中 A 所示)、664 bp (圖中 B 所示); Lane 2 為 XbaI 切割
pET 5T△ - D32A-HAHis 質體,可得到 5688 bp (圖中 C 所示)、355 bp (圖中
D 所示) 之 band; Lane 3 為 BamHI、NotI 切割 pET 5T△ -D32B-HAHis 質體,
可得到5379 bp (圖中 E 所示) 、400 bp (圖中 F 所示); Lane 4 為 NcoI 切割
pET 5T△ -D32B-HAHis 質體,可得到 5352 bp (圖中 G 所示)、427 bp (圖中 H
所示) 之 band; Lane 5 為 BamHI、NotI 切割 pET 5T△ -D34A-HAHis 質體,
可得到5379 bp (圖中 I 所示)、460 bp (圖中 J 所示); Lane 6 為 AflIII 切割
pET 5T△ -D34A-HAHis 質體,可得到 2788 bp (圖中 K 所示)、2101 bp (圖中
L 所示)、950 bp (圖中 M 所示) 之 band; Lane 7 為 BamHI、NotI 切割
pET 5T△ -D34B-HAHis 質體,可得到 5379 bp (圖中 N 所示)、754 bp (圖中 O
所示); Lane 8 為 AflIII、EcoRI 切割 pET 5T△ -D34B-HAHis 質體,可得到
3006 bp (圖中 P 所示)、2101 bp (圖中 Q 所示)、1026 bp (圖中 R 所示) 之 band。
【圖3.7】 Lane 1 為 EcoRV、NotI 切割 pET 5T△ -D2E-HAHis 質體,可
得到5371 bp (圖中 A 所示)、1494 bp (圖中 B 所示) ;Lane 2 為 AflIII 切割
pET 5T△ -D2E-HAHis 質體,可得到 2883 bp (圖中 C 所示)、2101 bp (圖中 D
所示)、1881bp (圖中 E 所示);Lane 3 為 BamHI、NotI 切割 pET 5T△ -D3E-
HAHis 質體,可得到 5379 bp (圖中 F 所示)、1486 bp (圖中 G 所示); Lane
4 為 XhoI 切割 pET 5T△ -D3E-HAHis 質體,可得到 5329 bp (圖中 H 所示)、
切割pET 5T△ -D2NS1-HAHis 質體,可得到 5268 bp (圖中 L 所示)、803 bp (圖
中M 所示)、347 bp (圖中 N 所示)之 band; Lane 7 為 BamHI、NotI 切割
pET 5T△ -D2NS1(d)-HAHis 質體,可得到 5377 bp (圖中 O 所示)、730 bp (圖
中P 所示); Lane 8 為 NcoI 切割 pET 5T△ -D2NS1(d)-HAHis 質體,可得到
5268 bp (圖中 Q 所示)、841 bp (圖中 R 所示)之 band。
【圖3.8】 Lane 1 為 MluI、XhoI 切割 pET-30a(+)-HAHis 質體,可得到
4404 bp (圖中 A 所示)、1018 bp (圖中 B 所示) ;Lane 2 為 BamHI、XhoI 切
割pET-30(a) -D2NS1-HAHis 質體,可得到 5382 bp (圖中 C 所示)、1194 bp (圖
中D 所示) ;Lane 3 為 AflII、MluI 切割 pET-30a(+)-D2NS1-HAHis 質體,
可得到4699 bp (圖中 E 所示)、1877 bp (圖中 F 所示)。
3.5 序列結果比對
將實驗室建構於質體中的insert 基因定序。此質體為以 pET 5T△ -HAHis
為骨架,所含的insert 為 Dengue virus 2 之 PL046 strain(DV-2 PL046)的非
結構蛋白(NS2A、NS2B、NS4A、NS4B、NS1)以及外膜蛋白(E)的全
長基因片段與 Dengue virus 3 之 H87 strain(DV-3 H87)的非結構蛋白
(NS2A、NS2B、NS4A、NS4B)以及外膜蛋白(E)的全長基因片段。其 5’端及 3’端有藉由 PCR 引入之 cloning sites:Xho I 及 Xba I。將定序完成之
序列與NCBI 所發表之 DV-2 PL046 strain(AJ968413)與 DV-3 H87 strain
(M93130)序列互相比對,在 PL046 strain 的比對中,除了 NS2B 基因序
列與DV-2 PL046 strain(AJ968413)上所公佈的 NS2B 基因序列完全相同之
外,NS2A 則有 4 個鹼基不同、NS4A 有 2 個鹼基不同、NS4B 有 3 個鹼基
不同、NS1 與 E gene 各只有 1 個鹼基不同;而 H87 strain 與 DV-3 H87 strain
(M93130)比對結果中,發現 NS2A 有 2 個鹼基不同,NS2B 有 4 個鹼基 不同、NS4A 有 3 個鹼基不同、NS4B 有 3 個鹼基不同、E gene 有 8 個鹼基
不同。其中在NS2B 突變鹼基於 4173- 4174 位置發現有兩個鹼基發生 deletion
(dTA),NS4A 突變鹼基也在 6563 位置發現 deletion(dA),由於 DV-3 H87
Site-directed Mutagenesis 的方法將 deletion 的部分修補。
由定序結果發現,大部分突變之鹼基突變為silent mutation,少部分則
突變為missense mutation,關於非結構蛋白以及外膜蛋白基因之改變鹼基與
胺基酸將列於【表1~2】。
3.6 登革熱病毒非結構蛋白以及外膜蛋白(E protein)在 E.coli C41(DE3)
和C43(DE3)中的表現
將已建構好的質體轉形於 E. coli C41( DE3 )和 C43 ( DE3 )作表現,所 得之轉形菌株(transformants) 在 LB broth 中培養,並加入 0.5 mM IPTG 誘 導(induction) 四小時後,把所收取的細胞予以打破,分為上清液及 pellet,
利用 SDS-PAGE 分析(所分析的蛋白質含量中,上清液蛋白質約 10 μg、
pellet 約 100 μg)並以 Coomassie blue staining 或 Western blot 偵測蛋白質之
表現,E. coli C41( DE3 )和 C43 ( DE3 )菌株之蛋白質偵測結果將列於【表 3】。
欲表現DV-2 PL046 strain 與 DV-3 H87 strain 兩種 strain 所得到轉譯完
成之蛋白質分別為 D2NS2A-HAHis、D2NS2B-HAHis、D2NS4A-HAHis、
D2NS4B- HAHis、D2E-HAHis、D2NS1-HAHis 與 D2NS1(d)-HAHis,分子
量大小分別預測為28.9、19.4、21.7、32.1、59、44.7 與 32.1 kDa。
DV-3 H87 strain 由 E. coli C41( DE3 )和 C43 ( DE3 )兩種菌株所得到轉
譯完成之蛋白質分別為D3NS2A-HAHi、D3NS2B-HAHis、D3NS4A-HAHis、
D3NS4B-HAHis、D3E-HAHis,分子量大小分別預測為 28.6、18.8、21、31.2、 58.3 kDa。
3.6.1 登革熱病毒非結構蛋白 NS2 與 NS4 的表現
3.6.1.1 pET 5T△ -D2NS2A-HAHis, pET 5T△ -D3NS2A-HAHis 蛋白質表現結
果
欲表現DV-2 PL046 strain 與 DV-3 H87 strain 兩種 strain 之 NS2A,所
PL046 與 H87 strains,無論是上清液與 pellet 皆無法清楚看到蛋白質大量表 現(over-expression)的現象。
以Western blot 偵測,在 DV-2 PL046 strain 以 anti-HA 抗體做偵測,可
在 C41(DE3)與 C43(DE3)菌株於 pellet 中偵測到一條符合預期的蛋白
質片段(DV2- NS2A-HAHis,約 29 kDa),並於 60 kDa 與 17 kDa 大小附近
也可以被偵測到蛋白質【圖3.9】。
在DV-3 H87 strain 中,以 anti-HA 抗體做偵測,除了 C41(DE3)偵測
不到符合預期大小的片段之外(DV3-NS2A-HAHis,約 29 kDa),其餘結果皆
與DV-2 PL046 strain 部分相似,於 60 kDa 與 17 kDa 大小附近也可以被偵
測到蛋白質【圖3.10】。 Anti-HA Anti-His C41 C43 C41 C43 Supernatant DV2-NS2A (PL046) Pellet ○ ○ Supernatant DV3-NS2A (H87) Pellet ○ (”○”代表能利用抗體找到符合預期大小的片段)
3.6.1.2 pET 5T△ -D2NS2B-HAHis, pET 5T△ -D3NS2B-HAHis 蛋白質表現
結果
欲表現DV-2 PL046 strain 與 DV-3 H87 strain 兩種 strain 之 NS2B,所得
到轉譯完成之蛋白質分別為D2NS2B-HAHis 與 D3NS2B-HAHis,分子量大
小分別為預測為19.4 kDa 與 18.8 kDa。由 Coomassie blue staining 分析 PL046
與 H87 strains,無論是上清液與 pellet 皆無法清楚看到蛋白質大量表現
(over-expression)的現象。
的上清液之外,皆可以 anti-HA 抗體偵測到一條約符合預期大小的片段 (DV2-NS2B-HAHis,約 19 kDa),但在 19 kDa 大小附近也偵測到另外兩條
分子量大小相似蛋白質【圖3.11】。
不同於PL046 strain,H87 strain 在兩種菌株 pellet 的表現下,可在 43、
19 與 17 kDa 大小附近以 anti-HA 與 anti-His 抗體偵測到蛋白質,其中 19 kDa 符合預期的大小(DV3-NS2B-HAHis,約 19 kDa)【圖 3.12】。 Anti-HA Anti-His C41 C43 C41 C43 Supernatant DV2-NS2B (PL046) Pellet ○ ○ Supernatant DV3-NS2B (H87) Pellet ○ ○ ○ ○ (”○”代表能利用抗體找到符合預期大小的片段)
3.6.1.3 pET 5T△ -D2NS4A-HAHis, pET 5T△ -D3NS4A-HAHis 蛋白質表現
結果
DV-2 PL046 strain 與 DV-3 H87 strain 兩種 strain 之 NS4A,所得到轉譯
完成之蛋白質分別為D2NSBA-HAHis 與 D3NS4A-HAHis,分子量大小分別
為預測為21.7 kDa 與 21 kDa。由 Coomassie blue staining 分析 PL046 與 H87
strains,無論是上清液與 pellet 皆無法清楚看到蛋白質大量表現(over- expression)的現象。
以Western blot 偵測,DV-2 PL046 strain 中 C41(DE3)與 C43(DE3)
菌株可在上清液與pellet 中偵測到符合預期大小的片段(DV2-NS4A-HAHis,
約22 kDa),不過在 pellet 中,C41(DE3)與 C43(DE3)菌株亦有 17 kDa
的片段與inclusion body 的現象發生,將 pellet 的蛋白質含量降低分析(約
H87 strain 可於兩菌株之 pellet 以 anti-HA 抗體測到兩條分子量約 40 kDa 與符合預期大小的片段(DV3-NS4A-HAHis,約 21 kDa),以 anti-His 抗體偵
測,僅能從pellet 偵測到分子量約 40 kDa 的片段(約預期片段兩倍大小) 【圖3.14】。 Anti-HA Anti-His C41 C43 C41 C43 Supernatant ○ ○ DV2-NS4A (PL046) Pellet ○ ○ Supernatant DV3-NS4A (H87) Pellet ○ ○ (”○”代表能利用抗體找到符合預期大小的片段)
3.6.1.4 pET 5T△ -D2NS4B-HAHis, pET 5T△ -D3NS4B-HAHis 蛋白質表現
結果
欲表現DV-2 PL046 strain 與 DV-3 H87 strain 兩種 strain 之 NS4B,所得
到轉譯完成之蛋白質分別為D2NS4B-HAHis 與 D3NS4B-HAHis,分子量大
小分別為預測為32.1 kDa 與 31.2 kDa。由 Coomassie blue staining 分析 PL046
與H87 strains,無論是上清液與 pellet 皆無法清楚看到蛋白質大量表現(over-
expression)的現象。
以Western blot 偵測,在 PL046 strain 中,可在 C41(DE3)與 C43(DE3)
菌株之上清液與 pellet 以 anti-HA 與 anti-His 抗體皆可以偵測到符合預期大
小的片段(DV2-NS4B-HAHis,約 32 kDa)。不過在pellet 的部分,以 anti-HA
在兩種菌株的表現下,另有兩條20 kDa 與 17 kDa 大小的蛋白質可以被偵測
【圖3.15】。
H87 strain 在 DV3-NS4B-HAHis 的表現結果與 PL046 strain 結果相似,
pellet 以偵測到符合預期大小的片段(DV3-NS4B-HAHis,約 32 kDa),在 17 kDa 大小附近也被偵測到分子量較小的蛋白質【圖 3.16】。 Anti-HA Anti-His C41 C43 C41 C43 Supernatant ○ ○ ○ ○ DV2-NS4B (PL046) Pellet ○ ○ ○ ○ Supernatant ○ ○ ○ ○ DV3-NS4B (H87) Pellet ○ ○ ○ ○ (”○”代表能利用抗體找到符合預期大小的片段) 3.6.2 登革熱病毒外膜蛋白的表現
3.6.2.1 pET 5T△ -D2E-HAHis, pET 5T△ -D3E-HAHis 蛋白質表現結果
DV-2 PL046 strain 與 DV-3 H87 strain 兩種 strain 之外膜蛋白,所得到
轉譯完成之蛋白質分別為D2E-HAHis 與 D3E-HAHis,分子量大小分別為預
測為 59 kDa 與 58.3 kDa。由 Coomassie blue staining 分析 PL046 與 H87
strains,無論是上清液與 pellet 皆無法清楚看到蛋白質大量表現(over- expression)的現象。
以Western blot 偵測,在 DV-2 PL046 strain 中以 anti-HA 抗體於 C41(DE3)
與C43 (DE3)菌株之 pellet 偵測到 70 kDa 大小的蛋白質,並於 C41(DE3)
菌株中另可可測得表現符合 DV2-E 大小的蛋白質(DV2-E-HAHis,約 59
kDa)【圖 3.17】。
H87 strain 在 C41(DE3)與 C43(DE3)菌株的表現方面一致,在上
清液與pellet 中以 anti-HA 抗體可以偵測到符合預期的片段(DV3-E-HAHis,
約58 kDa),pellet 的部分亦有 70 kDa 與 50 kDa 大小蛋白質被偵測,利用
Anti-HA Anti-His C41 C43 C41 C43 Supernatant DV2-E (PL046) Pellet ○ Supernatant ○ ○ DV3-E (H87) Pellet ○ ○ ○ ○ (”○”代表能利用抗體找到符合預期大小的片段) 3.6.3 登革熱病毒非結構蛋白 NS1 的表現 3.6.3.1 pET 5T△ -D2NS1-HAHis 蛋白質表現結果
由於非結構蛋白與外膜蛋白在 E.coli C41(DE3)以及 C43(DE3)表
現系統表現量不佳,因此想藉由相同的蛋白質表現系統,用來表現 DV-2
PL046 strain 之非結構蛋白 NS1,觀察蛋白質在 E.coli C41(DE3)以及 C43 (DE3)系統表現狀況。
轉譯完成之蛋白質D2NS1-HAHis 的分子量大小約為 44.7 kDa。 結果
由Coomassie blue staining 分析,無論是上清液與 pellet 皆無法清楚看到蛋
白質大量表現(over-expression)的現象。
利用anti-HA 抗體偵測時,僅 C41(DE3)菌株可於上清液偵測 50 kDa、
45 kDa、40 kDa 到蛋白質。在 pellet 的部分,在 C41(DE3)與 C43(DE3)
菌株皆可在50 kDa、45kDa、40kDa 的大小偵測到蛋白質,45 kDa 大小的
片段符合預期結果(DV2-NS1-HAHis,約 45 kDa),利用anti-His 抗體的偵測
結果與anti-HA 的結果相似,但並無法偵測到符合預期大小的片段。根據結
果觀察,45kDa 大小的 band 相較於另外兩條 50 kDa 與 40 kDa 的 band 訊號
較弱【圖3.19】。
為了探討此三條蛋白質的表現結果是否為C41(DE3)與 C43(DE3)
菌株所造成,因此將pET 5T△ -D2NS1-HAHis 質體轉形於 E.coli BL21(DE3)
清楚看到蛋白質大量表現(over-expression)的現象,但在 pellt 中卻可以觀 察到蛋白質大量表現產生。
進一步利用Western blot 進行確認,利用 anti-HA 抗體偵測時於上清液
與pellet 同樣可以在 50 kDa、45 kDa、40 kDa 的位置偵測到蛋白質,45 kDa
大小的片段符合預期結果(DV2-NS1-HAHis,約 45 kDa),利用anti-His 抗體
的偵測結果與anti-HA 的結果相似【圖 3.20】。
3.6.3.2 pET 5T△ -D2NS1(d)-HAHis 蛋白質表現結果
為 了 確 認 此 三 條 蛋 白 質 , 因 此 表 現 另 外 建 構 的 質 體 ,pET 5T△ -
D2NS1(d)-HAHis,此質體與 pET 5T△ -D2NS1-HAHis 不同點在於其 insert
之NS1 基因大小不同,將 NS1 基因(全長 1059 bp)的末端截短,得到 NS1(d)
基因(全長723 bp),藉此觀察蛋白質表現狀況有何差異。
D2NS1(d)-HAHis 的分子量大小約為 32.1 kDa,藉由 Coomassie blue staining,在上清液無法清楚看到蛋白質大量表現(over-expression)的現象,
但在pellet 的部分,C41(DE3)與 C43(DE3)菌株可在 40 kDa、26 kDa
的大小以Coomassie blue staining 偵測到,卻無法於 32 kDa 大小附近觀察到
符合預期大小之NS1(d)-HAHis 的表現。
利用Western blot 偵測,利用 anti-HA,C41(DE3)與 C43(DE3)菌
株可於上清液與pellet 偵測到大小約 40 kDa、32 kDa、26 kDa 的蛋白質,
32 kDa 符合預期大小。(DV2- NS1(d)-HAHis,約 32 kDa);利用 anti-His 抗
體偵測結果,除了上清液無法偵測到符合預期大小的片段,與anti-HA 結果
相仿【圖3.21】。根據結果觀察,33 kDa 大小的 band 相較於另外兩條 40 kDa
與26 kDa 的 band 訊號較弱,結果呈現與 D2NS1-HAHis 相似。
3.6.3.3 pET30a-D2NS1-HAHis 蛋白質表現結果
將 NS1-HAHis 基因建構於 pET-30a(+)載體上,形成 pET30a-D2NS1
子量大小約為49.9 kDa。結果由 Coomassie blue staining 分析,無論是上清
液與pellet 皆無法清楚看到蛋白質大量表現(over-expression)的現象。
利用anti-HA 抗體偵測時,不論是上清液及 pellet,C41(DE3)與 C43
(DE3)菌株皆可在 55 kDa、50 kDa、45 kDa 的大小偵測到蛋白質,50 kDa
大小的片段符合預期結果,利用anti-His 抗體的偵測結果與 anti-HA 的結果
相似。根據結果觀察,更換載體(由 pET 5T△ -HAHis 換到 pET30a(+))並
不能有效改善雜片段的形成【圖3.22】。 Anti-HA Anti-His C41 C43 BL21 C41 C43 BL21 Supernatant ○ ○ ○ DV2-NS1 (PL046) Pellet ○ ○ ○ ○ ○ ○ Supernatant ○ ○ DV2-NS1(d) (PL046) Pellet ○ ○ ○ ○ Supernatant ○ ○ ○ DV2-NS1 (pET30a(+)) Pellet ○ ○ ○ ○ (”○”代表能利用抗體找到符合預期大小的片段)
肆、討論
4.1 質體建構與序列分析
將本實驗所使用的Dengue virus type 2,Taiwan local strain PL046 之基
因NS2A、NS2B、NS4A、NS4B、E、NS1 與 NCBI 網站基因資料庫所公佈 之DV-2 PL046 strain(AJ968413)作基因序列比對,於核苷酸的部分其相 似度介於99.39 ~ 100%,而胺基酸的相似度則介於 99.08 % ~ 100%,幾乎 沒有序列比對上的差異;而將H87 strain 與 NCBI 網站基因資料庫所公佈之 DV-3 H87 strain(M93130)比對,核苷酸相似度界於 99.46 % ~ 99.69 %,其 胺基酸相似度介於98.46% ~ 99.54%,序列的比對結果差異亦不大。造成鹼 基不同與胺基酸序列的些微差異,可能是RNA 病毒複製所造成,或是利用 PCR 建構質體的過程中所導致的突變【表 1~2】。 4.2 表現登革熱病毒非結構蛋白 NS2 與 NS4 與外膜蛋白在 Ecoli C41(DE3) 和C43(DE3)表現系統 首先將實驗室已建構好DV-2 PL046 strain 與 DV-3 H87 strain 基因之
pET 5T△ -HAHis 質體【圖 3.1】轉形於 E. coli C41 (DE3)與 E. coli C43 (DE3)
作表現,再將轉形質體後的大腸桿菌C41(DE3)與 C43(DE3)菌株經 0.5
mM IPTG 誘導表現 4 小時之後,萃取上清液以及 pellet 中的蛋白質,經由 SDS-PAGE 蛋白質電泳、以及西方點墨法分析。由於 C 端同樣含有 HA-His-tag,因此可以利用 anti-HA-HRP 或 anti-His-HRP 抗體來做蛋白質
偵測與表現分析。由於蛋白質的表現普遍不佳,無法藉由 Coomassie blue staining 來觀察蛋白質表現狀況,因此本實驗主要利用西方點墨法的方式來 觀察蛋白質表現狀況。 NS2A-HAHis 可以經由西方點墨法的方式在預期的位置(29 kDa)所偵 測到,並且在 PL046 strain 與 H87 strain 中所表現的結果彼此相似。除了 NS2A-HAHis 之外,在 17 kDa 大小附近也可以被偵測到分子量較小的蛋白