以反溶劑再結晶法純化亞硫酸鹽
呂權訓、陳竑妙、吳瑞泰、蔡政賢、蔡平賜 國立高雄應用科技大學 化學工程與材料工程學系 E-mail : charles1@cc.kuas.edu.tw摘 要
焙燒爐燃燒廢觸媒原料會產生大量的含硫廢氣,這些含硫廢氣雖可利用氫氧化鈉水溶液,水洗飛灰固 體廢棄物,但仍必需負擔高額的飛灰固體廢棄物的掩埋處理費用。飛灰固體廢棄物經初步的成分分析,除 了少量未回收的金屬外,含相當高比例的亞硫酸鈉及亞硫酸氫鈉。此兩種物質目前在工業上有相當多的用 途,需求量也很多。因此,本文將探討以“反溶劑再結晶法” 應用於飛灰固體廢棄物中,分離純化出亞硫酸 鈉之可行性。文章中將分別說明“反溶劑再結晶法” 純化技術的幾項重要製程條件,如添加於飛灰固體廢棄 物中粉末與水量的比例、添加氫氧化鈉溶液的效應以及以 SEM、EDS、XRF 等儀器探討添加反溶劑(乙醇) 濃度對再結晶產物之品質的影響。 關鍵詞:再結晶、反溶劑、水洗飛灰、固體廢棄物。1. 前 言
許多工廠常常會排放出許多廢氣,這些廢氣含有許多對環境有害物質,因此「空氣污染防治法施行細 則」,特將空氣污染物分八種分別加以監控管制,其中第一種氣狀污染物包含硫氧化物(SOx)、一氧化碳(CO)、 氮氧化物(NOx)、碳氫化合物(CxHy)、氯氣(Cl2)、氯化氫(HCl)、氰化物(HCN)、二硫化物(CS2)、氟化物氣體 (HF 及 SiF4)、鹵化烴類(CmHnXx)及全鹵化烷類(CFCs)等。其中燃煤所產生之大量硫氧化物(SOx)造成環境問 題當嚴重,也是管制的重點。 國內一些環保廠商以從事廢觸媒回收,使廢料能有效循環再利用,達成資源化廢棄物經濟效益。其中 焙燒爐燃燒廢觸媒原料可回收一些鉬、釩等有價值金屬,但也會產生許多含硫飛灰固體廢棄物,初估每天 會產生出公噸級以上的固體廢棄物,這不但是對環境造成負擔,公司也必需負擔這些固體廢棄物的掩埋處 理費用。 以氫氧化鈉鹼液水洗硫氧化物(SOx)廢氣,所產生的飛灰固體廢棄物中化學反應如下[1]:(1)
SO
H
O
H
SO
2+
2→
2 3)
2
(
2
2
2 3 2 3 2SO
NaOH
Na
SO
H
O
H
+
→
+
)
3
(
2
3 3 2 3 2SO
Na
SO
NaHSO
H
+
→
由反應式(2)及(3)可推知飛灰固體廢棄物中應含有大量的亞硫酸鈉及亞硫酸氫鈉,其中亞硫酸鈉(Na2SO3) 的分子量 126.04,在各種工業上有很重要的應用[2],如印染工業作為脫氧劑和漂白劑,用于各種棉織物 的煮煉,可防止棉布纖維局部氧化而影響纖維強度,並能提高煮煉物的白度;在感光工業用作顯影劑;在 有機工業用作間苯二胺、氮基水楊酸鈉等生產的還原劑,以防止反應過程中半成品的氧化;在食品工業用 作脫水蔬菜的還原劑,以防止蔬菜中的綠色素變質發黃;在無機工業用作生產氰化亞銅等的還原劑;水處 理中用于處理鍋爐用水。而亞硫酸氫鈉(NaHSO3)分子量 104.06,密度 1.48。為白色顆粒或結晶性粉末,有 二氧化硫的微臭。在水中易溶,在乙醇或乙醚中幾乎不溶。有強還原性,應用在染料、藥物、紙漿(蒸煮),羊絨漂白的清洗及染色時硫酸代用品,為強力固體酸,消毒劑,礦物分解助熔劑,並用於食物防腐、麥稈 漂白、電鍍銅和黃銅等[3]。 若能將將亞硫酸鈉或亞硫酸氫鈉從固體廢棄物中分別純化分離,不僅可以達到減少廢氣物對環境的負 擔,純化所得之產品也可做為民生工業所用。以再結晶技術回收飛灰固體廢氣物須實驗設定出許多製程條 件,如溶劑種類、單一溶劑或混合溶劑搭配、溶劑濃度、溫度、靜置條件、是否添加晶種、是否添加其他 雜質凝聚劑等操作變因等。本文之主要目的是探討以“反溶劑再結晶法”於固體廢棄物中純化出亞硫酸鈉之 可行性。文章中將分別說明“反溶劑再結晶法”純化技術的幾項重要製程條件,如:添加於飛灰固體廢棄物 中粉末與水量的比例、添加氫氧化鈉溶液的效應以及以 SEM、EDS、XRF 等儀器,探討添加反溶劑(乙醇) 濃度對再結晶產物之品質的影響。
2. 實驗方法
本實驗所使用之藥品有氫氧化鈉(Sodium hydroxide NaOH, 96 %, SHOWA)、乙醇(Ethanol C2H5OH, 98%,
友和),實驗所處理之飛灰固體廢棄物來自國內環保廠商。本研究先製備飽合亞硫酸鈉水溶液,再配合添加 反溶劑(乙醇)的方式,低溫靜置獲得再結晶亞硫酸鈉產物。詳細的實驗步驟如圖一所示,分述如下:
1. 先利用篩網將相當少量之的大粒徑固體廢棄物分離收集。
2. 室溫(25℃)下,將 25ml 之 RO 水加入過篩後之固體粉末以形成飽和溶液,攪拌均勻後再進行抽氣過濾 分離溶液中之不溶解固體粉末(a),獲得澄清飽和溶液。
3. 澄清飽和溶液再加入約 5ml 之 NaOH(aq)(10N)溶液,提高飽合溶液中的[OH-]濃度,以磁子攪拌器攪
拌均勻後,溶液中會產生微量固體懸浮粉末,以濾紙/瓷漏斗抽氣過濾可濾出這些懸浮粉末(b),而過濾 後之高pH 值澄清飽和溶液則進行下一步驟之再結晶程序。
4. 再結晶的程序是以添加不同毫升的乙醇作為反溶劑,置入冰箱並降溫至 1℃,如此可降低飽和溶液之 溶解度,而獲得水合結晶物。將結晶物烘乾後,進行SEM、EDS、XRD 分析。
掃描式電子顯微鏡 (Scanning Electron Microscope, SEM/EDS)是用來觀察亞硫酸氫鈉表面形狀、顆粒大 小以及表面元素分析,本研究是採用Hitachi S3000N,其成像原理是利用一束電子束掃描試片的表面,並將 表面產生之訊號 (包括二次電子、背向反射電子、吸收電子、X 射線等) 加以收集經放大處理後,輸入到 同步掃描之陰極射線管(CRT),以顯現試片圖形之影像。為了增加樣品之導電性,通常進行拍攝前會先在樣 品表面鍍金。X-光繞射分析儀 (X-ray Diffract meter, XRD)是採用日本 RIGAKU D/max IIB,Tint-2000- X-ray Diffract meter,在電壓 40KV 及電流 30mA 下,分析亞硫酸酸鈉粉末晶體結構。使用 CuKα 輻射光之單色
器,以掃描速度4。
/min,掃描角度(2θ)20-80。
,進行X-ray 繞射分析測得結晶結構,並由繞射圖之波峰與標 準圖譜比對判斷結晶純度。
抽
氣過濾
圖1 實驗流程圖3. 結果與討論
3.1 水的添加量 由於很難固定應該添加多少固體粉末與水的比例,才能使溶液達到飽和狀態,所以實驗時以室溫下 (25℃),添加過量的粉末使溶液達過飽合狀態。根據 8 次實驗的結果,約 22.57±0.69 克的固體粉末添加 50ml 的水,即可使溶液達成過飽和狀態,此時溶液可以觀察出有懸浮的未溶解固體粉末,過濾此過飽合溶液即 可獲得室溫下(25℃)澄清的飽和溶液。 3.2 添加氫氧化鈉的效應 添加氫氧化鈉的目的是為了提高飽合溶液中的[OH-]濃度,使溶液中的亞硫酸氫根離子(HSO3-)與氫氧化 鈉(OH-)反應成亞硫酸氫根離子(SO 32-),其反應式如下所示: NaHSO3 + H2O → Na+ + HSO3- (4) HSO3- + OH- → H2O + SO32- (5) 當添加氫氧化鈉與水的體積比為1:10 時,澄清溶液中開始產生固體懸浮物,依方程式(5)推估,這些固 體懸浮物應為過量的亞硫酸氫根離子(SO32-)與鈉離子(Na+)形成亞硫酸鈉固體,而於溶液中過飽析出,但此 舉是否會有其他雜質一併析出需要再進一步分析這些固體懸浮物。 3.3 反溶劑(乙醇)的添加量對再結晶產物影響 再結晶是比較能獲得純亞硫酸鈉的方法之ㄧ,亞硫酸鈉對水的溶解度在室溫下約為63g/100ml,然而亞 硫酸鈉對乙醇的溶解度則較差,因此乙醇可當作亞硫酸鈉飽和溶液的反溶劑。於澄清飽和溶液中加入反溶 劑(乙醇),可因乙醇會與水互溶,造成原澄清飽和溶液達到過飽和狀態,誘發亞硫酸鈉晶體的沉澱析出;其 中前所添加之氫氧化鈉則因與乙醇的互溶性良好,可繼續溶解於溶液中,達成選擇性再結晶之目的。圖2(a)、圖 3(a)分別為飛灰固體原始粉末及添加 20ml 乙醇之再結晶產物之 SEM 圖形。由圖 2(a)可觀察 到粉末呈現不規則情形,相較於圖3(a)其 SEM 圖呈現較為規則的結晶產物。圖 2(b)及圖 3(b)分別為飛灰固 體原始粉末,及添加 20ml 乙醇之再結晶產物之元素分析圖譜,兩圖都可觀察出碳(C)、氧(O)、鈉(Na)、硫 (S)等為主要元素峰,其中碳(C)可能是製作試片時,使用的碳膠帶所造成的。其餘的氧(O)、鈉(Na)、硫(S) 等元素,與本研究再結晶預計產物亞硫酸鈉(Na2SO4)所含的元素相吻合。
固體廢棄物
篩離大粒徑固體
澄清飽和水溶液
過飽合溶液,固體析出
澄清飽和水溶液
再結晶
過飽和溶液
10N 氫氧化鈉
加入
RO 水
抽氣過濾
添加反溶劑
1. XRF
2. EDS
3. SEM
結晶物
粉末
粉末(a)
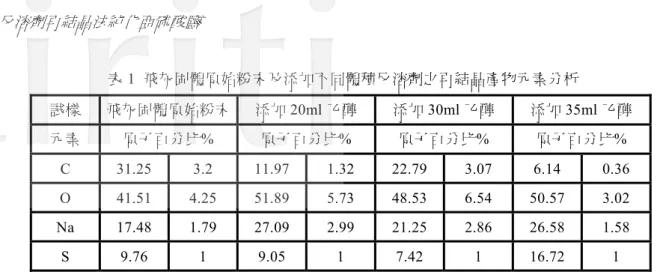
表1 為整理後之飛灰固體原始粉末,及添加不同體積反溶劑之再結晶產物 EDS 元素分析,為使數據更 易觀察比較,將硫(S)原子比例設為 1,以估算其他原子相對於硫(S)原子的比例,用來判定是否獲得純亞硫 酸鈉。理論上若為純亞硫酸鈉(Na2SO4)的元素分析,其硫(S)原子與鈉(Na)原子相對比例應為 1 比 2。表 1 飛 灰固體原始粉末之硫(S)原子與鈉(Na)原子相對比例為 1 比 1.79,顯示結晶產物之鈉(Na)原子不足,若將前 方程式(1)~(3)比較,可推估為飛灰固體原始粉末中含有亞硫酸氫鈉(NaHSO4)導致。 添加20ml 乙醇之產物其硫(S)原子與鈉(Na)原子相對比例為 1 比 2.99,表示有多餘的鈉(Na)原子,這與 本研究中為促使亞硫酸氫鈉反應成亞硫酸鈉,所添加之氫氧化鈉(NaOH)有關。當添加之氫氧化鈉與再結晶 產物一併析出,元素分析中就可能觀察到較多的鈉(Na)原子相對比例。添加 30ml 乙醇之產物其硫(S)原子與 鈉(Na)原子相對比例為 1 比 2.86,表示有多餘的鈉(Na)原子,與上述添加 20ml 乙醇原因一致;然而當數據 由1 比 2.99 變為 1 比 2.86,表示多餘的鈉(Na)原子比例變少了,這表示添加較多量的反溶劑(乙醇)可造成鈉 (Na)原子比例變少。 添加35ml 乙醇之產物,其硫(S)原子與鈉(Na)原子相對比例為 1 比 1.58 低於 1 比 2,顯示結晶產物可能 又有亞硫酸氫鈉產生。推論添加乙醇來誘發再結晶的過程,似乎也造成溶液中亞硫酸根離子(SO32-)因缺少 氫氧化鈉的氫氧根離子(OH-),方程式(5)依勒沙特列原理,又逆向反應變回亞硫酸氫根離子(HSO 3-),因此造 成亞硫酸氫鈉的產生。 (a) (b) 圖2 飛灰固體原始粉末(a)SEM 圖形及(b)EDS 元素分析圖譜
(a) (b) 圖3 添加 20ml 乙醇之再結晶產物(a)SEM 圖形及(b)EDS 元素分析圖譜
表1 飛灰固體原始粉末及添加不同體積反溶劑之再結晶產物元素分析 試樣 飛灰固體原始粉末 添加20ml 乙醇 添加30ml 乙醇 添加35ml 乙醇 元素 原子百分比% 原子百分比% 原子百分比% 原子百分比% C 31.25 3.2 11.97 1.32 22.79 3.07 6.14 0.36 O 41.51 4.25 51.89 5.73 48.53 6.54 50.57 3.02 Na 17.48 1.79 27.09 2.99 21.25 2.86 26.58 1.58 S 9.76 1 9.05 1 7.42 1 16.72 1 圖4 為加入 30 毫升及 35 毫升之乙醇再結晶粉末 SEM 圖,加入 20 毫升之乙醇再結晶粉末之結晶性較 為完整如圖 3(a)所示,而加入 30 毫升及 35 毫升之之乙醇再結晶粉末,雖也可看到結晶區塊,但同時也看 到許多不規則粉末,這些不規則的粉末配合前所描述之EDS 元素分析,可歸為氫氧化鈉(NaOH)或亞硫酸氫 鈉(NaHSO4)。 圖5(a)為加入 20 毫升之乙醇再結晶粉末 XRD 圖,若與圖 5(d)亞硫酸鈉之 XRD 標準圖譜比對下,可發 現加入20 毫升之乙醇再結晶粉末的 XRD 圖與標準圖譜相當吻合,與前 SEM 所觀察到加入 20 毫升之乙醇 再結晶粉末的結晶性最好一致。 圖5(b)及圖 5(c)圖譜與亞硫酸鈉之 XRD 標準圖譜比對,亦可觀察出主要仍為亞硫酸納,含有些許雜質 譜線。 (a) (b) 圖4 加入(a)30 毫升(b)35 毫升乙醇再結晶粉末放大倍率 2000 倍之 SEM 圖
SHS-8 20 30 40 50 60 70 80 (a) SHS-10 20 30 40 50 60 70 80 (b) 20 30 40 50 60 70 80 (c) (d) 圖5 加入(a)20 毫升(b)30 毫升(c)35 毫升之乙醇再結晶粉末 XRD 圖(d)亞硫酸鈉之 XRD 標準圖譜
4. 結 論
本文中探討以“反溶劑再結晶法”於飛灰固體廢棄物中幾項重要製程條件,其中粉末與水量的比例於約 22.57±0.69 克粉末添加 50ml 的水,即可使溶液達成過飽和狀態。添加氫氧化鈉與水的體積比為 1 比 10 時, 可使溶液中的亞硫酸氫根離子(HSO3-)與氫氧化鈉(OH-)反應成亞硫酸氫根離子(SO32-)。以 SEM、EDS 以及
XRD 的分析可知,添加過量的乙醇(35ml)反而導致產生較為不好的亞硫酸鈉結晶,而添加 20ml 乙醇之再結 晶產物,每次可獲得最佳之亞硫酸鈉結晶,產率約為 30%,因此以“反溶劑再結晶法”分離純化純的亞硫酸 鈉是相當可行的策略。
參考文獻
[1] Joslyn M.A.and Braverman J.B., “The chemistry and technology of the pretreatment and preservation of fruit and vegetable products with sulfur dioxide and sulfites,” Adv Food Res., Vol. 5, pp. 97-160, 1954.
[2] 呂民基,紡織品染色法,台北:華聯出版社,1971。
[3] http://www.chemicalbook.com/ChemicalProductProperty_CN_CB4111698.htm
[4] Raymond E. V. and Thompson A. R., “Crystallization of Anhydrous Sodium Sulfate,” Ind. Eng. Chem., Vol.42, No.3, pp. 464–467, 1950.