1
光觸媒進行人工光合作用
Artificial Photosynthesis by Photocatalysts計畫編號:NSC-91-2214-E-002-021
執行期限:91年8月1日至92年7月31日
主持人:吳紀聖 台灣大學化學工程研究所
計畫參與人員:曾怡享 陳志賢 羅健峰 台灣大學化學工程研究所
一、中文捎耍 人工光合作用是降低大氣層中CO2溫室氣 體濃度並發展再生能源的最佳程序之一。以 改良式溶凝膠法製備一系列Cu/TiO2觸媒, 進行CO2光催化還原生成甲醇。在CO2還原 反應,UVC(254 nm)光源催化下,CuCl2-1h 與CuCl2-3h的2wt% Cu/TiO2觸媒,在28小時 後可達甲醇產量為1000 µmol/g-catal。分析 結果Cu/TiO2觸媒表面的Cu並非單一價數, 但主要價態為Cu+。 關鍵詞:光催化,二氧化碳,Cu/TiO2, AbstractThe artificial photosynthesis is one of the
best processes to reduce CO2 in the atmosphere
as well as to develop renewable energy. A
series of Cu/TiO2 were prepared by a modified
so-gel methods. Methanol was generated by the
photocatalytic reduction of CO2. The maximum
methanol yield reached 1000 µmole/g-catal
under 28 hours UVC (254 nm) irradiation using
2wt% Cu/TiO2 by CuCl2-1h and CuCl2-3h
methods. The Cu+ was the major species on the
Cu/TiO2 though multiple chemical status of Cu existed.
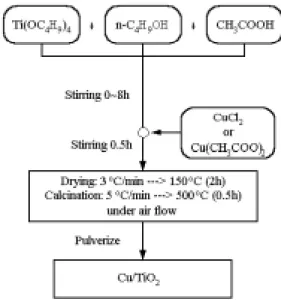
Keywords: photocatalysis, carbon dioxide, Cu/TiO2. 二、緣由與目的 近 年 來 二 氧 化 碳 之 排 放 帶 來 的 溫 室 效 應,造成全球氣候變遷。藉由光觸媒,將太 陽能轉成化學能儲存之技術,備受重視,但 目前國內外之的研究成果顯示,仍因受限於 光轉化效率之低落,而無法普及應用。因 此,若可改善光觸媒之光效率,使之具備實 際應用之價值,利用光觸媒可將二氧化碳還 原,轉變成可作為替代能源之甲醇等化學 品,則可同時解決環境與能源之議題。以光 觸媒進行光催化還原CO2生產碳氫化合物, 是模擬植物光合作用,具有再生能源和降低 CO2的優點,是根本解決CO2和能源的最佳 選擇。 三、實驗 使用光觸媒二氧化鈦以光誘導的方式還 原二氧化碳。Fig. 1 簡示觸媒製備,觸媒製 備 過 程 為 加 入 Ti(OC4H9)4、 n-C4H9OH 、
CH3COOH,以CuCl2或Cu(CH3COO)2為前驅
物 , 採 改 良 式 溶 凝 膠 法 並 經 150o C 乾 燥 、 500oC煆燒,製備出一系列不同Cu loadings 之Cu/TiO2。再利用UV光源(波長= 254 nm或 365 nm)進行二氧化碳飽和水溶液之光催化 還原反應,產物分析得甲醇及微量之溶氧 [1]。 進 行 光 催 化 實 驗 時 , 先 以 超 高 純 度 99.9999v% 的二氧化碳通入含氫氧化鈉之光 觸媒懸浮水溶液中,待二氧化碳飽和後,再 以紫外光照射以進行二氧化碳之光還原反 應,最後以GC-FID分析液相產物為甲醇, 並且以溶氧偵測器測得少量氧氣。 以UV-Vis、SEM、XRD、XPS、XAS和 EXAFS進行觸媒物性分析。 四、結果與討論 為探討進行二氧化碳光還原反應之最佳 觸媒,首先根據之前之實驗結果[1]發現,銅 含量2%的Cu/TiO2觸媒有最佳之反應結果, 因 此 本 實 驗 之 觸 媒 皆 製 備 銅 含 量 為 2% 之
Cu/TiO2觸媒。Fig. 2 的TEM照片以銅前驅
物 在 Ti 溶 膠 水 解 8 小 時 後 加 入 製 得 的
2%Cu/TiO2觸媒,可發現製得的Cu/TiO2粒徑
小於20 nm。
2 CuCl2前驅物在不同時間添加入溶膠製得的 Cu/TiO2觸媒光催化活性比較,隨著光催化 時間的增加,甲醇產量提昇;比較照光時間 28小時的甲醇產量發現,在Ti溶膠水解8小 時後再加入CuCl2的CuCl2-8h觸媒產量約為 260 µmol/g;若是將CuCl2在溶凝膠水解之初 即加入一起水解,CuCl2-0h觸媒則會有兩倍 以上的活性,約為600 µmol/g得甲醇生成; 在Ti溶膠水解期間加入CuCl2的CuCl2-1h、 CuCl2-3h則展現更佳的活性,28小時後的甲 醇產量可達1000 µmol/g。若比較四種觸媒的 甲醇平均產率亦可發現,光催化速率依序為 CuCl2-3h > CuCl2-1h > CuCl2-0h > CuCl2 -8h。 為瞭解當光源波長增加對觸媒活性的影 響,選用活性較佳的觸媒進行波長365 nm光 源的活性測試。Fig. 4顯示以UVA為光源, 各 種 不 同 條 件 製 備 的 Cu/TiO2的 光 催 化 活 性,在之前的UVC光源光催化反應結果已知 CuCl2-3h觸媒有最佳的活性表現,24h產量 高達600 µmol/g,但是當UV光源改用較長波 長(365nm)的UVA時,CuCl2-3h的光催化活 性 並 非 最 佳 的 , 此 時 甲 醇 產 量 僅 有 4 µmol/g,若將觸媒以氫氣還原後,由圖可見 r-CuCl2-3h的最後甲醇產量或平均產率亦有 下降的趨勢;CuCl2-0h觸媒的活性也不是很 高,其甲醇產量上下跳動較不規則,並非隨 著光源曝照時間增加而產量隨之增加;r-CuAc2-8h觸媒則是在12h後才開始可以偵測 到甲醇的生成,24h後的產量與前述兩種觸 媒相當,亦為4 µmol/g。相較之下,CuCl2 -8h觸媒在此光源下的產量最高,24h光照約 有10 µmol/g的甲醇生成,但相較於UVC光 源,產量仍僅有其5%。 Cu/TiO2觸媒,利用TPR-TPD方式,由氫 氣的消耗量估算觸媒表面的Cu含量,除以所 添 加 的 理 論 Cu 含 量 , 得 銅 的 分 散 度 。 在 XRD的分析實驗,由於Cu含量太低,且推 測製得觸媒之Cu顆粒極小且分散,因此並未 能觀察到任何有關Cu的繞射峰,推測Cu以 微小粒子形式分散在TiO2架構中。由XPS檢 測觀察到Cu(2p)光電子束縛能的位置與形 狀,可藉此分析其所表示Cu價位。分析結果 推測製得一系列Cu/TiO2觸媒表面的Cu並非 單一價數,但主要價態為Cu+。為了更進一 步確定銅之價數與狀態,利用同步輻射光源 進行X光吸收光譜的分析。 Fig. 5為不同CuCl2與溶膠混合時間(0 ~ 8h) 製得之觸媒的Cu FT-EXAFS圖譜,圖中顯示 四種不同混合時間的觸媒,皆在1.5Å處有重 疊之主要特性峰,並在0.9Å處有一肩峰;四 者的差異主要出現於2.4 ~ 2.6Å的特性峰強 度,對CuCl2-3h觸媒而言,其在2.6 Å的特性 峰強度高於其他三者兩倍,CuCl2-8h與其波 峰形狀相似,2.6Å與3Å的特性峰部分重疊; CuCl2-0h與CuCl2-1h則分別在2.6、2.4Å有特 性峰。 由Fig. 5可發現屬於CuO的特性峰並不明 顯,所存在的1.5Å特性峰,屬於Cu2 O的Cu-O鍵結,位於2.5Å主要特性峰則表示更外層 的Cu(I)-O,由2.5Å這特性峰強度增強的結果 顯示,當添加Cu量越多或是CuCl2-3h 的製 程,將會有較大顆粒的Cu2O產生[2]。 可見光下具有光催化效果的二氧化鈦光 觸媒,是以摻合V的二氧化鈦,其UV-Vis吸 收位置均較純的二氧化鈦偏向較長波長區 域。結果在V/TiO2發現(Fig. 6),隨著V的 量越多,紅位移愈顯著。上述的結果代表當 V摻入二氧化鈦的結構中時,其可改變二氧 化鈦之整體能隙,進而達到吸收可見光波長 的目的,其原因可能是因為V的3d orbital 在 二氧化鈦的價帶與傳導帶中,形成其它的能 階。 在薄膜光觸媒製備技術方面,採用浸漬 覆 膜 法 (Dip-coating) 鍍 於 玻 片 和 光 纖 , 經 500oC鍛燒後膜厚在60~600 nm,以ASTM標
準的覆膜附著性測試,Fig. 7(a) SEM顯示其 成膜狀況良好且附著性佳。Fig. 7(b) SEM顯 示已鍍膜之光纖直徑約62 µm。 影響光催化之因素包括覆載金屬、表面 OH基與內部Cl-離子因為分別扮演抓取電子 或電洞的角色,金屬在TiO2粒子內部及表面 適當的分配比例、適當的OH比例將影響光 激發電子電洞之抓取與傳遞,進而影響電子 電洞的分離效果;較強的Cu與TiO2作用力與 粒子內部適量且均勻的Cu分布,將影響光電 子的傳遞至表面之效率;觸媒表面金屬及 OH基,呈現正電的表面將使得碳酸根易於 吸附,因而促進光催化活性。
3
五、參考文獻
1. I-H. Tseng, W.-C. Chang, J. C.-S. Wu, Photoreduction of CO2 using sol–gel derived titania and titania-supported copper catalysts, Applied Catalysis B 37, 37 (2002)
2. I-H. Tseng, J. C.-S. Wu, H.-Y. Chou, Effects of sol-gel procedures on the photocatalysis of Cu/TiO2 in CO2 photoreduction
Journal of Catalysis, in press 2003.
Figure 1: Procedure of sol-gel method to
prepare Cu/TiO2
Figure 2: TEM of 2 wt% Cu/TiO2
Irradiation time (h) 0 5 10 15 20 25 30 35 M et h anol y iel d ( µ m o l/ g-cat al ) 0 100 200 300 400 500 600 700 800 900 1000 1100 CuCl 2-0h CuCl2-1h CuCl2-3h CuCl2-8h Figure 3: 混入溶膠時間(0、1、3、8h)對 2%Cu/TiO2觸媒光催化活性之影響;使用 光源為UVC (254nm)。 CuCl2-8h CuCl2-0h r-CuCl2-3h CuCl2-3h r-CuAc2-8h Irradiation time (h) 0 5 10 15 20 25 30 M et h an o l y iel d ( µ mol/g) 0 2 4 6 8 10 12 14 Figure 4 : 不同製程製得2%Cu/TiO2觸媒 之光催化活性;”CuCl2、CuAc2”表示金屬 前驅物種類,”0、3、8h”表示Cu前驅物 混入溶膠時間,”r-“表示觸媒經過氫氣還 原;使用光源UVA (365 nm)
4 o Distance (A) 0 1 2 3 4 5 6 7 8 M agnitude 0.000 0.002 0.004 0.006 0.008 0.010 0.012 0.014 CuCl2-0h CuCl2-1h CuCl2-3h CuCl2-8h Figure 5: 以CuCl2(s)為前驅物,混入溶膠 時間(0、1、3、8h)對2%Cu/TiO2觸媒 Cu(Ka) FT-EXAFS圖譜之影響 300 400 500 600 0.0 0.5 1.0 1.5 2.0 2.5 3.0 (g) (f) (e) (d) (c) (b) (a) K-M ab so rp ti o n nm
Figure 6: V/TiO2經400o
C-30min鍛燒之UV-VIS吸收光譜,(a)TiO2、(b)V/Ti=0.01、 (c)V/Ti=0.02、(d)V/Ti=0.029、 (e)V/Ti=0.035、(f)V/Ti=0.052、(g)V2O5 (a) (b) Figure 7: (a)F-HXXS-3%-R20鍍膜光纖斷 面SEM圖;(b)鍍膜光纖SEM圖