第一章
物質的組成
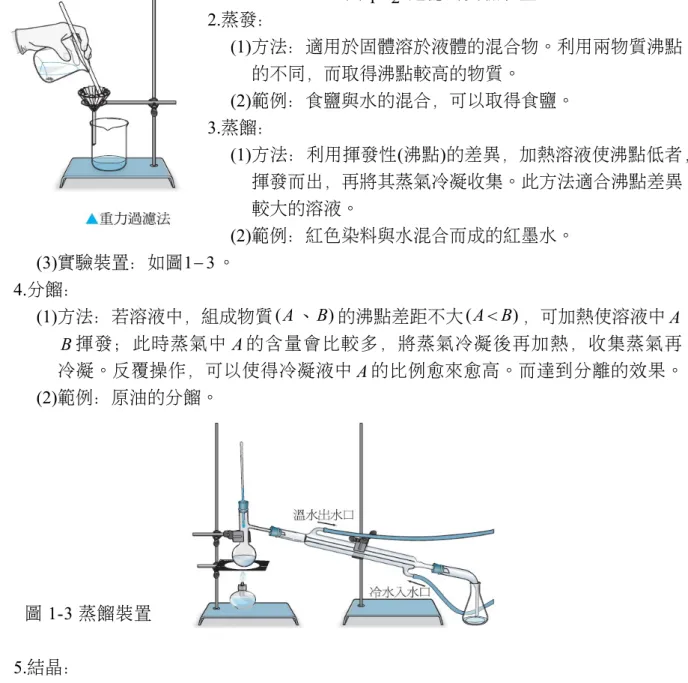
1-1 物質的分類 一.物質的分類:化學家依物質的性質,將所有的物質分為兩大類,即純物質與混合 物。如圖1 1 所示。 1.純物質:具有一定組成、性質的物質;依其成分可分為元素與化合物。 (1)元素:由單種原子所組成的純物質,無法用一般化學方法,分離出更簡單的物 質。目前已知的元素共有112 種,其中 88 種存於自然界。如,氧氣(O2)、氮氣 ) (N2 、黃金( Au)等等。 (2)化合物:由兩種或兩種以上原子,依一定比例所組成的純物質,可用一般的化 學方法,分離出更簡單的物質。如,二氧化碳(CO2)、氨氣(NH3)等等。化合 物具有其特性,但不具有成分元素的性質。 2.混合物:由兩種或兩種以上的純物質以任意比例混合而成。其中所含的純物質仍 保有原化學性質,可用物理方法,分離出所含純物質。又可分為均勻混合物(溶 液)和不均勻混合物。 (1)均勻混合物:即溶液,如糖水、黃銅及空氣等。此等混合物在巨觀上無法分辨 其組成成分。在微觀上,這些成分仍保有各自的性質,可用物理方法分離。 (2)不均勻混合物:如砂石等。 3.物質的分類的原則是依據物質的性質予以系統化,因此也可將元素分成金屬與非金 屬;而化合物亦可分為有機化合物與無機化合物兩種。 4.純物質與混合物的比較: 純物質 混合物 定義 僅具單一種成分的物質 由兩種以上成分所混合而成的物質 特性 (1)組成一定 (2)定壓下,具有固定的熔點與沸點 (3)可再區分為元素及化合物 (1)各成分仍保有其性質 (2)各成分的比例可以改變 (3)定壓下,熔點與沸點並不固定 分離方式 無法利用物理方法分解之 可利用物理方法分離出純物質 實例 食鹽、鐵、碳酸鈣 食鹽水、空氣、合金 5.元素與化合物的比較 元素 化合物 定義 不能用一般化學方法再分解的最 由兩種以上之元素依一定的比例組簡單物質 成,可用化學方法再分離出成分元 素的純物質 分離方式 無法以化學方法再分解 可利用化學方法分離出元素 實例 金、氧、水銀、硫黃 水、氫氧化鈉、酒精 圖 1-1 二.物質的性質: 在日常生活中,我們處理的對象,往往是由為數極多的分子所組成的物體,而 非分子本身,而化學所要探討的是分子層次的物質性質,所觀察的則是所有分子整 體的性質,即所謂的巨觀現象。化學家研究物質,是為了瞭解其性質,進而加以應用 所謂的物質是占有空間,具有質量,且具有其固定的性質。而物質的性質通常可分為 物理性質與化學性質: 1.物理性質:物質在不發生化學變化下(只發生物理變化),能由感官辨認或用儀器 量度的性質稱為物理性質,如顏色、沸點、熔點、密度、溶解度及延展性等。 2.化學性質:物質發生化學變化時,所表現的特性,稱為化學性質,如可燃性、助 燃性、酸鹼性、氧化力及還原力等。 三.物質的分離:通常混合物可經由物理方法分離而得到兩種或兩種以上的純物質;而 利用物理性質上的差異來分離物質的方法稱之為物理方法。常見的物理方法有 1.溶解與過濾: (1)方法:選擇合適的溶劑,將混合物中的某成分溶解,再以濾紙將不溶性成分與 溶液分離。 (2)範例:食鹽與沙子的混合。 (3)實驗裝置:如圖1 2 。
圖 1 2 過濾的實驗裝置 2.蒸發: (1)方法:適用於固體溶於液體的混合物。利用兩物質沸點 的不同,而取得沸點較高的物質。 (2)範例:食鹽與水的混合,可以取得食鹽。 3.蒸餾: (1)方法:利用揮發性(沸點)的差異,加熱溶液使沸點低者, 揮發而出,再將其蒸氣冷凝收集。此方法適合沸點差異 較大的溶液。 (2)範例:紅色染料與水混合而成的紅墨水。 (3)實驗裝置:如圖1 3 。 4.分餾: (1)方法:若溶液中,組成物質(A、B)的沸點差距不大(A<B),可加熱使溶液中A B揮發;此時蒸氣中 A的含量會比較多,將蒸氣冷凝後再加熱,收集蒸氣再 冷凝。反覆操作,可以使得冷凝液中A的比例愈來愈高。而達到分離的效果。 (2)範例:原油的分餾。 圖 1-3 蒸餾裝置 5.結晶: (1)方法:將當溶液中的溶劑量減少或溫度下降,可使溶質析出的現象。將固態混合 物以適合的溶劑溶解,再經由過濾與結晶的程序,使其純化的過程。 (2)範例:食鹽(NaCl)與硝酸鉀(KNO3)的混合物。 (3)實驗裝置:如圖1 5 。 (4)結果:會析出溶解度隨溫度變化比較大的物質。 翰林 P7 翰林 P7
圖1 4 石油分餾的裝置 圖1 5 結晶法的操作步驟 6.層析: (1)方法:利用物質在惰性介質中吸附力的差異來分離混合物 的方法。當物質與介質間的作用力愈大,其移動速率愈慢。 (2)範例:墨水層析。 (3)實驗裝置:如右圖1 6 。 (4)大致上可分成濾紙層析與管柱層析等方法。 7.萃取: 圖 1 6 層析法 (1)方法:利用某種物質對於兩種互不相溶的溶劑之溶解度差異,而將此物質由溶 解度較小的溶劑中移至溶解度較大的溶劑中。 (2)範例:以環己烷萃取水層的碘。 1.下列有關各種分離物質方法的敘述中,正確的是 (A)過濾法可將溶液中的溶質與溶 劑分開 (B)蒸餾時冷凝管所用的冷卻水是由上方水管進入 (C)蒸餾酒精的水溶液, 蒸氣冷凝後的液體為純酒精 (D)分餾石油,所得的汽油產物是混合物。 2.化合物與元素的不同點是 (A)前者含多種原子,後者僅含一種原子 (B)前者含多個 原子,而後者僅含一個原子 (C)前者性質不一定,後者性質固定 (D)前者可利用 化學方法分解成其他物質,後者不能再分解成其他物質 (E)前者是純物質,後者 是混合物。 3.下列有關化合物與混合物的敘述中,錯誤的是 (A)化合物有一定的熔點,而混合物 無一定熔點 (B)化合物經由化學反應生成,混合物則經由物理變化生成 (C)化合 物的組成固定,混合物則不固定 (D)化合物與混合物均可藉物理方法分離。 4.分餾石油時,是利用不同成分間何種性質的差異? (A)熔點 (B)沸點 (C)密度 (D)化 學性質。
5.一混合物經濾紙色層分析後,結果如右下圖。若各成分與濾紙間的作用力為F1,各成 分與展開液間的作用力為F2,則混合物中的哪一種成分之(F2 F1)值最大? (A)甲 (B)乙 (C)丙 (D)丁 (E)戊。 6.下列物質中,屬於元素的有哪些?化合物的有哪些?純物質有哪些?混合物有哪 些?哪些具有固定的沸點與熔點? (甲)過氧化氫(H O2 2( )l ) (乙)漂白水 (丙)18K金 (丁)碳六十 (戊)黃銅 (己)汽油 (庚)黃金 (辛)雙氧水(H O2 2(aq)) 7.常見混合物的分離方法有(甲)過濾(乙)蒸餾(丙)分餾(丁)結晶(戊)層析(己)萃取。下列各 混合物的分離,可採用上述的何種方法? (1)由食鹽水中分離出氯化鈉。(選最簡單) (2)由紅墨水中分離出水。 (3)由綠色樹液中分離出葉綠素。 (4)由藍色原子筆液中分離出不同色素。 (5)由沸點相近的苯與甲苯溶液中,分離出苯。 (6)由混濁的泥水中,分離出泥沙。 8.下列各種物質分離的方法中,利用物質沸點不同使其分離的是 (A)過濾 (B)傾析 (C)蒸餾 (D)分餾 (E)層析。
9.下列物質中,屬於純物質的有 (A)鹽酸 (B)空氣 (C)硫酸銅晶體(CuSO4‧5H O2 ) (D) 食鹽水 (E)金剛石。 <Homework 1-1> 1.物質可以三種狀態存在,這三態間主要的差異是 (A)組成物質不同 (B)組成物質的 形狀不同 (C)粒子大小不同 (D)粒子間的距離不同。(D) 2.下列那些物質於常溫常壓下,具有一定的體積與形狀 (A)銅絲 (B)氮氣 (C)汞 (D)水 晶 (E)糖水。(AD) 3.下列那些不是物質? (A)水 (B)光 (C)聲音 (D)空氣 (E)二氧化碳。(BCD) 4.下列那些是純物質? (A)水銀 (B)糖水 (C)鈉 (D)葡萄糖 (E)空氣。(ACD) 5.醬油、牛奶、乙醇、空氣、金剛石及水銀。在這六種物質中,屬於純物質的共有 (A)1 (B)2 (C)3 (D)4 種。(C) 6.下列那些是混合物的性質? (A)組成可以改變 (B)不具組成物質的性質(C)性質隨組 成而異 (D)可用物理方法分離 (E)都是非均勻狀態。(ABCD) 7.下列有關元素及原子的概念,那一項敘述是正確的 (A)純物質甲受熱分解產生純物 質乙及氣體丙,則物質甲不可能是元素 (B)具有物質特性的最小單元是原子 (C) 由兩種相同元素組成的多種化合物,性質必相同 (D)乾淨的空氣是純化合物。(A) 8.下列有關常見物質的分類的敘述,何者正確? (A)純水可經由電解生成氫氣及氧氣, 所以不是純物質 (B)食鹽由氯化鈉組成,所以是純物質 (C)糖水為純糖溶於純水 所組成,所以是純物質 (D)不鏽鋼不易生鏽,所以是純物質。(B) 9.下列各項為小毛在觀察蠟燭燃燒的實驗時,所得的記錄,何項為化學性質的描述 ? (A)蠟燭為圓柱形 (B)加熱時熔化為液體 (C)產生的二氧化碳可使廣用指示劑呈黃 色 (D)產生的水可使白色硫酸銅粉末變藍色 (E)燭心為三股棉線組成。(CD) 10.下列各組物質中,屬於同素異形體的有 (A)石墨與鑽石 (B)水與重水(C)一氧化碳 與二氧化碳 (D)白磷與赤磷 (E)鈾 235 與鈾 238。(AD) 11.下列關於水的各項敘述中,正確的有 (A)一個水分子共有 8 個電子(B)水可與蔗糖 形成氫鍵 (C)水可與鉀金屬反應生成氫氣 (D)水可與乙醇以任何比例互溶 (E)重水 分子中每個氘原子有2 個中子。(BCD) 12.下列各項敘述中,屬於化學性質的有 (A)水的凝固點為0oC (B)鐵在潮濕的環境下
容易生鏽 (C)煤氣燃燒 (D)水的密度在4oC時最大 (E)非金屬氧化物溶於水呈酸性。 (BCE) 13.下列各種物質性質的敘述中,屬於物理性質的有 (A)鈉為銀白色的物質 (B)金的延展 性極佳 (C)氫為可燃性的物質 (D)汞為液態的物質 (E)硫酸具有強腐蝕性。(ABD) 14.下列各種方法中,屬於化學方法的有 (A)過濾 (B)電解 (C)傾析 (D)蒸餾 (E)沉澱。(BE) 15.下列有關濾紙色層分析法的敘述中,錯誤的是 (A)此法為利用物質比重的不同以分 離物質 (B)與濾紙間作用力愈大的物質,在濾紙中展開的距離愈遠 (C)利用濾紙色層 分析法可分離出植物色素的成分 (D)濾紙色層分析法須在真空環境中進行 (E)多數時 候,會利用加熱的方式以加快濾紙色層分析的速度。(ABDE) 16.下列有關過濾的敘述中,錯誤的是 (A)不可應用於將水分解得氫氣與氧氣 (B)利用物 質顆粒大小不同的原理 (C)抽氣過濾法是利用瓶內外壓力差迫使溶液快速通過之過濾 法 (D)可利用過濾法分離食鹽水 (E)經過濾後所得的物質不一定為純物質。(D) 17.下列各種方法中,可用來確知柴油是純物質或混合物的方法是 (A)測其沸騰時的溫 度 (B)測其密度 (C)燃燒 (D)過濾 (E)傾析。(A) 18.常見的混合物分離方法有 (A)層析法 (B)蒸餾法 (C)過濾法 (D)傾析法 (E)昇華法。欲 從下列混合物中分離出括號()內所顯示的物質時,宜用上述哪一種方法? (1)碘固體與氯化鈉的混合物。(碘固體)。(E) (2)葡萄酒。(乙醇)。(B) (3)泥水。(水)。(C) (4)染料。(各種色素)。(A) (5)含碳酸鈣固體的水溶液。(碳酸鈣固體)。(D) 19.下列有關純物質的敘述中,正確的是 (A)均勻物系均為一種純物質 (B)就微觀而言, 一種純物質是由同一種粒子所組成 (C)若一黃色氣態純物質加熱後無法再被分解,則 必為化合物 (D)純物質包含元素與化合物 (E)純物質具有一定的熔點、沸點及化性。 (DE) 20.下列常使用於分離物質的實驗器材中,名稱錯誤的有(AE) 1 - 2 原子與分子 (A) (B) (C) (D) (E) 錐形瓶 燒杯 玻棒 蒸餾瓶 抽濾漏斗
物質是由分子所組成的;而分子又是由原子所組成的;然而原子是由更小的粒子,如 質子、中子與電子所組成的。其中具有物質特性的最小粒子是分子;組成物質的最小粒 子則是原子。而常見的化學反應類型有: 1.化合:兩種以上的物質反應生成一種化合物的反應。ABAB。 2.分解:一物質經反應後,生成兩種或以上物質的反應。ABAB。 3.取代(置換):化合物中ㄧ元素被另一種元素取代的反應。ACBABC。 4.複分解(交換伴侶):二種化合物先行分解後,再進行反應生成二種新的化合物。 CB AD CD AB 。 一.質量守恆定律(質量不滅定律): 1.提出者:法國科學家拉瓦節(1774)。號稱近代化學之父,推翻燃素說,提出氧化理論 2.內容:於密閉容器中的一般化學反應,其反應前(所有反應物)總質量等於反應後(所 有生成物加剩下反應物)總質量。 3.說明:物質是由原子所組成,而化學反應則是原子重新排列產生新物質,於其過程 中原子的種類、數目均不變,故反應前後總質量不會變。 1.某化學反應方程式3A2BC2D,今有2.7g 的 A 與4.2g的 B 一起反應,一段 時間後, A 完全用完而 B 則剩下1.4g並產生了1.8g 的C ,則可得 D 多少公克? 2.已知2A 3BC,且 A 、B 、C 表不同的分子;若 A 、B 分子量分別為 24 及 12, 則C 的分子量是多少? 3.已知今有15.3g 的 A 物質和10.5g 的 B 物質完全反應,生成7.5g 的C物質、 g 8 . 1 的 D 物質與0.3mol的 E 物質,則 (1)可產生 E 多少公克? (2) E 的莫耳質量是多少?
二.定比定律(定組成定律): 1.提出者:法國科學家普勞斯特(1799)。 2.內容:同一化合物不論其來源或製備方法,其組成元素的質量比恆為一定值,適用 於化合物。 4.甲、乙兩位學生,利用不同方法分別得到水,甲生並分析其中含有氫元素的比例是
9
1
,而乙生分析結果發現氫與氧的比恆為1:8。根據此結果可證實何種定律。 5.根據定比定律。試寫出下列空格的答案。(F 19、H 1、O16、Si28) (1)A的化學式? (2)B=? (3)C的化學式? (4)D的化學式? (5)E的化學式? 三.道耳吞原子說:英國科學家道耳吞(1802)所提出的,其內容可解釋質量守恆定律與 定比定律,其內容如下: 1.任何物質皆由原子所組成,原子是組成物質的最小單位,不能在分割了。 (爭議)因為原子可分割成質子、中子與電子,甚至介子。 2.相同元素的原子具有相同的質量與性質,不同元素的原子則具有不同的質量與性質。 (爭議)因為有同位素的存在。所以相同元素的原子可能具有不同的質量。 3.化合物是由不同元素的原子以不同的比例相結合而形成不同化合物。 4.化學反應只是原子間的重新排列,反應前後原子種類與數目不變。 (爭議)現有核反應,反應前後會有新原子生成或原子被用掉。 5.原子說的修正:依照現有的化學知識,原子說的內容應做下列修正。原子說的內容 現有概念 原子無法再被分割成更小的粒子。 原子可再分割為電子、質子、中子等更小 的粒子。 同一元素的原子具有相同的質量及性質。 同 一 元 素 的 質 量 未 必 相 等 , 如 同 位 素235 92U 、 238 92U 為同一元素但質量不同。 不同元素的原子之質量與性質互異。 不同元素的質量未必不相等,如同量素14 6C、 14 7N為不同元素但質量相同。 發生化學變化時,化合物中的原子重新排列 組合,原子的種類及數目不變。 若涉及核變化,則原子的種類會產生改 變,如氫可經核熔合變為氦。 6.根據道耳吞原子說,則下列敘述中正確的有 (A)碳原子都是相同的 (B)氯有兩種同位 素 (C)氧原子與氫原子的性質不同 (D)原子是由原子核與電子所組成 (E)水中的氫原 子與氫氣中的氫原子是相同的。 7.利用原子說可解釋下列哪些基本定律? (A)定比定律 (B)倍比定律 (C)亞佛加厥定律 (D)氣體反應體積定律 (E)質量守恆定律。 四.倍比定律: 1.提出者:英國科學家道耳吞(1804)。 2.內容:當兩種元素化合時可形成多種化合物,若將其中一元素質量固定,則另一元 素之質量比恆成固定簡單整數比。 8.下列各組化合物中,可以說明倍比定律的有(A)O2、O3 (B)NH3、N2H4 (C)NO、 2
NO (D)HNO2、HNO3 (E)PCl3、PCl5。
9.化合物甲由 2.0 克的A與5.0 克的B化合而成;化合物乙由4.0 克A與12.5 克的B所 化合而成。若甲之化學式為A B2 4,則化合物乙的可能化學式?
10.若元素 A 、B 可結合成甲、乙兩種化合物;已知化合物甲6.0g中含有3.2g 的 B 元 素,化合物乙2.7g 中含有0.7g的 A 元素。若甲化合物之化學式為 AB ,則乙化 合物的化學式可能是什麼? 11.已知某化合物A2B315.0g 中含有4.5g 的 B ,另一含 A 、B 之化合物中, B 占重 量16% ,其化學式可能是 (A)A3B2 (B) AB (C)A2B (D)AB2。 12.已知化合物A2B的重量百分組成分別是60%的 A 與40%的 B ,則化合物 AB 的 重量百分組成分別是多少? 五.氣體反應體積定律(氣體化合體積定律): 1.提出者:法國科學家給呂薩克(1808)。 2.內容:定溫定壓下,參與反應的氣體或生成的氣體,其體積比恆成簡單整數比;若 為一氣體反應(反應物、生成物均為氣體)時,化學反應方程式中的係數比即是莫耳數 比亦是體積比(反應物是消耗,而生成物則是生成)。 六.亞佛加厥假說: 1.提出者:亞佛加厥(1811)。 2.內容:同溫、同壓下,同體積的氣體分子具有相同的分子數(莫耳數)。亦可改成同溫、 同壓下,氣體分子的體積比等於分子數比等於莫耳數比。
七.同位素:是指具有相同的原子序(質子數、化學性質),不同中子數(質量數、物理性質) 的元素。如:原子序=1(氫:1H 1 、氘 H 2 1 、氚 H 3 1 )、氧( O 16 8 、 O 17 8 、 O 18 8 )。 13.於NTP下,2.0L的氫氣含有
a
個分子,則同條件下,6.0L的氦分子,其含有的 分子數是多少? 14.已知,1.0L的氮氣可與3.0L的氫氣反應,產生2.0L的氨氣,則4.0L的氮氣可 與15.0L的氫氣反應,產生多少的氨氣? 15.已知常溫常壓時甲、乙、丙均為氣體,且兩體積的甲會與一體積乙化合成兩體積之 丙。若甲的化學式為 A2,則乙之化學式可能為下列何者? (A)A B2 (B)AB2 (C) 2 2 A B (D)A B2 3 (E)B2。 16.曉華分析鉛的兩種氧化物,分析之後得知其中含鉛的重量百分率分別是92.83%與 89.62%,當其所含的氧重量相等時,則所含鉛重量的比大約是 (A)3:2 (B)2:1 (C)1:2 (D)2:3。 17.同溫同壓下,氣體反應(甲)N2(g) 3H2(g) 2NH3(g) (乙)N2(g) O2(g) 2NO(g) (丙) ) ( 2 ) ( 3 ) ( 5g PCl g Cl g PCl ,則下列關於反應後氣體密度變化的敘述中,正確的是 (A) 甲密度變大 (B)乙密度不變 (C)丙密度變小 (D)甲密度變小 (E)甲乙丙密度均不變。18.同溫同壓下,氣體甲2.0L重1.20g,氣體乙1.0L重0.64g。已知,乙氣體是氧氣,而 甲氣體僅由氧與氮元素所組成,則下列各化學式中,可能是甲的是 (A)N O2 (B)NO (C)NO2 (D)N O2 5。 19.將空氣加熱至2000o C,空氣中的氮氣與氧氣會發生反應。若反應前後體積不變,該 反應的主要產物是(A)N O2 (B)NO (C)NO2 (D)N O2 5。 20.由於 1.0 公克的氫可與 8.0 公克的氧作用生成 9.0 公克的水,所以道耳吞認為水分子 的分子式是HO,而氧的原子量為8。如果 11 公克鈾的氧化物中,含有 10 公克的鈾 則根據道耳吞理論,下列敘述中,正確的是 (A)鈾的氧化物應該是UO,鈾的原子 量為80 (B)鈾的氧化物應該是UO2,鈾的原子量為240 (C)鈾的氧化物應該是U O2 3, 鈾的原子量為240 (D) 鈾的氧化物應該是U O3 8,鈾的原子量為80。(92 學測) 八.原子與分子的比較: 1.原子: (1)構成物質的最小粒子。 (2)元素與化學反應的最小粒子。 (3)其性質隨元素的種類而異。 (4)化學反應原子重新排列組合成新物質。 2.分子: (1)保留物質性質的最小粒子。 (2)由原子所組成,可分成 碳六十(C60) 分 子結構 a.元素態分子:由相同元素所組成,如氫氣(H2)、氧氣( )O2 、氮氣(N2)。
b.化合物分子:由不同元素所組成,如水(H O2 )、氨氣(NH3)。 c.單原子分子:如鈍氣,氦(He)、氫氣(H2)、氮氣(N2)、一氧化碳(CO)。 d.雙原子分子:如氧氣( )O2 、氖(Ne)、氬(Ar)、氪(Kr)、氙(Xe)、氡(Rn)。 e.多原子分子:如硝酸(HNO3)、碳六十(C60)、白磷( )P4 、葡萄糖(C H O6 12 6)。 21.下列有關原子與分子的敘述中,正確的是 (A)若兩個化合物具有相同的原子種類與 數目,則兩化合物是相同的 (B)同種類的原子可形成不同的分子 (C)氫原子與氫分子 的性質相同 (D)分子是由同一種原子所組成 (E)分子為具有物質性質的最小粒子。 22.下列科學家與其提出之理論(或定律)的配對中,錯誤的有 (A)普魯斯特-定比定律 (B) 拉瓦節-倍比定律 (C)道耳頓-原子說 (D)給呂薩克-氣體化合體積定律 (E)亞佛加 厥-分子說。 下列哪些化學反應式中,各物質的體積變化量比恰為反應式中對應的係數比? (A)H2( )g I2( )g →2HI( )g (B)2H2( )g + O2( )g → 2H O2 ( )l (C)3H2( )g + N2( )g → 2NH3( )g (D)NH3( )g + HCl( )g → NH Cl4 ( )s (E)N2( )g + 2O2( )g → 2NO2( )g 。 (ACE) <Homework 1-2> 1.已知,反應A3B2C,若 A 、B 、C 表不同分子,且 A 、B 的分子量分別是28、 2 ,則C的分子量是多少?(17) 2.已知某金屬1.0g,在空氣中加熱後變成金屬氧化物1.25g ;今若有1.0g的該金屬 氧化物,則可還原得到多少金屬?(0.80g) 3.已知,定溫定壓下, L2 的甲氣體可與 L4 的乙氣體作用,並產生 L4 的丙氣體,若 乙氣體不含 A 原子,甲氣體只含 A 、B 兩種原子,則下列化學式中,可能是甲的有
(A)AB2 (B) AB3 (C) A2B2 (D) A2B3。(C) 4.已知, L4 的氧氣重6.4g,於同溫同壓下,而2.0L某氣體重4.6g,則某氣的分 子量是多少?(46) 5.均為氣體的甲、乙、丙,於同溫同壓下 2 體積的甲與 1 體積的乙,可化合生成 2 體積的 丙,若甲的分子式為 A2,則乙的分子式可能為 (A)AB2(B) AB (C)A2B3(D)A2B2 。(D) 6.若 A 、B 兩元素可組成甲、乙兩種化合物,於甲化合物中, A 佔75%,乙化合物中 A 佔80%;若甲化合物的分子式為AB4,則乙化合物的分子式可能是?(AB3) 7.於化合物AB2中, A 元素的重量百分比是30.4%,則化合物A2B3中, A 元素的 重量百分比是多少?(36.7%) 8.利用道耳吞原子 可解釋下列基本定律?説 (A)定比定律 (B)倍比定律 (C)質量守恆定律 (D)亞佛加厥定律 (E)氣體反應體積定律。(ABC) 9.甲烷(CH4)與乙烷(C2H6)的混合體積為100mL,經完全燃燒可得同狀況下的二氧 化碳160mL,則混合氣體中乙烷的體積百分率是多少?(60%) 10. 已知 有某 氣 態 烴(CxHy)10mL, 經 完 全 燃 燒 後 , 可 生 成 同 溫 同 壓 下30mL的 ) ( 2 g CO 與40mL的H2O(g),則x y?(11) 11.已知1.0L的 A 氣體與1.0L的 B 氣體可化合生成2.0L的C氣體;若 A 氣體是 2
H ,則 B 氣體可能是 (A)Cl2 (B)HCl2 (C)H3Cl2 (D)H4Cl2 (E)Cl4。(ADE)
12.已知化合物AB2、AB3中,含 B 的重量百分率分別是a%、b%,則
a
與b的關係 為何? ) 300 200 ( b b a 13.下列各組物質中,可以說明倍比定律的是 (A) 2 4 SO 、 4 ClO、 4MnO (B)LiF 、LiCl、
LiBr (C)O2、O3 (D)NO、NO2、NO3。(D) 14.某化合物之化學式為A B2 3,且10 公克中含有 3.3 公克的B;另一也含有A、B兩元 素之化合物X 中,B之重量百分率為25%,則X 之化學式可能為何?(AB) 15.道耳吞原子說是根據何種理論所提出的? (A)由實驗結果看到原子的存在 (B)歸納實 驗結果,假設原子的存在 (C)根據希臘古代哲學家的理論 (D)根據拉瓦結的燃燒實驗。 (B) 16.在1000mL的氧氣中,進行放電實驗使其產生臭氧(3O2 2 )O3 。反應後,在同溫同下 壓下,其總體積變成900mL,則下列敘述中,正確的是 (A)生成臭氧100mL (B)生成 臭氧200mL (C)剩下氧氣800mL (D)剩下氧氣700mL (E)反應後臭氧的莫耳數佔混合 氣體總莫耳數的2 9 。(BDE)(80 日大) 17.根據定比定律。試寫出下列空格的答案。(C12、H 1、O16、N 14、Si28) (1)A的化學式?(H O2 ) (2)B的化學式?(N O2 3) (3)C的化學式?(CH4) (4)D的化學式?(SiO2)
(5)X 應為多少?( )14 3 (6)Y應為多少?(3) (7)Z應為多少?(7) 18.某元素X 所形成的五種氣體化合物, 於常溫常壓下,每24.5L的重量及其 中所含X 的重量百分比如右表。基 於原子學說及本實驗結果,X 的 原子量可能是 (A)3 (B)6 (C)8 (D)12 (E)16。(ABD)(91 指考) 1802 年道耳頓提出以下的原子學說, 從 現在的化學知識來看,下列何者仍然正確? (A)一切物質都是由原子組成 (B)相 同元素的原子,具有相同的質量及性質 (C)化合物分解所得的原子與構成化合物 的同種原子性質相同 (D)原子是基本粒子,不可分割 (E)不同元素的原子性質不 同。(ACE) 1-3 原子量與分子量 原子、分子、離子是構成物質的基本粒子,但因這些粒子非常微小,肉眼看不見,無 法取單一粒子秤其質量,因此採用相對質量。同時可從化學反應中發現,基本粒子以一 定的個數比和質量比進行反應,因此可以推知它們的個數與質量間存在某一定種關係。 同一種原子或分子的平均質量均相同,因此使用質量來推算個數,便成為可行的辦法。 一.原子量: 1.原子太小、太輕,因此原子的質量,無法直接測量,目前仍採用相對原子量。 化合物 重量(克) 含X 的% 甲 60 80 乙 44 82 丙 44 27 丁 30 80 戊 16 75
2.西元1961年,國際純粹與應用化學聯合會(簡稱IUPAC)規定,以12C的原子質量 為12.0000,做為原子量的比較標準,其他原子的質量,都是和12C原子比較所得 的相對質量。 3.原子質量單位(簡稱
amu
), g g amu 24 23 1.66 10 10 6.02 1 1 1 個12C原子質量 的 12 1 。 4.某元素的原子質量與碳原子質量比等於該元素一個原子的質量和一個12C原子質量 的比;即 0000 . 12 待測原子的原子量= 原子的質量 同數的待測原子質量 與 12 12 C C 。 5.許多原子有同位素存在,依其存在含量,便可計算出平均原子量。可利用下列數學 式求得,M M1X1M2X2 M3X3 、、、、。 6.在週期表中所列各種元素的原子量,都是平均原子量。 7.原子量是一個相對值,沒有單位的。 二.分子量: 1.定義:為該分子中,各組成原子的原子量總和。 2.單位:由於原子量是相對質量,故分子量也是相對質量;所以也是沒有單位的。 1.已知,某元素 20 個原子重620amu,則此元素的原子量是多少? 2.已知下列各元素的原子量:C 12、H 1、O16、N 14、Cl 35.5、Cu64、 32 S 、Ca 40、P31,求下各化合物的分子量或式量: (1)葡萄糖(C6H12O6)(2)硫酸(H2SO4)(3)尿素(CO(NH2)2)(4)磷酸鈣(Ca3(PO4)2) (5)丙酮(CH3COCH3)(6)氯化四氨銅(Cu(NH3)4Cl2) 3.等數目的12C原子與某未知原子,進行質量測定,可得兩者的質量分別為18.0g 與 g 0 . 24 ,則該未知原子的原子量為若干?4.已知,某原子的原子量為14.0,取若干12C原子,測得質量為144.0g,取與其等 數目的某原子,其質量應為若干克? 5.一個CO2分子的質量是多少? 6.自然界中,硼有兩種同位素 B10 與 B11 ,而硼的平均原子量是10.8,則自然界中, 兩種同位素的含量比( B10 : B11 )是多少? 7.同溫、同壓下,若10mL的甲烷分子含有a個原子,則多少毫升的氮氣也含有a個原子 (A)5 (B)10 (C)25 (D)50。 三.亞佛加厥常數:於12.0000g的12C中,含有6.021023個12C原子,而此一數目 即稱之為亞佛加厥數,化學上以N 來表示;同時這麼多的粒子數也剛好等於1 莫耳。 四.莫耳:表示粒子數目的一種單位,與亞佛加厥數同數目的粒子數稱為 1 莫耳。 1.莫耳是基本量,凡是 1 莫耳的任何物質,均含有6.021023個粒子。 2.莫耳可應用於分子、原子、離子、電子的計量。這些微粒都具有數目多、質量小的特性。 五.莫耳質量是指 1 莫耳物質的質量,通常以克為單位。 1.克原子量:以克為單位的原子量,稱為克原子量。如,氧原子的莫耳質量為 16 克, 即1 莫耳的氧原子,質量為 16 克,也就是氧的克原子量是 16 克。 2.克分子量:對分子化合物而言,以克為單位的分子量,稱為克分子量。如,水分子 的莫耳質量為18 克,即 1 莫耳的水分子,質量為 18 克,也就是水的克分子量是 18 克。 3.克式量:簡式中各組成原子的原子量總和,稱為式量,以克為單位則稱為克式量。
如,氯化鈉的克式量是58.5 克。 六.莫耳體積(Vm):一莫耳物質的體積,稱為莫耳體積。 1.氣體的莫耳體積: (1)氣體的莫耳體積隨溫度、壓力而改變,故須在一定溫度及壓力下測定。 (2)在STP(0oC、1 atm.0 )下,任何氣體的莫耳體積為22.4L。 (3)在NTP(25oC、1 atm.0 )下,任何氣體的莫耳體積為24.5L。 (4)1 莫耳體積的任何氣體,均含6.021023個氣體分子。 2.固體及液體的莫耳體積與物質的種類,溫度高低有關,而與壓力無關。 3.莫耳體積的應用:求氣體的分子量;氣體的分子量=氣體的密度×同狀況下之莫耳 體積。 七.莫耳數:莫耳是物質的基本量,與長度、質量、時間同為基本量。在化學計量上可簡 化計算,並可看出質量,原子數,分子數,以及反應物與產物的量的關係。 (1)莫耳數= 23 10 02 . 6 粒子數 。 (2)原子的莫耳數=克原子量質量 = 23 10 02 . 6 原子數 。 (3)分子的莫耳數=克分子量質量 = 23 10 02 . 6 分子數 = 同狀況下的莫耳體積 氣體的體積 。 (4)溶液中溶質的莫耳數CM V 體積莫耳濃度(M)
溶液體積(L)。 八.分子量或原子量可用不同方式表示。如,碳的原子量可表示為: (1)碳的原子量為12.011。 (2)一個碳原子的質量為12.011amu。 (3)一莫耳碳原子的質量為12.011克。 九.莫耳數( )n 的計算: 算法 由粒子數( )N 23 6.02 10 N n 。 由重量( )W W n M ,M 表示分子量、原子量或者式量。 由莫耳濃度(CM) n C MV ,V 表示溶液體積,單位是公升。 有氣體體積( )V ( 22.4 V n STP下), ( 24.5 V n STP下)。 由電量( )Q 96500 96500 Q Q I t n F ,F 表一莫耳電子電量,I 表電流。莫耳數的換算: 8. 碳 在 自 然 界 中 有 兩 種 同 位 素 ,12C質 量 為12.0000 , 佔 98.892 % ,13C 質 量 為 13.0033,佔 1.108 %,求: (1)碳的平均原子量? (2)12 克的碳含若干個碳原子?若干個12C原子? 9.下列各項物質的量,屬於 1 莫耳的有 (A)16 克的氧原子 (B)1.0 克的氫分子 (C)含 24 10 2 . 1 個氧原子的氧氣 (D)STP下11.2 升的氮氣 (E)0.25 莫耳的P4中的磷原子 數。 10.化合物CH2FCF3是目前符合環保所使用的新冷媒,試問:(C12、H 1、 16 O 、F 19) (1)其莫耳質量為若干克? (2)1 個分子的CH2FCF3質量為若干? (3)在153.0g的CH2FCF3中,共有該化合物 (a)若干莫耳?(b)若干個分子?(c)含有若干莫耳的C 原子、 F 原子? 11.已知,於STP下,某氣體的密度為1.96g L,求 (1)該氣體的分子量?
(2)1 升的該氣體含若干個分子? 12.下列各項物質的質量最大的是 (A)2 個水分子 (B)32amu氧分子 (C)1023莫耳氫分子 (D)5 10 23克金原子。 13.某有機化合物中,氫的重量百分率為8%,又每個分子的該化合物中,含有20個H 原子,則該有機物的分子量是多少? 14.已知某化合物中,氧的重量百分率是32%,則該化合物的可能分子量是 (A)50 (B)100 (C)160 (D)200 (E)320。 15.已知,某化合物中,氧的重量百分率是32%,則該化合物的可能分子量是 (A)50 (B)100 (C)160 (D)200 (E)320。 22.某金屬的原子量為
w
,若取該三價的金屬氧化物x
克,將其完全還原後,可得 y 克的金屬,則該金屬的原子量w
,可用哪一個式 子來表示? (A)x8yy (B) y y x ) ( 16 (C) x16yy (D) x24yy (E) x24yy 。(E)<Homework 1-3> 1.下列有關原子量的敘述中,正確的有 (A)現行原子量的標準是12C 12.0000,而碳 的原子量為12.011 (B)一個12C原子的質量為12.0000amu (C)12.0000 克的金剛石含 23 10 02 . 6 個碳原子 (D)6.021023個12C原子重12.0000amu (E)12.011 克碳所含 碳原子數大於12.0000 克的12C原子數。(AB) 2.氫的原子量為 1.01,問 2.02 克的氫氣所含的氫原子數目與下列那一項的分子數一樣 多? (A)1 莫耳氧氣 (B)1 莫耳水 (C)2 莫耳氮氣 (D) 3 2 莫耳氨。(C) 3.有四種物質(甲)一個氧分子(乙)一個氮原子(丙)1.01010莫耳的氧氣(丁)1.01010 莫耳原子的銅,則其質量由大而小的順序為 (A)甲乙丁丙 (B)丁丙甲乙 (C)甲乙丙丁 (D)乙甲丙丁。(A) 4.下列何者所含的氧原子數最多? (A)7.2 克的水(H2O) (B)6.021022個臭氧( ) 3 O (C)0.2 莫耳的三氧化二鐵(Fe2O3) (D)2 莫耳的二氧化碳(CO2)。(D) 5.同溫同壓下,1 升的氣體所含原子數以何者最多? (A)N2H4 (B)CH4 (C)C2H6 (D) 3 NH 。(C) 6.有 1 克的下列物質所含之分子數以何者最多? (A)H2O (B)C6H12O6 (C)CH4 (D) 2 CO 。(C) 7.下列各物質,那些代表 1 莫耳的數? (A)32 克的硫分子(S8) (B)16 克的氧分子(O2) (C)17 克的氨分子(NH3) (D)4 克的He原子 (E)含1.8061024個原子的水。(CDE) 8.在STP下,某氣體0.625 克佔 0.50 升,則此氣體可能為 (A)N2 (B)Cl2 (C)O2 (D) 2 CO 。(A) 9.下列那一個是國際原子量的現行標準? (A)碳元素之平均原子量訂為 12.0000 (B)氧元 素之平均原子量訂為16.0000 (C)訂碳-12 為 12.0000 (D)訂氧-16 為 16.00。(C) 10.今有 15.3 克的 A 物質和 10.5 克 B 物質完全反應,生成 7.5 克 C 物質,1.8 克 D 物質 及0.3mol的 E 物質,求 E 的莫耳質量。(55gmol) 11.下列質量的大小順序是如何?(甲)一個碳原子(乙)1.0 克的碳原子(丙)1 克原子的碳 (丁)10000amu。(丙>乙>丁>甲) 12.將2.50g的硫酸銅晶體(CuSO4‧5H O2 )加熱至某溫度,變成1.78g 的粉末,則此 粉末的化學式可能是為何?(CuSO4‧H O2 ) 13.完全燃燒xmol的正丁烷(C4H10)可得 ymol的二氧化碳(CO2),則
x
與 y 的關係 式為何?(y 4x) 14.下列各選項中,具有最多氧原子的是 (A)3.2 公克的氧氣 (B)STP下2.24 公升的氧氣 (C)3.01 10 22個氧分子 (D)0.2 莫耳的氧氣。(D) 15.有一反應,由X 與Y化合生成Z 。其反應方程式如下, 2X 3Y 2Z,而反應物X 與生成物Z的質量關係圖如 右圖。則(93 學測)(1)當有 4 公克的Z生成時,需要多少公克的Y?(1) (2)若有 21 公克的X ,最少需要多少公克的Y才可 完全反應?同時可生成多少公克的Z?(7、28) 16.科學家計畫製造一太空電梯,以探測外太空與火星。支撐這太空電梯的纜繩是由一 束10 億條、長達 10 萬公里的奈米碳管所製成,同時每條碳管均含有7.2 10 17個碳原 子,是估計這束纜繩至少需要多少公斤的碳來製備? (A)0.12 (B)2.40 (C)7.20 (D)14.4。 (D)(93 學測) 17.滅蚊是防止登革熱的治本方法。而二溴乙烷(C H Br2 4 2 188)是滅蚊劑中的重要成份。 試問1.88 公克的二溴乙烷中, (1)含有多少個溴原子?(1.20 10 ) 22 (2)共有二溴乙烷多少莫耳?(0.01) 18.同溫、同壓下,等重的下列各氣體,體積最大的是 (A)He (B)CH4 (C)CO (D)O2。(A) 19.承上題,體積最小的是 (A)He (B)CH4 (C)CO (D)O2。(D) 20.某化學工廠之廢水中,含有鎘離子(Cd2)的重量百分率是0.0003%,則此廢水中 2 Cd 的含量是多少ppm?(3) 21.警方查獲的假酒中含有甲醇5000 ppm(1ppm相當於重量比106),則該假酒中,每 0.6L含有多少mL的甲醇?(甲醇與已醇的密度均為 0.78 g mL ) (A)1 (B)3 (C)5 (D)6。 (B)(92 學測) 1-4 溶液 一.溶液的定義:兩種或兩種以上的純物質混合,所組成的均勻、單相的混合物。 二.溶液的組成: 1.溶質:被溶解的物質;如,糖水中的糖、碘酒中的碘固體、汽水中的CO2。一般而言 溶液中的溶質可以有一種或一種以上。 2.溶劑:溶解其他物質的物質;如,糖水中的水、碘酒中的酒精。一般而言,溶液中 的溶劑只能有一種。 3.溶液:由溶質與溶劑所組成的一種均勻混合物。 4.習慣用法:
(1)溶液中,量多者為溶劑,量少者為溶質。 (2)若是 AB 溶液,則 A 是溶質, B 是溶劑。 (3)與水混合時,則不論量多少,水一定是溶劑。 (4)混合前後,狀態不變者為溶劑,改變者為溶質。 三.溶液的分類: 1.依形態:根據所形成溶液的狀態來區分,可分成 (1)固態溶液:所形成的溶液,其外觀是固態。如,合金、鈉汞齊、氫於鈀。 (2)液態溶液:所形成的溶液,其外觀是液態。如,糖水、汽水、酒、碘酒。 (3)氣態溶液:所形成的溶液,其外觀是氣態。如,空氣、水煤氣、天然氣、液化石油氣 2.依溶劑種類: (1)水溶液:當溶劑是水的溶液,則稱之為水溶液 (以 aq 來表示)。如,食鹽水 ) (aq NaCl 、鹽酸 HCl(aq)。 (2)非水溶液:當溶劑不是水的溶液,則稱之為非水溶液。如,氯的四氯化碳溶液 ) ( 2CCl4 Cl 、碘的酒精溶液 I2(C2H5OH)。 3.依導電度分: (1)電解質水溶液:溶質溶於水後,會解離並產生離子。如, 2 ) ( 4 ) ( ) ( 4 2SO aq 2H aq SO aq H 或者 2 ) ( 4 2 ) ( ) ( 4aq Cuaq SO aq CuSO 。 (2)非電解質水溶液:溶質溶於水後,不會解離。如,C6H12O6(aq)、C3H5(OH)3(aq)。 四.溶液的重要性: 1.植物由根部吸收養分、動物的消化作用、醫療用針劑、口服藥均以水溶液進行。 2.動物的體液、植物的體液、海洋均為溶液。 3.實驗室的試劑、大部分工廠的製程也都以溶液狀態呈現。 1.下列各項敘述中,正確的有 (A)溶液是一種混合物 (B)兩種純物質經由化學反應後, 可得一種均勻的物料,此物料即是溶液 (C)通常所見的金飾為固態溶液 (D)空氣是一 種氣態溶液 (E)食鹽溶於水得食鹽水,是一種化學變化。 2.下列各選項中,不屬於溶液的有 (A)空氣 (B)海水 (C)24K 金 (D)硬水 (E)乾冰。
3.下列各反應中,必為放熱反應的有 (A)酸鹼中和 (B)燃燒 (C)水合作用 (D)氣體溶解於 水 (E)固體溶解於水。 4.下列各項敘述中,屬於溶液特性的是 (A)有一定的組成 (B)長久靜置時,溶質與溶液 劑可分離 (C)可藉濾紙分離溶質與溶劑 (D)溶質均勻分散於溶劑中。 5.下列各種溶液中,屬於電解質溶液的是 (A)碘酒 (B)糖水 (C)汽水 (D)高梁酒。 6.空氣中含有多種氣體,如氮氣、氧氣、氬氣、二氧化碳。若將空氣是為溶液,則可將何 種氣體是為溶劑?(A)氮氣 (B)氧氣 (C)氬氣 (D)二氧化碳。 7.下列物質溶於水時,不發生化學變化的是 (A)氯化鈉 (B)二氧化硫 (C)氧化鎂 (D)氨。 8.一般化學反應時,常將固體反應物配製成溶液,其原因有 (A)有流動性,使接觸面積 變大,反應容易進行 (B)容易量取 (C)計量方便 (D)容易稱取 (E)儲存容易。 9.對同一種溶液而言,下列各項敘述中正確的是 (A)只有一相 (B)只有一種成分 (C)表面 上所受的壓力愈大時,其沸點愈低 (D)皆可導電。
10.常溫常壓下的下列物質,(甲)空氣 (乙)乾冰 (丙)咖啡 (丁)硬水 (戊)重水 (己)24K 金 (庚)黃銅 (辛)生鐵(壬)不繡鋼(癸)豆漿。屬於 (1)純物質的有哪些? (2)固態溶液的有哪些? (3)膠體溶液有哪些? 11.下列各選項中,不屬於溶液的是 (A)黃銅 (B)空氣 (C)白金 (D)糖水 (E)不銹鋼。 12.下列各項敘述中,錯誤的是 (A)氯化鈉(NaCl( )s )為離子固體,所以氯化鈉晶體可以 導電 (B)硝酸銨水溶液(NH NO4 3(aq))能導電 (C)醋酸為電解質,所以CH COOH3 ( )l 能 導電 (D)熔融態之硫酸鉀中,亦有離子的存在 (E)導電度是1.0M 的HCl大於1.0M 的 3 CH COOH 。 13.下列關於溶液性質的敘述中,正確的有 (A)一般溶液為均勻系 (B)溶液中溶質的粒子 極小,無法用肉眼辨識 (C)於常溫、常壓下,一定是液態 (D)空氣是一種溶液 (E)兩 物質形成溶液時,均能以任何比例混合。 五.溶液濃度的表示法 1.重量百分率: (1)定義:每100公克溶液中所含溶質的公克數。
(2)數學式: (%) 100% 100% 溶質克數溶質克數 重量百分率 溶液克數溶劑克數溶質克數 。 (3)性質:溫度的改變,並不會影響重量百分率。 14.今有一25%、400公克的氫氧化鈉水溶液,則該溶液中之溶質、溶劑的克數分別是 多少? 15.今有一20%、400公克的氫氧化鈉水溶液,欲使其濃度成15%,則須加入10%的 氫氧化鈉水溶液多少克? 2.體積百分率: (1)定義:每100毫升溶液中所含溶質的毫升數。 (2) (%) 100% 100% 溶質毫升數溶質毫升數 體積百分率 溶液毫升數溶劑毫升數溶質毫升數 。 (3)性質: a.該數值大小會隨溫度的改變而改變 b.一般而言,只適用於酒的濃度與辛烷值的算法。 16.已知10oC時,酒精與水的比重分別是0.80、1.00。試求重量百分率為30%酒精水 溶液中,所含乙醇的體積百分率。 3.重量莫耳濃度(Cm): (1)定義:每1000公克的溶劑中所含的溶質莫耳數。 (2)數學式: 1000 溶質莫耳數溶質克數溶質分子量 重量莫耳濃度 溶劑公斤數溶劑克數 。 (3)性質:溫度的改變,並不會影響重量莫耳濃度。 17.已知1000公克的氯化鈉水溶液中,氯化鈉佔有58.5公克,則該氯化鈉水溶液的重
量莫耳濃度是多少
m
?(Na 23、Cl 35.5) 18. 已 知 , 下 列 各 化 合 物 的 水 溶 液 , ( 甲 )CH3COOC2H5 ( 乙 )C3H5(OH)3 ( 丙 ) OH H C6 5 (丁)C12H22O11,其重量百分率皆為1%,則這些水溶液的重量莫耳濃 度大小順序是如何?(C 12、O16、H 1) 4.體積莫耳濃度(CM): (1)定義:每公升溶液中所含的溶質莫耳數。 (2)數學式: 1000 溶質莫耳數溶質克數溶質分子量 體積莫耳濃度 溶液公升數溶液毫升數 。 (3)性質:該數值大小會隨溫度的改變而改變。 19.已知 2 公升的氯化鈉水溶液中,氯化鈉佔有58.5公克,則該氯化鈉水溶液的體積 莫耳濃度是多少 M ?(Na23、Cl 35.5) 20.已知1200公克的氯化鈉水溶液中,氯化鈉佔有58.5公克,且該水溶液的密度為 mL g 2 . 1 則該氯化鈉水溶液的體積莫耳濃度是多少 M ?(Na23、Cl 35.5) 5.莫耳分率: (1)定義:成分物質的莫耳數與全部物質莫耳數總和的比。 (2)數學式: A C B A A X n n n n A ... 的莫耳分率 ,且XA XB XC ...1。(3)性質:溫度的改變,並不會影響莫耳分率。 21.將294公克的CaCl2‧2H O2 溶於728公克的水中,且此水溶液的密度為1.2gmL, 則(Ca40、Cl 35.5) (1)該溶液的重量莫耳濃度是多少
m
? (2)該溶液的體積莫耳濃度是多少 M ? (3)該溶液中溶質的莫耳分率是多少? 22.已知,重量百分率為98%的濃硫酸水溶液,其密度為1.84gmL,則 (1)該溶液的重量莫耳濃度是多少m
? (2)該溶液的體積莫耳濃度是多少 M ? (3)該溶液中溶質的莫耳分率是多少? 23.若葡萄糖與蔗糖兩水溶液具有相同的莫耳分率,則下列各選項中,亦會相同的是 (A)重量莫耳濃度 (B)體積莫耳濃度 (C)體積百分率(D)重量百分率。 6.百萬分之一( ppm): (1)定義:每公斤溶液中所含溶質的毫克數(mgkg);常用於稀薄溶液,亦可說成每 公升溶液中所含溶質的毫克數(mgL)。 六.溶液的稀釋與混合: 1.溶液混合或稀釋後,溶質總重與溶質莫耳數維持不變。 2.兩液體混合後,體積不一定有加成性。七.溶液的配製: 1.配置溶液的常用器材: 容量瓶 量筒 安全吸球 吸量管 滴定管 2.固體溶質配製溶液: (1)範例:以配製0.01M 、1000mL的硫酸銅水溶液(CuSO4(aq))為例。其流程圖如圖 1 8 所示。 (2)步驟: 1 Step 用稱量紙或燒杯或稱量瓶,稱取定量的溶質;並加水搖晃使其完全溶解。 2 Step 倒入1000mL的容量瓶中。 3 Step 以蒸餾水清洗。 4 Step 再加蒸餾水至容量瓶刻度線。 5 Step 蓋上瓶蓋,搖盪混合。
Step1 Step2 Step3 Step4 Step5 圖1 8 固體溶質之溶液配製 3.液體溶質配製溶液: (1)範例:以配製1.0M 、1000mL的鹽酸水溶液(HCl(aq))為例。其流程圖如圖1 9 所 示。 (2)步驟: 1 Step 以安全吸球連接分度吸量管或吸液管,吸取定量體積之濃溶液。 2 Step 吸取燒杯內的濃鹽酸(所需量)。 3 Step 於1000mL的容量瓶內,先放入適量的蒸餾水水,再慢慢加入濃鹽酸。 4 Step 加水至容量瓶刻度線。 5 Step 蓋上瓶蓋,搖盪混合。 (3)安全吸球的使用順序:先按住A(排氣栓)按S(吸液栓)最後按E(排液栓)。
Step1 Step2 Step3 Step4 Step5 圖1 9 液體溶質之溶液配製 24.下列各種濃度表示法中,其值會受溫度影響而改變的有 (A)莫耳分率 (B)體積百分率 (C)重量莫耳濃度 (D)重量百分率 (E)體積莫耳濃度。 25.已知,甲酸(HCOOH)溶液的濃度為23.6M ,比重為1.20。則其重量百分率濃度 為(A)90.5%(B)87.3%(C)78.5%(D)69.1%。 26.將濃度2.0M 的溶液一瓶,倒去半瓶,再加水至滿,攪拌均勻後再倒去
3
4
後,再 以3M 的溶液加滿,則最後溶液的濃度為若干 M ? (A)1.5 (B)2.0 (C)2.5 (D)2.8。 27.若市售硫酸比重為1.84,且重量百分率為98%,試求配製下列各濃度溶液所需市 售硫酸溶液的體積。 (1)500g、20%的H2SO4溶液。 (2)500mL、6.0M 的稀硫酸。 (3)400g、2.0m的硫酸溶液。 28.將25.0g的膽礬(CuSO45H2O)溶於200g的水中,則(1)其中含有CuSO4多少克?多少莫耳? (2)含CuSO4的重量百分率是多少? (3)含CuSO4的重量莫耳濃度是多少? (4)含CuSO4的莫耳分率是多少? 29.市售硝酸比重為1.42,且重量百分率為63%,若以下列各濃度表示時,其濃度的 數值為若干? (1)容積莫耳濃度。 (2)重量莫耳濃度。 (3)莫耳分率。 30.下列各項敘述中,正確的是 (A)重量百分率濃度相等的溶液,溶質分子量愈大者, 其重量莫耳濃度愈大 (B)莫耳分率相等的水溶液,其重量莫耳濃度相等 (C)若有一溶 液的容積莫耳濃度為aM ,重量莫耳濃度為bm,則ab (D)有甲乙兩水溶液的濃 度依次為
am
、aM ,則甲的濃度較大。 31.有關濃度p%溶液的敘述中,錯誤的有 (A)每100g溶液中,就有 p 克的溶質 (B)體 積VmL、 密 度 為dgmL的 溶 液 , 其 質 量 為Vdp% (C)100g的 溶 劑 可 配 成 p 100 104 克的溶液 (D)同一溶液,溫度愈高, p%愈小。32.欲配製0.10M 的標準溶液100mL,最好要使用下列哪一個100mL的儀器? (A)燒杯 (B)量筒 (C)燒瓶 (D)容量瓶 (E)錐形瓶。(95 指考) 八.溶解與沉澱: 1.溶解:當固體置入液體溶劑中,其粒子會離開固體表面進入液體中的現象。 2.沉澱:當固態物質自溶液中析出的現象。 3.溶解平衡:當溶質溶於溶劑中的溶解速率等於溶質的結晶速率時,而且溶劑溶解溶 質已到達最大量,則稱之為達溶解平衡。是一種動態平衡,而此時的溶液是一飽和 溶液。如圖1 10 所示。 圖1 10 溶解平衡的示意圖 九.飽和溶液: 1.定義:定溫、定壓下,當溶質溶於定量溶劑中的量達到最大值時,此溶液即是。 2.性質:當溶液已是飽和溶液後,即使加入更多的溶質,溶液中溶質的溶解量仍不會 有所改變;但溶解與沉澱的過程仍在進行,且處於一種動平衡的狀態。 十.過飽和溶液: 1.定義:當溶質濃度大於飽和溶液的溶液,即是。 2.配製:可先於較高溫度時,配置一飽和溶液,並除去其中之所有雜質後,再緩緩降 溫,即可得過飽和溶液。但於降溫的過程中,不可有搖晃、攪拌或其他固體進入。 3.應用: (1)熱敷包:塑膠袋內裝有過飽和醋酸鈉水溶液,使用時按壓塑膠袋內的圓盤,讓圓 盤粗糙凹痕露出,促進結晶核心的生成,使醋酸鈉結晶析出並放出熱量。 (2)人造雨:若天空中有過飽和水蒸氣存在,可以在天空散布碘化銀(AgI)與乾冰, 前者與冰晶的形狀相似,可以作為晶種,促進水蒸氣凝結成水,後者降低溫度 (乾冰昇華會吸熱),使過飽和水蒸氣凝結成水而降雨。 十一.未飽和溶液: 1.定義:當溶質濃度小於飽和溶液的溶液,即是。 2.如何使未飽和溶液變成飽和溶液。 (1)定溫下,加入溶質或蒸發溶劑。 (2)降溫或升溫,要視溶解度與溫度的關係來決定。
十二.溶解度(S): 1.定義:定溫、定壓、定量溶劑下,所能溶解的最大溶質量。 2.單位: (1)溶解最大溶質克數100克溶劑。 (2)溶解最大溶質莫耳數1公升溶液 M 。 (3)每公升溶液中所含有的溶質克數( Lg )。 (4)每公斤溶劑中所含有溶質的莫耳數(molkg)。 3.分類: (1)可溶:當溶液濃度大於101M 。 (2)微溶:當溶液濃度介於101 ~104M 之間。 (3)不可溶(難溶):當溶液濃度小於104M 。 4.溶解度曲線:如圖1 11 所示。 十三.影響溶解度的因素: 1.溶質與溶劑的本性: 圖1 11 溶解度曲線 (1)同類互溶:如,酒精易溶於水,但四氯化碳不易溶於水;碘不易溶於水,但易 溶於酒精。 (2)離子水合:水合能愈大,則愈容易溶於水。 (3)氫鍵:具有氫鍵的化合物,比較容易溶於水。 2.溫度: (1)當物質溶於水,為吸熱反應時;則溫度愈高,該物質的溶解度會愈大。如,絕大 部分的固體(例外的有氫氧化鈉(NaOH)、硫酸鈣(CaSO4)、硫酸鈰(Ce2(SO4)3) )與液體均是如此。同時,若吸熱愈多,則溫度溶解度的影響會愈大,如,硝酸 鉀(KNO3);若吸熱愈少,則溫度溶解度的影響會愈小,如,氯化鈉(NaCl)。 (2)當物質溶於水,為放熱反應時;則溫度愈高,該物質的溶解度會愈小。如,全部 的氣體與少數的固體氫氧化鈉(NaOH)、硫酸鈣(CaSO4)、硫酸鈰(Ce2(SO4)3) 均是如此。其原因是,當溫度增加時,氣體分子擁有較高的動能,使氣體分子更 易脫離液面,故溶解度會變小。 (3)常見固體、氣體溶解度與溫度的關係圖。如圖1 12 、圖1 13 所示。
圖1 12 溫度對固體溶解度 圖1 13 溫度與氣體溶解度 3.壓力: (1)對於固體與液體而言,壓力幾乎不會影響其溶解度。 (2)對於氣體而言,其影響就很大;可利用亨利定律來解釋。 十四.亨利定律: 1.內容:於定溫下,定量溶劑所溶解某氣體之重量與氣體液面上的分壓成正比。但溶 解之氣體體積則與氣體壓力無關。 2.數學式:W kP或S kP,其中, W :代表定量溶劑中所溶解的氣體重量。 k :代表比例常數;亦可稱之為亨利常數。 P :氣體的壓力。 S :氣體在定量溶劑中的溶解度(M)。 3.限制:亨利定律只適用於稀薄溶液及高溫低壓時。並不適用於極易溶於水或可與水 反應的氣體;如,氨氣(NH3)、氯化氫(HCl)、二氧化硫(SO2)、硫化氫(H2S)、二 氧化碳(CO2)、氯氣(Cl2)、二氧化氮(NO2)等等。 33.已知硝酸鉀(KNO3 101)於15oC時的溶解度為26g 100gH2O,今將28 克的氫氧 化鉀(KOH 56)溶於100 克水中,再與重量百分率60%硝酸(HNO3 63)水溶液 52.5 克混合,而溫度不變,則可析出若干克固體? 34.對於定溫下的飽和溶液而言,下列各項敘述中,錯誤的有 (A)溶液中所能溶解的溶 質已達最大量 (B)溶質與溶液共存,而且溶解速率與結晶速率相等 (C)溶液的濃度為 一定值 (D)於溶液中再加入溶質時,溶質可溶解而得過飽和溶液。
35.下列各方法中,可用來區分未飽和溶液、飽和溶液、過飽和溶液? (A)加入晶種 (B)以 顏色辨識 (C)再加入溶劑 (D)加熱。 36.於某溫度時,化合物甲的飽和溶液
x
克中有溶質a
克,而化合物乙的飽和溶液x
克 中則有溶質b克,則於此溫度下,甲、乙兩化合物的溶解度比值是多少? 37.定溫下,將x
克的某物質完全溶於定量的水中,得到VmL、密度為 3 cm g d 的飽和 溶液,則該溶液的重量百分率是多少? 38.下列關於溶解度的敘述中,正確的有 (A)液體溶於液體的溶解度,大都是因本性而 異 (B)氣體溶解度隨溫度升高而增大 (C)固體溶解度隨溫度升高而增大 (D)氣體溶解 度與其平衡時的氣體壓力成反比。 39.當固體溶解於液體中,會影響溶解度的因素是 (A)溫度 (B)攪拌 (C)接觸面積 (D)壓力。 40.已知硝酸鉀(KNO3 101)之溶解度(g 100gH2O),於20oC 是32、80oC是169, 則 (1)20oC 時,硝酸鉀飽和溶液的重量百分濃度是多少%? (2)80oC時,硝酸鉀飽和溶液的重量莫耳濃度是多少m
?(3)80oC時,200g飽和溶液的溫度降至20oC 時,可析出多少克的硝酸鉀? (4)在20oC 時,某硝酸鉀飽和溶液升至80oC時,需加入27.4 克的硝酸鉀,則原來 飽和溶液的重量是多少公克? 41.在20oC 時甲物質在水中的溶解度為 g gH O 2 100 20 ,則 (1)此溶液在20oC 時的重量百分率濃度是多少? (2)今有甲物質的飽和溶液 240 克,加熱至60oC時,若蒸發掉5.0 克的水,並再加入 60 克的甲物質恰可再達飽和。則60oC時甲物質的溶解度是多少g gH O 2 100 ?而 重量百分率又是多少? 42.已知某溫度下,於 100 克的水中加入
a
公克的CuSO4或加入b公克的CuSO4‧ 2 5H O均可使溶液恰好變成飽和溶液,試寫出a
與b的關係式。 43.對定量液體而言,氣體壓力為Patm,溶解度為x
公克,溶解的氣體體積為VmL, 當壓力變成nPatm時,其溶解度變成多少公克?體積變成多少mL? 44.已知,aoC 時,硝酸鉀( 101) 3 KNO 的溶解度為4.0m,取此溫度下的硝酸鉀飽和 溶液560g冷卻至boC時,結果有硝酸鉀80.8g析出。則 (1)aoC時,硝酸鉀的溶解度是多少? (2)boC時,飽和的硝酸鉀溶液濃度是多少? 45.下列各種氣體中,不遵守亨利定律的有 (A)NH3 (B)HCl (C)CO2 (D)SO2 (E)Cl2。 46.下列各項因素中,與氣體在水中溶解度較沒有關係的是 (A)水溫 (B)氣體壓力 (C)氣 體體積 (D)氣體種類。 47.於20oC時,某物質的不 飽和溶液濃度為 20%,若加入8.4g的溶質或蒸發 掉 g 2 . 26 的水,均可使其變成飽和溶液,則該物質於20oC 時的溶解度是多少? 48.
x
、 y 、z
三種不含結晶水的鹽類;20oC 時,x
鹽的飽和溶液濃度為20%; g 0 . 10 的 y 鹽飽和溶液蒸乾後可得1.0g的 y ;50.0g的水最多可溶解20.0g的z
,則x
、 y 、z
的溶解度大小順序是如何? 49.已知,KNO3的溶解度如下: gH O g C o 2 100 150 75 ; oC g gH O 2 100 40 25 。今 將100.0g、75oC的飽和硝酸鉀水溶液冷卻至25oC ,則有多少克的硝酸鉀析出? 50.右圖為BaCl2在純水中的溶解度曲線,則(Ba137、Cl 35.5、O16) (1)圖中 B 點的重量百分率是多少? (2)下列各項敘述中,錯誤的是 (A) A 表示過飽和溶液, 若由60oC上升至70oC則變成飽和溶液 (B)C 點表示 未飽和溶液,若由55oC下降至50oC則變成飽和溶液 (C)圖中 B 點移到 D 點,則有固體的析出 (D)BaCl2在純水中的溶解過程為放熱反應。 (3)在50oC 時,將24.0g的 ) ( 2 s BaCl 溶入60.0g的水中, 則需將溫度升到多少度才可變成飽和而完全溶解? 51.下列何者與氣體在水中的溶解度較無關係? (A)水的溫度 (B)氣體的壓力 (C)氣體的 種類 (D)氣體的體積。(89 日大) <Homework 1-4>
1.欲將KNO3與CuSO4的固體混合物分離,下列各種特性中,最恰當的是 (A)沸點 (B)
熔點 (C)顏色 (D)溶解度。(D) 2.將搖過的罐裝汽水,打開瓶蓋後會有大量汽水噴出,此結果與下列何種定律關係最為 密切? (A)拉午耳定律 (B)亨利定律 (C)道耳吞分壓定律 (D)查理定律。(B) 3.某生欲配製食鹽水溶液,將200g的食鹽加到500g的水中,於20oC 時發現水中仍 又未溶解的固體,則此溶液為 (A)未飽和溶液 (B)飽和溶液 (C)過飽和溶液 (D)理想溶 液。(B) 4.於50oC 時,某物質的溶解度為 O gH g 2 100 150 ,則今有一 mL 50 的該飽和溶液,則 重量百分率是多少?(60%) 5.下列那一條件可增加氣體對水的溶解度 (A)高溫高壓 (B)高溫低壓 (C)低溫高壓 (D)低 溫低壓。(B) 6.現有硝酸鉀飽和溶液
a
克;於溫度不變時,下列各種措施中,能使溶液的重量百分 率濃度改變的是 (A)加入硝酸鉀10g (B)加入10g 的水 (C)蒸去10g的水 (D)取出 g 10 溶液。(B)7.下列各種物質對水的溶解度是隨溫度上升而減少的有 (A)CaSO4(B)MnSO4 (C)
Cl
8.若在toC 、Patm下,100g的水可溶解某氣體W 克、體積VmL;若在toC 、nPatm 下,100g的水可溶解某氣體aW 克、、體積bVmL,則
a
?、b ?(a n、b 1) 9.下列各項措施中,可加速固體的溶解速率,但無法增加溶解度的是 (A)攪拌 (B)研磨 使顆粒變小 (C)加熱 (D)加水 (E)液面加大壓力。(AB) 10.將60oC時,定量硝酸鉀飽和溶液的溫度降至20oC 時,沒有發生變化的是 (A)溶液 的質量(B)溶液中溶質的質量 (C)溶質的溶解度 (D)溶液中溶劑的質量。(D) 11.求下列各飽和溶液中溶質的溶解度(g100g水) (1)某溫度時,50.0g的水最多溶解18.0g的氯化鈉。(36 100 ) 2O gH gNaCl (2)某溫度時,100.0g、20%的硝酸鉀溶液中再加入45.0g的硝酸鉀時,恰達飽和。 ) 100 25 . 81 ( 2 3 O gH gKNO (3)某溫度時,硝酸鉀飽和溶液的濃度為25%。(33.3 100 ) 2 3 O gH gKNO (4)某溫度時,硝酸鉀飽和溶液的濃度為4m。(40.4 100 ) 2 3 O gH gKNO 12.已知,硝酸鉀在100oC的溶解度為 O gH g 2 100 246 ,則在 C o 100 時,100g、 % 10 的硝酸鉀溶液中,必需蒸發若干克的水才能成為飽和溶液?(85.9g) 13.某溫度下,於 100 的克水中加入x
公克的CuSO4或加入 y 公克的CuSO4‧5H O2 可 使溶液恰好達到飽和,則x
與 y 的關係式為何? ) 9 2500 1600 ( y y x 14.已知,硝酸鉀在20oC 時的溶解度為 O gH g 2 100 32 ,今在100.0g、 % 10 的硝酸鉀 溶液中需要再加若干克的硝酸鉀才可達飽和?(18.8g) 15.下列哪一種改變,可使密閉容器中,氮氣對水的溶解度增加? (A)定容時,加入定 量的氧氣 (B)增加水量 (C)縮小容器的體積 (D)定壓下,加入定量的氧氣。(C) 16.將搖過的鋁罐裝可樂,打開瓶蓋會有大量氣體伴隨可樂噴出,此實驗結果與哪一個 定律最密切? (A)拉午耳定律:溶液蒸氣壓 (B)亨利定律:氣體溶解度與壓力 (C)溫 度升高氣體溶解度變小 (D)道耳吞分壓定律。(B) 17.將2mol的尿素溶於水配成400mL的水溶液,求此溶液的容積莫耳濃度。( M5 ) 18.將63.0g的草酸晶體(H C O2 2 4‧2H O2 )溶於水中,配成500mL的水溶液,求此溶 液的容積莫耳濃度。( M1 )19. 將1.50g 的 NaOH 加 入100mL、0.625M 的 NaOH(aq)中 , 再 加 水 至 總 體 積 為
mL 200 ,則此混合水溶液的體積莫耳濃度是多少?(0.5M) 20.將濃度4.0M 的食鹽水溶液,倒去一半體積後再加水至滿,攪拌均勻後再倒去 4 3 後 又用水加滿,則此最後溶液的濃度是多少?(0.5M)