國立交通大學
生物科技研究所
碩士論文
癌症標靶材料作用於細胞與分子機制之探討:
1.多光子趨動標靶化奈米鑽石誘發癌細胞死亡之機制
2.anti-CEACAM6 與 anti-HER-2 單一抗原結合功能區抗體於乳
癌標靶治療之研究
Cell and molecular mechanism study of cancer targeting materials :
1. The mechanism of cancer cell death for multi-photon triggered
target-based nanodiamonds;
2. Application of single domain antibodies (anti-HER-2 and
anti-CEACAM6) in breast cancer targeting therapy.
研究生:陳虹瑋
指導教授:張家靖
中華民國一百年七月
癌症標靶材料作用於細胞與分子機制之探討:
1.多光子趨動標靶化奈米鑽石誘發癌細胞死亡之機制;
2.anti-CEACAM6 與 anti-HER-2 單一抗原結合功能區抗體於乳癌標靶治
療之研究
Cell and molecular mechanism study of cancer targeting materials :
1. The mechanism of cancer cell death for multi-photon triggered
target-based nanodiamonds;
2. Application of single domain antibodies (anti-HER-2 and
anti-CEACAM6) in breast cancer targeting therapy.
研 究 生:陳虹瑋 Student:Hung-Wei Chen
指導教授:張家靖 Advisor:Chia-Ching Chang
國 立 交 通 大 學
生 物 科 技 學 系
碩 士 論 文
A ThesisSubmitted to Department of Biological Science and Technology National Chiao Tung University
in partial Fulfillment of the Requirements for the Degree of
Master in
Biological Science and Technology July 2011
Hsinchu, Taiwan, Republic of China
I 癌症標靶材料作用於細胞與分子機制之探討: 1.多光子趨動標靶化奈米鑽石誘發癌細胞死亡之機制; 2.anti-CEACAM6 與 anti-HER-2 單一抗原結合功能區抗體於乳癌標靶治 療之研究 學生:陳虹瑋 指導教授:張家靖 教授 國立交通大學生物科技研究所 碩士班
摘要
癌症的標靶治療可標定癌細胞,減少對正常細胞的傷害,故比傳統治療更有 效。本研究結合奈米技術以及生物技術,發展出對癌細胞具有靶向性的奈米粒子。 在癌症細胞當中,通常會存在一些特殊表現或調控之因子,這些調控因子即 為標靶治療的理想目標。本研究中以肺癌與乳癌作為模式,針對肺癌大量表現之 生長激素受體、乳癌特殊表達之癌胚抗原相關細胞黏著分子6 (Carcinoembryonic antigen-related cell adhesion molecule 6, CEACAM6)與人類表皮生長因子受體 2 (Human epidermal growth factor receptor 2, HER-2),分別設計出標靶化之奈米粒子 與單一抗原結合功能區抗體作為標靶治療之工具。 許多癌症細胞會內生性分泌生長因子,利用生長激素在腫瘤細胞的特殊表 現,使羧酸化奈米鑽石與重組的生長激素受體結合蛋白以及綠色螢光蛋白接合成 一複合體,此複合體能夠專一性的結合於具有高度表現生長激素受體的A549 人 類非小細胞肺腺癌細胞株的細胞膜上。細胞毒性測試結果指出,羧酸化奈米鑽石 -生長激素受體結合蛋白-綠螢光蛋白複合體具有低生物毒性,高度生物相容之特 性。當細胞羧酸化奈米鑽石-生長激素受體結合蛋白-綠螢光蛋白複合體接合於 A549 肺腺癌細胞表面,同時經由脈衝雷射的誘導使得奈米鑽石爆炸並造成細胞 表面受損,並經由細胞凋亡機制導致細胞死亡。因此,此實驗之設計猶如一奈米 手術,或許能夠建立為一種新的癌症治療策略,亦或為生物醫學所應用。 另一方面,癌胚抗原相關細胞黏著分子 6 與人類表皮生長因子受體 2 皆高度 表現於乳癌細胞當中,且與乳癌之進程相關。藉由免疫駱馬後,分離、純化出單 一抗原結合功能區抗體,並以抗體保守區(conserve region, Fc)接合不同的單一抗 原結合功能區抗體,測試其對乳癌細胞株MCF-7 之影響。同時,我們也以歐洲 紫杉醇作為對照組與單一抗原結合功能區抗體之治療效果作比較。由實驗結果顯 示,針對乳癌之進程,單一抗原結合功能區抗體可以經由誘導乳癌細胞凋亡進而 抑制腫瘤細胞之增生,並且藉由減低基質金屬蛋白酶2 (MMP-2)、基質金屬蛋白 酶9 (MMP-9)之活性,以及抑制單核球趨化蛋白 1 (MCP-1)、細胞內黏附因子 1 (ICAM1)、血管細胞黏附因子 1(VCAM-1)等等,以減少巨噬細胞浸潤乳癌細胞之II 能力、降低乳癌細胞遷移、侵犯、轉移,以及阻礙癌症血管新生、使腫瘤體不再 增大。相較於歐洲紫杉醇之療效,單一抗原結合功能區抗體更為一具有臨床潛力 之抗體藥物。 總而言之,癌症的標靶化治療對周圍細胞不具傷害性,且可針對不同癌症細 胞所表現特定分子,設計擁有較佳治療效果的分子或方法。於本實驗中,以針對 生長激素受體所設計的奈米鑽石複合物,經由奈秒雷射誘發導致癌細胞凋亡,為 高專一性的光敏療法平台開發。而針對CEACAM6 與 HER-2 的單一抗原結合功 能區抗體,更具全面性阻止癌症進程的療效,故此研究之奈米鑽石複合物與單一 抗原結合功能區抗體分別為非小細胞肺腺癌與乳癌標靶治療之理想因子。
III
Cell and molecular mechanism study of cancer targeting materials: 1. The mechanism of cancer cell death for multi-photon triggered
target-based nanodiamonds;
2. Application of single domain antibodies (anti-HER-2 and anti-CEACAM6) in breast cancer targeting therapy.
Student:Hung-Wei Chen Advisor:Dr. Chia-Ching Chang Department of Biological Science and Technology
National Chiao Tung University
Abstract
Targeted cancer therapy is more effective than conventional treatments and less harmful to normal cells. In this study, we have combined nanotechnology and biotechnology to develop a novel cancer cell targeting therapy.
Growth factor are autocines, will be overexpressed in varies tumors. We expressed recombinant green fluorescence protein (GFP) and growth hormone receptor binding protein (GHRBP) which could specify recognize growth hormone receptor (GHR) which is located on cell surface of the non-small cell lung cancer cells line, A549. By conjugated with carboxylated nanodiamond (cND) and expressed protein, the cND-GHRBP-GFP complex shows a low toxicity, high biocompatible, specificity, and observable properties. Following recognizing by cND-GHRBP-GFP, A549 were triggered by pulse laser. Results indicate that laser pulsed
cND-GHRBP-GFP nano-blast recognized A549 will induces cell surface damage and resulting cell death by apoptosis pathway. According, we have developed a novel strategy for non-small cell lung cancer targeting therapy by combining nanodiamond conjugated hormone receptor binding protein and laser pulse.
Carcinoembryonic antigen-related cell adhesion molecule 6 (CEACAM6) and human epithelial growth factor receptor 2 (HER2) are overexpression in breast cancer cell, but not in normal cells. They are associated with the progression of breast cancer. Therefore, they could be use as cancer markers of antibodies targeting therapy.
Anti-CEACAM6 and anti-HER-2 single domain antibodies (sdAb) were cloned from heavy chain only IgG of an immunized llama immune library and fused with Fc fragment. A breast cancer cell line, MCF-7, was used to test the therapy efficiency, and conventional chemotherapy drug, docetaxel, was used as a control of the experiment. Our data indicated that anti-CEACAM6 and anti-HER-2 sdAb could
IV
reduce breast cancer cell proliferation and induced tumor cell apoptosis. Western blotting indicated anti-CEACAM6 and anti-HER-2 could induced caspase-9 activation, and PARP cleavage; reduced MCF-7 secreted MMP-2, MMP-9 activity; inhibited MCP-1, ICAM-1, and VCAM-1 expression. In other words,
anti-CEACAM6 and anti-HER-2 sdAb could inhibit breast cancer progression by reduce breast cancer cell migration, invasion, monocytes infiltration, and angiogenesis. Therefore, anti-CEACAM6 and anti-HER-2 sdAb are ideal candidates for the breast cancer with CEACAM-6 and HER-2 overexpression.
Conclusion, Growth hormone receptor, CEACAM6, and Her-2 are idea target markers for non-small cell lung cancer and breast cancer targeting therapy.
V
誌謝
新竹,一開始是個沒有味道的城市,但在南大路與西大路口的第一張沒有待 轉格卻未待轉來著的紅單,以及機車被拖吊到大停車場……種種可說是埋下了 〝瘋城〞與我的〝孽〞緣。 心中的小叛逆引領我進入到與原先領域相差甚遠的生物物理實驗室,還好有 靖淳學姐、瑤貞學姐、芳馨學姐以及子正學長給我上了實驗室〝入門〞課程,暑 假常麻煩子歡與明勳當我的地圖,曾博的〝吼~我真的要準備一支電極棒了哦!〞 也滿有效果的,更要大大感謝我的指導教授 張家靖博士,對於我這個物理不太 行的學生多加包容,並耐心的指導,以及給予我至 Anaheim 參與國際會議的機 會,是我人生中滿精彩的一段學習與回憶。 雖然後半年被寫論文這件事搞得有點精神不正常,哈!不過實驗室的大家真 是大好人,每天跟我一起胡言亂語,到底是誰在寫論文啊?哈!。初進實驗室時 〝這個實驗室好怪…鄭博跟學亮學長好恐怖,像流氓…〞,不過感謝爸爸要他當 斯文人的 鄭財木博士,在物理實驗室裡您與學亮真是讓我備感親切,教了我非 常多的技術與知識,超感謝您~我一定不會跟別人講你取嫩妻的!還有阿娟不喜歡 底迪,快放她去交男朋友啦!學亮不要再一天到晚說自己實驗亂做,根本在聲東 擊西吼!哪天發了 PNAS 記得提拔我,謝謝!還要祝你們家的琪琪美女、嘟嘟、彎 彎與未來更多小學亮平安快樂,健康順心!每天照顧我們一群小毛頭的憲儀姐~ 常開車帶我們趴趴走,我不會忘記妳跟妳家超可愛胖迪、悅悅與小藍馬 5 的!畢 業後 MSN 和 FB 沒事也會開著跟您繼續網拍!啊~李醫師,我們只是討論而已,沒 有要買哦~哈!謝謝星原學長讓我當了幾天的台大醫院新竹分院研究助理。謝謝輔 宣學長這個物理老人,常講一堆我聽不懂的@#$%^&*,但您真的很有耐心耶!不過 說實在,女朋友勒!!您該更新一下追美湄的招數了吧…。 常常一天跟我在一起最多時間的娟姐,我必須說,美國行有妳真好,雖然蠢 到爆~哈哈哈!畢業了八卦還是要常常 update 嘿!偉賢同學,謝謝你在電腦啦~軟 體啦~等等的幫助,真的!賺錢固然重要,身體也要顧哦~哈!昌翰同學,自彈自唱 的天天想妳都過這麼久了,祝你跟你的雙魚女孩可以開花結果,改天帶來一起聚 餐囉!小象邦邦,你搞笑歸搞笑,不要再迷路了~你要自立自強啊!至少 google map 看一看要認真記阿…。還要感謝趙老師與趙老師實驗室的光凱學長、惠芳學姐實 驗上的指導,趙家同學、學弟妹的照顧,讓我的細胞實驗能順利進行。感謝同步 輻射中心 胡宇光博士願意出借共軛焦顯微鏡。 最後,謝謝鼓勵我到交大唸書的爸媽,有你們讓我求學過程一路順利,不需 擔心生活上的問題,並且給予我精神上的支持。也謝謝健銘、波克、一百、大大…… 等大學好友,一起努力度過這兩年。大學的指導教授 黃建富博士,即使我們畢 業、離開實驗室,但對我們的關心與照顧絲毫未減,謝謝您!還有丹瑜,不管妳 未來的規畫如何,我永遠支持。於此,感謝更多關心我的人。Ya~我畢業囉:)VI
目錄
中文摘要... I Abstract ... III 誌謝... V 目錄... VI 表目錄... XI 圖目錄... XII 縮寫表... XIV 序論... 1 1 癌症發生與特性... 1 2 癌症的治療... 1 3 細胞死亡與其分子機制... 2 4 實驗動機... 6 壹、 多光子趨動標靶化奈米鑽石誘發癌細胞死亡之機制... 7 壹、第一章 研究背景... 8 壹-1-1 肺癌 ... 8 壹-1-2 奈米材料於生物醫學之應用 ... 8 壹-1-3 多光子效應 (multiphoton effect) ... 10 壹、第二章 研究動機與策略... 11 壹-2-1 研究動機 ... 11 壹、第三章 實驗策略原理... 13 壹-3-1 蛋白質的表現與純化 ... 13 壹-3-2 EDC、sulfo-NHS 的蛋白質接合 ... 13壹-3-3 原子力顯微鏡 (Atomic force microscopy, AFM) ... 14
壹-3-4 動態光散射儀 (Dynamic light scattering, DLS) ... 14
壹-3-5 螢光儀 (Fluorescence spectrometer) ... 14
壹-3-6 奈秒脈衝雷射 (Nano-second pulse laser) ... 15
壹-3-7 拉曼光譜 (Raman spectum) ... 15
壹-3-8 蛋白質定量法 ... 16
壹-3-8-1 Bradford dye-binding method ... 16
壹-3-8-2 紫外光吸收法 (UV absorption) ... 16
壹-3-9 十二烷基硫酸鈉聚丙烯醯胺凝膠電泳 (SDS-PAGE) ... 16
壹-3-10 西方墨點法 (Western blot) ... 17
壹-3-11 錐蟲藍排除法 (Trypan blue exclusion) ... 17
壹-3-12 MTT ... 17
VII
壹-3-14 共軛焦顯微鏡 (Confocal microscopy) ... 19
壹-3-15 免疫細胞染色 (Immonocytochemistry) ... 20
壹-3-16 酵素連結免疫吸附法 (Enzyme-linked immunosorbent assay,ELISA) ... 20 壹、第四章 實驗材料與方法... 21 壹-4-1 實驗材料 ... 21 壹-4-1-1 細胞株來源... 21 壹-4-2 實驗方法與步驟 ... 21 壹-4-2-1 蛋白質之表現與純化... 21 壹-4-2-2 5 nm 羧酸化奈米鑽石之螢光 3D 全光譜分析... 22 壹-4-2-3 羧酸化奈米鑽石表面接合生物分子... 22 壹-4-2-4 以動態光散射儀分析 cND-GHRBP-GFP 複合體之平均粒徑大小 ... 23 壹-4-2-5 以原子力顯微鏡分析 cND-GHRBP-GFP 複合體之外型與均勻程 度... 23 壹-4-2-6 GHRBP 之抗體製備 ... 23 壹-4-2-7 細胞培養... 24 壹-4-2-8 利用倒立式螢光顯微鏡觀察 cND-GHRBP-GFP 複合體表現之螢 光與奈米鑽石之位置... 25 壹-4-2-9 觀察 cND-GHRBP-GFP 複合體於細胞內之位置 ... 26 壹-4-2-10 以錐蟲藍細胞染色觀察細胞死亡情形... 26 壹-4-2-11 利用細胞化學免液染色觀察細胞凋亡與細胞壞死相關蛋白 . 26 壹、第五章 實驗結果... 28 壹-5-1 重組生長激素受體結合蛋白質表現與純化 ... 28 壹-5-2 5 nm 羧酸化奈米鑽石 3D 螢光光譜 ... 30 壹-5-3 5 nm cND、GHRBP 以及 pET30a-Eam-GFP 之細胞毒性測試 ... 31 壹-5-4 cND-GHRBP-GFP 複合體粒徑大小、構形分析,以及細胞毒性測試 ... 33 壹-5-5 GHRBP 抗體的取得與效價分析... 37 壹-5-6 羧酸化奈米鑽石-生長激素-綠螢光蛋白複合體表現於 A549 細胞膜 39 壹-5-7 分別選定 5 mJ 與 30 mJ 作為 266 nm 以及 532 nm 奈秒脈衝雷射於癌 細胞與cND-GHRBP-GFP 之作用功率 ... 40 壹-5-8 A549 肺腺癌細胞分別經由 266 nm 以及 532 nm 雷射激發後之細胞型 態觀察與存活率分析... 43 壹-5-9 cND-GHRBP-GFP 複合體經由雷射激發後對於大量表現生長激素受 體之A549 肺腺癌細胞選擇性抑制細胞增殖能力 ... 46 壹-5-10 分別以 266 nm 與 532 nm 雷射激發後觀察 A549 細胞中細胞發炎因 子COX-2 之表現 ... 48
VIII 壹-5-11 以 266 nm 與 532 nm 雷射激發後觀察 A549 細胞中 caspase-3 之表現 ... 52 壹-5-12 以 266 nm、532 nm 雷射激發後觀察 A549 細胞中細胞凋亡誘導因子 AIF 之表現 ... 56 壹-5-13 大量表現生長激素受體之細胞株 ... 60 壹、第六章 討論... 61 壹-6-1 cND-GHRBP-GFP 複合體之定量與特性分析 ... 61 壹-2 多光子效應對奈米鑽石與細胞之影響 ... 62 壹-6-3 cND-GHRBP-GFP 複合體經由雷射激發後,造成癌細胞損壞與死亡之 可能路徑... 63 壹-6-4 接合癌症標靶因子之奈米鑽石日後可能之應用 ... 64 貳、 anti-CEACAM6 與 anti-HER-2 單一抗原結合功能區抗體於乳癌標靶治 療之研究... 65 貳、第一章 研究背景... 66 貳-1-1 乳癌背景 ... 66 貳-1-2 乳癌之進程 ... 66 貳-1-2-1 細胞不正常增生... 66 貳-1-2-2 巨噬細胞浸潤癌症細胞... 66 貳-1-2-3 癌細胞侵犯組織... 67 貳-1-2-4 血管新生... 67 貳-1-2-5 癌細胞轉移... 68 貳-1-3 目前乳癌之治療 ... 68 貳-1-4 人類上皮生長因子受體 2 ... 69 貳-1-5 癌胚抗原相關黏著分子 6 ... 69
貳-1-6 簡介單一抗原結合功能區抗體(single-domain antibody, sdAb) ... 70
貳-1-7 單一抗原結合功能區抗體應用於 CEACAM6 表現相關之癌症治療現 況... 71 貳、第二章 研究動機與策略... 72 貳-2-2 研究動機 ... 72 貳-2-2 研究策略 ... 73 貳-2-2 研究策略貳、第三章 實驗原理 ... 73 貳、第三章 實驗原理... 74 貳-3-1 蛋白質的表現與純化 ... 74 貳-3-2 明膠蛋白酵素電泳法 (Gelatin zymography) ... 74 貳-3-3 十二烷基硫酸鈉聚丙烯醯胺凝膠電泳 (SDS-PAGE) ... 75 貳-3-4 西方墨點法 (western blot)... 75
貳-3-5 錐蟲藍排除法 (trypan blue exclusion) ... 75
IX
貳-3-7 Calcein AM 染色法 ... 75
貳-3-8 免疫細胞化學染色 (immunocytochemistry) ... 76
貳-3-9 螢光顯微鏡 (fluorescence microscopy) ... 76
貳-3-10 Annexin V/PI assay ... 76
貳-3-11 流式細胞儀 (flow cytometer) ... 77 貳、第四章 實驗材料與方法... 79 貳-4-1 實驗材料 ... 79 貳-4-1-1 細胞株來源... 79 貳-4-2 實驗方法 ... 79 貳-4-2-1 蛋白質之表現與純化... 79 貳-4-2-2 細胞培養... 80 貳-4-2-3 細胞活性分析... 80 貳-4-2-4 藉由免疫細胞化學染色偵測 CEACAM6 與 HER-2 於細胞內之 表現... 80 貳-4-2-5 基質金屬蛋白酶活性分析... 81 貳-4-2-6 單核細胞趨化蛋白表現分析... 81 貳-4-2-7 細胞浸潤能力分析... 82 貳-4-2-8 細胞基質侵蝕力分析... 83 貳-4-2-9 血管新生能力測試... 84 貳-4-2-10 利用西方墨點法偵測細胞訊息傳遞及凋亡蛋白之表現... 85 貳-4-2-11 利用 Annexin V/PI 雙染色並以流式細胞儀進行細胞凋亡分析 ... 86 貳、第五章 實驗結果... 87 貳-5-1 sdAb 與 HCAb 抗體表現與純化 ... 87 貳-5-2 HER-2 與 CEACAM6 蛋白質表現於 MCF-7 與 THP-1 細胞中 ... 88 貳-5-3anti-HER-2 抗體與 anti-CEACAM6 抗體抑制 MCF-7 細胞的增生及基 質金屬蛋白酶的活性... 91 貳-5-4 單一抗原結合功能區抗體誘導乳癌細胞 MCF-7 死亡之分析 ... 92 貳-5-6 anti-CEACAM6 抗體依濃度依賴性抑制單核球細胞趨化蛋白之表現 ... 97
貳-5-7 anti- CEACAM6 抗體與 anti-HER-2 抗體降低細胞黏附因子 ICAM-1 以及VCAM-1 之表現 ... 98
貳-5-8 anti- CEACAM6 抗體與 anti-HER-2 抗體抑制免疫球細胞 THP-1 對 乳癌細胞MCF-7 的浸潤作用 ... 99
貳-5-9 anti- CEACAM6 抗體與 anti-HER-2 抗體抑制 MCF-7 的侵犯作用 ... 101
貳-5-10 anti- CEACAM6 抗體與 anti-HER-2 抗體降低 MCF-7 所誘發的 HUVECs 血管新生作用 ... 103
X 貳-5-11 單一抗原結合功能區抗體誘導細胞凋亡相關蛋白之表現 ... 105 貳、第六章 討論... 106 貳-6-1 單一抗原結合功能區抗體之優點 ... 106 貳-6-2 單一抗原結合功能區抗體透過細胞凋亡路徑抑制乳癌細胞之增生 ... 106 貳-6-3 單一抗原結合功能區抗體抑制乳癌細胞中基質金屬蛋白酶 MMP-2、 MMP-9 活性 ... 106 貳-6-4 單一抗原結合功能區抗體抑制 THP-1 細胞浸潤乳癌細胞之作用 .. 107 貳-6-5 單一抗原結合功能區抗體抑制 MCF-7 乳癌細胞之侵犯與轉移 ... 108 貳-6-6 單一抗原結合功能區抗體抑制乳癌之血管新生能力 ... 108 貳-6-7 anti-HER-2 單一抗原結合功能區抗體與 Herceptin 於乳癌治療之差異 ... 109 貳-6-8 單一抗原結合功能區抗體之應用 ... 109 結論... 111 參考資料... 112
XI
表目錄
表一、細胞凋亡與細胞壞死的型態學差異... 3
表二、蛋白質變性之緩衝溶液內含成分... 21
表三、蛋白質摺疊過程各步驟之摺疊緩衝溶液內含成分... 22
XII
圖目錄
圖 1、細胞死亡之分子機制... 6 圖 2、MTT 於細胞內之作用機制 ... 18 圖 3、螢光能階圖... 18 圖 4、倒立螢光顯微鏡光路圖... 19圖 5、利用 EDC 與 sulfo-NHS 接合 cND、rEaGH 及 GFP ... 23
圖 6、pET28a-GH 以 IPTG 誘導大量表現後之 SDS-PAGE ... 28
圖 7、pET30a-Eam-GFP 以 IPTG 誘導大量表現後之 SDS-PAGE ... 29
圖 8、pET30a-Eam-GFP 以 His-tag 管柱純化後之 SDS-PAGE ... 29
圖 9、以螢光儀觀察 5 nm 羧酸化奈米鑽石之 3D 螢光光譜圖... 30 圖 10、利用 MTT 分別分析 cND、GHRBP、pET30a-Eam-GFP 對 A549 細胞之細 胞毒性。... 32 圖 11、以原子力顯微鏡觀察 cND-GHRBP-GFP 複合體 ... 34 圖 12、以動態光散射儀量測 cND-GHRBP-GFP 複合體之平均粒徑大小 ... 35 圖 13、利用螢光儀觀察 cND-GHRBP-GFP 複合體之螢光光譜圖 ... 35 圖 14、以螢光顯微鏡觀察 cND-GHRBP-GFP 複合體 ... 36 圖 15、利用 MTT 分析 cND-GHRBP-GFP 於 A549 細胞中之細胞毒性 ... 36 圖 16、 mouse anti-rEAGH 抗體效價測試結果 ... 37
圖 17、以西方墨點法測試 mouse anti-rEAGH 抗體於不同之細胞株以及純 BSA 與rEaGH 蛋白質之專一性 ... 38 圖 18、cND-GHRBP-GFP 複合體於細胞內之共軛焦顯微鏡影像 ... 39 圖 19、經由 266 nm 雷射以 0.1 s/step 激發奈米鑽石之拉曼光譜圖 ... 41 圖 20、經由 532 nm 雷射以 10 s/step 激發奈米鑽石之拉曼光譜圖 ... 42 圖 21、A549 細胞經由處理 cND-GHRBP-GFP 複合體與雷射激發後之顯微明視 野影像... 44 圖 22、細胞處理 cND-GHRBP-GFP 與雷射激發後之活性分析 ... 45 圖 23、以西方墨點法分析肺癌細胞株 A549 與正常肺細胞株 HFL-1 內之生長激 素受體表現... 47 圖 24、以 cND-GFRBP-GFP 複合體處理細胞以及 532 nm 雷射誘導後細胞存活率 之分析... 47 圖 25、以 266 nm 與 532 nm 雷射激發及歐洲紫杉醇處理後,A549 細胞中細胞發 炎因子COX-2 之表現 ... 51 圖 26、266 nm 與 532 nm 雷射激發及歐洲紫杉醇處理後,A549 細胞中細胞凋亡 蛋白質caspase-3 之表現 ... 55 圖 27、以 266 nm 與 532 nm 雷射激發及歐洲紫杉醇處理後,A549 細胞中細胞凋 亡誘導因子AIF 之表現 ... 59
XIII 圖 28、不同癌症細胞株內之生長激素受體表現... 60 圖 29、原子力顯微鏡掃描示意圖... 62 圖 30、癌症進程示意圖... 68 圖 31、sdAb 與 HCAb 抗體之構築與結構示意圖 ... 71 圖 32、構築單一抗原結合功能區抗體之 DNA 片段於 pSJF2 載體中之策略簡圖 ... 74 圖 33、 Calcein AM 細胞染色法示意圖 ... 76 圖 34、Annexin V/PI 細胞雙染色法原理示意圖 ... 77 圖 35、流式細胞儀示意圖... 78 圖 36、單核球細胞浸潤乳癌能力分析實驗流程圖... 83 圖 37、乳癌細胞侵蝕細胞基質能力分析實驗流程圖... 84 圖 38、上皮細胞血管新生能力分析實驗流程圖... 85 圖 39、 2A3 與 2A3-Fc 抗體之表現 ... 87
圖 40、 觀察 MCF-7、THP-1 和 HUVEC 三種細胞株內之 HER-2 與 CEACAM6 表現... 90
圖 41、 細胞內 sdAb 2A3 與 HCAb 2A3-Fc 抑制細胞增生能力之分析... 91
圖 42、以 Annexin V/PI 分析經由 sdAb 與 HCAb 處理 72 小時後之乳癌細胞 MCF-7 ... 94
圖 43、 sdAb 2A3 與 HCAb 2A3-Fc 抑制細胞內之 MMP-2 與 MMP-9 之活性分析 ... 96 圖 44、HCAb 2A3-Fc 抑制細胞內 MCP-1 表現量之分析 ... 97 圖 45、sdAb 與 HCAb 處理 MCF-7 細胞後細胞分泌之細胞黏附因子表現量分析 ... 98 圖 46、分析經由 sdAb、HCAb 處理後,免疫球細胞 THP-1 對 MCF-7 之浸潤作 用... 100 圖 47、分析經由 sdAb、HCAb 處理後,乳癌細胞 MCF-7 之侵犯作用 ... 102 圖 48、分析經由 sdAb、HCAb 處理後,乳癌細胞 MCF-7 與周邊上皮細胞 HUVECs 之血管新生作用... 104 圖 49、sdAb 與 HCAb 處理 MCF-7 細胞後細胞內之細胞凋亡相關蛋白質表現量 分析... 105
XIV
縮寫表
Abbreviation All written
AFM AIF Amp II
atomic force microscopy apoptosis-inducing factor amphiphysin II Apaf-1 Arf ATR/Chk1 Bax Bcl-2 BCRC β-ME BSA caspase CBG250 CD66c CEA
apoptotic protease activating factor 1 ADP-ribosylation factor
ataxia telangiectasia and Rad3-related check point kinase-1 BCL2-associated X protein
B-cell lymphoma 2
Bioresource Collection and Research Center beta-Mercaptoethanol
bovine serum albumin cysteine aspirate protease coomassie boilliant blue G-250 cluster of differentiation 66c carcinoembryonic antigen CEACAM6 C. elegans CH1 CMV CNT
carcinoembryonic antigen-related cell adhesion molecule 6
Caenorhabditis elegans constant domain 1 cytomegalovirus carbon nanotube Cox-2 CSF-1 cyclooxygenase-2 colony-stimulating factor 1 Cyto C dATP DED DLS DMEM cytochrome c deoxyadenosine triphosphate death effector domain
dynamic light scattering
Dulbecco’s Modified Eagle Medium DMSO dimethyl sulfoxide
DTT DIABLO DISC ECGS
dithiothretol
direct IAP-binding protein with low pI death-inducing signaling complex endothelial cell growth supplement
XV E. coli EDC EDTA EGF EGFR ELISA ER ER ERK FADD FLICE FSC GEF100 GPI H2O2 HCAb HER-2 His-Tag HRP HUVECs IDC IPTG JNK MAPK MCP-1 MEFs MMPs Escherichia coli 1-ethyl-3-[3-dimethylaminopropyl]carbodiimide hydrochloride ethxlenediaminetetraactic acid
epidermal growth factor
epidermal growth factor receptor enzyme-linked immunosorbent assay endoplasmic reticulum
estrogen receptor
extracellular signal-regulated kinase Fas-associated death domain
procaspase-8/FADD-like interleukin 1-converting enzyme forword scatter
guanine nucleotide exchange factor 100 glycosylphosphatidylinositol
hydrogen peroxide heavy chain antibody
human epidermal growth factor receptor 2 histidine tag
horseradish peroxidase
human umbilical vein endothelial cells invasive ductal carcinoma
isopropyl β-D-1-thiogalactopyranoside c-jun N-terminal kinases
mitogen-activated protein kinase monocyte chemoattractant protein-1 murine embryonic fibroblasts matrix metalloproteases MTT NCHS Nd:Y3Al5O12 NF-κB NV center Orip PA PARP PBS pCMV PCS 3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyltetrazolium bromide National Center for Health Statistics
neodymium-doped yttrium aluminium garnet
nuclear factor kappa-light-chain-enhancer of activated B cells nitrogen-vacancy defect center
origin of replication polyadenylation
poly ADP-ribose polymerase phosphate buffered saline cytomegalovirus promoter photon correlation spectroscopy
XVI PDGF PDA PEI PI PR pro-A-SMase pro-pre-CAM PS PSPD PVDF RANTES RIP1 RNAi sdAb SDS-PAGE SH2 Sulfo-NHS TAM TEM TIMPs TNF-α TNFR TNF-R1 TNT TPL TRADD TRAF2 Smac SSC VEGF VH VHH WHO
platelet-derived growth factor pancreatic ductal adenocarcinoma polyethylenimine propidium iodide progesterone receptor pro-acid sphingomyelinase pro-pre-cathepsin D phosphatidylserine
position sensitive photo-diode polyvinylidene difluoride
regulated upon activation, normal T-cell expressed, and secreted ubiquinol-cytochrome c reductase, Rieske iron-sulfur polypeptide 1 RNA interference
single domain antibody
sodium dodecyl sulfate-polyacrylamide gel eletrophoresis gel srcoma homdogy 2, src homology 2
N-hydroxysulfosuccinimide sodium salt tumor-associated macrophage
transmission electron microscopy tissue inhibitor of metalloproteinases tumor necrosis factor α
tumor necrosis factor receptor
tumor necrosis factor receptor superfamily emeber 1a trinitrotoluene
adenovirus tripartite leader
tumor necrosis factor receptor – associated death domain TNF receptor –associated factor 2
second mitochondria derived activator of caspase side scatter
vascular endothelial growth factor variable domain
VH of heavy chain
1
序論
1 癌症發生與特性 根據衛生署公佈資料,民國九十九年的十大死因,癌症仍然高居第一位,並且已經 連續二十九年佔踞十大死因首位,根據統計,大約每十二分四十八秒就有ㄧ人死於癌症 [1]。導致癌症的原因有很多,其中包括了環境汙染[2]、吸煙[3]、病毒感染[2]、遺傳[4] 與賀爾蒙[5-7]等多種原因,但在所有的癌症細胞中都有ㄧ個共通性,即是癌症細胞的基 因訊息均有突變,造成了癌細胞不會受到正常生理限制調控且可繼續生長[8-10]。與正 常細胞相較之下,癌細胞擁有以下特性: a.無細胞分裂次數限制[8, 10] b.可自體分泌生長 因子 (Autocrine) [11-13] c.不受細胞凋亡機制 (aoptosis)的調控[14-16] d.不受細胞間接 觸抑制 (contact inhibititon)[17-19] e.有轉移至其他組織的能力[20, 21] f.具有促使血管新 生 (angiogenesis)的能力[22-24]。面對癌症細胞的多變性極高死亡率,目前常使用的治 療方法可分為傳統的手術與化療,以及結合生物技術的療法,包括標靶治療與免疫療法 等。 2 癌症的治療 2-1 傳統療法 較常見的傳統療法包括外科切除、放射線療法、及化學藥物療法。 2-1-1 外科切除 當癌症初期,癌細胞尚未轉移時,可進行外科切除癌症病變的區域,如果手術進行 順利並且將病灶部位切除乾淨的話,是可以完全將癌症治癒的。目前較著名的例子為治 療乳癌的乳房切除術 (mastectomy)[25, 26] 與治療前列腺癌的前列腺切除術 (prostatectomy)[27]。但是因為在病灶附近可能會有些許肉眼無法辨識的癌細胞存在,導 致手術後仍殘存癌症復發的風險。除此之外,並非每個部位的癌症均適合使用手術治 療,例如淋巴癌等。而當癌細胞擴散後,手術即無法成為單一或是主要的治療方式 [27-30]。 2-1-2 放射線療法 放射線療法利用對人體具有傷害性的放射線,依據癌細胞生長快速的特性,所設計 出來的一種療法。因癌細胞生長與分裂速率較正常細胞快速,故遭到放射線攻擊細胞內 的去氧核醣核酸 doxyribonucleic acid, DNA),使所受到的傷害也會較大,放射性療法的 好處是可控制放射線侷限於需治療之部位。放射線療法可應用之範圍廣泛,包括乳房肺 臟、胰臟、皮膚等固態瘤 (slid tumor)或是淋巴癌、血癌等均可使用。不過,在進行高劑 量的放射線治療時,仍有機會對週遭正常細胞產生傷害,並產生治療的副作用[31-33]。 2-1-3 化學藥物療法 利用干擾細胞分裂的藥物阻斷癌細胞的生長,其作用原理與放射線療法相似,大部 分的化學藥物均無專一性,會對其他細胞造成影響,故除了最基本的對藥物產生過敏 外,常見的副作用還有消化系統的潰瘍、噁心、嘔吐、及造成白血球、紅血球、血小板2 數量降低等,常會造成癌症病人卻步[34-36]。 2-2 新興療法 有鑑於傳統療法常伴隨嚴重副作用,導致病人醫療意願以及醫療效果下降,新興的 癌症治療方式可以專一性的攻擊癌細胞,且不影響正常細胞。目前此類療法包括了免疫 療法、光敏療法、標靶藥物療法。 2-2-1 免疫療法 人體中的淋巴球除了 T 細胞與 B 細胞外,另外有大約 15%~20%的天然殺手細胞 (ntural kller cll, NK cell)。天然殺手細胞與 T 細胞與最大的不同點在於天然殺手細胞不需 要巨噬細胞所呈現的表面抗原,即可快速的攻擊癌細胞,且目前天然殺手細胞的來源為 來自病人體內,經過體外培養使細胞增多後在注射進患者體內,故並不會有排斥反應的 問題產生[37-40]。目前日本已有數十例成功的案例,其中包括乳癌、肺癌等[41, 42]。 2-2-3 光敏療法 光敏療法又稱為光動力學療法、光化學療法等。其原理為將光敏劑注入體內,在輔 以雷射以特殊波長激發光敏劑,產生一系列反應,使得與光敏劑接合的分子被破壞,在 癌症治療中,目前常使用的光敏劑為血卟啉衍生物(HPD),此衍生物對腫瘤細胞有較 強的親和力,故對腫瘤細胞有較大的傷害。相較於腫瘤細胞,光敏劑在正常組織中停留 的時間較短,不容易產生副作用。惜一般在注射光敏劑後,患者需避光一~二月,避免 非預期的副作用產生[43-45]。 2-2-2 標靶治療 標靶治療的原理為阻斷癌細胞特有的分子機制來達到殺死癌細胞的目的。其作用目 標主要針對癌細胞訊息傳導、血管新生的機轉及特定表面抗原,藉由藥物或是單株抗體 [46-50]結合並阻斷癌細胞特有的表面抗原與特定的分子機制,達到抑制癌細胞生長、導 致癌細胞細胞凋亡及抑制癌細胞侵蝕能力的效果。其優點是對癌細胞有專一性,並不影 響週遭的正常細胞,也不容易產生嚴重的副作用。但因為癌細胞的多變性,導致每位患 者身上的癌細胞在基因突變的位置也不盡相同,故標靶治療藥物並非適合每一位癌症患 者,在進行標靶藥物治療前,必須先進行基因檢測及評估,以期取得較佳的治療效果。 不論是傳統療法或是新興療法,均希望對癌細胞造成較大的傷害,並且對於週遭的 正常細胞產生較小的影響,所以對於每次治療的放射線或是藥物的劑量都必須精準計 算,以期癌細胞藉由細胞凋亡途徑死亡,並避免高劑量的放射線或是藥物導致癌細胞與 週遭正常細胞產生壞死 (necrosis)的情形,進而引起免疫反應並導致附近細胞及組織受 損[51-57]。 3 細胞死亡與其分子機制 細胞死亡的路徑主要可以區分為細胞凋亡與細胞壞死(圖 1),細胞凋亡主要指的是 主動的、有計畫性的細胞死亡途徑,並且可以避免非預期性的發炎反應 (inflammation) 產生[58-62];而細胞壞死主要被歸類為被動的,被環境影響的非計畫性死亡,並會釋放細 胞內的發炎物質導致發炎反應的產生[63-66]。換句話說,當細胞受損而進行細胞凋亡
3 時,並不會對附近的細胞或組織產生不良的影響,而細胞壞死則會對附近的細胞或組織 產生不良的影響,進而導致其受損。除了生理影響上的區別外,一般判斷細胞凋亡與壞 死的方式,主要是尤其外觀上的不同(表一)及其分子機制的差異進行判斷。 表一、細胞凋亡與細胞壞死的型態學差異 參考文獻[61-65, 67, 68] 3-1 細胞壞死與其分子機制 細胞壞死被稱為一個非計畫性的細胞死亡模式,在此情況下,細胞會迅速膨脹,細 胞膜破裂,細胞內的物質會被釋放出來。導致離子平衡、溶小體內容物被釋放,在這種 情形下,細胞本身無法承擔死亡所帶來的後果,而進一步造成細胞毒性並釋放發炎因子 影響到附近的細胞與組織[67, 68]。在病理上,細胞壞死常與缺血、中風及神經退化性疾 病有關[69-71]。然而,最近的研究指出,細胞其實可以控制是否走向壞死路徑[72-75], 也就是說,除了無法預期的傷害外,細胞其實也可以選擇是否走向壞死路徑。其原因可 能是當其他細胞死亡路徑被抑制,細胞又需要死亡時,細胞可能會選擇以壞死路徑造成 細胞死亡[76, 77]。但是因為其造成的發炎反應及對週遭細胞或組織的傷害,所以通常是 被放在較後面的選擇順位,此外,在演化上,越高等的生物會有更多的自噬 (autophagy) 與細胞凋亡機制可代替壞死機制[75, 78]。事實上,當使用藥物毒殺細胞時,常會發現細 胞凋亡與細胞壞死共同產生的情形[79],此結果也反映出了無法使用簡單的方式檢測並 量化細胞壞死的程度[80]。 在分子機制方面,當死亡受體 (death receptors)接受到訊息後,會聚集並啟動訊息傳 導路徑,依照不同的細胞,造成細胞凋亡或細胞壞死[81]。腫瘤壞死因子 α (tumor necrosis factor α, TNF-α),可誘導多種細胞凋亡,但在 L929 小鼠纖維肉瘤細胞株內,腫瘤壞死因 子α 可誘導細胞壞死[82],其作用機轉主要是改變細胞膜的通透性且失去脫氫酶 (dehydrogenase)的活性,並誘導腫瘤壞死因子-細胞激素 5 (cytokine 5)的產生[83],另外, 加入泛硫胱氨酸蛋白酶 (cysteine asparate protease, caspase)抑制劑 zVAD-FMK 可增強腫 瘤壞死因子α 所誘導的細胞壞死[84],此外,在小鼠胚胎纖維母細胞 (murine embryonic fibroblasts , MEFs)中,加入泛硫胱氨酸蛋白酶抑制劑可將腫瘤壞死因子 α 所誘導的細胞 凋亡途徑改變為細胞壞死途徑[85],此結論也可呼應細胞壞死路徑可當作細胞凋亡路徑 被阻斷時的替代路徑。Fas 相關死亡區域 (Fas-associated death domain, FADD),是決定 細胞走向細胞凋亡或是細胞壞死的關鍵開關[86, 87],在細胞壞死路徑中,當腫瘤壞死因 子α 與腫瘤壞死因子受器超級家族 1a (tumor necrosis factor receptor superfamily member
細胞凋亡 細胞壞死
型態變化 細胞皺縮,胞器完整 细胞腫脹 (cell swelling),結構被破壞 細胞核 濃縮 (nuclear condensation) 細胞核腫脹
染色體 聚集,緻密 鬆散,分散
4
1a, TNF-R1)結合後,並不會造成更多的 Fas 相關死亡區域與受器結合[88-90],並且迅 速的在質膜 (plasma membrane)形成含有腫瘤壞死因子受器超級家族 1a、腫瘤壞死因子 受器相關因子2 (TNF receptor-associated factor 2, TRAF2)與 RIP1 (ubiquinol-cytochrome c reductase, Rieske iron-sulfur polypeptide 1)之複合體[91],迅速活化 NF –κB (nuclear factor
kappa-light-chain-enhancer of activated B cells)與有絲分裂原活化蛋白激酶
(mitogen-activated protein kinases,MAPKs)[92],例如 p38 有絲分裂原活化蛋白激酶 (p38 mitogen-activated protein kinase, p38 MAPK)、c-jun N 端激酶 (c-jun N-terminal kinases, JNK)與細胞外訊息調節激酶 (Extracellular signal-regulated kinases, ERK)等 [93]。在腫瘤壞死因子受器超級家族 1a 被細胞內吞 (endocytosis)作用所吞噬後,腫瘤壞 死因子受體相關死亡區域蛋白質(tumor necrosis factor receptor – associated death domain , TRADD)會與 Fas 相關死亡區域及原硫胱氨酸蛋白酶 8 (procaspase-8, FADD-like
interleukin-1-converting enzyme, FLICE)或原硫胱氨酸蛋白酶 10 (procaspase-10)形成第二 個複合體[94, 95],被吞噬進來的囊泡 (vesicle)會與含有原酸性鞘磷脂酵素
(pro-acid-sphingomyelinase , pro-A-SMase)及含有原前組織蛋白酶 D (pro-pre-cathepsin D,pro-pre-CAD)的反式高爾基氏囊泡 (trans-Golgi vesicles)融合,並活化多囊泡核內體 (endosome)內的酸性鞘磷脂酵素與組織蛋白酶 D [96, 97]。如果第一個複合體沒有成功誘 導出大量的抗凋亡蛋白 (anti-apoptotic protein),則細胞會走向凋亡路線。反之,如果有 大量的抗凋亡蛋白產生,則細胞會走向壞死路徑[84, 98]。當細胞走向壞死路徑時,一些 發炎因子如TNF-α、NFκB、COX-2 等會被誘發表現並對周圍細胞產生傷害[99, 100]。 3-2 細胞凋亡及其分子機制
細胞凋亡,或稱程序性細胞死亡 (programmed cell death),此現象首先於線蟲 (Caenorhabditis elegans, C. elegans)中被發現[101],成熟的線蟲有1090個體細胞,其中有 131個體細胞會於發育過程中經由細胞凋亡方式死亡,在不同的個體中,這131個體細胞 死亡的時機與方式是一模一樣的,代表其中有個嚴謹且精準的機制調控細胞死亡,且不 影響其他細胞的正常生長發育[101]。細胞凋亡在生長以及維持體內平衡扮演重要的角 色,且常伴隨者發育或衰老過程[102-107],維持細胞組織內的平衡,或是在免疫反應或 細胞受損時,扮演者防禦者的角色,清除損壞的細胞[108-110],雖然有多種途徑可誘導 細胞凋亡[111-116],但相同的細胞凋亡誘導物並非對所有的細胞均有相似的效果,例如 Her-2抗體只對乳癌細胞有效[117],對其他組織的細胞並不會造成影響。而細胞凋亡主 要分為兩種起始途徑,內在 (inner/ intrinsic/ mitochondria)路徑以及外在 (outer/ extrinsic/ receptor) 路徑[118-121],外在路徑主要是受到一些凋亡訊息所誘導,如Fas或腫瘤壞死 因子α,與細胞膜上的Fas或腫瘤壞死因子α受器結合後,與受器相連接的Fas 相關死亡 區域會與原硫胱氨酸蛋白酶8及原硫胱氨酸蛋白酶10的同源區域-死亡效應區域 (death effector domain, DED)結合,形成死亡誘導訊息複合體 (death-inducing signaling complex, DISC),並自催化 (autocatalytic)及切割原硫胱氨酸蛋白酶8或原硫胱氨酸蛋白酶10,使 其成為活化態的硫胱氨酸蛋白酶8 (active caspase-8)或硫胱氨酸蛋白酶10 (active
5 化且切割下游的原硫胱氨酸蛋白酶3、6、7[125, 126],讓細胞走向凋亡路徑。除此之外, 活化態的硫胱氨酸蛋白酶也會將屬於細胞淋巴瘤基因2 (B-cell lymphoma 2, Bcl-2)的促 細胞凋亡蛋白Bid切割並活化,導致粒線體膜電位改變,啟動細胞凋亡的內在路徑 [127-129]。除了外在路徑可以活化細胞凋亡的內在路徑,還有許多的物理或化學傷害(如 紫外光[130]等)、抑癌基因以及致癌基因 (c-Myc, c-Fos, p53等)的表現、去氧核醣核酸受 損、氧化壓力、錯誤摺疊的蛋白質堆積、以及其他的壓力因子導致內在細胞凋亡路徑的 啟動[111, 113, 131]。當路徑啟動時,促細胞凋亡蛋白質細胞淋巴瘤基因2家族成員Bax、 Bak、Bim、Bid會被活化[132-134],或是內質網 (endoplasmic reticulum, ER) 釋放鈣離 子,鈣離子隨後會進入粒線體[135-137],這兩種方式皆會導致粒線體外膜膜電位改變並 產生孔洞,造成细胞色素C (cytochrome c)及一些促細胞凋亡分子產生,如第二粒腺體衍 生活化硫胱氨酸蛋白酶因子 (second mitochondria derived activator of caspase, Smac)/ 低 等電點直接結合細胞凋亡抑制蛋白 (direct IAP-binding protein with low pI, DIABLO)[138, 139],細胞凋亡誘導因子 (apoptosis-inducing factor, AIF)等[140, 141]。而細胞色素C被釋 放至細胞質時,會與凋亡蛋白酶啟動因子1 (apoptotic protease activating factor 1,
Apaf-1)、原硫胱氨酸蛋白酶9 (procaspase-9)形成凋亡小體 (apoptosome)[142, 143],進一 步切割與活化硫胱氨酸蛋白酶9,活化的硫胱氨酸蛋白酶9 (active caspase-9)會切割與活 化下游的原硫胱氨酸蛋白酶3、6、7 (caspase-3, -6, -7)[144, 145],並開始細胞凋亡路徑, 例如切割修復去氧核醣核酸的多核醣核酸聚合酶 (Poly (ADP-ribose) polymerase,
PARP)[146],水解維持細胞核膜骨架的lamin (class V intermediate filaments)蛋白[147, 148],使得細胞出現凋亡小體 (apoptotic body)等細胞凋亡型態並死亡。
在本研究中,我們藉由觀察發炎因子之一-環氧酵素2 (cyclooxygenase-2, COX-2)判 定細胞是否走向壞死路徑,並以硫胱氨酸蛋白酶3、硫胱氨酸蛋白酶9、多核醣核酸聚合 酶[149-151]、細胞凋亡誘導因子等判斷細胞是否走向凋亡途徑。
6 圖 1、細胞死亡之分子機制 4 實驗動機 癌症不容易被完全根治,一般對於癌症治療的效果多以〝 年存活率〞為標的。因 為化學藥物與放射性療法為非專一性的治療,所以作用區域並非侷限於病變區域,也容 易對於癌細胞週遭組織的損害與引起強烈的副作用,這些結果會降低治療的效果及造成 病人的負擔。當癌症復發時,再重覆化學藥物與放射性治療,對於週遭正常細胞的重複 性傷害,並不亞於癌症細胞帶來的傷害。目前結合生物科技方式,可將抗癌藥物或是物 質傳送至癌細胞,且不會對週遭正常細胞造成影響,此方式即為〝標靶治療〞。標靶治 療作用只針對癌細胞,並可藉由所攜帶的藥物或是物質造成癌細胞以細胞凋亡方式進行 死亡,不會造成週遭細胞或組織的傷害,可有效的抑制癌症的增生或使癌細胞減少並達 到治療的效果。在本研究中,我們利用結合生長激素的奈米鑽石標定肺癌細胞,並利用 雷射激發使奈米鑽石體積爆炸並對癌症細胞造成傷害; 或利用可與乳癌細胞特殊表現受 體CEACAM6與HER-2結合的單一抗體,達到標靶治療的目的,並藉由探討其死亡分子 機制與抑制癌症增生能力,建立新的癌症治療平台與方法。
7
8
壹、第一章 研究背景
壹-1-1 肺癌
依世界衛生組織 (World Health Organization,WHO)歷年公布之世界癌症排名,肺 癌 (lung cancer)之致死率一直列於前三名,於 2010 年之統計資料公佈,無論男性或女
性,因肺癌死亡之比率皆佔所有癌症之冠,分別為29%以及 26%,而在新增癌症病例中
也都位居第二名[152]。故本研究在篩選了具有生長激素大量表現的癌細胞中,設定以肺 癌為研究題材,而肺癌通常又粗分為兩類:小細胞肺腺癌 (small cell lung cancer, SCLC) 與非小細胞肺腺癌 (non small cell lung cancer, NSCLC)。大約 20%-25%的肺癌患者屬於 小細胞肺腺癌,而其他大多數約75%-80%則歸類為非小細胞肺腺癌患者[153, 154],故 本研究選擇以A549 非小細胞肺腺癌細胞作為主要之研究對象。 壹-1-2 奈米材料於生物醫學之應用 「奈 (nano)」為一數量級單位,等於 10-9,而「奈米 (nanometer)」則為對物質尺 度之描述,等於10-9米。奈米技術於1990 年代開始受到重視,繼機械、電子、資訊科 技後被稱作第四次工業革命,至今已廣泛發展於各領域[155],其目的是以原子、分子或 巨分子之尺度為基礎[156],針對這些物質的結構或裝置作探討及應用,並有別於過往能 夠發展出更具功能或效率之目標物。 奈米科技中的一環-奈米材料為科學研究中的熱門題材,舉凡物質之幾何形狀涵蓋 於一奈米至三百奈米間 (即達到奈米尺度)者[156, 157]皆可包含於其中,而其主要之類 型則包含了奈米粉末或奈米顆粒 (nano powder/ nano particle)、奈米纖維 (nano fiber)、 奈米薄膜 (nano film)、奈米塊材 (nano bulk)等等。奈米粉末或奈米顆粒指的是粒徑大小 小於一百奈米以下的粉末或顆粒,為一種介於原子、分子與巨分子間的固體顆粒材料, 例如:奈米金、奈米鑽石等;奈米纖維即為三維空間中,有兩個維度處於奈米尺度之線 狀材料,亦及直徑或厚度達到奈米尺度並且長度較長之線狀材料;常見如;奈米線、奈 米碳管;奈米薄膜係指由奈米尺度之顆粒或晶體所構成之薄膜狀結構,此材料每一層厚 度皆於奈米等級的單層膜或多層膜,例如:矽、砷化鎵等,這些材料具有良好之光電特 性,多應用於光電、半導體產業;奈米塊材則是將奈米粉末以高壓或高溫之方式使材料 成型,通常依此方式所得之奈米材料在特性上會與一般材料有高度特異性,像是具有高 比熱、高強度、高導電性、高韌性、高熱膨脹性質等等。而以上這些奈米材料所表現之 結構特性更有別於一般,像是尺寸小、具有高表面積與體積比、為高密度堆積之結構, 並有高結構組合彈性,這些奈米材料在結構上的特點與優勢造就了其更高的利用價值。 以下列舉一些常見於生醫領域所應用之奈米材料: (一) 奈米金 (nanogold):在多種奈米金屬材料中,奈米金粒子因為良好的生物相容性及 特殊光學性質,而被研究最為廣泛。目前奈米金粒子應用於生物醫學上的項目包括了光 子標靶治療、生物檢測、活體影像觀察等。在光學上,奈米金粒子的特殊吸收波長會因 粒徑大小增加而產生紅位移的情形,舉例來說,當奈米金粒子直徑為3 nm 時,其吸收
9 波長為509 nm,而當直徑增加到大約 10 nm 時,其特殊吸收波長則會紅位移至 518 nm 左右,此特殊光學性質較常應用於免疫檢測部分,如驗孕棒等,當分散的奈米金粒子因 其上所接合之抗原抗體反應而聚集時,會從原本的淡粉紅色變為深藍色,可供肉眼直接 判定檢驗結果。此外,奈米金也因為擁有強的吸光係數即可改變的特殊吸收波長特性, 故在光敏治療法中也佔有一席之地[158, 159]。
(二) 奈米碳管 (carbon nanotube,CNT):於 1991 年由日本 NEC 公司研究員 Sumio Iijima 以弧狀放電法置備碳60,並以穿透式電子顯微鏡觀察碳的團簇(cluster)時意外發現直 徑約1-30 奈米石墨平面捲曲而成之管狀材料,此即為多層奈米碳管(multi-walled)的 發現[160, 161]。在生物醫學上,奈米碳管因為其生物毒性,導致應用的範圍較為侷限[162, 163],不過仍有人成功將奈米碳管應用於細胞的微注射[164]。
(三) 微脂體 (liposome):細胞膜 (cell membrane)由脂質雙層膜 (lipid bilayer)組成,成分 主要為磷脂類 (phospho-lipid),其中脂肪酸鏈為疏水端,磷酸端為親水性,脂肪酸鏈包 埋於雙層膜之中,而磷酸端裸露於外層,造成整體親水性之構型。微脂體的構型與細胞 膜相似,可均勻分布於水溶液中,並具有高度生物相容性即可分解性,故被應用於生物 載體部分。水溶性物質與疏水性物質可被分別包埋於球心及脂雙層內,並藉由細胞膜的 吸附 (absorption)、融合 (fusion)與膜間轉換 (inter-membrane transfer)等方式將所攜帶的 藥物或物質帶入細胞[165-167]。
(四) 量子點 (quantum dot):當量子點的三維皆被限制於100 nm以下時,其電子與電洞 會被侷限於非常小的空間中,使其再結合的機率變大,導致發光效率相對增加。而量子 點在激發光的能量超過其能隙 (band gap)時,會吸收光子並導致電子由共價帶 (valence band)躍升至導電帶 (conduction band),當電子由導電帶回到共價帶時,會放出螢光。當 塊材的大小變小時,因原子數減少,造成能階密度 (density of states)降低,能階間隔變 大,有效能帶增大,導致吸收與螢光光譜產生藍位移 (blue shift)現象。換句話說,當粒 子越小,相同材料所製成之量子點會有更短之螢光光譜。所以即便是單一光源,量子點 可以因為大小不同而產生不同的螢光顏色,另外量子點相較於傳統螢光染劑,擁有更佳 之亮度與穩定度。故量子點可用於長時間與即時的生物分子追蹤,對於診斷與醫療治療 有相當大的應用空間[168-170]。 (五) 奈米鑽石 (nanodiamond): 奈米鑽石大約在 1980 年代被發展出來,主要的製造方法 為使用黃色炸藥-三硝基甲苯 (trinitrotoluene, TNT)在負氧的環境下爆炸產生,因為奈米 鑽石於短時間 (<10-6秒)的高溫高壓下生成,故其顆粒大小大約只有 4~10 nm。由結晶學 來看,因為奈米鑽石生成的時間短,溫度高 (103 K),加熱速度過快 (109 K/s),導致鑽 石內的晶體生成時容易出現大量的晶格缺陷,稱為氮空位缺陷中心 (nitrogen-vacancy defect center, NV center),有研究指出,奈米鑽石中的氮空位缺乏中心與螢光有關[171, 172]。一般而言,最外層與最內層電子軌域間之能量差即為能隙 (band gap),而在奈米 鑽石中,因所含有的原子數減少,各原子被周圍原子的影響也變少,產生量子侷限效應 (quantum confinement effect),產生非連續性的離散電子能階,而能隙也會因奈米化而變 寬,電子能階非連續化及能隙變寬現象,稱為量子尺寸效應 (quantum size effect)[173, 174]。
10 奈米鑽石已經被證明有高度生物相容性及低生物毒性,可當做輸送基因與藥物的載體 [175-177],並且經由吸收雷射的能量後,會因熱聲子效應而使其轉換為石墨結構 (sp3 to sp2),造成體積膨脹[178],可破壞特定目標,達到治療的目的。 壹-1-3 多光子效應 (multiphoton effect) 多光子激發 (multiphoton absorption)為一非線性之光學效應,指的是於高強度之激 發光激發下,一個分子同時吸收多個光子,由基態轉變為激發態之過程,其吸收能量等 同於頻率為n 個單光子所提供之能量,即能量為 n。於單光子效應中,分子經由逐次吸 收單個光子先躍遷至中間態,再藉由吸收單個光子而躍遷達到最終激發態,故在單光子 吸收效應中,分子會停留在許多不同能階的階段性激發態;而雙光子激發則是受激發之 分子同時吸收兩個光子而躍遷至激發態,其所受能量相當2之單光子激發能量,但因需 要兩個光子同時激發而躍遷至激發態,故躍遷機率 (transition rate)正比於入射光強度的 平方,且雙光子受吸收截面低之緣故使得其須極高之瞬間功率方可產生有效激發;而於 多光子吸收過程中,分子會直接由基態躍升至最終激發態,不會有任何的階段性激發態 存在,此為三者最大之差異[179, 180]。 一般來說,多光子效應所需吸收之光子密度非常高,一般於自然界中不易發生,本 實驗室使用高密度脈衝雷射來做為實驗工具,而使用多光子效應激發時須考量生物分子 與細胞所能承受之最大能量[181],而對於奈米鑽石之多光子吸收效應,雖然其因此原理 激發可造成結構上劇烈改變,但應用於生物體中則必須配合在生物分子或細胞所能承受 之功率範圍,故須進一步探討此奈米分子於生物醫學之應用性。
11
壹、第二章 研究動機與策略
壹-2-1 研究動機 本研究結合了奈米科學及生物技術開發了一項新的癌症奈米標靶粒子 (nano targeting complex),其利用奈米鑽石為基礎,接合上與癌細胞具有靶向性之生物分子來 做為一治療工具。奈米鑽石本身內部為一穩定的sp3結構並具有高度生物相容性,由本 實驗室先前研究指出,經由高脈衝雷射之激發後奈米鑽石結構重新排列成sp2,以穿透式電子顯微鏡 (transmission electron microscopy,TEM)影像觀察得知其體積膨脹十多倍 之多[178],依此特性與概念設計出的奈米標靶粒子-羧酸化奈米鑽石與生長激素受體結 合蛋白及綠螢光蛋白之複合物 (cNDGHRBP-GFP complex),其接合了肺癌細胞表面大量 表現之生長激素受體的專一性結合蛋白,也做為一競爭劑 (antagonist),以及可用來標定 癌細胞位置的綠螢光蛋白,加上高脈衝雷射誘導奈米鑽石爆炸,可進行破壞癌細胞組織 之動作,此為類光敏治療的方法,可免除侵入性手術問題,並準確控制癌細胞死亡之程 度與區域,避免大量細胞同時死亡所帶來的傷害。依照上述特性,可將多光子趨動標靶 化奈米鑽石開發為新一代癌症治療平台。 依實驗策略,我們想知道細胞經處理 cNDGHRBP-GFP 並使用高能脈衝雷射激發 cNDGHRBP-GFP 後可以對癌細胞造成何種程度之影響,並且於學術上,我們研究當中 誘導細胞死亡或損傷之分子機轉。爾後,加上癌症細胞特定表現或活化之標靶分子,期 望能夠發展並建立出一套針對清除癌細胞之目的具有更專一、有效率的標靶治療之系 統,並利用於生醫領域上。
12 壹-2-2 研究策略 利用化學法修飾使奈米鑽石表面羧酸 化,使帶有羧基(COOH- group) 免疫BALB/c 小鼠,取得重組生長激素 蛋白質之抗體 重組生長激素抗體效價(titer) 之生化分析 以化學交聯劑(cross-linker) EDC 及 sulfo-NHS 接合羧酸化奈米鑽石、重組 生長激素與綠螢光蛋白 利用化學法修飾使奈米鑽石表面羧酸 化,使帶有羧基(COOH- group)
cNDGHRBP-GFP 於 A549 肺腺細胞株內之細胞毒性(cytotoxicity)分析:MTT assay
cNDGHRBP-GFP 吞噬於細胞內之位置分析:Immunocytochemostry
選定奈秒脈衝雷射於 cND 與 A549 細胞之有效功率:trypan blue staining
多光子雷射激發細胞表面標靶化奈米鑽石 導致細胞死亡之分析:Immunocytochemistry
13
壹、第三章 實驗策略原理
壹-3-1 蛋白質的表現與純化
為了獲得實驗中所需要之癌症標定蛋白質及及觀察用標的物,我們使用本實驗既有 之分生技術,表現與純化出實驗中所需要之生長激素蛋白質與綠螢光蛋白。將所需之基 因片段與pET28a 與 pET-30a 載體做接合,而後送入大腸桿菌 (Escherichia coli,E. coli)
BL21(DE3)中,待細菌生長至對數期 (log phase) 時加入 IPTG 誘導蛋白質大量表現, IPTG 為乳糖相似物,可誘導乳糖操作組後的 T7 聚合酶 (T7 polymerase)大量表現,而被 誘導表現的T7 聚合酶會與載體 pET28a 及 pET-30a 上的噬菌體 T7 啟動子 (T7 promoter) 結合並誘導在T7 序列後端所接合之欲表現的基因;且 pET-30a 上含有組氨酸 (histidine) 之序列,一串六個組氨酸所組成的組氨酸標籤 (Histidine tag,His. Tag) 具有金屬親和 性,將含有組氨酸標誌之蛋白質通過含鎳離子 (Ni2+)的親和性層析管柱,此時組氨酸會 與鎳離子螯合而結合在管柱上,而菌液中其它不含組氨酸標誌的蛋白質會流出管柱中, 達到純化的效果。 壹-3-2 EDC、sulfo-NHS 的蛋白質接合 為了將奈米鑽石與蛋白質接合,製造有標靶功能的奈米鑽石,我們使用化學交聯 劑:二亞胺基碳與N-羥基硫代琥珀酰亞胺進行奈米鑽石、生長激素、綠螢光蛋白之接
合。二亞胺基碳 (1-Ethyl-3-[3-dimethylaminopropyl]carbodiimide hydrochloride ,EDC) 常 做為交聯劑 (crosslinker) 與 N-羥基硫代琥珀酰亞胺 (N-Hydroxysulfosuccinimide sodium salt,sulfo-NHS) 應用於一些化學接合反應中,以形成胺反應 (amine-reaction) 或是化合 物 (compound) 的接合。二亞胺基碳分子量 191.7,為一個零長度的交聯劑 (zero-length crosslinking agent) ,利用脫水方式聯結羧酸基 (-COOH) 與胺基 (-NH2);而分子量
217.13 之 N-羥基硫代琥珀酰亞胺在聯結羧酸基與胺基的反應中,對反應物進行修飾, 使其穩定而提高接合效率。任何化合物、生物分子或奈米粒子只要帶有羧酸基即可與二 亞胺基碳以及N-羥基硫代琥珀酰亞胺進行活化使能夠反應,與帶有胺基者,例如蛋白 質形成共價接合[182]。 為了使本實驗用的奈米鑽石利於與蛋白質接合,故事先會以化學修飾使奈米鑽石表 面帶有羧酸基,此時,利用水溶性之二亞胺基碳以及N-羥基硫代琥珀酰亞胺的活化, 羧酸基可以與蛋白質上的胺基形成醯胺鍵鍵結。N-羥基硫代琥珀酰亞胺在此反應中用以 修飾羧酸基使形成胺反應酯 (amine-reactive easter),而二亞胺基碳會在羧酸基與 N-羥基 硫代琥珀酰亞胺的羥基 (hydroxyl group) 間造成脫水反應,生成 N-羥基硫代琥珀酰亞胺 -酯的活化分子 (sulfo-NHS-ester-actived molecule),此中間物的穩定特性可以使反應更有 效率。而透過此分子上帶有羧酸基,其又會自發性與帶有胺基的分子發生反應,合成實 驗所需的cND-rEaGH-GFP 複合物。
14
壹-3-3 原子力顯微鏡 (Atomic force microscopy, AFM)
原子力顯微鏡是於1985 年由 Gerd Binnig 及 Heinrich Rohrer[183]所研發問世,其利 用探針與樣品之間的原子間作用力(包含靜電排斥力 (electrostatic repulsion)、萬有引力 (universal gravitation)、凡得瓦爾力 (van der Waals forces) )來描繪出樣品表面形貌[184, 185],幾乎可應用於所有樣品上。 AFM 系統可區分成三個部份,包含原子間作用力感測器:懸臂 (cantilever)、懸臂 偏移量感測器及位移掃描系統。利用懸臂上探針針尖之原子感測樣品表面原子間之作用 力,配合光學式雷射對焦於懸臂上並反射至位移敏感的感光二極體 (position sensitive photo-diode, PSPD) 定位,當原子間作用力變化造成懸臂產生彎曲偏移時,其雷射光反 射點亦產生偏移,此時感光二極體即可依雷射光點之偏移量推算懸臂偏移量,再配合壓 電晶體掃描器 (piezoelectric scanner) 進行三軸位移掃描,即可描繪出樣品表面之高低起 伏之形貌[186]。 本實驗利用原子力顯微鏡作為觀察cND-GHRBP-GFP 複合體之外型及均勻度分析。 壹-3-4 動態光散射儀 (Dynamic light scattering, DLS)
動態光散射儀又稱為光子關聯光譜法 (photon correlation spectroscopy,PCS)[187]。 當雷射光射入含有懸浮粒子的溶液中,雷射光會因為撞擊粒子而產生散射光,此時散射 的雷射光會隨時間而改變,再由其間散射光強度之變化來計算溶液中粒子之平均粒徑大 小與分佈。而其原理係利用一般粒子懸浮於溶液中時會進行布朗運動 (Brownian motion)[188],依粒子大小的不同,布朗運動的速度也有所不同,粒子愈小速度愈快, 反之粒子較大則速度較慢。動態光散射儀利用雷射光打入溶液中,當雷射光打中懸浮粒 子時會產生雷利散射 (Rayleigh scattering),且粒子進行布朗運動中不斷移動,散射光強 度隨時間改變造成不同之趨勢與幅度,此時,利用時序上的自相關函數求得其擴散系數 (diffusion coefficient),再以 Stokes-Einstein equation 計算出粒子之水和半徑。此儀器量測 範圍可從幾奈米至幾微米。 Stokes-Einstein equation: r T k D B 6 ...(Eq. 1) 在Stokes-Einstein equation 中,D 為擴散係數,kB為波茲曼常數 (Boltzman constant),T 為絕對溫度 (absolute temperature),為溶液之黏滯係數 (viscosity), r 為球形粒子之水 合半徑 (hydrophobic radius)。 利用動態光散射儀,可測定 cND-GHRBP-GFP 複合體之粒徑大小。 壹-3-5 螢光儀 (Fluorescence spectrometer) 當分子吸收可見光或紫外光時,位於基態 (ground state) 能階的電子會被激發至激 發態 (excited state),在激發態的電子隨即以不同的能量方式(光或熱)衰退回基態,此時 若以放出光的形式衰退回基態,即產生所謂的螢光 (fluorescence)。
15 針對固定波長的螢光判讀,儀器只會固定在實驗所設定的波常範圍進行檢測,而對 於全光譜之掃描,則儀器會針對每一組波長累積量測值。對於先前之文獻指出,奈米鑽 石因晶格缺陷致使其本身在雷射激發下會產生螢光訊號[171, 172]。但有趣的是,本實驗 所使用之奈米鑽石發現與過去研究不符合,無論以螢光顯微鏡之汞燈或共軛焦顯微鏡之 雷射光源做激發皆不產生螢光訊號,故利用螢光儀對於奈米鑽石作全光譜分析。全光譜 掃描一般來說可以幫助找出樣品的螢光波鋒,對於本研究則做為判讀奈米鑽石是否具有 螢光特性之研究工具。
壹-3-6 奈秒脈衝雷射 (Nano-second pulse laser)
超快雷射一般依雷射光之脈衝寬度可區分為飛秒 (femtosecond, fs)、皮秒
(picosecond, ps)及奈秒 (nanosecond, ns)等級,本實驗所使用之雷射為以 Nd:YAG 作為激 光介質之奈秒脈衝雷射。
Nd:YAG (neodymium-doped yttrium aluminium garnet; Nd:Y3Al5O12) 為一種晶體,現
在常用作為固態雷射 (solid-state lasers) 的激發光源 (pumping source) 中的激光介質。 其中,Nd 為化學鑭系元素汝,原子序為 60;YAG 為 Y3Al15O12,是釔鋁石榴石晶體。 傳統的雷射光指的是必須以光學共振腔來收集所激發出的光以減低耗損;而在Nd:YAG 雷射中,將Nd 原子植入 YAG 晶體後,當 Nd 游離為 Nd3+並形成Nd:YAG,其即為一個 四能階之系統,同時具有激發率高且雷射光強之優點。並且於1964 年,首次由 Geusic 等人進行由Nd:YAG 所媒介之雷射操作[189]。 以 Nd:YAG 作為激光介質激發後,會產生 1064 nm 之紅外光雷射,而若經由倍頻器, 則可達到532 nm 之綠光雷射及 266 nm 之紫外光雷射光,並使用於本實驗中。另外,奈 秒脈衝雷射因加工速率高,並具有低操作成本之優點,故現今已廣泛應用於工業加工上。 壹-3-7 拉曼光譜 (Raman spectum) 所謂之拉曼 (Raman)光譜起因於光之散射 (scattering)所造成,即入射光之電磁波電 場向量與被激發之物質其本身所帶的電子交互作用下,導致入射光線散射。拉曼光譜 中,利用聲子 (phonon,為晶格中的振動)與光子 (photon)之間的交互作用,量測並計算 光子散射前後之能量差,由此可進一步得之光子的振動模式 (vibration mode)為何,又可 以說,拉曼光譜與分子之振動能 (vibration energy)相關。 一般,當入射光與分子作用時,電子會由最低能階之基態 (groundstate)躍遷至虛態 (virtual state),此時分子不會吸收能量,而隨即以散射之方式將能量釋放出來。若此釋 放出之能量恰相等於入射光子的能量,則此散射光稱做雷利散射 (Rayleigh scattering); 反之,若此釋放出之散射光能量不等於入射光子之能量,則此散射光稱為拉曼散射 (Raman scattering)。在拉曼光譜中為偵測散射光子與入射光子之頻率差,ω,此即為拉曼 位移 (Raman shift),而這之中所對應之能量即代表分子之振動能量。 在光的散射現象中,入射光光子被分子散射之機率約為百萬分之一,其中大多數散 射光都為雷利散射,而拉曼散射之強度則僅只有雷利散射強度之千分之一。對於拉曼散 射強度較微弱之特性對於實際偵測上所造成的限制,於1968 年美國科學家 Tobin 率先
16 利用雷射光作為激發光源來量測蛋白質樣品之拉曼光譜,此方式大大增強了拉曼散射之 訊號[190],而後,以雷射光作激發光源之拉曼光譜儀廣泛應用於化學、生化方面的研究。 於此,本實驗係利用拉曼光譜作為觀察經由不同條件下之雷射激發後,奈米鑽石內部化 學結構的改變。 壹-3-8 蛋白質定量法
壹-3-8-1 Bradford dye-binding method
此蛋白質定量方法使用考馬司亮藍 G-250 (Coomassie Brilliant Blue G-250,CBG250)
染劑來做為呈色的物質。當CBG250 與芳香族胺基酸或鹼性蛋白質結合後,其最大吸光
波長 (λ)會由 465 nm 轉為 595 nm[191],而 CBG250 會依不同 pH 環境下呈現不同顏色,
於酸性環境時為茶色,在中性下為藍色,故蛋白質所提供相對中性之環境可使CBG250
變成藍色。依此原理,藉由所生成的藍色產物與樣品混合液在O.D.595 時測定之吸光值
可進一步推算內含蛋白質量的濃度,即其所呈現之藍色深淺與蛋白質含量成正比。 操作時,將標準蛋白-牛血漿白蛋白 (bovine serum albumin,BSA)序列稀釋成不同 濃度,加入CBG250 反應後,以 ELISA reader 讀取波長 595 nm 之吸光值,依此吸光值 做出一條標準曲線,將樣品所測得之吸光值對照標準曲線後,可得出待測蛋白質之濃度。 壹-3-8-2 紫外光吸收法 (UV absorption)
由胺基酸所組成的蛋白質,其中的酪胺酸 (tyrosine)、色胺酸 (tryptophan) 及苯丙 胺酸 (phenylalanine)等屬於芳香族胺基酸,三者之側鏈帶有苯環 (aromatic ring),因苯 環具有穩定的共軛雙鍵,使之具有可吸收紫外光之特性。當中,酪胺酸與色胺酸在λ= 280 nm 時有最大吸光值,而苯丙胺酸則在λ= 260 nm 時有最大吸光值。因為色胺酸之 吸光值大於酪胺酸,而此二者之吸光值又遠大於苯丙胺酸,故通常會將苯丙胺酸之吸光 值忽略不計算入內[192]。 一般操作時,會將分光光度計在波長為 280 nm 下量測,所測得之待測樣品吸光值 與標準蛋白質之標準曲線做比對,所得蛋白質樣品之吸光值會與溶液中的蛋白質含量成 正比,因此當吸光值在線性範圍時(即 O.D.值小於 1),皆可進一步推測蛋白質濃度。 壹-3-9 十二烷基硫酸鈉聚丙烯醯胺凝膠電泳 (SDS-PAGE)
十二烷基硫酸鈉聚丙烯醯胺凝膠電泳 (sodium dodecyl sulfate polyacrylamide gel electrophoresis,SDS-PAGE)為一種常用於分離蛋白質分離之技術。主要是經由十二烷基 硫酸鈉 (sodium dodecyl sulfate,SDS)將蛋白質進行變性處理,利用聚丙烯胺凝膠 (polyacrylamide gel)之膠體內孔洞大小決定蛋白質於膠體中之泳動速率。一般來說,欲 分離脂蛋白質分子量愈大,所受之阻力亦愈大,則移動之速率慢,移動距離短;反之, 欲分離之蛋白質分子量愈小,其所受阻力也愈小,此時其泳動之速率相對快,移動之距 離也遠。根據此原理,可依不同濃度之聚丙烯胺形成不同孔洞大小,進一步可分離不同 分子量大小之蛋白質。
17 壹-3-10 西方墨點法 (Western blot) 西方墨點法一般是以十二烷基硫酸鈉聚丙烯醯胺凝膠電泳為基礎,以期來分離不同 分子量之蛋白質樣品,並進一步轉漬到固相載體上(常用例如:NC membrane、PVDF membrane),在固相載體中,蛋白質會以非共價鍵的形式吸附於其上,同時能夠維持十 二烷基硫酸鈉聚丙烯醯胺凝膠電泳時分離之多胜肽的生化活性。本實驗室所使用之固相 載體為聚二氟乙烯膜 (polyvinylidene difluoride membrane, PVDF membrane),其為一種 疏水性材質,蛋白質可藉由本身之疏水端接合於其上。 利用能夠與目標蛋白質互相辨識之特定一級抗體 (primary antibody) 作為一個探針 (probe),藉由兩者的專一性結合並以帶有一些發光物質或酶之二級抗體 (second antibody) 來標記與作為後續顯色,而後利用加入此發光物質的基質 (substrate) 使具有 目標蛋白之位置顯色,再利用曝光、壓片之技術以分析樣品中微量之目標蛋白表現量以 及可約略估算其分子量。此研究皆使用接有辣根過氧化酶 (horseradish peroxidase, HRP) 之二級抗體,並使用之基質係為化學發光法之ECL 試劑盒,辣根過氧化酶能夠有效的
催化氨基苯二酰一肼 (luminol) 與過氧化氫 (hydrogen peroxide, H2O2) 反應,即可產生
化學冷光放光。最後藉由曝光後壓片,以顯影劑顯影、定影劑定影即可進行數據分析。
壹-3-11 錐蟲藍排除法 (Trypan blue exclusion)
錐蟲藍 (trypan blue)係於 1904 年由德國科學家 Paul Ehrlich 首先合成,常用於細胞 染劑,常應用於觀察與分析細胞之存活。一般,活細胞之細胞膜為完整的,對物質進出 具有選擇性的通透性,此時,染料無法滲透入細胞中,則細胞不會有顏色,且於顯微鏡 下多為圓形且光亮;而不健康或死亡之細胞,因細胞膜通透性改變亦或是細胞膜破裂, 使得染劑得以進入細胞中,故細胞會呈現藍色。此時,藉由顯微鏡下細胞顏色之區隔, 可便於實驗分析細胞存活狀況。 壹-3-12 MTT 3-(4,5-二甲基噻唑-2-烴基)-2,5-二苯基四氮唑溴鹽
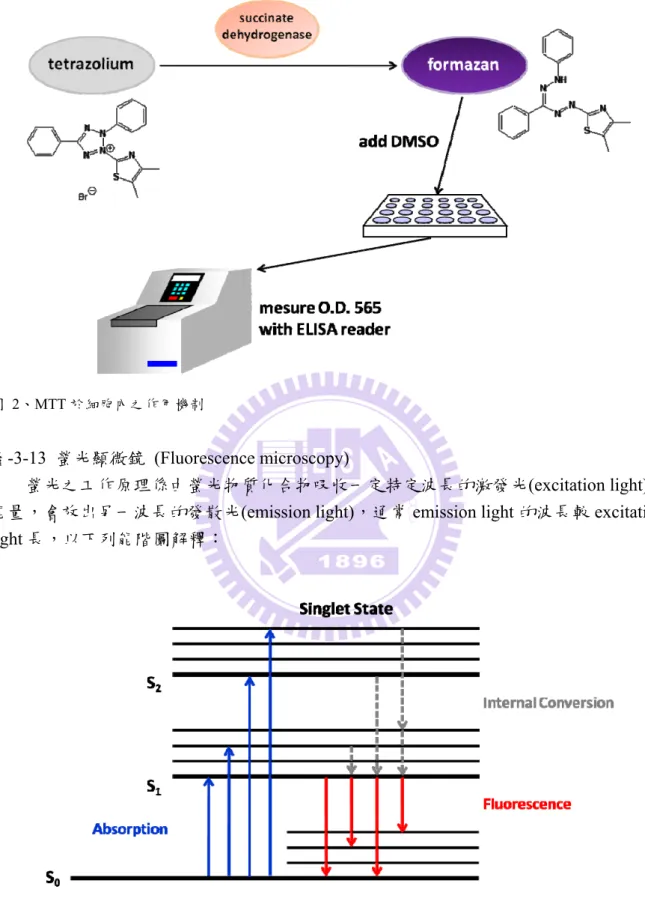
(3-(4,5-Dimethylthiazol-2-yl)-2,5-diphenyltetrazolium bromide,MTT)由 Mosroann 於 1983 年所提出,因活細胞粒線體當中的琥珀酸去氫脢 (succinate dehydrogenase)可以將 MTT 的四唑紫 (tetrazolium)還原成紫色且不溶於水的甲臢 (formazan),formazan 會堆積於活 細胞中,利用二甲基亞碸(dimethyl sulfoxide,DMSO)溶解之,再以 565 nm 的光作激發, 而後讀取O.D.值進行數據分析。又 formazan 與活細胞數目成正比,即其代表活細胞中 粒線體之活性,故可依此方法推算活細胞之比例。
18 圖 2、MTT 於細胞內之作用機制
壹-3-13 螢光顯微鏡 (Fluorescence microscopy)
螢光之工作原理係由螢光物質化合物吸收一定特定波長的激發光(excitation light)的 能量,會放出另一波長的發散光(emission light),通常 emission light 的波長較 excitation light 長,以下列能階圖解釋:
圖 3、螢光能階圖