國
立
交
通
大
學
環境工程研究所
碩
士
論
文
液相法製造程序對中孔洞沸石型吸附材
特性及其丙酮吸附量影響之研究
Effects of liquid phase synthesis
procedures on the characteristics of
mesoporous silica adsorbent and acetone
adsorption
研 究 生:林怡君
液相法製造程序對中孔洞沸石型吸附材特性及其丙酮吸附量影響之研究 研究生:林怡君 指導教授:白曛綾 國立交通大學環境工程研究所碩士班 摘 要 中孔洞沸石型吸附材因具有高比表面積及可調整孔洞大小之優 勢,故為奈米科技重要研究範疇之一,但其價昂貴且目前為止應用於 揮發性有機物之研究數量不若針對沸石之研究般廣泛。本研究以液相 法製成中孔洞沸石,研究重點包括(1)討論室溫(RT)及高溫(HT)凝膠合 成兩種不同合成程序(2)添加乙醇與否(3)改變界面活性劑與矽的莫耳 比例,作為中孔洞沸石製成的操控變因。接著將製成之中孔洞沸石以 熱重分析儀進行丙酮吸附試驗,並選出前述試驗中結果具代表性之的 中孔洞沸石,進行反覆吸脫附試驗,以了解各項變因對丙酮吸附的影 響,並與商業沸石進行比較。 HT法製成之吸附材雖比表面積較RT法低,且孔洞大小較RT法 大,但具有均勻的孔洞分佈且結構性較好。RT法製成之吸附材其對 丙酮之飽和吸附量均較HT法高。當界面活性劑與矽莫耳比例為 0.3、 添加乙醇情況下,RT法可得到最高的比表面積 1334 mP 2 P /g,而當界面 活性劑與矽莫耳比例為 0.3、不添加乙醇情況下可得到最高的丙酮飽 和吸附量132 mg/g。添加乙醇確可使製成之吸附材孔洞大小變小。而 本研究中添加乙醇與否及改變界面活性劑與矽莫耳比例對丙酮飽和 吸附量影響並無一定趨勢。在對丙酮反覆吸脫附的試驗中,其劣化程 度為ZSM-5>RT03>HTE03>HT03,因此可能最佳的配方製成之吸附 材為HT03。 關鍵字: MCM-41,沸石,界面活性劑,丙酮吸附,空氣污染,中
Effects of liquid phase synthesis procedures on the characteristics of mesoporous silica adsorbent and acetone adsorption
Student:Yi-Chung Lin Advisor:Dr. Hsunling Bai Institute of Environmantal Engineering
National Chial Tung University Abstract
The mesoporous adsorbent is an important subjest on nanotechnology because it has high specific surface area, and its pore size can be adjusted. But it’s expensive and therefore research on its application to air pollution control has been limmited. In this study mesoporous adsorbents are synthesized via liquid phase methods. The research topics include effects of (1) room temperature(RT) and hydrothermal(HT) synthesis (2) ethanol addition and (3) surfactant/silica molar ratio on the characteristic of mesoporous silica adsorbent and acetone adsorption. The acetone adsorption capacity was tested by thermogravimetric analysis(TGA).
The adsorbents synthesized by HT method have lower specific surface area than that synthesized by RT method, but their pore distribution is uniform and obvious crystal array. The acetone adsorption capacity of adsorbents synthesized by RT method is higher than that by HT method. When surfactant/silica molar ratio is 0.3 with ethanol addition, the highest specific surface area of adsorbent synthesized at room temperature achieved at is 1334 mP
2
P
/g, and when surfactant/silica molar ratio is 0.3 without ethanol addition, the highest acetone adsorption capacity of adsorbent synthesized at room temperature is achieved at 132 mg/g. Furthermore, the addition of ethanol reduces pore size of adsorbents. Addition of ethanol or not and change of surfactant/silica molar ratio have no especial relation to acetone adsorption capacity. Inferior quality of adsorbents damaged during repeated acetone adsorption-desorption test is in the sequence of ZSM-5 > RT03 > HTE03>HT03, so the synthesis method of HT03 may be the best prescription in this study.
致謝
兩年多的研究生活,既不長也不短,其中的點點滴滴將成為未來 的回憶盒子,成為一個人生道路上的里程碑。在這學習的過程中,除 了在課業或是專業領域上的知識更加深入外,同時也體悟了研究上所 需的創造巧思及研究精神,這其中的挫折與成就感之經歷過程是無法 比擬的。 能夠順利完成這本論文,指導老師的功不可沒,除了指引我研究 方向及實驗的問題討論,也包括論文的撰寫與修改,而口試當天的口 試委員,李壽南博士及張淑閔老師,則提醒我論文上的缺陷及不足, 提供各方面的建議使這本論文更盡善盡美,學生由衷感謝。 而在整整兩年多的學習過程中,最感謝的莫過於老師給予的幫 助,無論是研究上的指導或者是解決人生道路上的迷思,一路走來總 是點著明燈指引我方向,同時感謝李博士給我在各方面的資助以及鼓 勵,讓我更有動力完成學業。還有,這段期間與實驗室同仁們,育旨 學長、建志學長及錦德學長除了提點我在課業上遇到的困難外,亦常 指點我研究上的問題所在,並花心思幫助我解決實驗所遇到的瓶頸, 謝謝你們。文智、民谷、菁芳、成光及彥暉,還有已畢業的學長們郁 茗、偵紜及昱翬,讓我在實驗室感受到同樂與同學習的歡樂氣氛,使 研究生活的日子更添色彩,也很謝謝你們。 然後還要感謝我的家人,在背後支持我想走的路,能夠照自己想 做的去發展是最幸福的。亦感謝夜貓、八神、若雲、小緒、小茵、蘇 蘇及小賴等,還有其他同人界的朋友,支持我在課業以外發展畫圖的 興趣,很感謝你們! 尚有更多的未提及之背後英雄,因為有你們的幫忙,我才能很順 利的從這裡畢業,更多的感激之言此時此刻道不盡。目錄
TU 表目錄UT... vi TU 圖目錄UT... vii TU 第一章 前言與研究目的UT...1 TU 第二章 文獻回顧UT...3 TU 2.1 中孔洞材MCM-41 的基本特性UT...3 TU 2.2 MCM-41 的合成機制UT...4 TU 2.3 MCM-41 的製成方法UT...5 TU 2.3.1 水熱法及凝膠法UT...6 TU 2.3.2 常溫下合成UT...7 TU 2.3.3 其他UT...8 TU 2.4 製程因子對吸附材之影響UT...9 TU 2.4.1 添加乙醇對吸附材之影響UT...9 TU 2.4.2 改變界面活性劑對矽之莫耳比例對吸附材之影響T ...10U TU 2.5 MCM-41 對有機污染物的吸附特性及去除應用UT...11 TU 第三章 實驗方法UT... 24 TU 3.1 實驗所需之藥品及設備UT... 24 TU 3.1.1 實驗藥品UT...24 TU 3.1.2 實驗儀器設備UT...24 TU 3.2 實驗方法UT... 25TU 3.3.1 中孔洞沸石製成UT...25 TU 3.3.2 中孔洞沸石基本特性分析UT...27 TU 3.4 有機物吸附試驗UT... 33 TU 第四章 結果與討論UT... 41 TU 4.1 製程對吸附材特性之影響UT... 41 TU 4.1.1 製成方法對吸附材之特性的影響UT...41 TU 4.1.2 添加乙醇與否對吸附材特性之影響UT...45 TU 4.1.3 改變界面活性劑與矽莫耳比例對吸附材之特性的 影響UT...48 TU 4.2 吸附材對丙酮吸附測試UT... 50 TU 4.2.1 吸附材對丙酮之飽和吸附測試及初步篩選UT...50 UT 4.2.2 以熱重分析儀對吸附材進行反覆吸脫附試驗T....51U TU 4.3 吸附材成本估算UT... 53 TU 第五章 結論與建議UT... 75 TU 5.1 結論UT... 75 TU 5.2 建議UT... 77 TU 參考文獻UT... 78
表目錄
TU 表2-1 MCM-41 合成方法中水熱或凝膠法、室溫下合成及後合成法之 差異比較UT...14 TU 表2-2 水熱法合成MCM-41 之方法步驟差異比較UT...15 TU 表2-3 中孔洞材MCM-41 對有機物之吸脫附研究UT...16 TU 表3-1 三種合成吸附材方法於步驟中之差異比較UT...35 TU 表4-1 不同合成方法製成之吸附材命名UT...56 TU表4-2 參考Liu et al. (2003)製成的中孔洞沸石BET分析結果UT...56
TU 表 4-3 不同製程對吸附材之表面特性及丙酮的吸附容量影響之結果T ...57U TU 表4-4(a) 合成中孔洞材所需藥品總重與產物重量關係UT...58 TU 表4-4(b) 合成中孔洞材之成本初估UT...59
圖目錄
TU
圖2-1 由CUBU16UBUTMA/SiOUBU2UBU/HUBU2UBUO作為原料製成M41S的結構UT...18
TU 圖2-2 M41S中主要分類中孔洞材之 XRD圖UT...19 TU 圖2-3 MCM-41 的可能合成機制UT...20 TU 圖2-4 Si源與界面活性劑合成之機制示意圖UT...20 TU 圖2-5 添加乙醇與否與添加量對中孔洞材之孔洞影響UT...21 TU 圖2-6 乙醇添加量對吸附材之孔徑分佈影響UT...21 TU
圖2-7 Liu et al. (2003)所製成之MCM-41(E0)之TEM結果UT...22
TU
圖2-8 Liu et al. (2003)所製成之MCM-48(E20)之TEM結果UT...22
UT 圖2-9 製程中添加乙醇量多寡對中孔洞材之XRD繞射圖結果影響T.23U UT 圖2-10 全新與反覆再生後各吸附劑吸附丙酮之飽和吸附量比較T....23U TU 圖3-1 本研究之流程UT...36 TU 圖3-2 吸附劑之製程RT法流程示意圖UT...37 TU 圖3-3 吸附劑之製程HT法流程示意圖UT...38 TU 圖3-4 X-射線在結晶面間的繞射示意圖UT...39 UT 圖3-5 未進行鍛燒前RTE03 進行TGA測試其鍛燒前重量之變化T...40U TU 圖3-6 已鍛燒過RT04 進行TGA測試其鍛燒後重量之變化UT...40 TU圖 4-1(a) RT法中添加乙醇部分丙酮之飽和吸附量及比表面積與 Surfactant/Si莫耳比例關係UT...60 TU 圖4-1(b) RT法中無添加乙醇部分丙酮UT...60 TU 之飽和吸附量及比表面積與Surfactant/Si莫耳比例關係UT...60 TU圖 4-1(c) HT法中添加乙醇部份丙酮之飽和吸附量及比表面積與 Surfactant/Si莫耳比例關係...60
Surfactant/Si莫耳比例關係UT...60 TU 圖 4-2(a) 不同方法(RTE03;HTE03)添加乙醇下所製成吸附材之孔徑 分佈圖UT...61 TU 圖 4-2(b) 不同方法(RT03;HT03)無添加乙醇下所製成吸附材之孔徑 分佈圖UT...61 TU 圖4-3(a) RT03 之TEM照相結果UT...62 TU 圖4-3(b) HTE03 之TEM照相結果UT...62 TU 圖4-3(c) HT03 之TEM照相結果UT...63 TU 圖4-4(a) RT法製成之吸附材的XRD測試結果UT...64 TU 圖4-4(b) HT法製成之吸附材的XRD測試結果UT...65 TU 圖 4-5(a) RT法中添加乙醇與否(RTE03、RT03)吸附材之孔徑分佈圖T ...66U TU 圖 4-5(b) HT法中添加乙醇與否(HTE03、HT03)吸附材之孔徑分布圖T ...66U TU 圖 4-6(a) RT法中有添加乙醇(RTE02、RTE03、RTE04)吸附材之孔徑 分布圖,並與ZSM-5 比較UT...67 TU 圖4-6(c) HT法中添加乙醇(HTE02、HTE03、HTE04)吸附材之孔徑分 布圖,並與ZSM-5 比較UT...68 TU 圖4-6(d) HT法中無添加乙醇(HT02、HTNE03、NTNE04)吸附材之孔 徑分布圖,並與ZSM-5 比較UT...68 TU 圖4-7 吸附材之比表面積與丙酮飽和吸附量關係圖UT...69 TU 圖4-8 新鮮ZSM-5 對丙酮吸脫附之吸脫附重量變化UT...70 TU 圖4-9 新鮮RT03 對丙酮吸脫附之吸脫附重量變化UT...70 TU 圖4-10 吸附材經反覆吸脫附後之丙酮飽和吸附量UT...71 圖4-11 吸附材對丙酮之吸附指標...71
TU 圖4-12(b) ZSM-5 反覆吸脫附 1 次UT...72 TU 圖4-12(c)ZSM-5 反覆吸脫附 5 次UT...72 TU 圖4-12(d) 新鮮RT03UT...72 TU 圖4-12(e) RT03 反覆吸脫附 1 次UT...72 TU 圖4-12(f) RT03 反覆吸脫附 5 次UT...72 TU 圖4-12(g) 新鮮HTE03UT...73 TU 圖4-12(h) HTE03 反覆吸脫附 1 次UT...73 TU 圖4-12(i) HTE03 反覆吸脫附 5 次UT...73 TU 圖4-12(j) 新鮮HT03UT...73 TU 圖4-12(k) HT03 反覆吸脫附 1 次UT...73 TU 圖4-12(l) HT03 反覆吸脫附 5 次UT...73 TU 圖4-13(a) 不同製程中有添加乙醇部份之產率UT...74 TU 圖4-13(b) 不同製程中無添加乙醇部份之產率UT...74 TU 圖4-14(a)不同製程中有添加乙醇部份之成本UT...74 TU 圖4-14(b) 不同製程中無添加乙醇部份之成本UT...74T
第一章 前言與研究目的
自沸石問世後,由於其多孔徑結構與高比表面積,而普遍應用於 觸媒擔體及污染物的吸附回收等,加上再生率高於活性碳、於存放時 因不具有高著火性的安全考量(Khan and Ghoshal, 2000),已有漸漸以 沸石取代活性碳之趨勢。但是不管是觸媒領域或是吸附劑的應用,由 於沸石孔徑分佈不均,部分孔洞窄小使得大分子無法進入孔洞與觸媒 發生反應或是被吸附,而減低其沸石表面孔洞之利用率。因中孔洞沸 石型吸附材可視需要調整孔洞大小,加上其屬於奈米科技之研究範 疇,故成為現今常被研究討論的主題。 雖然投入中孔洞沸石的相關研究眾多,但多數文獻強調於其中的 製程產物之特性,較少針對中孔洞沸石應用於有機物吸附的探討,以 致於中孔洞沸石型吸附材於揮發性有機物研究方面的數據仍稍嫌不 足;另外,因中孔洞沸石的價格昂貴,造成其應用於空氣污染控制方 面之研究相當少。因此除了已知其有良好的吸附能力外,若更能減少 其製程所需材料與能源消耗,以降低其製造成本,此外目前使用沸石 多應用於沸石轉輪,已將半導體工業製成中之有機廢氣去除,但沸石 轉輪的年限取決於沸石本身的使用壽命,在不斷的進行吸附、脫附、 冷卻的循環中,對於沸石本身的結構會產生永久性的破壞,並且高沸 點之有機物會阻塞沸石之孔洞,加速沸石老化。本研究製成之中孔洞 沸石期可應用於沸石轉輪的範疇,因此探討其使用的壽命長短為商業 化過程中必得探討的問題,其牽涉到可否節省轉輪之經濟成本。若可 證實中孔洞沸石比一般沸石更具有反覆吸脫附的能力,則可大大的提 升中孔洞沸石型吸附材於應用上的價值。
因此本研究目的將探討製成上的不同對吸附材之特性以及吸附 能力的影響,詳細討論的細節如下: 1. 以(1)不同合成方法(2)添加乙醇與否(3)改變界面活性劑與矽的莫 耳比例,三種不同變因探討製成中孔洞沸石之特性及其材料成本 分析。 2. 討論上述不同變因對有機物吸附的影響。 3. 由前述實驗中找出測試結果較具代表性的數個中孔洞吸附材,進 行反覆吸脫附試驗,觀察吸附材劣化情況,以探討上述變因對吸 附材使用壽命的影響,並與商用沸石進行比較。
第二章 文獻回顧
本研究的主題在於探討製程中因子的改變對中孔洞材其特性及 對有機污染物的吸附效果的影響,並選用 MCM-41 作為研究重點。 因此本章將對其基本特性、常見的製成方式及對有機物吸附特性分別 敘述。2.1 中孔洞材 MCM-41 的基本特性
中 孔 洞 材 中 最 受 矚 目 的 是M41S 家 族 , 其 包 括 MCM-41 、 MCM-50 、 MCM-48 及 分 子 有 機 八 面 結 構 (molecular organic Octomer)(Davis and Burkett, 1995),辨別的方式之一就是其在結構上的明顯差異,MCM-41 一般具有規則六角晶形孔徑,MCM-48 是立方 體結構,MCM-50 為層狀結構,而分子有機八面結構其實為一個不穩 定結構,其個別結構如圖2-1,並由圖 2-2 瞭解M41S家族之孔洞排列 繞射圖的特性。其中最常被學者作為孔徑特性對吸附影響的討論的研 究主題是MCM-41(Selvam et al., 2001)。除了上述所提,MCM-41 因具 有規則排列的六角形或圓柱形孔洞的結構,且其製備容易,不需考慮 製成過程中孔洞形成的網狀組織或孔洞形成的阻塞現象,孔徑大小分 佈均勻,且孔徑大小經過良好的修飾及調整約可為1.5~20 nm,孔洞 體承受大小範圍很廣,比表面積可高達 700~1500 cmP 2 P /g,具有高吸 附容量、良好的熱穩定性、水熱穩定性及物理機械穩定性等優點,均 是MCM-41 會成為研究重點的原因。
2.2 MCM-41 的合成機制
MCM-41 的製成原理主要是由於帶正電端的有機界面活性劑在 溶液中會因具有一端疏水、另一端親水的性質,使在溶液中會聚集並 形成微胞的結構,當溶液中有帶負電的矽氧化合物時,則會取代親水 端原本的負電離子,藉此過程形成特殊的晶形結構。
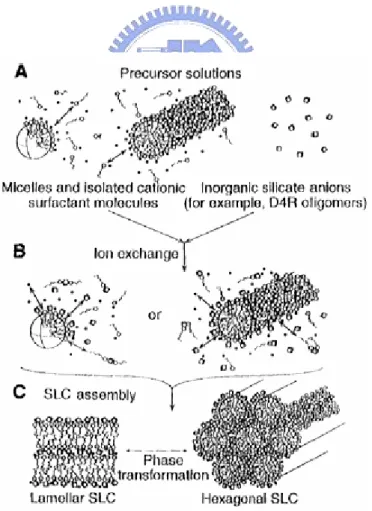
Beck et al. (1992)研究支持液晶相模板(Liquid crystal template)為 MCM-41 形成機制的理論,如圖 2-3 所示。MCM-41 形成的可能途徑 1,界面活性劑會先在溶液中聚集,如前述提及,因為界面活性劑的 兩端存在於水中的性質不同,因此疏水端的長鏈有機物會聚集而形成 微胞,露出親水的離子一端,在親水的一端主要為帶負電荷的陰離 子。而此微胞可能先濃縮或聚集自組裝(self-assembly)成稈狀的結構, 甚至可能形成六角晶形堆積的液晶相(Liquid Crystal Phase),當溶液中 一旦存在矽氧化物,因為原先界面活性劑所帶的親水端陰離子容易被 後來的矽氧化物所取代,因此最後矽氧化物便因此與界面活性劑因為 庫倫引力形成其特殊的六角晶形結構,此便為MCM-41 的前驅物質; 而在途徑2 中,則可能因為矽酸鹽的添加,則反而促使界面活性劑形 成的微胞直接自組裝成六角晶形結構。Øye et al. (2001)文中亦將中孔 洞 M41S 的合成分成兩個不同的途徑(1)矽或鋁矽化合物在前驅物溶 液中先形成液晶相(2)額外添加的無機物種多少會影響界面活性劑的 自組裝時的排列,其說法與Beck et al. (1992)相近。 但是Firouzi et al. (1995)對中孔洞沸石的合成過程中,界面活性 劑如何組裝成形以及矽氧化物如何規則排列,提出如圖2-4 的模式解 釋。其合成的步驟為:A. 在溶液中的界面活性劑先自行組裝成一個 微胞的桿狀結構,此時並未有六角晶形結構出現,然後B.當溶液裡有
溶液中添加矽源,則與界面活性劑之親水端離子進行離子交換,最後 C. 過程是進行矽酸鹽的液晶相組裝形成六角晶形或是層狀結構。 Forouzi et al. (1995) 與 Beck et al. (1992)及 Øye et al. (2001)理論的相 異處在於其認為溶液中僅存在界面活性劑時,並不會合成六角晶形的 結構,必須要有矽源存在才會發生。 因此於合成中孔洞沸石過程中,界面活性劑的存在將促成矽酸鹽 等矽源可以規則排列成管狀微胞的聚合物,矽酸鹽的 OH 端再彼此相 接合,而形成最後的異晶相結構,而界面活性劑的種類及碳鏈長度對 形成結構的影響於下一節說明。
2.3 MCM-41 的製成方法
表2-1 為較常見 MCM-41 的合成方法中水熱或凝膠法、室溫下合 成、氣相合成法及後合成法間差異的比較。在製成 MCM-41 的方式 中,又以為水熱法(Hydrothermal synthesis)及凝膠法(sol-gel)最普遍。 兩種方法的MCM-41 前驅物合成方式極為相似,水熱法是在過程中, 將適當合成比例的 MCM-41 混合攪拌後所得之前驅物膠體溶液置於 壓力鍋內,於特定溫度下反應一段時間,最後將所產生的沈澱物加以 過濾、烘乾、鍛燒;而凝膠法的配方不須在壓力鍋下反應合成,其餘 過程與水熱法並無太大差異,後續將兩者合併做介紹;另外,因為水 熱法或凝膠法於過程中可能需要加熱,因此亦有文獻研究發展出可在 常溫下合成中孔洞材,以下則將常溫下合成 MCM-41 之方法另外敘 述。2.3.1 水熱法及凝膠法 過去研究沸石的製成多以水熱法製備,因此在研究中孔洞沸石的 初期研究,亦是以水熱法及膠凝法為多數學者研究的對象,其主因之 一是由於能大量生產,這對於工業上的用途及供應需求有很大的優 勢。因水熱法或是凝膠法合成中孔洞沸石是目前最為普遍的方式,故 論及文獻不少,本研究將有涉獵到的文獻,簡述其中合成的差異性將 之整理至表2-2 中。 水熱法或是凝膠法的製成原理是將矽氧化合物作為矽源,並以烷 基類做為模版,在一定溫度下攪拌反應數小時形成結晶結構,然後過 濾、乾燥並鍛燒,而其中的比例調配或是選擇作為原料的藥品不同均 會影響生成的產物。以探討界面活性劑碳鏈長為例,Beck et al. (1992) 將 40g水、18.7g矽酸鈉與 1.2g硫酸先混合攪拌 10 分鐘,再以界面活 性劑/矽莫耳比例為 0.5 的比例添加入各種不同鏈長的界面活性劑 CBnBHB2n+1B(CHB3B)B3BNP + P ( 四 級 氨 鹽 界 面 活 性 劑 , Quaternary ammonium surfactants), n=8, 9, 10, 12, 14, 16,混合攪拌 0.5 小時,然後再加入 水20g,然後置於壓力鍋在 100℃反應 144 小時後過濾、烘乾並在 540 ℃下鍛燒,鍛燒期間前1 小時先通氮氣、後 6 小時再通空氣。實驗的 結果發現當界面活性劑的鏈長越長,其所得之孔徑大小越大,且可得 到對苯的吸附量(在 50 Torr)也隨之增高。 討論矽源跟水的比例對合成中孔洞材的影響,孫 (1995)等人採水 熱 方 法 , 將 一 定 比 例 的 水 、NaOH( 或 TMAOH) 、 界 面 活 性 劑 (CBnBH2Bn+1(CHB B3B)B3BNX, X=Cl, Br, n=12, 16),和適量的 1, 3, 5-三甲苯(MES) 混合,溶解後加入矽源或TEOS攪拌成一凝膠相,後裝入不銹鋼反應 槽,在110~160℃下進行水熱反應,產物經過濾乾燥後在 550℃下鍛
或是層狀,另外高水矽比亦可提升產物的比表面積。 2.3.2 常溫下合成 水熱法或是凝膠法為較常見的合成沸石方式,亦是合成MCM-41 初期研究常用的方法,但過程中因需控制溫度以及需在壓力鍋等密閉 環境下合成,在過程中增加控制變因,因此逐漸有學者探討若在常溫 下合成MCM-41,對產物結構、基本性質有哪些影響,並且若能在常 溫下合成所需之產物,亦可以減少中間過程中的能量消耗。 孫 (1995)等人除上述研究水熱法中,尚討論在室溫下合成中孔洞 材。作者是以不同比例的材料合成MCM-41,選用 TEOS 為矽源,與 水、界面活性劑及鹼下混合攪拌一段時間,再過濾、乾燥、鍛燒。實 驗結果,當在酸性環境下(pH≦1)及鹼性環境下(pH≧10)時,反應時 間大於0.5 小時,可得到中孔洞大小、六角晶形的產物,但是其所得 的孔徑遠小於以水熱法的方式合成。 Liu et al. (2003)在常溫下探討在製成中孔洞沸石時,醇類的濃度 及 種 類 對 產 物 的 晶 形 結 構 的 控 制 與 影 響 。 作 者 使 用 的 醇 類 有 CBnBHB2n+1BOH, n=1, 2, 3,以TEOS(Tetraethyl orthosilicate)作為矽源、
CTMABr(Cetyltrimethylammonium bromide)作為界面活性劑,在鹼性 環境下,合成中孔洞沸石的前驅物的溶液,再按照一般常見的程序, 攪拌反應2 小時、過濾、乾燥,最後鍛燒。當製成的樣品中無醇類的 添加時,則製成的中孔洞沸石經過TEM(穿透式電子顯微鏡)的照相觀 察,其形狀為規則排列的六角晶形,此符合MCM-41 的特徵之一,而 隨著醇類比例的增加,其實驗的結果,晶形會有以下變化MCM-41(六 角晶形)→MCM-48(正方體)→層狀(Lamellar)→輻射排列的六角封閉
Voegtlin et al. (1997)討論合成過程中,pH對產物的影響。配製方 法是將CTMABr溶於鹼性溶液,再將作為矽源的矽酸鈉加入,並以HCl 控制pH,在室溫下反應一段時間後進行過濾乾燥及鍛燒。討論的pH 為 8.5~12,當pH為 12 時,其產物經過 4 小時的鍛燒的程序後會產 生不規則的孔洞分佈,因為在高pH下,CTMABr/SiOB2B比例高,使得 陽離子與SiOB2PB -P 結合,進而減少矽酸鈉取代界面活性劑尖端的陰離子機 會,因此聚集性較不好。當pH控制在 8 時,除了孔徑大小符合中孔 洞外,吸附型態為type-Ⅳ,為典型的MCM-41。 2.3.3 其他 氣相合成法亦是另一項合成 MCM-41 的選擇,主要因為相較於 一般液相合成法,如水熱法或是凝膠法等,氣相合成法所需要之合成 時間短且迅速。較早期發展出氣相法的研究,是由Lu et al. (1999)提 出,氣相合成的原理是利用氣膠噴霧的方式將前軀物溶液霧化,霧化 過程中快速將前軀物溶液中之乙醇及水分揮發掉,促進自組裝,短時 間內可使中孔洞晶形結構形成,最後進入高溫鍛燒將做為模版之界面 活性劑趕出便形成中孔洞材。氣相合成法中的變因與液相合成法類 似,例如改變界面活性劑碳鏈長度(Lu et al., 1999;Fan et al., 2001) 及 添加膨化劑(Lu et al., 1999;Rao et al., 2002)可改變孔洞大小孔洞大 小、中孔洞的結構與特性。
其他合成MCM-41 的方法尚有後合成法(Post-synthesis),其是將 原先已製成的其他中孔洞沸石作為矽源,經過二次合成的水熱法程 序,使之結構轉為六角孔洞的 MCM-41。此程序以 Xia and Mokaya (2003)為例,進行試驗的中孔洞沸石有 HMS、SBA-15、MCM-48 等
進行水熱反應。其中SBA-15 製成的 MCM-41 的 XRD 圖譜接製成的 有很接近的尖峰(Peak)位置,BET 結果也都很相近,但 SEM 的結果 顯示形態明顯與直接合成的 MCM-41 有差異。另外,後合成法可以 提升MCM-41 的結構或是特性,像是 Inagaki et al. (2004)為了使後合 成法製程之MCM-41 具高熱穩定性,先將 ZSM-5 鹼化,接著再添加 CTMABr 合成中孔洞材,再將多餘之已鹼化的 ZSM-5 濾掉即可得到。 Lin et al. (2001)則是用後合成法增加 MCM-41 的熱穩定性、水熱穩定 性並且增加原本沸石之孔洞大小。其他關於後合成法可以參考表 2-1 中提及的其他文獻。
另外,除了上述的合成法外,尚有微波合成(Park et al., 1998;Park et al., 2004)及超音波法(Run et al., 2004),因較水熱或是凝膠法之合成
時間短,亦是現今合成MCM-41 方法中學者所感興趣的部分。
2.4 製程因子對吸附材之影響
於合成過程中,可改變的因子眾多,包括矽源、界面活性劑的選 用不同、pH、反應時間、鍛燒溫度及添加有機物等,皆可能改變吸 附材之孔洞大小及結構,進而影響吸附成效外。於本研究中所感興趣 的部分是界面活性劑與矽的比例、乙醇的添加對吸附材特性以及吸附 的影響,故後續論述部分將以此為重點。 2.4.1 添加乙醇對吸附材之影響 於液相合成中所添加的乙醇在整個液相合成中所扮演的角色一 直是爭論的議題之ㄧ。依據Zana et al. (1981)提出當乙醇於溶液中的於2.4 mole/L 時乙醇是作為共溶劑(cosolvent)。Tan and Rankin (2004) 探討添加乙醇多寡於對孔洞形成的影響,此可以由圖2-5 及圖 2-6 之 孔徑分佈圖說明。當無添加乙醇時,所形成之微胞以界面活性劑作為 模版,而乙醇穿插於界面活性劑之間(見圖 2-5(a)),因而增加了吸附 材之孔洞大小並使洞形狀為六角晶形;隨著乙醇添加量的增加,增加 界面活性劑之臨界微胞濃度,此時乙醇是為共溶劑,此時會促使疏水 端的部分容易聚集,因此形成之孔洞較無添加乙醇時小,而孔洞形狀 也由六角晶形轉變為立方體。另外,乙醇作為共溶劑時,當氯離子濃 度高 時 乙 醇 的 添 加 可 縮 短 形 成 中 孔洞材的時間(Lin H. P. et al., 2001)。Grün et al. (1999)則是發現在添加乙醇製成的 MCM-41 具有圓 球狀的外觀,亦同時可以縮短合成的時間,此特點對於擴大規模製造 MCM-41 很有助益。
其他文獻(Anderson et al., 1998;Lin et al., 1999;Liu et al., 2003)
亦提出乙醇的添加可以改變吸附材之孔洞大小,甚至根據 Lin et al. (1999)研究發現當界面活性劑碳鏈越長時,若要以醇類控制孔洞大 小,則醇類的碳數以較少的尤佳,但是對於界面活性劑碳數達 12 以 上時,使用乙醇甚至可改變中孔洞沸石之結構。與本研究參考文獻 Liu et al. (2003)作法中,論及將製成材料中增加乙醇一項,會使中孔 洞沸石型態由 MCM-41(圖 2-7)轉變成 MCM-48(圖 2-8)結構的結果相 符,而且其比表面積以添加乙醇時較高,其對孔洞晶格改變的影響也 可由圖2-9 看出,因此若應用於吸附揮發性有機物的成效而言,是否 有影響,是可以作為探討的。 2.4.2 改變界面活性劑對矽之莫耳比例對吸附材之影響
質對吸附的影響較為顯著,而合成材料中之界面活性劑的功用,是可 自組形成中孔洞沸石的液晶相結構,使矽源可以依照界面活性劑的結 構 形 成 所 需 的 晶 形 , 已 有 文 獻 提 出 改 變 界 面 活 性 劑 的 碳 鏈 長 度 (Nguyen et al., 1998;Beck et al., 1992)對孔洞大小的影響,進而影響 其吸附效能,因為當界面活性劑的碳鏈長度越長,其形成微胞的的直 徑越大,最後合成之中孔洞沸石其孔徑亦隨之增加。但針對同一種界 面活性劑,而合成的Surfactant/Si 的莫耳比例不同時,Chen and Wang (2002)文中討論當減小 Surfactant/Si 莫耳比例除了比表面積減小外, 孔洞體積跟晶格大小(d-space)亦有影響,另外吸附材對熱的穩定性有 提高現象。Liu et al. (2006)提出提高界面活性劑與矽莫耳比例將增加 中孔洞吸附材的比表面積及孔洞體積,但對孔徑大小並無影響,但提 高界面活性劑與矽之比例會妨礙MCM-41 的結構性(Mendonza et al., 2006)。Léonard et al. (2003)的研究結果發現,在水熱合成的過程中改 變界面活性劑與矽的莫耳比例,當莫耳比較低時會得到在 SEM 外觀 上為繩狀或是環狀狀聚集的MCM-41,但是高莫耳比時可以得到圓球 狀的聚集外形,另外與Liu et al. (2006)同樣的也發現界面活性劑與矽 的莫耳比例增加對於孔洞的大小改變並不顯著。
2.5 MCM-41 對有機污染物的吸附特性及去除應用
關於 MCM-41 對於有機物吸附的研究,整理如表 2-3。MCM-41對液態氮的吸附曲線一般呈現IUPAC(International Union of Pure and Applied Chemistry,國際純粹與應用化學聯合會)所定義的 typeⅣ型吸 附,表示其具有高度的多孔性質,但是對於有機物的吸附型態則可能 因吸附質及吸附溫度的不同,使得等溫吸附曲線可能因此具有差異。
MCM-41 對有機物吸附相較於其他吸附劑的優勢,Zhao et al. (1998)將 MCM-41 與 Y 沸石、活性碳對苯、四氯化碳、正己烷及水氣 進行吸附的試驗及比較,MCM-41 均有比其他文獻研究的吸附材較佳 的吸附結果呈現。Zhao et al. (2001)研究顯示 MCM-41 對極性的有機 物,如甲醇有較好的親和力。 Serrano et al. (2004)利用相同原料,不同製備方法—水熱及凝膠 法製成MCM-41,其對於相同的有機物吸附能力會有所差異,凝膠法 無論對甲苯、異丙醇及水的吸附容量均遠高於水熱法,另外凝膠法製 成的中孔洞沸石對此三種物種有較強的吸附能力。而且利用凝膠法製 成的中孔洞材對丙酮及異丙醇的吸附能力較好,但對水的吸附能力不 好,顯示其疏水的特性。 Nguyen et al. (1998) 探 討 不 同 界 面 活 性 劑 碳 鏈 長 度 製 成 之 MCM-41,討論乙醇及甲苯的吸附結果及滯化現象(hysteresis),實驗 結果發現當碳鏈長度由C=8 增加至 18 時,對苯的吸附型態會由 type Ⅰ轉為 typeⅣ,作者以 C=16 的界面活性劑製成之中孔洞材,在 0、 15、15℃對苯及乙醇進行吸脫附研究發現,雖然溫度變化對於單位重 量之吸附量的沒有明顯改變,但是在0℃時 MCM-41(C=16)對苯的吸 附會有滯化現象。Qiao et al. (2004)利用 C=10 至 C=18 鏈長的界面活 性劑製成孔洞大小2.4~4.2 nm 的 MCM-41,結果顯示隨著孔洞大小及 體積變大,正己烷吸附容量變高,另外當提升吸附溫度時,明顯降低 MCM-41 對正己烷之吸附量。 另外,沸石轉輪已應用於半導體工廠或是其他 VOC 污染源,使 用沸石的主要原因是為其具有可重複利用的優勢,但由林(2005)研究 結果顯示在重複進行10 次吸脫附試驗時,ZSM-5 沸石對於丙酮的吸
吸脫附期間,對於丙酮的吸附能力變化較小,其結果如圖2-10 所示。 此顯示在反覆吸脫附過程中 ZSM-5 比 HNZP 更快劣化導致對丙酮之 吸附量減少,可能之原因是含鋁之 ZSM-5 沸石於反覆吸脫附過程中 會催化丙酮形成積碳鍵物質,阻塞原先之吸附位置造成吸附效能降 低。 雖然 MCM-41 吸附有機物已有許多的相關論述及研究,但是截 至目前為止,利用製成之 MCM-41 於 VOCs 之進行反覆吸附測試研 究甚少,本研究即擬以液相法製成中孔洞材,並測試其吸附有機物的 效果與吸脫附的重複試驗。 另外在選用有機物作為研究方面,根據新竹科學園區歷年工廠採 樣結果顯示(行政院環保署,2002;張書豪和張木彬,1999),IC 產業 及光電產業所排放之主要空氣污染成分,大多以丙酮及IPA 為主,其 用途主要為顯影製成使用之光阻劑及去光阻劑,或是清洗基版的溶劑 (蘇茂豐,2003)。丙酮及 IPA 對於排放總量的貢獻程度大約在 50~80 %,其餘依工廠程度有異,如 2-丁酮、甲苯、二甲苯、乙酸丁酯、
propytlene glycol monomethylethy acetate(PGMEA)及三氯乙烷等。由
白等(2000)報告中丙酮佔半導體晶圓廠 VOCs 總排放量的最大比
例,加上已有文獻顯示 MCM-41 對其他苯、甲苯、乙醇、異丙醇的
研究(可參考表 2-3),對於吸附丙酮的研究尚鮮少,因此進行測試的 有機物故選用丙酮作為有機物的試驗。
表2-1 MCM-41 合成方法中水熱或凝膠法、室溫下合成及後合成法之差異比較 方法 水熱或凝膠法合成 室溫下合成 氣相合成法 後合成法 原理 將 矽 氧 化 合 物 作 為 矽 源,並以烷基類做為模 版,在一定溫度下攪拌反 應 數 小 時 形 成 結 晶 結 構,然後過濾、乾燥並鍛 燒。 將 矽 氧 化 合 物 作 為 矽 源,並以烷基類做為模 版,在室溫下攪拌反應數 小時形成結晶結構,然後 過濾、乾燥並鍛燒。 利用氣膠噴霧的方式 將含矽化物及烷基類 類模版的前軀物溶液 霧化,促進自組裝,短 時間內可使中孔洞晶 形結構形成,最後進行 鍛燒。 將原先已製成的其他 沸石作為矽源,經過二 次合成的水熱法程序 合成 MCM-41。 差異 1. 矽 源 種 類 多 為 含 矽 的藥品,天然的礦石 亦可以合成。 2. 合 成 通 常 控 制 在 一 定 溫 度 下(80 ~ 110 ℃)。 1. 矽 源 種 類 多 為 含 矽 的藥品,天然的礦石 亦可以合成。 2. 在室溫下合成。 1. 矽源種類多為含矽 的藥品。 2. 無乾燥及過濾的過 程。 主要為矽源是多為已 合成之其他種類沸石 或 結 構 不 規 律 的 沸 石,合成過程與前面兩 種無太大差異。 可參考之 文獻 Beck et al. (1992) 孫等(1995) 其他請參考表2-2 文獻 Voegtlin et al. (1997) Liu et al. (2003) Choma et al. (2005) 孫等(1995) Lu et al. (1999) Fan et al. ( 2001) Rao et al. (2002) Chen et al. (1999) Lin et al. (2001) Lin and Mou (2002) Xia and Mokaya (2003) Inagaki et al. (2004)
表2-2 水熱法合成 MCM-41 之方法步驟差異比較
參考文獻 合成莫耳比例或材料 合成溫度
及時間 pH 鍛燒條件或其他後續處裡方法
Sanhueza et al., 2006 SiOB2B/AlB2BOB3B = 8.86;
SiOB2АB 0.1CTABА0.10、0.25NaB2BO:250、330 HB2BO
110℃;48 小時 -- 600℃;6 小時
Liang et al., 2006 BTEE:a C18TABr:b C18-3-1:2.60 NaOH:
463 HB2BO(a:0~0.61;b:0~0.49)
95℃;3 天 -- 無鍛燒過程,但以乙醇及氯酸之
混合液將界面活性劑去除。
Mendonza et al., 2006 SiOB2:B 0.33, 0.66 CTAB:1.87、3.74 EthAc:240、
1000HB2BO
90℃; 3、10 天
9.5-11.0 600℃;20 小時
Gaydhankar et al., 2006 SiOB2B:0.24 CTMABr:0.25 TMAOH:26 HB2BO 110℃;
0~96 小時
-- 540℃;6 小時
Choma et al., 2005 1 TEOS:12.5 NHB4BOH:54 EtOH:x surfactant:
174 H2O,
where x = 0.54 M for C10,0.49 M for C12, 0.45 M for C14,0.41 M for C16,0.39 M for C18 100℃;5 天 -- 兩階段鍛燒: 1. 從室溫以 1.8 K/min 升溫到 550℃後停留 1 小時,並通以 氮氣鍛燒。 2. 隔天再以 1.8 K/min 升溫到 550℃後停留 5 小時,並通以 空氣斷燒。
Amama et al., 2005 1 SiOB2B:0.33 CTMAOH:81 HB2BO 100℃;6 天 11.5 兩階段鍛燒:
1. 從室溫升溫到 540℃後停留 1 小時,並通以氮氣鍛燒。 2. 再以 540℃後停留 6 小時,並
通以空氣斷燒。
Baute et al., 2005 1 TEOS:0.21 CTPB:3.9 NHB4BOH:126 HB2BO
1 TEOS:0.12 CTAB:2.4 NHB4BOH:74 HB2BO
先室溫下合成 4
h,再以 100℃水
熱5 天
表2-3 中孔洞材 MCM-41 對有機物之吸脫附研究(參考林(2005)重新彙整) 製成中孔洞材特性 有機物物種 飽和吸附量 比表面積(mP 2 P /g) 孔洞大小(nm) 等溫吸附型態 (測試溫度, K) 參考文獻 備註 甲醇 NA 985 2.95 NA Zhao et al. (2001) 乙醇 約6-15 mmol/g(273-303K) 937-1318 1.87-3.37 Ⅰ,Ⅳ(273-300) Nguyen et al. (1998) 不同碳鏈長C=8~18 界面活性劑 異丙醇 NA 914-1065 1.4-2.4 NA Serrano et al. (2004) 水熱法及凝膠法製備中孔洞材 約 3-9mmol/g(273-303 K) 937-1318 1.87-3.68 Ⅰ,Ⅳ(273-300) Nguyen et al. (1998) 不同碳鏈長C=8~18 界面活性劑 約700 mg/g(473K) 1060 2.25(PSD) Ⅳ(473) Zhao et al. (1998) NA 985 2.95 NA Zhao et al. (2001) 苯
NA 1160(無提及) NA Freunlidch(348-498) Choudhary and
Mantri (2000) 探討有機物發生在吸脫附動力 MCM 表面的
NA 914-1065 1.4-2.4 NA Serrano et al. (2004) 水熱法及凝膠法製備中孔洞材
甲苯
NA 1160(無提及) NA Freunlidch(348-498) Choudhary and
Mantri (2000)
探討有機物發生在MCM 表面的
吸脫附動力
p-二甲苯 NA 1160(無提及) NA Freunlidch(348-498) Choudhary and
Mantri (2000) 探討有機物發生在吸脫附動力 MCM 表面的 約1050 mg/g(473K) 1060 2.25(PSD) Ⅳ(473) Zhao et al. (1998) 四氯化碳 8-20 mmol/g(273-303K) NA 3.4(MPW) Ⅴ(273-303) Branton and Reynolds (1999)
三氯乙烯 NA 1100 2.72 Ⅳ(303.15~323.15) Lee et al. (2004) MCM-41 吸附 TCE 的動力模式
探討
約560 mg/g(473K) 1060 2.25(PSD) Ⅳ(473) Zhao et al. (1998)
NA 854~1180 3.0~9.3 Ⅳ(303) Trens et al. (2004) 討論不同孔洞大小之MCM-41 對 正己烷之吸附動力
環己烷 NA 985 2.95 NA Zhao et al. (2001)
Mesitylene NA 1160(無提及) NA Freunlidch(348-498) Choudhary and Mantri
(2000) 探討有機物發生在吸脫附動力 MCM 表面的
混合有機物 NA 1030 2.9 NA Wu et al. (2006) 針對MCM-41 對混合有機物種脫
附層析以對有機物之吸脫附狀況
註:中孔洞特性部分是由液態氮進行吸脫附試驗,後面無括號註明即是比表面積為BET 推估之值,孔洞大小為 BJH 推估之值 NA:無提及
PSD:pore size distribution MPW:mean pore width
圖2-1 由CB16BTMA/SiOB2B/HB2BO作為原料製成M41S的結構(Davis and Burkett,
1995)
Disordered rods MCM-41 MCM-48
Lamellar phase Octamer RO-CB16BTMA
圖2-2 M41S 中主要分類中孔洞材之 XRD 圖(a)無規則排列的 MCM-41(b) 規則排列之MCM-41(c)MCM-48(d)MCM-50(e)八面體結構(Selvam et al.,
圖2-3 MCM-41 的可能合成機制(Beck et al., 1992)
圖2-5 添加乙醇與否與添加量對中孔洞材之孔洞影響,正四面體維矽酸 鹽,橢圓為乙醇,長鏈狀分子為界面活性劑(a)無添加乙醇(b)添加少量之乙
醇(c)添加中等量之乙醇(d)添加大量之乙醇(Tan and Rankin, 2004)
圖2-6 乙醇添加量對吸附材之孔徑分佈影響(SP1:無添加乙醇;SP2~SP5
圖2-7 Liu et al. (2003)所製成之 MCM-41(E0)之 TEM 結果
圖 2-9 製程中添加乙醇量多寡對中孔洞材之 XRD 繞射圖結果影響,0~58 分別代表所添加的乙醇莫耳比例( Liu et al., 2003)
第三章 實驗方法
3.1 實驗所需之藥品及設備
3.1.1 實驗藥品
1. TEOS(Tetraethylorthosilicate):藥品級 98 %, Merck Co., Inc., Germany. 2. CTMABr(N-Cytyl-N, N, n-trimethyleammoniumbromide): 分析級 99 %,
Merck Co., Inc., Germany.
3. 乙醇:藥品級 95 %, 島久藥品株式會社, 日本. 4. 氨水:藥品級 28%, 和光純藥工業株式會社, 日本.
5. 丙酮:藥品級 99 %, Fisher Scientific International Co., UK. 6. 商用 ZSM-5 沸石:CBV5524G, 太欣實業公司.
3.1.2 實驗儀器設備
1. 去離子水製造機:Progard 2, MILLIPORE, USA. 2. 電磁攪拌器:Cimares2, Thermolyne, Lowa, USA. 3. 溫度控制器:Tungtec Instruments, CO., LTD. 4. 高溫爐:A-550, VULCAN, Japan.
5. 比 表 面 積 分 析 儀 (High Resolution Surface Area and Porosimetry Analyser):ASAP 2020, Micromeritics, USA.
6. 熱重分析儀(Thermogravimetric Analysis, TGA):TG 209 F1, NETZSCH, Germany.
8. X 光粉末散射儀(X-ray Powder Diffractomer, XRD):MXP18, MAC Sience, Japan, 清大貴儀中心.
3.2 實驗方法
整個實驗的架構如圖 3-1 所示。以不同製成方法、改變 Surfactant/Si 莫耳比例及添加乙醇與否為主而製成的中孔洞材。在改變Surfactant/Si 莫耳 比例部分,先參考Liu et al. (2003)的莫耳比例。製成中孔洞沸石後,除了以BET、XRD 及 TEM 進行基本的特性分析外,亦以 TGA 分析其對丙酮之
吸附效率。再由上述各項結果選出具有代表性的吸附材,以TGA 進行對丙 酮的反覆吸脫附試驗,測試重複使用該中孔洞材對於丙酮去除效率的影 響,最後將以上結果作一個比較。另外,為了瞭解成品產量的回收率高低, 因此將製成之樣品進行成本的初估。
3.3 中孔洞沸石製程與相關基本特性
3.3.1 中孔洞沸石製成 於本研究中,最初之合成吸附材的方法是參考Liu et al. (2003),是為 室溫凝膠合成法(簡稱 RT 法)。但此法製成之吸附材經由 TEM 照相結果及 XRD 的晶相繞射結果,判斷仍尚待改善空間,故自行發展出合成另一種無 過濾過程之高溫凝膠合成的方式(簡稱 HT 法)。兩種合成方法在步驟上的差 異列表於表3-1,詳細之合成步驟於下面分段敘述。 另外,於製程過程中,由於原本參考Liu et al. (2003)方法製程之吸附 材尚待改善空間,考量將溫度提升,希望可以改善吸附材之孔洞結構,將原本室溫凝膠合成法中合成的部分,改為在90℃合成 4 天,命名為有過濾 過程之高溫凝膠合成法(簡稱 H 法)。但此法製程之吸附材經 XRD 及 TEM 分析的結果仍不夠良好,且除了界面活性劑與矽之莫耳比例為 0.3 外的其 他比例,因為在合成過程中,未達四天水分便已蒸乾,因此無法達到高溫 加熱合成 4 天的過程,故僅成功製成界面活性劑與矽莫耳比例為 0.3 的吸 附材,但為明確比較出界面活性劑與矽莫耳比例及添加乙醇與否等因素對 吸附材特性差異及吸附能力的影響,故將此法不併入本研究的討論範圍, 但其各項特性及吸附結果列於附錄中供參考。 ---室溫凝膠合成法(簡稱 RT 法) 首先是參考Liu et al. (2003)之製成方法,如圖 3-2 所示。首先,取去離 子水95 mL、氨水 8.3 mL於燒杯中混合,再依照Surfactant/Si莫耳比例添加 入適量的CTMABr,然後在室溫下以電磁攪拌器攪拌 15 分鐘;接著再加入 8.8 mL的TEOS,並在室溫下攪拌使之反應 2 小時。停止攪拌後,再以抽濾 法收集原本溶液中產生的白色沈澱物,連同濾紙進入烘箱以 120℃乾燥; 於烘箱放置隔夜,確認完全乾燥後,以刮杓將固體物取下後,放至高溫爐 內於 550℃鍛燒 6 小時,鍛燒結束後,待回復室溫並取之收集保存於乾燥
箱內。合成比例為1 TEOS:0.2、0.3、0.4 CB16BTMABr:11 NHB3:B 0 or 20 alcohol:
144 HB2BO,以 0.2、0.3、0.4 莫耳的CB16BTMABr作為改變Surfactant/Si莫耳比例 變因,0 或 20 莫耳作為乙醇添加與否的變因。 於探討添加乙醇與否,根據Liu et al. (2003)的結果是在乙醇與矽莫耳 比例為 20 時,其結構會由原先沒有加乙醇的六角晶形變成立方體,即 MCM-48,因此為瞭解當結構改變時,對於丙酮的吸附能力影響,故除設 計 Surfactant/Si 莫耳比例的改變,另討論其添加乙醇與否對吸附丙酮的影
響。 --無過濾過程之高溫凝膠合成法(簡稱 HT 法) 其方法步驟如圖3-3 所示。首先取去離子水 95 mL、氨水 8.3 mL於燒 杯中混合,再依照Surfactant/Si比例添加入適量的CTMABr,然後在室溫下 以電磁攪拌器攪拌 30 分鐘,以確認將藥劑完全混合;接著再加入 8.8 mL 的TEOS,繼續攪拌 10 分鐘,接著以加熱器控制加熱板之溫度為 80℃加熱 並靜置1 小時,此步驟除了可使沸石凝膠合成(sol-gel synthesis)外亦可將酒 精慢慢趕出,最後將溶液放置 160℃烘箱內將溶液蒸發至乾,約時 6 小時; 最後將樣品放置高溫爐,以 550℃鍛燒 4 小時。其合成物種之比例與RT法
同樣為1 TEOS:0.2、0.3、0.4 CB16BTMABr:11 NHB3:B 0 or 20 alcohol:144 HB2BO,
而其所改變的變因亦相同。
3.3.2 中孔洞沸石基本特性分析
1. 高解析比表面積分析儀 (High Resolution Surface Area and Porosimetry Analyser, ASAP):
--BET 比表面積計算原理
表面積分析技術,是利用存在氣體分子與樣品表面之間的凡得瓦力作 用力,量測系統內的壓力因吸附現象的改變,進而推算出其表面積。 Brunauer,Emmett 及 Teller 於 1938 年提出了由 Langmuir isothermal 衍生為 多層分子等溫吸附關係公式,其是利用氣體吸附實驗所得到的數據來推算
樣品之表面積,簡稱為 BET 法。參考王及王(2003)彙整之比表面積的計算
使用氣體吸附法需要確定吸附氣體的量,即是恰好固體外表面與連通 之內表面覆蓋上單層氣體分子所需要的吸附氣體的量,量測的時候將放置 樣品的容器保持在某個固定溫度再放入吸附氣體,當吸附氣體在壓力P時達 到平衡時樣品之吸附量,並且對壓力p/pB0B作圖,即得到一條等溫吸附曲線。 單層吸附量nBmB計算公式為:
(
)
[
0]
0 0 1 1 / 1 / p p C n C C n p p n p p m m a ⋅ − + = − 其中p:與吸附態氣體達到平衡的吸附氣體壓力(Pa) pB0B:吸附氣體的飽和蒸汽壓(Pa) nBaB:所吸附的比數量(mol/g) nBmB:單層吸附量(mol/g) C:BET 參數 在BET的圖中將(p/pB0B)/{nBa[1-(p/pB B0B)]}為縱軸對橫軸p/pB0B作圖,在相對壓力 0.05 至 03 範圍內得到直線y=ax+b,其中a=(1/nBmBC),b=(C-1)/(nBmBC),a及b之 數值可由作圖或線性回歸求出。因此可計算出單層吸附容量nBmB為: b a nm + = 1 而樣品每單位質量之比表面積(aBsB)即可求得: L a n as = m m 其中L:亞佛加厥常數(1/mol) 由BET 表面分析,可以得知中孔洞材的表面特性,此為中孔洞材的吸 附能力好壞的初步鑑定,但仍須進行污染物的吸附測試才可判定中孔洞材 的真正吸附成效。--BET 孔洞體積大小計算原理(Webb and Orr, 1998) 以BET 法求取孔洞體積(V)大小,其原理為利用樣品單位吸附層厚度 對某壓力下之氣體飽和吸附量作圖,將每一單點作切線,隨單點數增加, 其斜率會趨於一個穩定值。此時孔洞體積即可藉由下列式子求得:
(
S
S
)(
t
t
)
K
V
n n⎥⎦
⎤
⎢⎣
⎡
−
+
=
+2
2 1 11 其中V: 孔洞體積 SBnB與SBn+1B:分別代表通過第n與n+1 個數值點上之切線斜率 tBn+1B與tBn B:分別為第n+1 與n個數值點之吸附層厚度 K:氣、液間體積轉換常數 --平均孔洞尺寸(D)計算: 平均孔洞尺寸計算是以 4 倍孔洞體積除以 BET 比表面積值求得,如 下式所示: sa
V
D
=
4
--BJH 孔洞體積計算BJH的孔洞大小(Da及Dd)的計算是採用BJH(Barrett、Joyner and Halenda) 的方法,文中內容參考曾(1999)的整理,此方法藉由數學上分段逐步積分的 方式由大孔洞向小孔洞的脫附,P/PP 0 P 由近於1 的值向小於 1 的方向來分析。 主要的基本計算公式計算方法,當相對壓力由(P/PP 0 P )B1B降低至(P/PP 0 P )B2B時, 則會發生脫附,其結果可以以下列方程表示:
(
) (
)
2 0 1 0 / /p p p p →(
)
1 1 1 2 2 1 1 2 1 1 1/ V r /r t ,r r t Vp ∆ = p k +∆ p = k + 1 1 1 R V VP = ∆ 其中(
)
2 1 1 2 1 1 r / r t R = p k +∆ 其中VBp1B代表孔洞體積,rBp1B為孔洞半徑,tB1B為吸附在其表面的物理吸附 層厚度,ΔVB1B當壓力變化時的脫附體積,rBk1B為在物理吸附層裡面,為發生 毛細現象的位置之孔洞半徑。 同理可以推論,若繼續降低相對壓力,依上列類推,當進行 n 個點的 壓力變化之數值,加上實際上樣品對每一種口徑的孔洞有相當多個,對於 某一口徑的一群而言,將式子修正為:∑
− = ∆ =∆ 1 1 n j cj n tn t A V 其中Acj 代表 n 個口徑的孔洞而言之吸附一層吸附分子的表面積(
)
2 2 \ / kn n pn n r r t R = +∆∑
− = ∆ − ∆ = 1 1 n j cj n n n n pn R V R t A V !Ac = Ap×rc/rp = Ap×(rp−tr)/rp = Ap×C rp表示在一個相對壓力下的平均半徑,rc為脫附前後半徑的平均,tr為 相應對壓力下的物理吸附層厚度,AC 為被脫附物理吸附層的平均表面積< AP 為孔洞的表面積 式子則表示為∑
− = ∆ − ∆ = 1 1 n j pj j n n n n pn R V R t C A V 其中C =(
rp−tr)
/rp 如此即可求得計算BJH 之孔洞體積。 --比表面特性符號說明因本研究以 ASAP2020 儀器所分析出之表面特性結果,其可得到比表 面積、孔洞大小及孔洞體積的結果,其符號說明如下:
D:Adsorption average pore width (4V/A by BET) Da:BJH adsorption average pore diameter(4Va/A) Dd:BJH desorption average pore diameter(4Vd/A) V:Single point adsorption total pore volume of pores Va:BJH adsorption cumulative volume of pores Vd:BJH desorption cumulative volume of pores
2. 穿透式電子顯微鏡(Transmission electron microscope, TEM):
穿透式電子顯微鏡是利用高中空下(10P -5 P torr)、陰極燈絲加熱(2600℃) 尖端釋放電子,並輔以加速電壓,多重聚光裝置,將電子束穿透試片,呈 像於螢光板上(王及王,2003)。藉由TEM的觀察,可以瞭解製成之中孔洞 沸石的孔洞結構形狀及差異,並可觀察出其孔徑大小及分佈情形。
3. X 光粉末散射儀(X-ray Powder Diffractometer, XRPD)
X 光散射儀的原理,即是當 X 光照射於一物體的表面時,除了會產生 反射光以外,並會透過物體表面,在下層的各層的結晶面位置產生反射光, 因為下層之反射光比上一層的反射光多走一段 CB-BD 距離(見圖 3-4),因 為反射光的行走距離不同,而使的光線產生布拉格繞射現象,其公式如下: θ λ 2dsin n = 其中當做為布拉格繞射計算時n=1 λ:入射光波長
θ:入射角 X 光粉末散射儀光譜,之所以可以鑑定結晶性物質的存在,是因為粉 末的某些角度之表面的結晶結構若是規律的成某平面排列,當X 光照射後 則會產生繞射現象。粉末內部的晶格排列情況皆會影響到會產生繞射的角 度及其強度,因此可觀察出不同樣品其中的晶格差異,並鑑定出某一結晶 物質的存在。為瞭解吸附材之孔洞結構上的差異,故本篇研究以低角度(2 θ=2~8°)的繞射角分析吸附材之孔洞晶格排列。
4. 熱重分析儀(Thermogravimetric Analysis, TGA):
本研究利用熱重分析儀量測吸附材之飽和吸附量,其原理是在吸附材 的吸附過程中,因吸附有機物而使吸附材增加重量,當達吸附飽和時,重 量的變化將會趨於平緩,而其間的重量差異即為飽和吸附量。除測量飽和 吸附以外,若將儀器溫控設定提升至某溫度,除可觀察吸附材之脫附情形, 亦可進行反覆吸脫附有機物脫附及吸附材重量的變化(詳見 3.4 節)。 另外,因為鍛燒中孔洞沸石時,會將界面活性劑於製成成品中脫除掉, 觀察脫除期間樣品的重量變化以判斷是否有完全將界面活性劑脫除。方法 是將溫度變化控制先以10 K/min 將溫度上升到 550℃,然後停留 1 小時後, 再以10 K/min 將溫度上升到 900℃,觀察於鍛燒其間的重量變化,此試驗 將驗證550℃、6 小時鍛燒過程中是否可將界面活性劑完全趕出。以 RTE03 及RT04 之樣品為測試對象,結果如圖 3-5 及圖 3-6,由圖 3-5 之 RTE03 未 鍛燒的樣品在溫度未達550℃時重量便已明顯減少,後再維持 550 1℃ 小時 期間,重量的變化微小,故界面活性劑CTMABr 可以在進行鍛燒 6 小時期 間可完全趕出。見圖 3-6 之 RT04,該樣品是已鍛燒後的成品,其在整個測 試過程中,重量的變化相當微小,表示鍛燒過程中確實已將界面活性劑趕
出。
3.4 有機物吸附試驗
本研究過程中,主要將利用 TGA 測試出製成之中孔洞沸石對丙酮的飽 和吸附量。實驗開始前樣品先在烘箱以 120℃乾燥至少 1 小時,後取適量 之樣品放置 TGA 坩鍋內,接著先將溫度由室溫以 40℃/min 升至目標之吸 附溫度 45℃,當溫度達到 45℃後先停留一分鐘後再通以流量為 20 ccm 的 丙酮(濃度約為 15000 ppm)氣體進入系統,在固定的溫度為 45 ℃進行吸附 試驗,吸附時間為 1 小時,一旦吸附材與丙酮開始進行吸附時,吸附材重 量會逐漸向上升,一段時間後因吸附材已對丙酮達吸附飽和,故重量不再 改變,利用重量的改變差異經過換算,便可得到吸附材的飽和吸附容量, 藉此探討中孔洞材對丙酮的飽和吸附容量。 除了以TGA 對製成之吸附材進行飽和吸附量之測試外,根據前述測試 結果從中選出幾個樣品,進行反覆吸脫附之測試,試了解樣品於反覆吸脫 附過程中劣化情形,並與商用沸石 ZSM-5 比較。由張豐堂(2004)研究中, 對沸石轉輪進行不同溫度的脫附實驗,當溫度達 210℃時得到良好之脫附 效果 ,亦可使後續易冷卻轉輪溫度以利於進行下一次吸附,但由文中之實 驗結果,在180℃脫附結果略遜 210℃,且溫度越低對能源的消耗越少,故 脫附溫度選定為 200℃。進行反覆吸脫時,前面吸附部分的處理如同上段 提及,經過45℃等溫吸附 1 小時後,將停止通入丙酮氣體,經後一分鐘後 再將溫度以 40℃/min 升至 200℃,在升溫的過程中,丙酮已部分脫附,當 溫度上升至 200℃後仍持續脫附。另外,為了可在短時間內看出在反覆吸 脫附的過程中對吸附材的破壞,故將脫附時間定為24 小時,藉由高溫、長時間的環境下加速吸附材結構的破壞,並可縮短整個實驗時程,方便立即 比較出吸附材間之優劣。
表3-1 三種合成吸附材方法於步驟中之差異比較 步驟 方法 室溫凝膠合成法 (RT 法) 無過濾之高溫凝膠合成法 (HT 法) 藥劑添加時 之條件 當添加入水、CTMABr 及 氨(及乙醇)後先攪拌 15 分 鐘,再加入TEOS 當添加入水、CTMABr 及氨 (及乙醇)後先攪拌 10 分鐘, 再加入TEOS 合成過程 室溫下攪拌 2 小時 在室溫下攪拌10 分鐘後,在 80℃下攪拌 1 小時 過濾 有 無 烘乾 120℃下隔夜乾燥 直接以 160℃維持 6 小時, 將溶液完全蒸發至乾 鍛燒 550℃、6 小時 550℃、4 小時
二種製程方法 (RT法、HT法) 添加乙醇與否 改變界面活性劑與矽之莫耳比例 不同方法製成吸附材 吸附材基本特性探討 1. 表面特性 2. 孔洞分佈 3. 晶格結構 不同製程的吸附材對丙酮 之吸附影響探討 選出具代表性之樣品 對丙酮進行反覆吸脫附 1. 探討不同製程的吸附 材在反覆吸脫附過程中 劣化情況 2. 與商用沸石比較 結果比較與討論 對製成之樣品計算其成本 並進行比較 圖3-1 本研究之流程
DI water 95 mL
Ammonia 8.3 ml
CTMABr
With/without ethanol 46 ml
Stirring for 15 min
E-2
8.8 ml TEOS
Stirring for 2h
PumpFiltration
Drying at 120℃
overnight
Calcination at
550 ℃ for 6h
高溫爐 圖3-2 吸附劑之製程 RT 法流程示意圖圖3-5 未進行鍛燒前 RTE03 進行 TGA 測試其鍛燒前重量之變化
第四章 結果與討論
本研究之研究目的,即是探討(1)不同合成方法(2)乙醇添加與否(3) 不同的界面活性劑與矽的莫耳比例製成中孔洞沸石,依不同製成方法 的吸附材,探討吸附材之基本特性及對有機物的吸附的影響。 表4-1 為不同合成方法製成之吸附材的代號說明。變因包括不同 製成方法、添加乙醇與否、改變Surfactant/Si 莫耳比例,為方便閱讀, 故將目前樣品以各種代號敘述。室溫凝膠合成法(簡稱 RT 法)的樣品 皆命名開頭為RT(取自 Room temperature 的 RT),有添加乙醇之樣品 命名在RT 後面加上 E(取自於乙醇之英文 Ethanol 的 E),無添加乙醇之樣品在 RT 後面無 E 字樣;無過濾之高溫凝膠合成法(簡稱 HT 法) 命名皆開頭為HT (取自 Hydrothermal 中之 HT),有無添加乙醇的命名 方式比照室溫凝膠合成法。
4.1 製程對吸附材特性之影響
本節將利用比表面積分析儀對吸附材之分析結果來討論不同製 程對吸附材之比表面積、孔洞大小及孔徑分佈的影響,以穿透式顯微 鏡觀察吸附材之孔洞形狀及分佈情形,並以 X 光粉末繞射儀分析吸 附材的孔洞結構排列。 4.1.1 製成方法對吸附材之特性的影響 4.1.1.1對吸附材之比表面積及孔洞大小分佈之影響
室溫凝膠合成法(RT 法)是根據文獻 Liu et al. (2003)製成之方法,其RT 法的吸附材比表面積較低,且無論是平均孔洞及 BJH 計算出來 之孔洞均比所文獻製成之吸附材孔徑還大,推測可能的原因是製成的 過程中,對於鍛燒的溫控均無作層溫控制,僅在當溫度達550℃時便 直接鍛燒,界面活性劑及其他未反應等物質直接除去,很可能使結構 瞬間崩毀,此可能會影響產物的結構及孔洞,致使比表面積減少,不 過RT 法製成之吸附材仍具有相當高的比表面積,其孔洞大小亦符合 IUPAC 對中孔洞材質的定義。 表 4-3 是RT法及HT法所製成之吸附材之表面特性。由表 4-3 比 較不同製程方法中有添加乙醇部份之RTE03 與HTE03,RTE03 有較高 之比表面積1334 mP 2 P /g,但HTE03 得到的平均孔洞 3.5 nm較大;比較 無添加乙醇部份RT03 及HT03,與有添加乙醇相同的結論是,RT法製 成之RT03 同為比表面積較高的吸附材,而平均孔洞是HT03 較大。整 體來說,因為HT法在製程中改為高溫合成的過程,故可使結晶長大, 形成孔洞較大的結構,因此比表面積也較低,此與文獻結果一致 (Chen et al., 1997;Grün et al., 1999;孫等,1995),亦即在常溫下合 成沸石其孔徑大小較有經過水熱的高溫合成過程為小,但比表面積較 高溫合成為大(Choma et al., 2005) 。但由表 4-3 的結果觀察,兩種製 成方法的差異對總孔洞體積沒有明顯的影響趨勢。 將表4-3 的結果比表面積部分彙整成圖 4-1(a)~4-1(d),而從本研 究吸附材之 BET 比表面分析結果,比照圖 4-1(a)、圖 4-1(b)及圖 4-1(c)、圖 4-1(d),更明顯顯示出 RT 法比表面積高於 HT 法,且表 4-3 顯示 RT 法之吸附材之平均孔徑大小較小於 HT 法之吸附材,但是此 項結果與Igarashi et al. (2003)的比表面積及孔洞大小結果矛盾。 比較2 種製成方法之孔徑分佈圖,有添加乙醇見圖 4-2(a),無添
在 2.5 nm 出現一明顯波峰,樣品 RTE03 及 RT03 之孔洞分佈均小於 儀器分析範圍內,故無法判斷其主要粒徑分佈大小,但由趨勢可推測 其應該在在微孔洞範圍。由此結果可知,HT 法製成之吸附材存在中 孔範圍的孔洞,但依照圖 4-2(a)及圖 4-2(b)的波峰左側趨勢,仍顯示 HT 法製成之吸附材仍可能有微孔洞存在;而 RT 法之孔徑分佈可能 大部分落在微孔範圍。由圖4-2(a)的結果,HTE03 在中孔的孔洞體積
比 RTE03 多,但 HTE03 的總孔洞體積又比 RTE03 小,因此可推論 RTE03 在微孔部分的分佈比 HTE03 來的顯著;同樣 RT03 及 HT03 亦有相同的情況,此顯示以 HT 法製成之吸附材之孔洞較大。整體來 說HT 法的 D 較 RT 法的吸附材大,因為孔徑分佈的結果中 HT 法在 中孔洞的範圍有粒徑分佈,因此計算出來之平均孔洞大小較 RT 為 大。由孔徑分布圖之結果顯示HT 法中可以使吸附材於合成的過程中 增加聚合的機會,而形成吸附材的孔洞較大。 但是經計算出來的平均孔洞大小與孔徑分佈仍有相當之落差,表 4-3 的 RT 法的孔洞大小之計算結果在中孔範圍,但孔洞分佈卻落在 微孔範圍,而HT 法計算出來之平均孔洞大小亦比孔徑分布圖顯示之 結果大,且由表4-3 的 D、Da 及 Dd 結果以及 V、Va 及 Vd 的結果, 除了RT04、HTE04 及 HT04 的 Da 及 Dd、Va 及 Vd 相當接近以外, 其餘吸附材均不一致,可能因為其他吸附材之孔洞大小分佈不均,因 此所計算出來的平均孔洞大小無法與孔徑大小分佈圖相呼應。 4.1.1.2
對吸附材之孔洞結構的影響
Liu et al. (2003)製成的吸附材可得到均勻的孔洞分佈,其中有添 加乙醇之吸附材具有立方體的結構,為似 MCM-48(圖 2-8);無添加 乙醇之孔洞形狀為六角晶形是為典型之 MCM-41 的孔洞形狀(圖2-7)。將 RT03 與 RT 法所參考文獻 Liu et al. (2003)的結果圖 2-7 比較, 兩者吸附材同樣亦是在不添加乙醇及 Surfactnat/Si 莫耳比例為 0.3 的 情況下製成,RT03 的 TEM 照相結果(見圖 4-3(a))發現其孔洞大小並 不均勻,亦發現其孔洞形成並非二維的方向。自行研究出之HT 法製 程的HTE03,TEM 之照相結果如圖 4-3(b),其具有均勻的孔洞分佈, 顯示HT 法的製成過程中可以使沸石的長晶較為完整,推測 HT 法其 在合成過程中,先在 80℃過程中使之靜置使之緩慢將酒精脫除並繼 續結晶,後繼續在160℃將水蒸發至乾過程中使結晶成形,故孔洞較 為均勻。 4.1.1.3
對吸附材之孔洞晶格的影響
本研究製成吸附材之XRD 如圖 4-4(a)及圖 4-4(b)所示。本研究中 RT 法(圖 4-4(a))製成之吸附材其孔洞可能沒有特定的晶面排列,因此 XRD 沒有特別明顯的尖峰出現,尤其在製成樣品中有添加乙醇的部 分,其 XRD 的分析結果峰值遠比無添加乙醇部分更不明顯,但仍顯 示乙醇的添加會使晶格結構改變。另外,比較 RT 法中的 RTE03 及 RT03 與 Liu et al. (2003)的圖 2-9 結果,RT 法製成的樣品其 XRD 不若 Liu et al. (2003)中的繞射波峰明顯外,出現繞射的角度也不相同。 將RTE03、HTE03 之 XRD 結果比較,顯示 HTE03 在 2θ=2.56° 時有明顯的繞射波峰出現,而 RTE03 皆無任何較明顯之波峰出現; 在不添加乙醇的部分,比較不同方法製程之吸附材 RT03 及 HT03, 由圖4-4(b)顯示結果,HT03 在 2θ=2.16°、2.18°有非常明顯的繞射波 峰,RT03 雖然在 2θ=2.26 及 2.28°有峰值出現,但是波峰不大,顯 示不添加乙醇製程之吸附材在 2θ=2~3°間可以有較明顯之孔洞排 HT 法製成的 HT03 也具有良好的孔洞結構。以上之結果,顯示HT 法確實可以使吸附材在合成過程中長晶較為均勻,此與 TEM 的照相結果可以呼應。 由圖 4-4(a)及圖 4-4(b)的結果,除了呈現高溫凝膠過程可以使晶 格排列更為明顯外,由不添加乙醇的結果,HT03 出現的波峰比RT法 製成之其他吸附材小,而根據HT04 的趨勢,其所出現的晶格波峰角 度已低於儀器偵測極限,此與Choma et al. (2005)所得到之XRD分析有 相似的結果,亦即高溫合成的過程會使XRD的出現繞射波峰dB100B的位 置變小。 由上述結果得知,HT 法的 TEM 照相結果顯示有很均勻的孔洞 分佈,且呈現六角晶形孔洞形狀;RT 法的吸附材照相結果呈現孔洞 不均勻且無特定之形狀可以定義,可能其孔洞之排列不均一,故XRD 的繞射結果中並無明顯的孔洞結構。 HT 法與 RT 法間的差異除了在於合成溫度不同以外,HT 法也減 少過濾的步驟,在Chen et al. (1997)提及過濾為合成中孔洞吸附材之 首要步驟,此步驟可將於合成中多餘的離子去除並使孔洞結構更加完 整。但於本研究的吸附材 XRD 圖結果,反而是 HT 法的孔洞結構較 為明顯,且由目前的數據無法斷定有無過濾後,其合成過程中多餘的 離子及矽酸鹽對孔洞結構是否有影響。 4.1.2 添加乙醇與否對吸附材特性之影響 4.1.2.1
對吸附材之比表面積及孔洞大小分佈的影響
比較表 4-3 中 RT 法中有無添加乙醇的差異,其比表面積及 Dd 的孔洞變化與乙醇添加與否無一定的關係,但是平均孔洞大小 D 以 無添加乙醇的樣品較大,同樣的情況亦發生在HT 法,因此合成吸附2004)。另外,根據 Tan and Rankin (2004)說法,在無添加乙醇時,乙 醇是作為共界面活性劑,可使製成之吸附材孔洞較大,而當添加乙醇
時則作為共溶劑使吸附材孔洞較小,於表4-3 及上述的討論的得知,
在有添加乙醇時推測其乙醇是作為共溶劑之用途,與Tan and Rankin
(2004)說法一致,但 Liu et al. (2003)結果其製成過程中有無添加乙醇 與否對其孔洞之影響不顯著。因此由比表面積分析的結果,添加乙醇 與否雖會影響吸附材的表面特性,但除了平均孔徑大小有明顯的影響 趨勢,與比表面積並無明顯關係。 討論添加乙醇與否對吸附材之孔徑分佈影響,見圖4-5(a),RT法 因為無波峰出現,故無法判斷添加乙醇與否對孔徑分佈的影響,但由 圖所呈現的趨勢,推測不添加乙醇製成之RT03 的主要粒徑分佈之粒 徑可能大於添加乙醇製成之RTE03,與表 4-3 中平均孔洞大小HT03 比HTE03 大的結果相符;由圖 4-5(b)的HT法顯示HTE03 與HT03 的比 較,添加乙醇與否並無明顯影響在中孔洞範圍內之波峰分佈出現位置 (皆約 2.5 nm),不添加乙醇但仍些微使在中孔部份的孔洞體積增加, 但由圖的左側趨勢判斷,仍有多數孔洞的大小落在微孔範圍,且由表 4-3 的HTE03 及HT03 的V結果,HT03 的V比HTE03 多 0.042 cmP 3 P /g, 此數值比圖 4-5(b)中顯示之粒徑分佈之面積大(面積是利用三角形法 粗略計算,即為孔洞體積),故可推測微孔部分可能也受到添加乙醇 與否的影響。 4.1.2.2
對吸附材之孔洞結構的影響
由RT 法製成之 RT03 的 TEM 照相結果無得到分佈均勻的孔洞分 佈,且在 XRD 晶格分析的結果,其孔洞結構表現不夠明顯,而根據 HT 法製成之 HTE03 及 HT03 的 XRD 結果,兩者均有孔洞結構明顯的表現(可見 4.1.2.3 節說明),因此欲觀查 HT 法中添加乙醇與否對孔
洞分佈及影響。見圖4-3(b),HTE03 得到相當均勻的孔洞分佈,且孔
洞形狀為六角晶形(Liu et al., 2003;Beck et al., 1992);圖 4-3(c)為 HT03
的 TEM 照相結果,圖中顯示孔洞分佈均勻,但因 TEM 照相時拍攝 角度差異無法明顯判斷出為何種孔洞形狀。而由 HT 法中之 HTE03 及 HT03 的 TEM 照相結果顯示添加乙醇與否對孔洞分佈及形狀影響 不明顯。 4.1.2.3