國 立 交 通 大 學
材料科學與工程學系
碩 士 論 文
氧化鋅奈米結構之合成及其應用
Synthesis and Appications of Zinc Oxide
Nanostructures
研究生: 許守仁
指導教授: 林宏洲 博士
中華民國九十七年八月
氧化鋅奈米結構之合成及其應用
Synthesis and Appications of Zinc Oxide Nanostructures
研 究 生: 許守仁 Student: Shou-Jen Hsu
指導教授: 林宏洲 博士 Advisor: Dr. Hong-Cheu Lin
國 立 交 通 大 學
材 料 科 學 與 工 程 學 系
碩 士 論 文
A Thesis
Submitted Department of Materials Science and Engineering College of Engineering
National Chiao Tung University In partial Fulfillment of The Requirments
For The Degree of Master of Science In Materials Science and Engineering
Aug 2008
Hsinchu, Taiwan, Republic of China
誌謝
首先要誠摯的感謝指導教授林宏洲老師悉心的教導,使我得以一 窺材料科學領域之堂奧,不時的討論並指引我正確的方向,使我在這 短短的兩年中獲益匪淺。另外也要感謝黃華宗博士、呂世源博士、陳 煌銘博士在百忙之中能抽空擔任我的口試委員,因為有您的幫忙,使 得本論文能夠更臻完整而嚴謹。 兩年裡的日子,實驗室裡共同的生活點滴,學術研究上的討論、 言不及義的八卦閒扯…,都需感謝眾位學長姐、同學、學弟妹的共同 砥礪,你們的陪伴讓兩年的研究生活變得絢麗多彩。首先要感謝博仁 學長對我的細心教導,光潔、宗琦、詠哥、威宏、曉萍學長姊在實驗 上的鼎力相助,另外也要感謝阿之學長在 TEM 上的協助,還有陪著 我一路走來的同學柏儒、捷茵。此外也要感謝明益、瑜玲、家瑋、秀 帆、老魏等學弟妹,有你們的陪伴讓我研究所的生活更加豐富有趣。 Nathan、Hari、Sahu、Pilu、Sata 等印度同學,除了實驗上的幫忙外, 更是為實驗室帶來了許多歡樂。 兩年的光景匆匆而逝,回想過去,雖然過程是悲喜交加,但結果 卻是如此美好。要感謝的人太多了,那不如就謝天吧!Synthesis and Applications of Zinc Oxide Nanostructures
Graduate student: Shou-Jen Hsu Advisor: Dr. Hong-Cheu Lin
Department of Materials Science and Engineering
National Chiao Tung University
Abstract
Zinc oxide nanoparticles with different sizes and zinc oxide
nanorods with various aspect ratios have been synthesized with varying reaction conditions and identified by UV-vis spectroscopy, powder X-ray diffraction, and transmission electron microscopy. The methacrylate-modified ZnO nanoparticles used together with a photocurable monomer in the optically compensated bend (OCB) mode liquid crystal display shows an improving critical voltage. The silane coupling agent with pyridyl group has been synthesized successfully. Pyridyl-modified ZnO nanoparticles and nanorods have been self-assembled to a liquid crystalline homopolymer with smectic C phase through hydrogen bonding. The resulting supramolecular structures were characterized by polarized optical microscopy and X-ray diffraction.
氧化鋅奈米結構之合成及其應用
研究生:許守仁 指導教授:林宏洲
國立交通大學材料科學與工程研究所
摘要
本實驗成功的合成出具有不同粒徑大小之氧化鋅奈米粒子及不 同長寬比之氧化鋅奈米棒,並藉由紫外-可見光光譜、X-ray 粉末繞射 及穿透式電子顯微鏡鑑定其性質。接著將含有甲基壓克力基的表面改 值劑及合成出之含有砒啶基的表面改值劑接上氧化鋅奈米結構之表 面。其中將甲基壓克力基改值過後之氧化鋅奈米粒子與光聚合性單體 應用於光學彎曲補償液晶顯示模組,若在照光期間施以不同的電壓, 可發現其臨界電壓能有效的降低。將砒啶基改值過後之氧化鋅奈米粒 子及奈米棒與含有苯酸基之層列相液晶高分子形成氫鍵型分子結構 後,經由偏光顯微鏡及 X-ray 粉末繞射得以鑑定其液晶分子之排列行 為。目錄 第一章 序論--- 1 1-1 前言及奈米氧化鋅介紹--- 2 1-1-1 奈米氧化鋅之發光性質--- 3 1-1-2 奈米氧化鋅之應用性--- 4 1-2 文獻回顧--- 6 1-2-1 氧化鋅奈米結構的製備--- 6 1-2-1-1 氧化鋅奈米粒子的製備--- 6 1-2-2 奈米氧化鋅的表面改質--- 16 1-2-3 液晶簡介--- 20 1-2-3-1 液晶分類--- 20 1-2-3-2 液晶性質--- 22 1-2-3-3 液晶相的觀察與鑑定--- 25
1-2-3-4 高分子穩定型液晶 (Polymer Stablized Liquid Crystal)--- 26
1-3 研究動機--- 29
第二章 實驗部份--- 31
2-1 實驗儀器--- 32
2-2 實驗藥品--- 35
2-3-1 合成不同大小之氧化鋅奈米粒子--- 37 2-3-2 合成不同長度之氧化鋅奈米棒--- 37 2-3-3 合成含雙甲基壓克力基之照光聚合單體--- 38 2-3-4 合成含砒啶表面改質劑之氫鍵質子受體--- 39 2-3-5 合成具層列相之液晶高分子氫鍵質子予體--- 44 2-3-4 氧化鋅奈米結構之表面改值--- 46 2-3-4-1 合成甲基壓克力基表面改值之氧化鋅奈米粒子--- 46 2-3-4-2 合成砒啶基表面改值之氧化鋅奈米粒子與奈米棒--- 47 2-4 光電量測方法及裝置
---
47 第三章 結果與討論--- 49 3-1 氧化鋅奈米粒子性質討論--- 50 3-1-1 紫外-可見光光譜及螢光光譜性質結果--- 50 3-1-2 X-ray 粉末繞射結果--- 52 3-1-3 穿透式電子顯微鏡分析--- 54 3-2 氧化鋅奈米棒性質討論--- 55 3-2-1 紫外-可見光光譜及螢光光譜性質結果--- 55 3-2-2 穿透式電子顯微鏡分析--- 56 3-2-3 X-ray 粉末繞射結果--- 59 3-3 氧化鋅奈米粒子應用於光學彎曲補償(Optically CompensatedBend Mode)液晶顯示模組之探討--- 61 3-3-1 甲基壓克力基表面改質前後之奈米氧化鋅性質討論--- 61 3-3-1-1 紫外-可見光光譜及螢光光譜性質結果--- 61 3-3-1-2 熱重分析--- 62 3-3-1-3 紅外線光譜分析--- 62 3-3-2 照光期間施以不同電壓對光電性質的影響--- 63 3-4 氫鍵型奈米氧化鋅與高分子液晶複合材料性質探討--- 68 3-4-1 層列相液晶高分子 PBBBA 之性質探討--- 68 3-4-1-1 紫外-可見光光譜及螢光光譜性質結果--- 68 3-4-1-1 熱性質結果--- 69 3-4-1-2 X-ray 粉末繞射結果--- 71 3-4-2 砒啶表面改質後之奈米氧化鋅性質討論--- 73 3-4-2-1 熱重分析--- 73 3-4-2-2 紅外線光譜分析--- 75 3-4-3 氫鍵型奈米氧化鋅與高分子液晶複合材料的製備與分析---- 76 3-4-3-1 紅外線光譜分析--- 77 3-4-4 氫鍵型奈米氧化鋅與高分子液晶複合材料之性質探討--- 80 3-4-4-1 偏光顯微鏡紋理圖分析--- 80 3-4-4-2 X-ray 粉末繞射結果--- 82
3-5 結論--- 87 參考文獻--- 88
圖目錄
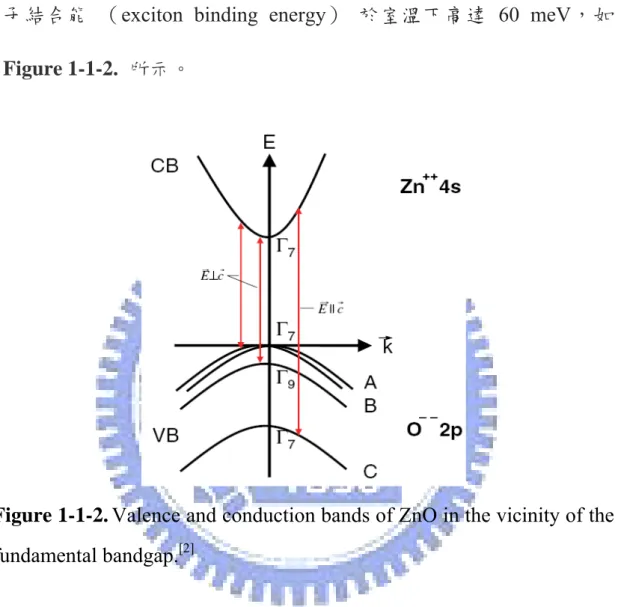
Figure 1-1-1. The wurtzite structure model of ZnO. The tetrahedral
coordination of Zn–O is shown.--- 2
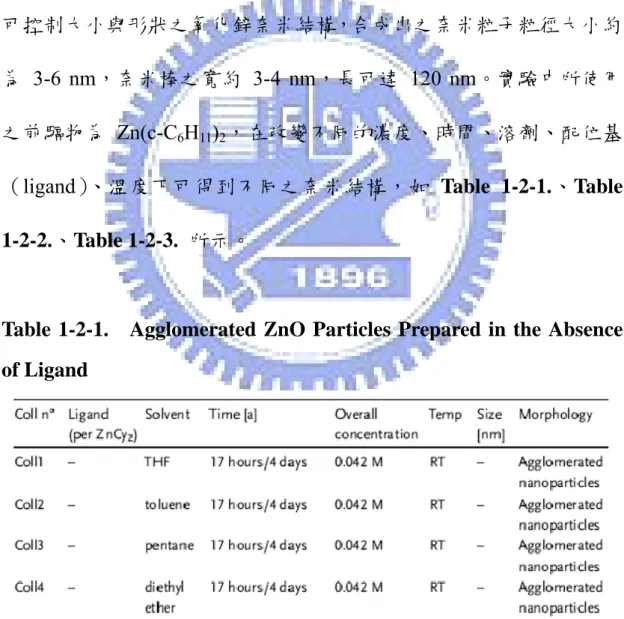
Figure 1-1-2. Valence and conduction bands of ZnO in the vicinity of the
fundamental bandgap.--- 3
Figure 1-2-1. Controlled photostability by interaction between NH2–ZnO
nanocrystals and aldehydes--- 18
Figure 1-2-2. Unidirectional light emitters were synthesized from
rod-shaped ZnO microcrystals and TOPO coated CdSe/CdS core/shell nanoparticles.--- 19
Figure 1-2-3. Schemtic of the phase-separated composite films (PSCOF)
structure.--- 26
Figure 1-2-4. Photographs taken through a microscope with samples
between crossed polarizers. From (a) to (d), the UV dosage applied varied from 0.75 to 20 mJ/cm2.--- 27
Figure 1-2-5. Dependence of critical voltage for splay-to-bend transition
on curing voltage (Vuv) for monomer-A-doped cells.--- 28
Figure 1-3-1. Construction of a typical OCB-cell--- 29 Figure 1-3-2. Schematic liquid crystal director orientation of
splay-to-bend transition in OCB-cell and a calculated Gibbs free energy vs. applied voltage in splay and bend states--- 29
Figure 2-4-1. Experimental setup of the electro-optical property
measurement.--- 48
Figure 3-1-1. UV-Vis absorption spectra of ZnO nanoparticles with (a)
[LiOH]/[Zn(OAc)2] = 3.3--- 50
Figure 3-1-2. Photoluminescence spectra of ZnO nanoparticles with (a)
[LiOH]/[Zn(OAc)2] = 1.4 (b) [LiOH]/[Zn(OAc)2] = 2.8, and (c) [LiOH]/[Zn(OAc)2] = 3.3--- 52
Figure 3-1-3. Powder X-ray diffraction spectra of ZnO nanoparticles
with (a) [LiOH]/[Zn(OAc)2] = 1.4 (b) [LiOH]/[Zn(OAc)2] = 2.8 (c) [LiOH]/[Zn(OAc)2] = 3.3--- 53
Figure 3-1-4. TEM images of ZnO nanoparticles with (a)
[LiOH]/[Zn(OAc)2] = 1.4 (b) Metharyl-modified ZnO nanoparticles with [LiOH]/[Zn(OAc)2] = 1.4--- 54
Figure 3-2-1. UV-Vis absorption spectra of ZnO nanostructures prepared
under different conditions. (a) 60℃ for 5 h; (b) 60℃ for 12 h; (c) 60 ℃ for 24 h; (d) 60℃ for 48 h; (e) 80℃ for 12 h; (f) 60℃ for 12 h in ethanol.--- 55
Figure 3-2-2. TEM images of ZnO nanostructures prepared under
different conditions. (a) 60℃ for 5 h; (b) 60℃ for 12 h; (c) 60℃ for 24 h; (d) 60℃ for 48 h; (e) 80℃ for 12 h; (f) 60℃ for 12 h in ethanol.--- 58
Figure 3-2-3. Powder X-ray diffraction spectra of ZnO nanorods
prepared under different conditions: (a) 60℃ for 5 h; (b) 60℃ for 12 h; (c) 60℃ for 24 h; (d) 60℃ for 48 h.--- 60
Figure 3-3-1. UV-Vis absorption and photoluminescence spectra of (a)
Z n O n a n o p a r t i c l e s b e f o r e m e t h a r y l - m o d i f i c a t i o n a n d ( b ) Metharyl-modified ZnO nanoparticles--- 61
Figure 3-3-2. Thermogravimetric analysis curves of (a) ZnO
nanoparticles before metharyl-modification (b) Metharyl-modified ZnO nanoparticles--- 62
Figure 3-3-3. FTIR spectra of (a) ZnO nanoparticles before
metharyl-modification (b) Metharyl-modified ZnO nanoparticles --- 63
Figure 3-3-4. Voltage-transmittance curves of OCB cells under
UV-exposure at 10Vpp for 50min. : (a) pure E7 LC, (b) doped with 1% monomer, (c) doped with 1% ZnO nanoparticle, and (d) doped with 1% monomer and 1% ZnO nanoparticle--- 64
Figure 3-3-5. Voltage-transmittance curves of OCB cells under
UV-exposure at 4Vpp for 50min. : (a) pure E7 LC, (b) doped with 1% monomer, (c) doped with 1% ZnO nanoparticle, and (d) doped with 1% monomer and 1% ZnO nanoparticle --- 65
Figure 3-3-6. Voltage-transmittance curves of OCB cells doped with 1%
ZnO nanoparticle under UV-exposure for 50min at (a) 10Vpp (b) 8Vpp (c) 6Vpp (d) 4Vpp--- 66
Figure 3-3-7. Dependence of critical voltage for splay-to-bend transition
on curing voltage--- 67
Figure 3-4-1. UV-Vis absorption and photoluminescence spectra of liquid
crystalline homopolymer PBBBA --- 68
Figure 3-4-2. Thermogravimetric analysis curves of homopolymer
PBBBA. The decomposition temperature (Td) is obtained from the onset
of the heating curve--- 69
Figure 3-4-3. DSC thermogram of homopolymer PBBBA. The data were
obtained from the second heating and the first heating processes---- 70
PBBBA--- 70
Figure 3-4-5. Powder X-ray diffraction spectra of homopolymer PBBBA
in the mesogenic phase was obtained at 130℃--- 73
Figure 3-4-6. Thermogravimetric analysis curves of (a) ZnO
nanoparticles before Pyridyl-modification (b) Pyridyl-modified ZnO nanoparticles--- 74
Figure 3-4-7. Thermogravimetric analysis curves of (a) ZnO nanorods
before Pyridyl-modification (b) Pyridyl-modified ZnO nanorods --- 74
Figure 3-4-8. FTIR spectra of (a) ZnO nanoparticles before
Pyridyl-modification (b) Pyridyl-modified ZnO nanoparticles--- 75
F i g u re 3 - 4 - 9 . F T I R s p e c t r a o f ( a ) Z n O n a n o r o d s b e f o r e
Pyridyl-modification (b) Pyridyl-modified ZnO nanorods--- 76
Figure 3-4-10. FTIR spectra of (a) Pyridyl-modified ZnO nanoparticles,
(b) Hydrogen bonded complex of pyridyl-modified ZnO nanoparticles and PBBBA with 1:10 mol % and (c) PBBBA--- 77
Figure 3-4-11. FTIR spectra of (a) Pyridyl-modified ZnO nanorods, (b)
Hydrogen bonded complex of pyridyl-modified ZnO nanorods and PBBBA with 1:10 mol % and (c) PBBBA--- 78
Figure 3-4-12. FTIR spectra of (a) ZnO nanopaticles , (b)
pyridyl-modified ZnO nanopaticles , hydrogen bonded complexes of pyridyl-modified ZnO nanoparticles and PBBBA with (c) 1:1 mol% (d) 1:5 mol% (e) 1:10 mol% (f) 1:50 mol % (g) 1:100 mol % and (h) PBBBA. --- 79
ZnO nanorods , hydrogen bonded complexes of pyridyl-modified ZnO nanorods and PBBBA with (c) 1:1 mol% (d) 1:5 mol% (e) 1:10 mol% (f) 1:50 mol % (g) 1:100 mol % and (h) PBBBA.--- 80
Figure 3-4-14. Polarized optical microscope image of hydrogen bonded
complexes : (a) pyridyl-modified ZnO nanopartcles and PBBBA with 1:50 mol % (b) pyridyl-modified ZnO nanopartcles and PBBBA with 1:100 mol % (c) pyridyl-modified ZnO nanorods and PBBBA with 1:100 mol %--- 82
Figure 3-4-15. Powder X-ray diffraction spectra of hydrogen bonded
complex of pyridyl-modified ZnO nanopartcles and PBBBA with 1:50 mol %--- 83
Figure 3-4-16. Powder X-ray diffraction spectra of hydrogen bonded
complex of pyridyl-modified ZnO nanopartcles and PBBBA with 1:100 mol %--- 85
Figure 3-4-17. Powder X-ray diffraction spectra of hydrogen bonded
complex of pyridyl-modified ZnO nanorods and PBBBA with 1:100 mol %. The inset shows the magnified scale for the smaller angle area.---- 86
表目錄
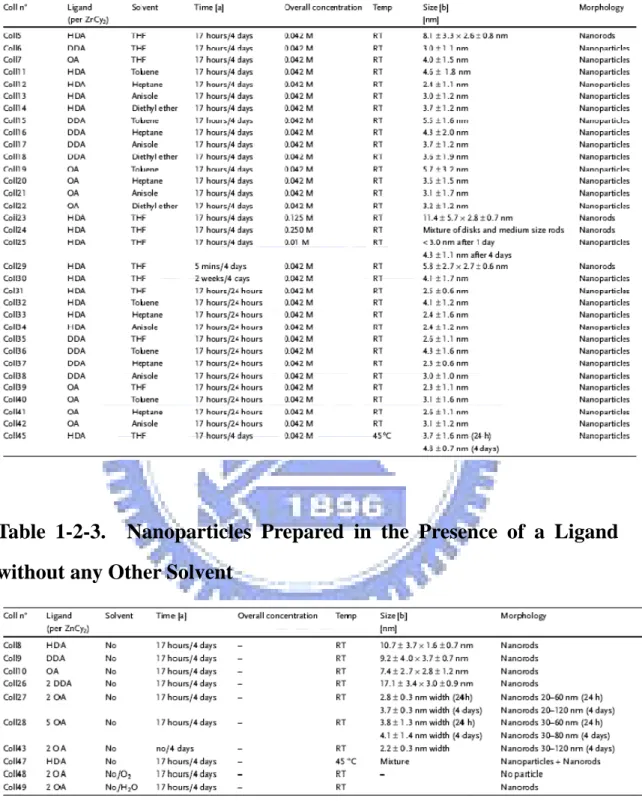
Table 1-2-1. Agglomerated ZnO Particles Prepared in the Absence of
Ligand--- 14
Table 1-2-2. Nanoparticles Prepared in the Presence of a Ligand and a
Solvent--- 15
Table 1-2-3. Nanoparticles Prepared in the Presence of a Ligand
without any Other Solvent--- 15
1-1 前言及奈米氧化鋅介紹
在無機發光材料中,以量子發光元件最常見,發光性的奈米粒子 亦被稱為量子點 (quantum dot),當 Ⅲ-Ⅴ 族與 Ⅱ-Ⅵ 族的半導體 粒子達到奈米等級時,會因為量子侷限效應 (quantum-confinement effect),隨著晶體粒子大小改變,有著不同的發光特性產生。氧化鋅 為 II-VI 族半導體材料,其具有寬能隙 (wide band gap)、發光性 (light-emitting)、壓電性 (piezoelectric)、價格低等特性。純氧化鋅 外觀為白色之粉體,屬於六方晶系之纖鋅礦 (wurtzite) 構造,空 間群 (space group) 為 P63mc 或稱 C6v ,鋅與氧皆為六方最密堆 積的方式交錯組成整個晶體,晶格常數 a 軸為 0.32495 nm、c 軸為 0.52065 nm,如 Figure 1-1-1. 所示。
Figure 1-1-1. The wurtzite structure model of ZnO. The tetrahedral
在能階上,LUMO 來自於 Zn2+ 之 4s 軌域;HOMO 來自於 O
2-的 2p 軌域,具直接能隙 (direct band gap) 大小為 3.37 eV,激
子結合能 (exciton binding energy) 於室溫下高達 60 meV,如
Figure 1-1-2. 所示。
Figure 1-1-2.Valence and conduction bands of ZnO in the vicinity of the
fundamental bandgap.[2]
1-1-1 奈米氧化鋅之發光性質
1996 年 Vanheusden[3] 等人發表了對於氧化鋅發光機制探討的
多種缺陷 (例如: 氧空缺 (vacancy) 或是插入型 (interstitial) 鋅
原子) 產生的深層能階發射 (deep level emission)。氧空缺形式
有下列三種:(1) 中性氧空缺 (neutral oxygen vacancy, VO0),(2)
單游離氧空缺 (singly ionized oxygen vacancy, VO*),(3)雙游離
氧空缺 (doubly ionized oxygen vacancy, VO**)。
1-1-2 奈米氧化鋅之應用性
奈米氧化鋅高激子結合能之特性使氧化鋅於室溫具有高激子放 射效率,因此目前氧化鋅被認為是非常具潛力的紫外-藍光光電材料。 另外,氧化鋅可吸收較本身能隙波長短之紫外線,若在氧化鋅中摻入 鋁或鎵等 IIIA 族元素,可降低電阻率以利製作透明導電膜[4],用作 透明電極的應用,另可用在場發射 (field-emission) 顯示器上。氧 化鋅通電後電壓與電流間有相當高的非線性關係,可用來製作可變電 阻[5]。於工業上可作為橡膠加速劑、顏料及陶瓷添加劑,其他還有化 妝品、紫外線吸收劑、奈米光觸媒、鋰電池、太陽能電池、和氣體感 測器等光電之運用等多方面用途。奈米氧化鋅具有半導體催化劑的電 子結構,在光照射下,當具有一定能量的光子或者具有超過這個能隙 的光子射入半導體時,一個電子從價帶 (valence band) 激發到傳 導帶 (conduction band),而留下了一個空穴。激發態的傳導帶電子和價帶空穴能夠重新結合消除輸入的能量和熱,電子在材料的表面態
被捕捉,價態電子躍遷到傳導帶,價帶的孔穴把周圍環境中的羥基電
子搶奪過來使羥基變成自由基,作為強氧化劑而完成對有機物 (或含
氯) 的降解,殺死病菌和病毒。在薄膜電晶體 (thin film transistor, TFT)
上[6-8],利用氧化鋅奈米棒可製作出高 ON/OFF ratio、高移動率 (mobility)、低臨界電壓 (threshold voltage) 之高效率薄膜電晶
體元件。在有機太陽能電池 (organic solar cell) 方面[9],氧化鋅可
用於取代 C61-butyric acid methyl ester (PCBM) 做為電子受體物質
1-2 文獻回顧
1-2-1氧化鋅奈米結構的製備
1-2-1-1氧化鋅奈米粒子的製備
氧化鋅奈米粒子的製備方法有很多種,可大致區分為物理法與化 學法。物理法包括有機金屬化學氣相沉積 (MOCVD)、氣液固相製 程 (vapor liquid solid growth process, VLS)、脈衝雷射沉積 (pulse laser deposition)、以及鋅粉蒸發反應等方式合成。化學法如化學沉澱 法、水熱合成法 (solvothermal)、溶膠凝膠法 (sol-gel) 及乳化法 (emulsion) 等,在此僅介紹化學法為主。
Bahnemann[10] 等人以醋酸鋅 (Zn(CH3COO)2‧2H2O) 在 50
℃ 下,劇烈攪拌溶解在異丙醇 ((CH3)2CHOH) 後,將全部溶液之 體積以異丙醇稀釋至十倍,再於 0 ℃ 一邊持續攪拌一邊快速加入氫 氧化鈉之異丙醇溶液,於 65 ℃ 水浴下加熱 2 小時後,再置於室溫 下 3 天,旋轉濃縮後即可製備出於異丙醇中之氧化鋅分散液,於 TEM 可見其粒子大小約 5 nm。Searson[11] 等人進一步利用此方法, 研究氧化鋅結晶之成長機制與不同條件下成長的速率,除了時間與溫 度的關係外,還研究了不同前驅物 Zn(CH3COO)2、Zn(ClO4)2 與 ZnBr2 的影響。如鹵素等陰離子對氧化鋅表面吸附力較強,較能防止 粒子變大或聚集。此外文獻中還探討溶解度對晶體成長的影響。當溶
解度愈大時,晶體成長速率就愈快,卻會造成晶體成長難以控制。而 影響溶解度的因素包括溫度、溶劑與陰離子種類。氧化鋅在水中的溶 解度約 5×10-5 M,在異丙醇中約 3×10-10 M,所以在水中晶體成長與 聚集的速率比在異丙醇中要快許多,反之卻難以控制其晶體成長。 Searson[12] 之 團 隊 另 於 上 述 反 應 過 程 中 加 入 有 機 覆 蓋 配 位 基 (capping ligand) 控制氧化鋅奈米粒子的成長。在加熱的過程中加 入帶有硫醇 (thiol) 或磷酸基 (phosphonic acid) 的長碳鏈配位 基,由於硫醇基與磷酸基可吸附粒子表面,使粒子原本隨著時間而變 大的結晶停止成長,並且可以由計算完全包覆所需配位基的量,與加 入配位基的時間,得到想要的粒子大小。 Kaneko[14] 等 人 所 用 之 逆 微 胞 法 , 將 二 丁 醇 基 鋅 ( zinc di-n-butoxide) 在氨水催化下使其在 polyoxyethylene(6)nonylphenyl ether(NP-6)/cyclohexane 溶液中水解,不同濃度的氨水與界面活性劑 的比例會形成不同類型的微胞,可以由此控制逆微胞的大小,進一步 控制粒子的大小,且不需加熱即可得到氧化鋅結晶。 Feldmann[15] 使用 polyol (指多個 OH 基且高沸點之醇類) 做 為溶劑,用來製備多種奈米粒子。是將金屬之醋酸化合物、醇類化合 物或鹵化物以加熱方式溶於高沸點之醇類 (DEG, diethylene glycol) 中,此文獻中製備的是摻雜有銦的氧化鋅 (ZnO:In3+) 做為 n 型透
明導電氧化物 (n-type transparent oxide)。首先,將醋酸鋅與醋酸銦 (5 mol%) 溶於 80 ℃ 之 DEG 中,在劇烈攪拌下加入 2 mL 水,然 後快速加熱至 180 ℃ 持續 2 小時,經過離心清洗後以超音波震盪 可再分散於乙醇中。產生之粒子為大小均一之球形粒子,粒徑大小為 80-90 nm。 Spanhel 與 Anderson[16] 等 人 則 是 先 將 醋 酸 鋅 溶 解 於 乙 醇 (C2H5OH) 中,配成 0.1 M 之 Zn2+ 溶液,在附有冷凝裝置下,於 80 ℃ 加熱 180 分鐘,蒸餾出 60% 體積的乙醇,剩下 40% 體積之 Zn2+ 乙醇溶液。將此母液再以乙醇稀釋至原體積,分別加入 0.1 M、 0.14 M、0.2 M 氫氧化鋰 (LiOH) 乙醇溶液,最後在置於 0 ℃ 下超 音波震盪 10 分鐘。若在室溫度下則會使粒子變大,使用氫氧化鈉 (NaOH)、氫氧化鉀 (KOH) 或是氫氧化鎂 (Mg(OH)2) 取代氫
氧化鋰,均會使溶液產生混濁之沈澱物,若用其他醇類溶劑如甲醇 (methanol)、 異丙醇 (2-propanol) 或鋅鹽如蟻酸鋅 (zinc formate)、草酸鋅 (zinc citrate),均會得到較差的結果。此外將三 種不同氫氧化鋰濃度之溶液取出數滴溶入純水中,測量其 pH 值, 顯示 0.14 M之氫氧化鋰溶液其 pH 值大致與等電點 (zero point of charge)(pH = 9) 相近,因此粒子表面略呈電中性。0.1 M 之 氫氧化鋰溶液其 pH 值約為 6.5,使粒子表面帶正電;0.2 M 之
氫氧化鋰溶液其 pH 值約為 8.2,則使粒子表面帶負電,影響粒 子的形狀與大小。
Xiong[17-19] 等人進一步以將醋酸鋅以其他鋅鹽取代。首先將 poly(ethylene glycol) methyl ether (PEGME)、高錳酸鉀 (KMnO4),
以及氫氧化鈉 (NaOH) 溶於水中,在室溫下反應24小時之後再將 所產生之二氧化錳 (MnO2) 沈澱過濾出,形成一無色透明溶液。
利用鹽酸將此溶液之 pH 值調至 2.0 後,再將溶劑抽乾,於真空烘 箱 下 以 100 ℃ 乾 燥 之 , PEGME 之 衍 生 物 [CH3O(CH2CH2O)nCH2COO]2 於是可以利用甲苯 (toluene) 在所得
固體中萃取出。氫氧化鋅 (Zn(OH)2) 可由氯化鋅 (ZnCl2) 與氫 氧化鈉製得後再以去離子水清洗。[CH3O(CH2CH2O)nCH2COO]2 與氫 氧化鋅在熱水下反應後可得 [CH3O(CH2CH2O)nCH2COO]2Zn 之水溶 液,將溶劑蒸出後在於真空烘箱下以 100 ℃ 乾燥之。所得知產物溶 於乙醇後加熱迴流三小時,再加入一定濃度之氫氧化鋰溶液,形成表 面帶有 PEGME 官能基之氧化鋅奈米粒子。經由改變不同的氫氧化 鋰濃度,可以獲得不同大小之奈米粒子,PL放光波長範圍可由 450 nm至 575 nm,分別可產生由藍光至黃光的光色。此外其螢光效率 (quantum efficiency) 也可由之前文獻所提及之 1-16%,提高至 18-31%。此團隊進一步於 70 ℃ 將甲基壓克力酸 (methacrylic acid,
MAA) 之水溶液與氧化鋅之粉末反應,形成甲基壓克力酸鋅鹽 (zinc methacrylate),將水抽乾之後再置於真空烘箱乾燥。將 0.1 M 甲基壓 克力酸鋅之乙醇溶液與 0.2 M 氫氧化鋰之乙醇溶液混合後於室溫下 反應一天,再於 40 ℃ 下旋轉濃縮至產生白色沉澱。此方式得到之 氧化鋅奈米粒子表面上具有甲基壓克力基,所以可以進一步與單體 MMA 或 styrene 反應,以產生氧化鋅與高分子的有機無機複合材料, 其 PL 放光波長在 420-464 nm 之間。 Liu[20-21] 等人則是進一步將鋅鹽前驅物做了更多的改變,以達 到所需之高發光效率、高材料熱穩定性、高加工性 (processability)。 首先將氯化鋅與氫氧化鈉之水溶液混合以得到氫氧化鋅,接著加入溴 醋酸 (bromoacetic acid) 水溶液,將此溶液於 70 ℃加熱至 pH 值 達到 6 左右,將未反應之氫氧化鋅過濾掉後取其濾液,此濾液旋轉 濃縮以除去大部分水後,再置於真空烘箱以 100 ℃ 乾燥之,得到溴 醋酸鋅 (zinc bromoacetate)。將 N,N-dimethyloctadecylamine 與溴醋 酸鋅溶於乙醇後,在劇烈攪拌下加熱迴流 24 小時。再把此溶液旋轉 濃縮至剩下少量溶劑,於 -12 ℃ 下以無水乙醚 (diethyl ether) 將 白 色 固 體 沈 澱 出 , 得 到 N,N-dimethyloctadecylammonium bromide acetate zinc salt (C18-Zn) 。 接 著 將 C18-Zn 與 lithium
數 分 鐘 , 將 溴 離 子 以 N-(Tf)2 取 代 , 形 成 N,N-dimethyloctadecylammonium bis((trifluoromethyl)sulfonyl) amide
acetate zinc salt (IL-Zn)。最後在室溫下將 IL-Zn 與氫氧化鋰以不同的 濃度比在乙醇下反應,以得到不同大小之氧化鋅奈米粒子。
Fu[22] 等人則是將二乙醇胺 (diethanolamine, DEA)、硝酸鋅 (Zn(NO3)2.6H2O) 的水溶液以及油酸 (oleic acid, OA) 一起放
入反應器中,先於室溫攪拌 30 分鐘後,再於 80 ℃ 反應兩小時。 比較之前文獻所合成出之氧化鋅奈米粒子,此方式不但較簡便,其 螢光效率更可達到 76%。
Demir[23] 等人以酸催化的方式以降低所需之反應時間、增加粒
子 分 佈 之 再 現 性 , 並 增 加 粒 子 之 結 晶 性 , 首 先 將對 甲 苯 磺 酸
(p-toluene sulfonic acid monohydrate, p-TSA) 溶 於 1- 戊 醇
(1-pentanol) 與對-二甲苯 (m-xylene) 以 2:1 體積比混合之溶液 裡,加入醋酸鋅後於 140 ℃ 迴流,產生之白色沈澱經離心後再以去 離子水與乙醇潤洗。於 40 ℃ 減壓濃縮下抽乾溶劑後,可得到粒徑 大小大約在 25-50 nm 之氧化鋅奈米粒子。 1-2-1-2 其他氧化鋅奈米結構的製備 除了奈米粒子之外,其他奈米結構如奈米棒 (rod)、線 (wire)、 平板 (plate)、針 (needle) 等等結構亦被許多研究團隊所發表。
Chen[24] 等人則是利用水熱法,並探討不同的反應溫度時間與 有機添加物來改變晶體形狀與大小,得到高結晶度、粒徑分布窄的氧 化鋅結晶。先將氯化鋅 (ZnCl2) 與氫氧化鈉以莫耳比 1:2 之比例 溶於去離子水,形成白色的氫氧化鋅 (Zn(OH)2) 沉澱,過濾後以 去離子水清洗,再將白色沉澱重新分散於水中,以鹽酸將 pH 值調 至 5-8 之間,攪拌 3 小時後在以壓力釜中不同的溫度與時間反應, 產物過濾後以去離子水清洗,並在室溫下乾燥。反應時添加銨類或二 醇類會使晶體之大小與形狀改變,所形成的棒狀、絲狀或片狀結構大 小約在 20-500 nm。
Peng[25] 等人使用硝酸鋅 (Zn(NO3)2‧6H2O) 製備出六角形
之奈米環 (nanoring) 與奈米碟 (nanodisk)。使用硝酸鋅與六甲 基四胺 (hexamethylenetetramine, HMT) 水溶液混合後,加入少量之 高分子 (polyacrylamide, PAM, Mw = 10 000;carboxyl - modified PAM, PAM - COOH, Mw = 200 000),加熱到 70 ℃ 迴流 30 分鐘後停止攪 拌在繼續反應 5 小時。接著冷卻至室溫以水清洗後,於 60 ℃ 在真 空烘箱乾燥之。由於所加入之高分子能選擇性吸附至氧化鋅晶體之基 面 (basal plane) 上,使得沿著 [001] 上得晶體成長受到抑制,而 使晶體沿著側向成長。 Cheng與Samulski[26-27] 等人也是使用水熱法以產生具有不同長
寬比 (aspect ratio) 之一維奈米棒。首先將醋酸鋅以及氫氧化鈉, 分別溶於甲醇溶液後,混合後將產生之澄清溶液置入壓力釜中。加熱 至 150 ℃ 後反應 24 小時。收集白色沈澱後以水和乙醇清洗,乾燥 後即為氧化鋅之奈米棒。此外還比較不同的反應溶劑對於生成之奈米 棒造成的影響,結果顯示使用乙醇比起使用甲醇可產生較大長寬比之 氧化鋅奈米棒。另外此團隊更於另一文獻中將氫氧化鈉以有機鹼四甲 基氫氧化銨 (Me4NOH) 取代,探討不同溫度、鹼濃度、反應時間、 水含量,對於氧化鋅奈米結構之影響。 Yin 與 O’Brien[28] 等人則是利用在有機溶劑中將醋酸鋅熱分解 的 方 式 合 成 氧 化 鋅 奈 米 棒 。 首 先 在 室 溫 下 將 醋 酸 鋅 溶 於 三 辛 氨 (trioctylamine) 與油酸之混合液中。10-15 分鐘內快速加熱至 286 ℃ 變為黃色之溶液,持續加熱一小時會產生混濁物,回到室溫後加 入適量乙醇,在加入正己烷使其其產生沈澱。產生之氧化鋅奈米棒寬 度平均約 2.2 nm,長度約為 43 nm。 Andelman 與 O’Brien[29] 等人則是在反應過程中加入不同包覆 劑 (capping agent),使得氧化鋅的形態學結構 (morphology) 能夠 得以控制,三種包覆劑分別為三辛氨 (trioctylamine, TOA)、十六醇 (1-hexadecanol, HD) 及 1-十八烯 (1-octadecene, OD)。首先將醋 酸鋅與包覆劑以 1:1 比例混合後,攪拌加熱至 180 ℃ 除氣 (degas)
一小時後,於氮氣下加熱至 286-300 ℃,直至溶液變為霧狀或白色停 止加熱。結果顯示 TOA 能產生奈米棒,HD 能產生奈米三角形 (nanotriangle),OD 能得到球形奈米粒子。在晶體成長中不同的晶 面會有不同之成長速率,因此當不同之包覆劑結合到不同晶面時,造 成表面能 (surface energy) 的差異,所以形態學結構也因而改變。 Kahn[30] 等人利用有機金屬合成法,改變不同反應條件下製備出 可控制大小與形狀之氧化鋅奈米結構,合成出之奈米粒子粒徑大小約 為 3-6 nm,奈米棒之寬約 3-4 nm,長可達 120 nm。實驗中所使用 之前驅物為 Zn(c-C6H11)2,在改變不同的濃度、時間、溶劑、配位基
(ligand)、溫度下可得到不同之奈米結構,如 Table 1-2-1.、Table
1-2-2.、Table 1-2-3. 所示。
Table 1-2-1. Agglomerated ZnO Particles Prepared in the Absence of Ligand
Table 1-2-2. Nanoparticles Prepared in the Presence of a Ligand and a Solvent
Table 1-2-3. Nanoparticles Prepared in the Presence of a Ligand without any Other Solvent
Sun 與 Sirringhaus[6-8] 則是改進 Pacholski 在先前所報導之方 法,將製備出之氧化鋅奈米棒利用在薄膜電晶體元件上。首先將醋酸
鋅及極少量的水溶於甲醇中,將此溶液在攪拌下加熱至 60 ℃,接著 將氫氧化鉀的甲醇溶液滴入反應瓶中,於恆溫 60 ℃ 下反應兩小時 又 15 分鐘,以形成大小約在 6 nm 之奈米粒子。為了降低所需之反 應時間,將溶液濃縮至原本之六分之一左右,再繼續於 60 ℃ 反應 五小時,以形成長度約在 65 nm 之氧化鋅奈米棒。
1-2-2 奈米氧化鋅的表面改質
表面改質是在無機奈米粒子的表面形成新的化學鍵或者物理包 覆上一層有機或無機化合物的方法。利用溶液中金屬離子、陰離子和 修飾劑的相互作用,與奈米粒子中的金屬離子或非金屬離子表面相互 作用以形成表面改質。通過對奈米粒子表面的修飾,可以達到:1) 改 善奈米粒子的分散性,防止粒子產生聚集 (aggregation) 而降低量 子效應;2) 提高粒子表面活性;3) 使粒子表面產生所需的物理、化 學、機械性質;4) 改善奈米粒子與其它物質之間的相容性。奈米氧 化鋅的表面修飾就是通過物理方法或化學方法對粒子表面進行處理, 以達到所需的粒子表面性質。 Norberg[31] 等人探討在不同的晶體成長期間,加入十二烷銨 (dodecylamine, DDA) 與三正辛基氧膦 (trioctylphosphine oxide, TOPO) 等,包覆劑對於氧化鋅奈米粒子發光性質所造成的影響。加入 DDA 後,能減少氧化鋅奈米粒子的表面缺陷,紫外光部份的 放光強度因而增加。
Guo 與 Yang[32] 等人則是在未加入氫氧化鈉使其水解之前,加 入不同量之聚乙烯吡咯烷酮 (poly(vinylpyrrolidone), PVP),結果顯 示隨著Zn2+/PVP之莫耳比降低,得到之奈米結構能由球形轉變為棒狀。 在發光性質方面,隨著PVP的比例增加,near band edge的紫外光放光 強度會增加,而defect-induced的綠光放光強度會隨之減少。
Demir[32-33] 在製作氧化鋅與 PMMA 的複合物的過程中,加入
tert-butylphosphonic acid (t-BuPO3H2),此包覆劑具有以下作用:1) 表
面被 t-BuPO3H2 附著後,能夠阻止oswald ripening,以降低晶體成長
速度;2) 增加奈米粒子於厭水性單體 MMA 的溶解度,以利聚合過 程。 修飾劑是一種同時具有與無機物和有機物分別反應的官能基之 化合物。在氧化鋅奈米結構之表面修飾上,其中一端與氧化鋅表面結 合,另一端可與分散介質有強的相互作用,或是進一步可與其他化合 物反應。因此,修飾劑可以實現對表面修飾的目的。常用的修飾劑有 矽烷 (silane) 修飾劑、鈦酸酯 (titanate) 修飾劑等。 Jana[34] 等人使用 N-(2-aminoethyl)aminopropyltrimethoxysilane (AEAPS),使氧化鋅外層帶有胺基,可與醛基反應之後形成亞胺鍵
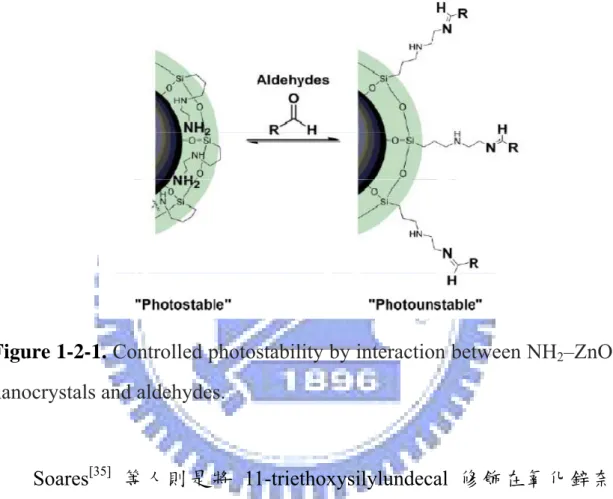
(imine ), 在 紫 外 光 的 照 射 下 , 其 可 見 光 的 發 光 會 發 生 淬 熄 (quenching) 效應,得以辨識生物體中帶有醛基 (aldehyde) 的 生物分子或是環境中帶有醛基之化合物,如 Figure 1-2-1. 所示。
Figure 1-2-1. Controlled photostability by interaction between NH2–ZnO
nanocrystals and aldehydes.
Soares[35] 等人則是將 11-triethoxysilylundecal 修飾在氧化鋅奈 米棒上,在紫外光的放光的強度能增加,且保持可見光範圍的放光強 度。
Hung 與 Whang[36] 利用 3-(trimethoxysilyl)propyl methacrylate (TPM) 使 氧 化 鋅 奈 米 粒 子 外 層 修 飾 上 壓 克 力 基 , 再 與 2-hydroxyethyl methacrylate (HEMA) 進 行 聚 合 , 形 成 ZnO/PHEMA 之奈米複合材料。除了表面官能基的改質之外,修飾
後的氧化鋅奈米粒子還可防止奈米粒子產生自身聚集,穩定奈米粒 子的粒徑大小。 Bourlinos[37] 等 人 則 是 在 鹼 性 溶 液 下 以 (CH3O)3Si(CH2)3N+(CH3)(C10H21)2Cl- 修 飾 氧 化 鋅 奈 米 粒 子 , 再 以 C9H19-C6H4-(OCH2CH2)20O(CH2)3SO3- K+ 將氯離子交換,可使再室溫 下原本未進行離子交換前的固體粉末態轉變為液態。
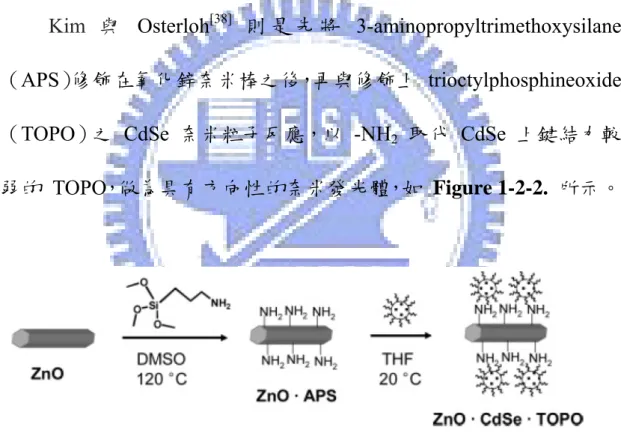
Kim 與 Osterloh[38] 則 是 先 將 3-aminopropyltrimethoxysilane (APS)修飾在氧化鋅奈米棒之後,再與修飾上 trioctylphosphineoxide (TOPO)之 CdSe 奈米粒子反應,以 -NH2 取代 CdSe 上鍵結力較
弱的 TOPO,做為具有方向性的奈米發光體,如 Figure 1-2-2. 所示。
Figure 1-2-2. Unidirectional light emitters were synthesized from
rod-shaped ZnO microcrystals and TOPO coated CdSe/CdS core/shell nanoparticles.
1-2-3 液晶簡介
對於一般常見的物質由結晶狀的固體 (crystalline solid) 相變為 各同向性的液體 (isotropic liquid),通常是經由單一過程的相變。但 有很多有機物由結晶固體到同向性液體間卻需要經過多個步驟的相 變。因此當中存在一個或多個介於結晶固體與各向同性液體間的中間 相 (mesophases)。由於這些中間相的分子次序是介於結晶固體與同向 性液體間,所以這些相的力學、光學性質和對稱性也介於結晶固體與 液體之間。 到目前為止,已被發現的這些中間相大致可被區分成兩大類別: (1) disordered crystal mesophases:一般稱之為「塑性晶體」 (plastic crystals)。其分子形狀常為圓球狀 (globular),故易形成分子位置有次 序性,但方向無次序性的相。因其分子位置仍保留三維晶格排列,故 不具流動性; (2) ordered fluid mesophases:通常稱為 「液態晶體」 (liquid crystals) 即一般簡稱液晶。由於此相常由長條狀 (rod-like) 或 圓盤狀 (dise-like) 的分子所組成。故易形成一分子重心位置無次序性, 但方向有次序性的相。由於此相分子重心位置不受限於晶格,故具有 一定程度的流動性。1-2-3-1 液晶分類
與氣態的三種基本物質狀態。液晶是長棒狀分子未端有強極性基的化 學材料,擁有下列特殊性質,為現今平面顯示元件基礎: (1) 液晶的流動性與結晶體的晶體特性 (2) 從低溫加熱固體融解,會溶化呈現白色混濁液體;再升溫,最後 成為等方向性的透明液體 (3) 施加電場、光、熱等外部刺激,分子的排列會被改變 液晶依形成方式、分子排列方式、分子量大小…與以分門別類。依形 成方式的不同而分為熱向型液晶 (thermotropic liquid crystal)、液向 型液晶 (lyotropic liquid crystal) 二大類。熱向型液晶為在不同溫度 範圍下有不同液晶相,此種液晶多應用於電氣-光學效果及溫度-光學 效果上;而液向型液晶乃在適當的溶濟中,當達到臨界濃度時所形成 液晶相,此類型液晶多存於生物體的物質中。再者,因液晶分子排列 狀態不同,分別命名為向列型 (nematic) 液晶相、層列型 (smectic) 液晶相、膽固醇型 (cholesteric) 液晶相。向列型液晶是由希臘語 而來,為絲狀的意思,以偏光顯微鏡觀察時,可見到如多數絲帶的光 學形態;層列型液晶則為希臘語黏土的意思,故此類型液晶一般如油 脂般的黏稠,在偏光顯微鏡下具有獨特的紋理;第三種膽固醇型液晶 則是基於,大部份的膽固型液晶是由膽固醇 (C27H46O) 所衍生出的化 合物而得名。
將液晶其他分類歸納整理,如 Table 1-2-4. 所示:
Table 1-2-4. The Classification of Liquid Crystalline
形成方式區分 熱向型液晶(thermotropic liquid crystal) 液向型液晶(lyotropic liquid crystal) 分子排列方式區分 向列型(nematic)液晶 層列型(smectic)液晶 膽固醇型(cholesteric)液晶 圓盤狀(discotic)液晶 分子量大小區分 高分子液晶 主鏈型高分子液晶 側鏈型高分子液晶 低分子液晶
其他 重複型液晶(reentrant liquid crystal) 鐵電性液晶(ferroelectric liquid crystal)
1-2-3-2 液晶性質
依據液晶分子結構之特性及液晶相時所具有基本現象,液晶具有 以下數種性質。
(1) 介電異向性 (dielectric anisotropy):液晶分子中一般皆含有極性 較大之未端基部份 (如: CN、F、Cl),加上液晶分子的電子結構上,
都是 σ 鍵或 π 鍵互相鍵結,使分子之電子有高效率及長距離移動能 力,故分子在外加電場下易受誘導而產生感應偶極矩(induced dipole)。 表示方法為:Δε = ε// - ε⊥。意即液晶分子之介電異向性定義為平行與 垂直方向介電常數之差。Δε 對起始電壓有決定性影響:Δε 愈大,所 需起始電壓愈低。Δε 的正負號也決定該分子排列之方向:Δε > 0 的 液晶,分子主軸會與感應偶極矩平行,可用在平行配向;Δε < 0, 則運用於垂直配向之電子元件。 (2) 電磁場效應:液晶排列之方向除了受電場影響外,也受磁場影響。 在電場或磁場除去後,液晶會逐漸回復原有之排列方向,此段時間稱 為應答時間 (response time)。此時間之長短會影響顯示器明暗對比 之程度,此數值也與液晶分子結構及液晶之厚度有關,故一般顯示器 cell gap 控制在 15 μm 左右。 (3) 黏滯性:液晶分子在外加作用力下分子轉動的反應速度與黏滯性 之大小有關:黏性小,反應快。黏滯性取決於分子活化能、溫度及分 子間吸引力。一般而言,液晶分子結構大或分子量大黏滯性相對變大。 故此亦是判斷液晶利用價值之重要指標之一,由於盤狀液晶分子於形 狀上的限制,故黏滯性相當可觀。
(4) 曲彈性 (cuvature elastic property):彈性係數對液晶顯像主要影 響有二:起始電壓與反應時間。彈性係數愈大,則起始電壓相對變大,
不過反應時間也加快。液晶之彈性常數取決於分子結構、形狀及操作 溫度:溫度增加,彈性常數迅速降低。 (5) 折射率 (refractive index):當一束非極化光通過一單軸晶體時, 會形成二束折射光,此種現象稱為雙折射 (birefringence)。液晶就 像是一種單光軸材料,具有二種折射率,當光進入一液晶材料時,光 的電場振動方向與液晶光軸垂直時,稱為 ordinary ray,其折射率為 no;與液晶光軸平行都稱為 extraordinary ray,其折射率為 ne。其雙 折射率之定義由以下說明: Δn = n// - n⊥ = ne - no Δn = 0 → liquid
Δn ≠ 0 → crystal or liquid crystal(birefringence)
液晶之所以具有光學異向性,乃因分子有極化異向 (anisotropic polarizability) 所造成,此現象與介電異向性之原因類似。液晶基於 下列的折射率異向性,而顯現出有用的光學性質: a) 入射光的進行方向會向分子長軸 (director, n) 方向偏向 (入射 於液晶的光會偏向主軸方向進行,此乃因液晶中 n// > n⊥,且光速 與折射率成反比,故與主軸平行的速率 v// 應比垂直方向速率 v⊥ 為 慢所致) b) 可改變入射光的偏光狀態 (直線、橢圓、圓偏光) 及偏光方向
c) 可將入射偏光依左右的旋光性而反射或使透過液晶之雙折性質是 使其液晶相具有鮮明色澤之原因,亦是辨別何種液晶相使用識別技巧, 後續會有詳細說明。 (6) 流變性質:此乃針對液晶高分子而言特殊性質。由於在液晶相時 分子具有規則性之排列,可減少分子間之糾纏,故液晶高分子較一般 高分子材料黏度低,流變性質高有利於模型之製成。 1-2-3-3 液晶相的觀察與鑑定 液晶亦被稱之為異方性液體,具有單一光軸特性。液晶分子之光 軸與分子軸方向一致,其液晶的光學性質為正,如:層列型或向列型 液晶;反之,如膽固醇型液晶之光軸則與螺旋軸方向一致,故其光學 性質為負。而液晶正負光學特性,最常見的觀察方法,乃利用偏光顯 微鏡觀察液晶所特有的雙折射性的光學紋理。將液晶分子置於二薄玻 璃片間,並架設好加熱裝置,通常在垂直偏光板下觀察。此手法可初 略識別液晶種類及決定液晶相的轉移溫度。即使是同名稱的光學紋理, 若液晶相不同則所觀測的光學紋理也會呈微妙的不同。而且,同一液 晶其所生成的紋理也會因所夾液晶分子玻璃片的表面狀態、液晶分子 狀態及液晶相的生成過程等不同而有顯著的不同。 一般而言,由等方向性液體行冷卻過程做觀察。向列型液晶於冷
卻過程中,在等方向性液體的暗視域上先有多數的光輝小球狀紋理 (droplet texture) 生成,其次這些小球會生長,集合而成纖維狀紋 理 (threaded texture) 及 schlieren texture。層列型液晶在等方向性 液體的暗視野中,先有多數的短棒狀紋理 (batonet texture) 及星狀 紋理 (star texture) 出現,這些將會交錯,集合而成種種的扇狀紋 理 (fan-shaped texture) 及 mosaic texture。尤其是,微細狀帶線扇 狀組織為chiral smectic C (強介電性) 液晶所特有。此扇狀組織於 膽固醇型液晶中亦可被發現,但在膽固醇型液晶下,若將二片玻璃性 稍微挪動時,則可轉移至特徵性的呈真珠光的 planer texture。表各種 液晶之特徵性雙折射光學。
1-2-3-4 高分子穩定型液晶 (Polymer Stablized Liquid Crystal)
Vorflusev 與 Kumar[39-40] 等人報導,在照光聚合後,高分子和 液晶小分子會產生相分離。高分子聚集在靠近 UV 光源的上玻璃基 板,而液晶小分子則會被排擠到下玻璃基板,如 Figure 1-2-3. 所示。
Figure 1-2-3. Schemtic of the phase-separated composite films (PSCOF)
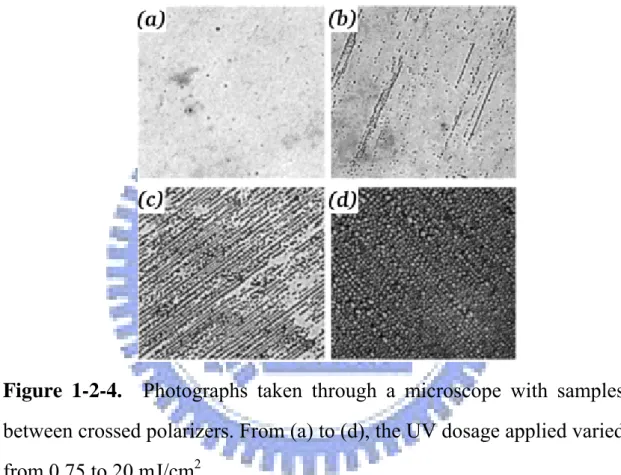
而在相分離機制上,該團隊也有做些探討。首先是 UV 光源的 強度對高分子的影響,從圖九,作者發現到當 UV 光源越弱,所行 成的薄膜越均勻,而當光源強度慢慢增強時,高分子就較易形成為水 滴狀。
Figure 1-2-4. Photographs taken through a microscope with samples
between crossed polarizers. From (a) to (d), the UV dosage applied varied from 0.75 to 20 mJ/cm2.
此外,對於其他影響單體聚合的因素,可由下公式來說明。
厚度,而 χ1 為 Flory-Huggins theory 的交互作用參數 (interaction
parameter),Jψ 單體擴散流率 (diffusion current)。
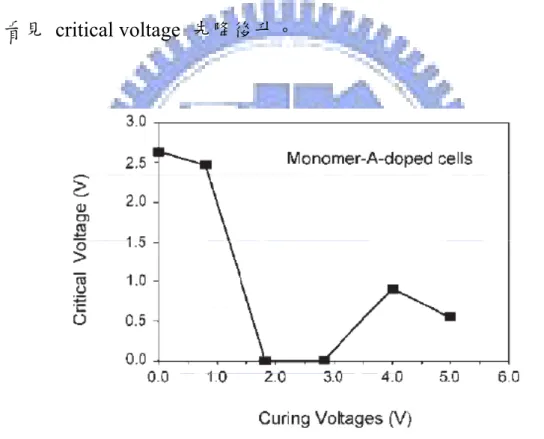
Chen[41] 等人於 2006 年 Japanese Journal of Applied Physics 中, 發表了利用高分子光配向技術在 polymer-aligned liquid-crystal Pi Cell 中,splay-to-bend transition 之臨界電壓 (critical voltage) 會隨著 不同 curing 電壓而改變,如 Figure 1-2-5. 所示,增加 curing voltage 可看見 critical voltage 先降後升。
Figure 1-2-5. Dependence of critical voltage for splay-to-bend transition
1-3 研究動機
光學彎曲補償(Optically Compensated Bend (OCB) Mode)液晶 顯示模組為一種液晶分子呈現上下對稱排列方式,有光學自我補償特 性之液晶顯示模組,如 Figure 1-3-1.所示,
Figure 1-3-1. Construction of a typical OCB-cell[44]
具有廣視角(wide viewing angle)以及快速應答(fast response) 等好處。
Figure 1-3-2. Schematic liquid crystal director orientation of
splay-to-bend transition in OCB-cell and a calculated Gibbs free energy vs. applied voltage in splay and bend states.[45-46]
摻雜光聚合性單體(photocurable monomer)於液晶盒,在照光 聚合後會形成相分離複合薄膜(phase-seperated composite film (PSCOF)),產生高分子穩定型液晶(polymer-stablized liquid crystal
(PSLC))。另一方面由於氧化鋅具有高介電常數,摻雜入高分子穩定 型液晶盒中,能補足高分子之低介電常數。且氧化鋅的寬能隙 (wide band gap)特性,使吸光範圍在可見光以外,因此具有良好的透明性, 將其應用於液晶顯示器,預期能減少穿透度的下降。本實驗利用雙壓 克力基的光聚合性單體,以及在氧化鋅奈米粒子表面改質為甲基壓克 力基,將兩者摻雜於E7 液晶後再進行照光聚合,進一步探討其光電 性質。 氫鍵型超分子結構液晶材料一直是本實驗室所研究方向之一, 然而再將氧化鋅之奈米結構進行表面改值後,即可與另一有機分子形 成超分子結構。本實驗合成出其中一端具有苯酸基的層列相液晶高分 子,另一方面合成出氧化鋅奈米粒子及奈米棒,並修飾為具有砒啶基 的官能基,使兩者間可以形成氫鍵作用力,進而探討其性質。
2-1 實驗儀器
1. 真空系統 (Vacuum Line & Schlenk line) 2. 偏光顯微鏡 (Polarized Optical Microscope) 型號:LEICA DMLP
偏光顯微鏡以兩片偏光片加上 Mettler FP900 與 FP82HT 組合 之加熱裝置,觀察樣品在加熱或冷卻過程中光學條紋之變化。可初步 判斷樣品是否具有液晶性質及其液晶相種類與溫度範圍。一般下偏光 片稱為 polarizer,上偏光片稱為 analyzer,上下偏光片交角為 90°。 3. 超導核磁共振光譜儀 (Nuclear Magnetic Resonance)
型號:Varian Unity-300
檢驗方法:將樣品溶於 d-solvent 中,利用所測得之 1H 與 13C 光譜 判斷化合物之結構與純度。化學位移單位為 ppm (δ),偶合常數單位 Hz,使用之 d-solvent 分別為 CDCl3、DMSO-d6、D2O。
d-solvent 1H (ppm, δ)
CDCl3 7.26
DMSO-d6 2.49
D2O 4.72
型號:TA TGA Q500 5. 紅外線光譜儀(Infrared Spectrometer) 型號:Perkin-Elmer Spectrum 100 型 6. 元素分析儀 (Elemental Analyzer) 型號:Perkin-Elmer 240C 由交通大學貴重儀器中心代測樣品。
7. 示差掃描熱量計 (Differential Scanning Calorimeter, DSC) 型號:Perkin Elmer Pyris 7
8. X 光粉末繞射儀(Powder X-ray Diffractometer) 國家同步輻射研究中心 BL01C 及 BL17A 9. 紫外光曝光機 型號:CL-1000L 燈源為 5 支 8 瓦特的雙燈管,輸入規格為交流電 115 伏特/60 赫茲/0.7 安培,主要波長為 365 nm,有效照射範圍 12.7×30.5×25.4 cm。
10. 光功率檢測計 (Optical Power Meter) 型號:Newport 1830-c
11. 任意波形產生器 (Function Generation) 型號:GW GFG-813
12. 數位示波器 (Digital Oscilloscope) 型號:Tektronix TDS 301213
13. 氦氖雷射 (He-Ne Laser)
型號:Unipgase,10 mW,波長 633 nm
14. 高速電源輸出放大器 (High Speed Power Amplifier) 型號:HPA20H10M 15. 穿透式電子顯微鏡 型號:JOEL JEM-2100 16. 紫外-可見光光譜儀 型號:Perkin-Elmer Lamda 9 17. 螢光光譜儀 型號:Hitachi F-4500
2-2 實驗藥品
溶劑 廠商
Acetone ECHO Dichloromethane Seechem
Ethyl Acetate ECHO
n-Hexane ECHO Tetrahydrofuran Mallinckrodt Ethanol Showa
Diethyl Ether TEDIA
Toluene TEDIA Triethylamine TEDIA Chloroform TEDIA Methanol ECHO Heptane ECHO **無水的 THF 是以金屬鈉乾燥,煮沸蒸餾而得;無水的 CH2Cl2 是 以 CaH2 乾燥,煮沸蒸餾而得;無水的 Et3N 是以 CaH2 乾燥,煮 沸蒸餾而得。 試劑 廠商
Potassium carbonate SHOWA Potassium iodide SHOWA
Tert-butylchlorodimethylsilane ACROS
n-Butyllithium ACROS Imidazole ACROS 2-Isopropoxy-4,4,5,5-teramethyl-1,3,2-dioxaborolane Aldrich
4-Iodopyridine ACROS Tetrakis(triphenylphosphine)palladium Ultra Fine
Tetra-n-butylammonium floride Alfa Aesar 3-(Triethoxysilyl)propyl isocyanate TCI
Dibutyltin dilaurate TCI Lithium bis((trifluoromethyl)sulfonyl)amide ACROS Magnesium sulfate, anhydrous SHOWA Potassium hydroxide SHOWA Sodium hydroxide SHOWA
Zinc Acetate SHOWA
Zinc Chloride RDH
4,4’-biphenol ACROS
2,6-Di-tert-butyl-4-methylphenol Lancaster
Methacryloyl chloride Lancaster
Ammonium chloride SHOWA
2-3 合成步驟
2-3-1. 合成不同大小之氧化鋅奈米粒子
[36] 將 3.29 g (15.0 mmol) 之 Zn(OAc)2.2H2O 溶於 150 mL 之 ethanol 中,在氮氣下加熱至 80 ℃ 迴流。迴流 2 小時後,開始藉 由 Dean-Stark 裝置移除 90 mL 之 ethanol,繼續回流 1 小時後,再 加入同體積 (90 mL) 的新鮮 ethanol,並冷卻至 0 ℃,形成前驅物溶 液。分別將 0.87 g (20.7 mmol)、1.74 g (41.4 mmol)、2.10 g (50.0 mmol)
之 LiOH.H2O 溶於 90 mL 之 ethanol 中,在 0 ℃ 兩小時內緩慢
加入前驅物溶液中,回至室溫後反應兩小時。待溶液變為澄清,使用 0.2 μm 之 glass fiber filter 過濾。以 3:1 的體積比加入 heptane 將濾 液中的氧化鋅奈米粒子沈澱出來,再使用 6000 rpm 的速度將奈米粒 子分離。最後將之溶回 ethanol 保存。
2-3-2. 合成不同長度之氧化鋅奈米棒
將 4.89 g Zn(OAc)2.2H2O 溶於 210 mL 的 CH3OH 中,攪拌下 加熱至 60 ℃。將 2.43 g 的 KOH 溶於 115 mL 的 CH3OH 中,再 緩慢滴入 Zn(OAc)2.2H2O 的溶液中。於 60 ℃ 持溫 2 個小時後, 降至室溫並使用旋轉濃縮儀抽掉溶劑,最後大約剩下 30 mL 的溶液。 接著分別再於 60 ℃ 加熱 5 小時、12 小時、24 小時、48 小 時後,停止加熱並靜置 2 小時。移除上層溶液,保留下層的白色固 體。再加入 150 mL 的 CH3OH,攪拌 1 小時後再靜置 10 小時。 移除上層溶液,下層再加入 50 mL 的 CH3OH,攪拌 30 分鐘。最 後先用 1500 rpm 的轉速離心,抽掉上層溶液,再用 6000 rpm 的轉 速離心,抽掉上層溶液,最後將所得之白色固體分散於 chloroform 中。
2-3-3. 合成含雙甲基壓克力基之照光聚合單體
Biphenyl-4,4'-diyl bis(2-methylacrylate) (1).將 3.0 g (16.0 mmol) 4,4’-biphenol 與 70.0 mg (0.3 mmol)
2,6-di-tert-butyl-4-methylphenol 置入反應瓶中,抽真空 30 分鐘,在
氮氣下加入 THF 150 mL。再於冰浴下加入 5.0 g (48.0 mmol)
methacryloyl chloride,最後再慢慢加入 15.6 mL (112.0 mmol)的
CH2Cl2 萃取,收取下層 CH2Cl2 溶液。抽乾溶劑後再以 silica gel 管 柱層析純化,沖提液為 hexane/ethyl acetate = 15:1, v/v,得到產物 0.9 g (產率 17%)。 1H NMR (300 MHz, CDCl 3): δ (ppm) 7.57 (dd, 4 H), 7.20 (dd, 4 H), 6.37 (d, 2 H), 5.77 (d, 2 H), 2.08 (s, 6 H).
2-3-4. 合成含砒啶表面改質劑之氫鍵質子受體
反應試劑與條件: (i) 6-bromohexanol, K2CO3, KI, acetone, reflux, 48 h;
(ii) TBDMSCl, imidazole, CH2Cl2, r.t., overnight; (iii) n-BuLi,
2-isopropoxy-4,4,5,5-teramethyl-1,3,2-dioxaborolane, THF, -78 °C, 1.5 h; (iv) 4-iodopyridine, K2CO3, Pd(PPh3)4, toluene/ethanol (3:1, v/v), 90 °C,
5 h; (v) tetra-n-butylammonium floride, THF, r.t., overnight; (vi) 3-(triethoxysilyl)propyl isocyanate, dibutyltin dilaurate, THF, reflux, 24 h.
6-(6-Bromonaphthalen-2-yloxy)hexan-1-ol (1).
將 6-bromonaphthalen-2-ol (7.0 g, 23.1 mmol), 6-bromohexanol (6.6 g, 27.7 mmol), potassium carbonate (9.6 g, 69.3 mmol) 以及少量 potassium iodide (c.a. 15 mg) 置入反應瓶中,再加入 250 mL 的 acetone,攪拌後加熱至迴流,在氮氣下反應 48 小時。降至室溫後, 旋轉濃縮抽乾溶劑,以 CH2Cl2/H2O 萃取。收取有機層以 Na2SO4 除 水,將溶劑抽乾,最後再以 silica gel 管柱層析純化,沖提液為 hexane/ethyl acetate = 3:1 (v/v),得到產物 6.1 g (產率 85%)。 1H NMR (300 MHz, CDCl 3): δ (ppm) 7.90 (d, 1 H), 7.65-7.56 (m, 2 H), 7.48 (dd, 1H), 7.15 (dd, 1 H), 7.08 (d, 1 H), 4.06 (t, 2 H), 3.67 (d, 2H), 1.87 (quint, 2 H), 1.67-1.43 (m, 6 H). (6-(6-Bromonaphthalen-2-yloxy)hexyloxy)(tert-butyl)dimethylsilane (2).
將化合物 1 (6.0 g, 18.6 mmol) 與 imidazole (1.9 g, 27.9 mmol) 溶於 200 mL 無水 CH2Cl2,再將 tert-Butyldimethylsilyl chloride
(TBDMSCl) (3.4 g, 22.3 mmol) 於 0 ℃ 氮氣下加入,回至室溫後反應 隔夜。將溶液加入水中後萃取,先移除有機層,剩餘之水層再以 CH2Cl2 萃取一次。將兩次萃取後之有機層以 Na2SO4 除水後,再旋
轉濃縮抽乾溶劑。最後再藉由 silica gel 快速管柱層析 (flash column chromatography) 純化,沖提液為 hexane/ethyl acetate = 20:1, v/v,得
到產物為白色固體 7.3 g (產率 90%)。 1H NMR (300 MHz, CDCl 3): δ (ppm) 7.90 (d, 1 H), 7.65-7.56 (m, 2 H), 7.48 (dd, 1H), 7.15 (dd, 1 H), 7.07 (d, 1 H), 4.05 (t, 2 H), 3.63(t, 2H), 1.85 (quint, 2 H), 1.61-1.41 (m, 6 H), 0.91-0.88 (m, 9H), 0.07-0.04 (m, 6H). tert-Butyldimethyl(6-(6-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl) naphthalen-2-yloxy)hexyloxy)silane (3). 將化合物 2 (6.0 g, 13.7 mmol) 溶於無水 150 mL 之 THF 中, 在於 -78 °C 氮氣下慢慢加入 n-butyllithium (2.5 M in hexane) 8.2 mL (20.55 mmol) 。 持 續 於 -78 °C 反 應 1.5 小 時 後 , 再 加 入 2-isopropoxy-4,4,5,5-teramethyl-1,3,2-dioxaborolane (5.1 g, 27.4 mmol), 回至室溫後反應隔夜。加水終止反應後以 CH2Cl2 萃取,取有機層加 入無水 Na2SO4 除水,並移去溶劑。最後再藉由 silica gel 快速管柱
層析 (flash column chromatography) 純化,沖提液為 hexane/ethyl acetate = 20:1, v/v,得到產物為白色固體 5.1 g (產率 80%)。 1H NMR (300 MHz, CDCl 3): δ (ppm) 8.28 (s, 1H), 7.80-7.75 (m, 2H), 7.69 (d, 1 H), 7.14-7.104 (m, 2H), 4.07 (t, 2 H), 3.63 (t, 2H), 1.86 (quint, 2H), 1.59-1.41 (m, 6H), 1.38 (s, 12H), 0.91-0.86 (m, 9H), 0.07-0.04 (m, 6H). 4-(6-(6-(tert-Butyldimethylsilyloxy)hexyloxy)naphthalen-2-yl)pyridin e (4).
將化合物 3 (5.0 g, 10.3 mmol)、4-iodopyridine (2.54 g, 12.4 mmol)、 anhydrous potassium carbonate (1.89 g, 13.7 mmol) 溶於 160 mL 之 toluene/ethanol (3:1, v/v) 溶劑中,在室溫下通氮氣 10 分鐘。接著加 入 Pd(PPh3)4 (0.12 g, 0.103 mmol),於氮氣下 90 ℃ 反應 5 小時。冷 卻至室溫後以旋轉溶縮抽乾溶劑,以 CH2Cl2/H2O 萃取。收取有機層 以 Na2SO4 除水,將溶劑抽乾,最後再以 silica gel 管柱層析純化, 沖提液為 CH2Cl2,得到產物 3.5 g (產率 78%)。 1H NMR (300 MHz, CDCl 3): δ (ppm) 8.68 (dd, 2H), 8.05 (d, J = 1 H), 7.82 (dd, 2H), 7.71 (dd, 1H), 7.62 (dd, 2 H), 7.22-7.16 (m, 2 H), 4.10 (t, 2 H), 3.64 (t, 2H), 1.88 (quint, 2 H), 1.67-1.44 (m, 6 H), 0.91-0.88 (m, 9H), 0.07-0.04 (m, 6H). 6-(6-(Pyridin-4-yl)naphthalen-2-yloxy)hexan-1-ol (5). 將化合物 4 (3.0 g, 6.88 mmol) 溶於 50 mL 之 THF 中,加入 13.76 mL (13.76 mmol) 的 tetra-n-butylammonium floride (1M solution in THF)。反應隔夜之後,加水終止反應,並以 CH2Cl2 萃取,使用 Na2SO4 除水再抽乾溶劑。最後再以 silica gel 管柱層析純化,沖提 液為 CH2Cl2/THF = 10:1, v/v,得到產物為白色固體 2.2 g (產率 86%)。 1H NMR (300 MHz, CDCl 3): δ (ppm) 8.67 (dd, 2H), 8.05 (d, 1H), 7.82 (dd, 2H), 7.71 (dd, 1H), 7.62 (dd, 2 H), 7.22-7.16 (m, 2 H), 4.11 (t, 2 H),
3.69 (t, 2H), 1.89 (quint, 2 H), 1.66-1.44 (m, 6 H).
6-(6-(Pyridin-4-yl)naphthalen-2-yloxy)hexyl 3-(triethoxysilyl)propylcarbamate (6).
將化合物 5 (2.0 g, 5.76 mmol) 溶於 40 mL 的 THF 中,在室溫、 通氮氣下將 2.84 g (11.48 mmol) 的 3-(triethoxysilyl)propyl isocyanate 與 36 mg (0.058 mmol) 的 dibutyltin dilaurate 慢慢滴入。加熱至迴流 後反應 24 小時後,抽乾溶劑再以 silica gel 快速管柱層析 (flash column chromatography) 純化,沖提液為 hexane/ethyl acetate = 1:2, v/v,得到產物為白色蠟狀固體 1.84 g (產率 56%)。 1H NMR (300 MHz, CDCl 3): δ (ppm) 8.68 (dd, 2H), 8.05(d, 1H), 7.82 (dd, 2H), 7.72 (dd, 2H), 7.62 (dd, 2H), 7.22-7.16 (m, 2H), 4.89 (s, 1 H), 4.13-4.05 (m, 4H), 3.82 (quart, 6 H), 3.18-3.13 (m, 2 H), 1.87 (quint, 2 H), 1.67-1.43 (m, 2H), 1.22 (t, 9 H), 0.63 (t, 2 H).
HRMS (EI): calcd. for C31H44N2O6Si, 568.2962; found 568.2968. Anal.
Calcd. for C31H44N2O6Si: N, 4.93; C, 65.46; H, 7.80. Found: N, 4.90; C,
2-3-5. 合成具層列相之液晶高分子氫鍵質子予體
反應試劑與條件:(a) DHP, PPTS, CH2Cl2, rt, 24 h; (b) (i) n-BuLi, THF,
-78 °C, 1.5 h; (ii) 2-isopropoxy-4,4,5,5-teramethyl-1,3,2-dioxaborolane, -78 °C to rt, overnight; (c) 1,4-dibromo-2,5-dimethoxy-benzene, K CO ,
Pd(PPh3)4, toluene/ethanol (3:1, v/v), 90 °C, 6 h; (d) 4-ethynylbenzoic
acid methyl ester, Pd(PPh3)2Cl2, CuI, PPh3, Et3N/THF (2:1, v/v), 70 °C,
overnight; (e) TsOH*H2O, methanol/CH2Cl2 (1:1, v/v), rt, overnight; (f)
10-bromodecanol, K2CO3, KI, acetone, reflux, 48 h; (g) KOH,
ethanol/THF (1:1, v/v), reflux, overnight; (h) acryloyl chloride,
N,N-dimethylaniline, 2,6-di-tert-butyl-4-methylphenol, dioxane, 50 °C, 4
h; (i) AIBN, THF, 65 °C, 48 h.
4-((4'-(10-(acryloyloxy)decyloxy)-2,5-dimethoxybiphenyl-4-yl)ethynyl )benzoic acid, monomer (8).
Yield: 1.15 g (70%). 1H NMR (300 MHz, CDCl3): δ (ppm) 8.09 (d, J = 8.7 Hz, 2H), 7.66 (d, J = 8.7 Hz, 2H), 7.49 (d, J = 8.7 Hz, 2H), 7.10 (s, 1H), 6.96 (d, J = 8.7 Hz, 2H), 6.89 (s, 1H), 6.40 (dd, J = 17.4 Hz, J = 1.5 Hz, 1H), 6.12 (dd, J = 17.4 Hz, J = 10.5 Hz, 1H), 5.82 (dd, J = 10.2 Hz, J = 1.5 Hz, 1H), 4.16 (t, J = 6.6 Hz, 2H), 4.00 (t, J = 6.6 Hz, 2H), 3.92 (s, 3H), 3.80 (s, 3H), 1.81 (quint, J = 6.6 Hz, 2H), 1.67 (quint, J = 6.6 Hz, 2H), 1.58−1.32 (m, 12H). HRMS (EI): calcd for C36H40O7, 584.2774;
found 581.3146. Anal. Calcd for C36H40O7: C, 73.95; H, 6.90. Found: C,
73.96; H, 7.00.
PBBBA, homopolymer (9).
Yield: 0.4 g (40%). Anal. Calcd. for C36H40O7: C, 73.95; H, 6.90. Found:
2-3-4 氧化鋅奈米結構之表面改值
2-3-4-1 合成甲基壓克力基表面改值之氧化鋅奈米粒子 將 3.29 g (15mmol) 之 Zn(OAc)2.2H2O 溶 於 150mL 之 ethanol 中,在氮氣下加熱至 80 ℃ 迴流 3 小時。在迴流 2 小時後, 開始藉由 Dean-Stark 裝置移除 90 mL 之 ethanol,接著再加入同體 積 (90 mL) 的新鮮 ethanol,並冷卻至 0 ℃,形成前驅物溶液。 分別將 0.87 g (20.7 mmol) 之 LiOH.H2O 溶於 90 mL 之 ethanol 中,在 0 ℃ 兩小時內緩慢加入前驅物溶液中,回至室溫後 反應兩小時,待溶液變為澄清,停止加熱。 將 6.0 g 的 3-(trimethoxysilyl)propylmethacrylate 溶於 10 mL 的 ethanol,在 0 ℃ 下緩慢加入上述溶液中,加完後保持在室溫反 應 12 小時。反應結束後使用 0.2 μm 之 glass fiber filter 過濾,並以 3:1 的體積比加入 heptane 將濾液中的氧化鋅奈米粒子沈澱出來,使用 6000 rpm 的速度,將奈米粒子分離。最後將之溶回 ethanol 保
2-3-4-2 合成砒啶基表面改值之氧化鋅奈米粒子與奈米棒 將步驟 2-3-1 與 2-3-2 合成出之奈米粒子與奈米棒以 purge 氮 氣的方式除去溶劑後 (200 mg) 置入反應瓶,在氮氣下加入 10 mL 的 toluene , 並 快 速 攪 拌 。 另 外 將 1 g 的 6-(6-(pyridin-4-yl)naphthalen-2-yloxy)hexyl 3-(triethoxysilyl)propylcarbamate 溶於 5 mL 的 toluene 中,再將之緩 慢加入上述溶液中。接著加熱至 110 ℃ 反應 12 小時,冷卻後再用 4000 rpm 的速度離心,並用 toluene 離心清洗多次後,將之保存於 CH2Cl2 中。
2-4 光電量測方法及裝置
利用液晶 E7 (Δε
= 13.8,Δ n = 0.2246,購自 Merck)分別溶 入不同比例之單體 (含雙甲基壓克力基) 以及表面改值過後 (含單甲 基 壓 克 力 基) 之 ZnO 奈 米 粒 子 , 藉 由 毛 細 現 象 填 入 optical compensated bend (OCB) 之液晶 cell (cell gap = 4.25 μm, active area = 1 cm2,購自美相)中,接著平放置 UV 曝光機平台上,以特定 UV 波長與外加電壓進行照光聚合。光電性質測量的儀器架設如 Figure
Figure 2-4-1. Experimental setup of the electro-optical property
3-1 氧化鋅奈米粒子性質討論
本實驗利用改變不同 LiOH 與 Zn(OAc)2 相對濃度的方式,來 調 控 不 同 粒 徑 大 小 之 氧 化 鋅 奈 米 粒 子 , 濃 度 比 分 別 為 [LiOH]/[ Zn(OAc)2] = 1.4, 2.8, 3.3。再利用紫外-可見光光譜儀、螢光 光譜儀、X-ray 粉末繞射儀及穿透式電子顯微鏡,以鑑定其結構和性 質。3-1-1
紫外-可見光光譜及螢光光譜性質結果
將 ZnO 奈米粒子溶於 ethanol 測得的紫外-可見光光譜數據,如 Figure 3-1-1. 下所示: 280 300 320 340 360 380 400 420 0 1 2 Ab so rb an ce (a .u .) Wavelength (nm) (a) (b) (c) λ1/2Figure 3-1-1. UV-Vis absorption spectra of ZnO nanoparticles with (a)
[LiOH]/[Zn(OAc)2] = 1.4 (b) [LiOH]/[Zn(OAc)2] = 2.8, and (c)
[LiOH]/[Zn(OAc)2] = 3.3.
定波長處呈現出一 shoulder 形式的氧化鋅特性吸收峰。文獻中指出, 由Meulenkamp[42] 之經驗式,可以估計氧化鋅奈米粒子的粒徑大小: 1240 λ ⁄ 3.301 294.0 D 1.09 D 其中,λ ⁄ 為 absorption shoulder,D 為粒子平均粒徑。 將測得的數據代入以上經驗式,以得到的粒子平均粒徑整理於下表: [LiOH]/[Zn(OAc)2] λ1/2 (nm) Diameter (nm) 1.4 347 3.5 2.7 331 2.7 3.3 320 2.3 由結果得知,當隨著 [LiOH]/[Zn(OAc)2] 濃度比例的增加,此 shoulder 的 onset 波長(λ1/2)會隨之降低,計算出之粒子平均粒徑 大小也隨之遞減。 將氧化鋅奈米粒子溶於 ethanol 測得的螢光光譜數據如 Figure 3-1-2.所示,可發現放光波長隨著粒子平均粒徑的變小而愈往藍位 移。
300 400 500 600 700 800 0 1 (a) (b) (c) PL Inte ns it y (a .u.) Wavelength (nm)
Figure 3-1-2. Photoluminescence spectra of ZnO nanoparticles with (a)
[LiOH]/[Zn(OAc)2] = 1.4 (b) [LiOH]/[Zn(OAc)2] = 2.8, and (c)
[LiOH]/[Zn(OAc)2] = 3.3
3-1-2 X-ray 粉末繞射
結果
Figure 3-1-3. 為 X-ray 粉末繞射的結果,與 JCPDS card 的 wurtzite(JCPDS 36-1451)結構相吻合。比較不同 [LiOH]/[Zn(OAc)2] 比例所製備得之氧化鋅奈米粒子之 X-ray 粉末繞射圖可知,隨著 [LiOH]/[Zn(OAc)2] 比例的增加,繞射峰的寬度會隨之變大。根據此 結果,可使用 Scherrer’s equation 來估計奈米粒子的粒徑大小: D 0.89λ βcosθ 其中,λ為 X-ray 波長 (0.775 Å),β 為繞射峰的半高寬(full
width at half maximum, FWHM),θ 為 Bragg 繞射角度。根據 (110) 晶面的繞射峰,計算出奈米粒子的粒徑大小依序為 3.9 nm、2.6 nm 及 2.3 nm,此結果與由紫外-可見光吸收光譜所得到之趨勢相同。 10 20 30 40 10 20 30 40 2θ (degree) (a) (100) (101) (102)(110)(103)(112) (b) (c)
Figure 3-1-3. Powder X-ray diffraction spectra of ZnO nanoparticles
with (a) [LiOH]/[Zn(OAc)2] = 1.4 (b) [LiOH]/[Zn(OAc)2] = 2.8 (c)
3-1-3 穿透式電子顯微鏡分析
Figure 3-1-4. 為 TEM 之圖片,圖 (a) 為改值甲基壓克力基前 氧化鋅奈米粒子之分佈情形;圖 (b) 則為改值後氧化鋅奈米粒子之 分佈情形。由圖可看出奈米粒子的粒徑大小大約都在 3 – 5 nm 之間, 改值後之氧化鋅奈米粒子較為分散。
(a)
(b)
Figure 3-1-4. TEM images of ZnO nanoparticles with (a)
[LiOH]/[Zn(OAc)2] = 1.4 and (b) Metharyl-modified ZnO nanoparticles
3-2 氧化鋅奈米棒性質討論
本實驗利用改變不同的持溫時間,合成出不同長度之氧化鋅奈米 棒,並探討在不同的反應溶劑與持溫溫度下,會對形成之氧化鋅奈米 結構造成何種影響。利用紫外-可見光光譜儀、X-ray 粉末繞射儀及穿 透式電子顯微鏡,以鑑定其性質。3-2-1
紫外-可見光光譜性質結果
由 Figure 3-2-1. 之紫外-可見光光譜圖可看到改變不同之持溫 (60℃)時間以及不同的與持溫溫度(80℃)與反應溶劑(ethanol), 其吸收波長約在 375 nm,且在不同的反應條件下並無明顯差異。但 相對奈米粒子來說,此吸收波長已有明顯的紅位移。 300 400 500 600 0.0 0.5 1.0 A b sor b anc e (a.u. ) Wavelength (nm) (a) (b) (c) (d) (e) (f)Figure 3-2-1. UV-Vis absorption spectra of ZnO nanostructures prepared
under different conditions. (a) 60℃ for 5 h; (b) 60℃ for 12 h; (c) 60 ℃ for 24 h; (d) 60℃ for 48 h; (e) 80℃ for 12 h; (f) 60℃ for 12 h in ethanol.
3-2-2 穿透式電子顯微鏡分析
Figure 3-2-2. 為 TEM 之圖片,圖 (a) 為於 60 ℃ 持溫 5 小 時的結果,可看出為短棒狀結構,寬度約在 5 - 10 nm,長度則約為 10 – 20 nm。圖 (b) 為於 60 ℃ 持溫 12 小時的結果,可看出棒狀 結構已增長至30 – 50 nm,但仍可看出還有一些球狀的粒子在其中。 圖 (c) 為於 60 ℃ 持溫 24 小時的結果,可看出為棒狀結構長度已 可達到 80 – 100 nm 左右,已經沒有看見球狀的奈米粒子。圖 (d) 為 於 60 ℃持溫 48 小時的結果,可看出為棒狀結構長度已達 100 – 120 nm 左右。圖 (e) 為於 80 ℃持溫 12 小時的結果,可看出為棒 狀結構長度仍為30 – 50 nm 左右。圖 (f) 為將甲醇改變為乙醇作為反 應溶劑,於 60 ℃ 持溫 12 小時的結果,可看到沒有形成棒狀結構反 而形成大小不一且球狀的奈米粒子,粒徑大小為 10 – 30 nm 左右, 此現象則與文獻中[27]所提及乙醇比起甲醇有利於棒狀晶體成長的結 果則相反。
(a) (b) (c)