國立宜蘭大學自然資源學系碩士論文 Department of Natural Resources
National Ilan University Master Thesis
六種殼斗科苗木之光度適應性研究
Study on Light-Intensity Adaptabilities of Six Fagaceae Species Seedlings
指導教授:林世宗 博士 Shu-Tzong Lin Ph.D.
研究生:葉韋欣 By:Wei-Hsin Yea
中華民國96 年 6 月
i
中文摘要
本研究將青剛櫟、錐果櫟、赤皮、毽子櫟、長尾尖葉櫧、鬼石櫟之苗 木栽植於模擬林下孔隙之蔭棚中(分別為相對光度60%、10%與3%),比較其 形質生長、光合能力與光消散機制,探討其光適應性。
各樹種之苗高、根徑、生物量與根部生物量分配比例皆隨處理光度之 增加而提升,但長尾尖葉櫧與鬼石櫟之苗高則於相對光度10%中具最大值。
葉面積比(LAR)與比葉面積(SLA)隨著遮蔭程度之增加而提升,反映出 低光處光合器官比例之提升與葉片之薄化,並以赤皮與毽子櫟調整幅度最 為明顯。葉綠體色素濃度隨遮蔭程度之增加而提升,Chl a/b與Car/Chl則呈 相反之趨勢,但赤皮之Chl a/b在各光處理間則無差異,此意味著樹種於低 光處將提升吸光效率與在高光處將增加光保護性物質。
最大總光合速率(Amax)、暗呼吸率(Rd)、光補償點(LCP)、最大電子傳遞 速率(ETRmax)與非光化學消散(NPQ)皆隨環境光度的提升而有增加之趨勢,
但長尾尖葉櫧與鬼石櫟之Amax與ETRmax則是在相對光度10%中具最大值。錐 果櫟之光量子效率(Qy)於相對光度60%中具有最大值,其餘的5種試驗樹種 則是在相對光度10%時具最大值。
午夜時除了毽子櫟之 PSII 最大光能轉換效率(Fv / Fm)於遮光處理間幾無 差異外,其餘者皆在相對光度 60%具較低值,顯示具有長期光抑制現象,
殊以長尾尖葉櫧最為嚴重;於此相對光度下,青剛櫟、錐果櫟、赤皮與毽 子櫟在正午時,其PSII 實際光能轉換效率(ΦPSII)約為長尾尖葉櫧與鬼石櫟之 2 倍;此時各樹種之熱消散(NPQ)皆為當日最大,並以錐果櫟、長尾尖葉櫧 與鬼石櫟之值最高、青剛櫟與赤皮次之,而毽子櫟最低。Fv / Fm在正午時,
青剛櫟、錐果櫟與毽子櫟之值較高,而赤皮、長尾尖葉櫧與鬼石櫟則較低。
螢光參數日域變化顯示出青剛櫟、錐果櫟與毽子櫟之非光化學消散主成份 為熱消散,而赤皮、長尾尖葉櫧與鬼石櫟則是光破壞與熱消散。
ii
依試驗結果顯示,青剛櫟、錐果櫟與毽子櫟光適應範圍較大。赤皮適 生於中高光域,鬼石櫟則為中低光域,於高光處皆易受光破壞。長尾尖葉 櫧在小孔隙環境具較好之生長與光合能力,其光適應範圍最狹窄。
【關鍵詞】殼斗科、生長、生物量、光合作用、葉綠素螢光、光適應、光 抑制。
iii
Abstract
This study explored the light-intensity adaptabilities of seedlings of Cyclobalanopsis glauca,Cyclobalanopsis longinux, Cyclobalanopsis gilva, Cyclobalanopsis sessililfolia, Castanopsis cuspidata var. carlesii and Lithocarpus castanopsisifolius. The seedlings were planted in 3 artificial shade houses(60%, 10% and 3% of full sun, respectively) to simulate light environments under forest canopy. The study will focus on growth performance, photosynthetic capacity, and mechanisms of light energy quenching.
Net growth, biomass, and biomass allocation to roots generally increased with increasing irradiation. However C. cuspidata var. carlesii and L.
castanopsisifolius grown under 10% of full sun had the highest net height growth.
Leaf area ratio(LAR) and specific leaf area(SLA) increased with increasing shaded, which enhanced photosynthetic apparatus ratio and reduced leaf thickness in relatively shaded place, in especially C. gilva and C. sessililfolia.
Chlorophyll and carotenoid content per unit mass increased with increasing shade, whereas Chl a/b and Car/Chl had opposite tendency. The results suggested that all species will enhance absorption efficiency in low light environment and will increase photoprotection substances in high light environment. But, Chl a/b of C. gilva didn’t differ significantly among 3 light regimes.
The maximum photosynthetic rate (Amax), dark respiration (Rd), light compensation point (LCP), maximum electron transport rate (ETRmax) and non-photochemical quenching parameter (NPQ) increased with increasing irradiation, while C. cuspidata var. carlesii and L. castanopsisifolius grown under 10% of full sun had the highest Amax and ETRmax. C. longinux grown under 60% of full sun had highest quantum yield (Qy), and the others grown under 10% of full sun had highest quantum yield.
iv
At midnight, maximum photochemical efficiency of PSII (Fv / Fm) of C.
sessililfolia was no significant difference among shade treatments, but other species grown under 60% of full sun had the lowest Fv / Fm suggesting chronic photoinhibtion, in especially C. cuspidata var. carlesii. At midday, ΦPSII of C.
glauca, C. longinux, C. gilva, and C. sessililfolia doubled that of C. cuspidata var. carlesii and L. castanopsisifolius under 60% of full sun. Meanwhile, the NPQ(heat quenching) of all species was highest in the daytime, highest in C.
longinux, C. cuspidata var. carlesii and L. castanopsisifolius, and lower in C.
glauca and C. gilva and then C. sessililfolia. At midday, C. glauca, C. longinux and C. sessililfolia had higher Fv / Fm than C. gilva, C. cuspidata var. carlesii and L. castanopsisifolius. Diurnal changes of fluorescence parameters showed the main factor of non-photochemical quenching of C. glauca, C. longinux and C.
sessililfolia was dissipation into heat, and that of C. gilva, Castanopsis cuspidata var. carlesii and L. castanopsisifolius was heat quenching and photodamage.
In conclusion, C. glauca, C. longinux and C. sessililfolia had a broader range of light adaption. C. gilva grew well in high and medium light regime, and L. castanopsisifolius grew well in medium and low light regime, both more susceptible to photodamage in high-light regime. Castanopsis cuspidata var.
carlesii had greater growth and photosynthesis capability at gap site, and it’s range of light adaption is the narrowest among all species.
【Key words】fagaceae species, growth, biomass, photosynthesis, chlorophyll fluorescence, light adaption, photoinhibition.
v
致謝
論文已達完成之際,回想這段不長也不短的求學路上,自覺受他人幫 忙與提攜甚多,使得本文得以順利完稿,因此將於此章答謝諸位之幫忙。
首先所要感謝的為指導教授林世宗博士,承蒙恩師於就學期間給予的 照顧與指導,使我在生活與學業上皆可無慮。老師於日常間之諄諄教悔,
使我對於人、事、物皆有更深入之瞭解;於學業上之殷切指導,乃至文成 後的逐字匡正,則使本文得以撥雲見日與趨於完善。論文初稿復蒙郭幸榮 博士、關秉宗博士、陳子英博士與鹿兒陽博士等諸位師長費心審稿與斧正 及給予寶貴意見,使本文可以更加完整與嚴謹,在此謹致上由衷感謝。
試驗期間,感謝長芳林業邱老闆於苗圃事務上與苗木管理上的幫忙;
感謝森林保育處棲蘭工作站林進龍主任,楊家凱、林亨勳同學,邱孟韋、
蘇柏翰、江武雋、官信利、蔡彥新、陳廷岡…….等學弟,楊涵馨、李思佳 學妹與陳小姐於試驗上給予之協助;尤其是家凱在我進行預備試驗時,曾 幫忙我至凌晨 3、4 點,特以感謝。在校期間,感謝林欣樺、魏瑞廷、王光 仁與張瑀芳等同學在學業與生活上之相互鼓勵與協助。我想我永遠不忘記 與猪哥、super、小孟、光仁等數人在數個颱風夜中,仍在努力“打拼"之 景象;亦不會忘記與小毛和家凱的定時小聚會,與猪哥在數個冬夜中的溫 泉之旅與光仁、亨勳的每天午晚餐後的閒聊;感謝你們豐富我的在學生活 並使之絢麗多彩。
最後感謝我的家人,在我就學習期間給予的支持,使我無後顧之憂並完 成學業,與感謝莉遜這幾年來的陪伴,謝謝大家。
葉韋欣 謹識于 國立宜蘭大學自然資源研究所 林世宗博士研究室 中華民國九十六年七月
vi
目 錄
摘要 ……… i
Abstract ………..…..………..………... iii
謝誌 ………... v
目錄 ……….………...……… vi
表目錄 ………..………… ix
圖目錄 ……….……….……….………… x
壹、前言 ………..……….………..……… 1
貳、前人研究 ……….……… 3
一、光度對苗木形質與生理之效應 …………...……… 3
(一)光度對苗高與基徑之效應 ………...……… 3
(二)光度對生物量之效應 ……….……… 4
(三)光度對葉部形態參數之效應 ……….……… 5
1.葉面積比 ………..………...…………... 5
2.比葉面積 ………….………...……… 6
(四)葉綠體色素含量 ………….……….……... 7
(五)光合反應曲線 ……….…....………… 8
(六)葉綠素螢光 ………..………. 10
二、光抑制 ……….………….. 15
三、試驗樹種之植群分佈與生態特性 ..………. 19
參、材料及方法 ……….……… 20
一、材料來源 ………...……… 20
二、試驗環境概述與設計 ………... 20
三、環境因子的量測 ………...……… 22
四、試驗方法與步驟 ………. 22
vii
(一)苗高與基徑 ………. 22
(二)葉面積與乾重 ……….……… 22
(三)葉片面積參數 ……….……… 22
(四)葉綠體色素含量測定 ……….……… 23
(五)光合反應曲線之測定 …………..………...…… 23
(六)葉綠素螢光參數之測定 ……….……… 25
1.快速光反應曲線 ………..……….. 25
2.不同處理光度下之 Fv / Fm ………. 26
3.螢光參數之日域變化 ……… 26
六、資料分析 ………..…….……….. 27
肆、結果 ……….………… 28
一、試驗地環境參數量測之比較 ………...……… 28
二、苗高與基徑之淨生長 ………...……… 31
三、生物量累積與分配 ………... 33
四、葉面積參數 ………..…………. 39
(一)葉面積比 ………. 39
(二)比葉面積 ……….……… 40
五、葉綠體色素含量 ………...……… 41
六、光合反應曲線與氣體交換參 ………..……… 44
(一)最大總光合作用速率 ……….……… 45
(二)暗呼吸速率 ………...………….. 46
(三)光量子效率 ……….……… 47
(四)光補償點 ……….……… 48
七、葉綠素螢光參數 ……….……… 49
(一)快速光反應曲線 ………. 49
viii
1.最大電子傳遞速率 ………...………. 49
2.非光化學消散 ………...………. 50
(二)PSII 最大光能轉換效率 ………..………. . 51
(三)螢光參數之日域變化 ……….…… 52
1.PSII 實際光能轉換效率之日域變化 ………....…… 52
2.非光化學消散之日域變化 …...………..………. 54
3.PSII 最大光能轉換效率之日域變化 ...……….. 56
伍、討論 ………...……….. 58
一、光度對苗木形質生長之效應……….……...………. 58
(一)苗高與基徑之淨生長 ………. 58
(二)生物量累積與分配 ………. 59
(三)葉面積參數 ………. 61
(四)葉綠體色素含量 ……… 63
二、試驗樹種之光合能力 ……….………..….. 66
(一)光合反應曲線之參數 ………. 66
(二)快速光反應曲線之螢光參數 ………. 70
三、試驗樹種之光消散方式 ……….………..……….. 73
四、試驗樹種生理生態特性 ……….……… 78
陸、結論 ……….……… 82
柒、參考文獻 ………. 84
捌、附錄 ………...…94
ix
表目錄
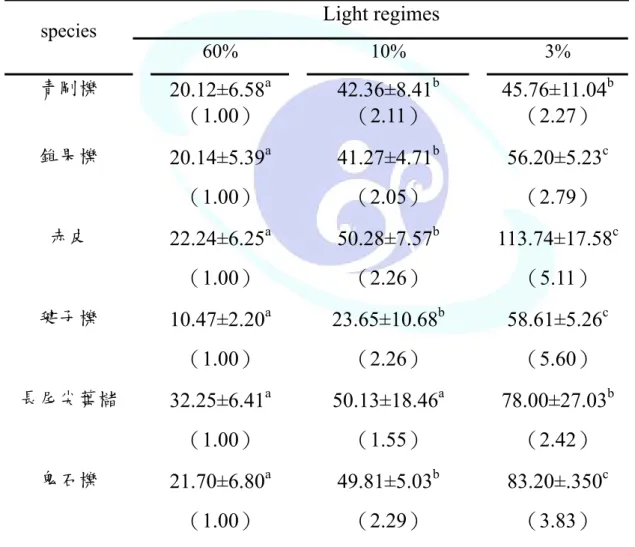
表 1. 不同處理光度下之 6 種試驗樹種之淨苗高生長與淨基徑生長 ... 31 表 2. 不同處理光度下之 6 種試驗樹種的葉面積比 …………...…….. 39 表 3. 不同處理光度下之 6 種試驗樹種的比葉面積 ……….… 40 表 4. 不同處理光度下之 6 種試驗樹種單位葉重下葉綠素、類胡蘿蔔素含 量與 Chl a/b、Car/Chl ………….………. 42 表 5. 不同光度處理下 6 種試驗樹種之最大光合作用速率 ……….… 45 表 6. 不同光度處理下 6 種試驗樹種之暗呼吸速率 ……….…… 46 表 7. 不同光度處理下 6 種試驗樹種之光量子效率 ………...…..…… 47 表 8. 不同光度處理下 6 種試驗樹種之光補償點 …………..…..……. 48 表 9. 不同光度處理下 6 種試驗樹種之 ETRmax …….…………..…….. 49 表 10. 在 RLC 光階為 1820 μmol photon m-2sec-1情況下,不同光處理的 6 種試驗樹種之 NPQ ……… 50
x
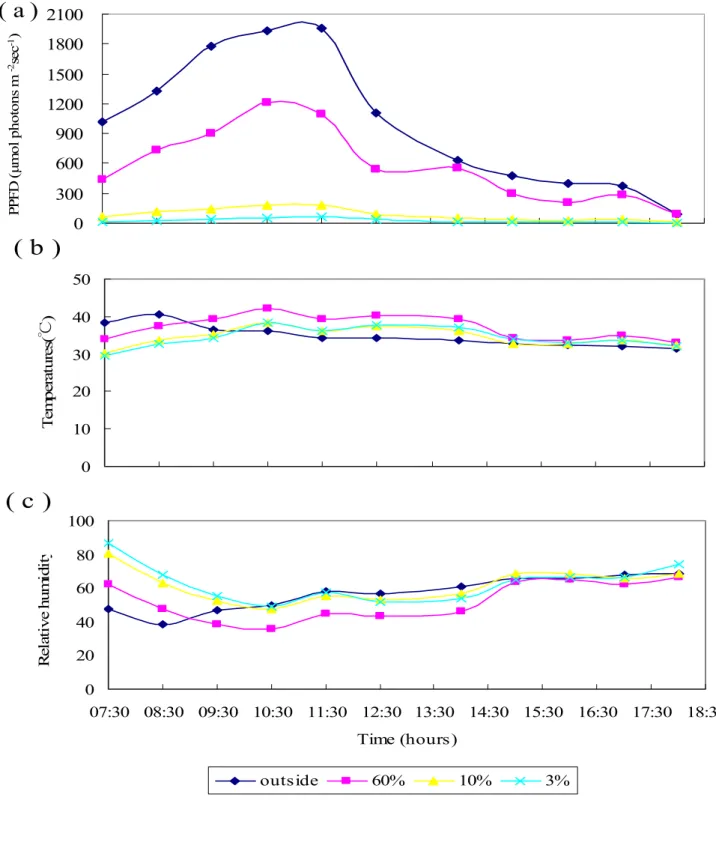
圖目錄
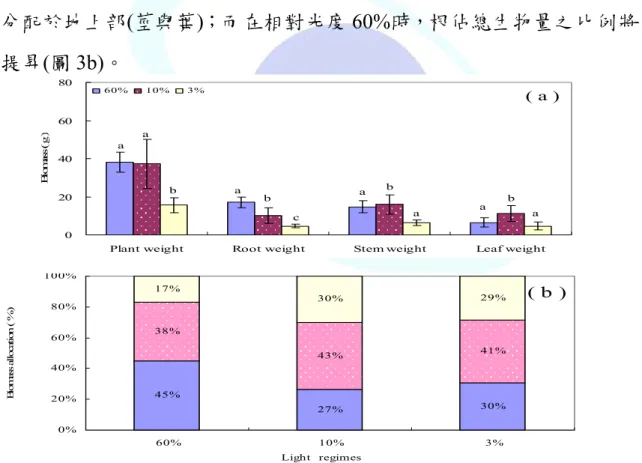
圖1、2006.02.14 試驗地(a)光度、(b)溫度與(c)相對濕度之日域變化 …... 29 圖2、2006.07.06 試驗地(a)光度、(b)溫度與(c)相對濕度之日域變化 .… 30 圖3、(a)青剛櫟於不同光度下,根、莖、葉與植物之生物量;(b)不同光 度下,青剛櫟生物量分配於根莖葉之比例 ……….… 33 圖4、錐果櫟於不同光度下,各部位之生物量(a)與生物量分配於各部位(根、
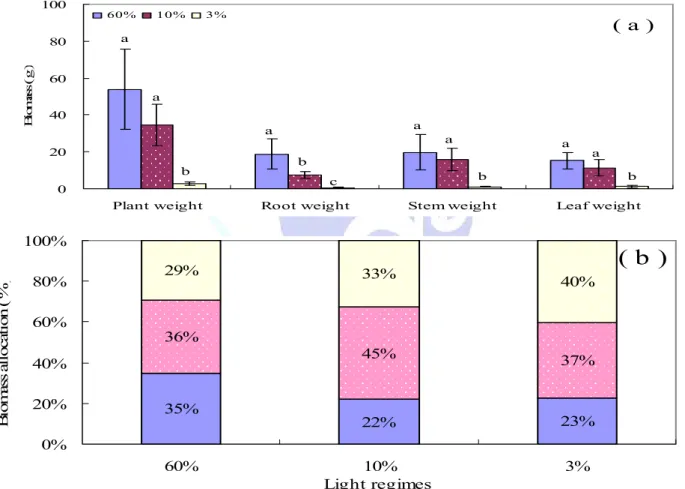
莖、葉)之比例(b) ………..……….. 34 圖5、赤皮於不同光度下,各部位之生物量(a)與生物量分配於各部位(根、
莖、葉)之比例(b) ……… 35 圖6、毽子櫟於不同光度下,各部位之生物量(a)與生物量分配於各部位(根、
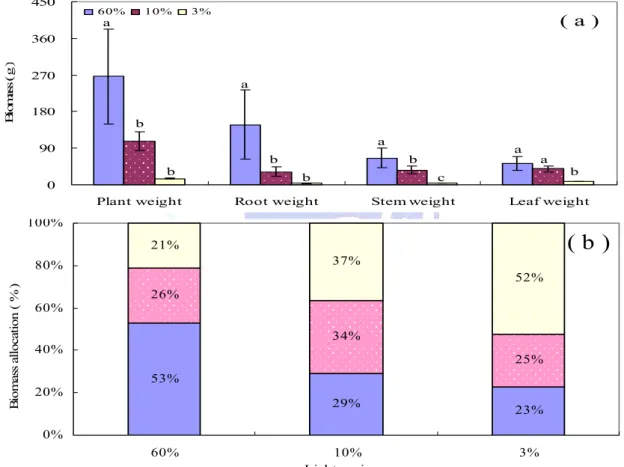
莖、葉)之比例(b) ………. 36 圖7、長尾尖葉櫧於不同光度下,各部位之生物量(a)與生物量分配於各 部位(根、莖、葉)之比例(b) ………….………..………. 37 圖8、鬼石櫟於不同光度下,各部位之生物量(a)與生物量分配於各部位(根、
莖、葉)之比例(b) ………...………. 38 圖9、不同光環境下 6 種試驗樹種-(a)青剛櫟(b)錐果櫟(c)赤皮(d)
毽子櫟(e)長尾尖葉櫧(f)鬼石櫟之光合反應曲線 ………..44 圖10、2006 年 7 月 6 日凌晨 0 點時,6 種試驗樹種在不同光度處理下之 Fv /Fm ………...………..……. 51 圖11、2006 年 7 月 6 日各處理光度下(a)相對光度 60%、(b)相對光度 10%,
(c)相對光度 3%,6 種試驗樹種 ΦPSII之日域變化 ………. 53 圖12、2006 年 7 月 6 日(a)相對光度 60%、(b)相對光度 10%,(c)相對光度 3%處理下 6 種試驗樹種 NPQ 之日域變化 ...……..……….…… 55 圖13、2006 年 7 月 6 日各處理光度下(a)相對光度 60%、(b)相對光度 10%,
(c)相對光度 3%,6 種試驗樹種 Fv / Fm 之日域變化 ………...… 57
1
壹、前言
太陽輻射(solar radiation)是植物生存所必需的資源,並影響植物之形 態與功能,其對於植物之生長、生存、演化,與分佈殊具重要之地位 (Quero et al., 2006)。然光量則是太陽輻射中最重要的屬性之ㄧ,乃其主導著光合作 用之進行(Kozlowski and Pallardy, 1997)。
森林生態系中,光量異質性普遍存在。植物為了提高對於光能之利用 效率與避免高光的傷害,通常採取多種調控措施,其中包括形質及生理方 面之調節,然2者間之調節又彼此牽引著,此乃促使植物適應其生長環境之 光度(Ashton and Berlyn, 1992;Duan et al., 2005)。惟植物隨環境變化而改變 其形態與生理之能力,稱之為可塑性;高度的可塑性可增加植物在多變環 境中之耐性,乃至於有較高之合適度(Duan et al., 2005)與馴化能力。植物在 適當光範圍內皆具馴化之潛能,然此適當範圍則依植物不同而異,且受其 自身基因所控制。若植物生長於適生之光環境外,將使其馴化不良 (Pearcy, 1998;Krause et al., 2001),使生長受阻礙,甚至導致植體的死亡。
儘管光能是植物所必須的,但卻無法將所吸收之光能全然的使用於光 化學上,部分的光能則由保護機制消散或致使植物光損害(photodamage) (Schreiber, 1997;Adir et al., 2003),此即是所謂之光抑制(photoinhibition)。
一些研究發現,陽性植物與陰性植物(或不同演替階段的植物)具有不的光防 禦機制(Ishida et al., 1999a;Krause et al., 2001;Griffin et al., 2004),而此在 一定的程度將影響它們生態地位(niche)之分化與於不同生態系中的豐度,因 此研究森林中各演替階段樹種之生理生態特性將有助於探索森林生態系的 更新與演替之律動。
殼斗科植物為台灣櫟林帶(Quercus zone)與楠櫧林帶(Machilus - Castanopsis zone)之重要樹種,多年來的相關研究仍以植群調查所得的生 態特性為主(陳子英,1994,2004;高瑞卿,2001;簡龍祥,2002;陳俊
2
雄、蘇鴻傑,2003;劉啓斌,2003;劉靜榆,2004),對於其生態生理特 性,近年雖有學者以模擬試驗方式加以深入探討,但相關研究仍有限。
本研究即以遮蔭網模擬不同的林下光量環境,測定楠櫧林帶與櫟林帶 中 的 6 種 殼 斗 科 苗 木 - 青 剛 櫟 (Cyclobalanopsis glauca) 、 錐 果 櫟 (Cyclobalanopsis longinux) 、 赤 皮 (Cyclobalanopsis gilva) 、 毽 子 櫟 (Cyclobalanopsis sessilifolia) 、 長 尾 尖 葉 櫧 (Castanopsis cuspidata var.
carlesii)、鬼石櫟(Lithocarpus castanopsisifolius)於不同光度下,若干形質及 光合反應與對光能之消散機制,藉以了解此6種殼斗科苗木之光適應性,進 而提供櫟林帶與楠櫧林帶之復育及苗木的科學管理之理論依據。
3
貳、前人研究
一、光度對苗木形質與生理之效應 (一)光度對苗高與基徑之效應
進行苗木品性評估時最易檢定的形質參數係屬苗高與苗徑二項;
通常苗木基徑較大者具較強之逆境耐性,且基徑量測亦具非破壞性取 樣之優點,故為應用廣泛之形態參數 (陳舜英,1997)。
環境光度之上升有利於樹種苗高生長,然高光也會限制部份植物 之高生長,遂多數樹種之苗木通常需要在部分遮蔭的狀態下才能臻於 最大高生長(Kimmins, 1997;Tang, 1997)。
林世宗與簡文村(1997)以台灣紅豆杉(Taxus sumatrana)為試驗樹 種,顯示台灣紅豆杉苗之苗高以於相對光度28%表現最佳;全光與6%
之低光均不利於苗高生長;基徑則以6%之低光最差。
陳舜英(1997)指出三斗石櫟(pasania hancei)於3種遮蔭處理下-絕 對光量分別為69、316與508 μmol photons m-2sec-1,其苗高與基徑之生 長在高光環境中是優於低光處。
周沛郁(2004)以三種臺灣原生闊葉樹種-樟樹(Cinnamomum camphora)、青剛櫟(Cyclobalanopsis glauca)與光臘樹(Fraxinus griffithi)之苗木為試驗對象;其試驗結果顯示強光皆對樹種之高生長 產生限制現像,樟樹於相對光度25%具最大高生長,而青剛櫟及光臘樹 之高生長則是在相對光度50%下表現較佳。然3者之基徑則皆具隨環境 光度上升而遞增之趨勢。
Kimmins(1997)指出非耐陰性樹種如閉果松(Pinus banksiana),在全 光下可達到最大苗高,但其苗高在光度減至50%之情況下只將略為下 降,基徑(diameter)則會顯著下降;耐陰種中的糖楓(Acer saccharum)與 美國梧桐(Platanus occidentalis)於相對光度20%時,即可達到最大高生
4
長,然在全光處則顯著抑制其高生長。
因此综合上述可得知,環境光度增加有利於苗高與基徑之生長,
但若光度過於強烈,反而將抑制苗高之生長。而光度與苗高及基徑間 之相關消長,將因樹種不同而有所差異。
(二)光度對生物量之效應
光資源的增加有助於植物生物量之累積。植物生物量之分配則依 樹種、生物週期、年齡與環境因子的不同而有差異,其中以環境因子 之影響力較大(Barnes et al., 1997)。
高光環境中,植物提升生物量分配於根部之比例,遂造成 shoot/root 的下降(Kimmins, 1997),此為植物對高光馴化的重要表徵之一,利於植 物因應光強環境所導致之水逆境產生(郭耀綸,2003)。低光環境下,植 物將較多的生物量投資於莖部之高生長與葉部的生長,以加強對光能 競爭與捕捉,並將造成 shoot/root 增加。一般而言,非耐陰性樹種較耐 陰性樹種具較大之shoot/root 比(Kitajima, 1994);而非耐陰性植物在低 光環境中,其生物量將急劇下降,形成細弱形之苗木,並造成 shoot/root 的增加(Kimmins, 1997;Tang, 1997)。
林世宗與簡文村(1997)亦曾指出台灣紅豆杉苗木之生物量隨光度 增加而有遞增之現象;而生物量分配於根部之比例亦隨光度增加而上 升,然葉子生物量分配比例優勢則顯見於低光處。
周沛郁(2004)之試驗結果顯示樟樹(Cinnamomum camphora)青剛 櫟(Cyclobalanopsis glauca)與光臘樹(Fraxinus griffithi)苗木之生物 量皆隨著處理光度增加,而有上升之趨勢;在低光下樟樹將較多生物 量分配於地上部,隨處理光度增加而逐漸加重對根部之投資比例。青 剛櫟(Cyclobalanopsis glauca)與光臘樹亦有相似之趨勢,但青剛櫟莖 部生物量亦有隨處理光度增將而上升之趨勢。
5
郭耀綸與江壁合(2003)對台灣假黃楊(Liodendron formosanum)、小 芽新木薑子(Neolitsea parvigemma)與台灣梭羅木(Reevesia formosana)之 試驗結果顯示,台灣假黃楊在相對光度為35%之環境下具最大生物量;
而小芽新木薑子與台灣梭羅木則是於試驗最大光度-相對光度65%有 較大生物量。3者在低光下將較多生物量分配於地上部,並隨處理光度 增加而逐漸提升對根部之投資比例。
Valladares et al. (2005)發現Ilex aquifolium之shoot/root將隨著處理光 度的上升而下降。但待環境光度至相對光度24%以上時,shoot/root下降 幅度相對減少,甚至在全光下shoot/root反而有上升現象。
(三)光度對葉面積參數之效應 1.葉面積比(Leaf area ratio, LAR)
LAR 為總葉面積與總生物量之比值(Lambers et al.,1998;Pearcy, 1998),可以用來評估植物體中生產器官(葉面積)與非生產器官之比 例。弱光環境下,植物可獲得之光能相對減少,遂藉由形態之改變以 截取更多之能量,故植物於低光處將分配較多生物量於地上部,尤其 著重於進行光合作用的葉部組織,以增進光能之捕捉,並導致增大葉 部之生物量與全株葉面積 (張安邦等,2000),遂植物之 LAR 於低光環 境將較高光處高 (Kitajima, 1994;Pearcy, 1998;Duan et al., 2005);LAR 在相對低光處之提升,被認為是植物形態上對於弱光環境適應所做出 之典型反映,其主要可提升植物光合作用速率對呼吸速率之比,然此 舉有利於植物於低光中具維持淨碳收支與生長(Kitajima, 1994)。
Valladares et al. (2005)以 Ilex aquifolium 為試驗材料,並將之放置於 6 種不同的相對光度環境中,其結果顯示 Ilex aquifolium 之 LAR 將隨著 處 理 光 度 的 增 加 而 遞 減 。 而 於 沈 介 文(2000) 、 林 怡 芳 (2005) 、 Poorter(1999) 、 Landhäusser and Lieffers(2001) 、 Senevirathna et al.
6
(2003)、Sánchez-ómez et al. (2006)之研究報告中亦發現相似之結果。
2.比葉面積 (specific leaf area, SLA)
葉片的形態結構對於光的吸收呈現高度的特化(specialized),因此 環境中光度之改變,將對葉片結構與內涵物濃度產生程度不一之效應 (Taiz and Zeiger, 2002)。葉片生長於遮蔭環境中(陰葉)相較於生長於全 光下(陽葉),通常會較大、較薄、少淺裂與具較少層的柵狀細胞(palisade cells) (Kimmins, 1997)。然而葉片之塑性與樹種之光耐性及其演替序列 之地位有關。一般而言,需光性樹種之塑性將會大於陰性樹種(Ashton and Berlyn, 1992;Sánchez-Gómez et al., 2006)。
SLA為葉面積與葉重之比值(Lambers et al., 1998;Larcher, 2003),
可用來觀測葉片形質之變化。弱光下, SLA的增加顯示出相同乾重下 捕光範圍增大,因而利於植物在弱光環境中之生長(Duan et al., 2005)。
高光下SLA的減小則顯現植物調整其單位葉重下之葉面積,使之蒸散面 積減小(Duan et al.,2005),避免水逆境的產生。SLA的減小亦透露出葉 片在高光環境下加厚之訊息(Lambers et al., 1998),此乃柵狀細胞長度與 其組織層次增加所致,而此現象將有利於植物葉片在高光下對光能截 取、分配與利用效率 (Lambers et al., 1998;Pearcy, 1998;Hopkins , 1999;Taiz and Zeiger, 2002;Duan et al., 2005)。
Ishida et al.(1999)以Shorea leprosula、Neobalanocarpus beimii與 Macaranga gigantea為試驗樹種,顯示環境光量的減少皆使3者苗木SLA 增加,相似的結果亦可見於沈介文(2000)、林怡芳(2005)、Denslow et al.(1990)、Davies(1998)、Poorter(1999)、James and Bell(2000)、Landhäu- sser and Lieffers(2001)、Jose(2003)、Senevirathna et al.(2003)、Valladares et al.(2005)、Naramoto et al.(2006)、Sánchez-Gómez et al.(2006)之文獻。
7
(四)葉綠體色素含量
植物進行光合作用的地方是葉綠體(chloroplast),其中行光反應的 部份是在葉綠體中的特殊化內膜-類囊體膜(thylakoid membranes)中進 行,類囊體膜中含有許多由葉綠素及蛋白質所組成的光系統,以推展 光反應。行光反應的部位可分為光系統 I(photosystem I, PSI)及光系統 II(photosystem II, PSII),分別具有反應中心(reaction centres,RCs)及天線 (antenna)系統。
光系統中的捕光複合體 (light-harvesing complexes,LHC),主要的 組成成分為葉綠素 a、葉綠素 b 以及類胡蘿蔔(carotenoids)。而反應中 心則由特殊化的葉綠素a 所構成的(Hopkins, 1999;Taiz and Zeiger, 2002 )。因此光能的吸收、傳導、轉換,消散過程中,葉綠體的色素將扮演 著重要的作用。
葉綠素 b 主要分布於光系統中的 LHC(Lambers et al., 1998;Pearcy, 1998;Hopkins, 1999;Taiz and Zeiger, 2002)。因此 Chl a/b 可以作為光 系統中,LHC 所佔之比例大小的指標(Lambers et al., 1998;Duan et al., 2005)。遮蔭環境下 Chl a/b 比例減少,反應著植物將能量投資於 chl b,
使光系統有較高比例的LHC。而高比例的 LHC 則可提供較大之天線系 統,使其更有效率捕捉較光能,增加低光度下光系統之活性(Lambers et al., 1998;Hopkins, 1999;Senevirathna et al., 2003;Duan et al., 2005)。
然Evans(1986)則具不同之觀點,其試驗結果顯示 chl b 濃度增加的確使 LHC 比例的增加,但對於整體吸光效率助益不大。在高光處,植物 Chl a/b 之增加,顯示具較低比例的 LHCII,此則利於減少光能之過度吸收 與降低光抑制現象產生(Krause et al., 2001)。多數的文獻指出高光處植 物之Chl a/b 將較遮蔭者高(Givnish, 1988;Lambers et al., 1998;Pearcy, 1998;Senevirathna et al., 2003;Duan et al., 2005)。另外 Pearcy(1998)則
8
指出陰性樹種之Chl a/b 塑性並不明顯,即使其處於高光環境下,此值 仍無太大變化,Krause et al. (2001)也提出類似的看法。
類胡蘿蔔素除了可當吸光色素外,也可對激態之葉綠素以熱消散之
方式進行去激,此則有效減少活性氧的產生與累積,降低光氧化傷害 之機率,因此類胡蘿蔔素兼具光吸收與光保護之功能(Hopkins, 1999;
Taiz and Zeiger, 2002),遂可將Car/Chl視為相對光保護能力之指標(Duan et al., 2005;Sánchez-Gómez et al., 2006)。較高的Car/Chl的植物通常具 較高的光保護能力,而多數文獻指出高光處植物之Car/Chl將較遮蔭處 理者高 (Lambers et al., 1998;Duan et al., 2005;Valladares et al., 2005)。
(五)光合反應曲線
光合反應曲線係以測量光度與固碳能力間之關係而來,其可作為 植物光合特性的資訊來源(Taiz and Zeiger, 2002)。當光合速率與呼吸速 率達平衡時,此點之光度則稱之光補償點(light compensation point, LCP)。然而光合作用的初階,光合速率是隨著光度以線性之方式快速 增加,此時曲線的斜率則為最大光量子效率,一般則以光量子效率 (quantum yield, Qy)示之。但光合速率與光度間的線性關係並非恆定,
當光度的再增加,光合速率之增加速度將趨近於平緩(level off),此轉 折點定義為光限制區之飽和點。在此之前光合速率的增加主要受限於 入射光,之後則將受限於 rubisco 羧化能力(Taiz and Zeiger, 2002)。光度 持續的再增加,光合速率仍以緩慢的速度增加,直到 CO2 限制區域之 飽和點到達;此點將作為光飽合點(light saturation point, LSP),並可將 此 點 的 光 合 速 率 定 義 為 光 飽 和 光 合 作 用 速 率 (light saturated photosynthetic rate, Asat)或最大光合作用速率(maximum photosynthetic rate, Amax)。超過此點,光度的再增加,反致使光合作用速率降低 (Kimmins, 1997)。
9
一般而言,冠層中陽葉(或苗木於相對高光環境)之光補償點、光飽 和點與光飽和光合速率通常較陰葉(或苗木於相對低光環境)來的高。同 樣的非耐陰樹種的光補償點、暗呼吸率、光飽和點與光飽和光合速率 則較陰性樹種高(Kitajima, 1994;Barnes et al., 1997;Kimmins, 1997;
Davies, 1998)。
游 智 偉 (2006) 以 台 灣 4 種 闊 葉 樹 種 - 三 斗 石 櫟 ( Pasania ternaticupula )、 青 剛 櫟 ( Cyclobalanopsis glauca )、 狹 葉 櫟
(Cyclobalanopsis stenophylloides)與樟樹(Cinnamomum camphora)
之苗木為試驗對象,並栽植於相對光度10%、50%及100% 之環境下;
其試驗結果顯示,各樹種之Amax皆隨處理光度增加而提升,其中三斗石 櫟與狹葉櫟於全光具最大值,而青剛櫟與樟樹則是於相對光度50%之 Amax較高。
郭耀綸等(2004)在台灣三十種闊葉樹陽葉氣體交換潛力之研究中 指出耐陰性樹種與非耐陰樹種間的光補償點、光飽和點與光飽和光合 速率均有顯著不同。非耐陰樹種之光補償點、光飽和點與光飽和光合 速率皆較耐陰性樹種大。Denslow et al. (1990)的試驗結果亦呈現陽性樹 種之光合作用速率將大於陰性樹種。
Kitao et al. (2000)將日本森林中,3 種不同演替階段之闊葉樹苗木
-Betula platyphylla var. japonica(先驅種)、Quercus mongolica(中度耐陰 之演替中期種),與 Acer mono(演替後期耐陰性種)放置於 3 種不同處理 光度之環境下,發現3 者之 Asat皆隨著處理光度的增加而提升,而 Betula platyphylla 之 Asat將明顯大於 Acer mono。
Griffin et al.(2004)以11種Illicium spp.作為試驗樹種,並將之馴化於 2種不同光處理環境下(全光,相對光度50%)。試驗結果顯示多數Illicium spp.植物於相對光度50%環境下,其的Amax將大於全光環境下,但陽性
10
植物在全光下仍可維持較高的Amax,甚至超過其在相對光度50%之值。
Ashton and Berlyn(1992)以4種Shorea species為試驗樹種。其結果顯 示隨著環境光度的增加,Amax也將提升。但環境光度若過於強烈,反而 會抑制耐陰性樹種之Amax。
上述研究顯示植物之光合作用速率將隨著環境光度之增加而提
升,但陰性植物的光合作用速率則有可能因高光而產生抑制之現象。
且在高光環境之中,陽性植物或先驅植物之補償點、飽和點與最大光 合速率通常較耐陰性植物或演替後期植物高 (Kitajima, 1994;Scholes et al., 1997; Ishida et al., 1999a;Kitao et al., 2000;Griffin et al., 2004)。
因此植物在高光環境中的Amax將可作為植物需光性的指標,Ashton and Berlyn(1992)在其報告中亦曾指出Amax可作為植物需光性的指標。
(六)葉綠素螢光
光照產生之激發能量是由天線吸光色素(antenna pigments)所吸 收,並將之轉換為激子後,傳遞至PSI及PSII之反應中心,此能量將用 來驅動光化學反應。光化學消散之路徑,包括著電荷分離(charge separation)及電子載體之電子傳遞,但此並非激發能焠熄之唯一路徑,
另外兩條之路徑為熱消散(吸光細胞之激發態以非輻射方式去激並轉換 為熱)及螢光消散(fluorescence quenching),而其中螢光只占總吸收能的 3-5%(Roháček and Barák, 1999)。依熱力學第一定律,此3種路徑彼此間 呈現一種相互競爭狀之狀態。假使某路徑之效能增加,將會使其餘二 種之效率減少。所以葉綠素螢光效益之測量,將可獲得光化學與熱消 散間消長的資訊(Schreiber, 1997;Maxwell and Johnson, 2000)。
葉綠素螢光效益的下降,即螢光消散的減低,其機制如下︰
(一)光化學消散(photochemical quenching, qP)︰激發能用於光化學反 應中(Krause and Weis, 1988)。
11
(二)非光化學消散(non-photochemical quenching):係指 PSII 中的單線 激發態(single excited state)葉綠素以非光化學的方式去激 ,並分為以下 3 種情況(1) qE︰能量依存消散(energy-dependent quenching)此與光誘導 下,類囊體膜內外產生質子梯度有關 (Krause and Weis, 1988)。一般而 言 qE 在 1.4 μs 內就可形成(Horton et al, 1994),而紓解則需 2-3 分鐘 (Horton et al,1996;White and Critchley, 1999)。除非處於在多重逆境下,
否則qE 將是主要的非光化學消散方式(Horton et al,1994)。(2) qT(狀態 轉換消散)︰LHCII 磷酸化導致分配至 PSII 的激發能量減少(Krause and Weis, 1988)。一般而言,10 分鐘的暗適應就足以使其紓解(Krause et al., 2001)(3) qI(光抑制消散)︰此消散與光合作用之光抑制有關(Krause and Weis, 1988)。主要歸因於 PSII 反應中心的破壞(遭單線激發態氧(singlet oxygen)與超氧(superoxide)破壞)與天線系統之能量消散(現存 zeaxanthin) 有關(Krause and Weis, 1991;Horton et al., 1994;Maxwell and Johnson, 2000;Jin, 2000)。其需幾小時或甚至幾天才可紓緩(Horton et al., 1996;
White and Critchley, 1999),而消散程度將可以 Fv / Fm來表示(Krause and Weis, 1988;Krause and Weis, 1991)。然在多數的情況下,螢光消散下 降的原因,主要以光化學與qE 為主(Krause and Weis, 1988)。
葉綠素螢光的測量是一種非破壞性的檢測方式,即可在不干擾自 然光合作用下獲得葉綠素螢光之效益,進而分析光合器官中結構與功 能上定性及定量的資訊。而此種分析方式已經成為植物生理學家和生 態生理學家最有力、最廣泛利用的技術之一(Roháček and Barák, 1999;
Maxwell and Johnson, 2000),其常用的參數如下︰
(一)Fv / Fm = ( Fm - FO ) / Fm代表PSII最大光能轉換效率(maximum photochemical efficiency of PSII)。此值於任何植物及生態型幾乎是不變 的;在正常情況下,此值約略為0.8左右(Krause and Weis, 1991;Lambers
12
et al., 1998)。但當植物處於逆境或受損時,Fv / Fm將會明顯減少。植物 在光抑制之情況下,其Fv / Fm將與最佳光量子效益(optimal photo yield of photosynthesis)呈線性關係(Krause, 1988;Krause and Weis, 1991),因此 Fv / Fm可作為光抑制或光系統II複合體的損害指標。這也是目前研究光 抑制最常使用的參數之ㄧ(Heinz Walz GmbH, 1999;Roháček and Barák, 1999;Krause et al., 2001)。
(二)ΦPSII=(Fm′- Fs) / Fm′為 PSII 實際光能轉換效率(actual efficiency of energy conversion in PSII),為光化學消散的參數之ㄧ。係指 PSII 將葉 綠素吸收之光能用於光化學的比例(Maxwell and Johnson, 2000)。由於此 參數不需經暗適應及提供 FO′即可獲得,因此常被使用於田野試驗 (Roháček and Barák,1999)。
(三)qP=Fm′- Fs / Fv′代表光化學消散(photochemical quenching) 。qP 可量化光適應狀態下,PSII光化學能力與PSII反應中心成氧化態之比例 (Björkman and Demmig-Adams, 1995;Roháček and Barák, 1999)。大致 來說qP與ΦPSII極為相似,其主要之差異為ΦPSII係指吸收能量用於光化學 之比例,而qP則為PSII反應中心開啟之比例(Maxwell and Johnson, 2000)。
(四)ETR or J=Φ× PPFD×0.5×0.84 為電子傳遞速率(electron transport rate)。可作為通過 PSII 電子的傳遞速率指標。其中 PPFD 為實際光合 光子流密度(Photosythetic photon flux density), 0.5 為所吸收之光能分配 於PSI 與 PSII, 0.84 為一般植物葉子的吸光係數(absorption coefficient ) 近 似 值 (Roháček and Barák, 1999 ; Maxwell and Johnson, 2000 ; Rosenqvist and Kooten, 2003)。由於PSI與PSII光能分配比例與葉子的吸 光係數皆使用常數,而非實際值,因此本文認為亦可將之視為相對電 子傳遞速率(Relative electron transport rate, r-ETR)。
13
(五)NPQ=Fm - Fm′/ Fm′為非光化學消散(non-photochemical quenching) 參數之ㄧ (Bilger and Björkman, 1990),雖然許多過程皆可形成NPQ,
但qE則為其主因 (Li et al., 2000)。NPQ可作為植物為了避免過多光能導 致的光破壞,而將激能從LHCII以熱的方式消散之指標 (Heinz Walz GmbH, 1999) 。 Bilger and Björkman(1990) 與 Björkman and Demmig -Adams (1995)指出在自然光域中NPQ與入射的PPFD呈線性關係,以及 NPQ的消長與葉中玉米黃質(zeaxanthin)之增減有高度相關。因此NPQ 可作為光適應狀態中,LHCII過量光能轉換為熱消散的指標(Roháček and Barák, 1999;Maxwell and Johnson, 2000)。
Ishida et al. (1999a) 以 2 種 龍 腦 香 科 植 物 Shorea leprosula
、
Neobalanocarpus beimii與同一生育地大戟科Macaranga gigantea為試驗 樹種,並將之栽植於2種不同孔隙環境下。其結果顯示出3者之ΦPSII之日 域變化將隨光度上升而下降,而NPQ則是隨光度的增加而上升。當日 r-ETR則與光度日過程變化趨勢相似,但Neobalanocarpus beimii之 r-ETR則在過份光強的情況將會降低。而相似的ΦPSII、NPQ與ETR與光 度日域變化的關係亦可由Ishida et al. (1999b)與Shirke and Pathre(2003) 文中發現。另外在全光下,需光性植物Shorea leprosula與先驅植物 Macaranga gigantea 之 ΦPSII與r-ETR 則 較 陰 性 植 物 Neobalanocarpus beimii大,而NPQ則是Neobalanocarpus beimii較大。Krause et al. (2001) 測量3種不同演替序列中的植物先驅植物Ficus insipida 、 先 驅 植 物 Cecropia obtusifolia 與 演 替 後 期 植 物 Ochroma pyramidale之Fv / Fm日域變化。結果發現3者Fv / Fm隨光度的增加而下 降,同樣的趨勢亦可在Jifon and Syvertsen(2003)與Senevirathna et al.
(2003)發現。且Ochroma pyramidale(演替後期植物) 之Fv / Fm在日過程 中衰退幅度將明顯高於2種先驅植物。。
14
综合上述可得知光度的增加將使螢光參數Fv / Fm和ΦPSII的下降與 qP、NPQ及ETR的上升,即光度的增加將使得植物的光合速率、光抑制 與非光化消散程度之提升,與光化學消散的降低,但若環境光度過高 則有可能反將抑制植物的光合能力(由ETR觀之)。而不同需光性或演替 地位的植物,其能量消散機制將有所差異;需光性植物與先驅植物主 要以光化學消散方式焠熄激能;陰性植物與演替後期之植物則主以非 光化學消散的方式消耗過多能量(Scholes et al., 1997;Krause et al., 2001
;Bertamini and Nedunchezhian, 2002;Griffin et al., 2004;Kitao et al., 2006)。
15
二、光抑制(photoinhibition)
光的利用效性是影響林木生存、成長與分佈的重要控制因子之ㄧ(Duan et al., 2005)。植物之光合系統經由演化,發展出可以吸收其所能吸收之最大 光能以作為推動光化學反應之能量(Long et al., 1994;Taiz and Zeiger, 2002) 但若植物無法有效的利用其所吸收之光能時,過剩的光能將導致有害物質 的產生如單線激發態氧與超氧與葉綠素,並致使其光氧化傷害。因此植物 需適當的保護機制以避免其光合器官發生不可逆之損害(Scholes et al., 1997;Müller et al., 2001;Taiz and Zeiger, 2002)。早期研究認為光抑制乃是 光合器官遭受到破壞(photodamage),遂使光合速率下降(Long et al., 1994),
然現今則認為光保護機機制(protective mechanisms)當屬光抑制的一部分 (Krause, 1988;Demmig-Adams and Adams, 1992;Scholes et al., 1997;Taiz and Zeiger, 2002)。
PSII為光抑制之初始點與主要的作用部位(Krause, 1988;Krause and Weis, 1991;Horton, 1994;Long et al., 1994;Adir et al., 2003)。Ort and Whitmarsh(1990)指出光照下的PSII可分為2類,其一佔的比例較大,並呈現 活化狀;另一則佔的比例較小,呈現失活狀。Krause and Weis(1991)更進一 步指出活化狀態的PSII位於基粒類囊體(grana thylakoid),而失活狀態之PSII 則處於基質類囊體(stroma thylakoid)。然而造成PSII分為2類的原因為LHII 吸收光能後,能量將傳遞反應中心,過程中將有可能產生活性氧,並有一 定機率使反應中心之D1蛋白質受到損傷,遂造成PSII呈現失活之狀態 (Demmig-Adams and Adams, 1992;Trebst, 1995)。然而D1蛋白質之損壞是可 修復的,首先PSII反應中心必須先自基粒類囊體移動到基質類囊體中。在基 質類囊體中D1蛋白質將完全降解與重新合成,並重組於反應中心。修復好 的反應中心將移回基粒類囊體,並恢復PSII的活性;而此過程 (D1蛋白質連 續 性 的 降 解 與 修 復) 稱 之 為 週 轉 (turnover) (Demmig-Adams and Adams,
16
1992;Trebst, 1995;Taiz and Zeiger, 2002)。Adir et al. (2003)指出任何的光度 下,都有機會產生光破壞。但在低光下,降解的過程將受修復機制所掩飾;
強光下,若修復速率持續性小於降解速率,將有可能使PSII反應中心產生長 期之破壞,並使光合能力下降 (Long et al., 1994;Trebst, 1995;Bertamini and Nedunchezhian, 2002;Adir et al., 2003)。然而不單只有受損之PSII反應中心 移入基質類囊體,未受損者(但不具功能性)亦會移入。此意味著PSII可藉由 反應中心與天線複合體的分離,以避免光能的過度吸收進而達到光保護的 作用,而此過程是可逆的(Demmig-Adams and Adams, 1992 )。
上述的過程將導出2個保護機制,其一為D1蛋白質的週轉,其二為可逆 性的PSII反應中心不活化。然而植物之光保護機制不單只有上述2種,以下 將略述其它保護機制:
(一) 類胡蘿蔔素(Carotenoid):類胡蘿蔔是吸光色素的一員,其主要功能 為吸收光能並將之傳遞至葉綠素中。若激發態的葉綠素無法立即將 能量使用於光化學反應中,則類胡蘿蔔將可直接對單線激發態氧(1O2) 與 三 線 態(triplet) 的 葉 綠 素 進 行 去 激 , 以 避 免 超 氧O2- 產 生 (Demmig-Adams and Adams, 1992;Hopkins, 1999;Taiz and Zeiger, 2002)。Demmig-Adams and Adams (1992)認為類胡蘿蔔具另一功能,
即其衍生物涉及葉黃素循環,可對單線激發態葉綠素(singlet excited state)進行去激。
(二) 葉黃素循環(Xanthophyll cycle):強光下,由於水的裂解反應和跨類 囊體膜的質子交換,遂類囊體膜兩側將產生跨膜質子梯度。而質子 在 類 囊 體 內 腔 之 累 積 將 導 致 內 腔 的 強 度 酸 化 , 並 誘 使 紫 黃 質 (violaxanthin) 去 環 氧 基 (de-epoxidation) 轉 換 為 花 藥 黃 質 (antheraxanthin)或玉米黃質(zeaxanthin)(Lambers et al., 1998)。高光下 葉綠素上的激能可轉至zeaxanthin (Lambers et al., 1998;Müller et al.,
17
2001)或xanthophyll cycle藉由控制了類囊體膜的結構,誘使與LHCII 形成一消散複合體(Horton et al,1994) 或為xanthophyll cycle(或為 zeaxanthin)與LHCII上Psbs蛋白質結合並引起LHCII結構改變,導致其 轉換為消散狀態(Li et al., 2000;Müller et al., 2001) 以熱的方式直接 消散。另外有研究指出xanthophyll cycle不單只作用於LHCII,也可以 以抗氧化劑(antioxidant)之態或減少膜的流動(fluidity) 的方式直接保 護類囊體,避免受光氧化破壞(photooxidative damage)(Müller et al., 2001)。
(三) LHCII磷酸化(LHCII phosphorylation):也就是所謂的狀態轉換(qT),
plastoquinone pool以還原態(reduced state)累積時,將活化類囊體上之 蛋白質激酶(threnine residue),並促使LHCII之磷酸化。當LHCII被磷 酸化,因負電相斥將使LHCII移至基質類囊體區,將使多數能量輸送 至PSI,反之若plastoquinone pool多成氧化態(oxidized state)則將使 LHCII移回基粒類囊體區。此機制可藉由調整LHCI與LHCII之大小,
精準的控制能量分配於2個光系統中,使葉綠體能更有效率的利用光 能(Krause and Weis, 1988;Whitmars, 1998;Malkin and Niyogi. 2000;
Taiz and Zeiger, 2002)。
(四) 光呼吸(Photorespiration):所謂光呼吸,是指伴隨光之光合產物再氧 化,釋放出CO2之過程 (Hopkins, 1999)。其發生原因主要是因Rubisco 同 時 具 有 催 化 羧 化(carboxylation) 反 應 與 氧 化 酶 反 應 (oxygenase reaction)的能力(Hopkins, 1999)。因此植物在常態大氣環境下行光合 作用,常常伴隨著光呼吸之產生。光呼吸看似有礙於光合作用之進 行 , 但 多 數 文 獻 則 指 出 光 呼 吸 具 光 保 護 之 性 質(Krause, 1988;
Demmig-Adams and Adams, 1992;Björkman and Demmig -Adams, 1995;Padmasree and Raghavendra, 1998;Hopkins, 1999)。其光保護
18
機制主要以消耗過剩之激能;在強光下可產生足夠之CO2,並使得 直線電子傳遞練持續運作,進而保護植物避免於光氧化之傷害 (Hopkins, 1999)。
(五) Mehler reaction:為呼吸作用的一種,茲將有利於促使O2之吸收 (Padmasree and Raghavendra, 1998)。但過程中PSI將直接還原O2並導 致活性氧的產生,因而具一定機率使光氧化破壞發生,但若有足夠 活性氧清除物質,則能有效降低光破壞發生之機率。Mehler reaction 將消耗NADPH,而此有助於直線電子流之續存,與Mehler reaction 自身之電子假循環皆可提供部份電子流並誘使較大pH梯度的形成,
遂 有 助 於 葉 黃 素 循 環 之 形 成 與 光 能 之 消 散(Demmig-Adams and Adams, 1992;Björkman and Demmig-Adams, 1995)。因此Mehler reaction將同時具備光破壞與光保護之性質,其與光呼吸同被歸類於 新陳代謝(metabolism)類的光保護機制(Krause, 1988;Björkman and Demmig Adams, 1995),而兩者皆有助於qE之形成(Krause, 1988)。
综合上述概念可得一個訊息,乃是天線系統每吸收一個光量子都會產 生相對恆定機率致使光抑制(光保護與光破壞)之產生。因而本文則將光抑制 定義為因依存光所產生的能量消散或PSII反應中心不活化或傷害(inactive or damage)致使最佳光合速率或光量子效益之降低。而葉綠素螢光參數Fv / Fm 可用來表示光抑制的程度,NPQ則可作捕光複合體II(LHCII)將過量輻射能 轉換為熱消散之指標(Roháček and Barák, 1999;Griffin et al., 2004)。
19
三、試驗樹種之植群分佈與生態特性
此 試 驗 是 以 台 灣 櫟 林 帶 ( Quercus zone ) 與 楠 櫧 林 帶 ( Machilus Castanopsis zone)等常綠闊葉林中之6種殼斗科樹種-青剛櫟(Cyclobalanopsis glauca)、錐果櫟(Cyclobalanopsis longinux) 、赤皮(Cyclobalanopsis gilva) 、 毽子櫟(Cyclobalanopsis sessililfolia) 、鬼石櫟(Lithocarpus castanopsisifolius)
、長尾尖葉櫧 (Castanopsis cuspidata var. carlesii)為試驗樹種。
青剛櫟主要分布於台灣的楠櫧林帶,多出現較乾燥之稜線,有研究指 出其林下徑級分佈呈現反J型,顯示青剛櫟小苗可在林下自然更新,其需光 性被認為屬中性樹種(陳俊雄與蘇鴻傑,2003;劉靜榆,2004);毽子櫟分布 於台灣楠櫧林帶與櫟林帶,其生態特性之相關文獻尚闕如。赤皮主要分布 於中北部的楠櫧林帶,常出現稜線。劉棠瑞與蘇鴻傑 (1983)指出赤皮林下 徑級呈現J形分佈,屬於陽性樹種;而陳俊雄與蘇鴻傑(2003)則指出可在鬱 閉的冠層覓得大量赤皮的小苗與幼樹,但達到樹冠層者則較少,認為赤皮 乃是藉由樹倒產生之孔隙以達到樹冠層。錐果櫟於台灣楠櫧林帶與櫟林帶 都可發現,可於乾燥稜線及溼潤溪谷地形生存。其林下徑級分佈呈現反J型,
若林下孔隙太小將被周圍樹側向擴張生長所填滿,較大一點孔隙錐果櫟將 可向上生長至冠層,屬於耐陰樹種(陳俊雄與蘇鴻傑,2003;劉靜榆,2004);
但也有研究指出錐果櫟林下徑級分佈不連續(劉靜榆,2004),因此有學者認 為其屬於孔隙種(陳子英,1994)。長尾尖葉櫧分布於台灣楠櫧林帶與櫟林 帶,多出現於稜線,其林下徑級分佈呈現反J型,屬於極盛相植群樹種。鬼 石櫟主要分布於台灣中部櫟林帶,生長於稜線部位亦可在蔽蔭之山谷或溪 畔發現其蹤跡,小苗可耐陰為極盛相植群樹種(劉靜榆,2004)(註:各樹種 在台灣屬優勢種之分布情形與其生態特性之前人研究請參閱附表1、2)。
20
參、材料及方法
一、材料來源
種子於2003年10月底至11月底進行採集。毽子櫟、錐果櫟、赤皮與長 尾尖葉櫧採自棲蘭山區。鬼石櫟則採自台大實驗林和社營林區。種子經過 4℃的層積後,於2004年的2月中旬播種於黑色育苗籃(46.5cm×26cm×6cm),
然 鬼 石 櫟 因 種 子 較 大 , 為 了 避 免 根 系 受 限 , 則 使 用 較 深 之 苗 籃 (46.5cm×26cm×10cm),介質為泥炭土、珍珠石、蛭石,其比例為1:1:1(林 怡芳,2005)。
於2004年3月7日開始將發芽苗從苗籃移至孔徑為18cm,深度16.9cm之 磚紅色容器,生長介質為壤土、泥炭土、珍珠石及蛭石,比例為3:1:1:
1。同年4月26日將苗木以隨機方式移到各光度處理之遮蔭棚(林怡芳,2005)。
2005年7月上旬將各蔭棚中各類苗木以隨機的方式,留下試驗所需的50 株苗木;2005年8月中旬鑒於苗木日漸生長,舊有的容器已不敷生長所需,
因此將所有苗木移至孔徑為23cm,深度22cm之磚紅色容器,生長介質為壤 土、泥炭土、珍珠石及蛭石,比例為3:1:1:1。2005年8月下旬始將150 株一年生青剛櫟苗,平均分配至各蔭棚內。
二、試驗環境概述與設計
試驗地位於宜蘭縣員山鄉臨時苗圃所搭毽之簡易溫室,溫室朝東南 方。遮蔭棚是以鑄鐵管為搭架之半弧形蔭棚,長寬高各為16.8m、4.9m及 2.9m,為了使棚內通風而在上方加開天窗,天窗比遮蔭棚高約0.6m。苗木 放置於棚內離地約60cm之平台上。蔭棚內部設有定時噴水系統,噴水之水 管高度約為2m。為了避免水分對於試驗造成影響,因此噴水之間歇將依季 節進行彈性調整(林怡芳,2005)。
為了瞭解不同林下光度對於6種試驗樹種苗木之形質與生理影響,本試
21
驗將模擬3種不同之林下光度,作為光度處理。一般落葉闊葉林下之相對光 量約為50~60%,鬱閉松類同齡林下約為10~15%,而溫帶闊葉林下相對光量 則是1~5%(王子定,1974)。林文智(2002)測量台灣南部多納針闊葉林林下與 林下孔隙之相對光度分別為3%及15%。王相華(1995)經實地調查墾丁天然 闊葉林內之孔隙中央之光度後,則以相對光度50%模擬300-500 m2孔隙、以 相對光度10%模擬30-50 m2與利用相對光度2.5%模擬1-3 m2孔隙。因此本試 驗分別將蔭棚光度設定為相對光度60%(高光)、10%(中光)及3%(低光)以模 擬中孔隙、小孔隙與林下之光環境。生長效應方面,Kitao et al. (2000)與Kitao et al. (2006)認為相對光度5%是日本北方闊葉林之林木生存所需光度之最低 限制,即使耐陰樹種也亦同;而相對光度10%始其具有正面之生長與生物量 累積。Barnes et al. (1998)指出能於1~3%相對光度下生存之樹種,歸屬於極 度耐陰性樹種(very tolerant species),能夠生存於3~10%之相對光度的樹種則 為耐陰性樹種(tolerant),於10~25%生存者則為中度非耐陰樹種(intermediate species),能於25~50%環境生長者則為非耐陰性樹種(intolerant species),而 極度非耐陰性樹種(very intolerant species)則是只能生存於相對光度50%以 上者。
3種試驗光度乃利用網孔均勻之雙層銀色塑膠針織遮蔭網(遮光之規格 為80%×80%及40%×60%)加以控制,內層均佳透明塑膠布,並將三間遮蔭 棚之相對光度分別調整為60%、10%及3%。為了使空氣流通,避免溫度過 高,將以開天窗之方式與將相對光度為60%之遮蔭棚四週的透明布拉至離 地面約60cm處,以減低棚內溫度過高所帶來之不良效應(林怡芳,2005)。
蔭棚之相對光度經2006年冬夏2日之實地測量,各約略為60.5%,9.2 % 及2.8%。每一蔭棚放置各樹種苗木50株,故每一蔭棚內有300株苗木,並以 隨機方式配置。
22
三、環境因子的量測 (一)光度測量
各處理蔭棚中與棚外空地之實際光量日域變化,將以光度計量器 (Light mater, LI-250, LI-COR, USA)搭配光量子感測器(Quantum Sensor, LI -190, LI-COR, USA)進行監測。於冬夏二季各測定1次,時間從上午7 點至下午6點,每一小時監測一次。
(二)溫度與溼度
以溫濕度計(HOBO, H8 Pro Series, Onset, USA)量測各處理蔭棚中 與棚外空地之溫度與濕度之日域變化。量測時間則與光度同步。
四、試驗方法與步驟
(一)苗高與基徑生長
苗木配置後,於2005年10月中旬始調查苗高與基徑,並在2006年6 月中旬進行複查。以求得試驗期間苗高與基徑之淨生長量。
(二)葉面積與苗木生物量
迨試驗結束後,以標準木法選取各光度處理下之各樹種苗木5株進 行生物量調查。樣本以清水洗淨後,先以手提式葉面積儀 (Portable Area Meter, LI-3000A, LI-COR, USA) 測量其葉面積。依根、莖及葉三部分,
分別放入烘箱內,以75℃烘至恆重(約3天)並秤取各部位之乾重。
(三)葉片面積參數
以上述破壞試驗取得之樣木葉乾重與葉面積換算葉面積比(Leaf area ratio,LAR)與比葉面積 (Leaf area per unit leaf mass,SLA)。
LAR:全株葉面積÷全株乾重(㎝2 g-1) (1)
SLA:葉面積÷葉乾重 (㎝2 g-1) (2)
23
(四)葉綠體色素含量測定
每一光度下之各樹種選取3株樣木。樣本摘取自樣木主梢頂端向下 第4或第5片己完全開展之成熟葉片。先自樣本秤取0.1克之樣品,並置 於研缽,加入2ml的80%丙酮與少量碳酸鈣粉研磨成漿後,再加入適量 的80%丙酮繼續研磨以萃取其葉綠體色素。萃取液經濾紙過濾後,定積 至50ml,並使用分光光度計(UV/ VIS Spectrophotometer, V-530, JASCO, Japan)測定葉綠體色素濃度,並將之帶入Lichtenthaler and Wellburn(1983) 對Arnon(1949)法所提出之修正公式,計算各葉綠體色素含量:
葉綠素a濃度(Chl a)(mg/g)=「12.21×(D663)-2.81×(D646)」×V/W ( 3 ) 葉綠素b濃度(Chl b)(mg/g)=「20.13×(D646)-5.03×(D663)」×V/W ( 4 ) 類胡蘿蔔素濃度(Car) (mg/g)=「1000×(D470)-3.27×Chla-104×Chlb」
×V/229W ( 5 )
Dλ:萃取液在λ波長(nm)之吸光度 V:萃取液總體積(l)
W:葉片鮮重(g)
(五)光合反應曲線之測定
於 2006 年的 5 下旬~ 6 月中旬,各光處理下之每一樹種,選取 5 株苗木作為測定樣木。測定前一天先將苗木移至生長箱內靜置,並施 予充足水分。樣本選自樣木主梢頂端向下第 4 或 5 片已完全展開之成 熟葉片進行光合反應曲線測定。以氣體交換系統(Gas exchange system, LI-6400, LI-COR, USA )作為試驗使用之儀器,測定前先需暖機 30 分 鐘,待其穩定後進行流速與 IRGA 歸零並設定所需之參數(CO2 濃度
24
360ppm,葉室 28℃,相對濕度 70±5%)。測定前,樣本先利用儀器的 紅藍光源以 500μmol photons m-2s-1的光量照射,使其光合器官誘發完 全,待淨光合作用速率穩定後(約略 10min),接以此次試驗的最高光量 階 2000μmol m-2s-1照之,待穩定後紀錄並依序降低光量級。光量級設 定為2000、1600、1200、900、700、500、300、150、50、0 μmol m-2s-1 等10 階。資料的紀錄將使用內建的 Light Curve 模式,設定當光量級的 系統總CV 值於 30 秒內的變化不超過 0.5%時,則進行數據的紀錄,而 在紀錄數據前則先行自動匹對(Match)。
所獲得之光度與其對應之淨光合速率配適於以下之光合模式 (Pearcy and Pfitsch,1995;Lambers et al.,1998):
( )
{ }
-Rd2
A 4
- A Q -
A
A Q max
2 max max
Θ
× Φ
× Θ
× +
× Φ +
×
=Φ (6)
公式(6)中,A 為淨光合速率,Amax為光飽和時之總光合速率(最大淨光 合速率加上暗呼吸率),Φ 為光量子效益(quantum yield),Θ 為曲線彎曲 度(curvature factor,介於 0 與 1 間),Rd 為暗呼吸率,而 Q 為入射光度。
藉由SPSS 統計軟體中的非線性模式(nonlinear model)推估出 Amax、Φ、
θ 及 Rd 4 個參數值。並將所得到之參數,經 Excel 畫出各處理苗木的 光合反應曲線。
LCP 與 Φ 則利用低光下之光合反應曲線求之。2006 年 7 月上旬,
每種光度處理下之每一樹種,另行選取 3 株苗木作測定樣木。測定的 前一天先將苗木移至生長箱內靜置,並施予充足水分。光階設定為50、
40、30、20、10、0 μmol m-2s-1等6 光階。其餘的試驗步驟、儀器使用 與資料紀錄方式等同於上述之光合反應曲線。由於在低光量下光合反 應曲線接近於線性,因此將所獲得的光量級與其相對應的光合作用速
25
率以直線回歸方式求得回歸式Yˆ=a+bx,其中b=Qy(即 Φ),LCP 則為Yˆ 等於零時,x 的值。
(六)葉綠素螢光參數之測定
1.快速光反應曲線(Rapid light curves,RLCs)
快速光反應曲線(RLCs)可以提供光系統中電子傳遞的詳細資訊 與光合活性之評估。不同於氣體交換法之光合反應曲線所能提供之 穩定狀態中的理想光合潛能,其可立即反映環境變動對植物光能利 用 之 影 響 , 亦 可 表 現 出 長 期 光 馴 化 對 於 植 物 之 效 應(Ralph and Gademann, 2005)。
於 2006 年的 5 下旬~ 6 月中旬,各光度處理下之各樹種,選取 5 株苗木作測定樣木,樣本選自主梢頂端向下第 4 或 5 片已完全展 開之成熟葉片。測定的前一天先將樣木搬入生長箱中並充分澆水 後,放置一晚(暗處理)。隔天先利用生長箱之光源(植物生長燈 PHILIPS, SON-T400 AGRO&鹵素燈 PHOENIX HALOGEN LAMP 1000W)施予 30 分鐘 150μmol m-2sec-1之光量激活光合器官後,再經 20 分鐘的暗適應。接著使用攜帶式葉綠素螢光分析儀(Portable Chlorophyll Fluorometer, MINI-PAM, Walz, Germany)進行 RLCs 的測 定,將待測樣本以葉夾(leaf clip)夾取,施以 8 個連續漸強之光階 104、210、350、500、680、980、1330、2000 μmol m-2sec-1 (儀器預 設值),每個光階持續 10 秒後(White and Critchley, 1999;Karim et al., 2003;Campbell et al., 2003;Ralph and Gademann, 2005),測量各光 階下之螢光產值,並求得螢光參數 ETR、NPQ。RLCs 測定時周遭 需保持黑暗狀態,以避免周圍光源干擾測量過程。將各光階所測得 之ETR 代入以下之模式(Ralph and Gademann, 2005)
26
ETR = ETR
max(1 - e
-(αQ ETRmax))
(7)上述模式中ETRmax為最大電子傳遞速率(maxium electron transport rate),α為光限制(light limited)區中的初始斜率(initial slope),Q 為入射光度。可藉由SPSS統計軟體中的非線性模式(nonlinear model) 推算出ETRmax。
2.不同處理光度下之Fv / Fm
此試驗於夜間12:00進行,其目的是為了解不同光處理下,各樹種
長期光抑制之程度。
2006年7月6日的晚上12點取各光度下,每一試驗樹種3株苗木 作為測定樣木,樣本選自主梢頂端向下第4或5片已完全展開之成熟 葉片進行螢光參數Fv / Fm之測定。樣本以MINI-PAM所連接之葉夾夾 住。此時測量光已開啟,並可得暗適應最小螢光量FO,接著以0.8秒 之飽和脈衝光(4500 μmol m-2 s-1)照之,測得Fm。將所得到之螢光值 帶入公式(8)中,即可獲得試驗樹種在此光度處理下之Fv / Fm。 3.螢光參數之日域變化
於2006年7月6日清晨於不同光處理下之各試驗樹種選取3株作 為樣木,並取其主梢頂端向下第4或5片已完全展開之成熟葉作為樣 本。樣本測定前先使其處於暗適應狀態25分鐘,後以MINI-PAM所 連接之葉夾夾住,並按照上述步驟(不同處理光度下之Fv / Fm)測得FO
與Fm。接著使樣本處於光適應狀態下20分鐘,再依循測試FO與Fm之 步驟,則得到Fs與Fm′,將所得到之螢光值帶入螢光參數公式(8)(9)(10) 後,即可獲得參數之數值。試驗期間從早上7:30~下午18:00,每2小 時測定一次。
27
Fv / Fm=(Fm – Fo) / Fm:光系統 II 最大光化學潛能 (8)
ΦPSII=(Fm′- Fs) / Fm′:PSII實際光能轉換效率 ( 9 )
NPQ= Fm - Fm′/ Fm′:非光化學消散 (10)
五、資料分析
試驗樹種於不同光度處理下之淨苗高生長與淨基徑生長將進行共變數 分析(ANCOVA),若排除共變項對自變項的影響後,處理間具顯著差異(P
<0.05),則以 LSD 進行事後分析。而光度處理對於試驗樹種之生物量、葉 面積參數、葉綠體色素含量與其之間比例、RLCs 之 NPQ 與午夜之 Fv / Fm 則以單因子變異數(ANOVA)比較其差異。若處理間具顯著差異(p<0.05),則 以LSD 進行事後分析處理。所有的分析皆以 SPSS version 10.0(SPSS, Inc., Chicago, USA )統計套裝軟體完成。
28
肆、結果
一、試驗地環境參數量測
於 2006 年 2 月 14 日(晴天)與 2006 年 7 月 6 日(晴天)以 LI-250 連接光 量子感測器(LI-190)量測當日光度之日域變化;HOBO 溫濕度計測量當日溫 度與相對濕度之日域變化。
2006 年 2 月 14,自清晨 7 點開始量測試驗地(空曠地與各不同遮蔭程度 之蔭棚)之光度、溫度,與相對濕度之數值。以空曠地為例,光度從清晨 7 點開始測量,其數值將隨著時間增加而遞增。11 點時到達當日之最高光度 (1545 μmol photons m-2sec-1),迨 11 點過後,光度將隨時間的增加而減少(圖 1a)。溫度趨勢如同光度,最高溫度出現於 11 點時(27.1 ) (℃ 圖1b),而相對 濕度之日域變化乃與光度,溫度相反,最低濕度出現於11 時(43%)(圖 1c),
11 點過後相對溼度將隨著時間的增加而遞增。相對光度 60%、10%與 3%之 蔭棚,其光度與溫濕度之日域變化趨勢,乃與空曠地一致(圖 1)。
2006 年 7 月 6 日隸屬於當年夏季,為了配合葉綠素螢光日過程之量測,
當日環境參數之量測,將始於上午7:30,並迄於下午 18 時。光度與相對溼 度日過程之變化趨勢相似於冬季,最高光度出現於當日11:30(圖 2a);溼度 則是在12:30 屆於最低(圖 2c);然則溫度在上午 8:30 達到最高(圖 2b )。光 度與溫度屆於最大值後,都將隨時間的增加而減少,而相對濕度則是到達 低點後,將隨著時間增加而趨於遞增 (圖 2c)。