國立臺灣大學醫學院暨工學院醫學工程學研究所 博士論文
Graduate Institute of Biomedical Engineering College of Medicine and College of Engineering
National Taiwan University Doctoral dissertation
使用斷層掃描影像建立全自動的 冠狀動脈分割與斑塊定量演算法
An Automated Algorithm for Coronary Artery Reconstruction and Plaque Burden Assessment in Multi-Slice Computed Tomography
洪培凱 Pei-Kai Hung
指導教授:陳中明 博士 Advisor: Chung-Ming Chen, Ph.D.
中華民國 105 年 7 月
July, 2016
口試委員會審定書
誌謝
攻讀博士學位的數個寒暑,是我生命中最精彩的歲月。儘管放棄學位的念頭 不時侵襲著不夠成熟的我,但我總會藉由思考著要在博士論文的致謝中留下那些 言語來勉勵自己重新出發。一路走來,有許多值得感激的人事物點滴在心頭,到 了真正要開始動筆寫致謝的一刻,我卻百感交集不知所云。我最先感謝的,應是 那些為我帶來磨難的人,包括我自己。感謝我的過去與現在、我的缺點與優點、
我的脆弱與堅強,讓我能持續努力使自己成為一個更好的人。
感謝我的指導老師陳教授中明,總是大方地給予我自由揮灑的空間,讓我得 以順著自己的學習曲線,感受學術研究與家庭生活的本質。感謝臺大醫院的王醫 師宗道、李醫師文正,您們總是無私地傾囊相授,兩位醫師的專業知識與生活態 度一直是我所景仰與嚮往的。在我人生中的兩個大日子裡(結婚宴客、論文口試), 能得到兩位偶像的祝福與加持,是我莫大的榮幸。感謝臺北醫學大學蔡醫師仁雨 的春風化雨,您那多到滿出來的父愛穿透了人與人之間的距離。您對晚輩的溫暖 關懷,亦是支持我完成博士學位的安定力量。
若說我在台灣大學醫學工程學研究所接受 data to knowledge 的訓練,那麼我 在衛生福利部的探險便是實現 knowledge to practice 的體驗。
從中規中矩的研究工作到五花八門的交辦任務,是如同雲霄飛車般印象深刻 的旅程,感謝林部長奏延與珮萱秘書帶給我的震撼教育。機關首長的智慧與身段、
首長秘書的細心與明快,著實令我大開眼界。是您們讓我開始省思,真正體認到 美好的事物(政策)得以開花結果前,其背後累積了多少動人的故事。感謝施技 監養志對我栽培與厚愛,不時引導著好傻好天真的我走回正軌。若說技監教導我
「做人的道理」,那麼教導我「做事的方法」的人就非顯揚博士莫屬了!再次感謝 諸位好長官的提攜,讓我得以站在各種不同的高度,欣賞著各種從未見過的風景。
最後,我要感謝那些愛我、支持我的人,感謝您們總是包容著不善於表達感 激的我。感謝您們無私的愛與陪伴,支持著看似堅強、實為逞強的我。感謝我的 父母,一路看著我成長茁壯;謝謝我的美豔人妻温惠與我的前世情人語彤,讓我 無後顧之憂地完成學業,並給我繼續努力的人生目標。
洪培凱 于 台灣大學展書樓 2016.8
中文摘要
動脈粥狀硬化所造成的心血管疾病每年都奪走許多寶貴的性命,已連年佔據 台灣十大死因之第二位。電腦斷層掃描影像是主要用來診斷此一疾病之影像工具。
為了對這個疾病有更深入的了解,我們透過電腦輔助診斷與全自動的影像分割演 算法來重建冠狀動脈結構,並探索血管管腔狹窄所衍伸之問題。
透過優化血管中心線萃取技術並提供血管狹窄程度之整合資訊,本研究致力於 建立全自動之電腦輔助診斷於心血管疾病之應用。本研究利用電腦斷層影像發展 全自動化之升主動脈分割方法來分割主動脈瓣處的「3顆球」結構,並利用K-mean 濾波器進行影像前處理,排除不必要之背景資訊,使本研究中的自適應區域成長 演算法得以完整分割冠狀動脈血管。組合所有具血管特徵之像素,並加上血管中 心線演算法後,便可對血管管腔中的資訊進行分析。
研究中發現「3 顆球」結構之確立有助於降低冠狀動脈起點偵測之難度。而整 合灰階值與管狀結構資訊之自適應區域成長演算法能在避免分割影像溢出的情況 下得到完整之冠狀動脈網路。藉由血管中心線萃取演算法,我們更得以沿著血管 方向分析此一血管路徑上是否發生狹窄、狹窄處之組成成分為何,藉已得到具臨 床價值之資訊。
在臨床運用上,本研究之成果將有助於更精準的描述心血管疾病以並提供相關 疾病進程之資訊。
關鍵字: 冠狀動脈分割、主動脈瓣分割、血管中心線萃取、斑塊內容物分析
ABSTRACT
Atherosclerosis, the leading cause of heart disease, is still ranked as second major cause of death in Taiwan. Multi-slice computed tomography (MSCT) is the conventional strategy for diagnosis. For the assessment of coronary artery disease, an automated computer-aided diagnosis system is essentially needed to clarify both lumen volume and coronary tree.
This research aims to develop automated system, improve the extraction of coronary artery centerline, and provide comprehensive information of stenosis. We collected MSCT images and developed an automated algorithm to extract ascending aorta along with coronary artery from serial computed tomography images. K-means clustering is applied for background exclusion, and the structure of ball-like aortic root is particularly segmented. In self-adjusting region growing scheme, the intensity of each voxel and its neighborhood are both calculated during the establishment of lumen volume. Assembling qualified voxels, the coronary tree is revealed and coronary artery centerline extracted. For further analysis, lumen volume is analyzed after vessel skeletonization is performed.
It was demonstrated the delineation of ball-like aortic root would simplify the detection of coronary artery ostium. Integration of neighborhood and vesselness information to the self-adapted region growing scheme was approved to prevent the occurrence of leakage and facilitate the inclusion or exclusion of voxels with similar intensity. With centerline extraction, analysis of vessel profile and quantitation of plaque burden were achieved and diagnostic information acquired.
For clinical practice, the automated algorithm and computer-aided tracking system will contribute to consistent and effective assessment for coronary artery disease.
Key words: coronary artery, aortic root, centerline extraction, plaque burden
目錄
口試委員會審定書 ...i
誌謝 ... ii
中文摘要 ... iii
ABSTRACT ...iv
目錄 ...vi
圖目錄 ...ix
表目錄 ... xii
Chapter 1 緒論... 1
1.1 前言 ... 1
1.1.1 醫療資訊之電子化 ... 1
1.1.2 醫療器材軟體之法規調和 ... 2
1.1.3 電腦輔助診斷之利基 ... 3
1.2 研究動機 ... 4
1.2.1 心血管疾病與肥胖趨勢的全球化 ... 4
1.2.2 動脈粥狀硬化之致病機轉 ... 5
1.2.3 動脈粥狀硬化之診斷方式 ... 6
1.3 研究目的 ... 9
1.3.1 冠狀動脈結構與血管堵塞風險評估 ... 9
1.3.2 冠狀動脈結構偵測之困難 ... 12
1.3.3 本研究之目的與利基 ... 14
1.4 文獻探討 ... 14
1.4.1 血管分割演算法 ... 14
1.4.2 冠狀動脈起點偵測 ... 15
1.4.3 冠狀動脈之血管中心線萃取與血管邊緣分割 ... 17
1.4.4 血管特徵分析 ... 21
1.4.5 關於本研究 ... 23
1.5 論文架構 ... 23
Chapter 2 研究方法與材料 ... 24
2.1 研究材料 ... 24
2.2 研究架構 ... 24
2.3 升主動脈分割 ... 25
2.3.1 升主動脈於首張 MSCT 影像中的位置 ... 26
2.3.2 以升主動脈為基準之座標轉換 ... 28
2.3.3 由升主動脈偵測冠狀動脈起點 ... 32
2.4 冠狀動脈結構重建 ... 34
2.4.1 管狀結構資訊(Frangi’s filter) ... 34
2.4.2 海森矩陣之應用(Hessian matrix) ... 36
2.4.3 整合影像灰階值與管狀結構資訊之區域成長演算法 ... 38
2.5 血管特徵分析 ... 39
2.5.1 血管中心線萃取 ... 39
2.5.2 血管特徵分析 ... 41
Chapter 3 研究結果與討論 ... 44
3.1 簡介 ... 44
3.2 升主動脈分割 ... 44
3.2.1 升主動脈分割結果 ... 44
3.2.2 分割結果說明與討論 ... 47
3.3 冠狀動脈結構重建 ... 47
3.3.1 冠狀動脈重建結果 ... 47
3.3.2 重建結果說明與討論 ... 51
3.4 血管特徵分析 ... 52
3.4.1 血管邊緣分析與比較 ... 52
3.4.2 血管切平面特徵分析結果 ... 56
3.4.3 血管分析結果說明與討論 ... 60
3.5 研究限制 ... 62
3.6 綜合討論與未來展望 ... 63
Chapter 4 結論... 64
REFERENCE ... 65
圖目錄
圖 1.1 我國電子病歷發展之過程與目標 [1]。 ... 1
圖 1.2 目前我國醫療器材軟體許可證之登記類別百分比 [3]。 ... 3
圖 1.3 104 年主要死因標準化死亡率與死亡人數占率。 ... 4
圖 1.4 104 年兩性十大死因死亡率。 ... 5
圖 1.5 心臟冠狀動脈與粥狀硬化示意圖 [9]。 ... 6
圖 1.6 電腦斷層掃描影像(1):(A)無顯影劑(B)有顯影劑。 ... 8
圖 1.7 電腦斷層掃描影像(2):(A)商用軟體所得到之冠狀動脈血管結構(B) 單一冠狀動脈血管之二維投影(C)依血管中心線拉直(B)之冠狀動 脈。 ... 8
圖 1.8 冠狀動脈之結構 [14]。 ... 10
圖 1.9 冠狀動脈分支處可能發生狹窄的 7 種情形 [14]。 ... 11
圖 1.10 電腦斷層掃描影像(3)。(A)部份血管因彎曲程度過大,導致無法於 同一平面顯示完整血管,(B)冠狀動脈與其他灰階值相近之組織相連 的例子。 ... 13
圖 1.11 電腦斷層掃描影像(4)。(A)升主動脈與冠狀動脈之輪廓(B)以型 態運算子排除冠狀動脈後之升主動脈輪廓。 ... 16
圖 1.12 依不同平面顯示冠狀動脈起點(如箭頭處),右下為冠狀動脈之三維結 構示意圖 [28]。 ... 18
圖 1.13 冠狀動脈中心線萃取演算法評比結果 [28]。 ... 19 圖 1.14 冠狀動脈血管管腔分割結果(臨床醫師與 5 種演算法之結果比較) [42]
... 20 圖 1.15 冠狀動脈縱向切面之灰階值特徵(上)與灰階值對應表(下) [43] .. 21 圖 1.16 透過 3 種不同視角觀測同一混合型斑塊,(A)原始影像(B)將不同灰
階值分佈之斑塊標上顏色(黃色:鈣化斑塊;紅色:非鈣化斑塊)(C)
斑塊輪廓 [43] ... 22 圖 2.1 本研究之架構 ... 25 圖 2.2 主動脈瓣之剖面於(A)血管攝影及(B、C)MSCT 影像,(D、E)中
明顯可見主動脈瓣之「3 顆球」結構 [51] ... 26 圖 2.3 MSCT 首張影像之灰階值分佈,M1、M2、M3 分別代表血液(與骨頭)、
軟組織、空氣之灰階值分佈 [23] ... 28 圖 2.4 以「3 顆球」為基準之座標系統變換(示意圖) ... 29 圖 2.5 早期冠狀動脈起點偵測之成果。以圓形圈選心臟(黃色)與升主動脈(紅
色)範圍,藍色處為自動偵測之左冠狀動脈(left main)起點。 ... 32 圖 2.6 實際輪廓與「3 顆球」輪廓之差異(示意圖) ... 33 圖 2.7 Gaussian kernel 之二階導數(左)與 Hessian matrix 所推導之特徵值向
量(右) [20] ... 35 圖 2.8 用於血管分割之六連通區域成長演算法 ... 38 圖 2.9 MHT 演算法中血管中心線萃取之流程(示意圖) ... 39 圖 2.10 MHT 演算法中(A)管狀結構模型函數與(B)相關向量示意圖。 ... 40 圖 2.11 血管特徵分析(示意圖) ... 43 圖 3.1 升主動脈分割結果呈現說明 ... 44 圖 3.2 臨床案例分析-1 ... 45
圖 3.3 臨床案例分析-2 ... 46
圖 3.4 冠狀動脈起點偵測與血管分割呈現說明 ... 48
圖 3.5 臨床案例分析-1 ... 49
圖 3.6 臨床案例分析-2 ... 50
圖 3.7 升主動脈分割(含部分冠狀動脈),紅色虛線部分為血管中心線。 .... 51
圖 3.8 兩種描述血管方法(RG & MHT)之血管內部直徑比例關係圖 [24] .. 53
圖 3.9 兩種描述血管切平面方法之比較圖-1。(A)以正圓圈選血管切平面中的 血管,(B)以血管分割演算法所得知結果圈選切平面中的血管,(C) 以(A)之結果分割斑塊,(D)以(B)之結果分割斑塊 [24] ... 54
圖 3.10 兩種描述血管切平面方法之比較圖-2。(A)以正圓圈選血管切平面中的 血管,(B)以血管分割演算法所得知結果圈選切平面中的血管,(C) 以(A)之結果分割斑塊,(D)以(B)之結果分割斑塊 [24] ... 55
圖 3.11 冠狀動脈重建(左)與指定血管之分析-1(右,刻度間隔:2 mm) .. 56
圖 3.12 冠狀動脈重建(左)與指定血管之分析-2(右,刻度間隔:2 mm) .. 56
圖 3.13 血管特徵分析 (刻度間隔:2 mm) ... 57
圖 3.14 血管特徵分析,並將鈣化斑塊之切平面展開(刻度間隔:2 mm)。 ... 59
圖 3.15 血管切平面展開圖之分析 ... 60
圖 3.16 血管特徵分析 ... 61
表目錄
表 2.1 海森矩陣之特徵值對應三維空間之型態特徵 ... 37
表 3.1 斑塊危險程度對應表 [24] ... 53
表 3.2 不同血管輪廓分割方法下之斑塊嚴重程度分析-1 [24] ... 54
表 3.3 不同血管輪廓分割方法下之斑塊嚴重程度分析-2 [24] ... 55
Chapter 1 緒論
1.1 前言
1.1.1 醫療資訊之電子化
隨著醫療技術日新月異,醫療資訊的取得也更加容易。醫學影像的分析與電 腦輔助診斷工具的發展亦應與時俱進,影像擷取及傳輸系統(Picture archiving and communication system, PACS)、電子病歷系統(Electronic Medical Record, EMR)、
醫療資訊管理系統(Health information system, HIS)之整合與加值應用,將有機會 成為下一個科技發展的重點。
衛生福利部延續過去衛生署時期的「網路健康服務推動計畫」、「衛生局所網 路便民服務計畫」,戮力推動國際醫療資訊標準之本土化以及推廣醫療院所實施電 子病歷。藉由 97 年開始實施之「國民健康資訊建設計畫」與 99 年開始推動「加 速醫療院所實施電子病歷系統計畫」,完成全國醫學影像交換中心的建置,此中心 也逐步擴充為全國電子病歷交換中心。101 年所啟動之台灣健康雲計畫(健康雲項 下包含「醫療雲」、「照護雲」、「保健雲」與「防疫雲」等四朵雲),透過健康資通 訊基礎建設及雲端化之概念,促使醫療院所、健康服務提供者互相合作,讓國民 得以用更便利得方式取得個人健康醫療之資訊。其中最重要的關鍵,便是電子病 歷交換計畫。
圖 1.1 我國電子病歷發展之過程與目標 [1]。
根據衛生福利部資料顯示,在「加速醫療院所實施電子病歷系統計畫」告一 段落後,全台估計有 282 家醫院、2,000 家診所及 2 家署立醫院實施電子病歷;其 中 142 家醫院可跨院查詢醫學影像及報告、血液檢驗、出院病摘或用藥紀錄等 4 大類電子病歷。在電子病歷雲端化後,醫師將可直接判讀病人於合作轉診醫院所 做的檢查報告,長期下來將可節省民眾就醫的時間與金錢,對居住於山區離島等 偏遠地區的國民健康更是影響深遠。預計於 2016 年時,全台 500 家醫院及 2 萬家 診所都將正式進入電子病歷時代。
1.1.2 醫療器材軟體之法規調和
為協助國內產業界投入年營業額高達 320 億美元之高階醫學影像器材市場,
經濟部技術處於 99 年舉辦「高階醫學影像診斷醫材產業發展研討會」,結合國家 中山科學研究院、工業技術研究院與國家衛生研究院等單位共同合作。從醫療影 像平台、訊號擷取與軟體辨識等領域投入研發,並輔以臨床驗證、快速試製、上 市法規等之協助,全力推動高階醫學影像產業發展 [2]。
財團法人醫藥品查驗中心醫療器材組亦於 104 年以專文「醫療器材軟體於國 際醫療法規管理論壇之定義與風險分類」對國際相關法規進行調和 [3]。其內文指 出:「歐美國家將獨立運作的醫療用軟體視為醫療器材,並加以管理。歐盟執行委 員會 (European Commission, EC)於 2007 年公告第 47 號指令 [4],擴大醫療器材 指令 93/42/EEC [5] 中的適用範圍,將具有醫療目的且獨立運作之軟體,納入醫療 器材列管,並定義為「獨立運作的醫療用軟體」(stand-alone software used for medical purposes);美國食品藥物管理局(Food and Drug Administration ,FDA)雖未將此類軟 體列於美國藥物食品化妝品管理法(Federal Food, Drug, and Cosmetic Act, FD&C Act)第 201(h)節的條文中,但仍將此類軟體以符合「預期用途作為診斷動物或人類 疾病或其他身體狀況;或用於治癒、減緩、治療或預防疾病;不經由動物或人類 身上的化學反應或新陳代謝之途徑達成其主要目的,來影響動物或人類身體的功 能或結構。」 [6],作為醫療器材之附件或是「醫療器材軟體 (medical device software) 」管理」。衛生福利部食品藥物管理署更委託工業技術研究院協助研擬「醫 療器材軟體確效指引(草案)」與「醫用行動應用程式指引(草案)」,並於 105 年 7 月召開說明會,顯見政府對醫療資訊此一領域之關注與投入。
1.1.3 電腦輔助診斷之利基
資訊科技日新月異,在各個領域都改善了傳統人力工作上的盲點,大幅提昇 工作效率與成本效益。使用電腦斷層影像(Multi-slice computed tomography, MSCT)
進行之醫療診斷需憑藉醫師或放射師之專業的知識與經驗判讀影像,惟 MSCT 影 像資料量龐大且逐張檢視影像耗費大量人力與時間。因此,近年來電腦輔助診斷 的發展逐步地減輕醫師們負擔,在整個診斷的過程中輔助醫師判讀影像並以客觀 與量化的角度提供醫師更準確、更多元的資料以加速診斷的速度與準確性。
診斷工具開發之成功與否的關鍵除繫本身功能設計的周延性外,亦取決於與 利害關係人(stakeholder)的良性互動。隨著醫療資訊的電子化與相關醫療器材軟 體法規的調和,電腦輔助診斷工具開發將會更為蓬勃發展。若能在電腦輔助診斷 工具設計之初通盤考慮各個環節,讓電腦輔助診斷的成果得以提升醫療品質、增 進國人健康自主管理與預防。我們的努力定能成為溫暖醫病關係、營造健康社會 的重要基石。
圖 1.2 目前我國醫療器材軟體許可證之登記類別百分比 [3]。
1.2 研究動機
1.2.1 心血管疾病與肥胖趨勢的全球化
依據衛生福利部最新公開之國人死因統計結果指出,104 年十大死因以慢性疾 病為主,死亡率依序為(1)惡性腫瘤(2)心臟疾病(3)腦血管疾病(4)肺炎(5)糖尿病(6) 事故傷害(7)慢性下呼吸道疾病(8)高血壓性疾病(9)慢性肝病及肝硬化(10)腎炎、腎 病症候群及腎病變。10 年來十大死因標準化死亡率及其占總死亡人數比率之變動 觀察,均呈上升者有高血壓性疾病與肺炎;均呈下降者有腦血管疾病、事故傷害、
糖尿病、慢性肝病與肝硬化與腎炎、腎病症候群及腎病變、慢性下呼吸道疾病;
另惡性腫瘤死亡人數占總死亡人數比率雖上升,標準化死亡率則呈下降 [7]。(註:
死因統計為符公共衛生之疾病預防及國際比較目的,係依世界衛生組織(WHO)
疾病分類之死因選碼準則定義,以導致死亡的原始病因作為統計依據,我國自 97 年起以國際疾病分類標準第 10 版(ICD-10)進行分類。另標準化死亡率係依世界衛 生組織(WHO)編布之西元 2000 年世界標準人口年齡結構調整計算。)
圖 1.3 104 年主要死因標準化死亡率與死亡人數占率。
惡性腫瘤 心臟疾病(高血壓性疾病除
外)
腦血管疾病
肺炎
糖尿病 事故傷害
慢性下呼吸道疾病
高血壓性疾病
腎炎、腎病症候群及腎病變 慢性肝病及肝硬化
1 2
3
4
5 6 7
8
9 10
-3.0 -2.0 -1.0 0.0 1.0 2.0 3.0
-60.0 -40.0 -20.0 0.0 20.0 40.0 60.0 80.0 100.0
成 長 率
( 標 準 化 死 亡 率 增 減 百 分 比
) 占率增減數
圖4 主要死因標準化死亡率與死亡人數占率--104年vs.94年
註:1.第一象限內各點表該死因不論成長率或占有率均在增加,其距離原點愈遠其影響力愈大。
2.第三象限表該死因不論成長率或占有率均在減少,其影響程度呈現萎縮。
圖 1.4 104 年兩性十大死因死亡率。
隨著現代化飲食與生活習慣改變,肥胖趨勢的全球化已在過去的 30 年內衍生 了許多醫療問題,包括了心血管疾病的形成與致死率的提升 [8]。根據台灣營養健 康狀況變遷調查(NAHSIT),隨著生活習慣與飲食環境的改變,肥胖趨勢亦有年 輕化的現象。估計投入於過重及肥胖所產生的代謝相關疾病的國家醫療支出已達 3%以上,世界衛生組織歐洲區署亦指出約 6%的健康照護成本與肥胖有關。肥胖更 是導致心血管疾病的高風險因子之一,肥胖趨勢的全球化與年輕化亦導致了罹患 心血管疾病致死的案例層出不窮,其中又以動脈粥狀硬化(atherosclerosis)等冠 狀動脈疾病(coronary artery disease)造成心肌梗塞致死的情況最為常見。肥胖問 題與心血管疾病不僅嚴重影響國人生命健康與生活品質,其衍生之龐大醫療與照 護成本更是引起了政府的正視,政府更疾呼「肥胖問題是國家安全危機」。因此,
宣導預防心血管疾病「早期發現、早期治療」已到了刻不容緩的地步。
1.2.2 動脈粥狀硬化之致病機轉
心臟是循環系統的動力來源,推動循環系統中血管的血液。冠狀動脈則是位 在心臟上的血管結構,分為左冠狀動脈與右冠狀動脈共同包覆心臟,其功能為供 心肌組織所需的氧氣與養分,使心肌能正常收縮維持體循環。若冠狀動脈上發生 了狹窄(stenosis)或是堵塞(obstruction)的情況,極有可能造成心肌的缺血
(ischemia),心肌組織無法正常運作後引發心肌梗塞(myocardial infarction),進 而影響循環系統導致無法回復的嚴重傷害(如圖 1.5)。
20.7 24.4
28.7 40.4 41.5 43.5
56.2 56.3
96.1
245.8
11.5 14.0 16.5 20.0 22.8 35.6 39.0 39.8 67.7 153.5
蓄意自我傷害(自殺)
高血壓性疾病 慢性肝病及肝硬化
慢性下呼吸道疾病 糖尿病
事故傷害 肺炎 腦血管疾病
心臟疾病(高血壓性疾病除外)
惡性腫瘤
敗血症 慢性下呼吸道疾病 事故傷害 腎炎、腎病症候群及腎病變
高血壓性疾病 肺炎 腦血管疾病
糖尿病 心臟疾病(高血壓性疾病除外)
惡性腫瘤
839.2 555.7
250.0 200.0 150.0 100.0 50.0 0.0 50.0 100.0 150.0 200.0 250.0
女性 男性
圖5 104年十大死因死亡率-男性 vs.女性
女性所有死因死亡率 男性所有死因死亡率
每十萬人口
圖 1.5 心臟冠狀動脈與粥狀硬化示意圖 [9]。
發生狹窄或阻塞的起因為冠狀動脈的內皮細胞受損後,膽固醇在其內皮細胞 下堆積造成血管管腔之形變。膽固醇的堆積,使得血管的內皮細胞改變性質,易 發生血小板堆積和平滑肌增生,形成所謂的動脈粥狀硬化 [10]。一般正常的血管 內壁是平滑暢通的,一旦管壁上生成動脈粥狀硬化的腫塊,血管壁會因此變得粗 糙不平且管徑變小、血流不暢順,影響氧氣與養份的供應。動脈粥狀硬化所形成 的斑塊(plaque)在結構上又可分為穩定的斑塊與不穩定的斑塊:穩定的斑塊通常 會造成血管狹窄並短暫地影響血流,造成小部分區域的心肌組織因缺血而無法正 常代謝,臨床上的症狀即為心絞痛;不穩定的斑塊則容易破裂,且破裂後會直接 堵塞後方小血管,造成大範圍的心肌組織缺血而導致心肌梗塞。由於斑塊的形成 是脂肪與膽固醇緩慢堆積於血管內皮下的過程,若能早期偵測不穩定的斑塊並定 期追蹤其進程,便能有效達到預防的目標。
1.2.3 動脈粥狀硬化之診斷方式
臨 床 上 可 用 來 偵 測 斑 塊 與 血 管 狹 窄 的 方 法 相 當 多 , 其 中 以 血 管 攝 影
(Conventional coronary angiography, CAG)與電腦斷層掃瞄(Multi-Slice Computed Tomography, MSCT)被廣泛使用。CAG 為侵入式的檢查,可直接觀測血管狹窄的
位置、數量以及嚴重程度;MSCT 的優勢則是非侵入式的檢查,提供了高解析度 的三維空間來保存冠狀動脈的資訊以及分辨鈣化斑塊與非鈣化斑塊之能力,成為 診斷冠狀動脈疾病之一大利器 [11]。
MSCT 是一種利用數位幾何處理後重建(Image reconstruction)的三維放射線 醫學影像。由於不同的生物組織對 X 射線的阻射率(Radio-density)也不盡相同,
可形成影像上的對比。透過電腦的三維重建技術將帶有對比資訊的灰階影像用電 腦軟體加以堆疊,即可形成立體影像。MSCT 影像中以 Hounsfield units(HU)為 標定密度之單位,水的 HU 被定義為 0。在一般 MSCT 影像中,HU 之分布範圍 從值 -3024 至 2000 左右,血液的 HU 約是 55,阻射率較高的物質(如鈣化的斑 塊或骨頭等硬組織)具有較高的 HU 值,顯示在影像上也較為明亮。在目標物與 背景物之阻射率差異較小時,對比較不明顯,可藉由顯影劑來幫助判讀。臨床上 電腦斷層掃描影像可分為含顯影劑與不含顯影劑兩種(如圖 1.6),由於含顯影劑 的影像中血管特別明顯,常用來觀察冠狀動脈血管管腔狹窄的問題,以及偵測冠 狀動脈鈣化斑塊 [12]。而不含顯影劑之電腦斷層掃描影像則著重在分析斑塊組成,
並提供血管鈣化指數 [13],反映出血管狀況和狹窄機率並分析其危險性。
雖然 MSCT 能提供大量資訊,且此一非侵入性檢查擁有低風險、較高的舒適 度、不需麻醉等等的優點,但如何在這些資訊中取得有利於醫師進行診斷的部分 著實為一大課題,且分析影像時往往容易因解析度不足及背景雜訊干擾而發生誤 判。透過市售軟體協助電腦輔助診斷的過程中,可由電腦系統(自動)找出心臟 與主動脈的位置,並且(手動)去除其他與心臟無關的組織;接著對原始影像進 行冠狀動脈影像血管結構分割,尋找完整冠狀動脈血管結構的走向與分布位置,
此步驟採取的演算法仍屬於半自動的區域成長分割演算法,仍需大量的人力輔助 來完成。儘管現階段使用之電腦輔助診斷工具需要大量人工介入操作,但其分析 結果確實有助於協助臨床醫師查看血管哪個區段發生狹窄,並協助偵測是否存在 斑塊(如圖 1.7)。
圖 1.6 電腦斷層掃描影像(1):(A)無顯影劑(B)有顯影劑。
圖 1.7 電腦斷層掃描影像(2):(A)商用軟體所得到之冠狀動脈血管結構(B)
單一冠狀動脈血管之二維投影(C)依血管中心線拉直(B)之冠狀動脈。
A B
1.3 研究目的
1.3.1 冠狀動脈結構與血管堵塞風險評估
本研究之目的在於分析冠狀動脈之結構與偵測冠狀動脈之狹窄。為了對研究 主題有更深入的了解,我們參考了 Sianos 等人有關「The SYNTAX Score」的研究 [14]。該研究指出,以左心室(left ventricle, LV)的循環供給作為區分,冠狀動脈 結構的種類可分為「right dominant」與「left dominant」兩大類。在右冠狀動脈(right coronary artery, RCA)支應 LV 的情況下(right dominant),RCA 大約支應了 16%
的 LV 循環,左冠狀動脈(left coronary artery, LCA)則支應了剩下的 84%。在 LCA 支應的 84%中,大約有 66%來自左前降支(left anterior descending artery, LAD)、
33%來自左迴旋支(left circumflex coronary artery, LCX)。相反的,在 RCA 不支應 LV 的情況下,則由 LAD 完全供應 LV 之循環(left dominant),冠狀動脈之結構亦 因對 LV 之循環供給差異而對應改變(詳如圖 1.8)。在 SYNTAX Score 的設定中,
每條管狀動脈之狀態(狹窄程度)都會列入評分計算,且會依據每條血管之重要 性設定其權重參數。對此,找到相對應血管進行評估亦為本研究的重點之一。
SYNTAX Score 對血管堵塞(occlusive lesion)程度之分析則較為簡略,僅藉 由二維之血管攝影影像對直徑 1.5mm 以上之血管進行評估,判斷標準為血管狹窄 處(diameter stenosis)是否造成了血管直徑(血液可流通之管腔部分)減少一半以 上。血管堵塞的風險評估則考量了實施侵入性血管攝影手術時是否容易破壞斑塊 造成出血,不同的堵塞狀況下亦會有不同的權重參數。在 SYNTAX Score 設定中,
將完全堵塞(100% diameter stenosis)的風險因子設定為 5、嚴重堵塞(50% - 99%
diameter stenosis)設定為 2、輕微堵塞(0% - 49% diameter stenosis)則設定為 1。
圖 1.8 冠狀動脈之結構 [14]。
已知斑塊的大小(直接影響血管管腔與血液流量)與斑塊內容物組成(是否 容易破裂造成後方小血管堵塞)都是評估血管堵塞的依據。在 MSCT 影像中,前 者可藉由斑塊的體積(volume)來進行定量分析,後者則可藉由斑塊結構內所有 像素之灰階值分佈(distribution)來進行定性分析。但圖 1.9 則揭露了另一項重要 的評估依據:「斑塊的位置」。由於斑塊的形成與血管內皮細胞受損有關,因此斑 塊可能發生於冠狀動脈中的任何位置,但同樣的斑塊出現在不同的位置卻可能造 成截然不同的風險。考量實施心導管手術時,導管必須來回穿梭於血管中,每次 移動都可能引發斑塊的破裂造成出血。因此 SYNTAX score 對出現在血管分支處或 血管彎曲處之斑塊亦會反映出較高的風險權重。
圖 1.9 冠狀動脈分支處可能發生狹窄的 7 種情形 [14]。
1.3.2 冠狀動脈結構偵測之困難
由§1.3.1 之臨床研究,可知在動脈粥狀硬化之嚴重度分析中,每條冠狀動脈、
每個血管分支、每段因存在斑塊而對應產生形變的血管管腔都至關重要。然而,
在 MSCT 影像中分割冠狀動脈卻存在許多困難。以解剖學的觀點來看,分割冠狀 動脈之困難在於:血管相對細小、多分支、血管走向差異、曲折、血管壁(尤指 斑塊堆積處)與周遭其他相鄰之軟組織差異不明顯。以造影工具的觀點來看,MSCT 影像分析之困難點則在於影像解析度受限於儀器、施打顯影劑之不確定性、外在 條件造成影像雜訊(artifact)等。
上述困難逐項說明如下:
一、 冠狀動脈相對細小:在不考慮血管狹窄與堵塞的情形下,MSCT 影像中幾條 主要的冠狀動脈其直徑大約都落在 3.0 mm ~ 5.0 mm 左右,相當於 6 ~ 9 個連 續像素之長度。然而,受限於多數造影工具之影像解析度,一般臨床分析中 僅只評估直徑 1.5 mm 以上之血管(相當於 3 ~ 4 個連續像素之長度)。由於 動脈粥狀硬化之風險評估與血液循環供應之穩定性有關,所以評估重點多半 放在主要的大血管上,細小血管則容易被忽略。另一方面,大血管的結構明 確,對於雜訊有較高的容忍度;反之,細小血管容易被雜訊引導而造成錯誤 的過度分割結果(leakage)。因此對臨床醫師與電腦輔助診斷而言,血管末梢 與血管狹窄(堵塞)處之 MSCT 影像會明顯受到 partial volume effect 之影響,
血管實際直徑與長度之判定存在有相當的難度。
二、 冠狀動脈具有多分支且其血管走向存在差異:不同個體(病歷)之冠狀動脈 結構均存在明顯差異,難以完全歸納正常冠狀動脈結構之特徵。少有冠狀動 脈結構(包括:血管分支位置、分支走向、血管長度)完全相等的兩個個體,
而此較難應用學習機之演算法(machine learning)達到完整分割冠狀動脈結 構的目標。
三、 冠狀動脈具有曲折變化之特性:確保心肌能維持正常循環,冠狀動脈分布在 心臟內外各處。冠狀動脈包覆在心臟表面,並隨著心臟結構之弧度對應改變 其曲折度,血管亦有可能出現劇烈的轉折。此一特性使得主動式輪廓模型 (active contour model) 或是漸進式搜尋的演算法難以偵測血管曲率變化或是 大幅度的血管方向改變。圖 1.10(A)即為一處因血管明顯轉折,使得部份
血管未能出現在同一平面上之案例。
四、 冠狀動脈邊緣與其他相鄰組織之灰階值過於相似:在影像解析度有限的狀態 下,冠狀動脈血管會與附近的心房、心室空間發生相連或緊鄰的情形如圖 1.10
(B)。此特性使得一般的血管結構分割的演算法在分辨血管分支與相鄰組織 時容易發生誤判。
五、 施打顯影劑:在進行電腦斷層掃描前,受測者會施打適當類型的顯影劑,以 加強血管結構與其他組織的對比度。但由於 MSCT 造影成像之掃描時取樣時 間需人工設定,考量顯影劑會隨著血液進入循環且病患身體循環狀況存在差 異,可能導致血管內亮度不均。可能產生顯影劑尚未流入部份血管(過早取 樣影像)或顯影劑已離開冠狀動脈(過晚取樣影像)之情況。
六、 電腦斷層掃描的 artifacts:在心臟的收縮過程中,冠狀動脈也會不斷的改變位 置。在心室充滿血液的情況下,能觀測到最完整之冠狀動脈結構。因此 MSCT 造影成像需考量 ECG-gating 方能取得完整的心臟影像。隨著心臟的收縮,週 期性的 ECG 訊號難免存在著些微差異。因此,若同一冠狀動脈血管分支之造 影成像參考了兩個不同週期的取樣影像,其影像交界處很可能會產生雜訊,
造成血管分割時的困難。
圖 1.10 電腦斷層掃描影像(3)。(A)部份血管因彎曲程度過大,導致無法於同 一平面顯示完整血管,(B)冠狀動脈與其他灰階值相近之組織相連的例子。
1.3.3 本研究之目的與利基
綜上,本研究的目的在於發展一套全自動的主動脈與冠狀動脈分割演算法達 到準確分割冠狀動脈結構之目的。希望此一全自動的設計能加速整個電腦輔助診 斷的流程與速度,直接輸出具臨床意義之分析數據供醫護人員與一般民眾作為參 考。並配合政府提供之雲端電子病歷服務與健康存摺等服務,對病患個人之健康 資訊提供加值應用。
1.4 文獻探討 1.4.1 血管分割演算法
本節主要就冠狀動脈結構分割的相關文獻作探討,並會對照本實驗室團隊歷 年的來研究加以說明。
血管分割是一門已經被廣泛研究的技術,建立準確之血管分割方法對於血管 視覺化相當重要。配合臨床上各種不同的造影工具的使用 (包含核磁共振影像、X 光血管攝影、電腦斷層掃描等),已有多種不同的血管分割技術被先後的提出以解 決臨床的需求(如腦血管、冠狀動脈等)。Kirbas and Quek 歸納了常見之血管結構 分割方法,其中較常見的分割方法可分為下列四類 [15]:
一、 圖形辨識 (Pattern recognition techniques)
圖形識別的方式在用於追蹤血管的方式相當直觀,但容易受背景資訊影響。
例如 Hennemuth 之研究 [16],分別透過二維與三維之區域成長演算法(region growing)尋找恰當之血管起點(seed point)後進行血管分割。但僅考慮影像 灰階值之演算法,往往會受到 partial volume effect 極大的影響,進而導致於 血管分支、血管狹窄、血管末梢等位置形成錯誤的分割結果。儘管 Mueller 等人試圖加入影像前處理(gray-scale morphological operators)來優化演算法,
但效果仍然相當有限 [17]。
二、 血管模型 (Model-based approaches)
Fotin 曾以單位圓柱作為漸進式搜尋冠狀動脈的基本幾何模型,並以 template matching 的方式試圖找出最佳的行進方向 [18]。但仍會受到背景訊息之影響,
且血管結構(尤其是分支處)亦難以透過基本幾何模型完整描述。
三、 血管追蹤 (Tracking-based approaches)
此類演算法被廣泛運用,且血管追蹤過程中往往能同時估計血管中心線之位 置 [19]。但多數追蹤血管中心線的方法仍需先以手動的方式來取得血管起點 與終點,十分耗費人力資源與時間,且人工介入極可能會影響分割結果。此 外,此方法在處理較細微血管分支時,亦無法發揮其優勢。
四、 管狀結構偵測(Tube-like object detection approaches)
此方法考量影像空間中每一像素(voxel),並評估該位置是否屬於血管(管 狀結構)之一部分 [20][21]。雖然利用三維管狀結構(Frangi’s filter)之特徵 值與特徵向量等資訊來取代原先利用灰階值來找血管的方法可得到不錯的成 果,但由於Frangi’s filter 運算量龐大且在血管分支處的資訊較為凌亂,因此 仍有其使用上之限制。
此 外 , 亦有 人 使用 運用 等 位 函數 ( Level set ) 的 方 法、 人 工智慧 ( Artificial Intelligence-based approaches)或類神經網路(Neural Network-based approaches)等 研究方法來進行血管之分割。綜觀以上方法後可發現,無論是單用哪類的方法都 有其優缺點和限制。
1.4.2 冠狀動脈起點偵測
冠狀動脈結構分割係利用§1.4.1 所述之演算法將血管片段匯集成一完整冠狀 動脈系統。依據使用者手動介入程度不同,可以分為「全自動分割」、「半自動分 割」、「介入式分割」三種模式。三種模式之最大差異在於是否由使用者手動給定 冠狀動脈起點、血管末梢點與其他控制點之位置,讓系統參考相關資訊後自行分 割出完整冠狀動脈結構。
在本研究團隊早期研究中 [22][23][24][25],便以全自動之冠狀動脈結構分割 為目標,並開發出 2 種偵測冠狀動脈起點(ostium)的方法。由於冠狀動脈是依附 在升主動脈的血管結構,因此在自動偵測冠狀動脈起點前須先對主動脈之位置與 形狀有良好的定義。首先,我們透過讀取與分析 MSCT 影像的第一張(位於心臟 上方),利用 Hough’s transform 偵測該影像中最顯著的圓形結構。依據心臟之解剖 生理學,此一位於心臟上方之圓形結構可能為升主動脈、降主動脈、肺靜脈或肺 動脈,需要加入額外的驗證程序方能確認該結構是否為升主動脈。確認升主動脈
位置後,再對該圓形輪廓進行形變計算,使其輪廓得以貼近實際之升主動脈空間。
在確認升主動脈位置與輪廓後,方執行偵測冠狀動脈起點之演算法:
一、 參考灰階值資訊偵測冠狀動脈起點:
此方法中,我們依據首張影像之升主動脈輪廓沿著升主動脈朝心室方向進行 掃描(screening),並偵測與紀錄每張影像中升主動脈輪廓的形變。由於冠狀 動脈出現的位置會在影像輪廓上造成極大的變化,因此我們假定在掃描過程 中,影像輪廓與其對應之面積產生一定程度變化時,該層影像即為冠狀動脈 出現之位置。圖 1.11(A)即為包含升主動脈與冠狀動脈之影像,經型態運 算子處理後,可得到去除冠狀動脈之升主動脈輪廓如圖 1.11(B)。將圖 1.11 之 2 個圖形相減後,可得到一段冠狀動脈血管,並取其前段血管之中心點位 置作為血管之起點。惟此一方法對雜訊有較弱的抵抗能力,在升主動脈輪廓 與臨近結構(影像灰階值相近之心房與心室)過於接近時,影像輪廓會露出
(leakage)至其他非冠狀動脈之結構中造成誤判。迄今,此一誤判狀況仍未 能有效解決,仍需仰賴人工介入將錯誤的分割結果另行排除。
圖 1.11 電腦斷層掃描影像(4)。(A)升主動脈與冠狀動脈之輪廓(B)以型態 運算子排除冠狀動脈後之升主動脈輪廓。
二、 參考管狀結構特徵值資訊偵測冠狀動脈起點:
另一方法即為參考管狀結構特徵值(Frangi’s value)來輔助判斷冠中動脈位 置。利用升主動脈之輪廓,並以較大的型態運算子排除掉冠狀動脈之變化,
如圖 1.11(B)。由於冠狀動脈起點為連結升主動脈最主要的管狀結構,因此 我們搜尋升主動脈輪廓周邊具有最大管狀結構特徵值之位置,並將之定義為 冠狀動脈起點。此一方法雖然可合理定義冠狀動脈之起點,但其前處理
(Frangi’s filter)之運算量過於龐大,且升主動脈之圓弧輪廓有時亦會因周邊 雜訊而產生偏高的最大管狀結構特徵值反應,影響主動脈起點之判斷。雖然 利用管狀結構特徵來偵測冠狀動脈起點的方式較少發生誤判情形,但此類誤 判情形仍需靠人工介入加以排除。
藉由上述兩種方法,估計冠狀動脈之起點資訊並提供後續血管分割演算法,便可 達到全自動之分割結果。
1.4.3 冠狀動脈之血管中心線萃取與血管邊緣分割
冠狀動脈之血管中心線與血管邊緣萃取已經被相當廣泛的研究。自 2004 年 MICCIA 協會(The Medical Image Computing and Computer Assisted Intervention Society)成立後,便持續關注電腦輔助診斷於心血管疾病之相關研究 [26]。在電 腦輔助診斷於心血管疾病研究方面領先全球的荷蘭,亦成立了一精研冠狀動脈研 究 相 關 演 算 法 的 研 究 平 台 ( Rotterdam Coronary Artery Algorithm Evaluation Framework) [27]。該平台研究的兩大主題為:
一、 冠狀動脈血管中心線萃取之演算法
二、 冠狀動脈狹窄偵測、斑塊定量與血管邊緣分割之演算法
在 2008 年舉辦之 MICCAI 工作坊中,該研究平台募集了 13 個研究團隊來共 同分享與比較彼此研發的冠狀動脈中心線萃取演算法 [28]。其中 13 個研究團隊又 被細分為 3 個組別:全自動組(5 個團隊)、半自動組(3 個團隊)與互動操作組
(5 個團隊)。在全自動組中,各團隊運用了§1.4.1 中所述及的血管分割演算法,
分別改良了圖形辨識(如 AutoCoronaryTree [29][30],VirtualContrast [31])、血管 模 型 ( 如 CocomoBeach [32] , DepthFirstModelFit [33] )、 血 管 追 蹤 ( 如 GVFTube’n’Linkage [34])之演算法,進而達到冠狀動脈中心線之萃取。在半自動
組中,各團隊運用類神經網路(如 AxialSymmetry [35],KnowledgeBasedMinPath [36])
與人工智慧(如 CoronaryTreeMorphoRec[42])等方法,透過成本函數(cost function)
計算冠狀動脈端點(起點到終點)間最佳路徑。在互動操作組中,則多屬於管狀 結構偵測之方式(如 3DInteractiveTrack [37],ElasticModel [38],MHT [39])、血管 追蹤之方式(如 Tracer [40])與類神經網路之方式(如 TwoPointMinCost [41])。根 據這些研究成果可發現,已有許多研究團隊開始混合多種以上之影像分割方法來 分析冠狀動脈結構,特徵值、特徵向量(Eigen-system)與海森函數(Hessian matrix)
等管狀結構偵測技術亦已被實作在協助血管追蹤之演算法中。
在此一冠狀動脈中心線萃取之競賽中,脫穎而出的演算法為 Friman 等人所發 展的 MHT(評比結果如圖 1.13)。此一演算法透過萊文貝格-馬夸特方法(Levenberg - Marquardt algorithm)尋找非線性最小平方法之最佳數值解,用以偵測管狀結構 之特徵(大小與方向)有顯著之成效。雖然此一方法需要利用手動介入(設定冠 狀動脈之起點),但其優異的冠狀動脈中心線萃取技術亦受本研究團隊青睞,此方 法亦被本研究團隊使用為主要之冠狀動脈中心線萃取演算法。
圖 1.12 依不同平面顯示冠狀動脈起點(如箭頭處),右下為冠狀動脈之三維結構 示意圖 [28]。
圖 1.13 冠狀動脈中心線萃取演算法評比結果 [28]。
在冠狀動脈狹窄偵測、斑塊定量與血管邊緣分割之演算法方面,在 2012 年舉 辦之 MICCAI 工作坊中,該研究平台募集了 11 個研究團隊來共同分享與比較彼此 研發的演算法 [42]。此研究中嚴謹的訂定了血管狹窄偵測與血管管腔空間分割之 評分標準,惟各研究團隊在各項評比中各擅勝場,並無相較之下較為突出之研究 方法。圖 1.14 為其中 5 種演算法之血管管腔空間分割結果與臨床醫師分割結果之 比較,在排除了鈣化斑塊之空間的情況下,血管管腔空間蜿蜒的程度較為明顯。
此研究之結論指出,多數演算法雖然可靈敏的偵測血管狹窄位置,但是目前血管 邊緣之描述之技術已有機會能達到近似臨床醫師手動分割般的準確程度。
本研究團隊將持續參考國際上之研究趨勢並不斷精進自身研發能量,參考前 人之研發成果精進冠狀動脈分割演算法,並對電腦輔助診斷於心血管疾病做出更 完美的演繹。
圖 1.14 冠狀動脈血管管腔分割結果(臨床醫師與 5 種演算法之結果比較) [42]
1.4.4 血管特徵分析
由§1.4.3 可發現,電腦輔助診斷於心血管疾病之研究並非僅止於找出主動脈、
冠狀動脈起點與冠狀動脈結構即可,血管特徵之描述也是此類研究中重要的環節。
因此我們回顧許多有關心血管疾病之臨床文獻,試圖找中具有臨床意義的參數,
並將該參數體現於我們的演算法當中。
由組織解剖學可知血管為多層結構,其最內層為血管之內皮細胞,動脈粥狀 硬化為血管內皮下堆積脂肪與膽固醇之過程。囿於 MSCT 影像之解析度有限,無 法呈現小於 1 個像素(約為長寬高都是 0.6 mm 的立方體)之構造,故 MSCT 影像 中多半僅能呈現血管/非血管之空間分佈,難以直接看到血管壁之結構,亦難以 偵測血管壁中的變化。考量血管壁實際存在之空間位置,亦有助於探討斑塊堆積 之進程。參考 Dey 等人於 2009 年的研究,我們可在 MSCT 影像中利用灰階值之區 間來定義心臟表皮脂肪(epicardial fat, EF)、非鈣化斑塊(non-calcified plaque, NCP)、
血管管腔(lumen)與鈣化斑塊(calcified plaque, CP)(如圖 1.15) [43]。圖 1.16 中針對一段含有混合型斑塊(同時存在鈣化斑塊與非鈣化斑塊)進行三種不同軸 向的顯示,並依其灰階值分佈之不同,區分出鈣化斑塊與非鈣化斑塊之分佈位置 與輪廓。
參考動脈粥狀硬化嚴重度分析之臨床研究並考量能在 MSCT 中實做之參數 [44][45][46][47][48][49][50],若要評估一段有狹窄問題的血管,我們可就下列參數 進行探討:
圖 1.15 冠狀動脈縱向切面之灰階值特徵(上)與灰階值對應表(下) [43]
一、 與體積有關之參數:
(一) 鈣化斑塊體積
(二) 非鈣化斑塊體積(含低亮度斑塊體積、中等亮度斑塊體積)
(三) 斑塊總體積
(四) 血管管腔體積
二、 與面積有關之參數(假定 1 段血管中共有 n 張切面):
(一) n 個血管切面面積(含斑塊)
(二) n 個斑塊面積(鈣化斑塊與非鈣化斑塊分開計算)
(三) n 個血管形變比例(血管切面面積/血管切面面積平均值)
(四) 1 個血管切面面積平均值
(五) 1 個最大血管管腔面積
(六) 1 個最小血管管腔面積
圖 1.16 透過 3 種不同視角觀測同一混合型斑塊,(A)原始影像(B)將不同灰階 值分佈之斑塊標上顏色(黃色:鈣化斑塊;紅色:非鈣化斑塊)(C)斑塊輪廓 [43]
三、 與斑塊有關之參數:
(一) 斑塊延伸長度
(二) 相對於血管中心,斑塊佔據血管管壁之比例
(三) 相對於血管中心,斑塊最厚處之位置
1.4.5 關於本研究
為達電腦輔助診斷於粥狀動脈硬化之目的及冠狀動脈分割之完整性,本研究 摒棄既有之冠狀動脈起點偵測演算法。重新以升主動脈之結構為基準並考量冠狀 動脈起點與三尖瓣之關聯,發展出更準確且抗雜訊之冠狀動脈起點偵測演算法。
延續實驗室於血管結構分割之卓著成果,我們以影像灰階值、Frangi’s filter 等參考 資訊分割出冠狀動脈結構,依據 MHT 之血管中心線萃取演算法來歸納並建構後續 血管特徵分析評估平台,最後帶入§1.4.3 之動脈粥狀硬化評估參數分析病情嚴重程 度。相關詳細方法將會於第二章描述。
1.5 論文架構
本論文架構共分為五章:
第一章「緒論」:
詳細介紹本研究的重要性以及所面臨的困難,並針對冠狀動脈起點偵測、血 管分割與中心線萃取、血管特徵分析等技術提供文獻之探討。
第二章「研究方法與材料」:
建構全面且全自動之冠狀動脈分割演算法,並介紹核心技術(升主動脈分割、
冠狀動脈起點偵測、血管分割與中心線萃取)之理論與實作方法。
第三章「研究成果與討論」:
呈現本研究之偵測、分割與評估成果,並作優缺點討論。
第四章「結論」:
思考本研究之未來應用與改良方向。
Chapter 2 研究方法與材料
2.1 研究材料
本研究起緣於台灣大學醫學工程學研究所、台大醫院內科部與台大醫院影像 醫學部之三方合作。由醫工所陳中明教授提供研究技術與人力,內科部王宗道醫 師與影像醫學部李文正醫師挑選罹患動脈粥狀硬化患者的 MSCT 影像。(使用於本 研究之完整影像約 20 組,多數影像由台大醫院之 GE LightSpeed VCT 64 切面電腦 斷層掃描儀所拍攝)。
醫療數位影像傳輸協定檔案(Digital Imaging and Communications in Medicine,
DICOM)為一通用之標準協定,主要應用於醫學影像的處理、儲存、列印與傳輸,
已被廣泛使用於接收與交換醫學影像及病人資料。透過台大醫院之 PACS 系統,取 出每組具臨床代表性之醫學影像的 DICOM 檔案,平均每組胸腔之 MSCT 影像由 將近 200 個 DICOM 檔案所組成。本研究中所使用之 DICOM 檔案為解析度 512*512 之影像檔案(實際大小約 20*20 平方公分)。
相較於電腦斷層掃描儀隨機安裝之商用軟體強調自由度較高之互動式使用者 介面(需要較多人工介入操作),其參數計算功能受限,僅能使用於計算特定參數。
因此,本研究利用 Matlab(版本:2014b, The MathWorks, Inc., Massachusetts, USA)
此一工具來匯入 DICOM 檔案並堆疊出胸腔 MSCT 影像之三維空間,並透過此一 開發平台原有之影像處理函式庫,進行後續影像分割演算法及冠狀動脈狹窄與斑 塊分析方法之設計與實現。
2.2 研究架構
本研究之架構如圖 2.1 所示,共可分為三大主要步驟:升主動脈分割(黃色)、
冠狀動脈結構重建(藍色)與血管特徵分析(綠色)。
為建構完整且全自動之電腦輔助診斷,應用於心血管疾病(動脈粥狀硬化), 我們將循序對升主動脈、冠狀動脈結構之空間進行影像分割,並透過血管中心線 萃取之技術,對血管特徵進行評估與描述。
圖 2.1 本研究之架構
2.3 升主動脈分割
為達到自動化冠狀動脈結構分割之目標,首要任務即為準確的估計冠狀動脈 起點。回顧本研究團隊過去在估計冠狀動脈起點之經驗,造成估計失誤的主因為 升主動脈過於接近周邊結構(通常為肺靜脈與左心室)而造成分割結果錯誤。因 此,對升主動脈準確的描述將有助於減少冠狀動脈起點估計失誤之情形。
升主動脈為主動脈弓(Aortic arch)向下至主動脈瓣(Aorta valve)之血管結 構,由於心臟之 MSCT 影像通常未涵蓋主動脈弓之位置,因此本研究中「升主動 脈空間」定義為 MSCT 首張影像至主動脈瓣之空間。升主動脈之血管壁與主動脈 瓣都是厚度較薄之結構,易受部分容積效應(partial volume effect)所影響造成影 像分割上之困難。拍攝心臟之 MSCT 影像會選在心室充滿血液的時間點上,以利 能觀測到最完整之冠狀動脈結構,此時之主動脈瓣結構恰好近似 3 顆圓球。因此,
我們以此「3 顆球」之結構作為心臟之基準點,加入形態學上的事前訊息(priori information)來對升主動脈進行精準分割。
圖 2.2 主動脈瓣之剖面於(A)血管攝影及(B、C)MSCT 影像,(D、E)中明 顯可見主動脈瓣之「3 顆球」結構 [51]
同時,分割主動脈瓣亦有其重要之臨床價值,特別是針對有關安裝人工瓣膜 之臨床研究 [51]。如圖 2.2 所示,此一「3 顆球」結構可視為心臟中之地標(landmark)。
另一方面,冠狀動脈之起點亦各別位於「3 顆球」當中的 2 顆球上面,冠狀動脈起 點與此「3 顆球」結構之相對關係是否與其他心血管疾病有關聯,亦是未來值得持 續探討之課題。因此,在本研究的第一部份「升主動脈分割」中,我們將旋轉原 始 MSCT 影像的座標軸,重建以「3 顆球」為基準的三維空間進行升主動脈分割 與冠狀動脈起點偵測。
在以「3 顆球」為基準進行座標轉換之前,須先估計此「3 顆球」之中心點(定 義:有一與三顆球相切之平面,取其平面上 3 個切點之中心點。我們將依據首張 影像尋找升主動脈之中心點,另以通過該中心點之矢狀面(sagittal view)與冠狀 面(coronal view)影像進行「3 顆球」中心之估計,並對此一中心點進行反覆迭 代,以期取得最佳之「3 顆球」中心點。
2.3.1 升主動脈於首張 MSCT 影像中的位置
在首張 MSCT 影像中,我們透過 K-mean 群聚演算法來定義升主動脈之灰階 值區間。K-mean 群聚演算法利用群集(clustering)的概念來對資料做分群 [52]。此
A
B C
D E
一演算法之主要目的是依照資料不同的特性來做區分,建立不同的群集以達到分 群的效果。K-mean 群聚演算法需事先指定群集的個數,經由不斷重複的疊代以降 低誤差目標函數之值,當目標函數趨近穩定時,即達到分群的結果。
假設針對某筆資料,欲分為 K 個群集,則 K-mean 群集演算法之流程為:
一、 隨機將資料區分到 K 個群集內,並求出 K 個群集各別的中心點。
二、 針對每筆資料去求其與 K 個群集之中心點的歐式距離(Euclid distance)。
三、 將每筆資料重新分配到距離最近的群集中。
四、 重新計算各個群集的中心點,並重複上述步驟,直到趨於穩定狀態或者狀態 不再改變時,即分群完成。
也就是說,假設有 n 筆資料(𝑥1, 𝑥2, … , 𝑥𝑛)欲分至 K 個群集(K < n),則 K 個群 集的中心點(𝑆1, 𝑆2, … , 𝑆𝑘)須滿足:
𝑎𝑟𝑔 min𝑠∑𝐾𝑖=1∑𝑥𝑗∈𝑆𝑖‖𝑥𝑗− 𝑢𝑖‖2 (公式 2.1)
其中𝑢𝑖為第 i 群中心點𝑆𝑖的平均值,使得每群集平方合(within-cluster sum of squares)
為最小。
首張 MSCT 影像包含升主動脈、降主動脈、肺靜脈、心房、骨骼、空氣、軟 組織以及非掃描區域,分析後可得到類似圖 2.3 之結果。K-mean 群聚演算法將首 張 MSCT 影像分為三個部分:
一、 非掃描區域、肺部內空氣(低灰階值分佈)
二、 軟組織(中等灰階值分佈)
三、 血管和骨骼(高灰階值分佈)
將上述第三類高灰階值像素之影像透過型態運算子加以修飾,保留形態完整之高 亮度結構,並評估這些區塊之面積、形狀與位置,便可在首張 MSCT 影像中取得升 主動脈之輪廓與中心點位置。
圖 2.3 MSCT 首張影像之灰階值分佈,M1、M2、M3 分別代表血液(與骨頭)、
軟組織、空氣之灰階值分佈 [23]
2.3.2 以升主動脈為基準之座標轉換
在以「3 顆球」為基準進行座標轉換之前,須先估計此「3 顆球」之中心點。
依據§2.3.1 所取得之升主動脈中心點,另以通過該中心點之矢狀面(sagittal view)
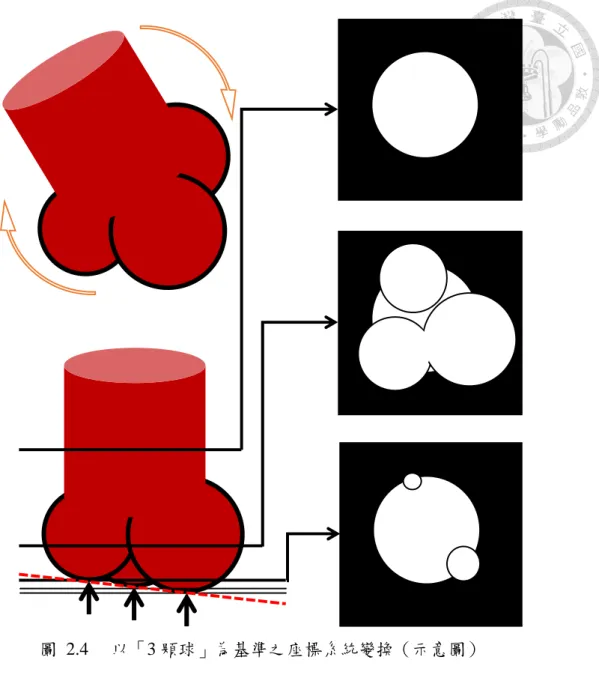
與冠狀面(coronal view)影像粗略估計「3 顆球」之中心與平面法向量。給定中 心點與平面法向量後,可重建新的座標系統如圖 2.4。沿著此一座標系統,可分別 進行「3 顆球」之分割,在座標系統中使用 level-set 演算法分割出每顆球之輪廓並 追蹤每顆球出現與消失的區間。
圖 2.4 以「3 顆球」為基準之座標系統變換(示意圖)
主動輪廓或 snake 形變模型之主要概念為輪廓的進化,透過演算法將輪廓收斂 於影像(𝑢0)中之最佳位置。使Ω為ℝ2之子集,∂Ω為此一子集之輪廓。𝑢0 ∶ Ω̅ → ℝ為給 定之影像,C(𝑠) ∶ [0, 1] → ℝ2 為影像參數。可將主動輪廓或 snake 形變模型之能量 函數定義如下:
J1(𝐶) = 𝛼 ∫ |𝐶′(𝑠)|𝑑𝑠01 + 𝛽 ∫ |𝐶′′(𝑠)|𝑑𝑠01 − 𝜆 ∫ |∇𝑢01 0(𝐶(𝑠))|2𝑑𝑠 (公式 2.2)
其中,α、β、λ為正值參數,此一方程式前兩項控制了輪廓之平滑程度,第三項則 將邊緣往實際影像輪廓拉近。藉由此能量函數之最小化,我們可透過第 3 項邊緣 偵測運算子(edge-detector)來使影像邊緣落在∇𝑢 最大化之位置。
同時,此一邊緣偵測運算子可參考影像中灰階值之梯度變化(gradient of 𝑢0)進行 重新定義,使得:
𝑔(|∇𝑢0(𝑥, 𝑦)|) =1+|∇𝐺 1
𝜎(𝑥,𝑦)∗𝑢0(𝑥,𝑦)|𝑝, 𝑝 ≥ 1 (公式 2.3)
∇𝐺𝜎∗ 𝑢0此項為使用高斯運算子(𝐺𝜎(𝑥, 𝑦) = 𝜎−12𝑒−|𝑥2+𝑦2|4𝜎 )對原始影像進行摺積,
使得此一運算子能在輪廓落在影像邊緣時有快速收斂的效果。同時定義 Lipschitz 函數𝜙(𝑡, 𝑥, 𝑦)來描述輪廓變化𝐶 = {(𝑥, 𝑦)|𝜙(𝑥, 𝑦) = 0},並導入速度參數𝐹如下:
𝜕𝜙
𝜕𝑡 = |∇𝜙|𝐹, 𝜙(𝑡, 𝑥, 𝑦) = 𝜙0(𝑥, 𝑦) (公式 2.4)
𝐹 = 𝑑𝑖𝑣 (∇𝜙(𝑥,𝑦)
|∇𝜙(𝑥,𝑦)|) (公式 2.5)
{
𝜕𝜙
𝜕𝑡 = |∇𝜙|𝑑𝑖𝑣 (∇𝜙(𝑥,𝑦)
|∇𝜙(𝑥,𝑦)|) , 𝑡 ∈ (0, ∞), 𝑥 ∈ ℝ2
𝜙(𝑡, 𝑥, 𝑦) = 𝜙0(𝑥, 𝑦), 𝑥 ∈ ℝ2 (公式 2.6)
據此,Chan 與 Vese 提出了 active contour with edge(level-set)這個方法 [53],
並定義能量函數如下:
𝐸(𝐶, 𝑚1, 𝑚2) = 𝑢 ∗ 𝑙𝑒𝑛𝑔𝑡ℎ(𝐶) + 𝑣 ∗ 𝑎𝑟𝑒𝑎(𝑖𝑛𝑠𝑖𝑑𝑒(𝐶)) + 𝜆1∗ 𝐹1 + 𝜆2∗ 𝐹2
(公式 2.7)
𝐹1 = ∫𝑖𝑛𝑠𝑖𝑑𝑒(𝐶)|𝐼(𝑥, 𝑦) − 𝑚1|2𝑑𝑥 𝑑𝑦 (公式 2.8)
𝐹2 = ∫𝑜𝑢𝑡𝑠𝑖𝑑𝑒(𝐶)|𝐼(𝑥, 𝑦) − 𝑚2|2𝑑𝑥 𝑑𝑦 (公式 2.9)
其中,u, v, λ1, λ2 為常數,length(C)為輪廓長度,area(inside(C))為輪廓內之面 積,m1 為輪廓內之平均灰階值、m2 為輪廓外之平均灰階值。此演算法之目的為 找到能量 E 之最小化,找到能量最小化時的對應輪廓即為最佳輪廓。
又定義一黑維賽德函數(Heaviside function)如下:
𝐻(𝑧) = {1, 𝑧 ≥ 0
0, 𝑧 < 0 , 𝛿(𝑧) =𝑑𝐻𝑑𝑧 (公式 2.10)
𝐴𝑟𝑒𝑎(𝜙 = 0) = ∫ 𝐻(𝜙(𝑥, 𝑦))𝑑𝑥𝑑𝑦Ω (公式 2.11)
𝑙𝑒𝑛𝑔𝑡ℎ(𝜙 = 0)= ∫ 𝛿(𝜙(𝑥, 𝑦)|∇𝜙(𝑥, 𝑦)|)𝑑𝑥𝑑𝑦Ω (公式 2.12)
故公式 2.7 可另改寫為:
𝐸(𝐶, 𝑚1, 𝑚2) = 𝑢 ∗ ∫ 𝛿(𝜙(𝑥, 𝑦)|∇𝜙(𝑥, 𝑦)|)𝑑𝑥𝑑𝑦
Ω
+ 𝑣 ∗ ∫ 𝐻(𝜙(𝑥, 𝑦))𝑑𝑥𝑑𝑦
Ω
+𝜆1∗ ∫ |𝐼(𝑥, 𝑦) − 𝑚1|Ω 2𝐻(𝜙(𝑥, 𝑦))𝑑𝑥 𝑑𝑦
+𝜆2∗ ∫ |𝐼(𝑥, 𝑦) − 𝑚2|Ω 2(1 − 𝐻(𝜙(𝑥, 𝑦))) 𝑑𝑥 𝑑𝑦 (公式 2.13)
其中:
𝑚1 =∫ 𝐼(𝑥,𝑦)Ω 𝐻(𝜙(𝑥,𝑦))𝑑𝑥 𝑑𝑦
∫ 𝐻(𝜙(𝑥,𝑦))𝑑𝑥 𝑑𝑦Ω (公式 2.14)
𝑚2 =∫ 𝐼(𝑥,𝑦)Ω (1−𝐻(𝜙(𝑥,𝑦)))𝑑𝑥 𝑑𝑦
∫ (1−𝐻(𝜙(𝑥,𝑦)))𝑑𝑥 𝑑𝑦Ω (公式 2.15)
將其能量函數𝐸(𝐶, 𝑚1, 𝑚2)導入 Lipschitz 函數後可得:
𝜕𝜙
𝜕𝑡 = 𝛿(𝜙) [𝑢∇ ∙ ∇𝜙
|∇𝜙|− 𝑣 − 𝜆1(𝐼 − 𝑚1) + 𝜆2(𝐼 − 𝑚2)] = 0, 𝑡 ≥ 0
(公式 2.16)
將上式寫為離散形式並移項∆𝑡:
ϕ𝑛+1 = ϕ𝑛+ 𝛿𝜀(𝜙𝑛) [𝑢∇ ∙ ∇𝜙
|∇𝜙|− 𝑣 − 𝜆1(𝐼 − 𝑚1(𝜙𝑛))2+ 𝜆2(𝐼 − 𝑚2(𝜙𝑛))2] ∆𝑡
(公式 2.17)
其中:
𝐾=∇ ∙ ∇𝜙𝑛
|∇𝜙𝑛|= 𝜙𝑥𝑥𝜙𝑦2−2𝜙𝑥𝜙𝑦𝜙𝑥𝑦+𝜙𝑦𝑦𝜙𝑥2
(𝜙𝑥2+𝜙𝑦2) 3 2
(公式 2.18)
綜上,即可利用主動輪廓之分割方法偵測主動脈瓣之輪廓變化。雖然此一演 算法可計算能量函數並同時偵測複數個結構之輪廓,但處理 2 個以上之輪廓時仍 不免有互相競合之情況,進而導致部分輪廓分割正確、部分輪廓分割異常之狀況。
為解決此一相互干擾之問題,本研究將此一「3 顆球」結構視為 3 個單球結構分別 進行主動輪廓之分析。
分割每顆球的輪廓並記錄其接近消失時之座標點(其物理意義為切平面之切 點),以這「3 顆球」之 3 個切點重構切平面,並計算中心點及平面法向量。反覆 更新中心點及平面法向量後,便可得到最佳之「3 顆球」座標系統。依據此一座標 系統,便可重組完整之「3 顆球」結構,亦可將此一結構對應回原始座標系統,於
圖 2.5 早期冠狀動脈起點偵測之成果。以圓形圈選心臟(黃色)與升主動脈(紅 色)範圍,藍色處為自動偵測之左冠狀動脈(left main)起點。
2.3.3 由升主動脈偵測冠狀動脈起點
圖 2.5 為冠狀動脈起點偵測之早期研究成果之一。此一方法追蹤每張 MSCT 影像中之心臟中心點並估計其分佈空間,並藉由霍夫變換(Hough transform)分割 出心臟分佈空間中最大之圓形結構(通常為升主動脈)。由此早期結果可發現於原 始堆疊之影像空間中,雖可用單一圓形結構搭配型態運算子(morphological operator)
來追蹤升主動脈之粗略空間位置,但其實際輪廓卻無法忠實呈現。在無法準確分 割升主動脈輪廓的情況下,亦難對冠狀動脈起點有恰當的描述。惟早期研究中所 運用之區域成長演算法並不需要使用準確的冠狀動脈起點資訊,故此一冠狀動脈 起點偵測不精確之問題並未獲得重視。
相較於直接以堆疊起的心臟 MSCT 影像進行升主動脈輪廓分割與冠狀動脈起 點偵測,座標轉換後之升主動脈結構能以更直覺之方式進行「3 顆球」之圓弧偵測,
而避免周圍雜訊之干擾。冠狀動脈自升主動脈結構延伸出去之走向因人而異且不 易預測,其走向常會導致開口處呈現漏斗狀,造成演算法無法判別此一漏斗結構 是否包含冠狀動脈之起始段(易被判讀為形狀特異之升主動脈橫切面)。以往直接 以堆疊起的心臟 MSCT 影像進行冠狀動脈起點偵測極易受到此一走向之干擾。透 過座標轉換,可明顯減少冠狀動脈走向對冠狀動脈起點偵測之影響。
圖 2.6 實際輪廓與「3 顆球」輪廓之差異(示意圖)
![圖 1.4 104 年兩性十大死因死亡率。 隨著現代化飲食與生活習慣改變,肥胖趨勢的全球化已在過去的 30 年內衍生 了許多醫療問題,包括了心血管疾病的形成與致死率的提升 [8]。根據台灣營養健 康狀況變遷調查(NAHSIT),隨著生活習慣與飲食環境的改變,肥胖趨勢亦有年 輕化的現象。估計投入於過重及肥胖所產生的代謝相關疾病的國家醫療支出已達 3%以上,世界衛生組織歐洲區署亦指出約 6%的健康照護成本與肥胖有關。肥胖更 是導致心血管疾病的高風險因子之一,肥胖趨勢的全球化與年輕化亦導致了罹患 心血管疾](https://thumb-ap.123doks.com/thumbv2/9libinfo/9599600.628681/18.892.149.780.123.546/年兩十大死因死亡隨著現代化飲食與生活所產生險因子之一肥胖趨勢.webp)
![圖 1.5 心臟冠狀動脈與粥狀硬化示意圖 [9]。 發生狹窄或阻塞的起因為冠狀動脈的內皮細胞受損後,膽固醇在其內皮細胞 下堆積造成血管管腔之形變。膽固醇的堆積,使得血管的內皮細胞改變性質,易 發生血小板堆積和平滑肌增生,形成所謂的動脈粥狀硬化 [10]。一般正常的血管 內壁是平滑暢通的,一旦管壁上生成動脈粥狀硬化的腫塊,血管壁會因此變得粗 糙不平且管徑變小、血流不暢順,影響氧氣與養份的供應。動脈粥狀硬化所形成 的斑塊(plaque)在結構上又可分為穩定的斑塊與不穩定的斑塊:穩定的斑塊通常 會造成血管](https://thumb-ap.123doks.com/thumbv2/9libinfo/9599600.628681/19.892.238.788.106.543/心臟冠狀動脈與粥狀硬化示意圖發生狹窄或阻塞的起因為冠狀動脈的.webp)

![圖 1.8 冠狀動脈之結構 [14]。](https://thumb-ap.123doks.com/thumbv2/9libinfo/9599600.628681/23.892.189.766.133.1014/圖18冠狀動脈之結構14.webp)
![圖 1.13 冠狀動脈中心線萃取演算法評比結果 [28]。 在冠狀動脈狹窄偵測、斑塊定量與血管邊緣分割之演算法方面,在 2012 年舉 辦之 MICCAI 工作坊中,該研究平台募集了 11 個研究團隊來共同分享與比較彼此 研發的演算法 [42]。此研究中嚴謹的訂定了血管狹窄偵測與血管管腔空間分割之 評分標準,惟各研究團隊在各項評比中各擅勝場,並無相較之下較為突出之研究 方法。圖 1.14 為其中 5 種演算法之血管管腔空間分割結果與臨床醫師分割結果之 比較,在排除了鈣化斑塊之空間的情況下,血管管腔](https://thumb-ap.123doks.com/thumbv2/9libinfo/9599600.628681/32.892.129.782.131.554/冠狀動脈中心線萃取演算法評比結果在冠狀動脈狹窄偵測斑之空間.webp)
![圖 1.14 冠狀動脈血管管腔分割結果(臨床醫師與 5 種演算法之結果比較) [42]](https://thumb-ap.123doks.com/thumbv2/9libinfo/9599600.628681/33.892.216.785.112.1057/圖114冠狀動脈血管管腔分割結果臨床醫師與5種演算法之結果比.webp)

![圖 2.2 主動脈瓣之剖面於(A)血管攝影及(B、C)MSCT 影像, (D、E)中明 顯可見主動脈瓣之「3 顆球」結構 [51] 同時,分割主動脈瓣亦有其重要之臨床價值,特別是針對有關安裝人工瓣膜 之臨床研究 [51]。如圖 2.2 所示,此一「3 顆球」 結構可視為心臟中之地標 (landmark)。 另一方面,冠狀動脈之起點亦各別位於「3 顆球」當中的 2 顆球上面,冠狀動脈起 點與此「3 顆球」結構之相對關係是否與其他心血管疾病有關聯,亦是未來值得持 續探討之課題。因此,在本研究的第一部份](https://thumb-ap.123doks.com/thumbv2/9libinfo/9599600.628681/39.892.130.784.120.514/主動脈瓣之剖面A血管攝影BCMSCT影像中明顯可見主動脈瓣之顆球同時分.webp)
![圖 2.3 MSCT 首張影像之灰階值分佈,M1、M2、M3 分別代表血液(與骨頭)、 軟組織、空氣之灰階值分佈 [23] 2.3.2 以升主動脈為基準之座標轉換 在以「3 顆球」為基準進行座標轉換之前,須先估計此「3 顆球」之中心點。 依據§2.3.1 所取得之升主動脈中心點,另以通過該中心點之矢狀面(sagittal view) 與冠狀面(coronal view)影像粗略估計「3 顆球」之中心與平面法向量。給定中 心點與平面法向量後,可重建新的座標系統如圖 2.4。沿著此一座標系統,可分](https://thumb-ap.123doks.com/thumbv2/9libinfo/9599600.628681/41.892.168.787.119.819/MSCT首張影像之灰階值分佈M分別代表血液與骨軟組織空氣之重建新.webp)