國立交通大學
應用化學研究所
碩士論文
離子溶液在毛細管電泳中的應用
The applications of ionic liquids
in capillary electrophoresis
研究生:藍敏慈
指導教授:謝有容 博士
離子溶液在毛細管電泳中的應用
The applications of ionic liquids
in capillary electrophoresis
研究生:藍敏慈
Student:Min-Tsu Lan
指導教授:謝有容 博士
Advisor:You-Zung Hsieh
國立交通大學
應用化學研究所
碩士論文
A ThesisSubmitted to Department of Applied Chemistry College of Science
National Chiao Tung University In Partial Fulfillment of the Requirements
For the Degree of Master of Science In
Applied Chemistry June 2008
Hsinchu, Taiwan, Republic of China
離子溶液在毛細管電泳中的應用 研究生:藍敏慈 指導教授:謝有容 博士 國立交通大學應用化學系碩士班 摘 要 離子溶液具有許多優點,如低蒸氣壓、化學性質穩定及熱穩定性好等, 應用於毛細管電泳上可與分析物作用提高分離的效率,為一新穎的材料。 苯二氮平類的藥物具有安眠、鎮定、抗痙攣以及肌肉鬆弛等作用,鑑於國 內濫用的情形日益攀升,目前關於苯二氮平的研究也越來越受到注目。在 本實驗中,將離子溶液的應用區分成兩個研究方向,一個是在當離子溶液 在毛細管電泳中做為添加劑時,其分離效率與機制的探討,一個則是將離 子溶液應用於線上濃縮方法以提高靈敏度,並降低偵測極限。 在第一部分的實驗中,首先利用三種不同陽離子的離子溶液當作修飾劑 比較分離效率,同時也固定陽離子種類比較陰離子的影響,由實驗結果證 實添加離子溶液確實有助於分離的效果的改善,其中陰離子影響程度大於
陽離子,因此我們嘗試只添加陰離子部分的鹽類 LiNTf2、LiPF6以及 LiOTf
測試分析物與陰離子間的作用關係。實驗結果發現在 300 mM LiNTf2條件 下,7 個苯二氮平藥物可在 18 分鐘內完全分離,除此之外,在比較三種不 同陰離子時 TfO- 、PF6 - 、Tf2N - 造成的影響時,Tf2N - 的效果比 PF6 - 與
測陰離子的 chaotropic effect 對分離有助益,當使用作用越強的 chaotropic anion,其分離效率越高。 在第二個實驗中,我們利用兩種離子溶液型態的界面活性劑(C16MIMBr 與 C16MPYB)做陽離子型的微胞,應用於掃掠式線上濃縮法,偵測低濃度 苯二氮平類藥物。實驗中測試了許多掃掠式線上濃縮參數,並將其條件最 佳化,如 pH、甲醇比例、界面活性劑濃度、緩衝溶液的離子強度以及樣品 注射時間等,由這些實驗結果顯示 C16MIMBr 與 C16MPYB 均可提高分離效 率和增加靈敏度,得到 C16MIMBr 的放大倍率為 31~59 倍,C16MPYB 則為 86~165 倍。當使用 C16MPYB 為微胞時,LOD(S/N=3)為 4.68~9.75 ng/mL, 最佳條件應用在經過固相萃取的尿液樣品中,也可成功的去除雜質干擾並 偵測得到七個樣品的訊號,其回收率在 76.6%到 88.3%之間,表示離子溶 液型態的界面活性劑可成功地應用於掃掠式線上濃縮法上。
The applications of ionic liquids in capillary electrophoresis
Student:Min-Tsu Lan Advisor:You-Zung Hsieh*
Department of Applied Chemistry, National Chiao Tung University
Abstract
Ionic liquids are novel materials that have many advantages such as low vapor pressure, chemical and thermal stability. Using ionic liquids in capillary electrophoresis can improve separation efficiency of interest analytes by the interaction between ionic liquids and analytes. Benzodiazepines are prescribed drugs for hypnotics, minor tranquilizers, anticonvulsants and muscle relaxant. The increasing events in abuse of benzodiazepines make these drugs attract more attentions nowadays in Taiwan. In this study, we divided the applications of ionic liquids into two parts. One part is using ionic liquids as the modifier in running buffer to improve separation efficiency, and according to the experimental results we could understand the separation mechanism between modifiers and analytes. The other is the application of ionic liquids in preconcentration method to enhance the sensitivities and achieve lower detection limits.
In the first part, we utilize three different cationic parts of ionic liquids as modifiers to compare the separation efficiency. The influence of anionic parts of ionic liquids was also evaluated. Both of them enhance the separation efficiency. We find out the anionic parts influence the analytical results more than the
LiPF6, and LiOTf, derives the relationship between anions and analytes. After
adding 300 mM LiNTf2, seven benzodiazepines can be completely resolved in
18 min. In addition, the performance of using Tf2N -
which was reported an anion with strong chaotropic effect, is much better than using PF6
-
and TfO- under the same concentration, meaning that the chaotropic effect of anions enhances separation efficiency. We can attribute these results that the more chaotropic anion is, the better resolution we can obtain.
In the second part, we take two cationic surfactants, C16MIMBr and
C16MPYB, which are reguarded as ionic liquids and used for sweeping-MEKC
The optimal separation conditions are rationalized by factors of pH, methanol, surfactant concentration, buffer ionic strength, and injection time. C16MIMBr
and C16MPYB illustrate the development of sensitivities and resolutions.
Sensitivity enhancement displays 31~59-fold improvement for C16MIMBr and
86~165-fold improvement for C16MPYB compared with normal-MEKC mode.
LOD(S/N=3)ranges from 4.68 to 9.75 ng/mL for C16MPYB. After extraction of
the urine with SPE cartridge and analyte with optimal conditions, seven benzodiazepines are able to be identified without interference of impurities; recoveries are between 76.6% and 88.3%. As a result, the sweeping-MEKC can be successfully achieved by these ionic liquid typed surfactants.
謝誌
由衷地感謝老師 謝有容教授在研究所兩年來,實驗上及生活上的指 導、鼓勵及關懷,使我獲益良多並順利完成論文,在此致上最深的謝意。 此外非常感謝口試委員王念夏教授、曾惠芬教授以及莊士卿教授撥冗指 導,給予許多珍貴的意見與建議,讓這份碩士論文更加完整。 特別要感謝秀麗學姊在實驗上的悉心指導與建議,在實驗遇到瓶頸 時,給予協助;而蘭英就像另一個學姊,不吝嗇地分享在實驗上的經驗與 方法,讓我做起實驗來可以事半功倍。還有要感謝冠文學長幫我解決電腦 的問題以及撰寫論文的經驗分享,此外謝謝亦文、滄浩、葉蓁以及志倫和 我一起與實驗奮鬥,還有謝謝艷如與婉君兩位萃取小天使,佩潔和雪怡為 我帶來歡樂,感謝這些實驗室夥伴陪伴我一起度過碩士班的歲月並包容我 的任性,讓我一點都不孤單。 除了實驗室的夥伴,也要感謝其他在這段期間給予我幫助的學長姐與 同學,謝謝沈經緯學長教我合成,小 p、小可與阿琨,在我合成離子溶液後, 協助我純化與測 NMR 定性,以及在實驗上給我建議的慧茹,常常陪我面對 低潮的盈眞與彥君,還有英子、kitty、育琳學姊、欣穎、鈺君、巧瑩等好友, 在實驗室之外,有你們這些好朋友陪著,更為我的碩士生涯增添不少色彩。 最後感謝我的家人在背後無條件的支持我讓我可以安心完成這篇論 文,並感謝國家科學委員會的計畫 NSC 95-2113-M-009-033-MY3 經費資助。目錄
頁次 中文摘要...Ⅰ 英文摘要...Ⅲ 謝誌...Ⅴ 目錄...Ⅵ 圖目錄...Ⅸ 表目錄... ...XI 一、離子溶液...1 1.1 簡介 ...1 1.2 性質 ...1 1.3 離子溶液在分析化學上的應用 ... 2 1.3.1 在萃取上的應用 ...2 1.3.2 在氣相層析上的應用 ...3 1.3.3 在液相層析上的應用 ...3 1.3.4 在毛細管電泳上的應用 ... 4 二、Hofmeister series...10 2.1 簡介 ...10 2.2 相關名詞介紹 ... 10 2.2.1 水籠 ... 102.2.2 kosmotrope and chaotrope ... 11
2.2.3 鹽溶與鹽析... 11 2.3 應用 ...12 三、毛細管電泳... 14 3.1 簡介 ...14 3.2 分離原理 ... 14 3.3 掃掠式線上濃縮簡介...15 3.3.1 陰離子界面活性劑掃掠式線上濃縮...16 3.3.2 陽離子界面活性劑掃掠式線上濃縮...16 3.3.3 中性界面活性劑掃掠式線上濃縮...17 3.3.4 掃掠式線上濃縮公式 ... 17 四、苯二氮平類藥物 ...22 4.1 引言 ...22 4.2 藥理學 ...22
4.3 臨床表現 ... 22 4.4 檢測技術回顧 ... 23 4.5 毛細管電泳應用在苯二氮平類藥物的分析...24 五、利用離子溶液輔助分離七種苯二氮平類藥物以及作用機制的探討 ....25 5.1 簡介 ...25 5.2 儀器裝置 ... 25 5.3 試藥 ...25 5.4 實驗方法 ... 26 5.4.1 新的毛細管調態 ...26 5.4.2 實驗前後毛細管處理及樣品注入與分離條件 ... 27 5.4.3 苯二氮平標準溶液配製 ... 27 5.4.4 離子溶液合成方式 ...27 5.4.5 添加不同比例的離子溶液 ... 28 5.4.6 添加不同陰離子的鹽類 ... 28 5.5 結果與討論 ... 29 5.5.1 添加離子溶液...29 5.5.2 添加陰離子鹽類 ...31 5.6 結論 ...33 六、離子溶液型態的界面活性劑應用於掃掠式線上濃縮... 47 6.1 簡介 ...47 6.2 儀器裝置 ... 47 6.3 試藥 ...48 6.4 固相萃取 ... 48 6.5 實驗方法 ... 48 6.5.1 新的毛細管調態 ...48 6.5.2 實驗前後毛細管處理 ... 49 6.5.3 苯二氮平標準溶液配製 ... 49 6.5.4 離子溶液合成方式 ...49 6.5.5 不同濃縮分離條件之測試 ... 50 6.5.6 真實樣品的應用 ...52 6.6 結果與討論 ... 53 6.6.1 不同 pH 之影響 ...53 6.6.2 不同比例的甲醇之影響 ... 53 6.6.3 不同界面活性劑濃度之影響 ... 53 6.6.4 不同離子強度緩衝溶液之影響...54 6.6.5 樣品區帶不同離子強度之影響...55 6.6.6 樣品注射時間...55
6.6.8 再現性分析及定量校正曲線 ... 56
6.6.9 尿液樣品之偵測與回收率 ... 57
6.7 結論 ...58
七、結論...79
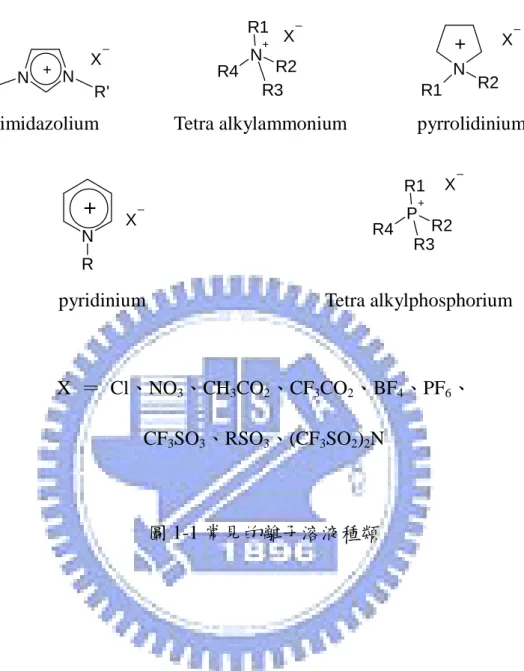
圖目錄
頁次 圖 1-1 常見的離子溶液種類...8 圖 1-2 離子溶液在毛細管中的作用機制...9 圖 2-1 水籠...13 圖 3-1 陰離子界面活性劑掃掠式線上濃縮示意圖...19 圖 3-2 陽離子界面活性劑掃掠式線上濃縮示意圖...20 圖 3-3 中性界面活性劑掃掠式線上濃縮示意圖...21 圖 5-1 苯二氮平類藥物結構式及 pKa...34 圖 5-2 離子溶液的結構式以及縮寫...35 圖 5-3 在緩衝溶液中不同[C2OHmim][Cl]比例對分離效果的影響...36 圖 5-4 在緩衝溶液中不同[EMIM][Cl]比例對分離效果的影響...37 圖 5-5 在緩衝溶液中不同[BMIM][Cl]比例對分離效果的影響...38 圖 5-6 在緩衝溶液中不同種類陽離子的離子溶液對分離效果的比較...39 圖 5-7 在緩衝溶液中不同[BMIM][PF6]比例對分離效果的影響...40 圖 5-8 在緩衝溶液中不同[BMIM][NTf2]比例對分離效果的影響...41 圖 5-9 在緩衝溶液中不同種類陰離子的離子溶液對分離效果的比較...42 圖 5-10 在緩衝溶液中不同濃度的 LiPF6對分離效果的影響...43 圖 5-11 在緩衝溶液中不同濃度的 LiNTf2對分離效果的影響...44 圖 5-12 在緩衝溶液中不同濃度的 LiOTf 對分離效果的影響...45 圖 5-13 在緩衝溶液中不同種類陰離子鹽類對分離效果的比較...46 圖 6-1 離子溶液型態的界面活性劑結構式...59 圖 6-2 使用 C16MIMBr 時不同緩衝溶液 pH 值對濃縮效果的影響...60 圖 6-3 使用 C16MPYB 時不同緩衝溶液 pH 值對濃縮效果的影響...61 圖 6-4 使用 C16MIMBr 時緩衝溶液中不同比例的甲醇含量對濃縮效果的影 響...62 圖 6-5 使用 C16MPYB 時緩衝溶液中不同比例的甲醇含量對濃縮效果的影 響...63 圖 6-6 緩衝溶液中不同濃度的 C16MIMBr 對濃縮效果的影響...64圖 6-8 使用 C16MIMBr 時不同離子強度的背景緩衝溶液對濃縮效果的影 響...66 圖 6-9 使用 C16MPYB 時不同離子強度的背景緩衝溶液對濃縮效果的影 響...67 圖 6-10 使用 C16MIMBr 時樣品區帶不同離子強度對濃縮效果的影響...68 圖 6-11 使用 C16MPYB 時樣品區帶不同離子強度對濃縮效果的影響...69 圖 6-12 使用 C16MIMBr 進行掃掠式線上濃縮時,注射時間對訊號高度的折 線圖...70 圖 6-13 使用 C16MPYB 進行掃掠式線上濃縮時,注射時間對訊號高度的折 線圖...71 圖 6-14 在 MEKC 模式與掃掠式線上濃縮模式使用 C16MIMBr 的比較...72 圖 6-15 在 MEKC 模式與掃掠式線上濃縮模式使用 C16MPYB 的比較...73 圖 6-16 尿液樣品未經過固相萃取管去除雜質的電泳圖...74 圖 6-17 尿液樣品經過固相萃取管去除雜質的電泳圖...75
表目錄
頁次表 6-1 掃掠式線上濃縮之檢量線的相關數據以及 LOD...76 表 6-2 掃掠式線上濃縮訊號的時間、高度與面積的再現性………...77 表 6-3 固相萃取管回收率再現性...78
一、離子溶液 1.1 簡介 在現今環保意識抬頭下,綠色化學漸漸開始受到科學家們的青睞,離 子溶液便是其中之一,過去幾年內更是蓬勃發展,並應用於各種領域中[1]。 所謂離子溶液,指由陽離子與陰離子組成的熔融鹽類,類似於氯化鈉等的 無機金屬鹽類,但最大的不同點在於離子溶液的陽離子為有機離子,具有 低熔點的特性,一般定義熔點低於 100℃ [1]。組成的離子種類並無特別的 限制,端看使用的需求[2],故離子溶液的種類繁多,通常是由含氮的陽離 子,如咪唑(imidazole)、吡咯啶(pyrrolidine)等,與多種陰離子組成,如 Cl–、PF6 – 、BF6 – 、(CF3SO2)2N – 、CH3CO2 – 等,目前最常見到的是室溫下的離 子溶液(Room-temperatue ionic liquid, RTIL),它的熔點低於室溫[1],在室 溫下是液態,易於操作,故目前大多的研究都是以這類型的離子溶液為主。 常見的離子溶液組成離子如圖 1-1 所示。 1.2 性質 構成離子溶液的陰陽離子決定離子溶液的性質[2-4],因此我們可以依 據實驗的需求,挑選離子的種類再進一步合成離子溶液,使得離子溶液的 應用性大幅提升,因此離子溶液又被稱為「可被設計合成的溶劑(designer solvent)」;除此之外,離子溶液還有以下特性:[3,4] 1. 低蒸氣壓 2. 熔點低 3. 化學性質穩定及熱穩定性好 4. 不易燃 5. 高導電性及高電容 6. 熱傳導好
7. 電化學適用電位範圍大(wide electrochemical potential window)
以綠色化學的觀點,離子溶液的優勢就是具有非常低的蒸氣壓,不易 產生有機揮發物,而不易燃的特性也增加了安全性。部分研究指出可用離
子溶液作萃取的溶劑並可以再回收利用,或是把反應物溶於離子溶液中可 以加速反應時間以節省能源[3]。 離子溶液的化學性質與物理性質,取決於組成的離子種類。以溶解度 來說,當陰離子水溶性 Cl- >PF6 - >Tf2N - ,則相同陽離子下,離子溶液的 水溶性依序為 Cl- >PF6 - >Tf2N - ;相較於傳統的有機溶劑,離子溶液因陰 陽離子構造的不同可與分析物產生許多種作用力(solvation power),例如 氫鍵、分散力(dispersion force)、π 電子間的作用力等,故離子溶液對許多 物質都有良好的溶解度,此外由於具有低蒸氣壓的優點,減少吸入的危險, 因此離子溶液很適合用作溶劑。已有文獻提出用 Abraham 對溶解度的解釋 模型來對離子溶液的溶劑特性做完整的解釋[5]。離子溶液的種類繁多,除 了良好的溶解效果受到注目外,其它性質如黏度、密度、親疏水性等等也 有相關的研究 1.3 離子溶液在分析化學上的應用 在上一節中,提到離子溶液的眾多優點,目前也廣泛應用於分析化學 的領域上,如萃取、氣相層析、液相層析、毛細管電泳等[3,4,6,7],以下分 別就各個領域的應用作介紹。 1.3.1 在萃取上的應用 離子溶液的一個特點就是依照需求,可自行合成出想要的性質,在萃 取上此項特性有極大的利用價值;舉例來說,當陽離子為咪唑類離子,離 子溶液的親疏水性藉由改變陰離子種類即可。此外相較於傳統的有機溶 劑,離子溶液對許多物種都有良好的溶解度,因此非常適合當作萃取的溶 劑。 在應用方面,離子溶液可以用於金屬離子的萃取,舉例來說,含特定 分子的離子溶液可以跟金屬離子 Hg2+ 與 Cd2+ 形成錯合物,因此可由水中萃 取出這兩種金屬離子[8];此外利用與冠醚(Dicyclohexyl-18-crown-6)不互 溶的離子溶液,Sr2+ 對離子溶液有比較大的分配係數,所以可以成功的由冠 醚中萃取出此金屬離子[9];在固相微萃取的應用上,特定離子溶液
1.3.2 在氣相層析上的應用 離子溶液的低揮發性與良好的熱穩定度,使其可在氣相層析的靜相上 做變化,在此大致把離子溶液在靜相上的應用分為三部分: 1.離子溶液用於靜相塗佈 2.利用離子溶液交聯作為靜相 3.製作具有掌性的靜相 離子溶液在氣相層析上最早的應用為靜相的塗佈,但是實驗結果效率 不佳且只適用於極性的化合物,直到後來咪唑類的離子溶液出現,在氣相 層析上的應用得以延伸。在 1999 年 D. W. Armstrong 在管柱上塗佈離子溶 液,使分離效率改善,不論分析物是極性或是非極性,管柱都可對分析物 產生選擇性[11];此外為了提高使用時的溫度,Armstrong 等人在 2003 年改 變了陽離子上的官能基以提高使用溫度,都證實了離子溶液可成功地應用 在靜相的塗佈[12]。 氣相層析最重要的一個參數就是溫度,但以上的研究使用溫度都有其 上限,因此在 2005 年有研究讓離子溶液像高分子般在分析管柱內行交聯反 應,得到的靜相到 335℃才會開始裂解,此外不論是利用塗佈方式或交聯的 方式,得到的靜相不會受限於分析物的極性,均有不錯的選擇性[13]。 離子溶液良好的溶解力更是增加了它的實用性,將具有掌性的環糊精 溶於離子溶液中,再進一步塗佈於管柱上[14],或是直接選擇性合成具有掌 性的離子溶液,做為氣相層析的靜相[15],如此一來得到的管柱便可應用於 分析掌性化合物。 1.3.3 在液相層析上的應用 在液相層析中,離子溶液根據不同的使用方式會有不同的功效;譬如 離子溶液在動相中佔有比例不同,影響也不同。當動相含有少量的離子溶 液,此時離子溶液就相當於一般的熔融鹽類,陰陽離子各自對液相層析有 影響,以逆相層析分析帶正電的化合物為例,離子溶液的陽離子比分析物 更容易吸附在管壁上[16],此外由實驗可以發現使用離子溶液作添加劑會改 善訊號形狀與拖尾[17],推測是因為陰離子會與分析物形成離子對,造成分
配係數的改變及減少靜電吸引力,所以當添加少量的離子溶液在動相時, 分析效果也會依添加不同種類的離子溶液而有差異。 當離子溶液比例提高,取代動相中的有機溶劑,這時就會與離子溶液 本身的溶劑性質相關,以 Waichigo 在 2006 年的研究為例[18],添加 20%(v/v) 的離子溶液與相同比例的甲醇相比,訊號順序沒有差異但加入離子溶液的 條件下計算得到的理論板數較高,表示分析效率較好,但這種使用方式較 少見,因為它的成本較高。 至於在靜相方面,離子溶液可與管壁上的矽利用離子交換的方式形成 鍵結,此管柱最多可以同時分離 11 種陰離子[19]。就應用性來說,提到的 三種方式還是以添加少量的離子溶液輔助分離最常見。 1.3.4 在毛細管電泳上的應用 截至目前為止,已有多篇文獻介紹離子溶液與毛細管電泳(CE)相關 的研究,利用 CE,我們可以分離偵測在合成離子溶液時的不純物[20],除 此之外,藉由 CE 得到的參數值可以反推計算得到離子溶液的物理性質與化 學性質,如黏度[21];不過在 CE 的偵測上,離子溶液最常見的應用為輔助 CE 分析樣品,大致上可歸因於幾種離子溶液的特性[22]: 1.易與分析物有額外的作用力,尤其以芳香族化合物最常見 2.可吸附於毛細管管壁上造成電滲流改變,可視為是一種動態的管壁塗佈 3.緩衝溶液添加離子溶液會使整體導電度、離子強度、電泳淌度等改變 4.某些特定的離子溶液因為具有微胞性質可形成微胞幫助分離 由上述的歸納結論可知,離子溶液在毛細管電泳上的應用廣泛,依據 離子溶液在毛細管電泳上的使用方式,分類舉例如下: 1.3.4.1 離子溶液作為背景緩衝溶液 將離子溶液直接稀釋後作為背景緩衝溶液,此時離子溶液會有動態塗 佈管壁的效用,通常會使電滲流反向;以水稀釋的離子溶液作為背景緩衝 溶液,離子溶液中的陽離子會吸附於管壁上,使電滲流反向,而分析物會
因,一是吸附在管壁上與緩衝溶液中的陽離子會使分析物速度減緩,另一 個則是分析物與陽離子會有作用力,如氫鍵、偶極偶極力或偶極誘導偶極 力;有文獻利用計算分析物與離子溶液的結合常數(binding constant),來 證實離子溶液(1-ethyl-3-methylimidazolium tetrafluoroborate, [EMIM][BF4])
與兒茶素(catechin)之間的作用力為偶極偶極力或偶極誘導偶極力[23]。 此外除了單純以離子溶液做為緩衝溶液,也有研究配合其他的修飾劑 對分析物作分離。2004 年 Qi 等人以離子溶液(1-butyl-3-methylimidazolium tetrafluoroborate, [BMIM][BF4])作為緩衝溶液配合β-CD 分離中藥中的蒽醌 (anthraquinone),在這篇研究中,利用分析物會因為大小不同而鑲嵌在 β-CD 的程度不一,造成和咪唑類陽離子的作用力有強弱區別而有分離效 果,換句話說,分析物所受到的作用力是由β-CD 與離子溶液競爭而來[24]。 當離子溶液的緩衝溶液用於非水相的電泳中,電滲流並不會像在水相 電泳中一樣會反向,在 M. Vaher 等人的研究指出,離子溶液與分析物之間 的作用才是分析物分離的關鍵,不論是在分析酚類(phenol)或芳香酸 (aromatic acid)[25]還是多酚類(polyphenol)[26],離子溶液陰離子的部 分也會影響到分析物的淌度。 1.3.4.2 離子溶液作為添加劑 截至目前為止,以離子溶液當添加劑的應用最為廣泛,舉例來說,M.-E Yue 利用添加離子溶液至硼酸緩衝溶液中,分離類黃酮(flavonoid),在實 驗中,添加了離子溶液後,分析時間縮短且解析度攀升,此外作者為了瞭 解分析物與離子溶液之間的作用,在經過改變陽離子上的碳鏈長度、碳鏈 形狀以及研究雜環上氫原子功用,推測是在第二個碳上的氫會與類黃酮上 的氧形成氫鍵,使分析物解析度提升[27]。 此外離子溶液也可與其他模式的毛細管電泳做結合,並當作修飾劑, 就 K. Tian 等人的研究為例,在以 SDS 為主的毛細管微胞電動層析〈Micell
Electrokinetic Chromatography, MEKC〉中,添加[BMIM][BF4]來輔助分離木
酚素(lignan),在一般只添加 SDS 的條件下,4 個標準品只有 3 個訊號, 在加入了離子溶液後,四種分析物可在 13 分鐘內分離,作者的推測是因為 當添加了離子溶液,離子溶液的陽離子會中和 SDS 所帶的負電,使得 SDS 的臨界微胞濃度下降,進而影響微胞的大小與形成,造成分離時的不同[28]。
在非水相電泳的應用裡,偵測 profen 類藥品,在乙腈與醇類組成的緩 衝溶液中,添加約 7 mM 的離子溶液(1-butyl-3-methylimidazolium bis(trifluoromethylsulfonyl)imide, [BMIM][NTf2]),會產生吸附於管壁上的陽 離子與殘留在動相中的陽離子競爭,造成分離[29]。 1.3.4.3 利用離子溶液塗佈在毛細管管壁上 不同於上述利用離子溶液當緩衝溶液或修飾劑時產生的動態塗佈現 象,Qin 等人利用共價鍵結方式將離子溶液的陽離子塗佈在毛細管管壁上, 並使用此處理過的毛細管成功地應用於 DNA 或尿液樣品的偵測[30,31]。在 毛細管管壁上額外塗佈一層物質有許多功用,通常是為了避免分析物吸附 在管壁上或是調整電滲流的大小,在 Qin 的研究中,管壁因帶正電使得電 滲流反向,在此舉出兩篇文獻應用為例。 針對 DNA 的偵測,一般是使用聚丙烯醯胺(polyacrylamide)塗佈的毛 細管作分析,在 Qin 的實驗中,除了用離子溶液塗佈的毛細管做研究,同 時也比較經由聚丙烯醯胺處理過的毛細管分析 DNA 片段的結果,兩者的電 滲流方向是相反的,利用離子溶液處理過的毛細管對於分析 DNA 的穩定性 較高,且時間較短[30]。 經過離子溶液塗佈過的毛細管也適用於尿液中的銨根離子與其他金屬 離子等偵測,金屬離子由於本身不易用光學的方法偵測,若要用發色團作 處理又會受到緩衝溶液 pH 值的限制,因此 Qin 等人利用離子溶液當緩衝溶 液並使用上述處理過的毛細管作偵測,此方法不受 pH 值限制並可成功的分 開金屬離子與銨根離子[31]。 1.3.4.4 微胞型的離子溶液 在離子溶液中,增加陽離子上烷基鏈的長度,當碳數到一個定值以上, 即可形成微胞[32,33],應用於電泳中效果不下於一般使用的界面活性劑。 以咪唑為陽離子主體的離子溶液,目前以帶 12、14、16 等碳數的離子溶液 與傳統的界面活性劑相比,臨界微胞濃度均小於傳統的界面活性劑[34],代 表它更容易在水中形成微胞,也比較疏水,分析效果更佳。在 Borissova 等 人在 2008 年發表的文獻中成功的以 MEKC 方式利用具微胞性質的離子溶液
與苯環衍生物[34]。 也有研究以其他種陽離子為主體,如吡咯啶;在 2006 年 Schnee 等人利 用 C16MPYB(N-hexadecanyl-N-methylpyrrolidinium bromide)對苯環類化合 物,如苯甲腈、酚、硝苯及苯,做 MEKC 分離[35],在這篇文獻中,除了 成功的分離這四種苯環類化合物,研究中更是提出利用離子溶液型的界面 活性劑的多種優點,在性質上,這種界面活性劑比較疏水且極性低,所以 跟疏水的分析物作用力會更好,此外臨界微胞濃度低,應用在毛細管電泳 上更是可以減低因添加太多界面活性劑造成離子濃度高而焦耳熱上升的問 題。
N N R' R X + N + R4 R2 R1 R3 X N R1 R2 X +
imidazolium Tetra alkylammonium pyrrolidinium
N R X
+
P+ R4 R2 R1 R3 Xpyridinium Tetra alkylphosphorium
X = Cl、NO3、CH3CO2、CF3CO2、BF4、PF6、
CF3SO3、RSO3、(CF3SO2)2N
圖 1-2 離子溶液在毛細管中的作用機制[22]:在毛细管電泳的分離過程中, 離子溶液的陽離子會有部分吸附在管壁上,一部分在緩衝溶液中,分析物
會因與兩者作用程度不同進而分離。(IL+
:離子溶液的陽離子部分;An:待
二、Hofmeister series 2.1 簡介 在 1887 到 1898 年間,Hofmeister 和他的夥伴用德文發表了一系列關於 鹽類在科學上的研究,其中最受注目的就是 Hofmeister 在固定離子強度下, 針對不同離子對卵蛋白素造成沉澱(鹽析,salting-out)現象的程度做一個 歸納排序,換句話說,也可把這序列視為各離子對蛋白質結構上穩定性影 響的強弱,此序列又稱為 Hofmeister series[36]。雖然依據不同的蛋白質性 質此序列會有些差異,但是 Hofmeister 教授的實驗也開創了許多後續的研 究與應用。以下列出常見的 Hofmeister series[37]: Anions:H2PO4 ->SO4 2->F ->Cl ->Br ->NO3 ->I ->ClO4 ->SCN -Kosmotrope ────────Chaotrope 2.2 相關名詞介紹 在 Hofmeister 提出了這一系列的鹽類造成的現象後,許多相關的名詞 應運而生,在此做一個詳細的介紹。
2.2.1 水籠(clathrate or clathrate hydrates)
一個水分子因為能夠在接受兩個電子的同时也可以提供兩個電子,故 最多能形成四條氫鍵。由水的四條氫鍵所形成的正四面體序列,產生了開 放結構以及三維結合網絡,跟一般液體內部的緊密結構截然不同[38]。在水 中加入疏水性物質,由於疏水的表面會使水無法產生氫鍵,為了因應這種 改變,水分子會在這些非極性物質的表面形成一層較不活動的隔離層,把 非極性物質隔離起來,避免氫鍵的減少,這個結構稱為水籠(clathrate), 此過程被稱為疏水水合(hydrophobic hydration)[38,39]。通常水分子之間 也會以氫鍵互相連結,這些氫鍵比較會不停斷裂再重新快速形成,而水籠 分子間所形成的氫鍵,則較為固定,無法自由除去或快速形成。相較之下, 這些水分子的周圍無法像一般的水分子可以形成氫鍵,週遭水分子的數量 較少[39]。水籠結構如圖 2-1 所示。
2.2.2 kosmotrope and chaotrope 在 Hofmeister 教授所提出的一系列文章中,有一篇提到了離子與水之 間相互的吸引作用,因此也拓展此序列的應用[36]。 一般把離子分成兩種類型,kosmotrope 跟 chaotrope。kosmotrope 與 chaotrope 兩者是相反的代稱,由上一節得知,水會依照特殊的鍵結方式形 成網狀的結構排列,kosmotropic ion 與水分子會有比較強的作用力幫助水分 子之間的鍵結,又稱為 order-maker 或 structure-maker,而相反地當添加的 離子與水分子的作用微弱,就會影響水分子之間的氫鍵,造成水無法形成 網狀結構,這類離子稱為 chaotropic ion,也稱為 disorder-maker 或
structute-breaker。回歸一開始所提的蛋白質,kosmotropic anion 與 chaotropic cation 會安定蛋白質使其穩定[40]。大致上的區分為多電荷的小分子為 kosmotrope,反之單一電荷或低電荷的大分子分類為 chaotrope。另一個概 略的判定適用於單電荷的離子,當陽離子的半徑大於 1.06Å 與陰離子半徑 大於 1.78Å 的離子視為 chaotropic ion[41]。
2.2.3 鹽溶與鹽析(salting-in and salting-out)
所謂鹽溶,就是在溶液中加入鹽類使蛋白質溶於水溶液中,相對的, 若加入鹽類會使蛋白質析出,則稱為鹽析。兩者機制不同,以下做一個簡 略的介紹: 蛋白質的表面富含胺基與羧基,使得蛋白質表面帶滿電荷,而帶電荷 的程度則與所處的環境有關;當溶液的 pH 值大於 pI(isoelectric point, 就 是蛋白質的等電點,代表蛋白質的淨電荷等於零),蛋白質的淨電荷為負, 彼此會互斥,不易沈澱,反之亦然。而如果蛋白質溶液的 pH 值等於 pI 時, 因淨電荷為零而聚集沉澱;此時提高溶液中的鹽濃度,則蛋白質的溶解度 也會提高,這是因為鹽所解析出來的大量正負離子,會阻斷蛋白質表面正 負電荷間的相吸,阻礙其聚集而增加溶解度,因而使得蛋白質溶入水中。 這個現象稱之為鹽溶[42,43]。 蛋白質分子表面的極性與非極性分布情形不一,多少有一些較不具極 性的區域,水分子會在這些非極性區的表面聚集,形成類似「水籠」的構 造,以便把蛋白質溶入水中。有時候在溶液中加入了鹽類,鹽類會解離出
離子,如硫酸銨的兩價離子,會吸引了大量水分子,使水籠無法有效隔離 蛋白質的非極性區,造成這些非極性區之間的吸引,因而沈澱下來。這個 現象稱為鹽析[42,43]。 鹽溶與鹽析雖然添加的鹽類不同,機制也不一樣,但由於經濟且方便, 經常應用於簡單的蛋白質分離。 2.3 應用 Hofmeister series 是一個實驗結果的歸納與整理,在此序列中對離子的 特性作影響程度的排序與理論解釋,目前實質上應用最多的是在蛋白質的 純化,如 4.2.3 節提到的鹽析與鹽溶[42,43],其餘大部分是在作理論的探討, 如生化大分子的影響[44],離子溶液中陰陽離子的性質[7,41],或是用這個 理論來解釋實驗結果,如 HPLC[45-47],在越來越多的研究刊出之後, Hofmeister series 的完整度也日趨完善。 對於生化分子來說,最直接的理論應用就是在蛋白質[48]與酵素[49]等 分子,這類的分子就像之前提到的一樣,當添加不同的離子,受到的影響 也不同。針對離子溶液的部分,主要是因為當離子溶液溶於水中,會分成 陰陽離子兩部分,所以非常適用 Hofmeiater 的理論,舉例來說,離子溶液 中常見的陽離子 BMIM+ 就比 EMIM+ 更 kosmotrope[41];至於在 HPLC 中, 在動相中添加鹽類會使分離的效果更好,主要就是因為鹽類中的離子是 chaotropic anion,他會影響分析物的滯留因子大小,進而幫助分離[45-47]。
三、毛細管電泳 3.1 簡介 傳統電泳進行高電壓分離時,由於高電壓引起的焦耳熱不易排出,而 嚴重影響傳統電泳的分離效率使其應用效果受限;直到 1981 年 Jorgenson 與 Lukacs 利用內徑為 75 μm 的毛細管配合高電壓對一系列的胺基酸作分離 的測試[50],當使用毛細管作為分離的管柱時,因為內徑極小,提高了管壁 的比表面積,增加散熱的速率,大大的降低高電場下所產生的焦耳熱,分 離效率也因此提升。許多相關的研究陸續發表,在第一台商業化毛細管電 泳的儀器出現後,技術日趨成熟,應用性也提高,成為現今分離技術中重 要的一環。 3.2 分離原理 電泳是指帶電粒子在電場中的遷移運動。電量為 q 的粒子 i 在電場 E 下的移動速率 vi為 r qE E vi i 6 (3-1) μi:分析物的遷移率(mobility of analyte) η:介質的黏度(viscosity of medium) r:分析物的粒子半徑(假設分析物呈球型) 在毛細管內通入緩衝溶液,注入分析物後加上高電壓,利用分析物遷 移速度的差異作為毛細管電泳的分離基礎。毛細管電泳使用的分離管柱一 般為 fused silica 材質,在 pH 大於 2 時,毛細管管壁上的 silanol group 會解 離,使管壁帶負電;通入緩衝溶液後,緩衝溶液中的陽離子因為受到管壁 上負電荷的吸引而在表面形成電雙層,電雙層中的水合陽離子會帶動管柱 中的溶液往負極,進而產生一個平板流(plate flow),稱為電滲流。 由 Von Smoluchowski 所推出的電滲流公式可知,電滲流速度與電場強 度、介電係數 ε、溶液黏度 η 以及塔電位 ξ(zeta potential,電雙層所形成的 電位差)有密切的關係。
E E veo eo (3-2)
veo:電滲流的移動速度(velocity of electroosmotic flow)
μeo:電滲流的遷移率(mobility of electroosmotic flow)
不論分析物會往哪一個方向移動,由於電滲流的速度遠大於分析物的 電泳速度,電滲流都會帶動管柱中的分析物往同一方向移動,因此在單一 方向就可偵測到分析物。此外,由於電滲流是一個平板流,所以對於分析 時的區帶擴散能降低到最小,分離的效率便能提升。 考慮電滲流的影響,分析物在毛細管中的移動速度為:
L V E E t L v eff eo i a a (3-3) 故 Vt L Leff a (3-4)v:分析物的移動速度(velocity of the analyte)
Leff:毛細管的有效長度(effective length of the capillary)
t:分析物的移動時間(migration time of the analyte)
μeo:電滲流的遷移率(mobility of the electroosmotic flow)
μi:分析物的遷移率(mobility of the analyte)
μa:分析物的有效遷移率(effective mobility of the analyte)
V:施加電壓(applied voltage) L:管柱全長(full length of tube)
當對毛細管施加正電壓時,電泳中正、負離子及中性物質的移動速度, 以正離子的移動速度最快,再來是中性分子,最後則是負離子。 3.3 掃掠式線上濃縮簡介 有鑑於一般 CE 在偵測極限上的限制,線上濃縮的方法也應運而生。在 1999 年 Quirino 及 Terabe 對掃掠式線上濃縮的定義為利用微胞擬靜相穿過 樣品區帶對樣品進行挑選與累積的技術[51],目前也有眾多研究證實其顯著 的濃縮效果。可依照界面活性劑的型態作為區分,而其原理與機制由以下 舉例說明:
3.3.1 陰離子界面活性劑掃掠式線上濃縮 陰離子界面活性劑掃掠式線上濃縮為最早被發展的掃掠式線上濃縮模 式,最常使用的界面活性劑為 SDS,在此方法中,使用低 pH 值的緩衝溶液 (必須小於 3)抑制電滲流,其機制如圖 3-1 所示,將毛細管內充滿含有 SDS 的緩衝溶液,爾後再以壓力注入一大段和背景緩衝溶液離子強度相近 但不含微胞的樣品溶液,最後將毛細管兩端置於含有陰離子界面活性劑微 胞的背景緩衝溶液中,在施加負向電壓下分析物接觸到陰離子界面活性 劑,與陰離子界面活性劑結合後會受到電極吸引而往出口端移動追趕上前 方化合物,造成樣品區帶濃縮。一般來說,因為抑制了電滲流,因此分析 物與界面活性劑的作用時間較長,濃縮效果也較好,利用此模式在紅葡萄 酒中偵測白藜蘆醇(trans-resveratrol)的含量,搭配使用低溫螢光儀偵測器 (low-temperature fluorescence spectroscopy),與傳統 MEKC 比較,使用掃 掠式線上濃縮法的靈敏度可提升 1500 倍,偵測極限也比使用液相層析儀得 到的偵測極限來的低[52]。當面臨壓力或生氣、緊張時,我們的身體會產生 一種賀爾蒙叫做皮質酮(corticosterone),促使腦幹皮層多巴胺(dopamine) 和正腎上腺素(norepinephrine)的釋出,使生物體對環境的變遷產生高度適應 的效果,對血液與尿液中皮質酮的濃度做檢測,結果指出 MEKC 模式下的 偵測極限為 7 ppm,而 sweeping-MEKC 的偵測極限為 3 ppb [53]。 3.3.2 陽離子界面活性劑掃掠式線上濃縮 常見的陽離子界面活性劑為四級銨鹽,如 CTAB、TTAB 或 DTAB。以 Terabe 教授在 2001 年的一篇以 TTAB 濃縮放大中性的類固醇及帶負電的酸 類化合物為例[54]。在毛細管電泳中,管壁帶負電,通入陽離子型界面活性 劑時,界面活性劑會吸附於管壁上使其帶正電,因此電滲流方向會與一般 電泳相反。由圖 3-2 所示,先通入一段含有界面活性劑的緩衝溶液,再注 入一段導電度與緩衝溶液相當的樣品區帶,對兩端施加反相電壓,此時因 為界面活性劑帶正電荷,所以會往負極移動,但分析物是順著電滲流方向, 使得兩者產生交集,彼此間相互作用,進而達到濃縮效果。在這篇文獻中, 類固醇的濃縮放大效果約 65 到 150 倍,而帶負電的酸性分析物因與陽離子 微胞有靜電吸引力,讓分析物的滯留因子變大,放大倍率更是提升至 670
小即可有良好的濃縮效果。 近年來關於陽離子型掃掠式線上濃縮也有多篇文獻,在 2006 年有一篇 以 CTAB 做掃掠式線上濃縮應用在尿液樣品中偵測低濃度的氟硝西泮及其 兩種主要代謝物,放大的倍率約在 120 到 200 倍[55];而在 Heineman 的研 究中,針對較不疏水或帶有負電荷的大分子做線上濃縮,最高約可得到 112 倍的放大效益[56];此外有許多實驗都顯示抑制電滲流可以提升濃縮效果, 以 2001 年 Terabe 教授的研究為例,利用在管壁上塗佈一層聚乙醯胺 〈polyacrylamide〉抑制電滲流,並加入 CTAC 進行濃縮,結果靈敏度大幅 提昇,約有 600 倍的濃縮效果[57]。 3.3.3 中性界面活性劑掃掠式線上濃縮 使用中性界面活性劑的優點在於中性界面活性劑因為不帶電荷不會增 加管內的焦耳熱,所以可加高使用的濃度。分離機制以 Terabe 教授在 2001 年發表的一篇利用中性界面活性劑 Brij35 應用於濃縮酚類衍生物作為代表 [58],在此篇研究中,先通入一段含中性界面活性劑的背景緩衝溶液,注入 樣品溶液後,將毛細管兩端浸入緩衝溶液中並開始施加電壓,由電滲流把 背景緩衝溶液帶入管中,此時分析物因為帶負電所以會往電滲流的反方向 移動,進而穿過背景緩衝容易受到界面活性劑影響開始堆積濃縮,累積完 成後便隨電滲流往偵測器移動而被偵測,得到的濃縮倍率約為 54~100 倍。 3.3.4 掃掠式線上濃縮公式 在 1999 年 Terabe 教授團隊有對 Sweeping-MEKC 的原理做詳盡的介紹 [51],我們以中性分析物為例來推導公式,參考圖 3-3。假設被掃掠過後的 長度為 lsweep,則 lsweep=d(ac)-d(mcc) (3-5)
其中 aa與 ac分別代表在負極端(cathodic end)與正極端(anodic end)
的分析物樣品溶液與緩衝溶液界面的分析物,mca與 mcc則分別代表位於負
極端及正極端的界面活性劑,圖的虛線表示 ac和 mcc的起始位置,當 aa接
公式(3-6)和公式(3-7)
d(mcc) = vmctsweep ; vmc = vep(mc) + veof (3-6)
d(ac) = va(MEKC)tsweep ; va(MEKC) = vep * (a) + veof (3-7) vmc:微胞的遷移速率 va(MEKC):ac與微胞結合後的遷移速率 vep(mc):微胞自身的電泳速率 vep * (a):分析物的有效電泳速率 tsweep:當 aa接觸到 mcc所經過的時間 vep(a) = μep(mc)E (3-8)
mc E k k a vep ep 1 * (3-9)
eof mc
inj sweep v v l t (3-10) veof = μeofE (3-11) μep(mc):微胞的電泳淌度 E:電場強度 k:滯留因子(retention factor)為分析物分布於微胞相與溶液相的比例 μeof:電滲流的電泳淌度 將上述公式加以整合,可以得到 k l lsweep inj 1 1 (3-12) 公式(3-12)也可應用在分析帶電荷的物質上。由公式(3-12)可知,當注 入長度(linj)固定時,分析物的滯留因子越大,lsweep就會變的越短,表示 濃縮效果越好;當 linj增加時,被掃掠的區間越長,所能進入毛細管內的分 析物樣品量越大,偵測極限就越低。四、苯二氮平類藥物 4.1 引言 根據衛生署統計國內精神醫療院所通報的藥物濫用種類,苯二氮平類 的鎮靜安眠藥,自88年來就僅次於海洛因、安非他命,高居藥物濫用的第 三位[61]。因此針對苯二氮平類的藥物偵測顯得日益重要。 4.2 藥理學[62] γ-aminobutyric acid(GABA,γ-胺基丁酸)是人體中主要的抑制性神經
傳導物質,GABA 受體有兩種形式,分別為 GABAA與 GABAB,苯二氮平
主要作用是結合到 GABAA形成錯合物,活化 GABAA受體,使氯離子通道 打開,當氯離子流入突觸後(postsynaptic)細胞,導致細胞膜的電位過極 化(hyperpolarization),達到抑制神經及肌肉細胞的興奮性作用。GABAA 受體在人體中分佈廣泛,苯二氮平類藥物依據作用位置的不同而有不同的 功效,主要有五種作用: 1. 抗焦慮(antianxiety)與鎮靜(sedation): 作用於大腦皮質與邊緣區(limbic area) 2. 安眠(hypnotics): 作用在網狀構造(reticular formation) 3. 肌肉鬆弛(muscle relaxant): 作用在脊髓 4. 抗癲顯(anticonvulsant): 活化 GABA 神經元 5. 失憶(amnesia): 作用在海馬回(hippocampus) 4.3 臨床表現 最早合成出來的苯二氮平類藥物是 1960 年上市的 chlordiazepoxide (Librium® ),截至目前為止,苯二氮平的種類繁多。幾乎所有的苯二氮平 類藥物都具有口服吸收良好、高脂溶性、易進入腦中的特性,由於作用時
第一用藥。鎮靜作用可以降低白天的焦慮不安、過度激動,而使人感到鎮 定;安眠作用可以產生想睡感覺,幫助入睡(on-set)及維持睡眠。通常低 劑量的苯二氮平藥物當作抗焦慮劑或鎮靜劑,高劑量當安眠藥。此外還有 使用在麻醉、抗痙攣(seizure control)、肌肉鬆弛劑、治療酒精戒斷、及減 輕接受化療的病人之噁心和嘔吐的症狀。 與其他的精神科用藥相比,苯二氮平藥物的副作用較少,最常見的副 作用是鎮靜(sedation),所以通常病人會被告知開車或使用危險儀器要小 心。當與其他中樞神經抑制劑合用時,會有加成作用(additive effects),易 發生過度鎮靜及呼吸抑制,這些藥物包括酒精、巴比妥鹽(Barbiturates)、 三環抗鬱劑(Tricyclic antidepressants)、抗精神藥物、鴉片類、抗癲癇藥物、 抗組織胺藥物及麻醉等藥物,苯二氮平類的藥物最大的優勢就是作用快、 有效、及較少的副作用,但以下幾類病人不建議使用 1.對它過敏
2.睡眠呼吸暫止症候群(sleep apnea syndrome)
3.嚴重呼吸功能不足(severe respiratory insufficiency)
苯二氮平因為有成癮性的危險,所以除非是無法有效以某些抗憂鬱劑 控制焦慮症狀的病人才會長期服用。目前國內所有苯二氮平類藥物皆列為 第三級或第四級管制藥物。 4.4 檢測技術回顧 針對苯二氮平類藥物的檢測,Olaf H. Drummer 在 1998 年發表的一篇文 獻中將苯二氮平的偵測技術歸納為兩大類[63],分別為非層析技術與層析技 術,兩者互相輔助,同時也應用於其他種藥物濫用的檢測。 非層析技術主要以免疫分析(immunoassay methods)為主,包括酵素 免疫分析法(enzyme immunoassay, EIA)[64]、偏極光免疫分析法
(fluorescence polarization immunoassay, FPIA)[64,65]、酵素連結免疫吸附 分析(enzyme linked immunosorbent assay, ELISA)[66,67]以及同位素免疫 分析法(radio immunoassay, RIA)[68]等,但這類技術的缺點是在檢測結果 的判讀上,有可能發生偽陽性與偽陰性的檢測結果。前者是因為檢體成分 複雜,含有可能與免疫分析技術中的藥物抗體產生交叉反應(cross-reaction)
的物質,使檢測結果呈現陽性反應;後者是因為當檢測為陰性的時候,就 不會再做進一步的確認,所以若藥物濫用者在自己的檢體中添加其他干擾 物如漂白水、食鹽、肥皂等,免疫分析的方法就不適用,此外免疫分析的 方法靈敏度除了受限於交叉反應,還有使用的抗體種類,故通常是在初步 篩選時使用免疫分析法。 除了上述幾種免疫分析技術,其他新穎技術如在電極上塗佈碳焦 (carbon-paste)來偵測尿液及血漿中的苯二氮平藥物及其代謝物[69],或是 用分子拓印技術萃取出藥物[70]等;但在近幾年的研究文獻中,偵測苯二氮 平類藥物還是以層析技術為主[71,72]。主要包括薄層層析法(thin-layer chromatography, TLC)[73]、高效能液相層析法(high-performance liquid chromatography, HPLC)[74]、氣相層析法(gas chromatography, GC)[75] 以及毛細管電泳法(capillary electrophoresis, CE)[76-80]等。
4.5 毛細管電泳應用在苯二氮平類藥物的分析 在眾多層析方法中,毛細管電泳具有分析效率好、高靈敏度以及樣品 需求量少等優點,是研究苯二氮平類藥物的有力工具。就結構上來看,苯 二氮平類藥物屬於不易帶電的分析物,在毛細管中會隨電滲流一起抵達偵 測器而不易區分,因此通常改變一些電泳條件來分離此類中性化合物,最 常見的方法是在緩衝溶液中添加界面活性劑,此方法又稱毛細管微胞電動 層析(Micell electrokinetic chromatography,簡稱 MEKC)[76,77],MEKC 的分離原理是在緩衝溶液中加入界面活性劑以及適量的有機溶劑,當界面 活性劑的濃度超過其臨界微胞濃度時,便會在緩衝溶液中形成微胞,在毛 細管電泳中扮演擬靜相(pseudostationary phase)的角色;整個緩衝溶液分 成溶液相及微胞相,會讓分析物在兩相之間產生一個動態平衡的分佈,毎 個分析物的分佈情形不同,進而分離樣品。另外也可對毛細管管壁做額外 的處理,如動態塗佈數層高分子以分析苯二氮平[78-80],顯示出毛細管電 泳是分析苯二氮平的一大利器。
五、利用離子溶液輔助分離七種苯二氮平類藥物以及作用機制的探討 5.1 簡介 在本實驗中,我們將利用離子溶液作為修飾劑,協助分離苯二氮平藥 物,並個別就陰陽離子對分析物所造成的影響做探討。離子溶液具有許多 優點,如低蒸氣壓、化學性質穩定與熱穩定性良好等,應用於毛細管電泳 上可與分析物作用提高分離的效率,已有許多研究證實離子溶液有良好的 輔助效果。截至目前為止,關於離子溶液在毛細管中的分離機制多著重於 陽離子的部分,文獻上指出離子溶液的陽離子與分析物可能會有產生氫鍵 [27]或偶極偶極以及誘導偶極力等[23]作用力幫助分離,但離子溶液就像一 般的無機熔融鹽類,如氯化鈉,溶於水中會解離出一對陰陽離子,以目前 的研究而言,單一個別離子的探討並不多,尤其是陰離子的部分,大多只 有嘗試不同種類對分離的影響,在毛細管中的作用及機制卻鮮少提及,因 此在實驗上首先固定陰離子種類,改變陽離子基團,之後再固定陽離子種 類,改變陰離子基團,兩者相互比較,並作更進一步的探討。 5.2 儀器裝置
使用貝克曼公司(Beckman Instrument, Fullerton, CA, USA)所製造的 毛細管電泳儀,P/ACE MDQ 系列進行實驗。紫外光-可見光光二極體陣列 (UV-VIS diode array)作為偵測器。儀器與分析數據由 Beckman Coulter MDQ 32 Karat software 控制與處理;以內徑 50 μm ,外徑 360 μm ,總長 50 cm (至偵測窗口為 40 cm)之二氧化矽毛細管(fused-silica capillary, Polymicro Technologies, Phoenix, AZ, USA)作為分離管柱,毛細管外層塗附 之聚亞醯胺(polyimide)以火焰灼燒約 0.2 cm ,再以乙醇輕微擦拭灼燒處, 去除塗附之聚亞醯胺以形成偵測窗口。管柱溫度控制在 25 ℃下,分離電壓 為 15 kV。樣品注射以壓力注射(0.5 psi)3 秒方式導入毛細管中。偵測器 吸收波長設於 230 nm。 5.3 試藥 所有試藥皆為分析級。苯二氮平類標準品七種包括安定(diazepam)、 氯氮平酸鹽(clorazepate)、氯二氮平(chlordiazepoxide)、溴西泮
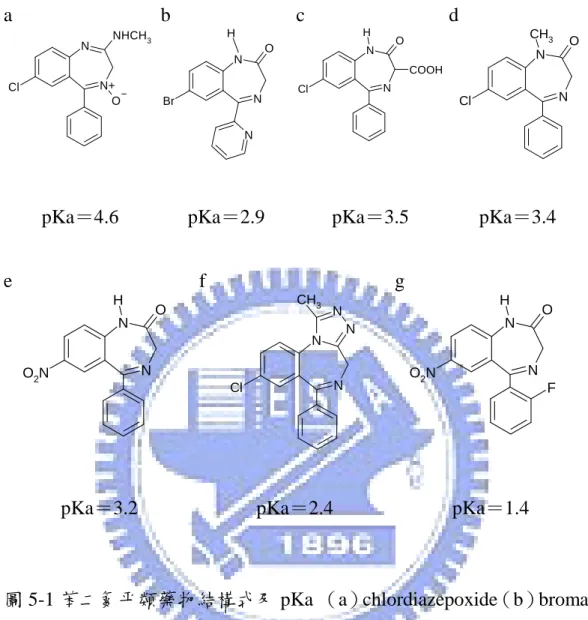
(bromazepam)、硝西泮(nitrazepam)、阿普唑他(alprazolam)、氟硝西泮 (flunitrazepam)結構式如圖 5-1 所示,皆購自 Sigma-Aldrich 公司(St. Louis, MO, USA)。二氯甲烷(dichloromethane, 99.99%)、1-氯丁烷(1-chlorobutane,
99.8%)購自於 Tedia 公司(Fairfield, OH, USA)。甲基引咪唑
(1-methylimidazole, 99%)、1-丁基-3-甲基咪唑氯鹽
(1-butyl-3-methylimidazolium chloride, 97.5%, 簡寫為[BMIM][Cl])、1-乙基 -3-甲基咪唑氯鹽(1-ethyl-3-methylimidazolium chloride, 97%, 簡寫為
[EMIM][Cl])、六氟磷酸鋰(lithium hexafluorophosphate, 98%, LiPF6)購自
於 Acros Organics 公司(Fairlawn, NJ, USA)。六氟磷酸鉀(potassium hexafluorophosphate, 99%, KPF6)購自於 Showa 公司(Tokyo, Japan)。氫氧
化鈉(sodium hydroxide, NaOH)、磷酸二氫鈉(sodium dihydrogen phosphate anhydrous, 99%)購自於 Fluka(Buchs, Switzerland)公司。Lithium
bis(trifluoromethylsulfonyl)imide(LiNTf2, 97%)、d-三氯甲烷(d-chloroform,
99.8 atom % D contains 0.05%(v/v) TMS, CDCl3)購自於 Sigma-Aldrich 公
司(Louis, MO, USA)。甲醇(methanol, 99.9%)購自於 Echo 公司(Miaoli, Taiwan)。鹽酸(hydrochloric acid, HCl, 37%)、2-氯乙醇(2-chloroethanol, 99 %)購自於 Riedel-deHaën 公司(Seelze, Germany)。乙腈(acetonitrile, 99.8%) 購自於 Mallinckrodt Chemicals 公司(Phillipsburgh, NJ, USA)。丙酮(acetone,
99.6%)購自於 J.T.Baker 公司(Phillipsburgh, NJ, USA)。磷酸氫二鈉
(di-sodium hydrogen phosphate anhydrous, NaH2PO4)購自於 Scharlau 公司
(Barcelona, Spain)。乙醇(ethanol, 95%)購自於 Shimakyu’s Pure Chemicals 公司(Osaka, Japan)。乙酸乙酯(ethyl acetate, 99.5%)購自 Grand Chemical
Company(Bangkok, Thailand)。實驗室所用的去離子水皆由 Milli-Q 水系統
(Millipore, Bedford, MA, USA)提供。 5.4 實驗方法
5.4.1 新的毛細管調態
本實驗所使用的毛細管內徑為 50 μm,外徑為 360 μm,管柱長 50 cm, 有效長度為 40 cm,毛細管外層塗附的聚醯亞胺以火焰燒除約 0.2 cm,在以 乙醇擦拭作為偵測窗口,裝置於 MDQ 卡夾中,新的毛細管柱在使用前依序
物,接著以去離子水沖洗 2 分鐘。為了讓毛細管內壁之矽醇基游離活化並 穩定,再以 1.0 M 氫氧化鈉水溶液沖洗活化毛細管內壁 10 分鐘,然後再以 去離子水沖洗 2 分鐘。 5.4.2 實驗前後毛細管處理及樣品注入與分離條件 每天實驗前以壓力注入的方式用甲醇、去離子水各清洗管內 10 分鐘, 在每一回要加電壓分離前會依序以甲醇 1.5 分鐘、去離子水 1.5 分鐘、0.1 M 氫氧化鈉水溶液 1 分鐘、去離子水 1.5 分鐘,最後再以使用的緩衝溶液沖洗 3 分鐘。樣品以 0.5 psi 壓力注入的方式注入 3 秒後,將毛細管兩端移至緩 衝溶液中施加 15 kV 進行分離。電解完後會用去離子水清洗毛細管 3 分鐘, 而每天結束實驗後,會以水洗 15 分鐘;在管子不用時,將毛細管的兩端浸 入去離子水中保存。 5.4.3 苯二氮平標準溶液配製 把固體的苯二氮平標準品以甲醇配成 1000 ppm 的標準母液,平常放置 於冰箱中保存(約 4℃),使用時將 1000 ppm 的甲醇標準母液以甲醇稀釋成 80 ppm,最後樣品溶液再以去離子水等比例的稀釋成 40 ppm。 5.4.4 離子溶液合成方式 實驗中所使用的離子溶液種類結構圖與縮寫列在圖 5-2,為了方便起 見,之後的實驗將這些離子溶液以縮寫代表。所有離子溶液在合成後均以 H1-NMR 對其作定性。 5.4.4.1 [BMIM][Cl] 將 1-methylimidazole 與 1-chlorobutane 以等莫耳數混合,在 80℃下加熱 迴流反應 48 小時,之後用乙酸乙酯洗兩次洗去殘留的雜質,最後再用減壓 濃縮的方式抽去殘留的乙酸乙酯[81]。 5.4.4.2 [BMIM][PF6] 將由上述方法合成出來的[BMIM][Cl]溶於約 50 mL 的丙酮中,加入等 莫耳數的 KPF6,在室溫下攪拌反應 24 小時,會有 KCl 的白色粉末沉澱,
利用重力過濾的方式將白色粉末過濾掉,用減壓濃縮除去丙酮,之後再過 濾一次除去雜質[23]。 5.4.4.3 [BMIM][NTf2] 取 0.035 莫耳的[BMIM][Cl]與 LiNTf2溶於 50 mL 丙酮,在室溫下反應 6 小時,之後用減壓濃縮除去丙酮,將剩下的溶液溶於 100 mL 的二氯甲烷, 用水洗三次,每次約用 25 mL,最後用減壓濃縮除去二氯甲烷[82]。 5.4.4.4 [C2OHmim][Cl] 將 25 ml 的 1-methylimidazole 加入 250 ml 乙腈(乙腈為溶劑),再將 30 ml 的 2-chloroethanol(基本上加入的量要與 1-methylimidazole 等莫耳數, 但要略為過量使 1-methylimidazole 可以完全反應),接著加熱至 70~80℃迴 流 48 小時,之後再除去溶劑即得到我們要的離子溶液[83]。 5.4.5 添加不同比例的離子溶液 5.4.5.1 不同種類陽離子的探討 在此以體積比方式個別添加 1%、5%、10%的離子溶液至緩衝溶液中, 離子溶液種類為[C2OHmim][Cl]、[EMIM][Cl]、[BMIM][Cl],緩衝溶液為 20 mM 磷酸緩衝溶液(pH 7.0)。 5.4.5.2 不同種類陰離子的探討 固定陽離子種類為[BMIM],改變陰離子種類;由於[BMIM][PF6]與 [BMIM][NTf2]的水溶性不好,所以在添加到緩衝溶液時,有加入甲醇來幫 助溶解。兩者分別以體積比的方式添加 1%、3%、5%,此外在添加 [BMIM][PF6]時,會加入 40%(v/v)的甲醇到緩衝溶液中,而對於 [BMIM][NTf2],則會加入 50%(v/v)的甲醇幫助溶解,緩衝溶液為 20 mM 磷酸緩衝溶液(pH 7.0)。 5.4.6 添加不同陰離子的鹽類
5.5 結果與討論 本實驗首先針對添加離子溶液的部份做探討,接下來以添加陰離子鹽 類作為研究個別離子對分析物的影響與機制分析。 5.5.1 添加離子溶液 5.5.1.1 不同種類陽離子的探討 離子溶液的組成可分為陽離子與陰離子兩個部份,在此先固定陰離子 種類為氯,比較不同陽離子造成的影響。在圖 5-3 中,[C2OHmim][Cl]在緩 衝溶液的含量由 1%到 10%,當添加比例為 1%時,對分離並無太大助益, 當添加的比例上升,可提升分離的解析度,但若超過了 10%(v/v),分離 效果並無增進,分析時間卻增加了,所以在[C2OHmim][Cl]加入的比例最好 的是 10%。 圖 5-3 使用的離子溶液陽離子帶有羥基,為了確定羥基是否會影響分離 的效率,以[EMIM][Cl](圖 5-4)作為對照組比較,當緩衝溶液含有 1% [EMIM][Cl]時,對於分析物的分離即有些微的影響(相較於圖 5-3(a)), 當緩衝溶液中的離子溶液含量增加,分離效果越好,但當添加比例到 10% 時,電流值已到儀器的電流上限(300 μA),故無法再以增加[EMIM][Cl]比 例來提升解析度。 由圖 5-3 與圖 5-4 可知,[EMIM][Cl]輔助分離效果比較好,在此以 [BMIM][Cl](圖 5-5)來觀察陽離子上的烷基鏈長短是否會改善分離結果, 同樣地,增加離子溶液的濃度可得到更進一步的分離效果;此外當離子溶 液的比例佔有 10%,也是到達儀器電流值的上限,故分離的效果無法再提
升。根據 3.2 節提到的公式(3-2),vEOF =(εξ/η)E,其中 ξ 為 Zeta 電位,
添加的濃度越高,緩衝溶液的離子強度增加,會壓縮電雙層使 Zeta 電位下 降,因此電滲流的速度減慢,分析的時間也隨之增加。整體歸納而言,添 加離子溶液濃度越高,有助於分離。 在無任何修飾劑的存在下,分析物為中性隨著電滲流一起抵達偵測 器。比較離子溶液在添加相同比例下,不同陽離子種類的影響,由圖 5-6 可知,效果最好的為[BMIM][Cl],其次為[EMIM][Cl],最後才是 [C2OHmim][Cl]。此外三種離子溶液的圖都顯示出分析物訊號是出現在電滲 流之前,表示在分離時是以帶正電的型式出現,故推測是陽離子可能會與
分析物有作用,造成苯二氮平會帶正電。 離子溶液中的咪唑類陽離子上含有電負度高的氮原子與帶正電的雜 環,會有許多不同可能的作用力,像是庫倫靜電吸引力、氫鍵、誘導偶極 力等[84],有文獻指出,離子溶液的陽離子與分析物可能會有產生氫鍵[27] 或偶極偶極以及誘導偶極力等[23]作用力幫助分離,推測在本實驗中也是類 似的作用力讓苯二氮平會與陽離子作用,進而協助解析度的提升。 至於帶有羥基的陽離子與烷基鏈上無任何官能基的陽離子結果上的差 異,推測是因為當陽離子帶有羥基時,水溶性增加,使得 C2OHmim + 變成 比較親水,另一方面,苯二氮平是屬於疏水性物質,相較於 C2OHmim + , EMIM+與 BMIM+ 等陽離子較疏水,疏水性的陽離子與疏水性的分析物間的 作用力可能較大,因此效果較好。 5.5.1.2 不同種類陰離子的探討 在上一節的比較結果可知,[BMIM][Cl]效果最好,所以用 BMIM+ 陽離 子為主體,進而比較 Cl- 、PF6 - 、Tf2N - 的作用。在圖 5-7 中,離子溶液的 比例由 1%到 5%,可以觀察到[BMIM][PF6]的分離效果並不顯著,此外由 於有添加部份的甲醇幫助[BMIM][PF6]的溶解,會改變緩衝溶液的黏滯度與 介電常數,進而改變的電滲流的大小,因此需要較多的分離的時間。 在圖 5-8 中為比較[BMIM][NTf2]的功效,因為[BMIM][NTf2]水溶性極 差,故添加了甲醇來幫助溶解,因此分析時間延長許多。在圖 5-8 看到添加 了 1%(v/v)的[BMIM][NTf2]便有些許的分離效果,當比例提高到 5%,樣 品便可完全分離,表示[BMIM][NTf2]為分離苯二氮平類藥物最適合的離子 溶液修飾劑。 針對不同陰離子,比較示意圖如圖 5-9。明顯地發現[BMIM][NTf2]效果 是最好的,此外圖 5-9(a)中訊號是出現在電滲流之前,但在(b)與(c) 圖中訊號會出現在電滲流之後,表示在分離時苯二氮平是帶負電的,在相 同陽離子下,改變陰離子種類會對樣品產生帶正負電的差異,表示陰離子 對樣品的分離比陽離子有更大的影響。由文獻以及本實驗中陽離子部分的 測試,推測離子溶液因可與分析物產生作用力而分離,故延續之前的推測, 代表陰離子與分析物之間也可能存有作用力,而陰離子的作用比陽離子大。
5.5.2 添加陰離子鹽類 在之前利用離子溶液當作修飾劑添加進入毛細管電泳的實驗中,我們 可由結果明顯觀察到陰離子對於分析的影響比較大,但由於添加時還要考 慮離子溶液本身的水溶性,必須添加額外的甲醇,可是添加甲醇後會對緩 衝溶液的黏滯度及介電常數有影響,所以改單純加入陰離子的鹽類來測試 陰離子在電泳中對分析上扮演的角色。 5.5.2.1 添加三種不同的陰離子鹽類 在圖 5-10 中,LiPF6的濃度由 200 mM 到 400 mM,在濃度為 200 mM 時,可發現 LiPF6對苯二氮平是有分離效果的,但可能濃度不足以使樣品完 全分開,故提高濃度看是否有更佳的輔助效果。當 LiPF6的濃度到了 400 mM 左右,可看得到七種樣品的訊號,但訊號的形狀不理想,可能是因為添加 的鹽類濃度太高,使得電流值太高,毛細管的散熱效果不像低濃度時好, 且時間增加,擴散效應更甚,讓訊號比較寬。 圖 5-11 是 LiNTf2不同濃度的比較,當 LiNTf2的濃度為 200 mM,訊號 還無法完全分開,當 LiNTf2的濃到提高到 300 mM,基線平穩,訊號可完 全分離,相較於離子溶液,分離時間需要 1 個小時左右,使用鋰鹽時約 18 分鐘內即可達成完全分離,分離效果優於離子溶液,當濃度到了 400 mM, 由於離子強度上升,分析時間增加,訊號也因擴散而變寬。 在圖 5-2 可知 TfO- 與 Tf2N - 結構類似,故添加 LiOTf 看是不是有相似 的效用。在圖 5-12 中,添加 200 mM LiOTf 時,確實有幫助樣品的分離, 當濃度由 200mM 提高到 400mM,訊號解析度確實有增長,但 400 mM 已 經到達 LiOTf 溶解度的上限,故無法藉由提高 LiOTf 的濃度增進解析度。 相同濃度下比較 3 種陰離子的影響,由圖 5-13 可知 Tf2N - 的效果最佳, PF6 - 與 TfO- 次之。在 Zhao 的研究文獻中,利用物理參數的計算得到 Tf2N - 比 PF6 - 更 chaotrope[41]。故推測本實驗陰離子的分離機制如下:苯二氮平 屬於疏水性物質,溶於水中會形成水籠,chaotropic effect 越強的離子,會 破壞水籠,使分析物裸露的機會增加,進而使陰離子與分析物的作用增加, 幫助分離。此外一般低電荷的大分子通常歸屬於 chaotrope,TfO- 的大小與 PF6 - 相近,故推測 PF6 - 與 TfO- 兩者的 chaotrope 程度差不多。
5.5.2.2 定性
由於苯二氮平的結構並無很明確的規律性,所以很難由結構上去判定 出現的順序,除了 bromazepam 之外,其他訊號的出現時間是依據 pKa 的大 小由大至小的順序出來。在相同濃度下,pKa 越大,表示不容易解離出氫 離子,越不容易帶負電,所以 pKa 越大會越早出現。
5.6 結論 使用離子溶液當作毛細管區帶電泳的修飾劑,通常會改變緩衝溶液的 性質,如電導度、黏度等,使得電滲流改變,而離子溶液上陰陽離子易與 分析物產生作用力幫助分離,這些都是離子溶液應用於毛細管電泳的優 勢。此外由於可自行設計離子溶液的性質,因此藉由改變構成離子溶液上 的陰陽離子以尋找最合適的離子溶液種類。 當固定陰離子為氯離子時,比較 C2OHmim + 、EMIM+ 與 BMIM+ 三種 陽離子,可發現在添加了離子溶液後,苯二氮平會因為與陽離子有作用力, 使得它帶正電,因而幫助了 7 個樣品的分離。由實驗得知,[BMIM][Cl]與 [EMIM][Cl]效果比[C2OHmim][Cl]來的好,推測是因為當陽離子多了羥基, 親水性增加,和疏水的[BMIM][Cl]與[EMIM][Cl]相比,與疏水的苯二氮平 作用力較弱,因此分離效果較差。 固定 BMIM+ 為陽離子時,改變不同的陰離子來做對比。由實驗結果可 知,當陰離子由 Cl- 變化成 PF6 - 與 Tf2N - ,苯二氮平的訊號由帶正電轉為帶 負電,表示陰離子的影響力比陽離子更甚,故改添加陰離子的鹽類探討分 離的效果。 經由添加離子溶液與陰離子的鹽類的比對,苯二氮平類藥物的分離效 果受到添加的陰離子種類影響較深遠,實驗結果發現當陰離子越 chaotropic,分離的效果越好,推測是因為 chaotropic 陰離子會破壞樣品分 子外圍的水籠使分析物裸露出來進而跟多餘的陰離子有作用力而輔助分 離,添加的鹽類濃度越高,作用力越強,讓樣品分開。在本實驗中,最佳 的分離條件為添加 300 mM 的 LiNTf2,七種樣品可在 18 分鐘內完全分開, 除此之外,時間與面積的在現性也很好。至於在定性方面,樣品分子會依 據 pKa 的大小由大至小出現。
a b c d N+ N Cl NHCH3 O
pKa=4.6 pKa=2.9 pKa=3.5 pKa=3.4
e f g
pKa=3.2 pKa=2.4 pKa=1.4
圖 5-1 苯二氮平類藥物結構式及 pKa (a)chlordiazepoxide(b)bromazepam (c)clorazepate(d)diazepam(e)nitrazepam(f)alprazolam(g)flunitrazepam N N O Cl COOH H N N Cl O CH3 N N H O O2N N N N N CH3 Cl N N O2N F H O N N N Br O H
(a)cation part (b)anion part 1-ethyl-3-methylimidazolium EMIM+ 1-butyl-3-methylimidazolium BMIM+ N N OH + 1-(2-hydroxylethyl) -3-methylimidazolium C2OHmim + Cl -Chloride Cl- bis(trifluoromethanesulfonyl)imide Tf2N - Trifluoromethanesulfonate TfO- Hexafluorophosphate PF6 - 圖 5-2 離子溶液的結構式以及縮寫(a)陽離子部分(b)陰離子部分 S F F F N S O F F F O O O F P F F F F F
s o
3-F
F
F
N + N N + N圖 5-3 在緩衝溶液中不同[C2OHmim][Cl]比例對分離效果的影響(a)1%(b)
5%(c)10%(v/v)[C2OHmim][Cl]
分離條件:20 mM 的磷酸緩衝溶液(pH 7.0);分離電壓:15 kV;注射壓力:
圖 5-4 在緩衝溶液中不同[EMIM][Cl]比例對分離效果的影響(a)1%(b)
5%(c)10%(v/v)[EMIM][Cl]。其餘分離條件同圖 5-3。訊號順序:
1. clorazepate, 2. diazepam, 3. chlordiazepoxide, 4. bromazepam, 5. nitrazepam, 6. alprazolam, 7. flunitrazepam.
圖 5-5 在緩衝溶液中不同[BMIM][Cl]比例對分離效果的影響(a)1%(b)
5%(c)10%(v/v)[BMIM][Cl]。其餘分離條件同圖 5-3。訊號順序:
1. clorazepate, 2. diazepam, 3. alprazolam, 4. chlordiazepoxide, 5. nitrazepam, 6. bromazepam, 7. flunitrazepam.
圖 5-6 在緩衝溶液中不同種類陽離子的離子溶液對分離效果的比較
(a)[EMIM][Cl](b)[BMIM][Cl](c)[C2Ohmim][Cl]。訊號順序同圖 5-5,
圖 5-7 在緩衝溶液中不同[BMIM][PF6]比例對分離效果的影響(a)1%(b)
圖 5-8 在緩衝溶液中不同[BMIM][NTf2]比例對分離效果的影響(a)1%(b)
3%(c)5%(v/v)[BMIM][NTf2]。其餘分離條件同圖 5-3。訊號順序:
1. chlordiazepoxide, 2. bromazepam, 3. clorazepate, 4. nitrazepam, 5. diazepam, 6. flunitrazepam, 7. alprazolam.
圖 5-9 在緩衝溶液中不同種類陰離子的離子溶液對分離效果的比較(a)
[BMIM][Cl](b)[BMIM][PF6](c)[BMIM][NTf2]。離子溶液在緩衝溶液中
圖 5-10 在緩衝溶液中不同濃度的 LiPF6對分離效果的影響(a)200 mM(b)
300 mM(c)400 mM LiPF6。其餘分離條件同圖 5-3。訊號順序:
1. chlordiazepoxide, 2. bromazepam, 3. clorazepate, 4. diazepam, 5. nitrazepam, 6. alprazolam, 7. flunitrazepam.
圖 5-11 在緩衝溶液中不同濃度的 LiNTf2對分離效果的影響(a)200 mM(b)
圖 5-12 在緩衝溶液中不同濃度的 LiOTf 對分離效果的影響(a)200 mM(b) 300 mM(c)400 mM LiOTf,訊號順序同圖 5-10,其餘分離條件同圖 5-3。
圖 5-13 在緩衝溶液中不同種類陰離子鹽類對分離效果的影響(a)LiOTf(b)
LiPF6(c)LiNTf2,訊號順序同圖 5-10,陰離子鹽類濃度皆為 300 mM,其
![圖 1-2 離子溶液在毛細管中的作用機制[22]:在毛细管電泳的分離過程中,](https://thumb-ap.123doks.com/thumbv2/9libinfo/8752126.206141/22.874.147.780.88.285/圖12離子溶液在毛細管中的作用機制22在毛细管電泳的分離過程.webp)
![圖 2-1 水籠[38]](https://thumb-ap.123doks.com/thumbv2/9libinfo/8752126.206141/26.874.142.783.86.782/圖21水籠38.webp)
![圖 3-1 陰離子界面活性劑掃掠式線上濃縮示意圖[59]](https://thumb-ap.123doks.com/thumbv2/9libinfo/8752126.206141/32.874.145.783.87.815/圖31陰離子界面活性劑掃掠式線上濃縮示意圖59.webp)
![圖 3-2 陽離子界面活性劑掃掠式線上濃縮示意圖[60]](https://thumb-ap.123doks.com/thumbv2/9libinfo/8752126.206141/33.874.140.783.80.791/圖32陽離子界面活性劑掃掠式線上濃縮示意圖6.webp)
![圖 3-3 中性界面活性劑掃掠式線上濃縮示意圖[58]](https://thumb-ap.123doks.com/thumbv2/9libinfo/8752126.206141/34.874.144.775.83.791/圖33中性界面活性劑掃掠式線上濃縮示意圖58.webp)
![圖 5-3 在緩衝溶液中不同[C 2 OHmim][Cl]比例對分離效果的影響(a)1%(b)](https://thumb-ap.123doks.com/thumbv2/9libinfo/8752126.206141/49.874.177.686.114.506/圖53在緩衝溶液中不同C2OHmimCl比例對分離效果的影響a1b.webp)
![圖 5-4 在緩衝溶液中不同[EMIM][Cl]比例對分離效果的影響(a)1%(b)](https://thumb-ap.123doks.com/thumbv2/9libinfo/8752126.206141/50.874.151.759.113.799/圖54在緩衝溶液中不同EMIMCl比例對分離效果的影響a1b.webp)
![圖 5-5 在緩衝溶液中不同[BMIM][Cl]比例對分離效果的影響(a)1%(b)](https://thumb-ap.123doks.com/thumbv2/9libinfo/8752126.206141/51.874.147.754.107.795/圖55在緩衝溶液中不同BMIMCl比例對分離效果的影響a1b.webp)