光聚合架橋性高分子離子液體應用於太陽能電池
全文
(2)
(3) 謝誌 感謝這兩年來,所有陪伴我、鼓勵我的人們,也要謝謝那些使我受 到挫折的人事物,讓我能看到自己的不足,並從中督促自我成長。 經由楊乾信教授的教導,使我在這兩年所獲得的知識及態度都受益 匪淺,以及感謝口委老師楊文都教授及林崇文教授,在口試時的殷切叮 嚀與指導,還有謝永堂教授及陳文正教授,在我未完成論文時給予我的 協助與幫忙。另外,還有親切善良的亞貞姊姊、子慧姊姊,以及怡雅姐 姐跟勝閔學長,陪伴且溫柔的鼓勵我跨越許多難關及困境,謝謝大家使 我能時常擁有充滿感謝的心情,擁有正面且積極的心態。 還有,要感謝實驗室的元岑、仕銘、峻嘉、琮勝等學長的提攜與教 導;實驗室的同學曉苑,還有學弟妹立德、倍毓、仲雅、志紘的協助; 以及與我一起胡鬧、一起快樂且充實的渡過這兩年碩士生涯的同學們。 最後,感謝家人對我愛與鼓勵,是我能完成這兩年碩士生涯的最大 動力,謝謝你們。. I.
(4) 目錄 謝誌………………………………………………………………………….Ⅰ 目錄 ................................................................................................................. Ⅱ 圖目錄 ............................................................................................................. Ⅵ 表目錄 ............................................................................................................. Ⅹ. 第一章 緒論 ..................................................................................................... 4 1.1 前言 ...................................................................................................... 4 1.2 離子液體介紹、發展與種類 ............................................................. 6 1.2.1 離子液體的介紹與發展 ............................................................ 6 1.2.2 離子液體的種類與應用 ............................................................ 9 1.3 研究動機和目的 ............................................................................... 11 1.4 研究架構 ........................................................................................... 13 第二章 文獻回顧 ........................................................................................... 14 2.1 從 IL 製作 PIL 介紹與應用 ............................................................. 14 2.1.1 從 IL 製作 PIL 的合成策略 ................................................... 14 2.1.2 陽離子基團聚合 ..................................................................... 15 2.1.3 陰離子及兩性離子基團聚合 ................................................. 17 2.1.4 共聚合物聚合 ......................................................................... 17 2.1.5 高分子離子液體的應用 ......................................................... 18 2.2 染料敏化太陽能電池 ....................................................................... 21 2.2.1 染料敏化太陽能電池之工作原理 ......................................... 22 II.
(5) 2.2.2 透明導電薄膜(Transparent conductive oxide, TCO) ....... 23 2.2.3 二氧化鈦(吸附層) .................................................................. 23 2.2.4 染料/敏化劑 ............................................................................ 24 2.2.5 電解液 ..................................................................................... 24 2.2.6 相對電極 ................................................................................. 26 2.3 儀器簡介 ........................................................................................... 27 2.3.1 傅立葉轉換紅外線光譜儀(Fourier-Transform Infrared ..... 27 Spectrometer , FT-IR) ..................................................................... 27 2.3.2 熱重量分析儀(Thermogravimetric Analysis , TGA) ............. 28 2.3.3 示差掃描熱分析(Differential Scanning Calorimetry , ........... 29 DSC) .................................................................................................. 29 2.3.4 X 光繞射分析儀(X-ray Diffractometer , XRD) ...................... 30 2.3.5 掃描式電子顯微鏡(Field Emission Scanning Electron Microscope , FESEM) ....................................................................... 32 第三章 含溴陰離子光聚合離子液體聚合物 ............................................... 33 3.1 前言 ................................................................................................... 33 3.2 實驗 .................................................................................................... 34 3.2.1 實驗儀器 ................................................................................. 34 3.2.2 實驗藥品 ................................................................................. 35 3.2.3 實驗步驟 ................................................................................. 35 3.2.4 材料性質分析 ......................................................................... 43 3.3 結果與討論 ........................................................................................ 46. III.
(6) 3.3.1 傅立葉轉換紅外線光譜分析 ................................................. 47 3.3.2 熱重量分析 ............................................................................. 48 3.3.3 示差掃描熱分析 ..................................................................... 49 3.3.4 X-光繞射分析 .......................................................................... 51 3.3.5 材料表面形貌分析 ................................................................. 53 3.3.6 導電度 ..................................................................................... 55 3.4 結論 ................................................................................................... 59 第四章 含 TFSI 陰離子熱聚合離子液體聚合物 ........................................ 60 4.1 前言 ................................................................................................... 60 4.2 實驗 ................................................................................................... 60 4.2.1 實驗儀器 ................................................................................. 60 4.2.2 實驗藥品 ................................................................................. 61 4.2.3 實驗步驟 ................................................................................. 62 4.2.4 材料性質分析 ......................................................................... 69 4.3 結果與討論 ........................................................................................ 73 4.3.1 傅立葉轉換紅外線光譜分析 ................................................. 73 4.3.2 熱重量分析 ............................................................................. 75 3.3.3 示差掃描熱分析 ..................................................................... 77 4.3.4 X-ray 繞射分析 ........................................................................ 78 4.3.5 材料表面形貌分析 ................................................................. 80 4.3.6 導電度 ..................................................................................... 82 4.4 結論 ................................................................................................... 85. IV.
(7) 第五章 離子液體聚合物應用在染料敏化太陽能電池............................... 87 5.1 前言 ................................................................................................... 87 5.2 實驗 ................................................................................................... 87 5.2.1 實驗儀器 ................................................................................. 88 5.2.2 實驗藥品 ................................................................................. 89 5.2.3 染料敏化太陽能電池製作 ..................................................... 91 5.3 結果與討論 ....................................................................................... 97 5.3.1 元件的 I-V 特徵曲線 ............................................................. 97 5.3.2 交流阻抗分析 ....................................................................... 103 5.3.3 IPCE 量測 .............................................................................. 106 5.4 結論 ................................................................................................. 109 第六章 結論與未來工作 ............................................................................. 110 參考文獻 ....................................................................................................... 112. V.
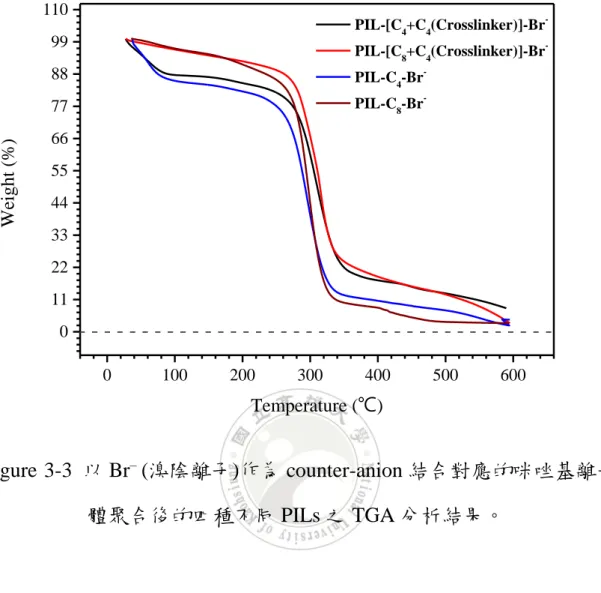
(8) 圖目錄 Figure 1-1 全球平均年溫度差及年份圖。 ................................................ 514 Figure 2-1 由單體聚合成高分子的主要分為兩種策略模式。 .................. 14 Figure 2-2 以熱聚合或光聚合法聚合出的網狀聚合化離子液體結構。 .. 16 Figure 2-3 以電化學法聚合出半共軛結構之聚合化離子液體結構。 ...... 16 Figure 2-4 一些陰離子型的聚合後的離子液體。 ...................................... 17 Figure 2-5 染料敏化太陽能電池示意圖。 .................................................. 21 Figure 2-6 DSSC 工作原理示意圖。 ............................................................ 22 Figure 2-7 布拉格定律示意圖。 .................................................................. 31 Figure 3-1 薄膜的導電度公式示意圖。 ...................................................... 46 Figure 3-2 以 Br– (溴陰離子)作為 counter-anion 結合對應的咪唑離子液體 聚合後的四種不同 PILs 之 FTIR 吸收光譜(分開疊圖)。.................. 47 Figure 3-3 以 Br– (溴陰離子)作為 counter-anion 結合對應的咪唑基離子液 體聚合後的四種不同 PILs 之 TGA 圖。 ............................................. 49 Figure 3-4 以 Br– (溴陰離子)作為 counter-anion,結合取代基為丁基(C4)咪 唑基離子液體,聚合後的線性型及含架橋性結構之兩種不同 PILs 之 DSC 圖。 ................................................................................................ 50 Figure 3-5 以 Br– (溴陰離子)作為 counter-anion,結合取代基為辛基(C8)咪 唑基離子液體,聚合後的線性型及含架橋性結構之兩種不同 PILs 之 DSC 圖。 ................................................................................................ 51 Figure 3-6 以 Br– (溴陰離子)作為 counter-anion,結合取代基為丁基(C4)咪. VI.
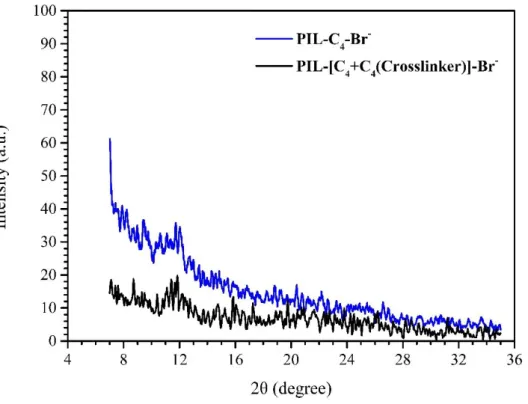
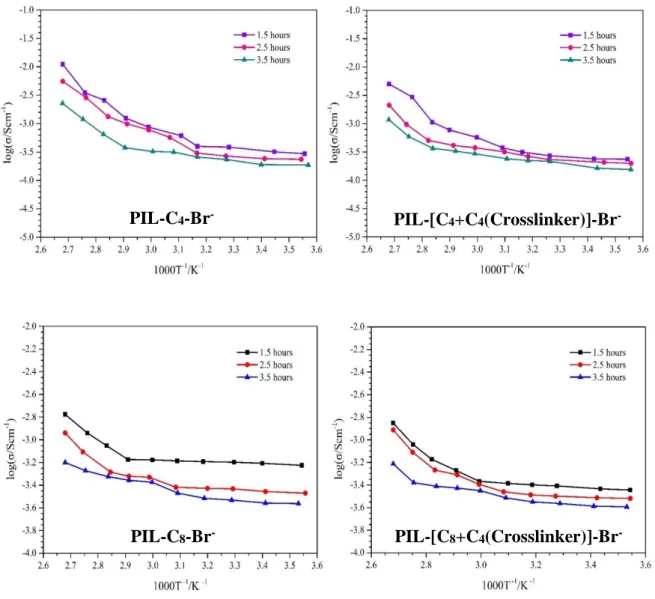
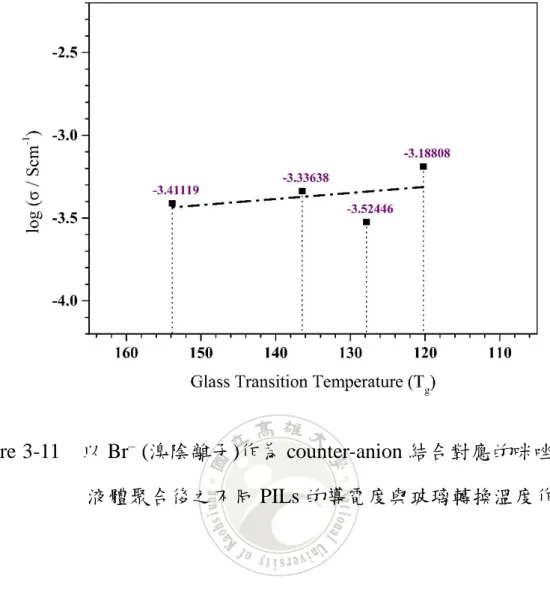
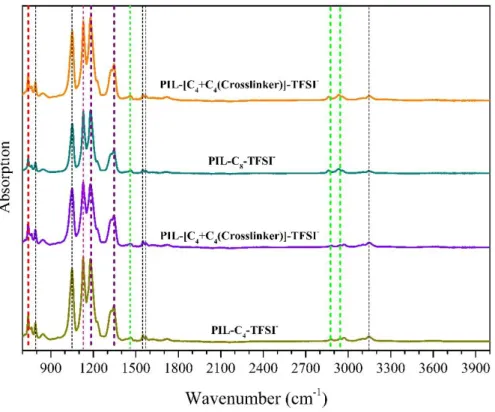
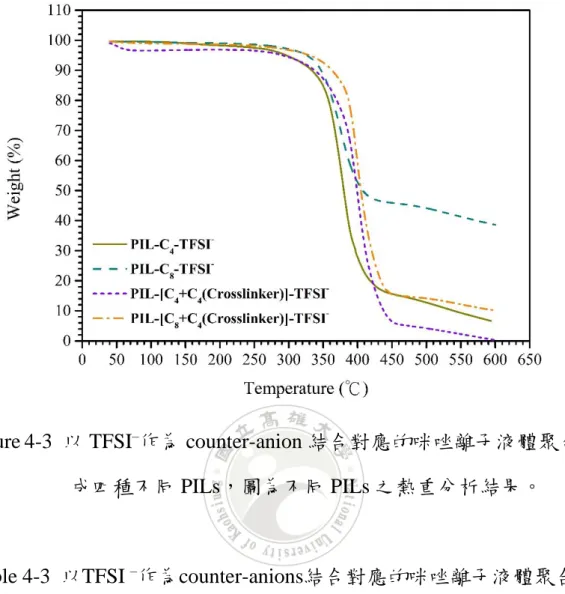
(9) 唑基離子液體,聚合後的線性型及含架橋性結構之兩種不同 PILs 之 XRD 圖。 ............................................................................................... 52 Figure 3-7 以 Br– (溴陰離子)作為 counter-anion,結合取代基為辛基(C8)咪 唑基離子液體,聚合後的線性型及含架橋性結構之兩種不同 PILs 之 XRD 圖。 ............................................................................................... 53 Figure 3-8 以 Br– (溴陰離子)作為 counter-anion,結合取代基為丁基(C4)咪 唑基離子液體,聚合後的線性型及含架橋性結構之兩種不同 PILs 之 表面形貌比較。 ..................................................................................... 54 Figure 3-9 以 Br– (溴陰離子)作為 counter-anion,結合取代基為辛基(C8)咪 唑基離子液體,聚合後的線性型及含架橋性結構之兩種不同 PILs 之 表面形貌比較。 ..................................................................................... 55 Figure 3-10 以 Br– (溴陰離子)作為 counter-anion 之咪唑基離子液體,不同 PILs 之導電度比較。 ............................................................................ 57 Figure 3-11 以 Br– (溴陰離子)作為 counter-anion 結合對應的咪唑基離子液 體聚合後之不同 PILs 的導電度與玻璃轉換溫度作圖。 ................... 58 Figure 4-1 以 TFSI–作為 counter-anion 結合對應的咪唑離子液體聚合後的 四種不同 PILs 之 FTIR 吸收光譜(分開疊圖)。 .................................. 74 Figure 4-2 以 TFSI–作為 counter-anion 結合對應的咪唑離子液體聚合後形 成四種不同 PILs,圖為不同 PILs 之熱重分析結果。 ...................... 76 Figure 4-3 以 TFSI–作為 counter-anion 結合對應的咪唑離子液體聚合後形 成四種不同 PILs,圖為不同 PILs 之 DSC 疊圖結果。..................... 78 Figure 4-4 以 TFSI–作為 counter-anion,結合取代基為丁基(C4)咪唑基離子. VII.
(10) 液體,聚合後的線性型及含架橋性結構之兩種不同 PILs 之 XRD 圖。 ................................................................................................................. 79 Figure 4-5 以 TFSI–作為 counter-anion,結合取代基為辛基(C8)咪唑基離子 液體,聚合後的線性型及含架橋性結構之兩種不同 PILs 之 XRD 圖。 ................................................................................................................. 80 Figure 4-6 以 TFSI-作為 counter-anion,結合取代基為丁基(C4)咪唑基離子 液體,聚合後的線性型及含架橋性結構之兩種不同 PILs 之表面形貌 比較。 ..................................................................................................... 81 Figure 4-7 以 TFSI-作為 counter-anion,結合取代基為辛基(C8)咪唑基離子 液體,聚合後的線性型及含架橋性結構之兩種不同 PILs 之表面形貌 比較。 ..................................................................................................... 82 Figure 4-8 以 TFSI-作為 counter-anion 之咪唑基離子液體,不同 PILs 之導 電度比較。 ............................................................................................. 84 Figure 4-9 以 TFSI-作為 counter-anion 結合對應的咪唑基離子液體聚合後 之不同 PILs 的導電度與玻璃轉換溫度作圖。 ................................... 85 Figure 5-1 染料敏化太陽能電池製作流程。 .............................................. 91 Figure 5-2 染料敏化太陽能電池元件。 ....................................................... 94 Figure 5-3 太陽能電池 I-V 特性曲線示意圖 .............................................. 95 Figure 5-4 IPCE 原理示意圖。 ..................................................................... 96 Figure 5-5 PIL-C4-Br-之不同比例下 I-V 量測結果。 .................................. 99 Figure 5-6 PIL-C8-Br-之不同比例下 I-V 量測結果。 ................................ 100 Figure 5-7 PIL-C4-TFSI-之不同比例下 I-V 量測結果。 ........................... 101. VIII.
(11) Figure 5-8 PIL-C8-TFSI-之不同比例下 I-V 量測結果。 ........................... 102 Figure 5-9 PIL-C4-Br-之不同比例下交流阻抗分析。 ............................... 104 Figure 5-10 PIL-C8-Br-之不同比例下交流阻抗分析。 ............................. 104 Figure 5-11 PIL-C4-TFSI-之不同比例下交流阻抗分析。 ......................... 105 Figure 5-12 PIL-C8-TFSI-之不同比例下交流阻抗分析。 ......................... 105 -. Figure 5-13 PIL-C4-Br 之 PILs 不同比例下 IPCE 量測結果。 ................. 107 -. Figure 5-14 PIL-C8-Br 之 PILs 不同比例下 IPCE 量測結果。 ................. 108 -. Figure 5-15 PIL-C4-TFSI 之 PILs 不同比例下 IPCE 量測結果。 ............. 108 -. Figure 5-16 PIL-C8-TFSI 之 PILs 不同比例下 IPCE 量測結果。 ............. 109. IX.
(12) 表目錄 Table 3-1 離子液體單體與高分子離子液體的結構與命名。 ................... 36 Table 3-2 具有架橋性之聚合後離子液體的結構。 ................................... 41 Table 3-3 以溴陰離子作為 counter-anions 結合對應的咪唑基離子液體聚 ................................................................................................................. 48 Table 4-1. 離子液體單體與高分子離子液體的結構與命名。 .................. 63 Table 4-2. 具有架橋性之聚合後離子液體的結構。 .................................. 68 Table 4-3 以 TFSI –作為 counter-anions 結合對應的咪唑離子液體聚合後的 四種不同 PILs 之熱分析比較。 ........................................................... 76 Table 5-1 不同成份之 PILs + DMPII 加入電解液之比例參數。 .............. 87 -. Table 5-2 不同 PILs(4C-Br )比例之效率表現。 ......................................... 99 -. Table 5-3 不同 PILs(8C-Br )比例之效率表現。 ....................................... 100 -. Table 5-4 不同 PILs(4C-TFSI )比例之效率表現。 ................................... 101 -. Table 5-5 不同 PILs(8C-TFSI )比例之效率表現。 ................................... 102. X.
(13) 光聚合架橋性高分子離子液體應用於太陽能電池 指導教授:楊乾信 博士(教授) 國立高雄大學 化學工程及材料工程學系 碩士班. 學生:陳善楣 國立高雄大學 化學工程及材料工程學系 碩士班. 摘要. 本研究主要是合成帶有乙烯基之咪唑基團(1-vinylimidazolium)的離子液體去接 上不同的碳鏈數目,將帶有不同陰離子基團的離子液體單體進行聚合得到不同種類 高分子離子液體,探討其材料特性:熱性質、化學鍵結結構、導電特性等。離子液體為 由陰離子及陽離子所組成的有機熔鹽,本身的性質有利於增加電子在電池中的傳導 能力。所以我們嘗試不同陰離子的離子液體單體,將其聚合且摻入部分於染料敏化太 陽能電池的電解液中,以此形成固態或膠態的染料敏化太陽能電池元件,來解決液態 染料敏化太陽能電池上常有的漏液問題,並且以溴離子及三氟甲烷磺酰亞胺離子為 陰離子,將帶有兩種不同取代基的線性型高分子離子液體分別加入帶有雙鍵結的高 分子離子液體,聚合成有架橋性的共聚和高分子離子液體﹐以溴離子及三氟甲烷磺酰 亞胺離子的線性型高分子離子液體混摻入電解液,在染料敏化太陽能電池(DSSCs)上 有 5.16 及 4.74 的效率。. 關鍵字:染料敏化太陽能電池、固態電解質、高分子離子液體. 1.
(14) Photopolymerization of Crosslinked Poly(Ionic Liquids) Applied to Dye Sensitized Solar Cells Advisor(s): Dr.(Professor) Chien-Hsin Yang Graduate Program in Chemical and Materials Engineering National University of Kaohsiung. Student: Shen-Mei Chen Graduate Program in Chemical and Materials Engineering National University of Kaohsiung. ABSTRACT. In this study, 1-vinylimidazolium-based ionic liquids with several lengths of carbon chains were first synthesized. Then, anion exchange and polymerization were employed to synthesize different types of ionic liquids and their corresponding polymeric ionic liquids. Material characteristics of these polymeric ionic liquids of thermal properties, chemical structures, electrical conductivity were analyzed and measured. An ionic liquid is composed of organic molten salt that contains anions and cations. The characteristics of such a liquid can promote increased electron conductivity in batteries. Ionic liquids exhibit the potential for applications using dye-sensitized solar cells (DSSCs). Therefore, we prepare the polymeric ionic liquids of different anion compositions and try to use to assemble DSSC devices. In this work, these polymeric ionic liquids were mixed with common used DSSC electrolytes to form a gel/solid type DSSC to solve the electricity leakage problem in DSSCs.. 2.
(15) Bromide ions and trifluoromethanesulfonimide ions were used as anions, and linear polymeric ionic liquids contained two types of substituent (C4 and C8) were separately added into a polymeric ionic liquids featuring double bond to form cross-linking copolymeric ionic liquids. The incorporation of linear polymeric ionic liquids, bromide ions and trifluoromethanesulfonimide ions, in electrolytes have the efficiency of 5.16 and 4.74 on the dye-sensitized solar cells (DSSCs). Keywords: dye-sensitized solar cells, solid electrolytes, polymeric ionic liquids. 3.
(16) 第一章 緒論 1.1 前言 隨著工業的高度發展帶來環境汙染的問題,人口急遽增長下伴隨對能 源的大量需求,在1973年爆發能源危機之後,人們逐漸意識到傳統能源 終有消耗殆盡的一天,能源的快速消耗,環境的日益惡化,迫使人類尋找 出一條從原料至最終產物的工業過程中,能降低對環境有害的廢物產生-----綠色化學是人類期許對環境友善的目標[1]。1951年,科學家們首次合 成出在室溫條件下是液體狀態之離子液體,之後室溫型離子液體(Room Temperature Ionic Liquid;RTIL)才被廣泛地運用於各個領域,近幾十年來 隨離子液體研究的快速發展,如今重點開發功能性導向的離子液體,其 種類已達到數百種之多,是綠色化學最熱門的研究題材之一,室溫型離 子液體具有高的化學及電化學穩定性、低的可燃性及極低的蒸氣壓與高 導電性等特性,雖然最初學術界與工業界大多做為揮發性有機溶劑的替 代品,如今已被發現越來越多的其他技術應用:如化學催化、有機和聚合 物化學、電化學、分析分離化學、能源、奈米技術和生物技術等領域[2]。 另一方面,人類對環境的過度開發及利用,導致地球氣候劇烈變化, 經年累月的燃燒化石燃料所排放出的二氧化碳對地球造成了溫室效應的 影響,不僅使得過去100年以來,地球的平均溫度上升了約0.6度(全球年 平均溫度差如Figure 1-1所示),也間接導致南北極冰山融化。人們意識到 開發新替代的能源且新替代能源必須要具備再生性及潔淨性等重要條件, 根據計算,我們只要能將抵達地表太陽能的百分之一轉換成可用的能量, 且以10%的光電轉換效率將其轉換成我們所能使用的電能,即可滿足我. 4.
(17) 們。因此太陽能電池受到世界各國的研究人員在開發新替代能源中佔有. 全球平均溫度差(℃). 絕對的重要性。. 年份. Figure 1-1 1850-2014 年的全球年平均溫度差(相對於 1961-1990 年),源 自英國氣象局哈得萊中心和和候研究小組、美國國家海洋及 大氣管理局國家氣候資料中心以及 NASA 空間研究所[3]。. 5.
(18) 1.2 離子液體介紹、發展與種類. 1.2.1 離子液體的介紹與發展 正、負離子間藉由庫侖靜電力相吸結合成的化學鍵結稱為離子鍵。原 子之間的電負性相差越大,鍵結強度就會越高,通常是金屬原子與非金 屬原子間的鍵結模式。電負度越大的原子越容易搶電子,以此符合八隅 體,兩者再以庫侖靜電力正負相吸而結合在一起,通常半徑越小或所帶 電荷越多,正負離子間的作用就會越強。離子化合物從固態相到液態相, 需要極高的溫度才能克服離子鍵結的束縛能,離子鍵結的強弱則會影響 該離子化合物的熔點、沸點和溶解性等特性,隨著陽離子半徑增大,陰陽 離子間的鍵結強度會下降,熔點也會隨之降低。離子構成的物質在室温 或室温附近温度下呈液態,稱為室温離子液體[4]。 現今,我們所知最早的離子液體可回溯至約一百年前。1914 年, Walden 發表了由濃硝酸和乙胺(EtNH2 + HNO3)反應製得史上的第一種離 子液體:硝基乙胺([EtNH3][NO3]),其熔點為 13-14℃[5],但通常包含少 量的水(200 至 600 ppm)。這個發現是現今所認為的離子液體最初的開始, 在材料界是一個新的分類的萌生,但在當時並沒有得到科學界的關注。 1948 年,Hurley 和 Wier[6,7]在田納西州的萊斯工學院發現了包含氯 鋁酸鹽的離子液體,他們用此溶液做電鍍鋁;於 1951 年,他們將 N-乙基 吡啶加入到 AlCl3 中(莫爾比=1:2),兩個固體混合物加熱後形成透明液體, 藉由增加陽離子與陰離子體積與結構間的不對稱性,來削弱陰陽離子間 的鍵結強度,首次合成出在室溫條件下是液體狀態之離子液體,但是,此 6.
(19) 種離子液體缺點是液體溫度範圍仍舊狹窄,而且,因其遇水會放出氯化 氫,對皮膚會有刺激作用,所以在當時並沒有太大的用途,也沒有把這個 體系進一步研究。 直到 1975 年,Osteryong 及 Wilkes[8]的研究小組第一次成功製得了 室溫的氯鋁酸鹽,藉由定出離子液體的相圖,推論出不同莫爾比例與熔 點間之關聯性,此時對離子液體的研究和發展,除了學術研究之外,主要 集中在電化學的應用上。 接著在 1976 年,在美國科羅拉多州立大學有學者在使用相同的系統 (AlCl3/[N-EtPy]Cl)作電解液進行有機電化學研究時,發現此種室溫離子 液體是良好的電解液,能夠與有機物相溶且不含質子。 20 世紀 80 年代末期,Hussey 所帶領的小組開始使用氯鋁酸鹽作為過 渡金屬錯合物的非水極性溶劑的研究,他們在期刊上發表的論文在當時 備受大家質疑[9],所以,於 1986 年最初向英國政府提出要發展離子液體 研究的建議時即被否定了,但也多虧了 Seddon 等人,發現含有氯鋁酸鹽 的酸性離子液體於 Friedel-Crafts 反應中是有效的催化劑,鹵化磷酸鹽可 被成功地用於親核芳烴的取代反應,才使離子液體變得廣為人知。 接著至 20 世紀 90 年代初期,Wilkes 及 Hussey 的團隊[10]發展出以 1-甲基-3-乙基咪唑基陽離子合成出氯化的 1,3-dialkylimidazolium (Mole fraction(AlCl3) = 50%),其熔點為 8℃,這種室溫型的離子液體具有物化 穩定性佳的特點,但是對於水氣極度敏感,必須在完全真空或是惰性氣 體環境下才能保存,使其應用的發展大幅降低,但也從此開始,離子液體 才開始有廣泛應用的發展;同一年,Wilkes 和 Zaworotko 合成出疏水性. 7.
(20) 且穩定性高的 1-乙基-3-甲基咪唑硼酸鹽(bmim[BF4]),因為此種類型的 離子液體非常適合作為反應介質,代表離子液體的方法的產生,自此以 後離子液體的發展正式展開[11]。 20 世紀 90 年代末期,Gratzol 和 Bonhote[12]發表了以 N(CF3SO2)2-作 為陰離子,然後以咪唑基團作為陽離子的離子液體,這種新型的離子液 體較第一代離子液體(第一代離子液體即最初於 1914 年發現離子液體的 Walden 開始),具有疏水性、安定性、低熔點、低黏度、高電熱穩定性質 等優點,至此之後,以 N(CF3SO2)2-作為陰離子基團的離子液體就成為被 廣泛使用之離子液體之一。從此,開始有學者去探討他們的性質,並得出 以下三個結論: (1)對稱型的陽離子形成的離子液體有較低的熔點。 (2)陰離子與陽離子之間若形成氫鍵,熔點會升高、黏度增加。 (3)陽離子若帶長鏈取代基的離子液體和有機溶劑的互溶性會增加。 從 21 世紀初開始,離子液體的研究方向逐漸改變,因為科學家們發 現,若是在陽離子或陰離子基團上嫁接不同的取代基,可以得到不同的 物理化學特性的離子液體,Sutton 曾說[4]過從理論上離子液體可能有一 萬億種,化學家們可以從中選擇適合自己工作需要的離子液體,從此,掀 起一股以此來應變在不同的應用上所需的離子液體的物理化學特性,即 所謂的功能化需求,像是導電性質、導熱性質、熔點等…物理特性;或是 配位能力、極性、溶解度等…化學性質,而從這個世代開始的離子液體就 被稱作是第三代離子液體 ——功能化離子液體,也被稱作 “Designer solvents[13]”。. 8.
(21) 1.2.2 離子液體的種類與應用[13-16] 離子液體是指在室溫或接近室溫下呈現液態的、完全由陰陽離子所組 成。與離子化合物比較,離子液體的熔點較低的主要原因,是因為離子液 體的結構中的取代基的不對稱性,使其原子或離子無法規則排列形成晶 體結構。一般由有機陽離子和無機陰離子組成,常見的陽離子像是:咪唑 鹽類(imidazolium)、吡咯烷鹽類(pyrrolidonium)、吡啶鹽類(pyridinium)等 等…;陰離子則有如:四氟硼酸根離子(tetrafluoroborate)、鎓六氟磷酸根離 子(hexafluorophosphate)、三氟甲磺酸根離子(triflates)等等。在較常被研究 的離子液體中,陽離子以咪唑鹽類,陰離子則以鹵素及其他無機酸離子, 例如四氟硼酸根等等為主[14]。. Figure 1-2 最常被使用的離子液體中,常見的陰離子基團與陽離子基團 種類。[14]. 9.
(22) 依照不同組合可達超過好幾十億種,熔點由801℃或低到-96℃,所以 為方便與一般有機熔鹽區別,將其定義為熔點低於100℃的離子液體稱為 室溫型離子液體[13],由於離子液體本身具有許多傳統溶劑沒有的優點, 具有好的化學及電熱穩定性、低燃點、極低的蒸氣壓及高離子導電性,還 有可調性高,除了可以替代一般傳統易揮發的有機溶劑應用於合成上, 也一直有新的應用機會持續被探討中。 離子液體具有安定性、熱穩定性、離子導電性、等電位點寬等優點, 有科學家探討其在電化學領域的應用,常用於電池的電解液、電鍍、生物 能源、燃料電池等;而離子液體同時也是可溶解極性與非極性化合物的 溶劑,因此,部分碳水化合物或動物纖維等生物高分子物,如;羊毛纖維、 木材等含有的纖維素,大部分皆可溶解於離子液體之中,也可以作為一 些碳水化合物反應的溶劑;另外,因為離子液體對大部分有機及無機物 質都具有一定的溶解能力,可以有效運用在有機物和金屬的萃取,加入 一些螯合劑使其形成金屬錯合物,使離子的疏水性增加來提升從水相中 萃取出來的能力;在環境領域上,因為不同於傳統揮發性有機溶劑,且在 水中有高溶解度,常用於汙染物的感測與去除、光觸媒的合成、二氧化碳 的捕捉,還有,以設計不同類型的離子液體來針對不同的廢棄物及汙染 物處理時的有機與無機成分的分離技術等;在無機及材料合成上,離子 液體早期只有用與有機化學反應的中的介質,或是於許多無機材料及無 機的奈米材料的合成上作為溶劑,近年來,在奈米金屬氧化物二氧化鈦 (TiO2)合成中,藉由加入離子液體來幫助形成銳鈦礦(anatase)結構的二氧 化鈦粒子提升結晶度[16],將離子液體作為吸收介質結合微波來加熱製備. 10.
(23) 出奈米材料,形成一種快速、無壓且低溫的合成方式。. 1.3 研究動機和目的 前面介紹許多離子液體的基本特性與應用,還有離子液體的發展至近 期研究。1996年,Grätzel等[17]就有提出應用於染料敏化太陽能電池的離 子液體的基本條件要求。首先,為了解決一般全有機的電解質容易揮發 且有毒性的問題,以全離子液體系統作為液態電解質,必須具備對水與 空氣的低敏感度、低黏度、高電導率且穩定性佳的特性才是適合染料敏 化太陽能電池的最佳電解液,但是一般效果都沒有全有機電解質來的好, 所以在後期,Grätzel等就以離子液體與有機溶劑的混合體系,加入可以共 溶的溶劑,其研究最高光電轉換效率可達11.8%,而且,在一般高效率的 染料敏化太陽能電池中,仍舊屬液態的電解質會有較好的效率表現。而 在固態電解質的表現中,以凝膠態的離子液體混摻入電解液中[18],形成 一種介於液態與固態之間的膠態的電解質,在研究中發現一般DSSC最常 使用的就是以咪唑類離子作為陽離子,因為他對TiO2有良好的吸附性且 能阻擋失去電子的染料分子與TiO2結合,藉由離子液體作為碘離子的溶 劑也可以增加在電解質中的離子傳導性,因此他們研究了一系列不同取 代基的咪唑基型離子液體,分析了他們的結構與性能的關係,發現性能較 好的離子液體一般具有一些特點,陽離子本身的非對稱性、取代基的大 小、陰陽離子之間的半徑比等等…,最主要還是取代基碳鏈越長,離子液 體本身的黏稠性會大幅降低電解質的流動,進而使效率降低,不過也有 學者發現在某一狀態下,碳鏈會形成液晶相的排列產生另一種離子傳導. 11.
(24) 的模式。 本研究主要在製作離子液體聚合物,探討其材料特性,期待適合用於 染料敏化太陽能電池(dye-sensitized solar cells)方面的離子液體聚合物。 染料敏化太陽能電池在商品化的過程,希望能解決容易漏液的問題,所 以我們將離子液體聚合後,將低分子量的高分子聚合物加入電解液中, 降低電解液在封裝後漏液的可能性,並期許能保有部分離子液體的離子 導電性,提升電子電洞的傳輸。. 12.
(25) 1.4 研究架構 製出以Br-為陰離子 的離子液體. 陰離子交換法. 以TFSI-取代Br-形成 第二種離子液體. 聚 合. 聚 合. 以光聚合聚合後,. 以熱聚合聚合後,. 進行FTIR、TGA、. 進行FTIR、TGA、. DSC、XRD、. DSC、XRD、. SEM、導電度的材. SEM、導電度的材. 料特性測試. 料特性測試. 進行電池光電轉化效率. 進行電池光電轉化效率. 測試、I-V curve量測,. 測試、I-V curve量測,. 並量測交流阻抗探討各. 並量測交流阻抗探討各. 項參數與光電池效率主. 項參數與光電池效率主. 要關係. 要關係. 13.
(26) 第二章 文獻回顧 2.1 從 IL 製作 PIL 介紹與應用. 2.1.1 從 IL 製作 PIL 的合成策略[2,14,19] 由離子液體單體聚合成聚合物的離子液體(poly(ionic liquids)),大部分 主要以陽離子基團作為主要單體骨架去進行鏈成長聚合(chain growth polymerization),形成大量的陰離子作為可移動分子,如乙烯基(vinyl)、苯 乙烯基(styrenic)、甲基丙烯基((meth)acrylic)等等…,常被作為高分子主要 骨架之基團,其 counter-ions 有四氟硼酸(BF4 -)、六氟磷酸(PF6 -)、三氟甲 磺酸(CF3SO3-)等…。從離子液體聚合為高分子離子液體主要分為兩種策 略模式:(1)直接從離子液體單體聚合。(2)從已聚合好的高分子長鏈中,修 飾其取代基或分子的結構。 CH3 n. H3C. CH3 n. H3C XLi. H2C. +. Polymerization. X-. Cl+. R. R. H2C XLi. -. Cl. +. Anion Exchange. CH3 n. H3C. R Anion Exchange + X-. +. Polymerization R. X-. R. Fig. general synthetic routes of polymeric ionic liquids. D. Mecerreyes / Progress in Polymer Science 36(2011) 1631. Figure 2-1 由單體聚合成高分子的主要分為兩種策略模式[2]。. 14.
(27) 過程(1)的反應較複雜且步驟繁複,但得到的共聚合高分子排列會較 整齊,並且控制在適當的聚合條件下可以得到 homopolymer;過程(2)的 反應將聚合與純化的步驟合而為一後,會使反應較簡單且容易,但是會 限制住之後離子交換時能使用的變化,無法定量、且是亂排排列的共聚 合物。除上述所列許多的陽離子基團種類,還有許多幾乎皆由傳統的自 由基聚合法來聚合。此外,現今有很多新型的聚合機制,像是原子轉移自 由基聚合反應(atom transfer radical polymerization)、可逆去活性自由基聚 合反應(reversible-deactivation radical polymerization)等…。由於本篇論文 是使用 imidazolium-type 的聚合化的離子液體進行研究,接下來就著重說 明此部分的介紹。. 2.1.2 陽離子基團聚合 高分子型態的離子液體有絕大部分是以陽離子基團(cationic moiety) 在高分子主要骨架上進行聚合,在相當常見的鏈成長聚合法(chain growth polymerization)中,咪唑基團是最常被使用的陽離子基團,其他還有如乙 烯基(vinyl)、苯乙烯基(styrenic)、甲基丙烯基((meth)acrylic)、甲基丙烯醯 胺((meth)acrylamide)等,這一類的高分子,大部分使用傳統的自由基聚合 方式去進行。近代期刊上也有出現新型之自由基聚合法,如:原子轉移自 由基聚合反應(atom transfer radical polymerization)、可逆去活性自由基聚 合反應(reversible-deactivation radical polymerization)、開環聚合反應(ringopening polymerization) 、 開 環 複 分 解 反 應 (ring-opening methatesis polymerization)等,所對應的 counter-ions 有 : BF4- (四氯硼酸)、 PF6- (六. 15.
(28) 氯磷酸)、 CF3SO3- (三氟甲磺酸)、 [(CF3SO2)2N]- (雙三氟甲基磺酸亞胺) 等。要能聚合出 liner homopolymer 和具有交聯網狀的高分子型態的離子 液 體 結 構 , 主 要 是 以 自 由 基 聚 合 法 去 聚 合 而 成 , 如 Figure 2-2 以 imidazolium diacrylate 為單體聚合成的有交聯結構的高分子[20],是以熱 聚合或 UV 光聚合的自由基聚合法得到的網狀高分子型態的離子液體結 構,一般多以鹵素離子和雙三氟甲基磺酸亞胺離子做為 counter-anions。. O. H2C. N+. O. N+. N. N. n. CH2 O. X-. X-. O. Figure 2-2 以熱聚合或光聚合法聚合出的網狀聚合化離子液體結構[2]。. 另外,還有以逐步成長或縮合聚合法,(1)將已聚合的高分子胺化後 再進行陰離子交換,將原本的離子取代為目標陰離子基團[2]、(2)或是利 用過渡金屬硼的催化,讓反應進行聚合[21]等、(3)以電化學聚合法使主要 聚合骨架中含有共軛結構的分子,此種半共軛的高分子型離子液體,在 同一個電活性聚合物上結合離子及電子傳導性質,增加其導電特性[22]。 R N XN (CH2). +. n. N R1 n. R2. Figure 2-3 以電化學法聚合出半共軛結構之聚合化離子液體結構[22]。 16.
(29) 2.1.3 陰離子及兩性離子基團聚合 相對而言,因為在合成上又增加更多的困難,以陰離子基團(anionic moiety)為主要聚合骨架的種類,相對於陽離子基團來說是少之又少,常 見的陰離子基團如:sulphonate( SO3R )、carboxylate( RCOO- )、 phosphoric( PO32-R )等等…。同樣地,以傳統的自由基聚合來說,最常 見的有乙烯基(vinyl)、苯乙烯基(styrenic)、甲基丙烯基((meth)acrylic)作 為主要結構接在上述陰離子基團的分枝進行聚合。 CH3 n. H3C. CH3 H3C. n. H3C. CH3 n COO-. SO3SO3-. Figure 2-4 一些陰離子型的聚合後的離子液體。[2]. 最後,一種被稱為兩性離子基團(zwitterionic moiety)之聚合化的離 子液體,這種高分子擁有兩個陽離子與陰離子,以共價鍵結方式連接在 主要的高分子結構中,但它的單體並非全都是以離子液體作為單體去進 行聚合,部分是以高溫下的固態融鹽去進行反應而得。. 2.1.4 共聚合物聚合 為了能得到有極高分子量的聚合物,共聚合是我們最常見到的方法之 一,將不同離子基團銜接在同一條主鏈上,且協調不同離子基團間的特 性,大部分共聚合高分子都是得到 random 或是 block 排列的高分子,並. 17.
(30) 且可以減少在聚合物主鏈還有尚未聚合的離子基團,近來也有出現以嵌 段共聚(RAFT)方法聚合出 block copolymer[23],這種聚合方式還上有許 多空間發展。. 2.1.5 高分子離子液體的應用[24,25] 下面簡單介紹幾種 poly(ionic liquid)常見的應用及特性。. 2.1.5.1 高分子電解質(polymer electrolyte) 離子導體本身必須就有離子導電特性,比起單純離子液體單體,聚合 後的離子液體有改善電池或燃料電池容易洩漏及可燃性高等缺點。高分 子型離子液體的不同大小、形狀、結構皆會影響其本身的離子電導率,因 為玻璃轉換溫度提升及可移動的離子減少導致導電性下降。離子液體單 體間陰陽離子本身的特性及間隙,例如:咪唑基陽離子基團在主鏈上單體 與單體間的空間若越長,可移動的分子或離子的變多,導電性進而上升; 另外,陰離子基團的不同也會影響,例如:分子量較大的 TFSI-陰離子,因 為使的陰陽離子間的鍵結強度減弱,使玻璃轉換溫度下降、導電性上升; 而擁有交聯網狀結構的離子液體單體聚合,往往也會因缺乏陰離子與陽 離子的可移動姓,固有低的離子導電特性。. 2.1.5.2 吸附劑(sorbent) 離子液體本身就有吸附氣體及分離廢棄氣體或汙水,以及作為氣體儲 存及傳送的介質的功能,所以在環境領域上是很熱門的材料,因為它不. 18.
(31) 易揮發且可以大量吸附及反覆運用,尤其是對溫室氣體 CO2 有明顯的效 果。聚合後的離子液體則被證實對 CO2 有更好吸附能力,早期就有學者 發表使用咪唑基團的高分子離子液體是有較優越性能,且陽離子基團上 取代基的不同會有對不同氣體的吸附性,而具有交聯網狀結構的固態薄 膜,對氣體的滲透性較低,這在高分子結構及分子組成上會有較多的解 釋。隨後他們又使用 tetra-alkyl ammonium 型的高分子離子液體,發現比 前者對 CO2 有更好的吸附性,但是其機制還尚未被證明。. 2.1.5.3 液晶相及奈米結構(liquid-phase and nano-structure) 學者們起初為了研究出異向性離子導體薄膜,無意間發現它具有一種 奈米尺寸的空間結構,也因此拓展另一條 PIL 的應用領域,如:奈米電子 學、光電子學、藥物傳輸等…。利用不同聚合法,讓離子液體自組裝成有 規則結構的具方向性的液晶相排列,Firestone 等人[26]則發現以 1-decyl3-vinylimidazolium 單體在水中可以自組裝出二維的六方層狀結構。. 2.1.5.4 電活性聚合物(electroavtive polymer) 離子液體也可用於與有電活性基團聚合的應用上,在一電場的作用改 變形狀或大小的聚合物,在受到巨大作用力時同時會有大幅度的變形, 結合離子液體優秀的電子傳導性能,運用在執行器或人工肌肉上的開發。 最早,Naudin 等人[27]是以咪唑基陽離子基團做為水溶性聚合物,為生物 檢測方面的應用,有些離子液體聚合後,會有液晶相排列的趨勢,與導電 聚合物結合下,可以使材料在很小的作用力下有極大的伸展,並且同時. 19.
(32) 有生物相容性,因此可以用來製備人造肌肉和微型設備等。. 2.1.5.5 分散劑(dispersant) 分散劑是能將固體顆粒與液體物料有效提高其分散能力的表面活性 劑,好降低固液間或液液間的表面張力。舉例來說,Mecerreyes 等人利用 poly(1-vinyl-3-3ethylimidazolium bromide)作為油相與水相間轉換的介質, 將碳奈米碳管及金奈米顆粒結合,奈米碳管(CNTs)與 PIL 可做為奈米金 屬 顆 粒 (PtRu/Pt) 的 催 化 劑 , 以 熱 聚 合 法 來 聚 合 出 poly(1-vinyl-33ethylimidazolium tetrafluoroborate)在奈米碳管表面將其改質後,有利於奈 米金屬顆粒的成長[28]。. 2.1.5.6 複合材料(composite material) 複合材料上,多使用咪唑基陽離子基團作為合成與聚合的單體,常被 應用在固態電解質上,除此之外,如以 1-vinyl-3-ethyl imidazolium 與丙烯 腈(acrylonitrile)共聚合後作為製作碳管的前驅物[29]。還有用無機結合有 機的複合材,將無機材料的特性與有機的 poly(ionic liquid)結合,舉例來 說,在染料敏化太陽能電池上作為擬固態電解液的應用等。甚至,運用離 子液體本身有高密度偶極矩的有機陽離子,將其作為良好的吸收微波介 質[30]。高分子離子液體在複合材料上合成的研究非常廣泛,拋棄過去使 用高溫/高壓的方法,逐漸朝低溫、常壓且短時間的合成方法,隨科技進 步與觀念提升,在國際上離子液體相關的議題也越來越多,可以看出未 來離子液體的發展是備受肯定的。. 20.
(33) 2.2 染料敏化太陽能電池[31,33] 染料敏化太陽能電池的整體結構主要可分為幾個部份,包括: (1) 基材(玻璃、塑膠或金屬材質) (2) 透明導電薄膜(FTO或ITO) (3) 多孔奈米二氧化鈦薄膜 (4) 染料光敏化劑 (5) 電解質溶液(碘離子/碘錯離子) (6) 幫助氧化還原催化用之相對電極(Pt) (如圖2-5). Substrate(FTO Glass) Cu Redox electrolyte Pt film. Figure 2-5 染料敏化太陽能電池示意圖[31]。. 21.
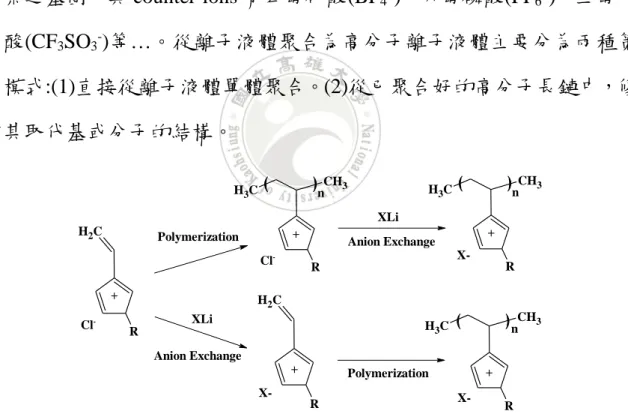
(34) 2.2.1 染料敏化太陽能電池之工作原理. Figure 2-6 DSSC 工作原理示意圖。[32] 染料敏化太陽能電池的工作原理示意圖如Figure 2-6所示。照射太陽 光後,多孔性奈米二氧化鈦層與電解液之間,發生光誘導反應而產生電 荷分離現象。因光敏化劑LOMO (lowest occupied molecular orbital)能階比 TiO2 導帶高(Ec: conduction band),故染料吸收入射光後,激發態電子迅速 注入半導體(TiO2)的傳導帶(conduction bend)中而形成染料陽離子(S+),並 透過導電玻璃經外部電路導出運送回到白金之相對電極,再將電子傳遞 至電解質中,藉由電解質進行氧化還原反應,還原之前失去電子之光敏 化劑。而電解液亦可經由相對應的相對電極處得到電子而還原。此一系 統構成染料敏化太陽能電池[33]。. 22.
(35) 電池的化學反應機制簡述如下[31]: 陽極:dye(S)+hν→dye*(S*) dye*(S*)+TiO2→e-(TiO2) + oxidized dye(S+) 2 oxidized dye(S+)+ 3 I-→2 S + I3陰極:I3- + 2 e-(Pt)→ 3 I-. 2.2.2 透明導電薄膜(Transparent conductive oxide, TCO) 在染料敏化太陽能電池當中,最常見的是於一般玻璃上鍍一層透明導 電薄膜,將受光激發而產生之光電流引導致外部電路,透明導電薄膜具 有高電導率、高透光係數、耐候性佳等等的優點。在太陽能電池中常見的 TCO 薄膜有 Tin-doped indium oxide(簡稱ITO) 、 Fluorine-doped tin oxide (簡稱FTO)、transparent conductive polymer(簡稱TCP)…等等材料。 本實驗使用FTO玻璃,FTO導電薄膜是利用氟摻入氧化銦降低散射效應, 採用噴霧熱裂解法所以不需要真空設備,降低成本,而且成膜後的耐酸、 耐鹼、耐候性佳,故一般實驗室研究皆採用此種導電薄膜。. 2.2.3 二氧化鈦(吸附層) 二氧化鈦有強的氧化及還原能力,常被用來當作光催化劑。在自然界 中,二氧化鈦是以銳鈦礦(anatase)、金紅石(rutile)、板鈦礦(brookite)三種 結晶態存在,在染料敏化太陽能電池中,anatase 相的二氧化鈦因能帶較 Rutile相的二氧化鈦還要大 (anatase 之 band gap 為 3.2 eV;Rutile 之 Band Gap為 3.0 eV ),當經紫外光照射後會產生電子電洞對時較不易掉回 23.
(36) 價帶,故其催化效果優於 Rutile。. 2.2.4 染料/敏化劑 染料是染料敏化太陽能電池中的重要組成部分,最早的構想是來自於 綠色植物行光合作用時的機制。假使利用光激發二氧化鈦來產生電子電 洞對,只有低於 388nm 之紫外光才能做到,但紫外光所佔太陽能光譜中 只有 6%,故必須以太陽光光譜中佔最高比例的可見光來激發電子電洞, 而染料即扮演將吸收波長提高至可見光區的角色,因此染料能藉由可見 光的驅使,將電子躍遷至二氧化鈦半導體電極,並接受來自電解質的電 子[34]。 一般染料必須要有以下幾點條件才能是好的染料[35],如:緊密吸附在 TiO2 表面、對可見光的良好吸收性、氧化態(S+)和激發態(S*)有高 穩定性和活性、高電荷(電子、電洞)傳輸效率、具有足夠的激發態氧化還 原電位、電子轉移過程中的自由能損失小。. 2.2.5 電解液 在染料敏化太陽能電池中,電解質(electrolyte)溶液之氧化還原對一般 是I3-及I-,其作用是將被氧化的染料分子還原回去,以避免染料分子又 將激發出的電子接收回去,並讓染料分子有持續激發出電子的能力。且I3 -. / I-在有機溶劑的擴散能力強,其能階與染料的HOMO能階較匹配,碘. 三根離子(I3-)會和經太陽光照射後,由二氧化鈦傳導帶上傳出的電子,在 對電極發生還原反應,染料則會被碘離子(I-)氧化,故電解液的作用是在. 24.
(37) 於使氧化還原反應完成。 本研究用來量測光電轉化效率元件中,所使用的是液態電解質,是將 含有碘離子的離子液體(ionic liquid)添加入液態電解質中,因為液態電解 質擁有高離子導電度導致較高的效率,且離子液體較傳統有機溶劑低熔 點、揮發性很低、化學穩定性佳以及高介電常數,因此可以有效的防止元 件密封不易,而使得電解質揮發或乾涸之缺點。 讓染料激發之電子有更多的機會傳導。目前電解液的研究方向有下 列三點: (1) 改善長時間日照的發電穩定性與熱穩定性。 (2) 取代傳統碘離子(I- / I3-)電解質,由於其有機溶劑 acetonitrile含有毒 性,對於人體健康有影響。 (3) 液體電解質有揮發現象,應用於染料敏化太陽能電池上會發生滲漏問 題,故需嚴密封裝。 目前所使用的碘化物,有濃度各為 0.1M~0.5M 的 LiI、NaI、KI、 R4NI(tetra- alkylammonium iodide) 以及 imidazolium-derivative 之碘化 物與濃度為 0.05M~0.1M 的 I2,再以適當的比例配製後,溶解於非質子 性溶劑中,一般常用的有: acetonitrile 、 propionitrile、methoxyacetonitrile 以及 propylenecarbonate等等[33]。 以離子液體取代全有機電解液,最常使用的是咪唑基陽離子基團,此 類陽離子不但可吸附在二氧化鈦表面,且在多孔隙的薄膜中形成穩定的 Helmholz 層,以阻隔了 I3- 與二氧化鈦表面的接觸形成再結合,使電池 整體的填充因子、光電轉換效率得以顯著增加。添加的離子液體的黏度. 25.
(38) 也會直接影響離子在電解質中的導電度以及電池的效能,因此,使用低 黏度的溶劑將能改善電池的效能[15]。. 2.2.6 相對電極 相對電極在染料敏化電池中扮演快速還原 I3- 的角色,所以有效的觸 媒催化劑是必須的,目前最廣泛被利用的為 Pt 觸媒,但其有效的程度(動 力學常數、化學穩定度、附著穩定度)卻強烈依賴著製作方法,如電化學 法(electrochemically)及蒸鍍法(vapor deposited)因穩定度不佳及還原能力 不好而不適用,濺鍍法(sputtering)最為被廣泛利用,其穩定性佳、製作程 序簡便,惟需消耗較多 Pt 而不適於大量生產, Papageorgiou 等人則發 展出熱沉積(thermal decomposition) Pt 法[36],此法不僅大量減少 Pt 用 量,在動力學參數、化學穩定性、機械強度及透明性上皆有其優異之處, 惟做法上較為麻煩。此外 Kay and Grätzel 也發展出利用多孔性碳(porous carbon)做為觸媒層[37],此觸媒層為碳黑(carbon black)、石墨、奈米結晶 性 TiO2 粉末的混合物,碳黑可連接分離的石墨片而提高導電度, TiO2 則作為黏著劑(binder)用,此項技術之最大優點在於成本降低,不過目前 的效能還是較 Pt 觸媒差。. 26.
(39) 2.3 儀器簡介. 2.3.1 傅立葉轉換紅外線光譜儀(Fourier-Transform Infrared Spectrometer , FT-IR) 於 1950 年末期,紅外線光譜儀開始被普遍運用在鑑定有機化合物上, 直到 1980 年傅立葉轉換紅外線光譜儀開始普及才又邁進一大步,此種光 譜分析方法在化學分析或材料分析上都有相當廣泛的應用,為研究一化 學分子因為吸收或發射紅外線輻射,而產生振動或振動-轉動的能量變化。 光譜涵蓋範圍為 12800 cm-1 至 10 cm-1,分為遠、中、近三個區域, 近紅外線光譜區域為 12800~4000 cm-1,可以觀測分子的某些振動模式倍 頻及組合光譜區的吸收,尤其是 –OH 及 –NH 伸縮振動的倍頻,及 –CH 伸縮振動與烃基變形振動的組合譜帶。中紅外線光譜的範圍為 4000~200 cm-1,即一般所指的紅外線光譜區域,依照分子特性可劃分為特性頻率區 (4000~1300 cm-1),此區域主要顯現分子一些主要的官能基的吸收頻,以 及指紋區(<1300 cm-1),此區主要是顯示分子結構的微細差異;遠紅外線 光譜區則涵蓋 200~10 cm-1,主要針對重原子部分的結構與成分分析。 紅外線光譜分析應用含括有機或無機化合物上各種官能基的檢測。有 機化合物分子結構中,各原子間發生震動(vibration),就可能對紅外線產 生特定波長的共振吸收,或是分子中含某一特性官能基時,通常會吸收 一特殊波長的紅外線,如此紅外線光譜便可推知具有哪些官能基,進而 可鑑定其分子結構[38]。. 27.
(40) 2.3.2 熱重量分析儀(Thermogravimetric Analysis , TGA) 熱重量分析儀(Thermogravimetric Analyzer)簡稱 TGA,是用於量測樣 品材料在特定溫度區間條件下的重量變化。主要原理為將樣品置於一個 加熱爐中,透過電腦程式來操控升溫、降溫或恆溫的過程,在加熱爐中持 續通入固定的環境氣體(例如:氮氣),當溫度上升時,在惰性氣氛中會受 熱分解,在空氣或氧氣中則會氧化燃燒,當到達樣品中某一材料成分的 裂解溫度、蒸發溫度、氧化溫度時,樣品會因為裂解、蒸發、氧化而造成 重量減少的現象,減少的部分有吸附在樣品上之小分子(例如:H2O)或樣品 本身分解之氣體,記錄其隨著溫度的重量變化,即可判定材料的裂解溫 度、熱穩定性、成分比例、樣品純度等特性。 熱重分析儀中,最重要的兩大元件是溫度控制系統和重量量測元件 (微量天平),微量天平位於加熱爐中其敏感度極高,故天平與樣品的載台 都要在密閉的系統中,以避免有外界氣流干擾或是震動而造成誤差,通 入氣體的流量也要是不對系統造成影響為原則,將加熱爐開啟後先進行 天平的校正,校正完畢後將樣品加入,樣品的加入會使天平失去平衡,天 平的平衡桿中心附近有電磁鐵,重量會讓桿端光電池將受光放電,電磁 鐵通電產生扭力讓天平恢復平衡,記錄器則會記下通過電磁鐵之電流, 將其訊號轉換為樣品重量的改變,並將此改變與溫度變化以作圖表示。 每個樣品中的成分不一,利用本身程式具有的溫度階段化功能,在不同 小分子分解或氧化時,中間過程給予一等溫階段,可以讓兩段的產物不 互相重疊,待第一階段完全後再繼續第二階段[39]。. 28.
(41) 2.3.3 示差掃描熱分析(Differential Scanning Calorimetry , DSC) 示差掃描熱分析是用於測量材料內熱轉換相關的溫度與熱流,藉由固 定速率之升、降溫或恆溫操作,紀錄測試樣品與參考樣品的熱流量差異。 通常被使用在材料的調查、選擇、比較樣品之間的各種相變化、比熱與相 變化之熱焓等,像是高分子、無機材料、生醫等領域之分析,包括結晶、 熔融、氧化、交聯固化、玻璃轉移…等反應,分析結晶度、純度及動力學。 分為功率補償式 DSC 及熱流式 DSC,學校公用實驗室所使用的是熱流式 DSC,機台開機時,需先配合冷凍乾燥機暖機 30 分鐘,先進行除水等動 作,再將待測樣品放入樣品槽內,另外一邊放置空白片來做為一熱流的 參考基準點,在特定氣氛下(一般為氮氣或氬氣),以熱流量的差異(Y)與 溫度(X)作圖記錄。放置的參考樣品及測試樣品是在同一加熱爐中,樣品 底部是一種以銅鎳合金製成的蓄熱板用於將熱傳遞到樣品,蓄熱板下方 有一鎳鋁-鎳鉻合金製的金屬板,形成一熱電偶好來量測空白樣品與待測 樣品之間的溫度差異,而因蓄熱板的熱容量遠大於載台及樣品,樣品所 能接受的熱流量和載台也有一定的差異,但彼此間能成固定比例關係, 故再將量測到的溫度差異轉換為熱流量差異之訊號,即可得到最後的數 據。一般熱流式 DSC 的誤差比起功率補償式的 DSC 以直接記錄其熱流 量方式,誤差較大約在 5%,可操作最高溫度約在 600℃左右,因樣品是 置於同一個爐內,所以要考慮其氣流速率及升降溫速率的關係,才能得 到正確性高的數據[39]。. 29.
(42) 2.3.4 X 光繞射分析儀(X-ray Diffractometer , XRD) 本實驗使用德國 Duker 公司所生產的 D8 型 X 光繞射分析儀,分析 鍍製的薄膜之晶格排向,X 光光源是銅靶(Cu Kα,λ=1.5405Å ),掃描之 繞射角度 2θ 由 5o 到 35o,每秒掃描 0.02o,操作電壓為 40kV,操作電流 為 40mA ,用以鑑定薄膜的結晶相。 1913年W.L. Bragg父子在從事晶體結構分析實驗中,從散射X光的分 佈情形,他們認為可以將繞射現象視為入射光被晶面反射。此種反射如 同鏡面反射,入射角等於反射角。在某些散射角下,從相鄰晶面散射波彼 此相位相同,光程差為波長的整數倍,因而產生建設性干涉。滿足此條件 便可產生繞射,稱為布拉格定律(Bragg's law),為晶體繞射X光時,布拉 格方程式之幾何關係。 2dhklsinθ=nλ 不同的晶體結構晶面間距dhkl會有所差異,因此會有不同組合之繞射角 {2θhkl}。 繞射的發生除了必須滿足布拉格條件外,也會受晶體對稱性影響。當 晶胞內所含原子數目不只一個時,由於這些原子彼此的對稱關係,而限 制了某些繞射發生,故當近乎單色光之X光照射晶體時,只有在特定的入 射角才會出現繞射玻,這是主要決定於晶胞的形狀、大小及對稱性。此 外,晶胞內組成原子不同時,由於各原子對X光散能力相異,故雖結構相 同也會造成不同繞射強度[40]。 X光繞射實驗決定高分子是否具有結晶度,及各高分子排列結晶整齊 性。. 30.
(43) Figure 2-7 布拉格定律示意圖[40]。. 31.
(44) 2.3.5 掃描式電子顯微鏡(Field Emission Scanning Electron Microscope , FESEM) 隨著材料科學的進步,微結構影響在材料本身的性質甚鉅,因此欲瞭 解材料本身的性質,就必須有良好的顯微分析技術及工具。電子顯微鏡 就是其中之一,其利用電子與物質作用所產生之訊號來鑑定微區域結構、 微細結構、化學成份、化學鍵結和電子結構的電子光學裝置。掃瞄式電子 顯微鏡原理的提出與發展,約與 TEM 同時;在 1935 年提出掃瞄式電 子顯微鏡的理論與構想,到 1942 年 Zworykin 等人發展出第一台實驗 室用掃瞄式電子顯微鏡。1965 年英國 Cambridge 公司首先推出商品化 的掃瞄式電子顯微鏡。在之後的數十餘年,隨著科技進步,儀器本身的能 力如:解析度、操作方便性不斷提升,而周邊之分析儀器也不斷的改良, 以追求更精確、更豐富的物質基本性質分析。 掃瞄式電子顯微鏡主要是來觀察物體的表面型態,其試片製作較簡單, 解析度可達奈米尺度且景深長,在觀察材料表面形貌上非常清楚而容易, 目前已被廣泛的使用。電子顯微鏡之工作原理,即以波長遠小於一般可 見光的高能量電子取代光源,因此解析度可大大的提升SEM 的主要工作 原理為電子鎗透過熱游離或是場發射原理產生高能電子束,經過電磁透 鏡組後,可以將電子束聚焦至試片上,利用掃瞄線圈偏折電子束,在試片 表面上做二度空間的掃瞄[41]。 本實驗使用場發射型掃描式電子顯微鏡(Hitachi S-4800)來作分析,在 分析前須將試片裁切成適當大小,並且鍍上一層適量的白金薄膜,此目 的乃是為了增加導電度,可以避免因為電荷累積而導致成像不良。. 32.
(45) 第三章 含溴陰離子光聚合離子液體聚合物 3.1 前言 自從有研究開始將離子液體取代原本電解液,並發現能打破以往在電 化學領域上的瓶頸後[42],離子液體開啟在電化學及電池領域上的應用, 越來越多研究開始在電池及電化學裝置上運用離子液體,得到良好的離 子傳導特性,並且可以改善循環特性、穩定性等等,但液態電解液仍然有 它的缺陷,以往的液態電解液是有毒且易揮發的,所以為了改善前者的 缺憾將電解液以對環境友善的離子液體做取代,然後加入離子液體聚合 物,採用離子液體與離子液體聚合物的混合,或甚至直接以離子液體聚 合物作為電解質,使得液態的電解液變成膠態、甚至是固態的電解質,希 望電池封裝不再會是問題,在材料機械性質上也能有進步。 離子液體聚合物相對單純離子液體而言,較適合去做出能符合設計的 高分子電解質,但是在離子導電性上,離子液體又有比較良好的表現,所 以將離子液體及離子液體的聚合物混合。對於整體染敏太陽能電池 (DSSCs)的效率,1-vinylimidazolium陽離子以iodide做counter-anion的離子 液體中有最佳的表現,所以我們嘗試改以溴陰離子為counter anion的離子 液體聚合物來為後面元件組裝的性能做基礎特性的探討。. 33.
(46) 3.2 實驗 3.2.1 實驗儀器 實驗儀器. 廠牌. 型號. DSC. TA Instruments. SDT-Q600. TGA. TA Instruments. SDT-Q100. 傅立葉轉換紅外光譜儀. Agilent Technologies. X光繞射分析儀. Duker. D8型. 掃描式電子顯微鏡. Hitachi. S-4800. 電化學分析儀. AUTOLAB. PGSTAT 320. 多功能電源電錶. Keithley. 2400型. 真空烘箱. DENG YNG. 高溫爐分解爐. TenOer. F-12-12. 超音波震盪洗淨器. DELTA. DC-400. 電子天平. Precisa. Cary 630. DOV30. XS365M. 磁石加熱攪拌器. CimarecTM. HP130910-33Q. 磁石加熱攪拌器. CORNING. PC-420D. 精密熱風循環烘箱. Binder. FD-23型. 加熱循環水槽. Julabo. MW-4型. 恆溫水循環機. EYELA. CCA-1111型. UV燈. 125W. 34.
(47) 3.2.2 實驗藥品 藥品. 化學式. 廠商. 純度 / 規格. 1-Bromobutane. C4H9Br. Alfa Aesar. 98+ % / 500mL. 1,4-Dibromobutane. C4H8Br2. Alfa Aesar. 98+% / 500mL. 1-Vinylimidazole. C5H5N2. Alfa Aesar. 99% / 100mL. 1-Bromooctane. C8H17Br. ACROS. 99% / 500mL. Methanol. CH3OH. AENCORE. 99.9% / 4L. Methanol. CH3OH. ECHO. 99.9% / 4L. 2-Propanol. C3H8O. ECHO. >95% / 20L. Acetone. C3H6O. ECHO. 95% / 20L. Ethanol. CH3CH2OH. ECHO. 95% / 20L. Ethyl ether. (C2H5)2O. ECHO. 99% / 20L. MERCK. ~250℃ / 1L. Silicon-Oil. 3.2.3 實驗步驟 3.2.3.1 含溴陰離子之高分子離子液體製備 首先,先合成出三種以溴離子為陰離子的含反應性官能團離子液體單 體,分別得到帶有丁基、辛基單反應性官能團的離子液體單體、以及雙反 應性官能團的離子液體單體。再分別均勻混合溶解後,加入適量的光起 始劑進行光聚合,得到四種不同分子結構的高分子離子液體,分別是到 帶有丁基及辛基的線性型高分子離子液體,以及將上述兩種單反應性官. 35.
(48) 能團單體,再添加雙反應性官能團的單體,形成兩種不同的具有架橋性 的高分子離子液體,再把這四種高分子離子液體去進行材料特性分析。. Table 3-1 離子液體單體與高分子離子液體的結構與命名。 離子液體單體與高分子離子液體的結構與命名. H2C. H2C. N. N. N. +. Br. +. N. -. H9 C 4. Br. -. H17C8. 1-vinyl-3-butyl-imidazolium bromide (IL-C4-Br-). 1-vinyl-3-octyl-imidazolium bromide (IL-C8-Br-). H2C. Br. -. +. N. N. N. +. N Br. -. CH2. 1-vinyl-3-[4-(1-vinyl-1H-imidazol-3-ium-3-yl)butyl]-1H-imidazol-3-ium dibromide (IL-C4(Crosslinker)-Br-). 36.
(49) H3C. H3C. n CH3. n CH3. N. N +. N. Br. H9C 4. +. N. -. H17C8. Poly(1-vinyl-3-butyl-imidazolium bromide) (PIL-C4-Br-). Br. -. Poly(1-vinyl-3-octyl-imidazolium bromide) (PIL-C8-Br-). H3C. N -. +. Br N. +. N. H3C. Br. n CH 3. -. N. n CH 3. Poly{1-vinyl-3-[4-(1-vinyl-1H-imidazol-3-ium-3-yl)butyl]-1H-imidazol-3-ium dibromide} (PIL-C4(Crosslinker)-Br-). 37.
(50) 3.2.3.2 具單一個雙鍵之離子液體單體合成 參考文獻[43]的合成步驟 H2C. H2C. 1-Bromobutane N. 15 houre, in methanol. N. N. N. +. Br. -. H9 C 4 H2C. H2C. 1-Bromooctane N. N. 15 hours,in methanol. N. N. +. Br. -. H17C8. (1) 取 0.2 mole 的 1-vinylimidazole 及 0.1mole 的 1-bromobutane 與 1bromooctane分別放置於兩個三頸瓶中。 (2) 分別加入30mL的methanol於三頸瓶中。 (3) 加熱至60℃,恆溫迴流反應15小時後,持續攪拌冷卻至室溫後。 (4) 在每分鐘5毫升的速度下,以1L的乙醚慢慢滴定至出現兩相分層。 (5) 取出下層液,靜置於抽風櫃抽氣5小時後放入真空烘箱靜置一天。 (6) 分別取得兩種透明黃色溶液。. 38.
(51) 3.2.3.3 具兩雙鍵之離子液體單體合成 參考文獻[43]的合成步驟 H2C. H2C Br. 1,4-Dibromobutane. N. -. +. N. N. N. N. 15 hours,in methanol. N. Br. +. -. CH2. (1) 取0.2 mole的1-vinylimidazole及0.1mole的1,4-dibromobutane放置於三 頸瓶中。 (2) 加入30mL的methanol於三頸瓶中。 (3) 加熱至60℃,恆溫迴流反應15小時後,持續攪拌冷卻至室溫後。 (4) 在每分鐘5毫升的速度下,以1L的乙醚慢慢滴定至出現兩相分層。 (5) 取出下層液,靜置於抽風櫃抽氣5小時後放入真空烘箱靜置一天。 (6) 取得白色塊狀固體產物。. 3.2.3.4 含溴陰離子之高分子離子液體製備 將上述三種離子液體單體分別混合成四種不同成分,以125W的UV燈 (固定高度=10公分)照光進行聚合。. 39.
(52) 3.2.3.4.1 含溴陰離子之線性結構固態高分子離子液體製備 H2C. H3C n CH3. acetone,photoinitiator N. N. N. UV light,6 hours. +. Br. +. N. -. Br. H9C 4. H9 C 4. -. H3C. H2C. n CH3. acetone,photoinitiator N. N. N. UV light,6 hours. +. Br. N. -. H17 C8. H17C8. +. Br. -. (1) 取0.004 mole的單體A及單體B,分別加入0.0002 mole的光起始劑後均 勻攪拌。 (2) 在塑膠培養皿上鋪一層保鮮膜,把(1)中的溶液倒在培養皿上,並使其 均勻擴散至整個圓表面。 (3) 在固定高度下(10公分),以UV燈照光,單體A正反面各照光2小時;單 體B正反面各照光1.5小時。 (4) 進行材料特性分析。. 40.
(53) 3.2.3.4.2 含溴陰離子之架橋性固態高分子離子液體製備 H2C. H2C. Br N. N. -. +. N. N N. N. Br. +. Br. +. (A). -. -. H9 C 4. CH2. H2C. H2C. Br N. N. -. +. N. N N. N. Br. +. Br. +. (B). -. -. H17C8. CH2. Table 3-2 具有架橋性之聚合後離子液體的結構。 具有架橋性之聚合後離子液體的結構. H3C. N -. Br N+. n CH 3. H3C n CH3. +. N. Br. N. -. +. H3C. N. N. H9C 4 n CH 3. (A) →(PIL-[C4+C4(Crosslinker)]-Br-). 41. Br. -.
(54) H3C. N -. +. Br N. n CH 3. H3C n CH3. +. N. H3C. Br. -. N. N. N H17 C8. +. Br. -. n CH 3. (B) →(PIL-[C8+C4(Crosslinker)]-Br-). (1) 取0.004 mole的單體A及單體B,分別加入0.0007 mole的單體C。 (2) 滴入0.025 mole的丙酮後,單體A+C加熱至90℃均勻攪拌至單體C完 全溶解;單體B+C則加熱至135℃均勻攪拌至單體C溶解。 (3) 放入烘箱中,加熱至50℃維持30分鐘。 (4) 拿出來後再加入0.0002 mole的光起始劑。 (5) 在塑膠培養皿上鋪一層保鮮膜,把(4)中的溶液倒在培養皿上,並使其 均勻擴散至整個圓表面。 (6) 在固定高度下(10公分),以UV燈照光,單體A+C正反面各照光9分鐘; 單體B+C正反面各照光25分鐘。 (7) 進行材料特性分析。. 42.
(55) 3.2.4 材料性質分析. 3.2.4.1 傅立葉轉換紅外線光譜儀(Fourier-Transform Infrared Spectrometer , FT-IR)分析 測量紅外線吸收及穿透光譜,樣品製備如下: (1) 將尚未聚合的液體,每一次皆滴入固定量於透明夾鍊袋中,並用相同 物品將其準確壓平,再進行光聚合,每個樣品皆於125W的UV燈下照 射3小時,形成稍有柔軟性的可透光的片狀薄膜,再將其剪裁成樣品槽 可適用的大小即可。 (2) 取適量的溴化鉀(KBr)和少許樣品混合,在研缽裡快速磨成細粉,再將 此混何物倒入壓錠的模具中,以油壓機施於壓力,即可得一透明薄膜。 將上述(1)和(2)放在儀器量測穿透光譜的樣品槽中固定,進行掃描之前, (1)樣品直接以空氣作為背景值,(2)樣品必須用純KBr薄片當作背景值先 掃描一次。(3)直接將樣品滴在鋪有一層保鮮膜的培養皿上成膜,形成可 撕下且較有厚度的膜,量測吸收光譜時利用ATR模式來量測樣品即可。 從4000到600cm-1 範圍之紅外光進行穿透式掃瞄即可得到結果。. 3.2.4.2 熱重分析 測量熱重分析儀時,樣品製備如下:成功製作出高分子膜後,先放置 室溫下1~2天(有些膜要放置更久),讓聚合後的膜因環境裡的水氣變軟, 可方便接下來的樣品製備,再取一小片將其先剪成小碎片,然後放在一 般研缽中仔細的研磨,研磨完成後會有如橡皮擦的皮屑般的樣品出現(為. 43.
(56) 符合TGA樣品的要求,必須將其研磨至均勻大小,以免有誤差值出現), 再放置在真空烘箱中乾燥,完成後即可取出進行TGA的量測。 先將陶瓷載台以小型噴火槍加熱,將載台內殘留灰燼燒掉後再以吸球 降溫至常溫,將兩邊載台皆放置加熱爐內之微量天平上進行校正,其校 正值必需在0.001mg以下,取出樣品載台將事先秤好的樣品放入,再放回 爐內之天平上記錄樣品重量,樣品重量以不超過5 mg為主,然後開始設 定溫度範圍、加熱速率及氮氣流量後即可開始量測。TGA分析參數:樣品 重量→5 mg;加熱速率→20℃/min;初始及終止溫度:40℃-600℃。. 3.2.4.3 示差掃描熱分析 樣品製備同TGA之樣品製備,下一步將樣品皆放入固態盤中,並確實 秤重至小數點後三位及記錄。接著進行機台暖機、除水等步驟,完成後, 在兩個載台上一邊放置空白片、一邊放置樣品,接著開始設定樣品重量 (樣品重量以不超過5 mg為主,以免爆盤汙染機台)、溫度範圍(最高不超 過裂解溫度為原則)、熱分析過程及氮氣流量。設定參數: (D)Ramp 10 °C/min to 295 °C→Ramp 10 °C/min to 40 °C ; (E) Ramp 10°C/min to 290°C→Ramp 10 °C/min to 40 °C;(G) Ramp 10 °C/min to 296 °C→Ramp 10°C/min to 40°C;(H) Ramp 10°C/min to 290°C→Ramp 10°C/min to 40°C。. 44.
(57) 3.2.4.4 X-光繞射分析 量測XRD的樣品必須是平整且厚度一致的膜(否則圖譜易傾斜),並且 在製作出高分子膜後,需放入烘箱高溫烘烤幾小時,將尚未聚合完全的 單體完全去除(以免汙染機台),完成後再取適當大小之樣品放置於標準載 台上進行量測。. 3.2.4.5 掃描式電子顯微鏡分析 SEM樣品必須是平整且厚度一致,進行量測之前必須先放入烘箱150 ℃高溫烘烤幾小時,將尚未聚合完全的單體完全去除(以免汙染機台),即 可取適當大小之樣品黏貼於標準載台上進行量測。另外,將離子液體在 鋁箔上成膜,可以幫助高分子膜量測時更加導電,拍攝出的畫面會更加 清晰。. 3.2.4.6 導電度測試 量測導電度時,樣品必須厚度一致,製備出不同聚合時間之高分子膜 後,剪裁出適當大小夾在兩根金屬圓柱之間,並連接Autolab電化學儀器, 進行定電壓(V)下電流的量測,並將電流值(I)記錄下來帶入下列公式,即 可得導電度。. σ(𝑆𝑖𝑒𝑚𝑒𝑛⁄𝑐𝑚) =. 1 𝑉 𝑏 𝑘×( )×𝑡×( ) 𝐼 𝑎. =. 1 𝜌(𝛺 − 𝑐𝑚). a = film long;b = film wide;k = 修正因子(4.5324);t=thickness 45.
(58) b. a t. Figure 3-1 薄膜的導電度公式示意圖。. 3.3 結果與討論 在本章節中所製備含溴陰離子的線性、交聯型固態高分子電解質膜中, 高 分 子 主 體 為 1- 乙 烯 基 咪 唑 基 ( 1-vinylimidazole ) , 以 1- 溴 丁 烷 (1bromobutane)及1-溴辛烷(1-bromooctane)作為取代基,在五元環的3位置 上分別接上丁基及辛基,加入起始劑後進行光聚合,形成兩種線性型固 態高分子膜,再添加以二溴丁烷合成有兩雙鍵之單體(白色固體)分別來交 聯兩種線性行固態高分子,形成有網狀結構之固態高分子膜。交聯劑 (crosslinking agent)會增加固態高分子膜的機械性質、熱安定性及玻璃轉 換溫度。本章針對含溴陰離子之線性、交聯型高分子離子液體膜之結構 與特性進行分析與探討,其探討焦點為: (1) 交聯後是否造成counter-ion運動行為的改變。 (2) 交聯後對熱分析結果的影響。 (3) 交聯後是否影響表面形貌、機械特性與高分子鏈之嵌段運動行為關係。 (4) 交聯後的結構變化與導電性質之關係。. 46.
(59) 3.3.1 傅立葉轉換紅外線光譜分析 由FTIR吸收光譜分析及參考文獻數據[44],可以明顯看到在 3394 cm-1 的位置有中等強度且寬廣的特徵鋒形,為 N - H 鍵的特徵吸收峰; 以及代表咪唑基的五元環中,1638 cm-1 峰值為環中的 C = C 拉伸鍵, 3065 cm-1 峰值則為環中C = C - H (sp2) 的拉伸鍵, 1544 cm-1 峰值為 C = N 的鍵結位置,1159 cm-1峰值為 C - N 的鍵結位置,以上四個峰值代 表結構中五元環的特徵吸收峰;還有,咪唑基五元環上的 R 取代基及 R1 取代基,分別是 2854 cm-1 、 2924 cm-1 及 2960 cm-1 三個峰值代表 C – C - H (sp3) 拉伸鍵結,1444 cm-1 峰值則表示取代基上 CH3 末端鏈的彎曲 鍵結位置;最後,600 cm-1 ~ 900 cm-1 這區域的鍵結,有可能是鹵素鍵結 在鍊末端,或是鹵素離子的存在產生[45]。. Figure 3- 2 以 Br– (溴陰離子)作為 counter-anion 結合對應的咪唑離子液體 聚合後的四種不同 PILs 之 FTIR 吸收光譜(分開疊圖)。. 47.
數據
![Figure 2-6 DSSC 工作原理示意圖。[32]](https://thumb-ap.123doks.com/thumbv2/9libinfo/8786697.218328/34.892.170.738.222.704/Figure26DSSC工作原理示意圖32.webp)
![Figure 2-7 布拉格定律示意圖[40]。](https://thumb-ap.123doks.com/thumbv2/9libinfo/8786697.218328/43.892.183.750.161.717/Figure27布拉格定律示意圖4.webp)
Outline
相關文件
Should an employer find it necessary to continue the employment of the Class A Foreign Worker(s), the employer shall, within four (4) months prior to the expiration of the
6 《中論·觀因緣品》,《佛藏要籍選刊》第 9 冊,上海古籍出版社 1994 年版,第 1
The prepared nanostructured titania were applied for the photoanodes of dye-sensitized solar cell.. The photoanodes were prepared by the doctor blade technique and the area
The research proposes a data oriented approach for choosing the type of clustering algorithms and a new cluster validity index for choosing their input parameters.. The
Wang, Solving pseudomonotone variational inequalities and pseudocon- vex optimization problems using the projection neural network, IEEE Transactions on Neural Networks 17
Hope theory: A member of the positive psychology family. Lopez (Eds.), Handbook of positive
Define instead the imaginary.. potential, magnetic field, lattice…) Dirac-BdG Hamiltonian:. with small, and matrix
Monopolies in synchronous distributed systems (Peleg 1998; Peleg