奈米樹狀高分子磁性複合金屬吸附貴重金屬之研究
1張俊祥、1林岱霖、2連興隆 1 國立高雄大學土木與環境工程學系 碩士班研究生 2國立高雄大學土木與環境工程學系 教授 NSC98-2221-E-390-008-MY3 摘要本研究的目的為利用奈米樹狀高分子複合磁性奈米顆粒 (Dendrimer-Magnetic Nano Particle-Gn,
MNP-Gn, n 為樹狀高分子之世代)吸附貴重金屬之研究,探討其吸脫附效率、複合材料的回收再利用 效率及回收貴重金屬之可行性。本研究利用複合材料 MNP-G3 吸附貴重金屬(Pd4+ 、Au3+ 、Ag+ ),探討 不同的水質參數及操作條件對吸附之影響,進而提升其可利用性及回收效率。磁性奈米顆粒 (Magnetic Nano Particle, MNP),製備過程容易,利用外加磁場,可快速回收。樹狀高分子 (Dendrimer) 是一種 三維立體結構的奈米材料,能夠有效率的吸脫附金屬離子,並且可以回收重複使用。本研究將 Dendrimer 鍵結在 MNP 上吸附金屬離子;在酸性條件下,將所吸附的金屬離子脫附,並且利用外加磁 場回收材料。本研究利用奈米樹狀高分子磁性複合金屬上述特性,進行吸附貴重金屬試驗。本研究主 要探討的影響因子包括貴重金屬種類與價數、材料用量及 pH 值。目前試驗濃度 5 g/L 的 MNP-G3 分 別吸附 20 mg/L 的 Au3+ 與 Pd4+ ,吸附效率可達 80%;並且與文獻中 MNP-G3 吸附效果最佳的 Zn2+ 在 相同濃度的競爭吸附時,仍具有不錯的吸附能力。 關鍵詞:奈米樹狀高分子、貴重金屬、吸附、回收再利用
一、前言及研究目的
一般我們所謂貴重金屬即金(Au)、銀(Ag)、 鈀(Pd)、鉑(Pt)、銠(Rh)、銥(Ir)、釕(Ru)、鋨(Os), 其中除了金、銀之外,其餘皆屬於白金族元素。 現 階 段貴 金屬 的主 要用途 除 了熟 知的 飾品 之 外,因為其特殊的材料特性,包含電子、電機、 化工、汽車、電鍍等產業中的觸媒、熱電偶及電 極材料都需要貴金屬,其使用於工業的數量大幅 度地超越原有的飾品用途,日本人甚至將黃金粉 末作為食品原料,因此貴金屬已經由原來的累積 保存便成大量的消耗。地球的資源有限而且珍 貴,在追求人類永續發展的前題下,開發與再生 利用是極為重要的[1]。磁 性 奈 米 顆 粒 (Magnetic Nano Particle, MNP) 為去除水中污染物之新穎材料,其製備方 式簡易,利用共沉澱法僅需使用亞鐵離子及鐵離 子混合溶液,調整 pH 值於鹼性條件下,便可以 製備出磁性奈米顆粒 (Fe3O4) 。國內研究中發 現,除本身可以吸附重金屬外,並具有利用外加 磁場,進行吸附後快速回收之優點[2]。 樹狀高分子 (Dendrimer) 是一種新穎奈米 材料,這種材料為三維立體結構,具有高分散 性、高反應性及可回收再利用等優點。根據研究 指出[3],樹狀高分子具快速及有效吸附金屬離子 之能力外,並且具有極佳之脫附能力,樹狀高分 子可重複使用。雖然樹狀高分子有上述優點,而 Diallo 等 人 提 出 利 用 超 微 聚 合 物 過 濾 機 制 (Polymer supported ultrafiltration, PSUF) 回收樹 狀高分子有上述優點[4],但是利用超微過濾膜 (ultrafiltration membrane) 方 式 回 收 , 其 單 價 昂 貴,就經濟層面而言,實際應用並不可行。 奈米樹狀高分子磁性複合金屬 (MNP-Gn, n 為樹狀高分子之世代)能處理重金屬污染水體,這 種複合材料能吸附水體中的重金屬離子,在酸性 條件下有極佳的脫附能力,並且利用磁性奈米顆 粒(MNP) 的特性,磁選分離,將重金屬離子從液 相轉移到固相,再利用 10 mL HCl (1%) 將吸附 的重金屬離子脫附濃縮,最後利用外加磁場將複 合材料回收[5]。 本研究欲將兩材料之優點吸附水體中貴重 金屬離子,藉由酸洗濃縮程序,將吸附於樹狀高 分子的貴重金屬脫附回收,最後再利用外加磁場 回收此複合材料,此複合材料具再利用及貴重金 屬濃縮之功能,降低材料成本,增加其應用性。
二、研究方法
2.1 實驗材料99.5%,廠牌:友合。甲醇 (methyl alcohol),化 學式:CH3OH,純度:99.5%,廠牌:Mallinckrodt Chemicals 。 甲 醇 (methyl alcohol) , 化 學 式 : CH3OH,純度:99.9%,廠牌:Sigma-Aldrich。 矽 烷 胺 基 (3-Aminopropyl-trimethoxysilian, ATPS),化學式:H2N(CH2)3Si(OCH3)3,純度:≧ 97.0%,廠牌:Fluka。乙二胺 (ethylenediamine), 化學式:NH2CH2CH2NH2,純度:≧99%,廠牌: Aldrich。丙烯酸甲酯 (methylacrylate),化學式: C4H6O2,純度:≧99%,廠牌:Fluka。含水氯化 鐵 (chloride hexahydrate),化學式:FeCl3‧6H2O, 純度:97%,廠牌:Showa。含水硫酸鐵 (Iron(II) sulfate heptaphydrate),化學式:FeSO4‧7H2O, 純度:99%,廠牌:Showa。氨水 (ammonium hydroxide),化學式:NH4OH,純度:29%,廠 牌:Tedia。氯化鋅 (zinc chloride),化學式: ZnCl2,純度:98%,廠牌:Riedel-dehaen。硝酸 銀 (Silver Nitrate),化學式:AgNO3,純度: 99.8% , 廠 牌 : Showa 。 三 水 合 四 氯 金 酸 (Hydrogen tetrachloroaurate(III) trihydrate),化學 式:HAuCl4‧3H2O,純度:99%,廠牌:Acros Orcanics 。 六 氯 鈀 酸 鉀 (Potassium hexachloropalladate(IV)),化學式:K2PdCl6,純 度:99%,廠牌:Aldrich。 醋酸鈀 (Palladium (II) Acetate, trimer),化學式:[PdC2H3O2]3,純度: 47%,廠牌:Anlace。去離子水 (de-ionic water), 15 mΩ/cm。
2.2 儀器分析方法
感應耦合電漿光譜儀 (ICP)
為了解 MNP-Gn 吸附及脫附之金屬濃度變 化,故於實驗期間取出適量水樣稀釋,並利用 Perkin Elmer, Optima 2000DV, ICP (Optical Emission Spectrometer) 量測。試驗主要參考環保 署 「水中金屬及微量元素檢測方法-感應耦合電 漿質譜法」,將稀釋水樣經 0.2 μm 之濾紙過 濾,實際濃度在依稀釋倍數得知。 2.3 材料製備 2.3.1 製備 Fe3O4 磁性奈米顆粒 (MNP) 鑑於先前所探討,Dendrimer 已證實可以鍵 結重金屬離子,但其後續收集仍嫌繁雜,故欲利 用磁鐵有磁性特性,將 Dendrimer 鍵結在磁性顆 粒上,藉此提高回收效率及有效降低成本。 本研究所使用之四氧化三鐵磁性奈米顆粒 MNP (magnetic nano particle) 配製方法,主要是參考 文獻做法[6],首先使用 Fe3+ 和 Fe2+以比例為 2:1 先進行水溶液混合,當混合均勻後再加入強 鹼水溶液 (NaOH 或是 NH4OH) 調整 pH 值約為 10,於定溫 80 度下混合攪拌 30 分鐘後冷卻, 最後用去離子水和乙醇沖洗幾次即完成所需四 氧化三鐵 (Fe3O4) 膠體材料。製備完成後將膠體 置於厭氧環境下吹乾,以利後續批次、合成實驗 備用,合成方程式及步驟如下:
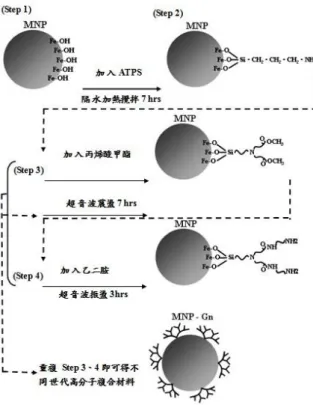
2FeCl3+FeCl2+8NH3+4H2O→Fe3O4+ 8NH4Cl (1) 1. 將 FeSO4‧7H2O 及 FeCl3‧6H2O 粉末分別定 量於 100 mL 的去離子水中,溶解後在混合攪拌 (pH=1.6)。 2. 攪拌過程加入氨水 (NH4OH) 使 pH=10。 3. 將此溶液於加熱攪拌器上定溫 80 ℃攪拌 30 分鐘。 4. 完成上述步驟後將此溶液靜置冷卻,在利用去 離子水及乙醇沖洗數次,使最後 pH 約為 8.9 左右。 5. 完成以上步驟經厭氧環境下風乾即可得磁性 奈米顆粒粉末。 2.3.2 奈米樹狀高分子複合磁性金屬 (MNP-Gn) 目前已知 Dendrimer 對於水中金屬之吸附效 果 相 當好 ,但 於回 收方法 依 舊以 超微 過濾 膜 (ultrafiltration membrane) 為主流,但此過濾膜單 價高,在實際運用上極為不便,故欲利用 MNP 帶有磁性之特性,將 Dendrimer 鍵結於四氧化三 鐵 (Fe3O4) 表面,最終回收只要利用磁力回收即 可,其合成示意圖及步驟主要如圖 1 所示: 1. 取吹乾之 MNP 粉末 2.5 g,利用乙醇定量至 200 mL,並加入 10 mL 矽烷胺基。 2. 利用磁石攪拌器搭配冷凝管定溫 60 ℃ 攪拌 7 小時,使其完全分散於乙醇中,完成後利用甲 醇沖洗即得零世代 MNP 膠體,隨即將此利用氮 氣吹乾以利後續定量使用。 3. 將製備好零世代 MNP 定量至 50 mL 甲醇中並 加入 20 mL 丙烯酸甲酯,利用超音波震盪 7 小 時,使其完全混合及反應均勻。完成後利用甲 醇沖洗五次,即可得半世代 (G 0.5 n) MNP 顆 粒。 4. 將上述半世代膠體顆粒再定量至 20 mL 甲醇 並加入 10 mL 乙二胺,利用超音波震盪 3 小 時。完成後,再利用甲醇沖洗三次,即得全世 代 (Gn) MNP 顆粒。 5. 將 3 及 4 步驟重複配製,即可得到不同世代之 磁性奈米顆粒。
圖 1.磁性奈米顆粒製備流程圖 2.3.3 酸洗程序 MNP-Gn 經酸洗程序後,不會破壞磁性奈米 顆粒與樹狀高分子之鍵結,並且證實經酸洗過後 之材料,確實可以提升吸附效率,而且藉由此前 置酸洗步驟,去除附著於官能基表面之雜質,並 可有效回復原本表面官能基吸附位址。其酸洗程 序做法如下:將 MNP-Gn 0.5 g 置於 50 mL D.I. Water,添加 HCl 使水中 pH = 3,然後經固液分 離並用去離子水沖洗數次後,即可使用。 2.4 批次實驗 實驗於室溫 25 ℃、165 mL 之血清瓶中進 行,並將血清瓶置於水平震盪儀上,以震盪速率 175 rpm 使水樣充分混合反應。每次使用複合材 料重量為 0.5 g,水樣體積為 100 mL,調整不同 濃度的金屬水樣、pH 進行批次試驗。實驗中, pH 調整將使用 NaOH 和 HCl 之稀釋溶液調整, 並於固定之採樣時間由反應系統中取 1 mL 水樣 稀釋以 ICP 分析之。
三、結果與討論
3.1 吸附能力試驗 本次試驗中,使用文獻中吸附重金屬能力最 好的 MNP-G3 對貴重金屬 Pd4+ 、Au3+ 進行吸附能 力試驗[7]。使用材料為 0.5 g,試驗環境以 pH 6.5 及 Pd4+ 、Au3+ 金屬濃度 20 mg/L 進行實驗。 實驗結果顯示,當試驗環境於 pH6.5,Pd4+、 Au3+濃度為 20 mg/L 時, 吸附效率都可達 80%, 而且可以發現反應皆在短時間 (約 4 hr) 就有效 果,結果證實 MNP-G3 對貴重金屬 Pd4+、Au3+具 有明顯的吸附能力。 3.2 水中 pH 值對 MNP-G3 吸附之影響 探討在不同 pH 值下,複合材料對貴重金屬 Pd4+、Au3+吸附能力影響。使用材料為 MNP-G3 0.5 g,試驗環境以 pH 6.5、pH 4 及 Pd4+、Au3+ 金 屬濃度 20 mg/L 進行實驗。 圖 2. MNP-G3 於 pH 6.5 與 pH 4 吸附 Pd4+試驗 圖 3.MNP-G3 於 pH 6.5 與 pH 4 吸附 Au3+ 試驗 圖 4.MNP-G3 於 pH 6.5 與 pH 4 吸附 Ag+試驗 實驗結果由圖 2、圖 3 與圖 4 可以觀察出,當 試驗環境為 pH 6.5 ,MNP-G3 的吸附效果明顯 優於 pH 4, 可以得知 MNP-G3 在偏中性的條件 下吸附能力較佳。文獻指出在低 pH 條件下,樹 狀高分子本身不利於錯合反應進行,因其 –NH2 官能基在酸性條件下易被質子化成 –NH3 + 官能 基,故不利於帶正電的金屬離子吸附[8] ;文獻 中 MNP-G3 界達電位的結果也顯示其等電點約 為 pH 6.2[9],故當 pH 小於 6.2 時,其表面帶正 電,反之則帶負電,與實驗結果相符。3.3 競爭吸附試驗 由於廢水中不只存在單一金屬離子,而且貴 重金屬離子的量一定會明顯低於一般重金屬離 子,所以該試驗的目的為探討金屬離子間的競爭 吸附情形,使用文獻中吸附效果最好的 Zn2+、與 貴重金屬離子做競爭吸附比較。 使用吸附貴重金屬能力最好的 MNP-G3 對濃 度皆為 20 mg/L 的 Zn2+ 、Pd4+ 、Au3+ 、Ag+ 進行競 爭吸附試驗。使用材料為 MNP-G3 0.5 g,試驗環 境以 pH 6.5 進行。 圖 5. MNP-G3 於相同濃度競爭吸附試驗(pH 6.5) 實驗結果由圖 5 可以觀察出,當試驗環境於 pH 6.5 時,Zn2+、Pd4+ 、Au3+ 的吸附效率較佳可以 達到 60%, Ag+吸附效率較差只有約 40%,結 果證實在同濃度的競爭吸附下,MNP-G3 對貴重 金屬 Pd4+、Au3+具有不錯的吸附能力。 因為廢水中含有大量的重金屬離子,而貴重 金屬離子的含量較低,因此使用吸附貴重金屬能 力最好的 MNP-G3 對濃度皆 200 mg/L 的 Zn2+與 20 mg/L 的 Pd4+、Au3+ 、Ag+ 進行競爭吸附試驗。 使用材料為 MNP-G3 0.5 g,試驗環境為 pH 6.5。 圖 6. MNP-G3 於不同濃度競爭吸附試驗(pH 6.5) 實驗結果由圖 6 可以觀察出,可以發現反應 在高濃度的 Zn2+ 存在時,對貴重金屬離子的吸附 效率非常 有限,且對 Zn2+的吸附效率約只有 10%,結果證實 MNP-G3 在高濃度的重金屬離子 存在下,對貴重金屬的競爭吸附影響顯著,但是 對 Zn2+也只有約 10%的吸附效率,而對貴重金屬 則看不出明顯的吸附情形。
四、結論
由於 Pd4+在 pH=7 時有沉澱行為產生,故後 續實驗時將 pH 調整至 6.5,而從 MNP-G3 吸附 Au3+與 Pd4+ 的結果來看,MNP-G3 具有不錯的吸 附效果,使用材料 0.5 g、 pH 6.5 時,吸附效率 可達 80%。 從貴重金屬單獨與鋅競爭吸附時,競爭吸附 情形較不顯著,但是在材料 0.5 g、 pH 6.5 時, 貴重金屬的吸附能力為 Pd4+ >Au3+ > Zn2+ >Ag+, 鋅離子的存在會降低貴重金屬的吸附量,但是貴 重金屬還是具有較佳的吸附能力,且貴重金屬的 總 吸 附量 也明 顯大 於鋅的 吸 附量 ,可 以發 現 MNP-G3 對貴重金屬有較好的吸附效果。參考文獻
[1] 廖南吉 (1988 ),貴金屬之化學及回收法,南 台圖書公司,15-33。 [2] 陳珮紋、秦靜如 (2005)利用利用 Fe3O4 磁 性顆粒處理化學機械研磨廢水,奈米研討會論文 集,85-92。[3] Xu, Y. and Zhao, D. (2005) Removal of copper from contaminated soil by use of poly (amidoamine) dendimers. Environ. Sci. Technol. 39, 2369-2375. [4] Diallo, M.S., Balogh, L., Shafagati, A., Johnson, J.H. Jr., Goddard, W.A. and Tomalia, D.A. (1999) Poly (amidoamine) dendrimer : A new class of high capacity chelating agents for Cu (II) ions. Environ. Sci. Technol. 33, NO5.
[5] 周志明 (2009) 奈米樹狀高分子複合磁性金 屬吸附眾金屬之研究,國立高雄大學土木與環境 工程研究所,碩士論文。
[6] Enzel, P., Adelman, N., Beckman, K.J., Campbell, D.J., Ellis, A.B. and Lisensky, G.C. (1999) Preparation of an aqueous-based ferrofluid. J. Chem. Educ. 76, 943.
[7] Chou, C.M. and Lien, H.L. (2010) Dendrimer conjugated magnetic nanoparticles for removal of zinc (II) from aqueous solutions. J Nanopart Res. DOI 10.1007/s11051-010-9967-5.
[8] Diallo, M.S., Balogh, L., Shafagati, A., Johnson, J.H. Jr., Goddard, W.A. and Tomalia, D.A. (1999) Poly (amidoamine) dendrimer : A new class of high capacity chelating agents for Cu (II) ions. Environ. Sci. Technol. 33, NO5.
[9]Pan, B.F., Gao, F. and Gu, H.C. (2005) Dendrimer modified magnetic nanoparticles for protein immobilization. J. Colloid Interface Sci. 284, 1-5.