國 立 交 通 大 學
應用化學研究所
碩士論文
新穎供真空紫外光激發螢光體製備與發光特性之研究
Synthesis and Luminescence Characterization of Novel
Phosphors for Vacuum Ultraviolet Excitation
研究生:鍾秀佩
指導教授:陳登銘 博士
新穎供真空紫外光激發螢光體製備與發光特性之研究
研究生:鍾秀佩 指導教授:陳登銘 博士
國立交通大學應用化學研究所
摘要
本 論 文 利 用 固 態合 成 法 於氫 氣 的 還原 氣 氛 下, 成 功 合成 了 YBa3(BO3)3:Tb 3+ 、 Ca5Al6O14:Eu 2+ 、 MCaPO4:Eu 2+ (M = Na, K) 、 Li4SrCa(SiO4)2:Eu 2+ 與 LiZnBO3:Mn 2+ 等五系列螢光體,並利用 X 光粉 末繞射及掃描式電子顯微鏡進行結構鑑定及晶相分析,並使用國家同 步輻射研究中心所提供的真空紫外光光源,以探討各螢光體於波長 147 nm 及 172 nm 的激發下,其所表現的發光特性和能量轉移機制, 詴圖開發新穎且應用於電漿平面顯示器的螢光材料。 YBa3(BO3)3:Tb 3+ 為源自於 Tb3+的 5 D4→ 7 F5躍遷的窄峰放射,放射 波長為 543 nm。此系列中,主體因含有硼酸根 BO3 3-陰離子團,因此 可以有效吸收真空紫外光光源,並且與活化劑之間表現了良好的能量 傳遞現象。 Ca5Al6O14:Eu 2+ 、NaCaPO4:Eu 2+ 、KCaPO4:Eu 2+ 及 Li4SrCa(SiO4)2: Eu2+等螢光體皆來自 Eu2+的 4f65d1→4f7躍遷之寬帶放射,放射波長隨 主體及結晶場環境而不同。其中,研究發現 Ca5Al6O14:Eu 2+ 主體對真II 空紫外光源的吸收度相當良好,但由於晶格中過短的 Ca-Ca 距離,使 得濃度淬滅效應特別顯著。而 KCaPO4:Eu 2+ 及 Li4SrCa(SiO4)2:Eu 2+的主 體於真空紫外光的吸收度較低或因主體與活化劑之間能量傳遞效率 低,因此降低了螢光體發光強度。 LiZnBO3:Mn 2+之發光也為寬帶放射,但由於主體吸收光源的效率 低,且 Mn2+ 的激發為 d-d 躍遷,因此發光強度較(Y,Gd)BO3:Eu 3+商品 為弱。
Synthesis and Luminescence Characterization of Novel
Phosphors for Vacuum Ultraviolet Excitation
Student:Hsiu-Pei Chung Advisor:Dr. Teng-Ming Chen
Institue of Applied Chemistry National Chiao Tung University
Abstract
The thesis attempts to investigate novel phosphors for the application in Plasma Display Panel. The novel vacuum ultraviolet (VUV) excited phosphors with chemical compositions of YBa3(BO3)3:Tb
3+ , Ca5Al6O14:Eu 2+ , NaCaPO4:Eu 2+ , KCaPO4:Eu 2+ , Li4SrCa(SiO4)2:Eu 2+ and LiZnBO3:Mn 2+
were successfully synthesized by solid state method. X-ray diffraction and electron microscopy were used to verify the phase purity, respectively. By using synchrotron radiation as a light source, photoluminescence spectra were used to study the luminescence performance and energy transfer mechanism of the phosphors.
We found under 172 nm excitation, YBa3(BO3)3:Tb 3+
phosphors
showed a intense and sharp yellowish-green emission at 543 nm
corresponding to the electric dipole 5D4 → 7
F5 transition of Tb 3+
. The observation can be rationalized by the presence of BO3
anionic group in the host that generally shows strong absorption in the VUV region. In
IV
addition, such good energy transfer efficiency is observed from host to activator Tb3+. Ca5Al6O14:Eu 2+ , NaCaPO4:Eu 2+ , KCaPO4:Eu 2+ and Li4SrCa(SiO4)2:
Eu2+ phosphors showed the broad emission due to the well-known transitions between the ground state 4f7 and the crystal-field split 4f65d configuration, which is strongly affected by the environments surrounding Eu2+ ions. It is found that the host of Ca5Al6O14:Eu
2+
absorbed the excitation energy efficiently, but the unusual short Ca-Ca distances lead to significant fluorescence quenching. Furthermore, the observed reduced PL intensity of KCaPO4:Eu
2+
and Li4SrCa(SiO4)2:Eu 2+
may correspond to the poor host absorption of VUV radiation and/or the low efficiency of energy transfer between host and Eu2+.
The spectroscopic results of LiZnBO3:Mn
2+
red phosphor also showed the broad emission with lower intensity, which affiliated with the 3d–3d forbidden transitions of Mn2+.
誌 謝
在螢光體實驗室兩年的碩士學程,即將劃上句點。本論文能順利 完成,幸蒙指導教授陳登銘老師兩年來對學生的指導跟教誨,於此獻 上最深的謝意。口詴期間,感謝口詴委員張學明主任、裘性天老師與 李積琛老師的蒞臨及論文疏漏處的指正,使得本論文更加完備。此外, 感謝同步輻射研究中心鄭炳銘老師提供光源以及儀器量測設備。 這兩年來,非常感謝這間開朗又溫馨的實驗室;謝謝親愛的佳蓁 姊姊、貴人學長德文以及同窗摯友雅容、思琦與七七的一路扶持與鼓 勵;還有阿吉與阿豪學長在實驗上的幫助;政玄、子蘊、阿婉、小拉 及小mo,可以當妳們的學妹我真的覺得很幸運;以及yoyo、晏瑩、 婉妤、阿專、毓傑、小P 和阿啾,真的很開心可以認識你們。 好朋友阿龍、麻吉俊明、家瑜、阿伯學長、阿ken、緯經、君君、 祥文哥、會長凱捷及室友春慈,與拉亞好朋友KB、小豪、小傅、雅 萍、蛋頭及曉微,感謝你們的陪伴,讓我在交大的最後一年留下了很 多很棒的回憶,我永遠記得!也謝謝佑佑哥哥這些時間的呵護陪伴。 此外,感謝所有陪我最久的寶貝小天使們,小婁、昆宏、奶壞、 舜傑、呆農、總統、Hebe、小關、兔寶、小可及毛驢,謝謝體貼又可 愛的你們,跟你們在一起是我最開心的日子。 最後,將特本文獻給我最愛的家人,感謝您們對我的養育及栽培。VI 總 目 錄 中文摘要………...I 英文摘要………...III 誌謝..………..………V 總目錄..………VI 表目錄..………IX 圖目錄..………X 第一章 緒論 ..………...………………1 1-1 前言…….………1 1-2 研究動機………2 第二章 背景簡介..………...……….………………4 2-1 真空紫外螢光材料簡介………....…………4 2-2 真空紫外螢光材料之發光機制………....…………8 2-3 真空紫外螢光材料之設計……….………9 2 - 4 稀 土 離 子 能 譜 … … … . 1 0 2 - 5 濃 度 淬滅 效應 … …… … …… …… … …… … …… .. . .. .. . .. .. . .. . .. .. . .. .. 1 5 2 - 6 同 步 幅 射 光 源 … … … . 1 6 第 三 章 主 體 晶 體 結 構 簡 介 … … … 1 8 3-1 YBa3(BO3)3……….18 3-2 Ca5Al6O14………19 3-3 NaCaPO4……….21 3-4 KCaPO4………...22 3-5 Li4SrCa(SiO4)2………...……….23 3-6 LiZnBO3………..24 第四章 實驗方法………………26 4-1 實驗藥品………………………….26 4-2 儀器設備……….28 4-3 實驗步驟與流程……….31 4-3-1 YBa3(BO3)3:Tb3+螢光體之合成………..32
4-3-2 Ca5Al6O14:Eu2+螢光體之合成 ………...………..33 4-3-3 NaCaPO4:Eu2+螢光體之合成………...……..34 4-3-4 KCaPO4:Eu2+螢光體之合成……….…….35 4-3-5 Li4SrCa(SiO4)2:Eu2+螢光體之合成………..……..36 4-3-6 LiZnBO3:Mn2+螢光體之合成………...37 第五章 結果與討論………………38 5-1 YBa3(BO3)3:Tb3+螢光體之研究……….…………………...38 5-1-1 主體合成與晶相分析………..………...40 5-1-2 螢光光譜與發光特性分析……….………...41 5-1-2-1 光致發光光譜之研究……….……….41 5-1-2-2 激發光譜之研究……….………46 5-1-3 CIE 色度座標之分析……….……….50 5-1-4 掃描式電子顯微鏡影像分析……….………...52 5-2 Ca5Al6O14:Eu2+螢光體之研究……….………..53 5-2-1 主體合成與晶相分析……….………...53 5-2-2 螢光光譜與發光特性分析……….………...55 5-2-2-1 光致發光光譜之研究……….……….55 4-2-2-2 激發光譜之研究……….………62 5-2-3 CIE 色度座標之分析……….……….64 5-2-4 掃描式電子顯微鏡影像分析……….………...66 5-3 NaCaPO4:Eu2+螢光體之研究……….………...67 5-3-1 主體合成與晶相分析………..………...67 5-3-2 螢光光譜與發光特性分析……..………...69 5-3-2-1 光致發光光譜之研究……….………...69 5-3-2-2 激發光譜之研究……….………..75 5-3-3 CIE 色度座標之分析……….77 5-3-4 掃描式電子顯微鏡影像分析……….…………...79
VIII 5-4 KCaPO4:Eu2+螢光體之研究……….………80 5-4-1 主體合成與晶相分析………...80 5-4-2 螢光光譜與發光特性分析………...81 5-4-2-1 光致發光光譜之研究……….81 5-4-2-2 激發光譜之研究………....84 5-4-3 CIE 色度座標之分析……….86 5-4-4 掃描式電子顯微鏡影像分析………...88 5-5 Li4SrCa(SiO4)2:Eu2+螢光體之研究………..89 5-5-1 主體合成與晶相分析………...89 5-5-2 螢光光譜與發光特性分析………...91 5-5-2-1 光致發光光譜之研究……….91 5-5-2-2 激發光譜之研究………93 5-5-3 CIE 色度座標之分析……….95 5-5-4 掃描式電子顯微鏡影像分析………...97 5-6 LiZnBO3:Mn2+螢光體之研究………..98 5-6-1 主體合成與晶相分析………...98 5-6-2 螢光光譜與發光特性分析………...99 5-6-2-1 光致發光光譜之研究……….99 5-6-2-2 激發光譜之研究……….….101 5-6-3 CIE 色度座標之分析………...103 5-6-4 掃描式電子顯微鏡影像分析……….105 第六章 結論………..106
表 目 錄
表 2-1 已開發之 PDP 螢光粉性質之比較...7
表 5-1 YBa3(BO3)3: x%Tb3+系列螢光粉 CIE 色度座標之比較………..51
表 5-2 Ca5Al6O14: x% Eu2 +系列螢光粉 CIE 色度座標之比較...65
表 5-3 NaCaPO4: x%Eu2 +系列螢光粉 CIE色度座標之比較...78
表 5-4 KCaPO4: x%Eu2 +系列螢光粉 CIE 色度座標之比較...87
表 5-5 Li4SrCa(SiO4)2: x%Eu2 +系列螢光粉 CIE 色度座標之比較………96
圖 目 錄
圖 2-1 交流電漿顯示器面板結構剖面圖...4
圖 2-2 紅色螢光粉(Y,Gd)BO3:Eu3+和 Y2O3:Eu3+之激發光譜...5
圖 2-3 擴展到 70,000cm-1的Dieke Diagram (2000)………..12 圖2-4 高濃度時Tb3+離子發生交叉弛豫之螢光淬滅示意圖...14 圖 2-5 高濃度活化劑造成螢光體濃度淬滅成因示意圖...16 圖 2-6 新竹國家同步輻射研究中心的加速器系統...17 圖 3-1 YBa3(BO3)3晶體結構示意圖...19 圖 3-2 YBa3(BO3)3沿著 c 軸方向俯視的排列示意圖...19 圖 3-3 Ca5Al6O14 晶體結構示意圖...21 圖 3-4 NaCaPO4 晶體結構示意圖...22 圖 3-5 KCaPO4 晶體結構示意圖...23 圖 3-6 Li4SrCa(SiO4)2晶體結構示意圖...24 圖 3-7 LiZnBO3沿著 a 軸方向俯視的排列示意圖...25
圖 4-1 國家同步輻射研究中心(NSRRC) BL03A (HF-CGM High Flux Beamline) 紫外-可見光光譜儀實驗裝置...30 圖 5-1 於 1100℃下所製備 YBa3(BO3)3之 X 光粉末繞射圖譜...38 圖 5-2 不同 Tb3+濃度取代(Y 1-xTbx)Ba3(BO3)3XRD 圖譜之比較...39 圖 5-3 YBa3(BO3)3發光光譜...40 圖 5-4 (Y0.99,Tb0.01)Ba3(BO3)3發光光譜...41 圖 5-5 (Y0.9Tb0.1)Ba3(BO3)3發光光譜...42 圖 5-6 不同 Tb3+濃度摻雜之 YBa 3(BO3)3: x%Tb3+發光光譜………..…43
圖 5-7 (Y0.7Tb0.3)Ba3(BO3)3與 Zn2SiO4:Mn2+商品發光光譜之比較...44
圖 5-8 不同 Tb3+濃度摻雜的 YBa 3(BO3)3: x%Tb3+與 Zn2SiO4:Mn2+商品發光光 譜之比較……..………..………..………44
圖 5-9 YBa3(BO3)3: x%Tb3+系列螢光粉其光致發光強度與相對輝度與 Tb3+濃 度之關係...45 圖 5-10 YBa3(BO3)3激發光譜...46 圖 5-11 (Y0.7Tb0.3)Ba3(BO3)3之激發光譜圖...48 圖 5-12 不同 Tb3+摻雜濃度之(Y 1-xTbx)Ba3(BO3)3激發光譜之比較...49
圖 5-13 (Y0.7Tb0.3)Ba3(BO3)3螢光粉與 Zn2SiO4:Mn2+商品之 CIE 色度座標之比
較..………..…………51 圖 5-14 (Y0.7Tb0.3)Ba3(BO3)3之 SEM 影像...52
圖 5-15 於 1200℃下所製備 Ca5Al6O14之 X光粉末繞射圖譜...53 圖 5-16 不同 Eu2+濃度取代(Ca 1-xEux)5Al6O14之 XRD圖譜...54 圖 5-17 Ca5Al6O14發光光譜……….55 圖 5-18 (Ca0.999Eu0.001)5Al6O14及(Ca0.98Eu0.02)5Al6O14之發光光譜...56 圖 5-19 不同 Eu2+濃度摻雜之 Ca 5Al6O14: x %Eu2+發光光譜……….57 圖 5-20 (Ca0.97Eu0.03)5Al6O14發光光譜之解析...58 圖 5-21 (Ca0.99Eu0.01)5Al6O14與 BAM 商品發光光譜之比較圖...59 圖 5-22 不同 Eu2+摻雜濃度的 Ca 5Al6O14: x%Eu2 +與 BAM 商品發光光譜 之比較...59 圖 5-23 Ca5Al6O14: x%Eu2 +系列螢光粉其光致發光強度與相對輝度與 Eu2+濃 度之關係………..61 圖 5-24 Ca5Al6O14激發光譜……….62 圖 5-25 (Ca0.99Eu0.01)5Al6O4之激發光譜………..……63
圖 5-26 (Ca0.99Eu0.01)5Al6O14螢光粉與 BAM 商品 CIE色度座標之比較…...……65
圖 5-27 (Ca0.99Eu0.01)5Al6O14之 SEM 影像……...………...……….66 圖 5-28 於 1100℃下所製備 NaPO4之 X光粉末繞射圖譜……….…………...…..67 圖 5-29 不同 Eu2+濃度取代 Na(Ca 1-xEux)PO4XRD 圖譜之比較………68 圖 5-30 NaCaPO4發光光譜………..69 圖 5-31 不同 Eu2+濃度之 Na(Ca 1-xEux)PO4發光光譜………..70
圖 5-32 Na(Ca0.99Eu0.01)PO4與 Na(Ca0.94Eu0.06)PO4發光光譜之比較……….71
圖 5-33 不同 Eu2+濃度之 NaCaPO
4: x %Eu2+發光光譜………...72
圖 5-34 Na(Ca0.98Eu0.02)PO4發光光譜之解析………..………73
圖 5-35 NaCaPO4:Eu2+與 Zn2SiO4:Mn2+商品發光光譜之比較………..…….74
圖 5-36 NaCaPO4: x%Eu2 +光致發光強度與相對輝度與 Eu2+濃度之關係…..….74
圖 5-37 NaCaPO4激發光譜………..75
圖 5-38 Na(Ca0.98Eu0.02)PO4激發光譜………..76
圖 5-39 Na(Ca0.98Eu0.02)PO4螢光粉與 Zn2SiO4:Mn2+商品 CIE色度座標之比較...78
圖 5-40 Na(Ca0.98Eu0.02)PO4之 SEM 影像……….79
圖 5-41 於 1050℃下所製備 KCaPO4之 X光粉末繞射圖譜…...………80 圖 5-42 KCaPO4發光光譜………81 圖 5-43 不同 Eu2+濃度之 K(Ca 1-xEux)PO4發光光譜………82 圖 5-44 不同 Eu2+濃度之 KCaPO 4: x %Eu2+發光光譜………83 圖 5-45 KCaPO4: x%Eu2 +光致發光強度與相對輝度與 Eu2 +濃度之關係………84 圖 5-46 KCaPO4激發光譜………85 圖 5-47 K(Ca0.98Eu0.02)PO4激發光譜………86
圖 5-48 K(Ca0.98Eu0.02)PO4與 Zn2SiO4:Mn2+商品 CIE色度座標之比較………….87
圖 5-49 K(Ca0.98Eu0.02)PO4之 SEM 影像…...………...88
圖 5-50 於 750℃下所製備 Li4SrCa(SiO4)2之 X 光粉末繞射圖譜………..89 圖 5-51 不同 Eu2+濃度取代 Li 4(Sr1-xEux)Ca(SiO4)2XRD 圖譜之比較………90 圖 5-52 Li4SrCa(SiO4)2發光光譜……….91 圖 5-53 不同 Eu2+濃度摻雜之 Li 4SrCa(SiO4)2: x%Eu2+發光光譜………...92 圖 5-54 Li4SrCa(SiO4)2: x%Eu2+發光強度與相對輝度與 Eu2+濃度之關係……...93 圖 5-55 Li4SrCa(SiO4)2發光光譜……….94 圖 5-56 Li4(Sr1-xEux)Ca(SiO4)2發光光譜……….94
圖 5-57 Li4(Sr0.98Eu0.01)Ca(SiO4)2螢光粉與 BAM 商品 CIE 色度座標之比較…...96
圖 5-59 於 900℃下所製備 Li(Zn0.99Mn)BO3之 X光粉末繞射圖譜………...98 圖 5-60 LiZnBO3發光光譜………...99 圖 5-61 不同 Eu2+濃度摻雜之 LiZnBO 3: x%Mn2+發光光譜…………....……….100 圖 5-62 LiZnBO3: x%Mn2+發光強度與相對輝度與 Mn2+濃度之關係…………101 圖 5-63 LiZnBO3發光光譜……….102 圖 5-64 Li(Zn0.99Eu0.01)BO3發光光譜………....102
圖 5-65 Li(Zn0.99Eu0.01)BO3螢光粉與(Y,Gd)BO3:Eu3+商品 CIE 色度座標之比
較………104 圖 5-66 Li(Zn0.99Eu0.01)BO3之 SEM 影像…...………105
緒論
1-1 前言
螢光粉被應用在發光和顯示產品上,已達半個世紀之久。各類型 螢光粉由於激發和放光波段不同其應用十分廣泛,包括從早期的日光 燈、霓虹燈等照明設備,一直到目前備受矚目的電子顯示器。就白光 發光二極體(White Light-Emitting Diode, LED)而言,其輕巧及壽命 長的優點,將取代過去的照明設備,而電子顯示器是所有螢光粉產業 中發展最為迅速的,其中陰極射線管(Cathod Ray Tube, CRT)長久 以來位居顯示器的首位。近年來隨著市場需求,省空間之平面顯示器
陸續被開發且商品化,如:液晶顯示器(Liquid Crystal Display, LCD)、
場發射顯示器(Field Emission Display, FED)、電致發光平面顯示器 ( Electroluminescent Display, ELD)、電漿顯示器(Plasma Display Panel, PDP)等,陰極射線管的地位已不復從前。這也突顯了螢光粉 在光電元件應用上所扮演角色的重要性。而電漿平面顯示器(PDP)由 於具備大尺寸、寬廣的視角、高對比、高解析度、快速反應時間、平 面畫面、無磁場干擾,及超薄體積等優點,因此在眾多大面積平面顯 示器中,PDP 仍佔有一定的市場比例。而 PDP 所用的真空紫外光 (VUV)激發的三基色螢光粉,是實現彩色 PDP 的關鍵材料。
此外,螢光粉也廣泛被應用於背光模組中,如發光二極體、冷陰 極燈管(Cold Cathode Fluorescent Lamp, CCFL)、平面螢光燈(Flat Fluorescent Lamp, FFL)等,這些背光模組主要是用來提供液晶面板 均勻、高亮度的光線來源。而平面螢光燈因無含汞,符合環保之要求, 且其為單一光源故只需要一個驅動電路、背光模組組裝容易、亮暗對 比性高,加上其平面造型的設計等優勢,適用於大尺寸液晶電視背光 模組之應用。由於無汞平面螢光燈其發光機制是使用氙氣(Xe)所 放射之真空紫外光激發內部的螢光材料,因此開發新穎真空紫外螢光 體之研究,對於 PDP 和 FFL 的發展而言皆具有不錯的潛力。
1-2 研究動機
由於 PDP 是藉由惰性氣體(He/Xe)放電產生真空紫外線(147 nm 與 172 nm)照射螢光粉而產生放光,因此其使用之螢光粉必頇能被 真空紫外波段所激發。真空紫外線的波長很短且能量較強,因而需要 採用性能更好的螢光粉。目前用於 PDP 的螢光粉商品主要有三種, 分 別 為 紅 光 (Y,Gd)BO3:Eu 3+ 、 綠 光 Zn2SiO4:Mn 2+ 及 藍 光 BaMgAl10O17:Eu 2+ ,上述螢光粉在真空紫外光的激發下均具有高效率 的 發 光 。 然 而 , 三 者 仍 有 尚 待 改 良 之 缺 失 , 如 : 紅 光 螢 光 粉 (Y,Gd)BO3:Eu 3+ 的色飽和度不佳,其色光略偏橘紅光;綠光螢光粉
Zn2SiO4:Mn 2+ 其殘光過長,容易在顯示中產生拖尾或殘影;藍光螢光 粉 BaMgAl10O17:Eu 2+ 在長時間使用下,發現有易劣化而使其性能降低 之情形。基於以上 PDP 螢光粉之缺點,探討螢光粉的發光特性、改 善螢光粉的性質或開發新型的螢光材料等,不僅有學術上的研究貢獻, 更有產業上的應用價值。 此外,在螢光粉主體的選擇上,目前已有許多無機化合物用來當 作 PDP 之螢光粉,其中具有磷酸根與硼酸根陰離子團之無機化合物, 由於其能隙夠大,因此較其他種類化合物有較高的機率可被高能量的 真空紫外光激發;而在矽酸鹽中,SiO4 4-陰離子團的理論吸收值為 171 nm,十分符合 PDP 的激發光源 172 nm。 因此,本研究重點在於開發新穎含硼酸根、磷酸根或矽酸根的真 空紫外激發螢光粉,論文中一共合成了五種不同系列的 RGB螢光體, 藉由摻雜不同的稀土離子,其中包括了寬帶放射的 Eu2+ 和 Mn2+ 離子 及呈線性放射的 Tb3+ 離子,以探討各螢光體在真空紫外光(147 nm 與 172 nm)激發下其發光特性和能量轉移機制。
第二章 背景簡介
2-1 真空紫外螢光材料簡介
電漿平面顯示器最早是於1964年由美國伊利諾(Illinois)大學的 D.L. Bitzer 和 H.G. Slottow[1]所發明。其發光原理與日光燈管類似,現 今電漿顯示器皆操作於交流模式(ACPDP),簡單的結構如圖2-1,其 基本結構是在兩片分別印有行列互相垂直之電極的玻璃基板內封入 氖、氙等惰性氣體,在電極間通以高電壓後使氣體游離產生電漿效應, 並放射真空紫外光激發塗佈於玻璃基板上的紅、綠、藍三基色螢光粉 發出可見光,透過空間混色和電路控制達到彩色顯示的畫面。 PDP內部之螢光粉為顯示過程中的關鍵材料,因此螢光粉的性能 影響了PDP的畫質亮度及其使用壽命。由於PDP螢光粉較普通螢光燈 螢光粉受到更強能量的VUV照射,因此需採用性能更好的螢光粉。 圖2-1 交流電漿顯示器面板結構剖面圖[2]以下分別簡介 PDP 真空紫外激發之三基色螢光粉: 1.紅色螢光粉[3][4][5] 目 前 PDP 採 用 的 商 業 紅 色 螢 光 粉 主 要 有 (Y,Gd)BO3:Eu 3+和 Y2O3:Eu 3+ 兩種,而其中(Y,Gd)BO3: Eu 3+ 較被廣泛的使用。這是由於 (Y,Gd)BO3:Eu 3+ 較 具 有 優 良 的 真 空 紫 外 吸 收 特 性 , 圖 2-2 為 (Y,Gd)BO3:Eu 3+ 和Y2O3:Eu 3+在真空紫外光區的激發光譜,可發現前者 在147nm激發下的有效吸收較後者高。但就色澤的飽和度而言,Y2O3: Eu3+的發射主峰在611 nm處;而(Y,Gd)BO3:Eu 3+ 位於595nm,因此其 色光呈現橘紅色,色純度較差。此外,雖然(Y,Gd)BO3:Eu 3+ 的發光效 率優於Y2O3:Eu 3+ ,但是其對真空紫外光的反應較慢,需要3ms的時 間才能將所吸收的能量以可見光的形式放射出來,此缺點不利於顯 示。
綜合上述性能之比較,兩者各有長處與缺失,而開發一色度好且 發光效率高的短餘暉紅色螢光粉為一重要的研究方向。 2. PDP綠色螢光粉[5] [6][7] PDP綠色螢光粉種類甚多,大致上可分為兩類,第一類是以 Mn2+ 作為活化劑之螢光粉,如Zn2SiO4:Mn 2+ 和BaAl12O19:Mn 2+[8];第二類為 Tb3+作 為 綠 光 來 源 的螢 光 粉, 如 (La,Ce)PO4:Tb 3+[9] 、 YBO3:Tb 3+和 CeMgAl11O19:Tb 3+ 。其中,Zn2SiO4:Mn 2+因發光效率高、色純度好及 良好的化學穩定性而廣泛應用於PDP中。但是由於Mn2+ 的發射躍遷在 選擇律中是屬於自旋禁戒,因此其餘暉時間很長,易在顯示過程中產 生殘影或拖尾之現象,而降低了PDP的顯示性能。表 2-1為至今已開 發的PDP螢光粉,可發現綠光Zn2SiO4:Mn 2+ 和紅光Zn3(PO4)2:Mn 2+螢光 粉的衰退期過長,造成在PDP的應用上有殘光過長之缺點。研究發現, 提高Mn2+ 摻雜濃度可以縮短餘暉時間,但發光效率也會隨之降低。 第二類的綠色螢光粉是Ce3+-Tb3+共摻雜的螢光粉。這類的螢光粉 在長波長的紫外光激發下,Ce3+受激發後起敏化作用將能量傳遞至 Tb3+,使其發射出高強度之綠光。然而此類螢光粉在真空紫外光的激 發下,Ce3+敏化的效果較小,因而其發光強度較低。除此之外,由於 Tb3+的主要放射峰位在543 nm,其色光呈現黃綠色,色純度較差,因 此綠色螢光粉也有待進一步的改良及開發。
3. PDP藍色螢光粉[5] PDP 用 藍 光 螢 光 粉 有 摻 雜 Eu2+的 鋁 酸 鹽 BaMgAl10O17:Eu 2+、 BaMgAl14O23:Eu 2+ ,摻雜Ce3+ 的矽酸鹽 Y2SiO5:Ce 3+[10] 以及摻雜Pb2+鎢 酸鹽CaWO4:Pb 2+。其中 BaMgAl10O17:Eu 2+相較 BaMgAl14O23:Eu 2+而言, 其色飽和度較高,因而成為目前最廣泛應用於PDP中的藍光螢光粉。 但在PDP的製程中,BaMgAl10O17:Eu 2+ 中的Eu2+離子在高溫下易氧化 成Eu3+ 離子。此外,其在長時間使用下,BaMgAl10O17:Eu 2+也會因受 到高能量真空紫外光的照射而造成晶格扭曲之情形[11] ,此現象嚴重降 低了PDP的使用壽命。除上述缺失之外,藍色螢光粉的發光強度不夠 高也是阻礙PDP發展的另一因素。因此,開發一穩定性佳且發光強度 高的藍色螢光粉為另一重要之方向。 表2-1 已開發之PDP螢光粉性質之比較[3]
2-2 真空紫外螢光材料之發光機制
真空紫外螢光粉的激發光譜中,常見下列五種不同類型的吸收峰: (1)主體晶格的吸收帶,此過程是由於電子從主體晶格的價帶躍遷 至導帶;(2)配位基到金屬離子的電荷遷移帶;(3)稀土離子4f-5d 的躍遷吸收;(4)稀土離子4f-6s 的躍遷吸收;以及(5)稀土離子 4f 組態內的躍遷吸收[12]。 在不同的主體及摻雜不同稀土離子的情況下,螢光粉的發光機制 也不相同。依照激發的受體則可分為兩種類型:一為光源直接激發活 化中心;第二則是光源先激發主體,再透過能量轉移至發光中心後使 其發光,此類型屬於間接激發。大部分的螢光粉受到光源147nm激發 時,其機制多屬於後者;而若當螢光體以172nm激發時,則視活化劑 種類不同,發生前者或後者皆有可能,也可能兩者同時發生。 螢光粉間接激發的發光機制可用能帶理論簡單的描述,當螢光粉 受到高能的真空紫外光激發時,可能使電子由價帶躍遷至導帶並形成 電子電動對,此電子電動對即在價帶和導帶內遷移,當其分別移動至 發光中心的激態和激發態之能階時,即被侷限住,最後經由電子電動 之再結合而釋出螢光;或者,當螢光粉受激發後形成激子,激子可在 晶體中移動而將能量傳遞至發光中心上,最後同樣透過電子電動之再 結合而放出螢光[13]。根據以上所述,可知一真空紫外激發螢光粉的發光效率決定於主 體吸收激發光源的效率以及主體與活化劑間能量轉移效率。
2-3 真空紫外螢光材料之設計
經由文獻歸納,可知欲設計高效率的真空紫外激發螢光材料,可 依照以下三項規則進行: 1.主體必頇於真空紫外光波段具有良好的吸收 由於真空紫外激發螢光體之放光機制是先由主體吸收能量,再將 能量傳遞至發光中心使其放光,因此對於一個好的真空紫外激發螢光 粉而言,其主體必頇在真空紫外光波段有良好的吸收,特別是在 147 nm 與 172 nm 兩個波長。目前已有許多無機化合物用來當作 PDP 之 螢光粉,其中具有磷酸根與硼酸根陰離子團之無機化合物,由於其能 隙(energy band gap)夠大,因此較其他種類化合物有較高的機率可被高能量的真空紫外光激發[14] 。 2.稀土離子活化劑之選擇 在螢光體合成中,欲摻雜的活化劑離子需考慮其與將取代的主體 晶格之離子半徑是否相近,以及兩者之價數是否符合。若兩離子半徑 差異太大時,易導致晶格扭曲而造成發光效率下降;而當兩者所帶電 荷有所差異時,需考慮電荷補償,常見的摻雜有Na+或 K+,以避免
因電荷不平衡而導致主體晶格缺陷的產生。 另外,各種稀土離子皆具有其特殊的發光特性,故需針對不同色 光需求而有不同之活化劑選擇。例如 Tb3+的典型放射為以 540nm 附 近之數根細窄峰,放光範圍屬於黃綠光;Eu2+其放光範圍由紫外光至 黃光區之寬峰;Mn2+亦為寬峰放射,放射光色依其配位環境可能為綠 光、橘紅光及紅光。 3.主體與活化劑間具有高效率之能量傳遞 真空紫外激發之螢光體除了能有效吸收激發光源,並且選擇適當 活化劑外,尚需具備一特性:主體與活化劑間能量傳遞的效率良好。 因真空紫外激發螢光體多是經由主體吸收激發光源後,將能量傳遞至 活化劑而使其放光,若主體吸收之能量無法有效傳至活化劑上,則無 法 產 生 預 期 的 放 光 效 率 。 欲 改 善 此 現 象 , 可 嘗 詴 加 入 敏 化 劑 (sensitizer),真空紫外激發螢光粉常見的敏化劑有 Pr3+ 和 Gd3+,前 者常見於量子剪裁,而後者多與 Eu3+搭配,作為主體與活化劑間的橋 樑以協助兩者之間的能量傳遞,進而提升螢光粉的發光強度。
2-4 稀土離子能譜
稀土元素(rare-earth elements)為元素周期表中從鑭(La)到鎦 (Lu)
的15 個鑭系元素及同族(ⅢB)的鈧(Sc)和釔(Y),總共17個元素。稀土
(n = 1 ~ 14, m = 0或1) 表示,每一個稀土離子皆具有豐富的可躍遷電 子能階和長壽命的激發態能階(10-2 ~ 10-6秒),能階躍遷通道可多達20 萬個,可以產生從近紫外到近紅外光學範圍內的躍遷吸收和放射,因 而可以作為各種螢光材料的發光中心。為了開發新穎的真空紫外螢光 材料,對於稀土離子的 f-f躍遷、f-d躍遷、電荷轉移帶(Charge transfer Band)等的電子遷移特性的理解便相當的重要;稀土離子能階位置圖 的建立為真空紫外螢光材料的研究帶來相當大的進展。 4f n能階圖的基礎最早建立於1968年,Dieke 和其團隊整理了稀 土離子的4f能階圖,並將此能階圖簡稱為「Dieke Diagram」;其實驗 結果是將各種稀土離子摻雜於高對稱性(C3V)的LaCl3主體中所取得的, 能量範圍在 0-42,000 cm-1[15],相當於紅外、可見與紫外光的波長。 由於主體晶格的對稱性與結晶場強度對於稀土離子4f n能階分裂的影 響相當地小,因此 Dieke Diagram 幾乎可以沿用於任何主體中所摻雜 的三價稀土離子。 隨後,美國Argonne 國家實驗室Carnall 等人詳細研究了各稀土 離子摻雜在 LaF3 主體中的光譜,其內容較為詳細,並且將理論計算 與實驗數據的結果詳細比對,以校正結晶場之作用;LaF3 在 UV及 VUV 波段皆具有良好的光學特性,Carnall 團隊成功地將稀土離子能 階圖擴展到50,000 cm-1 [16]。
而能量高於50,000cm-1之研究則相較困難,原因在於設備的缺乏 而造成量測上的困難。近年來,由於同步輻射光源的使用技術越來越 成熟,也為稀土離子的高能階躍遷提供了較完善的量測裝置;西元
2000年,荷蘭的R. T. Wegh 等人利用德國DESY同步輻射裝置對稀土
離子VUV 波段的激發光譜做了更詳細的研究;Wegh 研究團隊選擇
使用高純度的LiYF4 作為稀土離子摻雜的主體,並將 Dieke diagram
擴展到 70,000 cm-1[17],如圖2- 1。這些高能的能階圖譜,對於真空紫
外螢光材料的光譜解析以及能量轉移機制的探討,提供了更明確的研 究前景。
在本研究中,主要以稀土離子Tb3+ 、Eu2+ 及Mn2+作為發光中心, 分別摻雜於不同主體中,以探討其發光特性和機制。以下針對上述三 種稀土離子的電子遷移與發光機制做詳細說明: (1) Tb3+(4f 8) Tb3+離子的光致發光光譜呈線性放射,其放射波長多位於 450nm ~700nm,為綠光範圍,其所對應的電子躍遷為 5D4→ 7 FJ (J = 3, 4, 5, 6), 是典型的綠色螢光粉之活化劑。Tb3+的激發光譜除了微弱的 f-f 躍遷, 在紫外光波段可觀察到一位於 220 ~ 280 nm的寬吸收帶,此吸收帶是 源自於電子從Tb3+ 的基態4f 8 躍遷至激發態4f 7 5d,隨即從4f 75d經由非 輻射緩解至5 D3或 5 D4這兩個較長壽命期的激發態,最後再由 5 D3或 5 D4 能階向7 FJ多重基態能階發生躍遷輻射而放光 [18] 。 此外,當主體中Tb3+離子濃度較低時,可能產生較高能階的躍遷 5 D3→ 7 FJ,其為藍光或紫光發射;但當濃度提高時,則發生 5 D3躍遷放 射的濃度淬滅和5 D4躍遷發射的增強現象,即所謂的交叉弛豫(cross relaxation)。由於此過程是取決於兩發光中心之間的作用,故只有發 光中心超過一定濃度時才會產生交叉弛豫之現象。以下說明交叉弛豫 之過程,如圖所示,Tb3+ (1)離子與Tb3+ (2)離子為兩鄰近之發光中心, 當高濃度時兩離子之距離相對靠近,首先Tb3+ (1)離子將 5D3→ 5 D4 的 能量轉移至鄰近Tb3+ (2)離子,導致 Tb3+(2)離子產生7F6→ 7 F0 的吸收
躍遷。此一過程造成 Tb3+的 5 D3 放射發生發光強度減弱,而放光的 結果則由 5 D4的發射所主導。此過程可用下列簡式表示: 1 2 1 2 Tb3+ (5D3)+ Tb 3+ (7F6) → Tb 3+ (5D4) + Tb 3+ (7F0) 5 D3 1 5 D4 7F0 2 7F6 Tb3+(2) Tb3+(1) 圖2-4 高濃度時Tb3+離子發生交叉弛豫之螢光淬滅示意圖 (2) Eu2+ (4f 7) Eu2+的4f 7電子基態能階為8S7/2,最低激發態為4f 6 5d1,其放光壽 命為 10-5 ~ 10-6 s。除了在某些晶體結構中,Eu2+因結晶場作用較弱, 使6 PJ 能階低於4f 6 5d 能階,而產生6PJ (4f 7 )→8S7/2 (4f 7 )的尖銳放射;在 大 部 分 的 主 體 當 中 , 4f6 5d 能 階 易 受 到 結 晶 場 作 用 產 生 分 裂 (Crystal-field splitting) 而低於 6PJ ,導致 f→f間的能階躍遷並不常見, 而是 d→f電子躍遷的寬帶放射居多。Eu2+的放光位置會隨著晶場強 度的增加,而在光譜上有紅位移的趨勢,因此其發光波長所涵蓋的範 圍甚廣,可從近紫外至紅光。
(3)Mn2+(3d 5) Mn2+的電子基態能階為6 A1,其能階因受到強自旋軌域偶合的影 響,而分裂成多個光譜項,由於躍遷之電子牽涉到外層的 d 軌域,因 此 Mn2+ 的發射光譜亦呈現帶狀。Mn2+ 具有 3d5的外層結構,其發光 波長強烈地受到結晶場及其配位環境的影響,且由於 Mn2+在可見光 區的躍遷為 d→d 間的能階躍遷,在光學選擇律中屬於宇稱及自旋禁 制,所以在紫外或可見光的激發下,其發光訊號相當微弱。當 Mn2+ 佔據氧八面體配位的格位時,其發光波段位於橘紅光區;而 Mn2+佔 據四面體的格位時,則放射綠光,且由於四面體格位不具有反置中心, 因此其放射強度會稍強於當其佔據八面體格位時[18] 。
2-5 濃度淬滅效應
當一螢光體被活化而產生發光時,其過程牽涉到活化劑之間的能 量轉移;一活化劑受外界激發源所激發後,會將能量傳遞至其他未受 激發之活化劑離子,並產生發光。在多數情況下,螢光體中所摻雜的 活化劑高達一定濃度時,發光強度即不再提高,反而隨之降低,此現象稱為濃度淬滅效應 ( Concentration quenching effect ) ,此乃因活化
劑濃度過高時,能量於活化劑之間傳遞的機率大於發射之機率,因此 導致激發能量重複傳遞於活化劑之間,最終傳至主體晶格之缺陷,此 時能量則耗損於其中,因而造成螢光體的發光效率降低。
圖 2-5 高濃度活化劑造成螢光體濃度淬滅成因示意圖
2-6 同步輻射光源
同步輻射光為一連續波段的電磁波,涵蓋紅外線、可見光、紫 外線及 X 光等。根據電磁學理論,當帶電粒子運動速度或方向改變 時,會放射出電磁波。另外,同步輻射光具有以下特性:強度極強、 波長連續、準直性佳、光束截面積小、具有時間脈波性與偏振性。 首先電子經過線性加速器(linear accelerator)加速能量至五千萬 電子伏特,隨後進入增能環(booster ring)中,此電子束於環內運行並 非為連續的電子束,而會在特定區域集結為一束一束(bunch)的電子, 並且利用高頻腔(RF cavity)加速電子束,當電子束通過高頻腔後,逐 漸將能量提升至十五億電子伏特。因此,必頇調控適當的頻率使每束 電子位於高頻腔的波峰上達到頻率匹配,故稱為同步加速器。直到電 子加速接近光速(0.99999995 倍光速)後,經由傳輸線(transport line)引
入儲存環(storage ring)中保留。此外,在儲存環內安裝各類的插件磁 鐵(insertion device),此裝置為一系列極性交錯並排的磁鐵,藉此將電 子由偏轉一次變成多次偏轉,使同步輻射光的亮度則可以提高一千倍 以上。其中,增頻(wiggler)磁鐵與聚頻(undulator)磁鐵為代表:前著 利用提高磁場強度,使電子束偏轉後產生大範圍頻寬(可由軟 X 光至 硬 X 光)的光譜。後者將磁場交替的週期性變短,使電子束擺動幅度 變小、次數變多,再由特定頻率光譜形成建設性干涉,可大幅提升該 特定能量之亮度。 圖 2-6 新竹國家同步輻射研究中心的加速器系統
第三章 主體晶體結構簡介
3-1 YBa3(BO3)3
YBa3(BO3)3具有與兩種結構, -YBa3(BO3)3 的合成溫度為 1100
℃,當溫度在 1125-1134℃之間其晶相會轉變形成 -YBa3(BO3)3之結
構,本論文所合成樣品屬於-YBa3(BO3)3。Khaihina 等人
[19]
在 1999
年首度對-YBa3(BO3)3 進行晶體結構的解析,但當時 Khaihina 僅指
出-YBa3(BO3)3 屬於六方晶系(hexagonal),晶格常數 a = 9.4216(1) Å ,
c = 17.5990(2)Å ,空間群為 P63cm。直至 2004 年,Li 等人[20]較完整
地報導了-YBa3(BO3)3與-YBa3(BO3)3的晶體結構。Li 所報導的
-YBa3(BO3)3 其 JCPDS 卡號為 01-074-4000,晶格常數 a= 9.41908(6) Å 、 b = 9.41908(6)Å 、 c =17.5949(1)Å ,= = 90°、120°,Z= 6,V=1351.87Å3,空間群為P63cm,其結構如圖 3-1 所示。在 -YBa3(BO3)3晶格中,B 3+ 離子佔據三種格位,每一個 B3+離子皆與三 個 O 原子配為形成平面三角形,這些 BO3 3−三角形一層接著一層沿著 c 軸排列分佈;Y3+離子佔據兩種格位,分別與六個 O 原子配位形成 八面體(octahedral polyhedra),且 YO6與 YO6之間藉著沿 c 軸排列的 BO3 3− 三角形來連接,如圖 3-2 所示;Ba2+離子在晶格中有四種格位, 分別與六個和九個 O 原子形成扭曲的多配位體結構。
圖 3-1 YBa3(BO3)3 晶體結構示意圖
圖3-2 YBa3(BO3)3沿著 c 軸方向俯視的排列示意圖
3-2 Ca5Al6O14
Ca5Al6O14屬於正交晶系(orthorhombic),於 1978 年首度由 Vicent
數為 a = 11.253Å、b = 10.966Å、c = 10.290Å,V =1269.79Å3,Z = 4, 空間群為 Cmc21,JCPDS 卡號為 00-03-0149,圖 3-3 為其晶體結構示 意圖。在 Ca5Al6O14晶格中,Al 3+ 離子佔據四種格位,且四種 Al3+離子 皆分別與四個 O 原子配位形成扭曲的 AlO4四面體,AlO4四面體之間 藉著共享其頂角而形成五圓環,這些五圓環在空間上彼此連接而形成 網狀結構,每種 Al 格位的 Al-O 平均鍵長分別為 1.763、1.768、1.757 和 1.766 Å ;Ca2+離子佔據三種不同的格位,其中兩種為六配位,另 一則為八配位,這些以 Ca2+離子為中心的多面體藉著共享特定的面在 晶格中垂直[110]排列,這樣的排列情形造成 Ca5Al6O14晶格中 Ca-Ca 之間的距離相當的短( 3.200-3.267 Å ), 每種 Ca 格位的 Ca-O 的平均 鍵長分別為 2.367、2.401 與 2.503 Å 。 圖 3-3 Ca5Al6O14 晶體結構示意圖
3-3 NaCaPO4
NaCaPO4屬於正交晶系(orthorhombic),最初於 1942年由Bredig
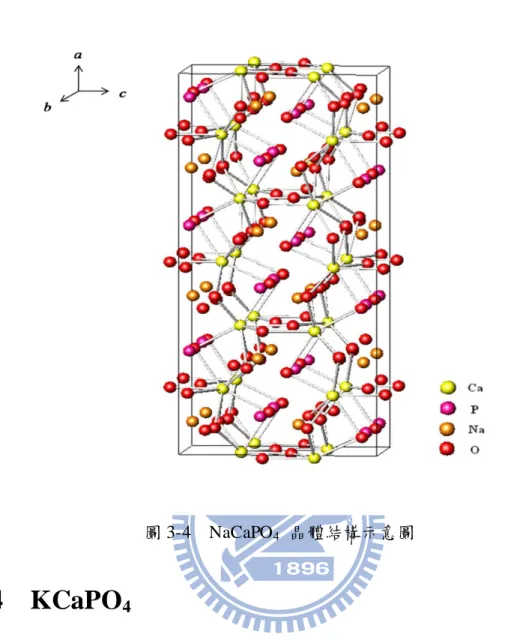
[22] 所報導,而後在 1983 年時 Amara 等人[23]對其進行更加詳細的晶 體結構解析, Amara 解釋 NaCaPO4 具有類 -K2SO4 之結構,其 JCPDS 卡號為 00-076-1456,晶格常數 a = 20.397(10)Å、b = 5.412(4) Å 、 c = 9.161(5)Å , Z = 12,V =1011.27Å3,空間群為 Pn21a,其 結構如圖 3-4 所示。在 NaCaPO4中存在兩種沿著 a 軸的直線排列, 一種是由[PO4]四面體與 Na 原子交錯而成,另一則是全部只有 Ca 原子,此兩種排列構成 NaCaPO4之晶格。而 NaCaPO4與-K2SO4 結構上最大的不同在於上述的直線排列中[PO4]四面體方向的不同, 且因為 Ca 和 Na 不同的配位情形造成 NaCaPO4的晶格常數 a 為 -K2SO4的三倍。在 NaCaPO4的晶格中,Ca 和 Na 均佔據有三種格 位,三種 Ca 原子皆為八配位,Na 原子則有六配位及十配位兩種配 位情形。此外,P 在晶格中也有三種不同的配位環境,皆以[PO4] 四面體的配位形式存在,P-O 的平均距離為 1.533 至 1.545 Å,四面 體的平均鍵角在 109.4 與 109.5°範圍之間。
圖 3-4 NaCaPO4 晶體結構示意圖
3-4 KCaPO
4 KCaPO4的晶體結構最先於 1942 年由 Bredig [22] 所發表,KCaPO4 具有與兩種結構,705℃為-KCaPO4與-KCaPO4之相轉換溫度, 當溫度高於 705℃時 KCaPO4以相的形式存在,因此本論文合成的樣品屬於-KCaPO4 之結構。-KCaPO4屬於六方晶系(hexagonal),
與 K3Na(SO4)2 [24] 結構相似,晶格常數為 a = b = 5.58Å 、c = 7.6Å , °,V =1269.79Å3,空間群為 P3m1。圖 3-5,顯示了-KCaPO4 之晶體結構中各離子的鍵結狀態。Ca 與 K 配位環境相同,佔據三種 格位,皆為六配位。
圖 3-5 KCaPO4 晶體結構示意圖
3-5 Li4SrCa(SiO4)2
Li4SrCa(SiO4)2晶體屬於正交晶系(orthorhombic),於 1995 年時由 Annapoorna 等人[25]報導其晶體結構與摻雜 Eu2+離子之螢光粉在紫外 光 波 段 激 發 下 的 發 光 特 性 。 Zhang 等 人 [26] 也 研 究 了 Li4SrCa(SiO4)2:Eu 2+ ,Mn2+的發光特性及能量傳遞,由此可見文獻中對 Li4SrCa(SiO4)2的發光性質已有初步的認識;Annapoorna 報導此晶體 呈無色透明,其 JCPDS 卡號為 01-083-0763,晶格常數 a = 4.983(2) Å 、 b = 9.930(2) Å 、c = 14.057(2) Å ,V = 695.56 (4)Å3,Z = 4,空間群為 Pbcm,而圖 3-6 為 Li4SrCa(SiO4)2晶體結構示意圖。晶格中,陽離子 Sr2+與 Ca2+均只佔據一種格位,Sr2+離子與十個 O 原子配位形成一扭曲的雙帽四方反稜柱體(bicapped square antiprism),而 Ca2+離子被六
兩種格位,且分別與四個 O 原子配位形成扭曲的四面體;以 Sr2+為中 心的多面體在 ab 平面上藉由共享二個氧原子而無限串連,Ca2+所形 成的八面體彼此之間則是完全獨立;以 Li4+為中心的多面體共用所有 的頂點在平行 ab 平面上形成以(Li2O4) 6-形式且無限延伸的二維結 構。 圖 3-6 Li4SrCa(SiO4)2晶體結構示意圖
3-6 LiZnBO
3LiZnBO3存在兩種結構,一為三斜晶系(triclinic),空間群為 P1 [27]; 另一為單斜晶系(monoclinic),空間群為 C2/c[28],本論文合成的結構 屬於後者。最早於 2001 年由 Chen 等人成功合成 LiZnBO3晶體,並 對其進行結構解析。Chen 所合成的 LiZnBO3 晶體呈無色透明,其 JCPDS 卡號為 01-070-76,晶格常數為 a = 8.746(2) Å、b =5.091(1) Å 、
c =6.129(1)Å ,= 90°、=118.75(3)°、90°,V =239.26(11)Å3, Z = 4。LiZnBO3為由 ZnO4四面體和 BO3三角形所構成的三維網狀結 構,ZnO4和 ZnO4之間共用一個邊而形成 Zn2O6二聚體,而每個 Zn2O6 藉著共用的 O 原子與其他六個 Zn2O6相連,這樣的網狀結構形成了六 角形的通道,而 Li 原子則佔據其中,如圖 3-7 所示。在此晶格中, 每個 Li 原子與五個 O 原子配位,其中與三個 O 原子的鍵結較強,鍵 長為 1.912(11) – 1.944(11) Å ,與另外兩個 O 原子鍵節較弱,鍵長約 2.350(13) – 2.767(13) Å 。 圖 3-7 LiZnBO3沿著 a 軸方向俯視的排列示意圖
第四章 實驗方法
4-1 實驗藥品
(1) 碳酸鋰 (Li2CO3,Lithium carbonate)
ACS reagent grade,MP
(2) 碳酸鈉 (Na2CO3,Sodium carbonate)
99.95%,Acros organics
(3) 碳酸鋇 (BaCO3,Barium carbonate)
99+%,Alfa Aesar, U.S.A.
(4) 碳酸鍶 (SrCO3,Strontium carbonate)
99.9+%,Aldrich Chemicals Company Inc., U.S.A.
(5) 碳酸鈣 (CaCO3,Calcium carbonate)
99+%,Aldrich Chemicals Company Inc., U.S.A.
(6) 碳酸鉀 (K2CO3,Potassium carbonate)
99%, Merck, U.S.A.
(7) 氧化釔 (Y2O3,Yttrium(Ⅲ) oxide)
99.99%,Signa-Aldrich Chemicals Company Inc., USA
(8) 氧化鋁 (Al2O3,Aluminum oxide)
(9) 氧化鋅 (ZnO,Zinc oxide)
99.9%,Aldrich Chemicals Company Inc., USA
(10) 二氧化矽 (SiO2,Silicon(Ⅳ) dioxide)
99.6%,~325 mesh,Aldrich Chemicals Company Inc., USA
(11) 氧化銪 (Eu2O3,Europium(Ⅲ) oxide)
99.9%,Signa-Aldrich Chemicals Company Inc., USA (12) 氧化錳 (MnO,Manganese(Ⅱ) oxide)
99.99+%,Aldrich Chemicals Company Inc., USA
(13) 氧化鋱 (Tb4O7,Terbium(Ⅲ,Ⅳ) oxide)
99.9%,Aldrich Chemicals Company Inc., USA
(14) 磷酸氫二銨 ( (NH4)2HPO4,Di-Ammonium hydrogen phosphate)
99%, Merck, U.S.A.
(15) 硼酸 (H3BO3,Boric acid)
4-2 儀器設備
(1) 箱型高溫爐 (High temperature furnaces)
使用新店市陵勝企業公司生產的箱型爐,加熱空間約為 7,056 cm3,配備 Eurotherm 818P 型溫控器及矽化鉬加熱元件,最高溫度可 達 1700 ℃。另有桃園縣平鎮市奇豪電熱有限公司生產的程式控溫升 降爐,溫度上限為 1620 ℃,加熱空間為 5,915 cm3 和 11,340 cm3 。 (2) 高溫管狀通氣爐 (High temperature tubular furnaces)
使用新店市陵勝企業公司製作的管狀爐,內徑 5 cm且長度 130 cm,其所使用的內襯鋼管及附件為鋒澤企業社以沃斯田鐵系 347 號 不銹鋼加工而成,其溫度上限為 1200 ℃。
(3) X 光繞射儀 (X-ray diffractometer)
X光繞射儀為 Bruker AXS D8 advance 機型,其光源為銅靶,功
率為 2.2 KW。X光源產生之原理為利用 40 kV 的操作電壓,加速電 子撞擊銅靶以激發銅原子,經單光晶體分光,使之產生波長為 1.5405Å 的 Kα X 射線,量測時之操作電流為 40 mA。掃瞄範圍之 2θ 值為 10至 80度,掃瞄模式為 2θ/θ,掃瞄速率為每分鐘 5度。量 測前先將分析樣品研磨成均勻細粉,固定在樣品槽上以進行量測;必 要時以矽粉做內標,以校正繞射峰之 2θ 值。最後利用 DIFFRAC PLUS Evaluation 軟體處理數據及圖像。
(4) 真空紫外光激放光譜儀(Vacuum Ultraviolet Photospectrometer) 使用國家同步輻射研究中心(NSRRC) 鄭炳銘博士實驗室BL03A (HF-CGM Hight Flux Beamline)所架設之光致發光光譜量測系統,結 合國家同步輻射研究中心所提供的真空紫外光作為激發光源,以研究 各類發光材料的螢光光譜和發光機制。實驗裝置如圖4-1所示,目前 光束線波長介於 35 nm ~ 350 nm之光源,該裝置使用CaF2作為分光 片以校正真空紫外光光源的強度。量測首先將樣品固定於樣品槽中, 在置入量測室中抽真空,當真空度到達 10-5 Torr 以下即可開始測量。 量測時設定掃描速度為5 Ǻ/sec,當測量放射光譜時,單光儀光柵光柵 調為0.5mm x 0.5 mm、入射光柵為0.3mm x 5.0 mm皆為可調;當測量 激發光譜時,單光儀光柵調為2.0mm x 2.0 mm、入射光柵為0.3mm x 0.5 mm,掃描波長範圍依需求設定。 (5) 真空紫外螢光光譜測詴系統 使用浙江省杭州市浙大三色儀器有限公司製作的真空紫外光光 譜儀,可測量真空紫外螢光粉於 147 nm 和172 nm波長激發下之發光 光譜、譜線帶寬、峰值波長、發光亮度、色度做標等參數,以及真空 紫外螢光粉之發光餘輝波形曲線等特性。本儀器以模擬PDP裝置之真 空紫外放電管提供 147 nm 和 172 nm 兩種波長作為激發光源,光譜 測量範圍為 350 ~ 800 nm,餘輝時間由 0.1 ms ~ 1 s。
圖 4-1 國家同步輻射研究中心(NSRRC) BL03A (HF-CGM High Flux Beamline) 紫外-可見光光譜儀實驗裝置 (6) 熱場發射掃描式電子顯微鏡(FESEN JSM – 6500F) 使用捷東股份有限公司 (JEOL)所產製之熱場發射掃描詴電子顯 微鏡,機型為 JSM-6500F,電子槍為熱場效型 In-Lens Thermal,放 大倍率為 25 ~ 500,000 倍,加速電壓為 1至 20 KV,解析度為 1.5 nm (@15 KV)、5.0 nm (@1.0 KV)
4-3 實驗步驟與流程
本研究全程是以高溫固態合成法製備螢光粉粉末,將反應物依 其化學計量比例秤量並混合均勻後,再於高溫爐中進行熱處理,在高 溫下藉由離子的擴散而結晶成相。將燒結完成後的粉體均勻研磨,並 利用X光繞射儀確認晶相無誤後,再利用國家同步輻射研究中心所提 供的真空紫外波段光源進行螢光體發光特性之研究。 此合成法為一種廣泛採用的技術,優點為合成步驟容易且產物之 結晶性高,但缺點為產物粒徑大小不均勻,雖然存在上述的問題,但 本研究著重開發新穎的螢光材料,因此選用固態合成法。 此外,本研究大部分樣品的合成尚還需要在還原氣氛中進行,例 如:YBa3(BO3)3:Tb 3+ 、Ca5Al6O14:Eu 2+ 、NaCaPO4:Eu 2+ 、KCaPO4:Eu 2+、 Li4SrCa(SiO4)2:Eu 2+等;本實驗利用高溫管狀爐裝置來進行,並在燒結 過程中提供適當濃度的氫氣以還原摻雜的活化劑離子,以下為各樣品 的合成步驟流程圖。
4-3-1 YBa
3(BO
3)
3:Tb
3+螢光體之合成
依化學計量秤取起始物 Y2O3、BaCO3、H3BO3 與 Tb4O9 進行以下 反應:(1-x)/2Y2O3+3BaCO3+H3BO3+x/4 Tb4O9 → (Y1-xTbx)Ba3(BO3)3 +3 CO2 (x=0.01~ 0.3),於瑪瑙研缽研磨均勻後, 放入氧化鋁坩堝中 將氧化鋁坩堝置於箱型高溫爐中,於 5%H2/95%N2氣氛下以1000 ~ 1100℃燒結8小時 將所得產物均勻研磨後,利用粉末X-ray繞射以鑑定結構,並進行 真空紫外光光譜、色度座標與SEM影像等量測分析4-3-2 Ca
5Al
6O
14:Eu
2+螢光體之合成
依化學計量秤取起始物 CaCO3、Al2O3 與 Eu2O3 進行以下反應:
5(1-x) CaCO3+ 3 Al2O3+ 2.5x Eu2O3 → (Ca1-x,Eux)5Al6O14+ 5(1-x)
CO2 (x=0.001~ 0.03),於瑪瑙研缽研磨均勻後,放入加蓋的氧化鋁 坩堝中 將氧化鋁坩堝置於高溫爐中,以1200℃在空氣下燒結 8小時 將燒結完的產物研磨均勻後,置於舟型坩堝中,利用管狀高溫爐, 於 40%H2 / 60%N2 氣氛下以1000℃退火處理6小時 將所得產物均勻研磨後,利用粉末X-ray繞射以鑑定結構,並進行 真空紫外光光譜、色度座標與SEM影像等量測分析
4-3-3 NaCaPO
4:Eu
2+螢光體之合成
依化學計量秤取起始物 CaCO3、Al2O3 與 Eu2O3 進行以下反應:
12(1-x) CaCO3+7 Al2O3+6x Eu2O3 →(Ca1-x,Eux)12Al14O33+12(1-x)
CO2 (x=0.001~ 0.03),於瑪瑙研缽研磨均勻後,放入加蓋的氧化鋁 坩堝中 將氧化鋁坩堝置於高溫爐中,以1000~1200℃在空氣下燒結 8小時 將燒結完的產物研磨均勻後,置於舟型坩堝中,利用管狀高溫爐, 於 15%H2/ 85%N2 氣氛下以1000℃退火處理6小時 將所得產物均勻研磨後,利用粉末X-ray繞射以鑑定結構,並進行 真空紫外光光譜、色度座標與SEM影像等量測分析
4-3-4 KCaPO
4:Eu
2+螢光體之合成
依化學計量秤取起始物 K2CO3、CaCO3、(NH4)2HPO4 與 Eu2O3 進 行以下反應:0.5 K2CO3+ (1-x) CaCO3+(NH4)2HPO4+ x Eu2O3→ K(Ca1-xEux)PO4+n CO2 (x=0.005~ 0.06),於瑪瑙研缽研磨均勻後, 放入加蓋的氧化鋁坩堝中 將氧化鋁坩堝置於高溫爐中,以1000~1100℃在空氣下燒結 8小時 將燒結完的產物研磨均勻後,置於舟型坩堝中,利用管狀高溫爐, 於 15%H2 / 85%N2 氣氛下以1000℃退火處理6小時 將所得產物均勻研磨後,利用粉末X-ray繞射以鑑定結構,並進行 真空紫外光光譜、色度座標與SEM影像等量測分析4-3-5 Li
4SrCa(SiO
4)
2:Eu
2+螢光體之合成
依化學計量秤取起始物 Li2CO3、SrCO3、CaCO3、SiO2與 Eu2O3 進
行以下反應:0.5Li2CO3+(1-x)SrCO3+CaCO3+SiO2+x/2 Eu2O3→
Li4(Sr1-xEux)Ca(SiO4)2+n CO2 (x=0.005~ 0.03),於瑪瑙研缽研磨均 勻後,放入加蓋的氧化鋁坩堝中 將氧化鋁坩堝置於高溫爐中,以700~900℃在空氣下燒結 8小時 將燒結完的產物研磨均勻後,置於舟型坩堝中,利用管狀高溫爐, 於 40%H2 / 65%N2 氣氛下以750℃退火處理6小時 將所得產物均勻研磨後,利用粉末X-ray繞射以鑑定結構,並進行 真空紫外光光譜、色度座標與SEM影像等量測分析
4-3-6 LiZnBO
3:Mn
2+螢光體之合成
依化學計量秤取起始物 Li2CO3、ZnO2、H3BO3 與 MnO 進行以下
反應:0.5 Li2CO3+(1-x) ZnO2+H3BO3+x MnO→ Li(Zn1-xMnx)BO3
+0.5 CO2 (x=0.001~ 0.02),於瑪瑙研缽研磨均勻後,放入氧化鋁坩 堝中 將氧化鋁坩堝置於箱型高溫爐中,以900℃燒結8小時 將所得產物均勻研磨後,利用粉末X-ray繞射以鑑定結構,並進行 真空紫外光光譜、色度座標與SEM影像等量測分析
第五章 結果與討論
5-1 YBa3(BO3)3:Tb
3+系列螢光體之研究
5-1-1 主體合成探討與晶相分析之研究
本實驗採傳統的高溫固態法合成 YBa3(BO3)3:Tb 3+系列螢光粉, 製程詳如 4-3-1節所述。圖 5-1為合成溫度 1100℃下所製備 YBa3(BO3)3 的 X 光粉末繞射(XRD)圖譜,將所得圖譜與 JCPDS 資料庫進行比對, 發現其繞射峰與 JCPDS 卡號 01-074-4000 所述幾乎完全吻合,因此後 續進行 Tb3+ 離子的摻雜時,皆以上述條件來進行。 圖 5-1 於 1100℃下所製備 YBa3(BO3)3之 X 光粉末繞射圖譜若 考 慮 陽 離 子 配 位 數 與 有 效 半 徑 之 關 係[29,30], 六 配 位 的 Tb3+(0.923Å )與 Y3+(0.9Å )半徑相近且具有相同價數,因此推論 Tb3+應 可順利取代 Y3+ 之格位。接著在氫氣還原氣氛下進行以 Tb3+為活化劑 取代主體中的 Y3+ ,分別摻雜 1~40%莫耳比例之 Tb3+,並量測其 XRD 圖譜。圖 5-2 為不同 Tb3+ 摻雜濃度的 XRD 圖譜,可發現 Tb3+摻雜後, 其濃度小於 30%之粉體其繞射峰雖稍往低角度位移,但繞射圖譜仍然 維持同樣的晶相圖形,沒有明顯的雜相產生,故由 XRD 圖譜可證實 Tb3+確實進入到 Y3+格位填佔。而當摻雜濃度高於 40%時,則開始出 現 TbBa3(BO3)3之相,因此便不繼續進行更高濃度之摻雜。 圖 5-2 不同 Tb3+濃度取代(Y
5-1-2 螢光光譜與發光特性分析
5-1-2-1 光致發光光譜之研究
圖 5-3 為未摻雜 Tb3+的 YBa3(BO3)3主體以真空紫外光 172 nm 激
發所得之光致發光(Photoluminescence, PL)光譜圖。由圖可知,其放光 範圍從 300 nm 至 500 nm,為一寬帶放射,最強放射波長位於 343 nm
處。由於 YBa3(BO3)3的自身活化放光範圍與其他硼酸鹽 La(BO2)3、
YAl3(BO3)4、LuBa3B9O18相近 [31,32] ,因此推論此放射峰是源自於 BO3 3-陰離子團,為三配位硼酸鹽類的典型放光。 圖 5-3 YBa3(BO3)3發光光譜 (ex= 172nm) 圖 5-4 為以 172 nm 波長激發 YBa3(BO3)3:1%Tb 3+ 所得發光光譜,
波長為 172 nm,可觀察到主體摻雜活化劑 Tb3+後的放光現象,放射 波長短於 450 nm 為一寬帶放射,而波長長於 450 nm 以上者為線性放 射。若將圖 5-3 與圖 5-4 相互對照,可發現兩張圖中 300 至 450 nm 波段的光譜其波形及位置皆很相似,且在圖 5-3 中,此區域最高峰波 長也接近 343 nm,因此可研判其為主體的放光;而波長在 450 nm 以 上之區域有四組主要的放射峰,這四組波鋒分別位於 488、543、583 和 624 nm,分別對應於 Tb3+之 5 D4→ 7 FJ (J = 6,5,4,3)放射。其中最高 峰值位在 543 nm 處,為 Tb3+之 5 D4→ 7 F5躍遷發射,而其餘三者分別 對應於 Tb3+的 5 D4→ 7 F6、 5 D4→ 7 F4和 5 D4→ 7 F3躍遷 [33] 。 圖 5-4 (Y0.99Tb0.01)Ba3(BO3)3發光光譜 (ex= 172nm)
圖 5-5 (Y0.9Tb0.1)Ba3(BO3)3發光光譜 (ex= 172nm) 圖 5-5 為以波長 172 nm 激發 YBa3(BO3)3:10%Tb 3+所得之發光光 譜,圖中同樣具有四組 Tb3+之 5 D4→ 7 FJ (J = 6,5,4,3)特徵放射峰,但 位於 450nm 以下之主體放射明顯減弱,並在 380 至 400 nm 處出現 Tb3+較高能階5D3→ 7 FJ之躍遷 [34],然而在更高濃度的摻雜則不見此峰, 此是由於發生交叉弛豫之緣故。若將圖 5-4 和圖 5-5 相比較,可發現 當 YBa3(BO3)3摻雜低濃度的 Tb 3+ 時,其波長短於 450 nm 的主體放光 相當明顯,然而隨著 Tb3+濃度增加,主體部分的放射漸弱甚至不復見, 同時 Tb3+之 f-f 躍遷之放射峰則相對增強許多,因此可以推論此主體 與稀土離子發光中心之間有能量傳遞的現象發生。
為了探討 YBa3(BO3)3:Tb 3+ 系列螢光粉在不同濃度 Tb3+摻雜下放 光強度之變化,因此將一系列分別摻雜 1~ 30% Tb3+ 的螢光粉以 172 nm 波長作激發,觀察其光致發光光譜,如圖 5-6 所示。當所摻雜的 Tb3+濃度越高時,Tb3+發光強度也相對提高,同時亦伴隨著主體自身 放光的減弱,這是由於主體將其所吸收的能量傳遞至活化劑 Tb3+,進 而增強了 Tb3+ 的發光。而當 Tb3+ 的摻雜濃度高達 30%時,主體放射 峰完全消失,表示主體將能量完全傳遞至 Tb3+上,同時螢光強度也達 到最高值。而若再繼續提高 Tb3+ 的摻雜濃度,則如 5-1-1 節所述,將
生成 TbBa3(BO3)3之競爭相,故由此可推斷(Y0.7Tb0.3)Ba3(BO3)3為此螢
光粉之最適化組成。
圖 5-7 (Y0.7Tb0.3)Ba3(BO3)3與 Zn2SiO4:Mn2+商品發光光譜之比較
圖 5-8 不同 Tb3+濃度摻雜的 YBa
3(BO3)3: x%Tb3+與 Zn2SiO4:Mn2+商品
圖 5-7 為 Zn2SiO4:Mn 2+
商品與最佳化組成(Y0.7Tb0.3)Ba3(BO3)3發
光光譜之比較。圖 5-8 則為不同 Tb3+ 摻雜濃度的 YBa3(BO3)3: x%Tb 3+ 與 Zn2SiO4:Mn 2+商品光致發光光譜之比較,圖中清楚顯示摻雜不同 Tb3+濃度的 YBa3(BO3)3: x%Tb 3+螢光粉與市售商品其放射強度之差異,
結果顯示(Y0.7Tb0.3)Ba3(BO3)3放光強度約為市售商品的六成。
圖 5-9 YBa3(BO3)3: x%Tb3+系列螢光粉發光強度與相對輝度與 Tb3+濃度之關係 (設 Zn2SiO4:Mn2+發光強度與輝度值為 1) 圖 5-9 表示含不同 Tb3+濃度的 YBa3(BO3)3: x%Tb 3+發光強度與相 對輝度與 Tb3+濃度之關係,方塊折線表示光致發光強度,星號折線代 表相對輝度,其中輝度值為放射光譜中可見光區域面積之積分值。圖 中顯示光致發光強度與 Tb3+濃度為正比關係且呈線性增加,然而在
Tb3+濃度為 1 mol % 時,其輝度值與放光強度不符,其原因是由於摻 雜 1mol % Tb3+,時主體在紫外光區的自放光貢獻較大之故,除此之 外,放射光譜的積分面積變化趨勢與放射強度變化則趨近一致,皆在 30 mol % Tb3+摻雜時為最高。另外,經由比較發現,最佳化學組成 (Y0.7Tb0.3)Ba3(BO3)3其發光強度約為商品的 55%,而相對輝度僅只有 商品之 32%。
5-1-2-2 激發光譜之研究
圖 5-10 YBa3(BO3)3激發光譜 (em= 343nm) 圖 5-10 為以波長 343 nm 監控 YBa3(BO3)3主體所得之激發光譜, 其吸收範圍約在 125 至 240 nm 之間,最強吸收峰波長位在 174 nm。硼酸鹽系統中,B-O 鍵結軌域及反鍵結軌域的能量差為 120 ~ 180 nm 之間,因此 YBa3(BO3)3主體激發帶主要源自 BO3 3-陰離子團的吸收[35]。 此外,主體的激發帶其部分也可能包含 O 2-→Y3+ 的電荷遷移帶(charge transfer band),即 O2−之 2p6 至 Y3+ 之 4p6 (4d+5s)軌域的電子躍遷。 O2-→Y3+之電荷遷移帶,依據晶格中 Y3+ 之配位數及 Y-O 鍵長的不同 而落在 150 ~ 210 nm 皆有可能[36] ,而圖 5-10 中主體吸收峰其波長符 合上述發生 O 2-→Y3+電荷遷移之範圍。因此,經由以上所述可以合理 推論 YBa3(BO3)3主體的激發帶是由 BO3 3-陰離子團及 O 2-→Y3+ 之 CTB 兩種吸收重疊而成。 另外,從圖 5-10 中可發現當波長為 172 nm 時,螢光粉之吸收強 度良好,由此可以說明 YBa3(BO3)3 為一良好的真空紫外光激發螢光 粉。由於主體在波長 172 nm 之吸收遠優於 147 nm,因此本研究選擇 172 nm 作為激發光源以量測 YBa3(BO3)3:Tb 3+ 光致發光光譜,如圖 5-3 至圖 5-8 所示。
圖 5-11 (Y0.7Tb0.3)Ba3(BO3)3之激發光譜 (em= 543nm) 圖 5-11 為摻雜 30% Tb3+ (Y0.7Tb0.3)Ba3(BO3)3的激發光譜,以 543 nm 波長監控,其最強的吸收峰波長為 243 nm,在 220 ~ 300 nm 之範 圍主要為 Tb3+ 的 4f8 -4f75d 吸收躍遷[37],當 Tb3+內一個電子被激發至 5d 軌域時,其激發態的組態可能有兩種,分別為高自旋態 9DJ或低自 旋態7 DJ,波長 220 至 265 nm 範圍屬於 7 FJ → 7 DJ躍遷;而 265 ~ 300 nm 間則為 7 FJ → 9 DJ之躍遷。此兩吸收峰強度的差別可以用 Hund’s rule 解釋,前者是 7FJ → 7 DJ,屬於 spin-allowed 的 f-d 躍遷,因此具有較 高的吸收強度;而後者是 7FJ → 9 DJ,為 spin-forbidden 的 f-d 躍遷,故 強度較低。
同樣,在圖 5-11 中,波長短於 200 nm 之吸收帶其波形看似複雜, 可能源自數種不同的吸收峰相疊而成。首先對照圖 5-10 及圖 5-11, 可發現此峰範圍涵蓋主體之吸收帶,因此推測此吸收帶有主體吸收之 貢獻。此外,根據 Jorgensen Eq.計算[38] ,Tb3+之電荷遷移帶其理論值 為 67500 cm-1 ,即 167 nm,而圖中 175 nm 處的吸收峰其與理論值 167 nm 相近,因此可確定此處亦有 O2-→Tb3+之 CTB 的貢獻。圖 5-12 為 Tb3+摻雜濃度分別為 1%、10%及 20%之 YBa3(BO3)3:Tb 3+激發光譜, 圖中顯示波長 175 nm 之吸收峰隨著 Tb3+濃度增加,其吸收強度也隨 之上升,由此可再次證明此處為 YBa3(BO3)3:Tb 3+ 之 O 2-→Tb3+ CTB。
綜合以上所述,在激發光譜中,主體吸收帶和 O2-→Tb3+ CTB 之 重疊;及光致發光光譜中,Tb3+主峰與主體自放光波峰的消長情形, 可說明 YBa3(BO3)3: Tb 3+ 螢光粉其主體與活化劑 Tb3+之間具有良好的 能量傳遞現象。
5-1-3
CIE 色度座標之分析
為了探討 YBa3(BO3)3: x%Tb 3+ 系列螢光粉其摻雜不同 Tb3+濃度 樣品之色度,本研究利用色度計量軟體計算各 Tb3+濃度的螢光粉在波 長 172 nm 激發下之 CIE 色度座標,其結果如表 5-1 所示。摻雜 1 mol % Tb3+的光譜由於其主體放光貢獻較大,其色度座標值落在 (0.25, 0.43);摻雜 5% 及 10% Tb3+的樣品之 CIE 色度座標為(0.28, 0.57);而 摻雜 20% 及 30% Tb3+ 的光譜沒有主體放光的貢獻,其 CIE 色度座標
值在(0.29, 0.61)處。圖 5-13 為最適化濃度(Y0.7Tb0.3)Ba3(BO3)3與商品
的 CIE 色度座標圖,商品 Zn2SiO4:Mn
2+
數值為(0.16, 0.72),以三角形
表示;而星號則表示本研究之樣品(Y0.7Tb0.3)Ba3(BO3)3,其色度座標
值為(0.28, 0.57),若以肉眼觀察其色光為黃綠色,為典型 Tb3+螢光粉
表 5-1 YBa3(BO3)3: x%Tb3+系列螢光粉 CIE 色度座標值之比較 Tb3+ / mol % x座標值 y座標值 1 0.25 0.43 5 0.28 0.57 10 0.28 0.57 20 0.29 0.61 30 0.29 0.61
圖 5-13 (Y0.7Tb0.3)Ba3(BO3)3螢光粉與 Zn2SiO4:Mn2+商品 CIE 色度座標之比較
5-1-4
掃描式電子顯微鏡影像之分析
圖 5-14 為 1100℃燒結 8 小時所得到的(Y0.7Tb0.3)Ba3(BO3)3螢光
粉之 SEM表面微結構影像。圖中晶粒形狀多呈現不規則,且多聚集
成較大塊狀,此現象是由於(Y0.7Tb0.3)Ba3(BO3)3係以固態法燒結合成,
因此容易造成顆粒不均勻。
5-2 Ca5Al6O14:Eu
2+系列螢光體之研究
5-2-1 主體合成探討與晶相分析之研究
本實驗採傳統的高溫固態法合成 Ca5Al6O14:Eu 2+,其詳細製程如 4-3-2 節所述。由於鋁酸鹽類的競爭相很多,因此 Ca5Al6O14粉體其合 成條件相當嚴苛,只有在 1200℃下才能合成純相。圖 5-15 為合成溫 度 1200℃下所製備 Ca5Al6O14的 X 光粉末繞射圖譜,將所得圖譜與 JCPDS 資料庫進行比對,發現其繞射峰與 JCPDS 卡號 00-009-0413 所 述 幾乎 完 全吻 合, 比對 結 果顯 示所 合 成之 粉體 為 結晶 性佳 的 Ca5Al6O14。因此後續進行 Eu 2+ 離子的摻雜時,皆以上述條件來進行。 圖 5-15 於 1200℃下所製備 Ca5Al6O14之 X 光粉末繞射圖譜若考慮陽離子配位數與其有效半徑之關係[29,30],在 Ca5Al6O14晶 格中,Ca2+ 具三種格位及兩種配位方式,分別是六配位(1Å )及八配位 (1.17Å ),而 Eu2+在此兩種配位環境下之離子半徑分別為 1.17 Å (六配 位)和 1.25 Å (八配位),兩者半徑皆相似,因此合理推論 Eu2+極有可能 對晶格中三種格位分別進行取代,但就結構上仍無法判定其取代之狀 況。圖 5-16為分別摻雜 0.1~3%莫耳比例 Eu2+之(Ca,Eu)5Al6O14 X 光粉 末繞射圖譜,可發現摻雜 Eu2+後,隨著其摻雜濃度之增加,繞射峰出 現寬化的現象,若忽略 2θ=31.4°處之雜相,基本上繞射圖譜仍然維 持相似的晶相圖形。 圖 5-16 不同 Eu2+濃度取代(Ca 1-xEux)5Al6O14 XRD 圖譜之比較 (*為 CaAl4O7)
5-2-2 螢光光譜與發光特性分析
5-2-2-1 光致發光光譜之研究
圖 5-17 為以真空紫外光 172 nm 激發未摻雜 Eu2+ 的 Ca5Al6O14主 體所得之光致發光圖譜。由圖可知,其自身活化放光為一介於 300 nm 至 450 nm 之高強度的寬帶放射,最強放射波長位於 318 nm 處,為紫 外光範圍。 圖 5-17 Ca5Al6O14發光光譜 (ex= 172nm) 圖 5-18 為(Ca0.999Eu0.001)5Al6O14及(Ca0.98Eu0.02)5Al6O14於波長 172 nm 激發所得之光致發光光譜,可觀察到主體摻雜活化劑 Eu2+後的放 光特性,呈現寬帶放射。圖中可分為兩部分加以討論,波長範圍小於390 nm 及 390 ~ 530 nm 處各有一 放射峰。390 nm 以下之波段其最強 放射位於 315 nm,若對照 Ca5Al6O14主體的放射光譜(圖 5-16),可得 知此放射帶是源自於主體的貢獻;而波長在 390 ~ 530 nm 之區域則為 Eu2+的 4f6 5d1→4f7 (8S7/2)放射躍遷,最高峰值位在 432 nm 處。 圖 5-18 (Ca0.999Eu0.001)5Al6O14及(Ca0.98Eu0.02)5Al6O14發光光譜之比較 (ex= 172nm) 此外,圖中顯示(Ca0.999Eu0.001)5Al6O14的放光具有上述兩種波峰, 而(Ca0.98Eu0.02)5Al6O14 光譜中主體部分訊號消失,只見後者之放射, 並且 Eu2+訊號增強。由以上現象可以合理推論:在(Ca1-xEux)5Al6O14 系統中,主體可以有效地將其所吸收的能量傳遞至活化劑,進而增強 螢光粉之放光。

![圖 3-5 KCaPO 4 晶體結構示意圖 3-5 Li 4 SrCa(SiO 4 ) 2 Li 4 SrCa(SiO 4 ) 2 晶體屬於正交晶系(orthorhombic),於 1995 年時由 Annapoorna 等人 [25] 報導其晶體結構與摻雜 Eu 2+ 離子之螢光粉在紫外 光 波 段 激 發 下 的 發 光 特 性 。 Zhang 等 人 [26] 也 研 究 了 Li 4 SrCa(SiO 4 ) 2 :Eu 2+ ,Mn 2+ 的發光特性及能量傳遞,](https://thumb-ap.123doks.com/thumbv2/9libinfo/8511607.185903/37.893.265.681.108.460/時由等人報導其晶體結構與摻雜+離子之螢光粉特性人研.webp)






