國 立 交 通 大 學
應用化學系碩士班
碩士論文
使用離心分配層析法
分離桑葉中的有效成分
Separations of Active Compounds
in Mulberry Leaves Using
Centrifugal Partition Chromatography
研 究 生:王柏森
指導教授:余艇 博士
使用離心分配層析法
分離桑葉中的有效成分
Separations of Active Compounds
in Mulberry Leaves Using
Centrifugal Partition Chromatography
研 究 生:王柏森 Student:Bo-Sen Wang 指導教授:余 艇 博士 Advisor:Dr. Tiing Yu 國立交通大學 應用化學系碩士班 碩士論文 A Thesis
Submitted to M. S. Program, Department of Applied Chemistry National Chiao Tung University
in Partial Fulfillment of the Requirement for the Degree of
Master of Science In
Applied Chemistry September 2012
Hsinchu, Taiwan, Republic of China.
I
使用離心分配層析法
分離桑葉中的有效成分
學生:王柏森 指導教授:余 艇 國立交通大學應用化學系碩士班 摘要 本研究利用離心分配層析來分離桑葉中的有效成分,Chlorogenic acid、 Isoquercitrin 、 Astragalin 、 Quercetin 3-(6-malonylglucoside) 和 Kaempferol 3-(6-malonylglucoside)。桑葉經由 60% (v/v)的乙醇萃取後所獲得的有效成分先經由高效能液相層 析串聯質譜進行初步鑑定,然後再使用乙酸乙酯和去離子水做批式萃取。本實 驗中使用離心分配層析的溶劑系統,為三成分溶劑系統(methyl t-butyl ether /acetone/H2O =6:4:10、7:3:10、8:2:10) 和 (methyl t-butyl ether /acetone/
H2O = 6:4:10、7:3:10、8:2:10)並加入溶劑系統總體積 0.6% (v/v)的 formic
acid、四成分溶劑系統(methyl t-butyl ether /acetone/H2O/EA =7:3:10:2) 和
(methyl t-butyl ether /acetone/ H2O/EA = 7:3:10:2)並加入溶劑系統總體積 0.6%
(v/v)的 formic acid,都是以上層有機相當作靜相,下層水相當作動相。在 900 rpm
II
前處理後的樣品經由離心分配層析製備分離,並使用紫外光-可見光譜儀線上偵 測系統,沖提液以分管收集器每 3 mL 收集一管,再以高效能液相層析分析各 收集管中不同成分的純度。在桑葉樣品中,所得到的純度分別為 Chlorogenic acid (70.2%),Isoquercitrin (97.3%),Astragalin (97.2%),Quercetin 3-(6-malonylglucoside) (69.1%),Kaempferol 3-(6-malonylglucoside) (69.6%)。
III
Separations of Active Compounds
in Mulberry Leaves Using
Centrifugal Partition Chromatography
Student : Bo-Sen Wang Advisor : Tiing Yu
M. S. Program, Department of Applied Chemistry National Chiao Tung University
Abstract
Separations of active compounds, including Chlorogenic acid, Isoquercitrin, Astragalin, Quercetin 3-(6-malonylglucoside) and Kaempferol 3-(6-malonylglucoside) in mulberry leaves, were carried out using centrifugal partition chromatography (CPC) in this study.
These five components in the crude extract by 60% (v/v) ethanol were first identified using HPLC-MS. After pre-extractions using ethyl acetate and water, we used solvent systems, (methyl t-butyl ether /acetone/H2O =6:4:10、7:3:10、8: 2:10) and (methyl t-butyl ether /acetone/ H2O = 6:4:10、7:3:10、8:2:10)
added with 0.6% (v/v) formic acid, four solvent systmes (methyl t-butyl ether /acetone/H2O/EA =7:3:10:2) , (methyl t-butyl ether /acetone/ H2O/EA = 7:3: 10:2) added with 0.6% (v/v) formic acid, to separate sample extracts. The descending elution mode was applied, i.e. the lower aqueous layer was used as the
IV
mobile phase, and the upper organic layer as the stationary phase. Under 900 rpm, the volume of the stationary phase retained was 188 mL in the separation cells of a total volume 240 mL; stationary-phase retention ratio was 78%. The CPC effluent monitored using an on-line UV/Vis detector was fraction-collected every 3 mL, and the fractions were further analyzed using HPLC . The purities were 70.2%, 97.3%, 97.2%, 69.1% and 69.6% for Chlorogenic acid, Isoquercitrin, Astragalin, Quercetin 3-(6-malonylglucoside) and Kaempferol 3-(6-malonylglucoside), respectively, under the optimized separation.
V
謝誌
畢業了!碩士班的生涯終於到了一段落了,這段時間的點點滴滴,都讓我印 象深刻,不論是愉快的,抑或是難過的,都是很好的經驗,在面對困難的時, 我總是告訴自己,上帝只會給你挺得過的考驗,這句話成為我的精神糧食,讓 我渡過重重的難關。 首先我要感謝恩師余艇,給予我實驗上的指導,以及讓我能如期去實習, 並在實習期間完成實驗及論文,這段時間老師也全力指導我完成論文以及口試, 真是辛苦老師了;感謝王念夏老師、許馨云老師,百忙中抽空來參加我的口試 與指導我論文應該注意的細節。 我特別要感謝台大李水盛教授,非常熱心的借我實驗的儀器,以及讓我到 台大去做實驗,讓我能夠順利的完成實驗;更要感謝李教授實驗室的學生,不 論在實驗上以及生活上都給予我很大的幫助,讓我能夠很方便的做實驗。 接著我要感謝泓哲、俐揚、沛穎,不論是學業或是實驗上都給我許多的幫 助,特別要感謝泓哲與俐揚,辛苦的清理實驗室的藥品與廢棄物、報帳、報廢 儀器等等,並處理了許多大大小小的事物。 最後我要感謝我的家人以及朋友們,還有在困難重重的實驗生活中所遇到的 許多貴人,有所有人的幫忙與支持,我才能夠如此順利的完成學業,在此我獻 上最大的感謝,謝謝。我終於畢業了!!VI 總目錄 摘要 ... I Abstract ... III 謝誌 ... V 第一章 緒論 ... 1 1.1 前言 ... 1 1-2 研究動機 ... 2 第二章 研究背景與文獻回顧 ... 3 2.1 桑葉的介紹 ... 3 2.1.1 桑葉的成分 ... 3 2.1.2 桑葉成分的功效 ... 3 2.1.3 桑葉中的有效成分與抗氧化作用的關係 ... 4 2.1.3.1 自由基簡介 ... 4 2.1.3.2 抗氧化劑 ... 4 2.2 逆流層析技術 ... 7 2.2.1 簡介 ... 7 2.2.2 逆流層析的分離理論 ... 8 2.2.3 逆流層析的儀器系統[20;21] ... 10
VII
2.2.4 逆流層析的特點 ... 14
2.3 離心分配層析 (centrifugal partition chromatography, CPC) ... 14
2.3.1 原理[22] ... 14 2.3.2 移動相與固定相的流動模式 ... 17 2.3.3 溶劑系統的選擇[24;25] ... 18 2.3.4 影響固定相滯留量的因素 ... 18 2.3.5 離心分配層析儀的應用 ... 19 第三章實驗 ... 20 3.1 實驗樣品和溶劑 ... 20 3.2 實驗儀器 ... 21 3.3 實驗流程 ... 23 3.3.1 桑葉的前處理流程 ... 23 3.3.3 純度的估計 ... 27 3.3.4 回收量的估計 ... 28 3.3.5 CPC 製備實驗步驟 ... 28 3.3.6 HPLC 分析收集液實驗步驟 ... 30 第四章 結果與討論 ... 31 4.1 以高效能液相層析串聯質譜儀分析鑑定桑葉萃取液 ... 31
VIII 4.2 以高效能液相層析串聯質譜儀分析鑑定批式萃取後的桑葉樣品 ... 35 4.2.1 以高效能液相層析串聯質譜儀分析鑑定批式萃後得到的 sample 1 .... 35 4.2.2 以高效能液相層析串聯質譜儀分析鑑定批式萃後得到的 sample 2 .... 37 4.3 以離心分配層析儀分離桑葉成分的實驗結果 ... 40 4.3.1 sample 1 分離的結果 ... 44 4.3.1.1 溶劑系統 MTBE / Acetone / H2O ... 44
4.3.1.2 溶劑系統 MTBE / Acetone / H2O/EA... 49
4.3.2 sample 2 分離的結果 ... 51
4.3.2.1 溶劑系統 MTBE / Acetone / H2O ... 51
4.3.2.2 溶劑系統 MTBE / Acetone / H2O/EA... 56
第五章 結論 ... 58
IX 圖目錄 圖 1、黃酮類基本結構 ... 5 圖 2、桑葉中五種成分的結構圖 ... 6 圖 3 、液相-液相層析方法 ... 9 圖 4、流體靜態平衡系統(HSES)示意圖[18] ... 11 圖 5、流體動態平衡系統(HDES)示意圖[19] ... 13 圖 6、CPC 儀器示意圖[22] ... 16 圖 7、CPC 的兩種流動模式[22] ... 17 圖 8、桑葉前處理的流程 ... 25 圖 9、三次批式萃取示意圖 ... 26 圖 10、CPC 實驗儀器裝置 ... 29 圖 11、HPLC 實驗儀器裝置 ... 30 圖 12、HPLC 分析桑葉萃取液的層析圖 ... 31 圖 13、peak a 測 ESI-MS 正電荷質譜圖 ... 32 圖 14、peak b 測 ESI-MS 正電荷質譜圖 ... 32 圖 15、peak c 測 ESI-MS 正電荷質譜圖 ... 33 圖 16、peak d 測 ESI-MS 正電荷質譜圖 ... 34 圖 17、peak e 測 ESI-MS 正電荷質譜圖 ... 34 圖 18、HPLC 分析 sample 1 的層析圖 ... 35
X 圖 19、peak b 測 ESI-MS 正電荷質譜圖 ... 36 圖 20、peak c 測 ESI-MS 正電荷質譜圖 ... 36 圖 21、HPLC 分析 sample 2 的層析圖 ... 37 圖 22、peak a 測 ESI-MS 正電荷質譜圖 ... 38 圖 23、peak d 測 ESI-MS 正電荷質譜圖 ... 38 圖 24、peak e 測 ESI-MS 正電荷質譜圖 ... 39 圖 25、CPC 分離 sample 1 的層析圖 ... 46 圖 26、HPLC 分析波峰Ⅰ、II、 III 的層析圖 ... 48 圖 27、CPC 分離 sample 1 的層析圖 ... 50 圖 28、CPC 分離 sample 2 的層析圖 ... 53 圖 29、HPLC 分析波峰 A、B、C、D 的層析圖 ... 55 圖 30、CPC 分離 sample 2 的層析圖 ... 57
XI 表目錄 表 1、 EA/BuOH/H2O 三成分溶劑系統,測試在不同組成比例中,桑葉中五種 目標物的分配係數值(KD) ... 40 表 2 、MTBE/Acetone/H2O 三成分溶劑系統,測試在不同組成比例中, Isoquercitrin、Astragalin 的分配係數值(KD) ... 41
表 3、MTBE/Acetone/H2O 三成分溶劑系統加 0.6% formic acid,測試在不同組成
比例中,Chlorogenic acid、Q3MG、K3MG 的分配係數值(KD) ... 42
表 4、在 MTBE:Acetone:H2O=7:3:10 的溶劑系統中,加入不同比例的 EA,所得
Isoquercitrin、Astragalin 的分配係數值(KD) ... 43
表 5、在 MTBE:Acetone:H2O=7:3:10 加 0.6% formic acid 的溶劑系統中,加入不
同比例的 EA,所得 Chlorogenic acid、Q3MG、K3MG 的分配係數值(KD) 43
表 6、CPC 分離 sample 1 的實驗參數 ... 44 表 7、Isoquercitrin 和 Astragalin 兩種成分在溶劑系統 MTBE / Acetone / H2O 的
分配係數值 ... 45 表 8、CPC 分離 sample 1 的實驗參數 ... 49 表 9、Isoquercitrin 和 Astragalin 兩種成分在溶劑系統 MTBE / Acetone / H2O/EA
的分配係數值 ... 50 表 10、CPC 分離 sample 2 的實驗參數 ... 51 表 11、Chlorogenic acid、Q3MG 和 K3MG 三種成分在溶劑系統 MTBE / Acetone
XII
/ H2O 加 0.6% (v/v) formic acid 的分配係數值 ... 52
表 12、CPC 分離 sample 2 的實驗參數 ... 56 表 13、Chlorogenic acid、Q3MG 和 K3MG 三種成分在溶劑系統 MTBE / Acetone / H2O/EA 加 0.6% (v/v) formic acid 的分配係數值 ... 56
1 第一章 緒論 1.1 前言 桑(桑葉、桑果、桑枝)早已被中醫學確認為藥食兩用的材料,藥效極好並廣 泛,可降糖、血壓、血脂、膽固醇、尿酸,亦有通血管、通便、利關節、安寧 等療效。中醫認為桑的療效廣泛,有止咳去熱,治療頭昏眼花、消除眼部疲勞、 消腫、清血,治痢疾、腹痛,有補肝、美膚等功效。 在近年來的研究中發現,幹桑葉中含粗蛋白 25%~45%,碳水化合物 20% ~25%,粗脂肪 5%,以及豐富的鉀、鈣和維生素 C、B1、B2、A 等,還有各種 微量元素銅、鋅、硼、錳等物質。桑葉中含有蛻皮固酮、羽扁豆酮、芸香甙、 桑甙、維生素、絛原酸、葉酸、延胡索酸、內消旋肌酸、植物雌激素等人體所 需物質。
離心分配層析(Centrifugal partition chromatography, CPC),是一種不使用固 體支撐固定相(support-free liquid stationary phase)的液相-液相層析技術,因為 CPC 是使用中空的管柱,在沖提過程中,管柱內部的固定相占總管柱的體積比 例往往可達到 60%以上,由於管柱中含有大量的固定相,所以比起典型的高效 能液相層析(high performance liquid chromatography, HPLC)更適合用來分離大量 的樣品。因此 CPC 目前被定位在製備型的層析儀器,可應用在天然物的分離, 能製備大量的天然物標準品,對於醫學或藥物開發的相關研究有著莫大的幫 助。
2
1-2 研究動機
本研究中,我們希望利用離心分配層析的技術,搭配有機-水相溶劑系統, 並找出最合適用來分離桑葉萃取物的 CPC 溶劑系統,使得桑葉樣品在移動相及 固定相有較理想的分佈,以期望達到分離、純化桑葉中的有效成分,包括 Chlorogenic acid ( 綠 原 酸 ) 、 Isoquercitrin 、 Astragalin 、 Quercetin 3-(6-malonylglucoside)(Q3MG)、Kaempferol 3-(6-malonylglucoside) (K3MG)等, 藉由 CPC 製備分離這五種有效成分的標準品,期望在醫學研究、藥物或保健食 品開發都能有所貢獻。
3 第二章 研究背景與文獻回顧 2.1 桑葉的介紹 2.1.1 桑葉的成分 桑葉為桑科植物,在古書籍中又稱神仙葉,世界最早的藥書《神農本草經》 記載:“桑葉除寒熱、出汗。”《本草綱目》:“治勞熱咳嗽,明目,長髮。” 《重慶堂隨筆》說 “桑葉,雖治盜汗,而風濕暑熱服之,肺氣清肅,即能汗解。 息內風而除頭痛,止風行腸胃之泄瀉,已肝熱妄行之崩漏,胎前諸病,由於肝 熱 者 尤 為 要 藥 。 ” 根 據 文 獻 [1;2;3] 的 研 究 , 桑 葉 中 存 在 Quercetin 3-(6-malonylglucoside)(Q3MG) 、 Chlorogenic acid 、 Isoquercitrin 、 Astragalin 、 Kaempferol 3-(6-malonylglucoside)(K3MG)這幾種主要的抗氧化物,大部分屬於 黃酮類(Flavonoid)的一種衍生物。 2.1.2 桑葉成分的功效 文獻指出[4;5;6],桑葉萃取物中,含有可做為葡萄糖苷酶抑制劑的成分,具 有抑制糖尿病的效果。桑葉成分具有神經保護作用、美白的功效、抗發炎[7;8;9]。 在文獻中證實[10;11;12],桑葉成分中的 Isoquercitrin、Q3MG 可以有效的抑 制低密度脂蛋白氧化。Chlorogenic acid 的功用包括阻止小腸吸收葡萄糖、阻止 肝糖酵素釋放葡萄糖進入血液、幫助脂肪燃燒和提供能量給肌肉等[13;14]; Astragalin[15;16]有助於減少發炎反應和止癢的功用;K3MG[17]具有預防罹患動 脈粥樣硬化之相關病症。
4 2.1.3 桑葉中的有效成分與抗氧化作用的關係 2.1.3.1 自由基簡介 身體代謝產生的游離電子或帶未鍵結電子的分子稱為自由基。少量自由基 是免疫系統釋出以破壞病毒或細菌,部份則參與製造荷爾蒙和活化酵素,細胞 粒腺體也需自由基激發電子傳遞鏈產生能量。過多自由基則具有攻擊性,會結 合或破壞細胞組織,故自由基也被視為心臟病和癌症的起源,且導致老化的主 因。 對人體產生重大影響的自由基形式以氧為中心,氧自由基使膠原蛋白和彈 性蛋白分解,使皮膚鬆弛、出現皺紋等等,以及促使蛋白質、核苷酸、脂肪的 代謝異常,細胞因此產生突變而引起疾病侵害細胞的正常生理機能,導致各種 疾病的發生,加速人體老化,甚至基因突變引起癌症。 2.1.3.2 抗氧化劑 抗氧化劑可定義為「能減緩或阻止氧化傷害的物質」。 抗氧化劑的作用: (1)藉著酶的催化或自身參與反應,除去自由基、氧化衍生物 (2)減少氧化衍生物的形成 (3)修復遭到攻擊的細胞 (4)摧毀受損太嚴重的細胞,並再形成一個新的細胞。
5
黃酮類的基本結構如圖1,桑葉中的有效成分大部分屬於黃酮類的一種衍生物, 含有抗氧化的能力,可以用來去除自由基,使用在食品中以控制酸敗,而添加 在飲食中則為防止癌症、慢性病及延遲老化的發生。
6
Chlorogenic acid Quercetin 3-(6-malonylglucoside)
Isoquercitrin Astragalin
Kaempferol 3-(6-malonylglucoside) 圖 2、桑葉中五種成分的結構圖
7 2.2 逆流層析技術 2.2.1 簡介 逆流層析[18]是一種固定相、移動相皆為液體的液相-液相層析,沖提過程 中能夠完全排除樣品對於固體固定相的不可逆吸附,造成對樣品的汙染問題或 管柱阻塞的問題。在沖提過程中利用樣品中不同分析物對於兩相溶劑之間分配 係數(partition coefficient)的相異而分離。 逆流層析技術的發展,起源於二十世紀 50 年代的逆流分佈法(countercurrent distribution, CCD) [19],它是一種不連續式的萃取方式,通常以數百個玻璃的分 離管進行萃取,但是因為儀器本身過於複雜且龐大,而過程中也需要比較長時 間來分離。直到 70 年代時,出現了一套液滴逆流層析(Droplet Counter Current Chromatography, DCCC)技術屬於流體靜力平衡系統(Hydrostatic equilibrium system, HSES)的一種。而 Y. Ito 等人對於之前的基礎理論開始深入研究,進而 發 展 出 逆 流 層 析 (countercurrent chromatography, CCC) ; 在 1982 年 Sanki Engineering Ltd. (Kyoto, Japan)也研發出了離心場不同於 CCC 的另一種離心分配 層析(centrifugal partition chromatography, CPC)儀器設備。
8
2.2.2 逆流層析的分離理論
逆流層析分離的基礎[20;21]是建立於逆流分佈法,CCD 是一種非連續式 的萃取方式,其過程可以用圖 3(A)說明:假設有多個連續萃取槽,分析物最初 在 L0中,而 U0、U1….Un和 L0、L1….Ln分別為不含分析物的兩相(U 代表上層液
相;L 代表下層液相)。當 U0和 L0混合後,分析物在上層相與下層相中分配, 達到平衡時,U0會萃取走部分分析物,再接著與 L1混合,完成平衡後,再依序 與 L2、L3….Ln混合;新的上層相 U1、U2….Un依序與 U0做相同的萃取動作。由 二項式定理可知,大部分的分析物最後會集中於某幾個萃取槽中。若一開始含 有兩種對於上下層相有著不同分配係數的分析物,藉由增加萃取槽的數目,就 可以提高分離的解析度,然而隨著萃取的次數增加,分析物的分佈也會變的比 較寬(broad)。 圖 3(B),為液相-液相分配層析法,亦是 CCD 基礎概念的延伸。分析物在 多個萃取槽間連續進行分配萃取,不同的物質會因為對於相與相之間的分配係 數不同而產生分離的情形,此為液相層析的基礎觀點。 圖 3(C),為一般所熟知 的液相層析,藉由管柱中填充的固體支持物(固定相),使液體以物理性吸附或化 學鍵結方式留在固體支持物的表面。相較之下,前者的缺點為,因為物理性吸 附若造成固定相容易在沖提過程中溶解在移動相中而減少,而後者之固定相雖 不會被移動相帶走,但卻會因為與分析物的吸附,造成層析峰的拖尾現象。
9 圖 3 、液相-液相層析方法 (A) 傳統步驟式液相萃取。 (B) 逆流萃取(CCE),兩相都是移動相,分別往反方向移動。 (C) 液相-液相層析(LLC),固定相是以固體支持物滯留在管柱中。 固體支持物 液相 樣品注入
10 2.2.3 逆流層析的儀器系統[20;21] 為 了 能 發 展 逆 流 層 析 成 為 實 用 的 層 析 儀 器 , 陸 續 開 發 出 具 有 穿 流 (Flow-through)性質、不同管柱結構和不同力場的儀器。因此,逆流層析的儀器 系統依分離的管柱本身的轉動方式可區分為兩種:流體靜態平衡系統和流體動 態平衡系統。
(1) 流體靜態平衡系統(Hydrostatic Equilibrium System,HSES)
在 HSES 系統中,管柱每一個部份所受力大小固定。固定相因重力場而滯 留在管柱中,樣品隨著移動相穿越固定相,並藉著樣品在移動相與固定相中的 分配係數不同而達到分離。圖 4 為 HSES 示意圖。圖 4(A),所使用的移動、固 定相事先平衡過,選擇固定相為下層相,先使其充滿管柱後將移動相(上層相) 由一端緩緩的注入,固定相會被移動相推出直到兩相的界面到達螺管底部,此 時由於重力場的作用,移動相開始往上穿越固定相直到螺管頂端,如此一直重 複直到分離管柱的末端,其每一圈的螺管都會保留住一半的固定相。圖 4(B)和 4(A)相反,使用平衡過的上層相當作固定相,而下層相為移動相,因此移動相與 固定相在螺管中會產生不同的平衡狀態。
11
圖 4、流體靜態平衡系統(HSES)示意圖[18] (A) 固定相為下層相,移動相為上層相。 (B) 固定相為上層相,移動相為下層相。
(2) 流體動態平衡系統(Hydrodynamic Equilibrium System,HDES)
在 HDES 系統中,螺旋管柱會藉由轉動所產生的扭力及離心力,將固定相 滯留在管柱中,這扭力是由希臘數學家阿基米德發現,藉由轉動螺旋形的管子, 可將河水取至水壩,此即所謂阿基米德扭力(Archimedes screw force)。此原理亦 被應用在 HDES 系統中。若螺旋管柱內存在有輕重兩相,受阿基米德扭力及重 力之作用下,輕重兩相因為受力不均,而在管柱中有不同的分佈,圖 5 說明在 重力場作用下,阿基米德扭力對旋轉中螺管的影響、圖 5(a)先將螺旋管中注滿水, 再導入氣泡或玻璃珠,封住螺管兩端,接著將螺管緩慢旋轉,由於阿基米德扭 力的作用,將使氣泡與玻璃珠帶往螺管的左端,此表示不管比水輕或比水重的
12 物質皆會向螺管的某一端移動,此端稱為螺管的頭端(head),而另一端則稱為尾 端(tail)。圖 5(b)中,利用平衡過的溶劑系統進行相同的實驗,圖 5(b)上圖是先將 螺管注滿較輕的一相,也就是溶劑系統的上層相,而較重的一相則由尾端打入, 此時較重的一相行為就像是水中的玻璃珠會往頭端移動,圖 5(b)下圖則先將較重 的一相注滿螺管,由尾端打入較輕的一相,其行為就像是水中的氣泡。圖 5(c), 先將螺管內填入等體積的輕重兩相,兩相會在螺管的每一圈形成分離,當螺管 開始轉動,任一相多餘的量則會被推至螺管尾端。因此,當螺管達到動力學平 衡,則兩相在螺管中的分佈將保持不變,使固定相維持程度的滯留。
13
圖 5、流體動態平衡系統(HDES)示意圖[19]
(a)將螺旋管中注滿水,再導入氣泡或玻璃珠,封住螺管兩端。 (b)先將較重的一相注滿螺管,由尾端打入較輕的一相。
14 2.2.4 逆流層析的特點 現代逆流層析技術為化合物的分離純化提供了一種新的方法,有別於一般 的高效液能層析管柱,它無需固體作固定相,所以不存在固體對樣品的吸附、 變性、失活、拖尾等現象,且能達到很高的回收率,節省昂貴的材料和溶劑的 消耗。逆流層析在不需更換不同極性的層析管柱情況下,藉由提高極性溶劑或 非極性溶劑比例的方法,可以實現流動相從弱極性到強極性或相反的轉變。由 於層析管柱容積大,無填充料,管柱內的空間幾乎全部都是有效空間,因此樣 品的負載能力強,製備分離量大,再現性好。
2.3 離心分配層析 (centrifugal partition chromatography, CPC)
2.3.1 原理[22] 離心分配層析屬於流體靜力平衡系統的一種,其儀器設計原理如圖 2-6 所示, 層析管柱由一系列刻在圓盤或圓筒內的導管相聯的柱體組成,依管徑大小的不 同管柱又可分為兩種,管徑小的稱 duct,主要是移動相流動的通道,管徑大的 稱 channel,滯留固定相的管柱部分,透過單軸旋轉產生恆定的重力場,固定相 被滯留在管柱中。管柱中兩個旋轉密封的接口分別連接移動相的進口和出口, 移動相是以液滴的形式在固定相中傳遞,樣品成分會在液滴的表面進行分佈, 因為不同的物質有不同的分配係數,因此經由自動化且連續式的萃取,就可以 把樣品成分分離。
15
(A)
16 (C) 圖 6、CPC 儀器示意圖[22] (A) CPC 外部構造與蝕刻在圓盤上的層析管柱。 (B) CPC 內部結構,由一系列圓盤組成。 (C) CPC 管柱中運作原理,移動相是以液滴的形式在固定相中穿越流析。
17 2.3.2 移動相與固定相的流動模式 根據 CPC 分離時實驗條件的不同,可以選擇其中一相當作固定相,另一相 則當作移動相,固定相與移動相可以互相交換。因此存在兩種模式,一種是上 升法(ascending mode) ,移動相的行進方向與重力場反方向;另一種是下降法 (descending mode) ,移動相的行進方向與重力場同方向,如圖 7 所示,上升法 是以下層相當作固定相,上層相當作移動相;下降法則是以上層相當作固定相, 下層相當作移動相。 圖 7、CPC 的兩種流動模式[22] 上圖:上升模式,下層相當作固定相,上層相當作移動相。 下圖:下降模式,上層相當作固定相,下層相當作移動相。
18 2.3.3 溶劑系統的選擇[24;25] 大部分的溶劑系統為兩相溶劑系統,通常包含水,加上其他有機溶劑,相 互達到飽和而成為不互溶的兩相溶劑,分別為移動相和固定相。其溶劑的成分 組合視其實驗的分離條件而決定。在離心分配層析當中,溶劑系統的選擇有幾 點必須注意:(1) 樣品有充分的溶解度 (2) 樣品不會被分解和去活性 (3) 適當 的分配係數 (4) 良好的固定相滯留量。 2.3.4 影響固定相滯留量的因素 在離心分配層析中,液體固定相在管柱中滯留的多寡影響了分離的效率, 在較高的固定相滯留量下可提高對樣品的承載量和分離的解析度。影響固定相 滯留量及分離的效率的因素分為下列幾點[26]: (a) 溶劑系統:在選擇適當的溶劑系統時必須考慮溶劑極性、對溶質的選擇性以 及溶質在不同溶劑中的溶解度。一般而言,分析物在兩相溶劑間最佳的分配 係數 KD需在 0.2 ~ 5 之間,才能獲得較佳的分離效果。但在二元的溶劑系統 中,KD值要落在此範圍不容易,因此,常藉由加入第三種甚至第四種可溶於 原先兩者的溶劑,用來調和原先溶劑在極性或是界面張力的差異。然後依 KD 來判斷分離結果,並決定移動和固定相。 (b) 儀器轉速:在較高的轉速下,固定相越容易滯留在管柱中,且因為轉動速度 大,離心力也較大,因此還可以加速移動相與固定相的分層,這兩個結果均
19 可提供較高的固定相滯留量,在有關於離心分配層析分離效果的研究中,若 可以得到固定相滯留量越大,解析度也較佳,所以在 CPC 機械結構可以承受 的轉速之下,轉動速度越快,分離效果越好。 (c) 移動相流速:當移動相流速越快時,越容易將固定相推出管柱,因此固定相 的滯留量會比較低。反之移動相流速若較慢,會達到較佳的固定相滯留量, 且可提高分離解析度,但相對地分離時間會變長。 2.3.5 離心分配層析儀的應用 因為 CPC 的固定相與一般填充管柱相比,能有較大的固定相體積,且具有 放大特性,所以在 CPC 的研究以天然物製備分離為主流[27],而在對於化學品 的純化分離方面研究亦不在少數。近年來也有學者將 CPC 與鏡像選擇物結合, 應用在分離鏡像異構物的分子[28],根據研究指出,CPC 可以成功製備分離鏡像 異構物,也成功的應用在蛋白質的純化[29]。
20 第三章實驗 3.1 實驗樣品和溶劑 (1) 桑葉 購買自苗栗縣泉明生態教育蠶業農場,編號為台灣桑葉 2 號(Mulberry NO.2)。大 部分研究桑葉的文獻[3;6;30;31]所選用的都是屬於 Morus alba L.品種的乾燥 桑葉。 (2) 溶劑
Deionized water, purified from Milli-Q plus, (Bedford, MA, USA) Ethanol, 99.5%, (TEDIA, Fairfield, OH, USA)
Ethyl Acetate, HPLC grade, 95%,(TEDIA,Fairfield,OH,USA) Formic acid, 98% up, (ACROS, Geel, Belgium, USA)
Acetonitrile (ACN), HPLC grade, 99.9%, (TEDIA, Fairfield, OH, USA) n-Butanol, HPLC grade, 95%, (TEDIA,Fairfield,OH,USA)
Methyl t-Butyl Ether (MTBE), HPLC grade, 99.8%, (TEDIA, Fairfield, OH, USA) Methanol, HPLC grade,99.5%, (TEDIA,Fairfield,OH,USA)
21
3.2 實驗儀器
(1) 離心分配層析儀
CPC 是由 Sanki (Tokyo, Japan)製造,型號是 CPC 240,內部主體由 12 個 disks 所構成,包含 2136 個 channels,最高可耐壓為 6.2×106
N/m2 (900 psi),管柱總容 積大約 240 毫升,此儀器的轉速為 0 - 2000 rpm。藉由轉動外部控制閥,就可輕 易選擇上升模式或下降模式的操作模式。
(2) 往覆式幫浦
此幫浦為 Series II Digital HPLC pump ,流速可由 0.01 mL/min - 9.99 mL/min,購買自 Pharma-Tech Research Company (Baltimore, MD, USA)。 (3) 高效能液相層析管柱
由 Polymer Laboratories 製造的 PLRP-S column (250 mm × 4.6 mm, 15 μm), 屬於 reverse phase column。
(4) 紫外光-可見光偵測器(UV-Visible Detector)
型號為 Bio-Rad Model 1801 UV-Visible detector (Bio-Rad, Hercules, CA, USA),偵測器外部與個人電腦連接,利用色層分析儀數據處理系統(訊華公司, 台北市)擇取實驗訊號。
(5) 紫外光-可見光譜儀(UV-Visible Spectrophotometer) Hewlett Packard 8453, (Waldronn, Germany)。
22
(6) 迴旋減壓蒸餾器
廠牌為 Buchi (Switzerland),型號是 R-114。 (7) 分管收集器
廠牌為 Advantec (Tokyo, Japan),型號是 CHF1215A。 (8) ESI-MS
廠牌為 Micromass (Manchester, England),型號是 Quattro Micro,主要使用 分子量小於 2000 電灑游離法質譜。
23 3.3 實驗流程 3.3.1 桑葉的前處理流程 由文獻[32]中得知,秤 2.0 g 乾燥的桑葉粉末,使用 20 mL 不同濃度的乙醇 水溶液(0%、20%、40%、60%、80%、100%,v/v),萃取 3 小時,用離心機 把萃取液離心,取出溶液的部分,剩餘的部分再加入 20ml 的相同的溶液,做相 同的萃取步驟,最後得到 40mL 的萃取液,然後用 HPLC 來分離,結果可發現 桑葉使用 60%的乙醇水溶液萃取,得到的 Flavonol compounds 含量最多,由於 研究目的是想分離出桑葉中的 Chlorogenic acid、Isoquercitrin、Astragalin、Q3MG、 K3MG 五種成分如圖 2 所示,大部分是屬於 Flavonol compounds,故在桑葉樣品 的前處理步驟中,則選用 60%乙醇水溶液做萃取。 桑葉前處理的流程如圖 8 所示: (1) 先用天平秤約 20g 的乾燥台灣桑葉 2 號,然後使用 500mL 的 60% (v/v)乙醇 做萃取,利用隔水加熱法,在 40 °C 的水浴中,加入磁石攪拌萃取 3 小時,之後 使用抽氣過濾來除去殘渣的部分,並保留濾液的部分,再使用迴旋減壓蒸餾器 把溶劑抽乾。但因為桑葉中的成分相當複雜,必須再藉由批式萃取除去極性較 大的化合物,使欲分離的目標物較為單純。 (2) 在步驟 1 得到的黏稠物中,加入 100 mL 的去離子水來溶解黏稠物,得到初 步的萃取液,再使用 300 mL 的 EA 做批式萃取(圖 9),先加入 100 mL EA(ethyl acetate),劇烈搖晃後,靜置 30 分鐘使兩相達到平衡,之後將下層水相轉移至另
24 一個分液漏斗中,再加入 100 mL EA,同樣劇烈搖晃後,靜置 30 分鐘使兩相達 到平衡,再把下層水相轉移,最後再加入 100 mL EA,待至平衡,把下層水相 取出做為步驟 3 使用,上述總共做了三次批式萃取,得到約 300 mL 的 EA 相和 100 mL 的水相。保留三次上層的 EA 有機相,並使用迴旋減壓蒸餾器把溶劑抽 乾,當作 sample 1。 (3) 經過步驟 2 的批式萃取後,最後得到 100mL 的下層水相,再分別加入 100 mL 的 EA 加 0.5 mL 的甲酸兩次,做批式萃取,總共使用 200 mL 的 EA,保留兩次 上層 EA 有機相的部分,並使用迴旋減壓蒸餾器把溶劑抽乾,當作 sample 2。在 EA 中加入甲酸的目的是為了萃取到含有-COOH 官能基的成分,因為加入酸可 以防止-COOH 官能基解離,而降低化合物的極性,故可以使得含有-COOH 官能 基的成分從水相被萃取到有機相當中。
25 圖 8、桑葉前處理的流程 秤20g的乾燥桑葉 萃取得到的濃稠物 初步萃取液 100mL的水相 100mL的水相 共200mL的EA相 減壓迴旋蒸餾 把溶劑抽乾 Sample 2 每次加入100mL的EA 加0.5mL的甲酸做批式 萃取,共萃取兩次 共300mL的EA相 Sample 1 減壓迴旋蒸餾把 溶劑抽乾 每次加入100mL的EA做批 式萃取,共萃取三次 加入100mL的去離子水 1.加入60%(v/v)的乙醇500mL 2.在40。C的水浴中隔水加熱並攪拌三小時 3.抽氣過濾把殘渣除去,保留濾液 4.用減壓迴旋蒸餾把溶劑抽乾
26 在步驟 1 得到的桑葉萃取黏稠物中加入 100 mL 的去離子水,形成 100mL 的桑 葉萃取液,再倒入分液漏斗中,接著加入 100 mL EA,劇烈搖晃後,靜置 30 分 鐘使兩相達到平衡,將下層相轉移至另一個分液漏斗中,保留上層相,在含有 下層相的分液漏斗中加入新的 100 mL EA,同樣劇烈搖晃後並靜置 30 分鐘,再 把下層相轉移至另一個分液漏斗中,保留上層相;最後一樣在下層相中加入新 的 100 mL EA,劇烈搖晃後,待至平衡,轉移下層相做為步驟 3 使用,保留上 層相,上述總共做了三次批式萃取,得到 300 mL 的上層 EA 相做為 sample1 和 100 mL 的下層水相做為步驟 3 使用。 圖 9、三次批式萃取示意圖
27 3.3.2 偵測桑葉成分在不同溶劑系統中的分佈情況 實驗初始首先嘗試兩相溶劑系統,將所配製的 20 mL 兩相溶液,加入約 10 mg 的桑葉樣品,劇烈的搖晃待靜置至平衡後,上、下層相各取 3 mL,然後用迴 旋減壓蒸餾器把溶劑抽乾,再分別加入 0.5 mL 的 HPLC 移動相,之後取 20 µL 注 入 HPLC,以紫外光-可見光偵測器偵測,偵測波長 350 nm,可得上、下層的層 析圖譜,同一成分在上下層的濃度比值,也就是層析波峰面積比值,可得各成 分在兩相中的分佈值(KD) l u D C C K Cu : 分析物在上層相的濃度(層析峰面積) Cl : 分析物在下層相的濃度(層析峰面積) 3.3.3 純度的估計 製備分離中草藥[28;33],一般純度計算方法,主要是藉由不同物質在 HPLC 層析圖中,單一物質的波峰面積佔總面積的百分比。 純度的計算: 100% HPLC (%) 所有層析峰的總面積 單一波峰面積 純度
28 3.3.4 回收量的估計 回收量估計值的計算方法[33],首先要確認樣品進樣於 CPC 的重量,然後 與 HPLC 層析圖中,單一物質的波峰面積佔總面積的百分比相乘,就可估算出 單一成分的回收量。 回收量估計值的計算: HPLC (mg) 所有層析峰的總面積 單一波峰面積 樣品進樣量 回收量估計值 3.3.5 CPC 製備實驗步驟 CPC 實驗儀器裝置如圖 10 所示[23] (1) 利用量筒量取特定體積溶劑,並置於分液漏斗內,配製成所需的溶劑系統, 然後靜置至溶劑兩相分層,分別取出上層相與下層相。 (2) CPC 調至 Descending 方向,在低轉速 300 rpm 下,使用往復式幫浦以流速 8 mL/min 將固定相填滿整個管柱。 (3) 啟動 CPC,使其轉速達到 900 rpm。 (4) 待其轉速穩定後,以流速 1.0 mL/min 將移動相注入 CPC,此時會有固定相 從 CPC 中被推出,移動相與固定相會在內部達到一個平衡,直到固定相不再持 續被推出時,紀錄被推出的固定相體積,並可以初步計算出此溶劑系統的固定 相滯留率。
29 (5) 當固定相不再流出,表示移動固定相已達到平衡,開啟開啟 UV-Vis 偵測器 (350 nm),並等待訊號穩定。 (6) 注入桑葉樣品溶液 5 mL,以上層相當移動相來沖提,並在樣品注入的同時 紀錄層析訊號。 (7) 每 3 分鐘收集一管,即每管中含有 3 mL 的沖堤液。 (8) 實驗完成後,CPC 停止轉動,用氮氣將管柱內的液體吹出並收集,紀錄有機 相和水相的體積,下層固定相的體積與總體積相除就是固定相滯留率。 (9) 在 CPC 停止轉動的情況下,先以 300 mL 甲醇沖洗管柱,再以 300 mL 去離 子水清洗,未流出之去離子水保存在 CPC 中。 圖 10、CPC 實驗儀器裝置 包含了梯度幫浦、CPC 儀器、紫外光偵測器、以及分管收集器。
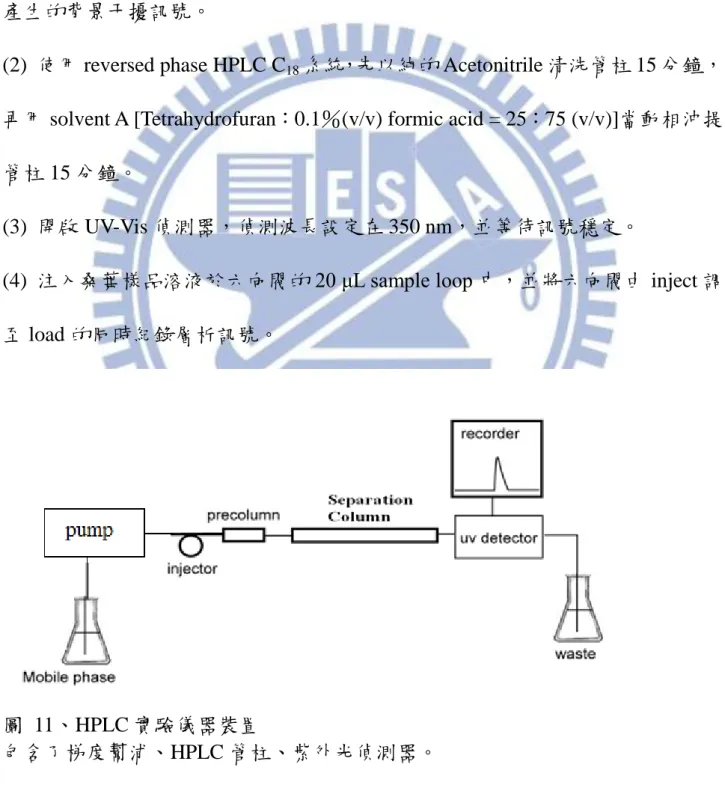
30 3.3.6 HPLC 分析收集液實驗步驟 HPLC 實驗儀器裝置如圖 11 所示 (1) 每支收集管先用迴旋減壓蒸餾裝置把溶劑抽乾,再加入 0.5 mL 的 HPLC 沖 堤的移動相溶解樣品,選擇用此移動相來溶解樣品,可避免掉因為溶劑不同而 產生的背景干擾訊號。
(2) 使用 reversed phase HPLC C18系統,先以純的 Acetonitrile 清洗管柱 15 分鐘,
再用 solvent A [Tetrahydrofuran:0.1%(v/v) formic acid = 25:75 (v/v)]當動相沖提 管柱 15 分鐘。
(3) 開啟 UV-Vis 偵測器,偵測波長設定在 350 nm,並等待訊號穩定。
(4) 注入桑葉樣品溶液於六向閥的 20 μL sample loop 中,並將六向閥由 inject 調 至 load 的同時紀錄層析訊號。
圖 11、HPLC 實驗儀器裝置
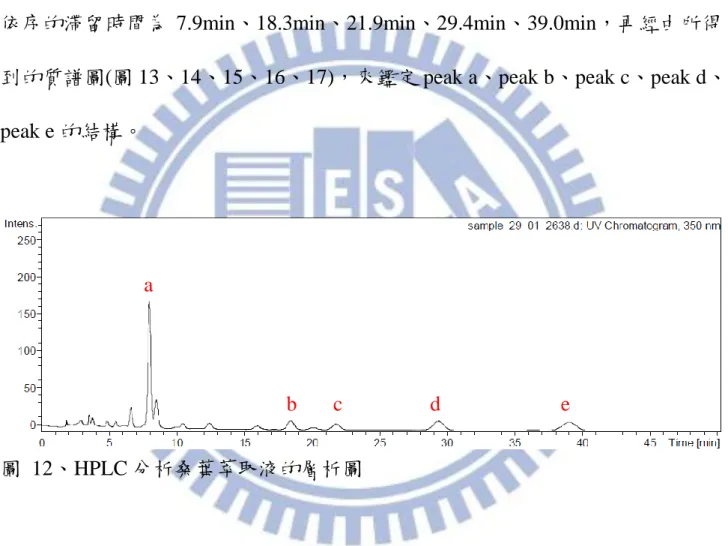
31 第四章 結果與討論 4.1 以高效能液相層析串聯質譜儀分析鑑定桑葉萃取液 本實驗中利用 HPLC-MS 分析桑葉萃取液,以波長 350nm 的 UV-vis 偵測器 偵測,得到層析圖(圖 12),將層析圖中五個波峰標記依序為 a、b、c、d、e,其 依序的滯留時間為 7.9min、18.3min、21.9min、29.4min、39.0min,再經由所得 到的質譜圖(圖 13、14、15、16、17),來鑑定 peak a、peak b、peak c、peak d、 peak e 的結構。
圖 12、HPLC 分析桑葉萃取液的層析圖
Chlorogenic acid 的分子量是 354.3 Da,經由 ESI-MS 正電荷分析 peak a 的結 果(圖 13),可由圖中發現〔M+H〕+
為 355.1 m/z 的訊號,是加一個質子的離子 訊號。162.9 m/z 的訊號,則是綠原酸斷 C-O 鍵後,右邊帶正電結構的 fragment 訊號。因此由質譜偵測鑑定後,可確定 peak a 的主成分為 Chlorogenic acid。
a
32
圖 13、peak a 測 ESI-MS 正電荷質譜圖
Isoquercitrin 的分子量是 464.4 Da,經由 ESI-MS 正電荷分析 peak b 的結果(圖 14),可由圖中發現〔M+H〕+ 為 465.0 m/z 的訊號,是加一個質子的離子訊號。 303.0 m/z 是(〔M+H〕+ -glucoside)失去一個葡萄糖苷基的訊號。因此由質譜偵 測鑑定後,可確定 peak b 的主成分為 Isoquercitrin。
33
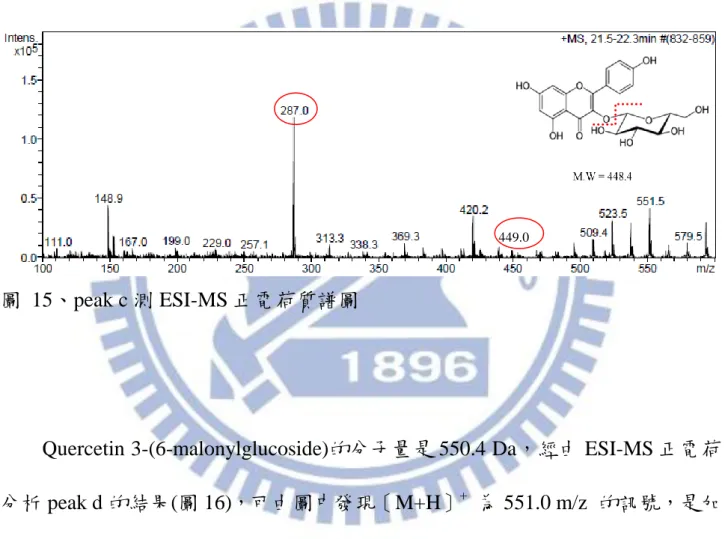
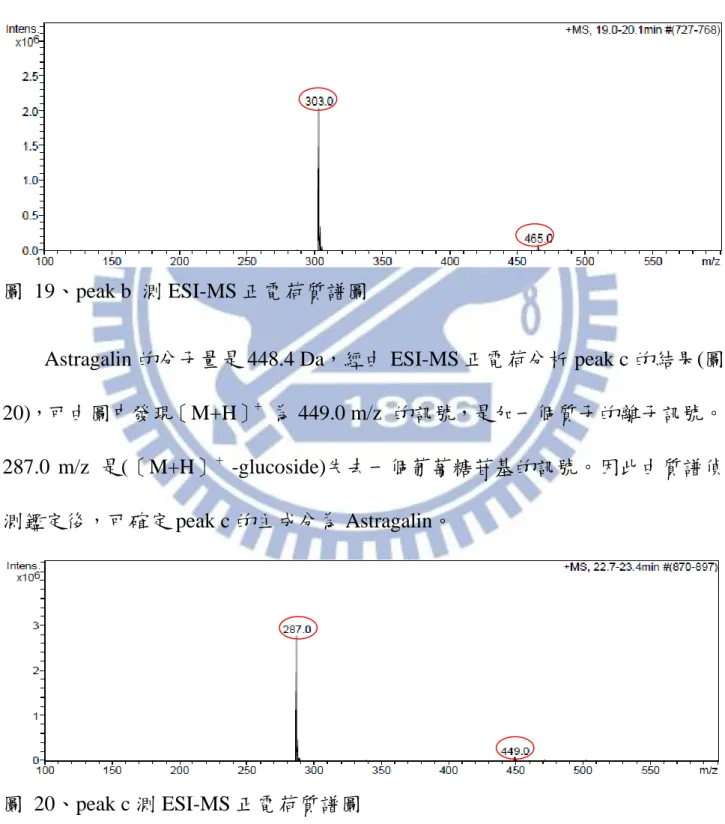
Astragalin 的分子量是 448.4 Da,經由 ESI-MS 正電荷分析 peak c 的結果(圖 15),可由圖中發現〔M+H〕+ 為 449.0 m/z 的訊號,是加一個質子的離子訊號。 287.0 m/z 是(〔M+H〕+ -glucoside)失去一個葡萄糖苷基的訊號。因此由質譜偵 測鑑定後,可確定 peak c 的主成分為 Astragalin。
圖 15、peak c 測 ESI-MS 正電荷質譜圖
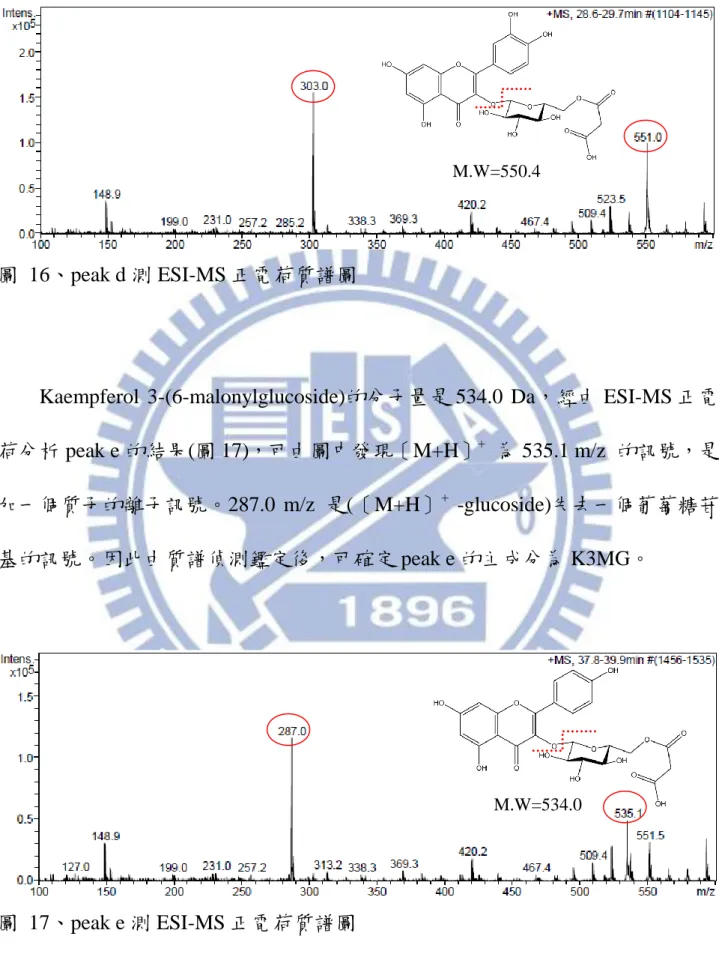
Quercetin 3-(6-malonylglucoside)的分子量是 550.4 Da,經由 ESI-MS 正電荷 分析 peak d 的結果(圖 16),可由圖中發現〔M+H〕+
為 551.0 m/z 的訊號,是加 一個質子的離子訊號。303.0 m/z 是(〔M+H〕+ -glucoside)失去一個葡萄糖苷基 的訊號。因此由質譜偵測鑑定後,可確定 peak d 的主成分為 Q3MG。
34
圖 16、peak d 測 ESI-MS 正電荷質譜圖
Kaempferol 3-(6-malonylglucoside)的分子量是 534.0 Da,經由 ESI-MS 正電 荷分析 peak e 的結果(圖 17),可由圖中發現〔M+H〕+ 為 535.1 m/z 的訊號,是 加一個質子的離子訊號。287.0 m/z 是(〔M+H〕+ -glucoside)失去一個葡萄糖苷 基的訊號。因此由質譜偵測鑑定後,可確定 peak e 的主成分為 K3MG。 圖 17、peak e 測 ESI-MS 正電荷質譜圖 M.W=550.4 M.W=534.0
35 4.2 以高效能液相層析串聯質譜儀分析鑑定批式萃取後的桑葉樣品 桑葉中的成分非常複雜,若要在如此複雜的成分中,針對目標物找出適合 CPC 的溶劑系統,使這些目標物有好的分配係數,會非常的困難。故在本實驗 當中,為了使樣品簡單化,加入 EA 做批式萃取,把目標物萃取到有機相中當作 sample 1。保留下來的水相,加入酸化的 EA 做批式萃取,把含有-COOH 官能基 的目標物萃取到有機相當中做為 sample 2。 4.2.1 以高效能液相層析串聯質譜儀分析鑑定批式萃後得到的 sample 1 本實驗中利用 HPLC-MS 分析 sample 1,以波長 350nm 的 UV-vis 偵測器偵 測,得到層析圖(圖 18),由圖 12 可知層析圖中兩個波峰標依序為 b、c,再經由 所得到的質譜圖(圖 19、20),再次鑑定 peak b 與 peak c 的結構。 圖 18、HPLC 分析 sample 1 的層析圖 b c
36
Isoquercitrin 的分子量是 464.4 Da,經由 ESI-MS 正電荷分析 peak b 的結果(圖 19),可由圖中發現〔M+H〕+ 為 465.0 m/z 的訊號,是加一個質子的離子訊號。 303.0 m/z 是(〔M+H〕+ -glucoside)失去一個葡萄糖苷基的訊號。因此由質譜偵 測鑑定後,可確定 peak b 的主成分為 Isoquercitrin。
圖 19、peak b 測 ESI-MS 正電荷質譜圖
Astragalin 的分子量是 448.4 Da,經由 ESI-MS 正電荷分析 peak c 的結果(圖 20),可由圖中發現〔M+H〕+ 為 449.0 m/z 的訊號,是加一個質子的離子訊號。 287.0 m/z 是(〔M+H〕+ -glucoside)失去一個葡萄糖苷基的訊號。因此由質譜偵 測鑑定後,可確定 peak c 的主成分為 Astragalin。
37
4.2.2 以高效能液相層析串聯質譜儀分析鑑定批式萃後得到的 sample 2
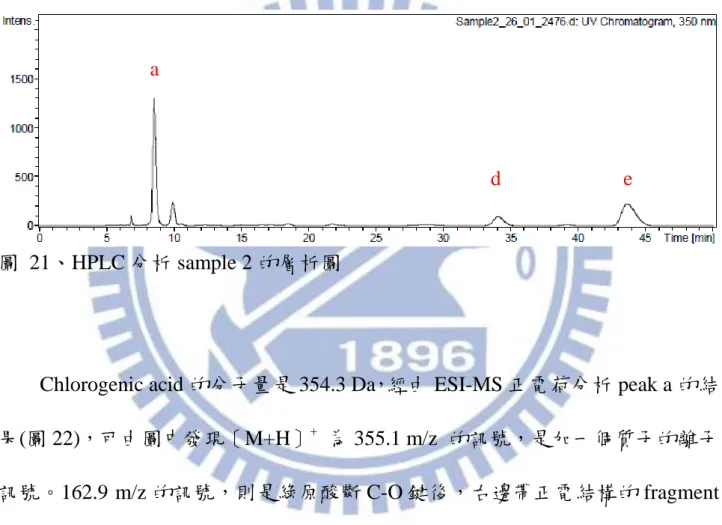
實驗中利用 HPLC-MS 分析 sample 2,以波長 350nm 的 UV-vis 偵測器偵測, 得到層析圖(圖 21),由圖 12 可知層析圖中三個波峰為 a、d、e,再經由所得到 的質譜圖(圖 22、23、24),再次鑑定 peak a、peak d 和 peak e 的結構。
圖 21、HPLC 分析 sample 2 的層析圖
Chlorogenic acid 的分子量是 354.3 Da,經由 ESI-MS 正電荷分析 peak a 的結 果(圖 22),可由圖中發現〔M+H〕+
為 355.1 m/z 的訊號,是加一個質子的離子 訊號。162.9 m/z 的訊號,則是綠原酸斷 C-O 鍵後,右邊帶正電結構的 fragment 訊號。因此由質譜偵測鑑定後,可確定 peak a 的主成分為 Chlorogenic acid。
a
38
圖 22、peak a 測 ESI-MS 正電荷質譜圖
Quercetin 3-(6-malonylglucoside)的分子量是 550.4 Da,經由 ESI-MS 正電荷 分析 peak d 的結果(圖 23),可由圖中發現〔M+H〕+ 為 551.0 m/z 的訊號,是加 一個質子的離子訊號。303.0 m/z 是(〔M+H〕+ -glucoside)失去一個葡萄糖苷基 的訊號。因此由質譜偵測鑑定後,可確定 peak d 的主成分為 Q3MG。 圖 23、peak d 測 ESI-MS 正電荷質譜圖
39
Kaempferol 3-(6-malonylglucoside)的分子量是 534.0 Da,經由 ESI-MS 正電 荷分析 peak e 的結果(圖 23),可由圖中發現〔M+H〕+ 為 535.1 m/z 的訊號,是 加一個質子的離子訊號。287.0 m/z 是(〔M+H〕+ -glucoside)失去一個葡萄糖苷 基的訊號。因此由質譜偵測鑑定後,可確定 peak e 的主成分為 K3MG。 圖 24、peak e 測 ESI-MS 正電荷質譜圖
40 4.3 以離心分配層析儀分離桑葉成分的實驗結果 使用 CPC 分離之前,先用分配係數值(KD值)來尋找適合的溶劑系統,若 KD 值在理想的範圍內(KD在 0.2 ~ 5 之間),表示能有較好的分離結果。EA/BuOH/H2O 三成分溶劑系統,經過多組不同比例(表 1)測試發現,桑葉中五種目標物都傾向 分佈在有機相,表示樣品的分配係數值不理想,所以 EA/BuOH/H2O 組成的溶劑 系統不適合應用在 CPC 分離 Chlorogenic acid、Isoquercitrin、Astragalin、Quercetin 3-(6-malonylglucoside)、Kaempferol 3-(6-malonylglucoside)這五個成分。 表 1、 EA/BuOH/H2O三成分溶劑系統,測試在不同組成比例中,桑葉中五種 目標物的分配係數值(KD) 4:6:10 6:4:10 9:1:10 Chlorogenic acid 13.53 7.43 1.83 Isoquercitrin 11.05 6.75 2.95 Astragalin 12.73 5.32 3.86 Quercetin 3-(6-malonylglucoside) 28.17 10.41 6.21 Kaempferol 3-(6-malonylglucoside) 31.87 10.37 9.46 EA/BuOH/H2O
41 之後根據文獻[27]的研究,嘗試選用 MTBE/Acetone/H2O 三成分溶劑系統, 測試多組不同比例(表 2、3),尋找適合的溶劑系統,分別應用在 CPC 分離 sample 1 與 sample 2。使得桑葉中五種目標物在兩相中不僅都有理想的分佈(KD在 0.2 ~ 5 之間),且任意兩個成分的 KD值相減,會得到較大值,KD值之差越大表示不同 的成分越容易被分開。
由表 2 中得知,sample 1 中的成分,在 MTBE:Acetone:H2O=6:4:10、7:3:10、
8:2:10 這三種比例的溶劑系統中有較好的分佈情形,故用 CPC 分離 sample 1 時, 使用此三種比例的溶劑系統來做實驗,其中 MTBE:Acetone:H2O=7:3:10 為最佳 化的溶劑比例。 表 2 、 MTBE/Acetone/H2O 三 成 分 溶 劑 系 統 , 測 試 在 不 同 組 成 比 例 中 , Isoquercitrin、Astragalin 的分配係數值(KD) MTBE:Acetone:H2O 4:6:10 5:5:10 6:4:10 7:3:10 8:2:10 9:1:10 Isoquercitrin 0.12 0.24 0.31 0.27 0.22 0.05 Astragalin 0.19 0.51 0.61 0.58 0.51 0.15
42
由表 3 中得知,sample 2 中的成分,在 MTBE:Acetone:H2O =6:4:10、7:3:10、
8:2:10(並加入 0.6% formic acid)這三種比例的溶劑系統中有較好的分佈情形,故 用 CPC 分 離 sample 2 時 , 使 用 此三 種 比 例 的 溶 劑系 統 來 做 實 驗 ,其 中 MTBE:Acetone:H2O=7:3:10(並加入 0.6% formic acid)為最佳化的溶劑比例。
表 3、MTBE/Acetone/H2O 三成分溶劑系統加 0.6% formic acid,測試在不同組成
比例中,Chlorogenic acid、Q3MG、K3MG 的分配係數值(KD) MTBE:Acetone:H2O 加 0.6%(v/v) formic acid 5:5:10 加 0.6%(v/v) formic acid 6:4:10 加 0.6%(v/v) formic acid 7:3:10 加 0.6%(v/v) formic acid 8:2:10 加 0.6%(v/v) formic acid Chlorogenic acid 0.34 0.21 0.20 0.22 Q3MG 0.46 0.40 0.43 0.40 K3MG 1.12 1.01 1.20 1.15 由表 2、3 得知,溶劑系統 MTBE:Acetone:H2O=7:3:10 為最佳化的溶劑比例, 接著再加入第四成分溶劑 EA,調和原先溶劑在極性或表面張力的差異,來尋找 更適合的 KD 值。嘗試選用 MTBE/Acetone/H2O/EA 四成分溶劑系統,測試在
MTBE:Acetone:H2O=7:3:10 的溶劑系統中,加入不同比例的 EA(表 4、5),尋找
43
由表 4 中得知,MTBE:Acetone:H2O:EA=7:3:10:2 為最佳化的溶劑比例。
sample 1 中的成分,在此溶劑比例當中有較好的分佈情形,故用 CPC 分離 sample 1 時,使用 MTBE:Acetone:H2O:EA=7:3:10:2 的溶劑系統來做實驗。
表 4、在 MTBE:Acetone:H2O=7:3:10 的溶劑系統中,加入不同比例的 EA,所得
Isoquercitrin、Astragalin 的分配係數值(KD)
MTBE:Acetone:H2O:EA 7:3:10:0.5 7:3:10:1 7:3:10:1.5 7:3:10:2
Isoquercitrin 0.26 0.32 0.35 0.43 Astragalin 0.54 0.64 0.71 0.81
由表 5 中得知,MTBE:Acetone:H2O:EA=7:3:10:2(並加入 0.6% formic acid)
為最佳化的溶劑比例。sample 2 中的成分,在此溶劑比例當中有較好的分佈情形, 故用 CPC 分離 sample 2 時,使用 MTBE:Acetone:H2O:EA=7:3:10:2(並加入 0.6%
formic acid)的溶劑系統來做實驗。
表 5、在 MTBE:Acetone:H2O=7:3:10 加 0.6% formic acid 的溶劑系統中,加入不
同比例的 EA,所得 Chlorogenic acid、Q3MG、K3MG 的分配係數值(KD)
MTBE:Acetone:H2O:EA 加 0.6%(v/v) formic acid 7:3:10:0.5 加 0.6%(v/v) formic acid 7:3:10:1 加 0.6%(v/v) formic acid 7:3:10:1.5 加 0.6%(v/v) formic acid 7:3:10:2 加 0.6%(v/v) formic acid Chlorogenic acid 0.15 0.22 0.27 0.30 Q3MG 0.34 0.50 0.67 0.75 K3MG 0.94 1.50 1.88 2.04
44
4.3.1 sample 1 分離的結果
4.3.1.1溶劑系統 MTBE / Acetone / H2O
sample 1 中主要包含 Isoquercitrin 和 Astragalin 兩種成分,已找出分離 sample 1 的 CPC 最佳化實驗參數(表 6),選用MTBE / Acetone / H2O 這組溶劑系統,是 因為溶劑極性適合分離目標物。由表 7 得到的分配係數值,得知 MTBE / Acetone / H2O = 6:4:10、7:3:10、8:2:10,此三組溶劑組成比例有較佳的分配係 數值,其中 7:3:10 為最佳化的比例。由表中可知 KD值都小於 1,表示樣品傾 向分佈在下層相,故最後選擇以 descending mode 作為實驗條件。管柱總體積 240 mL,靜相滯留量大約 188mL,靜相滯留率為 78%。 表 6、CPC 分離 sample 1 的實驗參數 溶劑系統 (MTBE / Acetone / H2O =6:4:10、7:3:10、8:2:10) 流動模式 Descending mode (下層相當動相) 樣品進樣量 5 mL (10 mg 溶於 6 mL 的動相) 轉速 900 rpm 流速 1.0 mL/min 偵測波長 350 nm
45
表 7、Isoquercitrin和Astragalin 兩種成分在溶劑系統MTBE / Acetone / H2O的分 配係數值 MTBE:Acetone:H2O 6:4:10 7:3:10 8:2:10 Isoquercitrin 0.31 0.27 0.22 Astragalin 0.61 0.58 0.51 由上述相同的實驗參數,三組不同的溶劑比例(6:4:10、7:3:10、8:2: 10),來進行 CPC 分離 sample 1 的實驗,圖 25(A)、(B)、(C)分別為三組的結果, 圖中可明顯觀察出存在 I、II、III 三個波峰。 (A) Ⅰ Ⅱ Ⅲ
46
(B)
(C)
圖 25、CPC 分離 sample 1 的層析圖 (A) MTBE / Acetone / H2O =6:4:10
(B) MTBE / Acetone / H2O =7:3:10 (C) MTBE / Acetone / H2O =8:2:10 Ⅰ Ⅰ Ⅱ Ⅲ Ⅱ Ⅲ
47 圖 25(B)為最佳化的溶劑比例 7:3:10 所得的結果,使用分管收集器收集 這三個波峰,先將分管收集器設定在第 40 分鐘前的沖提溶液不收集,之後設定 每 3 分鐘收集一管,波峰 I 收集 52-64 min(5-8 管);波峰 II 收集 82-100min(15-20 管);波峰 III 收集 115-145 min(26-35 管),然後進一步做 HPLC 分析。 由 HPLC 層析圖(圖 26)可得知,波峰 I 所含蓋的都是屬於極性較大的化合物, 分配係數值較小,所以最先被沖提出管柱外;波峰 II 主要是 Isoquercitrin 成分, 且純度約為 97.3%;波峰 III 則以 Astragalin 成分為主,純度約為 97.2%。經由 CPC 製備分離的兩個成分,純度都可到達 95%以上,因此樣品確實有被純化的 效果。 (A)
48 (B) (C) 圖 26、HPLC 分析波峰Ⅰ、II、 III 的層析圖 (A)波峰Ⅰ的層析圖為極性較大的化合物 (B)波峰 II 的層析圖主要包含 b(Isoquercitrin)成分 (C)波峰 III 的層析圖主要包含 c(Astragalin)成分 c b
49
4.3.1.2溶劑系統 MTBE / Acetone / H2O/EA
sample 1 中主要包含 Isoquercitrin 和 Astragalin 兩個成分,已找出分離 sample 1 的 CPC 最佳化條件(表 8)。其中選用 MTBE/Acetone/H2O/EA= 7:3:10:2,
是因為目標物可得到最佳的分配係數值(表 9)。由表中可知 KD值都小於 1,表示
樣品傾向分佈在下層相,故最後選擇以 descending mode 作為實驗條件。管柱總 體積 240 mL,靜相滯留量大約 188mL,靜相滯留率為 78%。
表 8、CPC 分離 sample 1 的實驗參數
溶劑系統 (MTBE / Acetone / H2O /EA=7:3:10:2)
流動模式 Descending mode (下層相當動相) 樣品進樣量 5 mL (10 mg 溶於 6 mL 的動相)
轉速 900 rpm
流速 1.0 mL/min
50
表 9、Isoquercitrin和Astragalin 兩種成分在溶劑系統MTBE / Acetone / H2O/EA 的分配係數值
MTBE:Acetone:H2O:EA 7:3:10:2
Isoquercitrin 0.43 Astragalin 0.81
由上述的最佳化實驗參數,進行 CPC 分離 sample 1,所得到的結果(圖 27), 可明顯觀察出存在 I、II、III 三個波峰,由圖可知在MTBE / Acetone / H2O 溶劑 系統中加入 EA,即 MTBE/Acetone/H2O/EA 溶劑系統,可以使得波鋒間距變大,
故在此條件下,smaple 1 中的成分有較好的分離效果。
圖 27、CPC 分離 sample 1 的層析圖 Ⅰ
Ⅱ
51
4.3.2 sample 2 分離的結果
4.3.2.1溶劑系統 MTBE / Acetone / H2O
sample 2 中主要包含 Chlorogenic acid、Quercetin 3-(6-malonylglucoside)和 Kaempferol 3-(6-malonylglucoside)三種成分,已找出分離 sample 2 的 CPC 最佳 化實驗參數(表 10),由表 11 得到的分配係數值,得知 MTBE / Acetone / H2O = 6: 4:10、7:3:10、8:2:10 加 0.6% (v/v) formic acid,此三組溶劑組成比例有 較佳的分配係數值,其中 7:3:10 為最佳化的比例。管柱總體積 240 mL,靜相 滯留量大約 188 mL,靜相滯留率為 78%。 表 10、CPC 分離 sample 2 的實驗參數 溶劑系統 (MTBE / Acetone / H2O ==6:4:10、7:3:10、8:2:10) 加 0.6% (v/v) formic acid 流動模式 Descending mode (下層相當動相) 樣品進樣量 5 mL (10 mg 溶於 6 mL 的動相) 轉速 900 rpm 流速 1.0 mL/min 偵測波長 350 nm
52
表 11、Chlorogenic acid、Q3MG和K3MG三種成分在溶劑系統MTBE / Acetone / H2O加0.6% (v/v) formic acid的分配係數值
MTBE:Acetone:H2O 加 0.6%(v/v) formic acid 6:4:10 加 0.6%(v/v) formic acid 7:3:10 加 0.6%(v/v) formic acid 8:2:10 加 0.6%(v/v) formic acid Chlorogenic acid 0.21 0.20 0.22 Q3MG 0.40 0.43 0.40 K3MG 1.01 1.20 1.15 由上述相同的實驗參數,三組不同的溶劑比例(6:4:10、7:3:10、8:2: 10 加 0.6% (v/v) formic acid),來進行 CPC 分離 sample 2 的實驗,圖 28(A)、(B)、
(C)分別為三組的結果,圖 28(A)、(B)中可明顯觀察出存在 A、B、C、D 四個波 峰,圖 28(C)的結果不理想,是因為在此比例下的溶劑系統不夠穩定,導致圖中 出現許多雜訊。 (A) A B C D
53
(B)
(C)
圖 28、CPC 分離 sample 2 的層析圖
(A) MTBE / Acetone / H2O =6:4:10 加 0.6%(v/v) formic acid
(B) MTBE / Acetone / H2O =7:3:10加 0.6%(v/v) formic acid
(C) MTBE / Acetone / H2O =8:2:10加 0.6%(v/v) formic acid A
B
C
54 圖 28(B)為最佳化的溶劑比例 7:3:10加 0.6%(v/v) formic acid所得的結果, 使用分管收集器收集這三個波峰,先將分管收集器設定在第 40 分鐘前的沖提溶 液不收集,之後設定每 3 分鐘收集一管,波峰 A 收集 52-64 min(5-8 管);波峰 B 收集 70-91 min(11-17 管);波峰 C 收集 103-136 min(22-32 管) ;波峰 D 收集 181-247 min(48-69 管),然後進一步做 HPLC 分析。 由 HPLC 層析圖(圖 29)可得知,波峰 A 所含蓋的都是屬於極性較大的化合 物,所以最容易被沖提出管柱外;波峰 B 主要是 Chlorogenic acid 成分,純度約 為 70.2%;波峰 C 則以 Quercetin 3-(6-malonylglucoside)成分為主,純度約為 69.1%; 波峰 D 則是 Kaempferol 3-(6-malonylglucoside)成分,純度有 69.6%。雖然所得的 成分純度不高,但主要是因為 sample 1 中的成分被萃取到 sample 2 中,只要在 萃取 sample 1 時平衡兩小時,即可改善結果。 (A)
55 (B) (C) (D) 圖 29、HPLC 分析波峰 A、B、C、D 的層析圖 (A)波峰 A 的層析圖為極性較大的化合物 (B)波峰 B 的層析圖主要包含 a(Chlorogenic acid)成分 (C)波峰 C 的層析圖主要包含 d[Quercetin 3-(6-malonylglucoside)]成分 (C)波峰 D 的層析圖主要包含 e[Kaempferol 3-(6-malonylglucoside)]成分 a a b c c e d
56
4.3.2.2溶劑系統 MTBE / Acetone / H2O/EA
sample 2 中主要包含 Chlorogenic acid、Quercetin 3-(6-malonylglucoside)和 Kaempferol 3-(6-malonylglucoside)三種成分,已找出分離 sample 2 的 CPC 最佳 化實驗參數(表 12),其中選用 MTBE/Acetone/H2O/EA=7:3:10:2 加 0.6% (v/v)
formic acid,是因為目標物可得到最佳的分配係數值(表 13)。管柱總體積 240 mL,
靜相滯留量大約 188mL,靜相滯留率為 78%。
表 12、CPC 分離 sample 2 的實驗參數
溶劑系統 (MTBE / Acetone / H2O /EA=7:3:10:2)
加 0.6% (v/v) formic acid 流動模式 Descending mode (下層相當動相) 樣品進樣量 5 mL (10 mg 溶於 6 mL 的動相) 轉速 900 rpm 流速 1.0 mL/min 偵測波長 350 nm
表 13、Chlorogenic acid、Q3MG 和 K3MG 三種成分在溶劑系統 MTBE / Acetone / H2O/EA 加 0.6% (v/v) formic acid 的分配係數值
MTBE:Acetone:H2O:EA 加 0.6%(v/v) formic acid 7:3:10:2 加 0.6%(v/v) formic acid Chlorogenic acid 0.30 Q3MG 0.75 K3MG 2.04
57
由上述的最佳化實驗參數,進行 CPC 分離 sample 2,所得到的結果(圖 30), 可明顯觀察出存在 A、B、C、D 四個波峰,由圖可知在MTBE / Acetone / H2O
溶劑系統中加入 EA,即 MTBE/Acetone/H2O/EA 溶劑系統,可以使得波鋒間距
變大,故在此條件下,smaple 2 中的成分有較好的分離效果。 圖 30、CPC 分離 sample 2 的層析圖 A B C D
58
第五章 結論
本實驗的目的,是利用離心分配層析的技術,搭配有機-水相溶劑系統,來 分離、純化桑葉中的有效成分,包括 Chlorogenic acid (綠原酸)、Isoquercitrin、 Astragalin 、 Quercetin 3-(6-malonylglucoside) (Q3MG) 、 Kaempferol 3-(6-malonylglucoside) (K3MG),並用 HPLC-MS 來確定其結構。在本實驗當中 使 用 了 三 成 分 溶 劑 系 統 MTBE/Acetone/H2O 與 四 成 分 溶 劑 系 統
MTBE/Acetone/H2O/EA,皆成功的分離純化桑葉樣品。
本實驗中用 CPC 來分離 sample 1 中的有效成分 Isoquercitrin、Astragalin, 純度可達到約 97%,而 sample 2 中的有效成分 Chlorogenic acid (綠原酸)、 Quercetin 3-(6-malonylglucoside) (Q3MG) 、 Kaempferol 3-(6-malonylglucoside) (K3MG),純度約為 70%,是因為 sample 1 中的成分被萃取到 sample 2 中,故在 萃取 sample 1 時,有機相與水相的平衡時間要夠長,以避免 sample 1 殘留在水 相中,最後被萃取到 sample 2 當中,造成純化結果不理想。未來可嘗試不同的 萃取條件,來增加分離的效果,並希望能達到純度提高的效果。
59
參考文獻
[1] T. Matsuoka, T. Kimura, N. Muraoka, "Research of the available constituents from mulberry tree". Tohoku Agricultural Research 47 (1994) 361–362. [2] A. Onogi, K. Osawa, H. Yasuda, A. Sakai, H. Morita, H. Itokawa, " Flavonol
glycosides from the leaves of M. alba L.". Shoyakugaku Zasshi 47 (1993) 423–425.
[3] B. Enkhmaa, K. Shiwaku, T. Katsube, K. Kitajima, E. Anuurad, M. Yamasaki, Y. Yamane, "Mulberry (Morus alba L.) Leaves and Their Major Flavonol Quercetin 3-(6-Malonylglucoside) Attenuate Atherosclerotic Lesion Development in LDL Receptor–Deficient Mice". J. Nuri. 135 (2005) 729-734.
[4] Asano N, Yamashita T, Yasuda K, Ikeda K, Kizu H, Kameda Y, et al.
Polyhydroxylated alkaloids isolated from mulberry trees (Morus alba L.) and silkworms (Bombyx mori L.). J. Agric. Food Chem. 49 (2001) 4208-4213.
[5] Oku T, Yamada M, Nakamura M, Sadamori N, Nakamura S. Inhibitory effects of extractives from leaves of Morus alba on human and rat small intestinal
disaccharidase activity. Br. J. Nutr. 95 (2006) 933-938.
[6] Taniguchi S, Asano N, Tomino F, Miwa I. Potentiation of glucoseinduced insulin secretion by fagomine, a pseudo-sugar isolated from mulberry leaves. Horm Metab Res 30 (1998) 679-683.
[7] Kang TH, Oh HR, Jung SM, Ryu JH, Park MW, Park YK, et al. Enhancement of neuroprotection of mulberry leaves (Morus alba L.) prepared by the anaerobic treatment against ischemic damage. Biol Pharm Bull 29 (2006) 270-274. [8] Lee SH, Choi SY, Kim H, Hwang JS, Lee BG, Gao JJ, et al.Mulberroside F
isolated from the leaves of Morus alba inhibits melanin biosynthesis. Biol Pharm Bull 25 (2002) 1045-1048.
[9] Choi EM, Hwang JK. Effects of Morus alba leaf extract on the production of nitric oxide, prostaglandin E2 and cytokines in RAW264.7 macrophages. Fitoterapia 76 (2005) 608-613.
60
[10] Doi K, Kojima T, Fujimoto Y. Mulberry leaf extract inhibits the oxidative modification of rabbit and human low density lipoprotein. Biol Pharm Bull 23 (2000) 1066-1071.
[11] Enkhmaa B, Shiwaku K, Katsube T, Kitajima K, Anuurad E, YamasakiM, et al. Mulberry (Morus alba L.) leaves and their major flavonol quercetin
3-(6-malonylglucoside) attenuate atherosclerotic lesion development in LDL receptor-deficient mice. J. Nutr. 135 (2005) 729-734.
[12] Katsube T, Imawaka N, Kawano Y, Yamazaki Y, Shiwaku K, Yamane Y. Antioxidant flavonol glycosides in mulberry (Morus alba L.) leaves isolated based on LDL antioxidant activity. Food Chem. 97 (2006) 25-31.
[13] W. Zheng, M. N. Clifford, "Profiling the chlorogenic acids of sweet potato (Ipomoea batatas) from China". Food Chem. 106 (2008) 147–152.
[14] K. L. Johnston, M. N. Clifford, L. M. Morgan, "Coffee acutely modifies
gastrointestinal hormone secretion and glucose tolerance in humans: Glycemic effects of chlorogenic acid and caffeine". Am. J. Clinical Nutrition 78 (2003) 728–733.
[15] M. Kotani, M. Matsumoto, A. Fujita, S. Higa, W. Wang, M. Suemura, T. Kishimoto, T. Tanaka, "Persimmon leaf extract and astragalin inhibit
development of dermatitis and IgE elevation in NC/Nga mice". J. Allergy Clin. Immunol. 106 (2000) 159-166.
[16] K. Ishiguro, H. Oku, "Antipruritic effect of flavonol and 1,4-naphthoquinone derivatives from Impatiens balsamina L.". Phytother Res 11 (1997) 343-347. [17] L. Wang, Y. C. Tu, T. W. Lian, J. T. Hung, J. H. Yen, M. J. Wu,. "Distinctive
antioxidant and anti-inflammatory effects of flavonols". J. Agric and Food Chem. 54 (2006) 9798-9804.
[18] Y. Ito, "Development of Countercurrent Chromatography". Anal.Chem. 56 (1984) 534-551.
[19] Y. Ito, N. B. Mandava, "Countercurrent Chromatography : Theory and Practice ". Marcel Dekker, Inc. (1998).
61
[20] W. D. Conway, "Countercurrent Chromatography : Theory and Applications". VCH Publishers, Inc. (1990).
[21] Y. Ito, W. D. Conway, "High-Speed Countercurrent Chromatography ". John Wiley & Sons, Inc. (1996).
[22] E. Delannay, A. Toribio, L. Boudesocque, J. M. Nuzillard, Z. H. Monique, E. Dardennes, G. L. Dour, J. Sapi, J. H. Renault, "Multiple dual-mode centrifugal partition chromatography, a semi-continuous development mode for routine laboratory-scale purifications". J. Chromatogr. A 1127 (2006) 45–51.
[23] E. Gavioli, N. M. Maier, C. Minguillo´n, and W. Lindner, "Preparative
Enantiomer Separation of Dichlorprop with a Cinchona-Derived Chiral Selector Employing Centrifugal Partition Chromatography and High-Performance Liquid Chromatography: A Comparative Study". Anal. Chem. 76 (2004) 5837-5848. [24] J. B. Friesen, G. F. Pauli, "Rational development of solvent system families in
counter-current chromatography". J. Chromatogr. A 1151 (2007) 51–59.
[25] Y. Ito, "Golden rules and pitfalls in selecting optimum conditions for high-speed counter-current chromatography". J. Chromatogr. A 1065 (2005) 145–168. [26] W. D. Conway, Y. Ito, "Resolution in Countercurrent Chromatography". J. Liq.
Chromatogr. 8 (1985) 2198-2207.
[27] J. C. Delaunay, C. Castagnino, C. Che`ze, J. Vercauteren, "Preparative isolation of polyphenolic compounds from Vitis vinifera by centrifugal partition
chromatography". J. Chromatogr. A 964 (2002) 123–128. [28] N. Rubio, C. Minguillon, "Preparative enantioseparation of
(±)-N-(3,4-cis-3-decyl-1,2,3,4-tetrahydrophenanthren-4-yl)-3,5-dinitrobenzamide by centrifugal partition chromatography". J. Chromatogr. A 1217 (2010)
1183-1190.
[29] I.A. Sutherland, G. Audo, E. Bourton, F. Couillard, D. Fisher, I. Garrard, P. Hewitson, O. Intes, "Rapid linear scale-up of a protein separation by centrifugal partition chromatography". J. Chromatogr. A 1190 (2008) 57-62.
62
[30] G. C. Yen, S. C. Wu, P. D. Duh, "Extraction and Identification of Antioxidant Components from the Leaves of Mulberry (Morus alba L.)". J. Agric. Food Chem. 44 (1996) 1687-1690.
[31] H. Y. Lin, L. S. Lai, "Isolation and viscometric characterization of hydrocolloids from mulberry (Morus alba L.) leaves". Food Hydrocolloids 23 (2009) 840–848. [32] T. Katsube, N. Imawaka, Y. Kawano, Y. Yamazaki, K. Shiwaku, Y. Yamane,
"Antioxidant flavonol glycosides in mulberry (Morus alba L.) leaves isolated based on LDL antioxidant activity". Food Chem. 97 (2006) 25–31.
[33] W. Zhi, Q. Deng, "Purification of salvianolic acid B from the crude extract of Salvia miltiorrhiza with hydrophilic organic/salt-containing aqueous two-phase system by counter-current chromatography". J. Chromatogr. A 1116 (2006) 149-152.
![圖 4、流體靜態平衡系統(HSES)示意圖[18] (A) 固定相為下層相,移動相為上層相。 (B) 固定相為上層相,移動相為下層相。](https://thumb-ap.123doks.com/thumbv2/9libinfo/8152620.167153/25.892.74.809.114.899/A固定相為下層相移動相為上層相B固定相為上層相移動相為下層相.webp)
![圖 5、流體動態平衡系統(HDES)示意圖[19]](https://thumb-ap.123doks.com/thumbv2/9libinfo/8152620.167153/27.892.102.737.99.909/圖5流體動態平衡系統HDES示意圖19.webp)