奈米樹狀高分子複合磁性金屬吸附重金屬之研究
152
0
0
全文
(2) 謝誌 感謝恩師 連興隆教授不辭辛勞的指導,在本人研究過程中提供所需 資源,可以無顧慮完成學業及學術論文的研究,對於生活上的大小事,也 如朋友一般適時關心與幫助,讓我能在學習過程中更感到溫暖;此外,感 謝口試委員 袁菁教授、席行正教授、翁誌煌教授百忙之中對於本論文予以 指正及建議,亦提供未來許多本研究可行方向,使論文更加完整。 感謝研究所兩年期間師長的教導,讓我對環工領域有更進一步的了 解。感謝親愛的地下水保護及復育實驗室夥伴君傑學長、佳靜學姊、俊祥、 嘉葦、雅菁、欣穆、靜宜、書丞、宗翰對我的教導及包容,同窗好友永惇、 登耀、茂恭、威呈、睿宏學期間的幫忙及勉勵,以及多年好友桂雯、耀挺 的勉勵及扶持,讓我在充滿挑戰的研究生活中,有前進的力量。感謝我的 父母親、姐姐及弟弟,謝謝你們一路支持與鼓勵,讓我可以全力專心於研 究上,完成研究所學業。其他亦有許多要感謝的夥伴,未能一一提起,在 此敬上萬分謝意,謝謝你們對我的照顧。 周志明. I. 2009 年 7 月.
(3) 目錄 第一章 前言............................................................................................ 1 1.1 研究緣起 ...................................................................................... 1 1.2 研究目的 ...................................................................................... 2 第二章文獻回顧........................................................................................ 3 2.1 重金屬污染處理技術................................................................. 3 2.2 奈米樹狀高分子 (Dendrimer)................................................... 8 2.2.1 起源 ............................................................................. 8 2.2.2 高分子演化階段 ......................................................... 9 2.2.3 樹狀高分子之特性 ...................................................11 2.2.4 合成增長樹狀高分子世代 ...................................... 12 2.2.6 樹狀高分子世代計算 .............................................. 15 2.2.7 樹狀高分子之優點 .................................................. 16 2.2.8 樹狀高分子之應用 .................................................. 17 2.2.9 樹狀高分子去除機制 .............................................. 24 2.3 磁性奈米顆粒 ( MNP)............................................................. 29 2.3.1 簡介 .......................................................................... 29 2.3.2 磁性奈米顆粒結構 .................................................. 30 2.3.3 磁性奈米顆粒製備 .................................................. 31 2.3.4 磁性奈米顆粒應用 .................................................. 33 2.4 重金屬去除技術........................................................................ 38 2.5 吸附理論 ................................................................................... 41 2.5.1 吸附之種類 .............................................................. 41 2.5.2 等溫吸附模式 ........................................................... 42 第三章 研究方法.................................................................................... 46 3.1 研究架構 ................................................................................... 46 3.2 實驗材料 ................................................................................... 48 3.3 實驗儀器 ................................................................................... 50 3.3.1 比表面積 (BET-N2)................................................. 50 3.3.2 界面穿透式電子顯微鏡 (TEM) ............................. 50 3.3.3 X光粉末繞射儀 (XRD) ........................................ 50 3.3.4 傅立葉轉換紅外線光譜儀 (FT-IR)........................ 51 3.3.5 界達電儀分析儀 (ZPC) .......................................... 51 3.3.6 感應耦合電漿光譜儀 (ICP) ................................... 51 3.4 模擬重金屬溶液配製............................................................... 52 3.5 材料製備 ................................................................................... 52 3.5.1 製備零價鐵金屬 (ZVI) ........................................................ 52 II.
(4) 3.5.2 製備Fe3O4 磁性奈米顆粒 (MNP) ......................... 52 3.5.3 奈米樹狀高分子複合磁性金屬 (MNP-Gn) .......... 53 3.6 批次實驗 .................................................................................... 56 3.6.1 ZVI、MNP、MNP-Gn 去除重金屬試驗............... 56 3.6.2 MNP-Gn飽和吸附試驗 ............................................ 57 3.6.3 MNP/MNP-Gn (濃縮)再利用試驗........................... 58 3.7 實驗之品保品管..................................................................... 60 第四章 結果與討論................................................................................ 61 4.1 材料特性分析 ........................................................................... 61 4.1.1 比表面積分析 .......................................................... 61 4.1.2 界達電位分析 .......................................................... 62 4.1.3 電子顯微鏡分析 ...................................................... 64 4.1.4 X光粉末繞射儀分析 ............................................... 68 4.1.5 傅立葉紅外光吸收光譜儀分析 .............................. 70 4.2 不同材料去除Zn2+試驗............................................................. 76 4.3 不同價數金屬對pH之試驗 ...................................................... 80 4.4 競爭吸附試驗 ............................................................................ 88 4.4.1 一價、二價、三價金屬競爭吸附試驗 .................. 88 4.4.2 二價金屬競爭吸附試驗 ........................................... 93 4.5 飽和吸附量試驗....................................................................... 97 4.6 酸洗MNP-G3 及MNP去除Cu2+ ............................................... 99 4.7 MNP/MNP-G3 去除 Cu2+重複再利用試驗........................... 102 4.7.1 MNP/酸洗MNP-G3 及濃縮再利用 ....................... 102 4.8 MNP/MNP-G3 去除 Zn2+重複再利用試驗........................... 107 4.8.1 MNP-G5 再利用試驗 ............................................. 107 4.8.2 MNP/MNP-G3 濃縮再利用 ................................... 108 第五章 結論與建議.............................................................................. 112 5.1 結論 ......................................................................................... 112 5.2 建議 ......................................................................................... 113 參考文獻................................................................................................ 115 附錄一 金屬分析之檢量線.......................................................... 128 附錄二 實驗數據 .......................................................................... 130 附錄三 口試委員意見回覆.......................................................... 140. III.
(5) 表目錄 表 2.1 含重金屬廢水之來源與成分 ............................................................... 4 表 2.2 水中重金屬整治技術 ........................................................................... 7 表 2.3 奈米樹狀高分子世代與表面官能基數量相對表............................. 15 表 2.4 奈米樹狀高分子之優點 ..................................................................... 16 表 2.5 化學共沈澱操作參數 ......................................................................... 32 表 2.6 磁性奈米顆粒於環境工程上之應用................................................. 37 表 2.7 零價鐵去除重金屬之機制 ................................................................. 39 表 2.8 奈米碳管去除重金屬 ......................................................................... 40 表 2.9 物理、化學吸附之比較 ..................................................................... 42 表 3.1 初步試驗參數表 ................................................................................. 56 表 3.2 不同價數金屬吸附試驗參數表 ......................................................... 57 表 3.3 飽和吸附試驗參數表 ......................................................................... 58 表 3.4 針對鋅進行再利用測試參數表 ......................................................... 58 表 3.5 針對鋅進行再利用及濃縮參數表..................................................... 59 表 3.6 MNP 及酸洗後 MNP-G3 去除銅參數表 ........................................... 59 表 3.7 MNP 及酸洗後 MNP-G3 濃縮再利用試驗參數表 .......................... 59 表 3.1 初步試驗參數表 ................................................................................. 56 表 3.2 不同價數金屬吸附試驗參數表 ......................................................... 57 表 3.3 飽和吸附試驗參數表 ......................................................................... 58 表 3.4 針對 ZN2+ 進行再利用測試參數表 .................................................. 58 表 3.5 針對 ZN2+進行再利用及濃縮參數表................................................ 59 表 3.6 MNP及酸洗後MNP-G3 去除 CU2+參數表........................................ 59 表 3.7 MNP及酸洗後MNP-G3 濃縮再利用試驗參數表 ............................ 59 表 4.1 MNP 和 MNP-GN 之比表面積 .......................................................... 62 表 4.2 各材料等電位點.................................................................................. 62 表 4.3 不同磁性奈米顆粒平均粒徑 ............................................................. 66 表 4.4 磁性奈米顆粒及樹狀高分子官能基之特徵波峰..............................71. IV.
(6) 圖目錄 圖 2.1 奈米樹狀高分子增長結構圖 ............................................................... 8 圖 2.2 聚合物發展歷程 ................................................................................. 10 圖 2.3 奈米樹狀高分子之結構與參數計算示意圖..................................... 12 圖 2.4 分歧/收斂合成示意圖........................................................................ 13 圖 2.5 以NH3 為核心合成奈米樹狀高分子 ................................................ 14 圖 2.6 環胺化反應過程圖 ............................................................................. 14 圖 2.7 奈米樹狀高分子世代計數法 ............................................................. 15 圖 2.8 不同世代於不同 pH 吸附量變異圖..….………….…………….........18 圖 2.9 殼/核合成步驟 .................................................................................. 20 圖 2.10 奈米樹狀高分子回收再利用示意圖............................................... 21 圖 2.11 (A) 加入 MA 合成半世代;(B) 加入 EDA 合成全世代;(C) 合成所 需世代 (Gn)………..…...……………….…..…………….........23 圖 2.12 銅與奈米樹狀高分子配位環境示意圖........................................... 26 圖 2.13 奈米鐵之界達電位分析圖 ............................................................... 27 圖 2.14 改變不同 pH 吸附水中砷之試驗………..….………….…….........27 圖 2.15 高分子捕捉金屬示意圖 ................................................................... 28 圖 2.16 四氧化三鐵之晶格結構 ................................................................... 30 圖 2.17 奈米樹狀高分子複合磁性金屬及吸附鍵結流程........................... 34 圖 2.18 加入乙酸脫附試驗 ........................................................................... 35 圖 2.19 製備 G-Dendrimer PAMAM-SBA-15 及 EDTA modified Gn-PAMAM-SBA-15 流程圖…..…...………….…………….........36 圖 3.1 研究架構圖 ........................................................................................ 47 圖 3.2 奈米樹狀高分子複合磁性金屬流程圖 ............................................ 55 圖 4.1 MNP 與 MNP-G3 界達電位圖 .......................................................... 63 圖 4.2 磁性奈米顆粒之 TEM 圖 .................................................................. 64 圖 4.3 MNP-G0 之 TEM 圖........................................................................... 65 圖 4.4 MNP-G3 之 TEM 圖........................................................................... 65 圖 4.5 吸附重金屬後之 MNP-G3,經還原後之 TEM 分析圖 .................. 66 圖 4.6 MNP 之 EDX 分析圖譜...................................................................... 67 圖 4.7 MNP-G0 之 EDX 分析圖譜................................................................ 68 圖 4.8 MNP XRD 標準圖譜 (PCPDFWIN) ................................................ 69 圖 4.9 MNP 複合不同世代高分子之 XRD 分析圖譜................................. 70 圖 4.10 MNP FT-IR 圖譜................................................................................ 72 圖 4.11 MNP-Gn (n=0、3、5) FT-IR 圖譜………..….……………….........73 圖 4.12 加酸脫附後之 FT-IR 圖譜………..….………….…………….........74 V.
(7) 圖 4.13 磁性奈米顆粒及高分子材料對重金屬 (Zn2+) 去除關係圖..........77 圖 4.14 ZVI 去除重金屬之影響關係圖 ....................................................... 78 圖 4.15 ZVI-G5 去除重金屬之影響關係圖 ................................................. 79 圖 4.16 不同價數金屬去除效率比較關係圖............................................... 82 圖 4.18 一價、二價金屬去除效率比較關係圖........................................... 84 圖 4.19 二價金屬 pH 6 去除效率比較關係圖………………………..........85 圖 4.20 二價金屬 pH 7 去除效率比較關係圖………………………..........86 圖 4.21 MNP-G3 去除重金屬 Zn2+之關係圖………………………...........87 圖 4.22 不同價數金屬於 pH 4 競爭吸附關係圖……………………..........89 圖 4.23 不同價數金屬於 pH 5 競爭吸附關係圖……………………..........90 圖 4.24 不同價數金屬於 pH 6 競爭吸附關係圖……………………..........91 圖 4.25 不同價數金屬於 pH 7 競爭吸附關係圖……………………..........92 圖 4.26 二價金屬於 pH 4 競爭吸附關係圖…………………………..........93 圖 4.27 二價金屬於 pH 5 競爭吸附關係圖…………………………..........94 圖 4.28 二價金屬於 pH 6 和 pH 7 競爭吸附關係圖.………………..........96 圖 4.29 Zn2+之飽和吸附量模擬圖........…..…..…..…..….…………............97 圖 4.30 MNP 去除重金屬 Cu2+之關係圖………..….……………….........100 圖 4.31 酸洗過後之 MNP-G3 去除重金屬 Cu2+之關係....…..…..….......101 圖 4.32 脫附劑 0.05 %,酸洗 MNP-G3 濃縮重複再利用及回收率圖 .. 103 圖 4.33 脫附劑 0.1 %, 酸洗 MNP-G3 濃縮重複再利用........................... 104 圖 4.34 脫附劑 0.1 %, 酸洗 MNP-G3 回收率圖....................................... 105 圖 4.35 脫附劑 1 %,酸洗 MNP-G3 濃縮重複再利用及回收率圖 ........ 106 圖 4.36 MNP-G5 重複再利用關係圖.......................................................... 108 圖 4.37 MNP-G3 濃縮重複再利用 ............................................................. 109 圖 4.38 MNP-G3 回收率關係圖.................................................................. 110 圖 4.39 MNP 濃縮重複再利用及回收率關係圖........................................ 111. VI.
(8) 奈米樹狀高分子複合磁性金屬吸附重金屬之研究 指導教授: 連興隆 博士 國立高雄大學土木與環境工程學系. 學生:周志明 國立高雄大學土木與環境工程學系. 摘要. 本論文研究主要目的是利用奈米樹狀高分子複合磁性金屬 (MNP-Gn, n 為樹狀高 分子之世代)去除水中重金屬,探討去除效率及可能之去除機制,並測試其回收再利用 及濃縮重金屬之可行性,提升其可利用性及回收效率。試驗主要分為三部份進行 : (1) 利用共沉澱法製備磁性奈米顆粒 (MNP),並製備複合樹狀高分子材料;(2) 以 MNP 及 MNP-Gn 對水中重金屬進行等溫吸附試驗; (3) 探討 MNP 及 MNP-Gn 之回收再利用 效率。試驗過程主要影響因子包括重金屬種類、世代、材料用量及 pH。XRD 分析確認 自製材料為 Fe3O4。奈米樹狀高分子複合磁性金屬經 TEM 與 BET-N2 分析得知,粒徑 大小約 10 nm,比表面積為 56.96 m2/g;利用 FT-IR 確認樹狀高分子成功複合於 MNP 表面。 樹狀高分子 (dendrimer)去除機制主要分為螯合作用及表面靜電引力之吸附兩種, 由本實驗結果發現,使用 MNP-G3 去除 50 mg/L Zn2+溶液,24 小時內可達 70 %以上 之去除效率。pH < 3 時,不利於 MNP-G3 吸附;反之,當提升 pH 則有利於重金屬之 吸附。MNP-G3 對 Zn2+最大飽和吸附量為 24 mg/g。酸性條件下,MNP-G3 去除不同價 數金屬之能力為 : As5+>Al3+>K+>Zn2+>Cu2+>>Li+,其中砷 (As) 於酸性環境下是以負電 型態存在,有效與帶正電之 MNP-G3 進行吸附,證明此系統有靜電交互作用之機制存 在;另一方面,一價金屬 Li+無明顯去除效率,證實低原子序鹼金族金屬無法進行錯合 反應,且金屬離子價數越高,其去除效率亦隨之增加。由 MNP-G3 進行回收再利用試 驗中發現,其再利用達 10 次以上。針對脫附劑測試發現僅需使用 10 ml HCl (1 %),即 可以有效將吸附於 MNP-G3 表面之金屬離子完全脫附。 關鍵字:奈米樹狀高分子、磁性金屬、回收再利用. VII.
(9) Dendrimer modified magnetic nanoparticles for adsorption of heavy metals Advisor: Dr. Hsing-Lung Lien Department of Civil and Environmental Engineering National University of Kaohsiung Student: Chih-Ming Chou Department of Civil and Environmental Engineering National University of Kaohsiung ABSTRACT Removal of heavy metals from wastewater using dendrimer modified magnetic nanoparticles (MNP-Gn, n is different generation) was examined in batch reactors. In this study, the MNP-Gn was synthesized, characterized and examined as reusable adsorbents of heavy mental. Parameters that may affect the adsorption such as the different metal ions、 dendrimer generation、MNP-Gn loading and pH were evaluated. X-ray diffraction spectra showed that the MNPs were in the form of Fe3O4. Field emission transmission electron microscope images showed that the particle size was about 10 nm. The specific surface area of MNP-Gn was 56.96 m2/g. Fourier transform infrared spectrometer indicated that dendrimers were successfully coated onto the surface of magnetic nanoparticles (Fe3O4). The adsorption efficiency of zinc ions increased with increasing pH. The result was observed that MNP-G3 removed Zn2+ about 70 % at pH 7. The maximum adsoption capacity determined by Langmuir model is 24 mg/g at pH 7 and 25 ℃. At pH less than 3, heavy mental is readily desorbed. In addition, the MNP-Gn can be regenerated using the doluted HCl aqueous solution (1 %) where Zn2+ and Cu2+ can be recovered in a concentrated form. It was found that the MNP-Gn underwent ten consecutive adsorption-desorption still retained the original removal capacity of Zn2+ and Cu2+. Key word: dendrimer、magnetic nanoparticles、reuse、recycle. VIII.
(10) 第一章 前言 1.1 研究緣起 土壤中及地下水之重金屬污染及工廠排放之重金屬廢液是台灣常見 且不易處理之環境問題,加上重金屬不像有機類物質可以降解轉換成較 簡單物質,以有效降低其濃度,因此,如何有效將重金屬固定或是從污 染區域移除,成為目前主要整治技術目標。依目前所使用傳統處理技術, 像是淋洗法、酸洗法,可以有效將重金屬從污染場址移除,達到法規標 準,但後續金屬離子和水溶液分離效果不彰,無法根本處理重金屬問題。 故針對後續處理重金屬廢液且可以有效回收成為技術開發的瓶頸。. 近年來,去除水體重金屬方法眾多,像是使用奈米零價金屬已被廣 泛研究於含氯有機污染物之還原降解及重金屬的吸附固定,近年來更已 逐步應用於現地污染整治上。由於奈米零價鐵具備對重金屬吸附及可受 磁之特性,成了做為土壤酸洗後,將酸洗液中重金屬吸附,再以磁選方 式分離奈米零價鐵與重金屬的適合材料。但其吸附後之脫附效果不佳且 回收再利用率低,限制其於環境之運用性。. 樹狀高分子 (Dendrimer) 是一種新穎且立體結構奈米材料,其有高 分散性、高反應性及可回收再利用等優點。據 Xu and Zhao (2005) 研究 指出,樹狀高分子具快速及有效處理重金屬之能力外,另具有極佳之脫 附能力,可重複使用。雖然有上述優點,但目前回收技術是利用超微過 濾膜 (ultrafiltration membrane)方式回收 (Diallo et al., 2005),其單價昂 貴,就經濟層面而言,實際處理大量重金屬廢液並不可行。. 1.
(11) 磁性奈米顆粒 (Magnetic Nano Particle, MNP) 為去除水中污染物之 新穎材料,其製備方式簡易,僅需使用二價鐵金屬及三價鐵金屬混合溶 液,調整 pH 於鹼性環境下,便可以製備出磁性奈米顆粒 (Fe3O4)。國內 研究中發現 (陳和秦, 2005),除本身可以吸附重金屬外,並具有利用外加 磁場,進行吸附後快速回收之優點。. 本研究欲將兩材料之優點去除水中重金屬,且藉由磁選分離,將吸 附於樹狀高分子的重金屬移除,且此複合材料具再利用及重金屬濃縮之 功能,降低材料成本,增加其應用性。. 1.2 研究目的 本研究主要目的為: 1. 探討奈米樹狀高分子複合磁性金屬(MNP-Gn)處理重金屬污染水體之 可行性,並探討其中不同環境參數之影響與可能機制。 2. 探討處理完重金屬後之奈米樹狀高分子複合磁性金屬 (MNP-Gn)於回 收再利用之成效,發展重金屬回收最佳操作技術。 結合以上兩點,本研究將藉由此複合材料 (MNP-Gn)探討回收金屬 之可行性。並希望利用此方法,回收水中重金屬後進行濃縮,已達最佳 經濟效益。. 2.
(12) 第二章 文獻回顧 2.1 重金屬污染處理技術 重金屬污染常在水體及土壤中被討論,而且屬於蓄積性污染物質 (conservative pollutants),於生態環境中無法自然分解,常經由微生物代 謝、轉化,再經由食物鏈之生物放大現象而積蓄於生物體內。常見重金 屬如汞 (Hg)、砷 (As)、鎘 (Cd)及鉻 (Cr)等在過去歷史上都發生過重大 污染事件,進而危害到人類的生活環境。在日本,發生舉世聞名的水俁 病 (Minamata disease),即是日本九州之熊本縣南端的水俁灣附近,因甲 基汞污染造成的危害。此外還有日本富山縣神通川流域之痛痛病 (Itai-Itai disease),則是上游採礦業者之排放廢水中含鎘,下游居民引水灌 溉,導致重金屬積蓄在植物體中,最終由人體吸收累積導致疾病產生。 在台灣本島部份,過去在南部沿海地區,因長期飲用含砷的地下水而罹 患烏腳病 (Blackfoot disease)。還有重金屬砷及鎘污染事件在台灣有發生 過實例,當這些重金屬物質累積在人體中,皆會對人體造成病變。但若 要有效去除水體或是土壤之重金屬都必須花費時間及經費,故要如何有 效提高去除效率及降低成本將是一大挑戰。. 台灣廢水重金屬主要來源為工廠廢水、半導體產業、金屬表面處理 產業及電鍍廠等大量含重金屬廢液之排放源,若這些廢液未經妥善處理 即排放,對人體及自然環境皆是一大影響,而其主要產生重金屬廢液之 產業整理如表 2.1 所示:. 3.
(13) 表 2.1 含重金屬廢水之來源與成分 金屬 銅 銀 鉻 鉛 鎳 鋅 鎘 砷. 廢水來源. 地下水標準 飲用水標準 電鍍、電線工業 1 1.0 照相沖洗業、電鍍 0.05 電鍍、鉻鞣皮製革 0.05 0.05 電池製造、鉛礦山、塗料製造 0.05 0.05 電鍍 0.1 0.1 電鍍、紡織工業 5 5.0 電鍍 0.005 0.005 礦石處理、製革廠、農藥、玻璃、染料製造 0.05 0.01 (改繪 楊, 2003;行政院環保署)(單位:mg/L). 此 外 , 近 日 常 被 廣 泛 討 論 的 便 是 化 學 機 械 研 磨 廢 水 (Chemical Mechanical Polishing, CMP),雖然這類廢水可以經過稀釋,其中固體物含 量、COD、金屬濃度皆可以通過事業放流水標準,而且只要經調整酸鹼 值即可以進入污水處理廠中,但是在美國半導體產業協會(Semiconductor Industry Associaytion, SIA)提倡節水策略及放流水標準越來越高下,這類 的重金屬廢水已經不能再用傳統稀釋方法處理 (鄧等, 2002)。在其他研究 發現,化學機械研磨之廢水,其因為製造過程中會使用大量超純水清洗研 磨過後晶圓之表面,故在廢水中常會含有大量奈米尺寸的懸浮物質,其因 顆粒過小難以沈降,導致去除效率不佳,更嚴重影響放流水水質 (陳和秦, 2005)。. 目前台灣針對土壤及水體中重金屬做回收較常用的處理方法,主要 有分為兩大方向: 土壤重金屬污染:目前土壤重金屬污染嚴重,而常見的處理方法大 都利用螯合劑及酸液淋洗的方法,但這些方法也會帶來一些環境的副作 用。另一方面,當土壤受重金屬污染後,其重金屬往往會被土壤表層的. 4.
(14) 植物所吸收,最後經由食物鏈到人體中。其中,不同植物在不同土壤中 對重金屬離子有不同的吸收與積聚作用,一般而言,農作物在土壤中吸 收重金屬的程度為:鎘>鋅>汞>銅>鉛>砷>鉻,其中鎘、鋅、汞、 銅、鉛等五類重金屬較可能被植物吸收且易積聚於植物體內 (葉, 2002)。 如果不能有效發展出處理重金屬技術,對於整個生態環境都會造成相當 大的衝擊。目前主要的整治技術大致可以分為三大類:(1)將污染物從土 壤中移除。(2)將污染物侷限於污染介質中以阻止或減少污染物釋出。(3) 用換土或稀釋方式降低重金屬污染濃度及危害 (陳, 2003)。就使用原理可 包含物理、化學及生物處理,相關比較如表 2.2 所示:. 水體中重金屬污染:目前常見的處理方法像是混凝沈澱法,會利用 硫酸鋁 (明礬)、氯化鐵、硫酸亞鐵等混凝劑加入水體中,進而形成膠羽 沉澱。此外還有薄膜過濾、電化學混凝…等方法,都已經在實場運用, 其各種技術原理及優缺點綜合比較如表 2.3 所示:. 5.
(15) 表 2.2 土壤重金屬整治技術 排土與客土 法 物理性 氧化法 還原法 化學性 酸洗法 淋洗法. 原理概述 優點 缺點 將 上 層 污 染 土 壤 移 適 用 於 重 金 屬 污 染 客土後須比原耕 除,隨後回填無污染 土壤。 地的水平高,若 土壤。 處理效果快速 為水田會有水管 理不便之虞。 污染土壤去處。 使金屬失去電子,改 有 效 處 理 含 氯 有 機 氧化還原速度較 變其氧化態,使其毒 溶劑、多環芳香烴、 難預測。 性、溶解性及移動性 酚 類 、 石 油 系 化 合 土壤孔隙阻塞。 降低。 物、無機氰化物。 地下生態環境衝 擊。 藉由控制地表下的 當污染物移動至還 氧化還原作用,使之 原區域時,將會進行 成為還原狀態。當污 還 原 性 分 解 或 因 沈 染 物 移 動 至 還 原 區 澱而被固定。 域時,將進行還原性 污 染 物 被 分 解 時 會 分解或因沉澱而被 產生二氧化碳或毒 固定。(六價鉻還原 性較低物質。 成三價鉻) 以 弱 酸 (0.1 N 可以經由前處理、萃 產生大量廢酸, HCl、醋酸、檸檬酸) 取、分離、萃取劑再 破壞土壤質地。 作 受 重 金 屬 污 染 土 生、土壤後續處理有 使用化學藥品可 壤之萃取劑。 效分離重金屬。 能會造成水質二 次污染。 利用酸或鹼 (HCl、 可 以 用 於 現 地 土 壤 廢酸可能會破壞 H3PO4、NaOH) 及螯 淋 洗 法 及 非 現 地 土 土壤質地。 合 劑 (EDTA 、 壤洗滌法。 DTPA、EDDS) 作為 淋洗液材料。. 植物復育法. 生物性. 利用植物根部將金 屬吸附、濃縮及沈 澱,此過程僅與物理 吸附作用有關,並不 涉及生物作用。目前 常選用陸生植物,因 陸生植物跟較水生 植物長且廣。. 價格低廉。 營造綠地 (景觀)。 綠色工程。 土壤穩定化。. 6. 整治時間長。 無法處理深層土 壤。 氣候因素影響植 物生長及整治成 效。 高濃度金屬對植 物體毒害。. 葉, 2002. 陳和高, 2002 葉, 2002. 陳, 2003. 吳, 2004. 陳, 2007.
(16) 表 2.2 水中重金屬整治技術 混 凝 沈 澱. 薄 膜 過 濾. 電 化 學 混 凝. 離 子 交 換. 金 屬 置 換. 電 解 沈 積. 原理概述 在水體中加入混凝劑 (鐵 鹽、鎂鹽) 使表面電雙層 壓縮,並使表面電位能下 降,最後使小顆粒凝聚成 大顆粒以重力方式沈降 利用薄膜微孔隙尺寸及 外加壓力使水分子可以 穿透薄膜,藉此留下大分 子污染物。目前已可以有 效去除膠體微粒、微生 物、有/無機污染物等. 優點 技術成熟 廣泛使用. 缺點 佔地空間大 產生大量污泥 加藥量不易控制. 技術成熟 佔地空間小 適用低濃度顆粒去 除. 易造成孔隙阻塞 分離顆粒大小範 圍需特別控制 不適大量極高濃 度污染物. 利用電壓產生電場效 應,將水中微粒電性轉變 成上下均勻的帶電體,使 顆粒間因電性相吸作用 聚集。金屬極板 (鐵、鋁 板) 釋出之鐵、鋁鹽使聚 集的顆粒因混凝機制而 去除 利用離子交換樹脂,藉由 交換/吸附水溶液中的陰 陽離子,達到去除水中離 子態污染物. 佔地空間小 可同時去除研磨顆 粒、氧化劑、金屬離 子等污染物 去除效率穩定,不受 CMP 廢液性質影響. 尚於研發階段 對於低濃度金屬 離子去除效果有 限. 金屬離子去除率佳 可再生利用. 化學置換反應以一正電 的金屬固體當做犧牲金 屬,將具負電性的金屬離 子還原置換出來,以達到 回收溶液中重金屬的目 的,而主要的驅動力,則 為兩種金屬反應物之氧 化還原電位差,造成兩反 應物間電子轉移 利用直流電漿金屬離子 還原沈積在陰極上,並可 以有效去除電鍍廢棄物 銅、氰化物 (鎘、鋅、銅)、 錫鉛合金 (金、銀、鎳). 成本較低 裝置簡便. 無法去除離子以 外之污染物 必須先去除 CMP 廢水中的氧化劑 操作費用高 回收量難估計 無法再生利用 過程會產生大量 氫氣,影響操作的 安全性. 回收金屬效率高 電極可重複使用 能源成本低. 7. 特殊溶液會腐蝕 金屬極板及產生 氯氣 有機物質會造成 金屬板沈積與萎 化現象. 資料來源 鄧等, 2002. 鄧等, 2002. 鄧等, 2002. 侯, 2004. 黃, 2005. 侯, 2004.
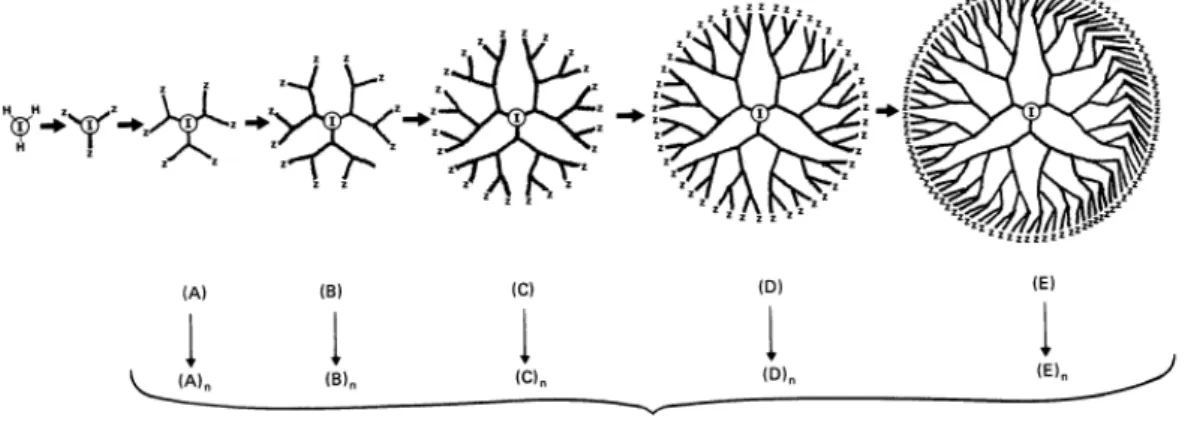
(17) 2.2 樹狀高分子 (Dendrimer) 2.2.1 起源 Dendrimer 起 初 是 於 1985 年 被 美 國 Dow 化 學 公 司 (Dow Chemical)的前科學家 Tomalia 博士所製成,它利用 Michael addition 製 備方式完成材料,而 poly (amidoaminedrimer) (簡稱 PAMAM) 即為最早 的 Dendrimer。此字是源於希臘文字中的 dendri- 像樹狀的分叉以及 meros- 一部份的意思組成 (蔡, 2005)。如圖 2.1 所示,就結構類似樹上 分枝會不斷生長出新的分枝,依此循環狀態生長下去,最後會形成類似 一立體圓球形狀;此外,Dendrimer 為一種尺寸小且具有多孔性的奈米 材料,其內部空間大、低黏度、結構設計多樣化等優點。與傳統的線性 高分子做比較,樹狀高分子具有較精確控制的結構,呈圓球狀或半圓球 狀;目前研究方面,以 PAMAM 為基礎所組成的一系列衍生物最先被用 來商業化,另外國內外也著重於材料及生化醫學方面研究,甚至於製作 儲存更大量資料的晶片及電子元件。. 圖 2.1 Dendrimer 增長結構圖 (Tomalia et al., 1985). 8.
(18) 2.2.2 高分子演化階段 日常生活中常會使用到高分子聚合物,最早於 1930 年首先開發出線 型高分子材料,也開創聚和物研究大門,隨後到 40 年代研發出交錯線型 聚和物,一直到現今也發展出樹狀高分子 (黃, 1994)。. 對於高分子的共價合成 (covalent synthesis) 主要可以分為三個階 段:(一) 傳統有有機化學 (traditional organic chemistry)、(二) 傳統聚合 物 化 學 (traditional polymer chemistry) 、 ( 三 ) 樹 枝 狀 巨 型 分 子 化 學 (dendritic macromolecular chemistry)。 從過去聚合物發展史中,已經從最初單純的原子態 (atoms),逐漸發 展到單分子狀態 (monomers),到現在的高分子材料 (polymers)。在這發 展期間,我們可以簡單將其分成四大類型:(a) 線型分子(linear),如塑膠 玻璃 (Plexiglass)及尼龍 (Nylon);(b) 交錯型分子 (cross-linked),如橡膠 (Rubbers)及環氧化合物 (Epoxies);(c) 分歧型分子 (branched),如低密 度聚乙烯 (low density polyethylene);(d)高分子型 (dendritic)。一般而言, 聚合物的型態決定了聚合物本身所展現出來的物理及化學性質,線型分 子和分叉型分子是屬於熱塑性聚合物 (thermoplastic polymer),而交聯型 分子是屬於熱固性聚合物 (thermoset polymer),而由圖 2.2 可以更清楚聚 合物發展歷程。. 9.
(19) 圖 2.2 聚合物發展歷程 (Tomalia et al, 2005) 由於不同的分子結構所呈現的聚合物特性都是獨一無二的,因此在 熱塑性及熱固性這兩塊聚合物的領域中蘊含著無限的商機。1922 年時提 出巨型分子假說,並且將苯乙烯經由加熱過程製造出聚苯乙烯,於 1953 年時對於聚合物巨型分子假說,大約有五十年的時間裡,在聚合物科學 的領域中將其簡易地分為兩大結構,即線型 (熱塑性)和交錯型 (熱固 性),並且致力於研究結構差異所導致的不同性質。也因此在第二次世界 大戰期間,大量的聚合物被發展出來而取代了天然聚合物;在 1960 年代 到 1970 年代時,長鏈分歧型的聚烯烴化合物及其它相關的分枝系統開始 被研發出來,近年來的研究重點則是著重於將聚烯烴類做成 “任意性的 長鏈分枝” (random long branched) 及 “樹枝狀結構” (dendritic topologies) (蔡, 2005)。. 10.
(20) 2.2.3 樹狀高分子之特性 Dendrimer 樹枝狀分子分叉具均一性,且當分歧到一定程度則成圓 球狀,如圖 2.2 所示,雖然看似結構複雜,但是基本單元相當單純,包 括了核心 (core)、重覆單元 (repeating unit)、末端單元 (terminal unit)。 此 外 , 較 次 要 部 位 還 包 含 分 岔 連 接 點 (branch juncture) 、 末 端 位 置 (terminal site)、空隙體積 (void volume)等 (Andrew, 2008)。. 此外可以利用一些計算公式,推算出表面官能基、分岐支鏈、分子 量之數量,對後續增長世代及吸附污染物都有很大助益(Tomalia et al., 2005),其計算方式及型態(圖 2.3)如下所示: 末端官能基 (Number of Surface): Z = NC Nb. G. (2.1). 分歧核心 (Branch core): ⎡ N G −1 ⎤ BC = N c ⎢ b ⎥ ⎢⎣ N b − 1⎥⎦. (2.2). 分子量計算 (Molecular Weight): ⎡. ⎤ ⎛ Nb G −1 ⎞ ⎟⎟ + M 1 N b G ⎥ ⎝ Nb ⎠ ⎦. Mw=MC+NC ⎢ M RU ⎜⎜ ⎣. 11. (2.3).
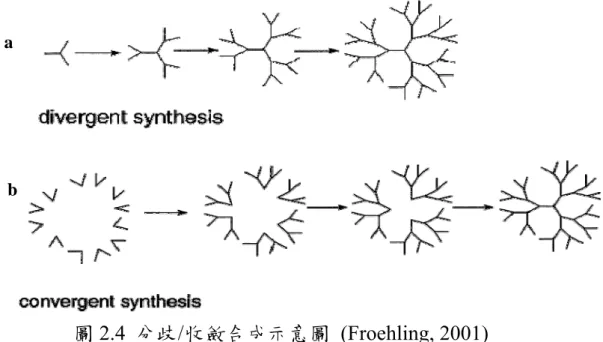
(21) 圖 2.3 Dendrimer 結構與參數計算示意圖 (Tomalia, 2005). 2.2.4 合成增長樹狀高分子世代 目前 Dendrimer 已經發展出兩種不同製程方式,主要可以將合成法 分成分歧型 (divergent synthesis) 和收斂型 (convergent type),此兩種方 法 都 可 以 有 效 助 於 世 代 增 長 。 如 圖 2.4 所 示 : (a) 分 歧 式 聚 合 法 (divergent synthesis):其法主要是利用單一 Dendrimer 核心,隨外部單體 加入,進行一連串物化反應,使 Dendrimer 不斷再生、擴充其世代。(b) 收 斂式聚合 (convergent synthesis ):主要先進行外圍分子反應並進行分枝產 生,每一分子都含許多官能基,其中官能基會和起始化合物進行反應, 不斷重複此步驟,即可得到所需世代之高分子聚合物 (Froehling, 2001)。 在此兩方法中,以第一種較為常見,且在製作過程上較為簡易。分 歧式分子量增加方式為指數型成長,而收斂式分子量則是以倍數形式增 加。此外,利用分歧式聚合法已可以發展出至 15 世代,並且可以依需求 發展出不同世代或是不同末端官能基之樹狀高分子。. 12.
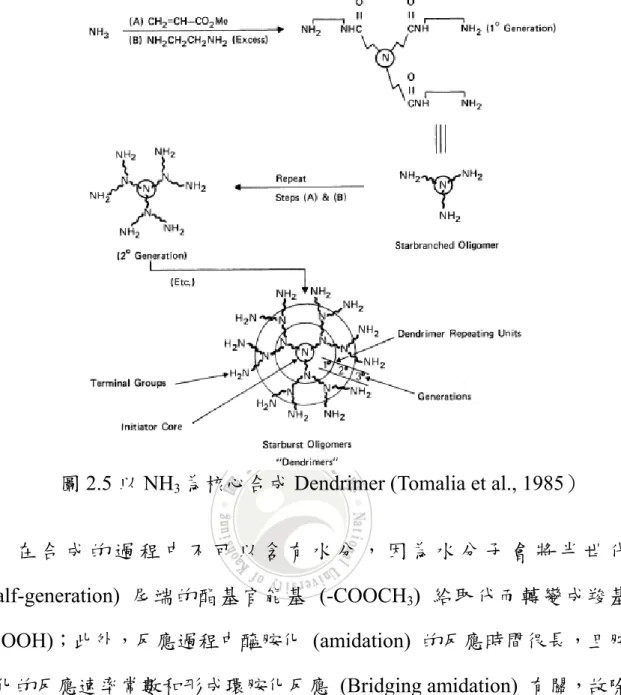
(22) a. b. 圖 2.4 分歧/收斂合成示意圖 (Froehling, 2001) 由 1985 年 Tomalia 等人所提出的方法,主要是利用胺 (amine)和 丙烯酸甲酯 (methyl acrylate) 於甲醇中進行 Michael addition 合成,其目 的先合成 Dendrimer 核心,隨後在加入過量的乙二胺 (ethylene diamine) 合成出支鏈核心,最後在進行醯胺化反應 (amidation),以生成第一代 PAMAM Dendrimer , 隨 後 只 要 一 直 加 入. methyl acylate 和. ethylenediamine 進行醯胺化,便可以依需求製造不同世代 Dendrimer (蔡, 2005;Tomalia et al., 1985)。其流程如圖 2.5 所示:. 13.
(23) 圖 2.5 以 NH3 為核心合成 Dendrimer (Tomalia et al., 1985) 在合成的過程中不可以含有水分,因為水分子會將半世代 (Half-generation) 尾端的酯基官能基 (-COOCH3) 給取代而轉變成羧基 (-COOH);此外,反應過程中醯胺化 (amidation) 的反應時間很長,且胺 基化的反應速率常數和形成環胺化反應 (Bridging amidation) 有關,故除 了考慮所需加入乙二胺的量以外,尚且要注意反應時的溫度不可超過 50 ℃,或使半世代的產物置於 120 ℃以上的高溫,因為產物可能會進行逆 向合成反應 (retro-Michael addition),如圖 2.6 所示:. 圖 2.6 環胺化反應過程圖 (Tomalia et al., 1985). 14.
(24) 2.2.6 樹狀高分子世代計算 Dendrimer 其中一項優點就是可以依不同需求製作不同世代的高分 子,其世代分類如圖 2.7 所示,計算方式是從表面官能基和核之間的分 支次數來定義。簡單的說,就是核的分支及表面官能基不算,再計算這 兩者間的分叉次數。末端官能基部份會依循一定倍率增加且均勻分布, 所以會有圓球狀的高分子結構產生 (黃, 1994)。. 圖 2.7 Dendrimer 世代計數法 (黃, 1994) 文獻中提到,隨著世代增加,末端官能基、分子量、直徑也會相對 增加,可由零世代 (G0) 4 個末端官能基增長至七世代 (G7) 512 個末端官 能基、甚至更多 (表 2.4)。理論上增加吸附位址,更可有效吸附金屬離子 (Tomalia et al., 2005)。 表 2.3 Dendrimer 世代與表面官能基數量相對表 Generation 0 1 2 3 4 5 6 7. NH2 Surface Groups 4 8 16 32 64 128 256 512. Molecular Formula C24H52N10O4S2 C64H162N26O12S2 C144H292N58O28S2 C304H612N122O60S2 C624H1262N250O124S2 C1264H2532N506O252S2 C2544H5092N1018O508S2 C5104H10212N2042O1020S2. 15. MW. Diameter (nm). 609 1.5 1,522 2.2 3,348 2.9 7,001 3.6 14,307 4.5 28,918 5.4 58,140 6.7 116,585 8.1 (改繪於 Tomalia, 2005).
(25) 2.2.7 樹狀高分子之優點 Dendrimer 其優點主要來自於它特殊的形狀及眾多末端官能基可以 吸附污染物,文獻提到,將 Dendrimer 至於水溶液中,有著 (a)可有效吸 附金屬離子,並可經化學反應形成奈米顆粒、(b) 容易控制尺寸及複合金 屬顆粒、(c) Dendrimer 空孔部份可以大量存放金屬離子、(d) 可依序將其 複合在載體表面、(e) 可將 Dendrimer 存放在奈米碳管反應器中使用 (Ploehn et al., 2002),其他優點如表 2.5 所示。. 表 2.4 Dendrimer 之優點 優點 低黏度 低毒性 分散性佳 高反應性 高乘載量 可回收再利用 多末端官能基 依不同目的設計成不同分子. 功能 水溶液中懸浮性佳 已有針對人體研究 易分散於液體中,且不易沉澱 反應速率快,短時間內即有成效 除末端官能基外、核心亦有吸附能力 依過濾程序重複使用 隨世代增長,可提升吸附能力 去除不同污染物則使用不同世代. 有了上述優點,針對去除水中重金屬會有很大助益,不過就目前回 收再利用方面只限於使用過濾膜,但其價格昂貴,所以目前尚未廣泛使 用。故本研究欲將 Dendrimer 複合於載體上,並使用磁性奈米顆粒複合 樹狀高分子之概念,藉此提高吸附量及回收效率。. 16.
(26) 2.2.8 樹狀高分子之應用 國外研究樹狀高分子已行之多年,並在水及土壤中都有應用實例。 學者 Xu and Zhao (2005) 就曾經使用不同世代、末端官能基之高分子進 行受污染土壤中金屬銅的回收,實驗結果發現,當改變 Dendrimer 世代 數、濃度、pH、末端官能基種類時,皆對去除率有影響,結果也發現當 使用 Dendrimer G4.5-COOH,試驗環境在 pH=6 時,最高去除率可達 90 %,證實高分子材料可以吸附鍵結銅離子,達去除之能力。在同篇文獻 也提到,如果 Dendriemr 相同劑量情況下,較低世代的高分子材料會可 以去除較多的金屬;此外,實驗結果也發現,利用不同類型的樹狀高分 子材料於酸性 (pH<3) 環境時,可有效將金屬脫附;反之,當環境 pH >5 以上將會提高吸附鍵結的能力,亦提供一回收再利用之想法。. 理論上,世代越高表面官能基會提供更多可鍵結金屬之位址,亦會 增加其對重金屬去除能力,但是 Xu and Zhao (2005) 於試驗中發現,世 代越高會對鍵結能力造成相當影響:(1) 在動力學觀點,顆粒較小的物質 (世代低) 相較於顆粒大的材料 (世代高) 所受到阻力較小。(2) 當高分子 世代較小時 (<3),雖然表面官能基群較少,但是表面較易和銅離子進行 鍵結;而當高分子世代較高時 (≧3),表面官能基數量雖提昇,形狀更接 近立體球形,但是表面官能基群緊實,反而不易和銅離子進行反應。. Diallo et al. (1999) 也利用更高世代 Dendrimer 來試驗,他使用 G3~G8 世代的 Dendrimer 測試,改變不同 pH 值,觀測其吸附銅離子變. 17.
(27) 化,由圖 2.8 可以清楚看到,當 pH 偏於酸性偏中性 (pH 5.9~6.1) 效果 最好,而且在同劑量條件下,世代越高其吸附鍵結效果越好;當偏向過 酸或是過鹼時,由圖可以發現鍵結效率極低,其文獻中解釋是因為過酸 或是過鹼,其氫離子或是氫氧根離子會劇增,導致 Dendrimer 末端官基 會形成質子配位基,佔據原本可以吸附重金屬的位置;另一方面,過酸 環境下,於其他文獻都提到會增加 Dendrimer 脫附效果,所以由此可以 發現除了在中性外,其他 pH 對於末端官能基會造成相當影響。. 圖 2.8 不同世代於不同 pH 吸附量變異圖 (Diallo et al., 1999) 相同研究團隊在 2005 年將 Dendrimer 樹狀結構比擬成一種超過濾 系統,藉此回收水體中二價銅。過程中,使用三種不同世代的 Gn-NH2 (n=3、4、5)高分子進行試驗,結果發現當提昇 pH 確實對於吸附效果 有明顯提昇,再次證明吸附系統中酸鹼值的重要性 (Diallo et al., 2005) 。 相同論點也在 Rether and Schuster 學者於 2003 年提出,試驗使用 PAMAM polymers 鍵結 (Dendrimer ligand) 去除重金屬 Co(II)、Cu(II)、. 18.
(28) Hg(II)、Ni(II)、Pb(II) 和 Zn(II)。結果顯示,當 pH 9 時,Cu(II)和 Hg(II) 會穩定鍵結於 Dendrimer 上,且可以藉由降低 pH 回收重金屬、將高分 子材料重複再利用。. 另有針對於赤鐵礦 (Fe2O3)進行吸附試驗 (Pan et al., 2004),實驗中 發現,降低 pH 會導致 Dendrimer 表面帶正電,也會造成如先前說提及 之質子化情形發生。而當利用 Dendrimer G3 於不同 pH 下測試發現,pH 9 時,帶正電的 Dendrimer 會吸附帶負電的赤鐵礦材料,而當 pH 降低為 4 時,赤鐵礦表面帶正電,故因兩者都帶正電,所以不利於吸附。依目前 研究顯示,Dendrimer 可有效利用表面官能基來吸附重金屬銅,此外亦有 應用於吸附其他重金屬 (Ag、Au、Pt) 之研究 (Zhou et al., 2001; Mansfield., 1996;Torigoe et al., 2001),上述之研究都是運用吸附鍵結之 方法將金屬與高分子結合。. 除了將金屬離子吸附於 Dendrimer 內部外,另有進一步利用還原機 制,將吸附於高分子中之離子態金屬,進一步轉換成元素態顆粒的研究。 像是利用 Dendrimer G6 吸附 Fe3+,隨後在加入 NaEt3BH (溶於甲苯中) 促使在其中還原成奈米鐵顆粒 (Knecht and Crooks, 2007)。Balogh and Tomalia (1998) 也是利用相同概念,先將 Dendrimer 放入含有 Cu2+水溶 液中進行吸附程序,隨後便將其還原成零價銅顆粒存放於高分子孔隙 中,實驗結果發現,結合後於室溫、厭氧環境下可以穩定達 90 天之久。 藉此可以看出樹狀高分子穩定性極佳之優點,並有利於未來實場之長時. 19.
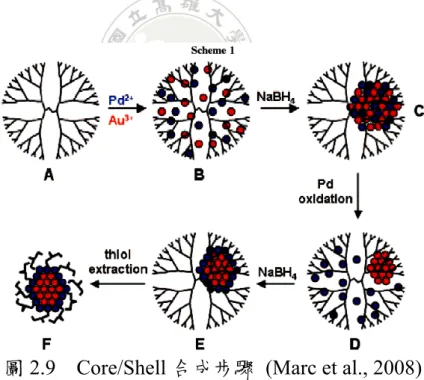
(29) 間應用。. 此外,亦利用 Core/Shell 之概念運用在高分子材料,如圖 2.9 所示, 將 Pd2+ 及 Au3+ 溶液中加入 Dendrimer,並使用 NaBH4 還原成奈米顆 粒,便可以在高分子內部形成 Pd/Au 的元素殼核狀態,最後再經萃取步 驟即可以得到表面包覆高分子的 Pd/Au 殼核型金屬 (Knecht et al., 2008)。其他還有很多試驗亦是利用相同原理將貴金屬 (Ag、Au、Pd、Pt) 還原成奈米顆粒儲存於 Dendrimer 之中,並進一步討論其粒徑分佈及表 面特徵研究 (Shi et al., 2007;Grohn et al., 2000;Korkosz et al., 2007; Richard et al., 2001)。. 圖 2.9 Core/Shell 合成步驟 (Marc et al., 2008) 由上述文獻回顧以可知樹狀高分子可有效吸附水中重金屬,故有學 者利用吸附完全之 Dendrimer 進行脫附試驗。Xu and Zhao (2005)利用螯 合劑 (EDTA) 與 Dendrimer G4.0-NH2 進行脫附比較測試,當 pH<4 會. 20.
(30) 造成表面官能基質子化 (protonated),使金屬離子脫附。將此高分子材料 進行銅離子吸附再試驗,結果發現吸附鍵結效果可以達到 51 % (未行 脫附前之鍵結效率 54 %),由此可以知道樹狀高分子材料具有回收再利 用之能力。Rether and Schuster 於 2003 年提出先將 Dendrimer 置於水樣 中,利用其類似螯合劑之功能固定金屬離子,隨後再將水樣通過超微過 濾膜 (ultrafiltration membrane) ,便可以有效將水中金屬離子隔離在過濾 膜上;此外,Diallo et al. (2005) 將 Dendrimer 與金屬離子水溶液混合吸 附後,先經過第一階段過濾,將吸附金屬離子之 Dendrimer 阻絕在薄膜 上,再利用酸性溶液進行金屬離子脫附 (圖 2.10),如此一來不但可有效 分離水中重金屬,更可以在脫附階段將 Dendrimer 回收重複使用。如果 能結合以上吸、脫附機制及高分子材料可以不斷重複回收利用之技術, 未來運用在處理水中貴重金屬回收,將會有相當大的經濟效益。. 圖 2.10 Dendrimer 回收再利用示意圖 (改繪 Diallo et al., 2005)。 除了重金屬可有效吸附回收之外,Baars et al. (1997) 利用 Dendrimer 21.
(31) G4 進行水中染料分離的試驗。先將 Dendrimer 溶於甲苯中,再利用極 性不同的原理,將甲苯與酸性染料充分混合。試驗發現,將 Dendrimer 置 入不同染料中,可以有效吸附水中酸性染料,並因為溶液極性不同,可 以有效將廢棄染料萃取至甲苯中,且實驗最後推算出來每莫耳的 Dendrimer 約可以吸附 20 莫耳染料;另外有學者 (Froehling., 2001),也 在 PP (Polyproylene, 聚 丙 烯 ) 管 製 作 過 程 中 加 入 含 有 烷 基 的 Dendrimer,並將 PP 管放入染料中,即可將染料有效固定於載體上,藉 此達染色效果。此外,另有高分子與其他材料合成之研究,像是將不同 濃度比例 Pt 和 Cu 溶液中置入 Dendrimer,經由吸附過程後再複合於奈 米顆粒載體上,觀察其合成效果及對 CO 吸附之成效評估 (Hoover et al., 2006)。這些不同於環工上之應用,也提供更多未來樹狀高分子運用的方 法。 Li and Bu 於 2004 年利用 PAMAM Dendrimer 在矽膠基材上增殖世 代之材料研發,實驗過程中利用 Michael addition 合成法,如圖 2.11 所示 : (A) 在帶有 NH2 的矽膠材料上加入丙烯酸甲脂 (Methyl acrylate, MA) 複 合半世代 (G0.5n)。(B) 將乙二胺 (Ethylendiamine, EDA) 加入半世代材 料中,即可得到一全世代樹狀高分子 (Gn)。只要重複以上步驟就可以在 基材上複合所需要的世代高分子。實驗過程中,可以利用 FT-IR 之官能 基鑑定,確認複合之高分子材料是否有成功。亦有學者利用聚乙醚基材 (PEI) 上面複合 CaCO3 薄膜,其中利用 poly (ethylenimine) 當作其中接 著材料,過程中利用高分子帶負電、基材及 CaCO3 帶正電之特性與電荷 相吸原理製成 CaCO3/polymer 複合薄膜 (Tanaka et al., 2000)。. 22.
(32) 圖 2.11 (A) 加入 MA 合成半世代;(B) 加入 EDA 合成全世代;(C) 合成 所需世代 (Gn) (Li and Bu, 2004) Dendrimer 除了於環境污染物去除之應用外,尚有於光學上的應用; 像是已有美國學者製作出苯基乙塊單體 (phenylacetylene monomers),其 合成方式是由一個核心開始,然後組成樹枝狀般的結構,目前最大的分 子組合共有 127 個載色體 (chromophores)。太陽光通過這個高分子材料, 會將核心內的感光分子 (photosensitive molecules) 變成電流,其效率達 99 % (蔡, 2005)。. 此外亦有使用於醫學上,Dendrimers 能在三十種不同的動物細胞上 達成 90 %的傳輸率。如果能夠找出生物體中蛋白質等物質的微量成 分,利用樹狀聚合物建立類似發光的機制,將可利用光行簡單、高感度 的偵測生物體內的微量成分,而不必使用化學方法來偵測;或是在一個 樹枝狀分子的枝條接上與病毒 DNA (RNA)互補的 DNA,使樹枝狀分子. 23.
(33) 可精準地附著在特定的對象上。然後藉著 X 光的照射,即可得知需要治 療的部位在何處。另一方面,在資訊系統上也可以於 Dendrimers 中心填 入大量的金屬原子而儲存大量二進位的資料。其他方面亦可以利用內部 大容量空孔部分,置入香味材料慢慢的釋放出來,且至少維持一天以上 (蔡, 2005)。. 從上述文獻回顧可以發現,目前高分子主要應用於兩大方向 : (1) 將 高分子材料複合於介質上,作為不同新穎材料之研發。(2) 去除水中重金 屬之研究,不過研究至今於回收及再利用兩大方向尚未有較佳解決辦 法。針對本研究中,其主要目的即為:(1) Dendrimer 可以有效進行重金 屬之吸、脫附,並可以有效回收再利用。(2) 可以將 Dendrimer 複合於其 他載體上。結合以上兩大優點,本試驗將試驗一有效回收之載體,於表 面複合上 Dendrimer,促使其有效進行回收再利用,並可以減少過濾回 收之龐大耗費,以達最大經濟效益。. 2.2.9 樹狀高分子去除機制 由於重金屬污染的去除,吸附作用仍是主要的方法之ㄧ,樹狀高分 子所具備之優點對重金屬的處理便顯現出極大優勢。Xu and Zhan, (2005) 研究顯示,水溶液之 pH 值、不同世代、不同末端官能基之奈米樹狀高分 子,對重金屬的吸附皆有影響,實驗發現,在相同質量條件下,低世代 的奈米樹狀高分子較高世代者吸附銅離子的效果為佳。不同末端官能基 (如-OH、-NH2、-COOH 等)對銅離子吸附的影響較不顯著。水中 pH 值被. 24.
(34) 認為是影響奈米樹狀高分子吸附效果最主要的因子,然而現階段研究結 果呈現不一致的紛歧看法。Xu and Zhan, (2005)指出,降低 pH 值有助於 提升銅離子之去除效率;然而,Diallo 等人於 2005 的研究則發現,奈米 樹狀高分子在鹼性條件下(pH 9),有最佳之銅離子吸附容量,在酸性條件 下 (pH 2~5),則完全無法吸附銅離子。此外,Diallo et al, (1999)早期之研 究則認為,奈米樹狀高分子在 pH 5.9~6.1 範圍間有最佳之銅離子吸附效 果。究其原因,可能與奈米樹狀高分子對重金屬的吸附,具有較複雜的 多重機制有關。相關吸附機制包括有:. (1)螯合作用 末端官能基之螯合作用是利用官能基與重金屬間形成之錯合結構 (complexation) ,達到吸附重金屬之目的,與傳統螯合劑如 EDTA 之功 能類似,其吸附量與末端官能基之間存在化學計量關係。其中,錯合簡 單來說就是以一個金屬原子或是陽離子為中心,利用其空價軌域及未共 用電子對之陰離子結合成複雜的帶電荷或中性原子團稱為錯合物,其中 如果要形成配位共價鍵,金屬則要具低能量的空價軌域 (鹼金族及鹼土 族便不適用於錯合反應),故由此可以得知,高價金屬會較低價金屬溶液 進行錯合反應。依據 Irving and Williams (1953),也經實驗得知,單獨二 價金屬其錯合穩定性也有強弱的排序 (Mn2+<Fe2+<Co2+<Ni2+<Cu2+> Zn2+)。趙介民 (2007) 亦提出金屬配位錯合方式又可以再細分為三種:(1) 分子內的氮原子,(2) 分子外的氮原子,(3) 分子內的氮原子和分子表面 的水分子。其詳細配位型態如圖 2.12 所示. 25.
(35) 圖 2.12 Cu2+與 Dendrimer 配位環境示意圖 (趙介民,2007)。 (2) 表面靜電引力之吸附 利用奈米樹狀高分子在水中 pH 高於等電位點 pHZPC 時,表面帶負電 荷之特性,達到吸附陽離子重金屬之目的。相同概念就如同於 Yuan and Lien. (2006)使用奈米鐵金屬 (Nanoscale Iron Particles)去除水中重金屬砷 之研究,結果由圖 2.13 所示,首先可由此圖得知奈米鐵之等電位點約為 4.4,當水體 pH 大於 4.4 時,顆粒表面帶正電;反之,則帶負電。尤其 砷金屬在水體中普遍以負電形式存在,故可以另由圖 2.14 得知,當 pH 較低時,去除效率明顯高於高 pH 值,其中去除之機制就是利用電荷相 吸之原理,達到去除重金屬之目的。 26.
(36) 圖 2.13 奈米鐵之界達電位分析圖 (Yuan and Lien, 2006). 圖 2.14 改變不同 pH 吸附水中砷之試驗 (Yuan and Lien, 2006). 27.
(37) (3) 內部空隙體積之空間捕捉效應 內部空隙體積之空間捕捉效應則是物理性作用,利用奈米樹狀高分 子存在之空隙體積,直接捕集將重金屬截留在裡面。如圖 2.15 所示, Knecht et al. (2008)將此高分子材料置入水體中,在短時間內,金屬溶液 會填滿其中,隨後加入還原劑將金屬進行還原程序,便可把金屬留在高 分子結構中。. 圖 2.15 高分子捕捉金屬示意圖 (Marc et al., 2008). 28.
(38) 2.3 磁性奈米顆粒 (Magnetic nano particle, MNP) 2.3.1 簡介 磁性奈米顆粒,顧名思義即是擁有磁性及兼具奈米性質材料。一般 物質的組成成分中當含有鐵、鈷、鎳這三種元素時,通常都會有磁性性 質的表現,而且這三個元素也是目前自然界中主要構成磁性物質的成分 之ㄧ,例如常見的磁性物質有鎳、鈷、鐵等 (鄭, 2006),若將這三個元 素與其他元素結合或取代,則可以形成各種不同特性的磁性材料。其中 氧化鐵 (iron oxide)是最常見的磁性材料,同時也是應用性最廣泛的磁性 物質。 氧化鐵的種類中主要是以四氧化三鐵 (Fe3O4)、三氧化二鐵 (Fe2O3) 為主,而三氧化二鐵是所有鐵的氧化物之最穩定型態,例如日常生活中 鐵鏽的成分其實就是氧化鐵。氧化鐵的磁性隨型態不同而有強弱之分, 其中四氧化三鐵是磁性最強的,三氧化二鐵次之,其原因與陽離子在晶 體結構中的排列有關 (鄭, 2006)。 當磁鐵轉化成奈米顆粒時,亦在環工運用上有相當助益。磁性奈米 顆粒已被研究多年,它不但體積小 (約可達 10 nm 以下)、高比表面積 (97 m2/g)、具磁性外,還具有兩種作用:(1)成核效應,是一種扮演核種的 角色,可以針對水中廢水有凝聚效果,加速凝聚成膠羽速率。(2) 加重效 應,磁鐵比重約為 4.9~5.2 g/cm2,當置入水中和懸浮固體物凝聚時,會 加速懸浮固體物的沈降 (陳和秦, 2004)。 磁性顆粒依照磁化率大小可以分為鐵磁性 (ferromagnetism)、順磁性. 29.
(39) (paramagnetism)、抗磁性 (diamagnetism)。其中鐵磁性物質磁化率遠大於 其他兩種,而順磁及抗磁性物質一般稱為非磁性物質 (張, 2005)。而本試 驗所製備的磁性奈米顆粒 (Fe3O4) 則屬於超順磁性物質,其磁化強度大 於一般順磁物質,且不會有殘磁現象,可以作為一個良好的磁性分離物 質。. 2.3.2 磁性奈米顆粒結構 Fe3O4 為一種 Spinel 結構,這個結構的命名是由於其原子排列的形 式與尖晶石礦 (MgO‧Al2O3) 相似所得到的,如圖 2.16,其中 M 代表金 屬原子,它可以是 Fe、Co、Ni、Mn 等金屬原子,而 O 則代表氧原子。 每單位 Fe3O4 中共有 56 個原子,其中 32 個是氧原子、另外 24 個是鐵 離子。其中 Fe 可為二價或三價,分別為 8 個 Fe2+及 16 個 Fe3+,為一個 穩定的 FCC (面心立方體) 結構 (劉和陳, 2000)。. 圖 2.16 四氧化三鐵之晶格結構 (劉和陳, 2000). 30.
(40) 2.3.3 磁性奈米顆粒製備 目前製作奈米顆粒方法眾多,不外乎就是分為物理、化學兩大方向, 其中物理方法又可以分為 : 機械粉碎法、金屬氣相合成法等;化學方法 可以分為共沈澱法、溶膠凝膠法、化學還原法等 (葉, 2008)。而就以磁性 奈米顆粒 (MNP)來說,最常使用是共沈澱法,是因為此製備方法操作簡 單、可大量製備、成本便宜和製備時間短等四個優點。 據文獻指出,化學沈澱法會因為藥劑使用量、操作條件不同而有不 同的粒徑大小。常見之磁性顆粒製備法常使用 Fe2+和 Fe3+ (比例為 1: 2) 水溶液,將此兩溶液混合均勻並加入鹼性溶液 (NaOH 或 NH4OH) 調 整至鹼性狀態 (pH=10),並於 80 ℃下攪拌形成黑色溶液狀態,最後經幾 次乙醇及去離子水沖洗,即可以得到奈米磁性膠液,其平均粒徑可以達 12 ± 2.0 nm、磁飽和率約為 83.3 units/g (Mehta et al., 1997)。其他化學共 沈澱配製方法及操作參數如表 2.6 所示:. 31.
(41) 表 2.5 化學共沈澱操作參數 1. 2. 3. 4.. 材料 FeCl3 FeSO4 NaOH SDS. 1. 2. 3. 4.. FeCl3 FeSO4 NaOH SDS. 1. FeCl3 2. FeSO4 3. NH4OH. 1. 2. 3. 4. 1.. 2. 1. 2. 3.. 操作條件 將 Fe :Fe3+ 以 2:1 比例混合攪 拌,並加入 NaOH 調整 pH 加/未加熱 加/未加 SDS 利用超純水清洗三次 將 Fe2+:Fe3+ 以 2:1 比例混合攪 拌,並加入 NaOH 調整至 pH 9.5 備用 加/未加 SDS 將 FeCl3、FeSO4 混合均勻,並加入 NH4OH 調整 pH=10 將溶液移至 80 ℃攪拌 30 min 用清水洗 2 次,經酒精洗一次至於 冷凍乾燥機 6 hr,即完成 pH= 9 環境下劇烈攪拌 製備完利用水清洗 5 次、乙醇 2 次 存放乙醇中備用. 粒徑分佈. 作者. 100 nm. 陳和秦, 2005. 60 nm. 陳和秦, 2005. 12.45 nm. 葉, 2008. 8.0±2 nm. Gan et al., 2005. 2+. 1. FeCl3 0.085 M 2. FeSO4 0.05 M 3. NH3OH 1.5 M. 1. 2. 3.. 1. 2. 3. 1. 2. 3. 4.. 1. 將材料混和並於室溫下滴定氨水 攪拌,即可得磁性顆粒. -. Saiyed et al., 2007. 1. 將 FeCl3、FeSO4、HCl 混合均勻, 加入 HCl 酸洗 2. 加入 0.5m NaOH 並於 80℃環境下 真空攪拌反應. 8.4±1.4 nm. Shi et al., 2007. <2 nm. Enzel et al., 1999. FeCl3 2 M FeSO4 1 M NH3OH 8 M FeCl3 2 M FeSO4 0.5 M HCl 0.4 M NaOH 0.5 M. 1. FeCl3 2. FeSO4 3. NH3. 1 將 Fe2+:Fe3+ 以 1:2 比例混合攪 拌,並加入 NH3 調整至 pH=10 備 用. 32.
(42) 2.3.4 磁性奈米顆粒應用 奈米磁鐵是屬於一超順磁材料,其磁化方向不固定在一個易磁化方 向,易磁化且無規律變化,國內已有學者使用磁性奈米顆粒進行試驗, 像是利用 MNP 吸附 CMP (Chemical mechanical polishing) 廢水之懸浮 顆粒,將 pH 固定約為 6 時,可以有效去除 95 %以上的懸浮固體物, 藉此降低水中濁度 (陳和秦, 2005)。另外,國內也有學者利用磁性奈米級 四氧化三鐵. (Magnetic nano- Fe3O4,MN- Fe3O4) 為吸附劑,針對酸性染. 料進行吸附特性探討,試驗初期針對 MNP 材料行界達電位測試,結果 發現等電位點約為 5.7,故當 pH 小於 5.7 時,表面帶負電荷,反之則帶 正電荷,故試驗過程使用 MN-Fe3O4 對兩種帶負電染料 (New coccine, NC and Indigo carmine, IC),並於酸性環境下進行吸附試驗,已達未來處 理酸性 CMP 廢水之可行性。結果發現當 pH=2 時,去除率可達 82 % 及 88 % (葉, 2008)。學者 (Saiyed et al., 2007) 曾利用 Fe3O4 來吸附血 液中的磷酸 (ALP),實驗結果可使 ALP 穩定覆著在磁鐵顆粒上。由此可 利用 MNP 在不同環境下之表面帶電荷特性,針對不同污染物進行吸附 整治。 國外針對 Dendrimer 研究已經行之多年,目前已可有效將磁性奈米 顆粒表面複合上本論文所探討的樹狀高分子,並進行物理性的分離 (Gruttner et al., 2005),但絕大部分領域偏向於生醫方面應用。像是有學者 首先利用共沉澱法製備出 (A) 磁性奈米顆粒 (MNP),並利用 (B) 矽烷 氨 (amini-silane) 在 MNP 表面形成鍵結,隨後加入 (C) 丙烯酸甲脂結 合形成半世代及 (D) 乙二胺形成外部核心,重複上述步驟可以在 MNP. 33.
(43) 表面有效合成出 Dendrimer Gn,(E) 最後將製備好帶有 Dendrimer 的磁 性顆粒進行 (F) 吸附鍵結試驗,最終亦可達到 95 %以上鍵結效率;此 外,在吸附達飽和後,可以藉由磁選分離原理,將吸附基材從溶液中有 效分離 (Pan et al., 2005),其流程如圖 2.17 所示:. 圖 2.17 MNP 合成 Dendrimer Gn 及吸附鍵結流程 (Pan et al., 2005) 此外,學者 (Pan et al., 2005)也是利用共沈澱法製備出 Fe3O4,在表 面加入前驅物 (ATPS)、乙二胺和丙烯酸甲酯合成出 Dendrimer 後,進行 血液蛋白 (bovine serum albumin, BSA) 鍵結吸附亦有極佳效果。其他文 獻中發現,利用奈米顆粒表面合成不同世代的 Dendrimer (G1~G6),並在 製備過程中加入 AEEA 作為 MNP 和 Dendrimer 之連接官能基,藉此確 保合成不會輕易分離,並於合成後進行 DNA 鍵結試驗,實驗結果發現 當世代越高,因表面官能基群越多,吸附鍵結效果越佳。此外,經由磁 選回收後可以重複再利用 (Yoza et al., 2003)。. 34.
(44) 除使用 AEEA 作為連接 MNP 及 Dendrimer 材料之外,另有利用丙 烯酸 (polyacrylic acid, PAA) 鍵結在磁性奈米顆粒上再藉此連接高分子 材料,製作出來之複合材料可以有效將酵素 (bromelain) 進行吸、脫附試 驗 (Chen and Huang, 2004);另一方面,(Mak et al., 2004)也利用相同 PAA 材料進行 MNP 之合成,將此材料置於含 methylene blue (MB) 污染水溶 液中可以有效吸附 MB (最大吸附量 0.199 mg/mg),並且實驗發現當溫 度及 pH 值提高,吸附效果亦有提昇之趨勢;另一方面,此種高分子材 料 (PAA) 複合 MNP 當吸附完 MB 後,只要加入乙酸 (4 Vol %) 即可 有 80 %脫附效果 (圖 2.18)。. 圖 2.18 加入乙酸脫附試驗 (Mak et al, 2004) Jiang et al. (2007) 在 SBA-15 多孔矽顆粒上首先複合出不同世代的 Gn-Dendrimer PAMAM-SBA-15,利用 EDTA 與其再次複合成 EDTA modified Gn-PAMAM-SBA-15 (圖 2.19)。實驗結果發現,使用單獨的高分 35.
(45) 子材料,或是再複合 EDTA 的複合材料,針對不同金屬 (Cu2+、Pd2+、 Zn2+等) 於短時間 (15 min)內皆有 70 %以上的去除效率,而且在吸附鍵 結後,將環境調整於酸性 (pH≦1.76) 下發現會有脫附之情況發生,其原 因是因為酸性環境下氫離子會和金屬離子行競爭吸附,氫離子較金屬離 子易鍵結於表面官能基上,故酸性條件下會不利於金屬離子吸附。. 圖 2.19 製備 Gn-Dendrimer PAMAM-SBA-15 及 EDTA modified Gn-PAMAM-SBA-15 流程圖 (Jiang et al., 2007) 除上述所提及之磁性奈米顆粒去除污染物之介紹外,在表 2.6 統整出 使用 MNP 及 MNP 複合其他高分子材料之去除率及飽合吸附量,更可以 證實 MNP 在環境工程上的高運用性。. 36.
(46) 表 2.6 磁性奈米顆粒於環境工程上之應用 作者 葉, 2008. Pan, 2005. 材料 Fe3O4. 污染物. 操作條件. 結果. 其他. 1. IC 5×10-5 M 2. NC×10-5 M 1. 吸脫附試驗可以為 5 次以上 1. NC 最大吸附量 1.11*10-4 mole/g new coccine 3. MNP 0.5 g 4. pH=2~5 indigo carmine 2. IC 最大吸附量 1.04*10-4 mole/g (溫度升高吸附量亦升高)2. 再生效率分別降低為 31 %與 40 % 5. Temp = 4~34 ℃. Dendrimer Bovine serum Gn /MNP albumin (BSA). 1. BSA 5 ml 2.50 mg Gn (n=0~5). 1. 最大吸附量約為 140 ug/mg. 2. 利用 FTIR 確認 Dendrimer 複合於 MNP particles. 1. 緩衝溶液(0.05 M pH=7.4) 1. 最大吸附量約為 140 ug/mg. Gao et Dendrimer 2. 利用 FTIR 確認 Dendrimer 複合於 MNP particles Streptavidin (SA) 2. SA 1ml (0.85 mg/mL) al., 2005 Gn /MNP 3. Gn/MNP 1ml (2.5 mg/mL) 3. 平均粒徑: 8.2 nm White, Plcys/Fe2O3 Heavy metal 2009. -. 1. Bromelain 6mg/L 2. pH=2~8 3. PAA/Fe3O4 5.18 g/ml. Chen, 2004. PAA/Fe3O4 Bromelain. Mak, 2004. 1. MB 2~4 mg/L Methylene blue 2. pH=2~10 PAA/Fe3O4 3. PAA/Fe3O4 22.4 mg/ml (MB) 4. 10~40 ℃. 1. 隨世代(Gn)升高,等電位點有降低趨勢。 2. 隨世代(Gn)升高,鍵結量有升高趨勢 1. PAMAM-MNP 不同世代,經由 UV 測試, 其特徵波長為 282 nm。. 1. Plcys/Fe2O3:除 Pb(II) 71 umol/g 以外,其他金屬最大吸 附量平均可達 340~680 umol/g 1. 脫附之金屬回收率平均達 50%以上 2. Fe2O3:除 Pb(II) 71 umol/g 以外,其他金屬最大吸附量平 均可達 164~522 umol/g 1. 最大吸附量 0.476 mg/mg. 1. 最大吸附量 0.199 mg/mg 2. PAA/Fe3O4 在兩分鐘可以完全吸附. 37. 1. PAA/Fe3O4 在一分鐘內可以完全脫附 2. Bromelain 經吸脫附後還有 87.4 %活性 1. 當溫度提昇,吸附量有增加趨勢 2. 吸附完 MB 後,只要加入乙酸 4 % Vol 即 可有 80 %脫附效果.
(47) 2.4 重金屬去除技術 除了上述所提及利用高分子材料去除重金屬技術外,目前尚有其他 新穎技術亦可以有效吸附重金屬。國內連等 (2004) 使用零價鐵金屬 (Zero Valent Iron, ZVI) 去除水溶液中 As,其主要是利用 ZVI 粒徑小 (100 nm)及高比表面積 (33.5 m2/g) 等優點,進行對重金屬之吸附。經實 驗發現 ZVI 等電位點約為 pH=4.4,在酸性條件下,便可以有效吸附水 中 As,且飽和吸附量約為 38.2 mg/g。陳等 (2003)利用自備之零價鐵金 屬進行去除水中重金屬之測試,結果發現吸附量為非奈米級鐵金屬之 30~60 倍。另外,使用零價鐵去除混合性污染物之研究中發現,ZVI 除了 可以有效還原降解含氯有機物 (四氯化碳) 外,亦可去除重金屬 (五價 砷、六價鉻、二價鉛與二價銅),故此奈米材料在未來去除污染物也具有 相當發展性。此外,由表 2.8 得知使用 ZVI 去除污染物各種機制,如果 機制為氧化還原作用,對於後續再利用應用將會相當有限。. 另外一方面,奈米碳管 (Carbon Nanotube, CNT) 此種新穎材料也有 去除重金屬之能力,如表 2.9 所示,無論是單獨使用 CNT、SWCNTs、 MWCNTs 或是改質後 (H2O2 、KMnO、HNO3) 之 CNT,皆可以在使用 少量材料下,達到有效去除重金屬之成效,而且目前已證實可去除多種 重金屬 (Pb2+、Cu2+、Cd2+、Zn2+ 等),並可經由再生步驟進行再利用程序, 不過最大缺點就是回收手續較為繁雜。. 38.
(48) 表 2.7 ZVI (Zero Valent Iron, ZVI)去除重金屬之機制 去除程序. 說明 還原反應. 氧化還原反應. 污染物 含氯有機物. 範例 四氯化碳、三氯乙烯、PCBs. 無機物. 硝酸根. 重金屬. Pb2+ + 2e- → Pb0 ↓ Cr6+ + 3e-→ Cr3+ As5+ + 2e- → As3+ (不顯著) As3+ + 3e- → As0 (未發現). (redox reaction) 氧化反應. 文獻 Johson et al.,1996 Lien and Zhang, 2001 Wang and Zhang, 1997 Farrell et al., 2001 Ponder et al., 2000 Ponder et al., 2000 Melitas et al., 2002 Melitas et al., 2002 Su and Puls, 2004. As 3+ ⎯oxidants ⎯⎯ ⎯→ As 5+ (oxidants = e.g., carbonate green rust, maghemite). 表面吸附. 透過如表面錯合 (surface complexation)等之 反應將重金屬立體鍵結於礦物或零價金屬 表面上。. 重金屬. 重金屬例如砷吸附於零價鐵金屬或其腐蝕氧化物表 面形成表面鍵結的砷。. Manning et al., 2002 Melitas et al., 2002 Su and Puls, 2004. 利用成核作用 (nucleation)將重金屬以重複 的分子單位在固相上生成。 於礦物形成過程中,將重金屬以次要組成份 結合於礦物。. 重金屬. Symplesite (Fe3(AsO4)2⋅8H2O) Realgar (As4S4). Lackovic et al., 2000. 重金屬. 砷與 Carbonate green rust (Fe4(II)Fe2(III)(OH)12CO3⋅xH2O)發生共沉澱。. Nikolaidis et al., 2003. (surface adsorption). 沉澱作用 (precipitation). 共沉澱作用 (co-precipitation). 39.
(49) 表 2.8 奈米碳管 (Carbon nano tubes, CNTs)去除重金屬 去除重金屬. 材料 (g/mL). 改質劑. 操作參數 pH C0 ( mg/L). Pb2+ Cu2+ Cd2+. CNTs (0.05/100). Cd2+. CNTs (0.05/100). H2O2、KMnO HNO3. 5.5. -. CNTs (0.02/100). HNO3. 5. CNTs (0.05/100). HNO3. CNTs (0.05/100) MWCNTs (0.05/100). Pb2+. Ni2+ Zn2+ Cu2+. SWCNTs (0.05/100). 未改質. 5. 10~60 5~30 2~15. MWCNTs (0.05/100) MWCNTs (0.05/100). 單獨金屬離子吸附 Pb2+ (97.08), Cu2+ (28.49), Cd2+ (10.86). 作者. Li, Y. H., et al., 2003. 競爭金屬離子吸附 Pb2+ (34.01), Cu2+ (17.04), Cd2+ (3.3) 未改質 : 1.10、H2O2 : 2.6 KMnO : 11.00、HNO3 : 5.1. Li, Y. H., et al., 2003. 10~60. 14.8~82.6. Li, Y. H., et al., 2006. 7. 2~14. 未改質 : 1、改質後 : 49.95. Li, Y. H., et al., 2002. HNO3. 5. 10~80. 35.6. Li, Y. H., et al., 2005. HNO3. 5. 2~15. 97.08. Li, Y. H., et al., 2003. NaOCl. 7. -. 未改質 : 9.22、改質後 : 47.85. Lu, C. and Liu, Y. 2006. 未改質 : 7.532、改質後 : 38.46. MWCNTs (0.05/100) SWCNTs (0.05/100). 飽和吸附量 (mg/g). NaOCl. 7. 10~80. HNO3. 5. 5~30. 40. 未改質 : 11.23、改質後 : 43.66 未改質 : 10.21、改質後 : 32.68 24.49. Lu, C. and Chiu, H. 2006 Li, Y. H., et al., 2003.
(50) 2.5 吸附理論 吸附機制是一般常見之結合、分離程序,其廣泛運用於環境工程理 論之使用。其中主要可以分為物理吸附、化學吸附、交換吸附,以下將 分別進行介紹。. 2.5.1 吸附之種類 (1) 物 理 吸 附 :主要原理為吸附劑表面與吸附質之間的凡得瓦爾力 (Vander Waals force) 作用所造成的吸附現象,也可以解釋為帶有相反電 荷的離子,利用靜電力被吸引於固相表面固定。其中因為兩者間吸引力 較小,具有很高的吸附速率且很快可達吸附平衡。此吸附機制另有一項 特性,即其吸附具有可逆性,當引力變小時就容易發生脫附反應。一般 而言,物理吸附機制屬於多層吸附,當溫度降低時,有利於物理吸附機 制進行。. (2) 化學吸附:主要原理為吸附質與固體表面因吸引力作用,所產生分子 軌域的重疊,進而形成化學鍵結 (Chemical bounds) ,其作用力遠大於物 理吸附之凡得瓦爾力,其是屬於一種強的吸引力,並具有反應速率慢, 且隨溫度增加,反應亦有速率有提升之情形。此外,進行脫附反應時, 吸附質的化學性質常會改變,吸附質不易脫附,反應較不具可逆性,屬 於單層吸附。 以上兩種吸附機制可以透過活化能來進行判定,當吸附熱小 (≦ 10 Kcal/mole),則屬於物理吸附,反之,當吸附熱較大時 (≧ 10 Kcal/mole),. 41.
(51) 則屬於化學吸附。兩者相互比較如表 2.9 所示: 表 2.9 物理、化學吸附之比較. 吸附力 吸附熱 選擇性 吸附速度 吸附層 定溫吸附量 可逆性. 物理吸附. 化學吸附. 凡得瓦爾力 10 Kcal/mole 以下 無(在低溫下均可) 很快(無法測定) 多分子層吸附 溫度增加而減低 容易脫附. 與原子價力相同 10~100 Kcal/mole 有選擇性 通常不太快 單分子層吸附 溫度增加而增加 不易脫附. (3) 交換性吸附:通常指的是吸附質和吸附劑表面相互具有帶電吸引力所 形成之吸附作用,像是離子交換就是屬於此類型,因此物質若具有較高 之價數及較小尺寸時,其靜電引力較大,吸附利益相對較強 (葉, 2008)。. 2.5.2 等溫吸附模式 等溫吸附方程式 (adsorption isotherm) 是指吸附反應中,吸附後之平 衡濃度和被吸附劑質量間的吸附關係,其中等溫 (isotherm) 意指反應中 是在相同溫度下所進行。四種常見的等溫吸附方程式為線性 Linear、 Langmuir、Freundlich 及 BET 方程式,至於何者較適用則需視狀況而 定,像是物質的特性、濃度、被吸附質的特性、吸附劑的種類、流體的 種類及環境因素等,皆會影響線性結果。. 等溫吸附平衡關係為一定量描述等溫吸附之行為,表示流體相與吸 附相固體粒子間所能達成之平衡關係。以吸附相的吸附量 (qe) 對水相中 的平衡濃度 (Ce) 作圖而得。本研究利用 Langmuir 方程式與 Freundlich. 42.
數據



+7
相關文件
Department of Electrical Engineering, National Cheng Kung University In this thesis, an embedded system based on SPCE061A for interactive spoken dialogue learning system (ISDLS)
Department of Mathematics National Cheng Kung
Department of Mathematics National Cheng Kung
Department of Mathematics National Cheng Kung
Department of Mathematics National Cheng Kung
Department of Mathematics National Cheng Kung
Department of Mathematics National Cheng Kung
Department of Mathematics National Cheng Kung