32
ndIChO • Theoretical Tasks
Student Code:
第三十二屆國際化學奧林匹亞競賽
理論測驗
Name
Student Code
32
ndIChO • 問題 1
10 分
具治療傷口藥效化合物的合成(Synthesis of Compounds with
Wound Healing Properties)
紫草寧(Shikonin)是一種紅色的有機化合物, 可從一種生長在亞洲的植物 Lithospermum erythrorhizon 的根部提煉而得到。此種草藥的應 用已有數世紀的歷史。而現今,此化合物依然被 應用在療傷的軟膏上。 OH O O OH OH Shikonin 紫草寧 1-1 紫草寧(Shikonin)共有幾個立體異構物(stereoisomers)呢? 2 1 分 1-2 是否所有紫草寧(Shikonin)的立體異構物(stereoisomers), 均具有相同的熔點(melting point)呢 ? yes no 在恰當的選項下空格中,打 X x 1 分
32
ndIChO • Problem 1 Student
Code
以下為紫草寧 Shikonin 合成途徑的一部份: OCH3 O O O CH3 O OCH3 O O O CH3 Reagent A Catalyst B Reagent C OH OCH3 O O O CH3 1-3 畫出試藥 A 的結構式(structural formula): 2 分 1-4 在適當的選項格打 X ,標示出試藥 A 的 IUPAC 學名 2-甲基-2-戊烯酉先氯 (2-Methyl-2-pentenoyl chloride) 1-氯-4-甲基-3-戊烯(1-Chloro-4-methyl-3-pentene) 4-甲基-3-戊烯酉先氯(4-Methyl-3-pentenoyl chloride) X 4-甲基-3-戊烯-1-醇(4-Methyl-3-pentene-1-ol) 4,4-二甲基-3-丁烯酉先氯(4,4-Dimethyl-3-butenoyl chloride)1-5 寫出試藥 C 的分子式(molecular formula): NaBH4或 LiAlH4
由於藥效佳,許多紫草寧衍生物( Shikonin analogues)相繼被合成,以檢驗其療 效能否有所提升。以下是其中一種衍生化途徑: Shikonin D E SOCl2 C16H15ClO4 C16H14O4 KOH in ethanol ethanol:乙醇 試藥 A 觸媒 B 試藥 C 70℃
Cl
O
32
ndIChO • Problem 1 Student
Code
1-6 畫出化合物 E 的結構式 (structural formula): 2 分 1-7 化合物 E,可能有幾個立體異構物(stereoisomers)呢? 2 1 分 以下是另一種紫草寧衍生物( Shikonin analogues)的衍生化途徑: OCH3 OCH3 O CH3O CH3O CH3 C21H29BrO5 1. Mg in diethyl ether 2. CO2 3. Aqueous HCl G C22H30O7 F HBr diethyl ether:乙醚;aqueous HCl:鹽酸 1-8 畫出化合物 F 的結構式 (structural formula): 2 分 1-9 畫出化合物 G 的結構式 (structural formula): 3 分 極性溶劑O
O HOH
O
C H3O OCH 3O
B r CH 3 C H3O OCH 3 C H3O OCH 3 O CH 3 C H3O OCH 3 COO HName
Student Code
32
ndIChO • 問題 2
10 分
丹麥與瑞典之間的橋樑
西元 2000 年 7 月 1 日,連接丹麥與瑞典的橋樑與隧道正式啟用。它包括了一條從哥本哈根到一個 人工島的隧道,和由此人工島到瑞典馬模市的橋樑。建築時所使用的最主要材料為混凝土和鋼鐵。 本題目與建築材料的生產與損壞時所牽涉到的化學反應有關。 混凝土主要由水泥,沙和小石頭組成。水泥主要的組成包含矽酸鈣和鋁酸鈣,是用 磨細的泥土和石灰石加熱而製成的。在製造水泥的步驟中,會加入少量的石膏 (CaSO4·2H2O),主要是用來增進混凝土的凝固。而最後的步驟中,因溫度升 高,會生成不需要的產物 CaSO4·½H2O。其反應式如下:CaSO4·2H2O(s) CaSO4·½H2O(s) + 1½H2O(g)
以下是在 25 C 時的熱力學數據,標準壓力:1.00 bar
化合物 H /(kJ mol–1) S /(J K–1 mol–1)
CaSO4·2H2O(s) –2021.0 194.0
CaSO4·½H2O(s) –1575.0 130.5
H2O(g) –241.8 188.6
氣體常數 Gas constant: R = 8.314 J mol–1
K–1 = 0.08314 L bar mol–1 K–1; 0 C = 273.15K
32
ndIChO • Problem 2 Student
Code
2-1 計 算 由 1.00 kg 的 CaSO4·2H2O(s) , 完 全 變 成 為 CaSO4·½H2O(s) 時 的
H(kJ)。試問此反應為吸熱還是放熱反應。
H
= - 1575.0 kJ mol-1 + 3/2 ( -241.8) kJmol-1 – ( -2021.0) kJmol-1 = 83.3 kJmol-1 n = m/M = 1000g / 172.18 g mol-1 = 5.808 mol nH = 484kJ x 以 x 號表示你的正確答案:吸熱反應 放熱反應 2 分
2-2 25 C 時,某密閉容器裝有 CaSO4·2H2O(s) , CaSO4·½H2O(s) 和 H2O(g),試計
算容器內水蒸氣的平衡壓力(bar)。 S
= 130.5 JK-1mol-1 + 3/2 × 188.6 5 JK-1mol-1 – 194.05JK-1mol-1 = 219.4 JK-1mol-1 G0 = H0 – t S0 =17886 Jmol-1 G0 = - RTlnK K = ﹝P(H2O)﹞3/2 = 7.35 × 10‐4 (bar) P(H2O) = 8.15 × 10‐3 bar 2 分 2 分 x
32
ndIChO • Problem 2 Student
Code
2-3 承上題(2-2),請計算當水蒸氣的平衡壓力為 1.00bar 時的溫度應為多少。 假設H 與S 不隨溫度而變化。 P(H2O) = 1.00 bar , 則 K= 1.00 及 G0 = -RTlnK = 0 G0 = H0 - TS0 0 = 83300 JK-1 – T × 219.4JK‐1mol‐1 T = 380 K 或 1070C 2 分 金屬的腐蝕牽涉到電化學反應,鐵的表面生鏽情形,其最初的電極反應式如下: (1) Fe(s) Fe2+(aq) + 2e–(2) O2(g) + 2H2O(l) + 4e– 4OH–(aq)
25 ºC 時,建立一個電化學電池以顯示上述的電極反應,此電池可表示為:
Fe(s) Fe2+(aq) OH–(aq), O2(g) Pt(s)
25 ºC 時,標準電極電位為:
Fe2+(aq) + 2e– Fe(s) E = – 0.44 V
O2(g) + 2H2O(l) + 4e
– 4OH–
(aq) E = 0.40 V
能士特因子(Nernst factor):R T ln10 / F = 0.05916 volt (at 25 ºC) 法拉第常數(Faraday constant): F = 96485 C mol–1
2-4 計算 25 ºC 時的標準電動勢(標準電池電壓), E 。 1 分 E0(電池) = E0 (右半電池) – E0 (左半電池) = 0.40 V – (-0.44V) = 0.84 V
32
ndIChO • Problem 2 Student
Code
2-5 寫出標準狀態時電池放電的總反應式。 氧化在負極發生 , (即左半電池) 左半電池: 2Fe → 2Fe 2+ + 4e- (乘以 2) 右半電池: O2 + 2H2O + 4e- → 4 OH- 全電池: 2Fe + O2 + 2 H2O → 2 Fe + 4OH - 1 分 2-6 計算 25 °C 時,總電池反應的平衡常數。 K = ﹝Fe+2﹞2 ﹝OH-﹞-4 / p(O2) (濃度單位為 M,壓力為 bar) G0 = - n FE0 = - RT lnK K = 6.2 × 1056 (M6bar-1) 2 分 2-7 標準狀態時,上述的總反應在電流為 0.12 A 的情況下進行 24 小時。假設氧氣 與水過量,計算 24 小時中,鐵(Fe)變成鐵離子(Fe2+ )的重量。 Q = It = 0.12A ×24 × 60 × 60s = 10368 Cn (e‐) = Q / F = 10368C / ( 96485 C mol‐1) = 0.1075 mol
m(Fe) = n (Fe) M(Fe) = (1/2) ×0.1075 mol × 55.85 gmol‐1
32
ndIChO • Problem 2 Student
Code
2-8 由下述條件,計算 25 °C 時的電池電位(E)。
[Fe2+] = 0.015 M, pH右邊半電池 = 9.00, p(O2) = 0.700 bar.
E(電池) = EO(電池) – 0.0596v log ﹝Fe+2﹞2﹝OH-﹞4 n p(O2) 濃度為 M , 壓力為 bar pH = 9.00 即 ﹝H+﹞ = 10 –9 M 及 ﹝OH-﹞ = 10-5 M so E = 0.084 v – 0.05916v log 0.0152(10-5)4 = 1.19 V 4 0.700 2 分
Name: Student
Code:
32
ndIChO • 問題 3
9 分 s
無機生物化學(Bioinorganic Chemistry)
平面四邊形錯合物,順-二氨二氯鉑(II)(cis-diamminedichloroplatinum(II))是一 種可治療癌症的重要藥物。 3-1 畫出順-和反-二氨二氯鉑(II)的結構,並標出何者為順式,何者為反式。 1 分 有好幾種離子化合物,其實驗式(簡式)與 Pt(NH3)2Cl2相同 3-2 請寫出所有可能離子化合物的正確分子式。這些化合物應符合: 1) 實驗 式(empirical formula )均為 Pt(NH3)2Cl2, 2) 陰陽離子均由單一平面四邊 形鉑(II)錯離子所構成, 3) 均只含一種陽離子和一種陰離子。正確的分子 式必須清楚地顯示每一個化合物中的鉑(II)錯離子組成。 4 分 NH3 Cl Pt Cl NH3 反 Cl NH3 Pt Cl NH3 順 ﹝Pt (NH3)4﹞﹝PCCl4﹞ ﹝Pt (NH3)3Cl﹞﹝Pt(NH3)Cl3﹞ ﹝Pt (NH3)3Cl﹞2﹝Pt Cl 4﹞ ﹝Pt(NH3)4﹞﹝Pt(NH3)Cl3﹞232
ndIChO • Problem 3
Student Code
3-3 試問鉑(II)離子中的 5d 軌域共有幾個電子? 1 分 平面四邊形的價 d-軌域分裂情形,可視為將八面體在 z 軸上的兩個配基取消, 而剩餘的四個配基在 x 和 y 軸上的鍵結變強。 3-4 一般的平面四邊形鉑(II)錯合物,其五個 5d 軌域中的哪一個軌域有最高的 能量(也就是最不可能填入電子的軌域)? 2 分 傳遞鐵蛋白(Serum transferrin ,簡稱 Tf) 是一種單蛋白質,在人體中的主要 功能為運送鐵(III),每一個 Tf 分子可結合兩個鐵(III)離子,結合時,兩個步驟 的平衡常數 K1 及 K2在 25 °C 下為: FeIII + Tf III)Tf K 1 = 4.7 1020M1FeIII + (FeIII)Tf III)
2Tf K2 = 2.4 1019M1
在雙鐵的蛋白 (FeIII)
2Tf 中,兩個鐵結合於相似,但非完全相同的位置上,而兩
種可能的單鐵蛋白(FeIII)Tf 則表示為:{FeIII.Tf} 與 {Tf.FeIII}。在平衡時的相對
量為: K = [{Tf.FeIII}][{FeIII.Tf}]1 = 5.9.
8
5d x2- y2, 在一四方平面錯合物 , 四配子的原子 , 在 x 及 y 軸上 , 若填滿電
32
ndIChO • Problem 3
Student Code
3-5 請計算 K1與 K1的值。K1= [{FeIII.Tf}][FeIII]1[Tf]1,K 1=
[{Tf.FeIII}][FeIII]1[Tf]1。K
1與 K1分別為兩種單鐵蛋白的常數。
單鐵蛋白濃度:﹝(FeIII)Tf﹞ = ﹝(FeIII. Tf)﹞+ ﹝(Tf . FeIII)﹞ K1’+ K1’’ = K1 , K1’K = K1’’ K1’ = K1 = 4.7 ×1020 M-1 = 6.8 ×10 19 M –1 1+k 1.59 K1’’ = K1 – K1’ = (4.7 – 0.68 ) × 10 20 M-1 = 4.0 × 1020 M-1 4 分 3-6 請計算 K2與 K2的值。K2= [(FeIII)
2Tf][FeIII]1[{FeIII.Tf}]1, K2=
[(FeIII)
2Tf][FeIII]1[{Tf.FeIII}]1。K2與 K2分別為由兩種不同單鐵蛋白形成
雙鐵蛋白時的常數。 K1’K2’ = K1’’K2’’ = K1K2 K2’ = K1K2 = 4.7 × 1020 M-1 × 2.4 × 1019 M-1 K1’ 6.8×1019M = 1.7 × 10 20 M-1 K1’’K2’’ = K1K2 So K2’’ = K1K2 = 4.7 × 1020 M-1 × 2.4 × 1019 M-1 K1’’ 4.0 × 1020 M-1 = 2.8 × 1019 M-1 4 分
32
ndIChO • Problem 3
Student Code
每一個結合的鐵(III)離子被不同配基的六個配位原子所包圍。除了碳酸根離子 的兩個氧原子配位於金屬外,組成蛋白質的下列胺基酸側鍵上的一個有配位潛 力原子也配位上去:一個天冬胺酸(aspartate)、一個組胺酸(histidine)和兩 個酪胺酸(tyrosine)。 3-7 請問,傳遞鐵蛋白(Tf)中,配位於鐵上的六個原子共有幾個氧。5 ( = 2(CO32-) + 1 (Asp (O-))+2(2×Tyr(O-))
Name: Student Code:
32
ndIChO •問題 4
10 分
天然物(A naturally occurring compound)
天然物 A,含有碳, 氫, 氧三種元素,其元素組成的質量百分比如下: C: 63.2 %, H: 5.3%, O: 31.5%. 4-1 推導出化合物 A 的實驗式(empirical formula): C8H8O3 1 分 圖 1 :天然物 A 的質譜圖(mass spectrum)
Name: Student Code:
32
ndIChO •問題 4
10 分
4-2 寫出化合物 A 的分子式(molecular formula) C8H8O3 1 分 若用氫氧化鈉水溶液,萃取天然物 A 乙醚溶液,則天然物 A 自乙醚中除去。若用 碳酸氫鈉(NaHCO3)水溶液進行萃取,則天然物 A 依然留在乙醚之中。 4-3 基於上述實驗觀察,天然物 A 屬於哪類化合物呢?在正確的空格中,打 X。醇 alcohol 酚 phenol 醛 aldehyde 酮 ketone 酸 acid 酯 ester 醚 ether
1 分
天然物 A 與多倫試劑【Tollens’ reagent,(Ag(NH3)2+)】作用,會引起銀鏡反應
(silver mirror)。
4-4 基於上述實驗觀察,天然物 A 具有哪一類的官能基?在正確的空格中,打
X。
hydroxy group of an alcohol hydroxy group of a phenol
醇類的羊巠基 酚類的羊巠基
carbonyl group of an aldehyde carbonyl group of a ketone
醛類的羊炭基 酮類的羊炭基
carboxylic group ester group
基 酯基
alkoxy group of an ether 醚類的烷氧基
1 分 X
Name: Student Code:
32
ndIChO •問題 4
10 分
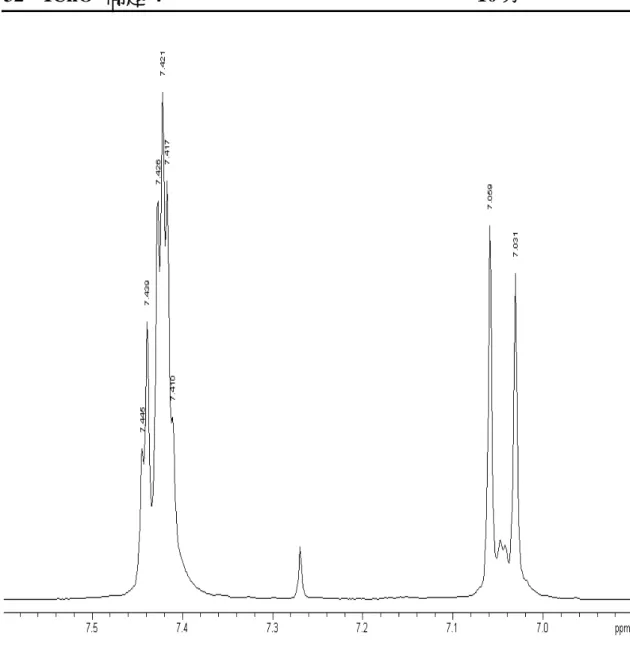
積分值 圖 2a 圖 2a 為化合物 A 的 300 MHz 1 H 核磁共振圖譜【溶劑為 CDCl3 (7.27 ppm),以四甲 基矽(tetramethylsilane)為標準物】。在化學位移 3.9, 6.3 和 9.8 ppm 的共振訊號為 單重峰(singlet)。圖 2b 為 6.9 –7.6 ppm 區域的放大圖。 有關偶合常數與化學位移數值,請參考附表(1)。Name: Student Code:
32
ndIChO •問題 4
10 分
圖 2b 6.9 –7.6 ppm 區域的放大圖
若加入一滴 D2O 之後,在 6.3 ppm 處的訊號消失
4-5 此觀察說明了下列何種現象?在恰當的選項方格中打 X
碳氫鍵上的氫原子交換 (Exchange of carbon-bonded hydrogen)
氫氧鍵上的氫原子交換 (Exchange of oxygen-bonded hydrogen) 稀釋效應 (Dilution effect)
Name: Student Code:
32
ndIChO •問題 4
10 分
水解 (Hydrolysis) 1 分 若將此樣品以 CDCl3稀釋,上題中的訊號將移向較低 ppm 處。 4-6 (多選題)基於上述觀察結果,下列哪一些敘述為正確?在恰當的選項方格 中打 X。氫鍵增強 (Increased hydrogen bonding) 氫鍵減弱 (Decrease in hydrogen bonding) 分子間氫鍵 (Intermolecular hydrogen bonding) 分子內氫鍵 (Intramolecular hydrogen bonding)
沒有氫鍵 (No hydrogen bonding)
4-7 基於上述觀察,畫出化合物 A 四種最有可能的結構式。 1 分 4-8 寫出質譜中 137 和 123 質量單位的譜峰,其相對應丟掉的斷裂碎片 (fragments)的結構式。 1 分 CH3 HC = O X X
CH
3 OHO
O
CH
3OH
O
O
CH
3 OHO
O
OHO
O
H3CName: Student Code:
32
ndIChO •問題 4
10 分
4-9 其中兩種異構物具較低的 pKa 值。寫出這兩種異構物的結構式。 1 分CH
3
OH
O
O
CH
3
OH
O
O
Name: Student Code:
32
ndIChO •問題 4
10 分
附表 1
1
H 化學位移
(
1H Chemical Shift
)
連接碳上的氫原子(Hydrogens attached to carbon)
甲基(Methyl) CH3–C– CH3–C=O– CH3–O–R CH3–OCOR 0.9 – 1.6 ppm 2.0 – 2.4 ppm 3.3 – 3.8 ppm 3.7 – 4.0 ppm 亞甲基(Methylene) CH2–C– CH2–C=O– CH2–OR CH2–OCOR 1.4 – 2.7 ppm 2.2 – 2.9 ppm 3.4 – 4.1 ppm 4.3 – 4.4 ppm 次甲基(Methine) CH– 1.5 – 5.0 ppm 視不同取代基而定。一般而 言,其化學位移較甲基或亞甲 基為高 烯火巠類(Alkene) 4.0 - 7.3 ppm 視不同取代基而定。 醛(Aldehyde) R-CHO 9.0 - 10.0 ppm
連接氧上的氫原子(Hydrogens attached to oxygen)
醇(Alcohols) ROH 0.5 -5.0 ppm
酚(Phenols) ArOH 4.0 - 7.0 ppm
酸(Carboxylic acids)
RCOOH 10.0 - 13.0 ppm
自旋偶合常數(Selected spin-spin coupling constants)
烷(Alkanes)(自由轉動) H-C-C-H 相鄰 6 - 8 Hz 烯(Alkenes) 順(trans) 反(cis) 偕(geminal) 11 - 18 Hz 6 - 12 Hz 0 - 3 Hz 芳香環(Aromates) 鄰(ortho) 間(meta) 對(para) 6 - 10 Hz 1 – 4 Hz 0 – 2 Hz
Name: Student
Code:
32
ndIChO • 問題 5
10 分
蛋白質與去氧核糖核酸(Protein and DNA)
去氧核糖核酸(DNA)的結構包含:2’-去氧-核糖甘(2’-deoxy-nucleotides)和腺 口票呤(adenine (A)), 鳥糞口票呤(guanine (G)), 胞嘧啶(cytosine (C))和胸腺嘧啶 (thymine (T))。相對應的 2’-去氧-核甘酸-5’-三磷酸酯(2’-deoxy-nucleotide-5’-triphosphates)的莫耳質量列於表2中。
表 2
dNTP 莫耳質量
Molar mass /g mol–1
dATP (腺口票呤 2’-去氧-核甘酸-5’-三磷酸酯 ) 487 dGTP (鳥糞口票呤 2’-去氧-核甘酸-5’-三磷酸酯) 503 dCTP (胞嘧啶 2’-去氧-核甘酸-5’-三磷酸酯) 464 dTTP (胸腺嘧啶 2’-去氧-核甘酸-5’-三磷酸酯) 478 5-1 計算雙股 DNA 的莫耳質量,該雙股 DNA 包含 1000 組鹼基對,其中4種不 同鹼基為等量分配。 dNTP 平均質量 = 483 g mol-1 M(H P2O72-) = 175 g mol-1 1000 組鹼基對雙股 DNA M(DNA) = (483-175) ×2×1000+2×175=616350 g mol-1 2 分
32
ndIChO • Problem 5
Student Code
利用PCR 法(聚合酉每鏈鎖反應),可將經純化後的 DNA 複製。若使用具熱穩定性 的聚合酉每酵素,在一定時間內,可使DNA 數量增加數倍。在最佳狀況之下,經每 一週期時間,雙股DNA 數量便增加一倍。 使用PCR 法,將一個前述雙股 DNA 分子複製 30 週次。 5-2 計算此實驗中所得到的 DNA 質量。 210 = 1073741824 (分子)DNA 總質量:m(DNA) = 1073741824 / Na ×616350 gmol-1 = 1.1 ng
2 分
利用細菌-病毒 T4 酵素-polynucleotide kinase (PNK),可使 ATP (-orthophosphate) 上末端磷酸酯基轉移到RNA 或 DNA 的末端 5’-羊巠基上。 當 ATP 上-P(最外圍的磷原子)被換成 32P,利用 PNK 酉每,便可以將這具有放射 性的32P 同位素轉移到 DNA 末端的5’位置上,致使 DNA 被加以標記。由此,32P 與 被標記的 DNA 的含量,可以透過測量而得知。 抽取經[-32 P]ATP和 PNK 處理的 100%標記雙股 DNA 溶液 10 µL。已知 37 天前所用 的[-32
P]ATP 的放射比活(specific activity)為 10 Ci/mmol 或 370 x109
Bq/mmol。32 P 的 半衰期(half-life)為 14.2 天,在衰變過程中,放射出-粒子。而現今抽出經標記 的 DNA 放射速度為 40000 -粒子/秒。 H H OCH2 OH OH H H O N N N N NH2 P O P O P O O O O O O O + H H HOCH2 O H H H O Base H H OCH2 OH OH H H O N N N N NH2 P O P O O O O O + H H OCH2 O H H H O Base P HO O O ATP DNA ADP 5'-P-DNA H H OCH2 OH OH H H O N N N N NH2 P O P O P O O O O O O O + H H HOCH2 O H H H O Base H H OCH2 OH OH H H O N N N N NH2 P O P O O O O + H H OCH2 O H H H O Base P HO O O ATP DNA ADP 5'-P-DNA -- - -- - -H H OCH2 OH OH H H O N N N N NH2 P O P O P O O O O O O O + H H HOCH2 O H H H H H OCH2 OH OH H H O N N N N NH2 P O P O P O O O O O O O + H H HOCH2 O H H H O Base H H OCH2 OH OH H H O N N N N NH2 P O P O O O O O + H H OCH2 O H H H O B O Base H H OCH2 OH OH H H O N N N N NH2 P O P O O O O O + H H OCH2 O H H H O Base P HO O O ATP DNA ADP 5'-P-DNA H H OCH2 OH OH H H O N N N N NH2 P O P O P O O O O O O O + H H HOCH2 O H H H O Base H H OCH2 OH OH H H O N N N N NH2 P O P O O O O + H H OCH2 O H H H O Base P HO O O ATP DNA ADP 5'-P-DNA -- - -- -
-32
ndIChO • Problem 5
Student Code
5-3 計算 DNA 溶液的濃度。 A= A0e
-kt 及 k = ln2 代入→ T1/2 A0 = 40000 dps = 243464 dps e-0.0488×37 其相對應於 243464 pmol 5’ – 32P – DNA = 658 pm 370 由於標定 DNA 之體積為 10μL 5’ – 32P – DNA 所以 DNA 之濃度約為 66μM 2 分將單股DNA,[-32P]ATP 與 PNK 混合培養,並從中取樣,測量被標記 DNA 的 -粒子的放射量,以觀察反應的進行。 對1 mL 實驗混合溶液進行追蹤,計算出標記反應以 9 nmol DNA/min 進行。若 PNK 的催化速度常數(又稱轉換數,turnover number)為 0.05 s–1,而莫耳質量為 34620 g mol–1(克/莫耳)。 5-4 計算實驗中 PNK 的濃度。單位為 mg/mL。 因 9 nmol 標記 DNA 之催化轉換數為 0.05 S-1 則 催化標記的 PNK 量為:
9 nmol / min = 3 nmol 其 等於 0.05 s-1 ‧60s/min
3 nmol × 34620 gmol-1 = 0.1 mg so PNK 之濃度 為 0.1 mg / mL
32
ndIChO • Problem 5
Student Code
芳香胺基酸,包括色胺酸(tryptophan),酪胺酸(tyrosine)和苯胺基丙酸 (phenylalanine)會吸收波長為 240 nm - 300 nm 的紫外光。 若 蛋 白 質 中 含 有 多 個 芳 香 胺 基 酸 , 則 該 蛋 白 質 的 莫 耳 吸 收 係 數 (molar absorptivity),
蛋白質, 將近似於每個芳香胺基酸莫耳吸收係數的總和(
胺基酸)。 酪胺酸(tyrosine),色胺酸(tryptophan)和苯胺基丙酸(phenylalanine)在波長 為 280 nm 處的莫耳吸收係數,
胺基酸(molar absorptivity)分別為:1400 M–1 cm–1, 5600 M–1 cm–1 和 5 M–1 cm–1。將濃度為 10 µM 的 PNK 溶液置於 1.00 cm 長的石英槽 中進行測量,在波長為280 nm 處,吸收率(absorbance)為 0.644。已知 PNK 的胺 基酸序列中包含14 個酪胺酸(tyrosine)和 9 個苯胺基丙酸(phenylalanine)。 5-5 計算 PNK 中色胺酸(tryptophan)殘基單元(residue)的個數。 Є色胺酸 = 5600 M-1cm-1 Є 酪胺酸 = 1400 M-1cm-1 Є苯胺基丙酸= 5 M-1cm-1 Є = A / c‧l → ЄPNK = 0.644 / 10μM×1.00cm = 64400 M-1cm-1 Σ(Є 酪+ Є苯) = (14×1400+9×5) M-1cm-1 = 19645 M-1cm-1 ΣЄ色 = ЄPNK - Σ(Є酪+Є苯) = (64400 – 19645) M-1cm-1= 44755 M-1cm-1 在 一 PNK 分子 中 之色胺酸殘基單元為: 44755 M-1cm-1 = 8 5600 M-1cm-1 2 分Name: Student
Code:
32
ndIChO • 問題 6
12 分
硬水
丹麥的土壤層中含有大量的石灰石,因長期與含有 CO2的地下水接觸,石灰石中的碳酸鈣成分 會溶解而變成碳酸氫鈣。因此,這種地下水都是硬水,若被當做飲用水時,水中高濃度的碳酸 氫鈣,往往又以碳酸鈣的形式沈澱下來而造成問題,例如在廚房及浴室經常可以看到這種情 形。 二氧化碳, CO2, 在水中為雙質子酸,0 °C 時,其 pKa值為:CO2(aq) + H2O(l) HCO3– (aq) + H+(aq) pKa1 = 6.630
HCO3– (aq) CO32– (aq) + H+(aq) pKa2 = 10.640
假設下列所有題目中均在 0 °C 時進行,且二氧化碳溶解在水中時的體積變化都 可以忽略,試回答下列各題。
6-1 二氧化碳的分壓為 1.00 bar 時,二氧化碳飽和水溶液中的二氧化碳濃度為
0.0752 M 。請計算在這些條件下,有多少體積的二氧化碳氣體,可以溶解
在1升的水中。
氣體常數(The gas constant):
R = 8.314 J mol–1 K–1 = 0.08314 L bar mol–1 K–1
1 分
C(CO2) = 0.0752 M n (CO2) = 0.0752 mol
由理想氣體方程式 PV = n RT
1.00bar ×V = 0.0752 mol × 0.08314 Lbar mol –1K-1
×273.15 K = V so V= 1.71 L
32
ndIChO • Problem 6
Student Code
6-2 二氧化碳的分壓為 1.00 bar 時,二氧化碳溶解在水中達飽和,請計算水中
氫離子的平衡濃度與二氧化碳的平衡濃度。 CO2(aq) + H2O (l) HCO3-(aq)+ H+(aq)
[H+] = [HCO3+] = x 及 [CO2] +[HCO3-] =0.0752 M
Ka = 10-6.63M = [H+][HCO3-] = X2 [CO2] 0.0752M – x [H+] = 0.000133 M 及 [CO2] = 0.0751 M 1 分 6-3 二氧化碳的分壓為 1.00 bar 時,二氧化碳溶解在濃度為 0.0100 M的碳酸氫 鈉水溶液中達飽和,請計算氫離子的平衡濃度。 CO2(aq) + H2O (l) HCO3- (aq)+ H+(aq)
[CO2] = 0.0751 M 及 [ HCO3] = 0.0100 M Ka = 10-6.63 M = [H+][HCO3-] = x × 0.0100M [CO2] 0.0751 M x = [H+] = 1.76 × 10-6 M 1 分 6-4 二氧化碳的分壓為 1.00 bar 時,二氧化碳溶解在濃度為 0.0100 M的碳酸鈉 水溶液中達飽和,請計算氫離子的平衡濃度。水的解離效應可忽略。 CO2 (aq)+ CO3-2(aq) 2HCO3-(aq) [HCO3-] = 0.0200 M
CO2(aq) + H2O (l) HCO3- (aq)+ H+(aq)
Ka = 10-6.63 M = [H+][HCO3-] = x × 0.0200 M
[CO3-] 0.0751M
x = [H+] = 8.8 × 10 –7 M
32
ndIChO • Problem 6
Student Code
6-5 0 °C 時,碳酸鈣在水中的溶解度為:100 mL 的水可溶解 0.0012 克。 請計
算,碳酸鈣飽和水溶液中的鈣離子濃度。 0012G CaCO3 在 100mL 水中
0012g / 100.0872 gmol-1 = 0.000012 mol CaCO3在 100mL 水中
so [Ca2+] = 1.2 × 10 –4 M
1 分
丹麥的地下水屬於硬水,主要是因為土壤中的石灰石,接觸到溶解在水中的二 氧化碳進行反應而造成的。其平衡反應方程式為:
CaCO3(s) + CO2(aq) + H2O(l) Ca2+(aq) + 2 HCO3– (aq)
0 °C 時,此反應的平衡常數 K 為 10–4.25M2 6-6 大氣中二氧化碳分壓為 1.00 bar 時,請計算水中碳酸鈣到達平衡時,水中 的鈣離子濃度。 K = [Ca2+][HCO3-] = 10-4.25 M [CO2] 且 2[Ca2+] = [ HCO3-] so 4 [Ca2+]3 = 10 -4.25 M2 [Ca2+] = 1.02×10-2 M 0.0751M 3 分 6-7 含有 0.0150 M 的氫氧化鈣溶液,在二氧化碳的分壓為 1.00 bar 下,使之到 達飽和,在問題 6-6 中所述的平衡條件下,請計算溶液中鈣離子的濃度。 C (Ca(OH)2) = 0.015 M
OH- (aq) + CO2(aq) HCO3-(aq)
所有 OH- -消耗掉 (K = 107.37
)
由題 6-6 , 知最大可能的 Ca2+是小的(也就是沉澱 CaCO3)
[Ca2+] = 1.02 × 10-2 M
32
ndIChO • Problem 6
Student Code
6-8 問題 6-7 的氫氧化鈣溶液,如果在分壓為 1.00 bar 的二氧化碳氣體存在 時,在到達飽和之前,就用水將體積稀釋成兩倍。請計算二氧化碳飽和溶 液中的鈣離子濃度。. C(Ca(OH)2) = 0.0075 M 再由題 6-5 , 最大的可能 Ca2+ 濃度是 1.02 × 10-2 M so [ Ca2+] = 7.5× 10-3 M , 不會有沉澱發生 2 分 6-9 以上述的數據,計算碳酸鈣的溶度積常數。K = [ Ca2+][HCO3-]2 = [ Ca2+][HCO3-]2 × [CO3-][H+]
[CO2] [CO2] [CO3-][H+]
= Ksp Ka1 Ka2
So Ksp = 10 –8.26 M 2