Prague, CZECH REPUBLIC
www.50icho.eu
理論試題
國家:
Chinese Taipei (Taiwan)
護照上姓名:
學生代號:
TWN-語言:
Chinese
50
th
IChO 2018
International Chemistry Olympiad
SLOVAKIA & CZECH REPUBLIC
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 1
目錄
說明 ... 2 常數與公式 ... 3 第 1 題 DNA ... 5 第 2 題 中世紀遺骸的運送 ... 10 第 3 題 電動車的崛起 ... 18 第 4 題 放射銅的管柱層析 ... 24 第 5 題 波西米亞石榴石 ... 29 第 6 題 讓我們去玩蘑菇捉迷藏 ... 35 第 7 題 Cidofovir ... 41 第 8 題 石竹烯 ... 48THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 2
說明
本理論試題本含封面共有 57 頁。
聽到【Start】命令,立即開始作答。
作答時間共 5 小時。
必須用筆清楚地在指定的答案區內作答。書寫在答案區之外的答案,均不計
分。
每人有 3 張草稿紙。如果你需要更多的計算空間,可利用考試卷的背面。請
注意,寫在答案區外的任何內容,均不計分。
週期表與可見光譜將另外提供,不在這試題本中。
僅可使用大會所提供的筆和計算機。
你可以要求大會提供官方的英文版試題本,但僅供釐清題目之用。
若你需要離開實驗室(例如: 吃點心或上廁所),請揮一揮藍色的 IChO 卡
片,監試人員會全程伴隨你。
在【Stop】命令前的 30 分鐘,監試人員將會提醒你。
當【Stop】的命令宣布時,你必須立即停止作答。若未停止作答超過半分鐘
或更久,將導致你的理論測驗成績無效。
【Stop】的命令宣布後,將你的試題本放回信封袋內,坐在座位上等候監試
人員收取。
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 3
常數與公式
Avogadro's constant: NA = 6.022 × 1023 mol−1
Universal gas constant: R = 8.314 J K−1 mol−1
Speed of light: c = 2.998 × 108 m s−1
Planck's constant: h = 6.626 × 10−34 J s
Faraday constant: F = 9.6485 × 104 C mol−1
Standard pressure: p = 1 bar = 105 Pa
Normal (atmospheric) pressure: patm = 1.01325 × 105 Pa
Zero of the Celsius scale: 273.15 K
Mass of electron: me = 9.109 × 10−31 kg
Unified atomic mass unit: u = 1.6605 × 10−27 kg
Å ngström: 1 Å = 10−10 m
Electronvolt: 1 eV = 1.602 × 10−19 J
Watt: 1 W = 1 J s−1
Ideal gas equation: pV = nRT
The first law of thermodynamics: ΔU = q + W
Power input for electrical device: P = U I
where U is voltage and I electric current
Enthalpy: H = U + pV
Gibbs free energy: G = H – TS
ΔGo = – RT lnK = – zFEcello ΔG = ΔGo + RT lnQ Reaction quotient Q for a reaction a A + b B ⇌ c C + d D: Q = [C] c[D]d [A]a[B]b
Entropy change: ΔS = qrev
T
where qrev is heat for the reversible process Heat change
for temperature-independent cm:
Δq = ncmΔT
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 4
Van ’t Hoff equation: d lnK
dT = ΔrHm RT2 ⇒ ln ( K2 K1) = – ΔrHm R ( 1 T2 – 1 T1)
Henderson–Hasselbalch equation: pH = pKa + log
[A–] [HA] Nernst–Peterson equation: E = Eo – RT zFlnQ Energy of a photon: E = hc λ
Relation between E in eV and in J: E eV⁄ = E J⁄
qe⁄C
Lambert–Beer law: A = logI0
I = εlc Wavenumber: ν̃ = ν c = 1 2πc√ k μ
Reduced mass µ for a molecule AX: μ = mmA mX
A + mX
Energy of harmonic oscillator: En = hν (n +1
2)
Arrhenius equation: k = A e− Ea
RT
Rate laws in integrated form:
Zero order: [A] = [A]0 – kt
First order: ln[A] = ln[A]0– kt
Second order: 1
[A] = 1 [A]0 + kt
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 5
Theoretical Problem 1
Question 1.1 1.2 1.3 1.4 1.5 1.6 Total
Points 5 5 4 12 12 24 62
7% of the total Score
Problem 1. DNA 第 1 題 DNA
迴文序列 (Palindromic sequences)是一種有趣的 DNA 序列,在具有迴文(palindromic)序列的雙股 DNA(dsDNA)物種中,某一股從 5’端到 3’端方向讀取的序列,會與其互補股從 5’端到 3’端的序列 吻合。因此,有迴文(palindromic)序列特性的雙股 DNA(dsDNA)是由兩條相同序列且互補的單股 DNA 結合而成。一個最佳的例子就是 Drew-Dickerson dodeocanucleotide(十二核苷酸) (1)。
(1) 1.1 具有迴文(palindromic)序列且含有十二個鹼基對的雙股 DNA(dsDNA),有多少種不同的組 合? 1.2 具有迴文(palindromic)序列且含有十一個鹼基對的雙股 DNA(dsDNA),有多少種不同的組 合? 雙股 DNA(dsDNA)的熔點 Tm是定義為當雙股 DNA(dsDNA)的起始量有 50%分解成為單股時的 溫度。
1.3 就 Drew-Dickerson dodeocanucleotide(十二核苷酸) (1)而言,假設 G–C 鹼基對使 DNA 雙股穩定 化的貢獻程度比 A–T 鹼基對還大,當 Drew-Dickerson dodeocanucleotide(十二核苷酸) (1) 其中
任何一對鹼基對被 G–C 鹼基對所取代時,會使熔點 Tm增加的機率有多少?
機率
5′-CGCGAATTCGCG-3′ | | | | | | | | | | | |
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 6
讓我們來分析從單股 DNA 形成雙股 DNA(dsDNA)時的熱力學,包括 DNA 長度對熱力學的影響以 及溫度對熱力學的影響。單股 DNA 結合成雙股 DNA(dsDNA)時的平衡常數,會因為屬於迴文
(palindromic)序列和屬於非迴文(non-palindromic)序列而有所不同。當一個起始濃度 cinit =
1.00 × 10−6 mol dm−3的雙股 DNA(dsDNA)加熱到熔點 Tm時即達到平衡狀態。
1.4 在熔點 Tm時,計算非迴文(non-palindromic)序列的單股 DNA 結合成雙股 DNA(dsDNA)時
的平衡常數,以及迴文(palindromic)序列的單股 DNA 結合成雙股 DNA(dsDNA)時的平衡常 數。 非迴文(non-palindromic)序列雙股 DNA(dsDNA) 計算: K = 迴文(palindromic)序列雙股 DNA(dsDNA) 計算: K =
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 7
當兩個單股 DNA 結合形成雙股 DNA(dsDNA)時,會造成系統自由能的變化。平均每一個 G-C 鹼
基對形成時的自由能變化相當於−6.07 kJ mol−1 ;而每一對 A–T 鹼基對則為 −1.30 kJ mol−1。
1.5 至少需要多少的鹼基對才能構成最短的雙股 DNA(dsDNA)的寡核苷酸(oligonucleotide),而
且此時它的熔點 Tm還能維持在 330 K 以上?
假設單股 DNA 結合成非迴文(non-palindromic)序列雙股 DNA(dsDNA)的平衡常數
Knp = 1.00 × 106 ;而單股 DNA 結合成迴文(palindromic)序列雙股 DNA(dsDNA)的平衡常數
Kp = 1.00 × 105。此時,這個最短的寡核苷酸(oligonucleotide)屬於迴文(palindromic)序列或非 迴文(non-palindromic)序列? 計算鹼基對的數目: 非迴文(non-palindromic)序列雙股 DNA(dsDNA)的鹼基對的數目: 。 迴文(palindromic)序列雙股 DNA(dsDNA)的鹼基對的數目: 。 最短的寡核苷酸(oligonucleotide)是: ☐ palindromic (P) ☐ non-palindromic (NP).
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 8 最後,讓我們簡化鹼基對分別對 DNA 雙股結合(association)的貢獻。在結合的過程中,自由能顯然 和溫度有關。Drew-Dickerson dodeocanucleotide(十二核苷酸) (1) 的熔點的倒數(1/Tm) 與雙股型態的初 始濃度 Cinit之對數關係如下圖。 注意: 標準濃度 c0 = 1 mol dm−3代入;圖中 Y 軸熔點的倒數(1/Tm) 乘上溫度單位 K 後(即 1 𝑇𝑚∙ 𝐾 )可使 數值無單位化。 cinit / 10−6 mol dm−3 0.25 0.50 1.00 2.0 4.0 8.0 Tm / K 319.0 320.4 321.8 323.3 324.7 326.2
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 9 1.6 計算單股 DNA 結合成 Drew-Dickerson dodeocanucleotide(十二核苷酸) (1) 時的標準焓 ΔH°
(standard enthalpy ΔH°)和標準熵(standard entropy ΔS°)。假設 ΔH°和 ΔS°均不隨溫度而改變。 計算:
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 10
Theoretical Problem 2
Question 2.1 2.2 2.3 2.4 2.5 2.6 2.7 2.8 Total
Points 1 4 4 2 6 10 17 14 58
8% of the total Score
第
2 題 中世紀遺骸的運送
在常溫下,外消旋化(racemization)是一種緩慢的反應。 因此,它可用於追溯生物樣本,並且還可以
研究它們的熱處理過程。 我們以L-isoleucine (L-Ile) (L-異白胺酸(L-Ile,(2S,3S)-2-胺基-3-甲基戊
酸)為例。 它在α-碳上異構化並形成(2R,3S)-2-胺基-3-甲基戊酸,也稱為D-allo-isoleucine (D-allo 鄰異白胺酸)。 由於構形僅在兩個立體中心的其中一個上發生變化,因此該過程稱為差向異構化 (epimerization)而非外消旋化。 2.1 勾選正確敘述 ☐ D-allo 鄰異白胺酸和 L-異白胺酸具有相同的比旋光度,但它們具有不同的熔點。 ☐ D-allo 鄰異白胺酸具有與 L-異白胺酸相同的比旋光度絕對值,但符號相反。兩種異構體的 熔點相同。 ☐ D-allo 鄰異白胺酸和 L-異白胺酸具有不同的比旋光度,但它們具有相同的熔點。 ☐ D-allo 鄰異白胺酸和 L-異白胺酸具有不同的比旋光度和不同的熔點。 ☐ D-allo 鄰異白胺酸不具有光學活性。 2.2 列出異白胺酸的每種立體異構物的絕對構形。 2S,3R (L-allo-isoleucine) 2R,3S (D-allo-isoleucine) 2S,3S (L-isoleucine) 2R,3R (D-isoleucine)
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 11
2.3 L-異白胺酸差向異構化的平衡常數 Kep 的值為 1.38(在 374K)。如果我們設定 L-異白胺酸的
Gibbs 自由能Gm° = 0 kJ mol−1,試求在問題 2.2 中所示的所有 A-D 結構,在 374K 的 Gibbs 自
由能。 A kJ mol−1 B kJ mol−1 C kJ mol−1 D kJ mol−1 2.4 如果考慮所有立體中心的立體異構現象,那麼三肽 Ile-lle-lle 最多有幾種可能的立體異構物? 立體異構物的個數為 在差向異構化開始時,我們可以忽略逆向反應。 差向異構化遵循一級動力學: 速率常數在 374K 下是 k1(374 K) = 9.02 × 10−5 h−1,在 421K 下是 k1(421 K) = 1.18 × 10−2 h−1。 在下面的計算中,將 L-異白胺酸的濃度簡記為[L],將 D-allo 鄰異白胺酸的濃度簡記為[D]。 我們可以定義 de(diastereomeric excess,非鏡像異構物超越值)的量為: de = [L] – [D] [L] + [D] × 100(%).
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 12 2.5 在 374 K 下,將 L-異白胺酸煮沸 1 943 小時。試問 a)在煮沸前,b)煮沸後,L-異白胺酸的 de 值(三位有效數字)各為多少? a)在煮沸前 Calculation: de = % (三位有效數字) b)煮沸後 Calculation: de = % (三位有效數字)
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 13 2.6 在 298 K 下,將 10%的 L-異白胺酸轉化為 D-allo 鄰異白胺酸需要多長時間?
Calculation:
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 14 事實上,逆向反應不可忽略。 正確的動力學方程式應表示為 讓我們定義x 為濃度([L])與其平衡值([L]eq)的偏差 x = [L] –[L]eq 可根據下式,推導出 x 隨時間的變化: x = x(0) × e – (k1 + k2)t , 式中 x(0)是 t = 0 時,濃度與平衡值的偏差。 2.7 在 374K 下,煮沸 1.00 mol dm−3 L-異白胺酸溶液 1 943 小時。正向反應的速率常數是 k1(374 K) = 9.02 × 10−5 h−1,L-異白胺酸差向異構化的 Kep為 1.38(在 374 K)。 在下面的計 算中,將 L-異白胺酸的濃度簡記為[L]和將 D-allo 鄰異白胺酸的濃度簡記為[D]。計算沸騰後之 a) [L]eq與 b)非鏡像異構物超越值(de)。(含三位有效數字) a) Calculation: [L]eq = mol dm−3 (含三位有效數字)
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 15 b) Calculation:
de = %
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 16 具有單一掌性中心的胺基酸進行外消旋化,例如 L-精胺酸(L-arginine)的外消旋化: 濃度隨時間的變化可表示為: ln 1 + [D][L] 1 – [D][L] = 2k1t + C 式中,[D]和[L]分別為 D-和 L-精胺酸在時間 t 的濃度,k1是速率常數,且 C 是根據初始濃度而決定的 常數。 1137 年,神聖羅馬皇帝 Lothar Ill 洛薩三世在他前往西西里島旅遊期間去世。為了便於遣返遺體,他 的屍體在死後立即被放入水中(373 K)煮沸一段時間。讓我們嘗試在化學動力學的幫助下,估算煮 沸時間。已知在 373 K、pH = 7 的條件下,蛋白質內精胺酸外消旋化的速率常數 k1為 5.10 × 10−3 h−1。 為了分析洛薩三世骨骼中精胺酸的異構物組成,我們需要先將精胺酸轉移到溶液中。洛薩三世的骨 頭在高酸性環境及 383 K 下,水解 4 小時,其光學異構物的比例為[D][L] = 0.090。而洛薩三世的妻子 Richenza 在她去世時則沒有被煮沸,但使用相同的程序將她的骨頭水解,在這種情況下,其比率為 [D] [L] = 0.059。(注意,外消旋化也在水解過程中發生,速率常數為k1 ',與 k 1不同)。 2.8 於 1137 年,神聖羅馬皇帝洛薩三世在水中煮了多久? 注意:在墳墓中的溫度下,精胺酸的外消旋化過程非常緩慢。由於兩個屍體只有 880 年左右之 久,我們可以忽略這段時間內的自然外消旋化。 Calculation:
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 17
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 18 Theoretical Problem 3 8% of the total Question 3.1 3.2 3.3 3.4 3.5 3.6 Points 2 6 7 3 7 8 Score Question 3.7 3.8 3.9 3.10 3.11 Total Points 6 10 5 2 6 62 Score
第
3 題 電動車的崛起
現今的運輸工具倚賴化石燃料的燃燒,儘管真實引擎燃燒的效率本質上是受限的,通常介於 20 至 40 %間。 3.1 勾選可使熱機效率提升的因素: ☐ 增加引擎之機械零件的阻力 ☐ 增加引擎中之燃料的燃燒溫度 ☐ 使引擎的操作溫度範圍變窄 ☐ 增加氣體的操作壓力 燃料電池可做為改進未來車輛之引擎效率的一種方法,而氫氧燃料電池可提升引擎效率。3.2 在 323.15 K 下,液態水之標準形成焓(enthalpy)為 ΔfH°(H2O,l) = −285.84 kJ mol−1,而異辛烷
(isooctane)之標準燃燒焓為ΔcH°(C8H18,l) = −5 065.08 kJ mol−1。計算在 323.15 K 下,純液態異
辛烷和純氫氣之比燃燒焓(specific combustion enthalpy,單位質量之燃燒焓)。需包括計算過程。 ΔcHs°(C8H18) =
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 19
3.3 計算使用氧氣和氫氣(兩者都是在 100 kPa 、323.15 K 之理想氣體)產生液態水的燃料電池的標
準電動勢(EMF)。利用下面的熵值(entropy),均在 323.15 K:
S°(H2O,l) = 70 J K−1 mol−1, S°(H2,g) = 131 J K−1 mol−1, S°(O2,g) = 205 J K−1 mol−1
需包括計算過程。 Calculations:
EMF = V
3.4 計算燃料電池在 353.15 K 下,產生液態水的理想熱力學效率(η)。在此溫度下,水的形成焓為
ΔfH°(H2O,l) = −281.64 kJ mol−1,而其反應 Gibbs 自由能變化為ΔrG° = −225.85 kJ mol−1。需包
括計算過程。
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 20 3.5 一高分子薄膜電解器使用 2.00 V 的電壓進行電解,其電源能量來自 10.0 MW 的風力發電,以 滿載的電力從晚上 10 點電解到隔天早上 6 點,共產生 1 090 kg 純氫氣。計算電解效率(其定義 為:產生氫氣的質量除以理論所產生氫氣的質量)。需包括計算過程。 Calculations: ηelectrolysis = % 3.6 一種由氫氣燃料電池驅動的電動車,其電動引擎最大功率為 310 kW 。若以最大功率的 15%, 100 km h−1的平均速率,由布拉格開到距離 330 km 遠的布拉提斯拉瓦(Bratislava),計算所需消耗之 氫氣質量。假設氫氣燃料電池產生電能的效率是 75%,電動引擎的效率是 95%,氫氣燃料燃燒的 Gibbs 自由能變化為 ΔrG = −226 kJ mol−1。需包括計算過程。 Calculations: m = kg
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 21 製造氫氣的低效率及儲存的安全問題,阻礙了運用氫氣於交通運輸技術的拓展。聯胺(hydrazine, N2H4)燃料電池也許是一個合適的替代品。 聯胺水溶液系統的標準還原電位如下: 3.7 在下面的 Latimer 圖中,填入聯胺和氨在所給酸鹼值條件下之主要形式,並寫出每一箭頭所代 表之電化學半反應之還原電位。列出所有必要的計算式。 a) 酸性環境下(pH = 0) b) 鹼性環境下(pH = 14) Calculations: N2(g) + 5 H+(aq) + 4 e− → N2H5+(aq) E° = −0.23 V
N2H5+(aq) + 3 H+(aq) + 2 e− → 2 NH4+(aq) E° = +1.28 V
N2(g) + 4 H2O(l) + 4 e− → N2H4(aq) + 4 OH− (aq) E° = −1.16 V
N2H4(aq) + 2 H2O(l) + 2 e− → 2 NH3(aq) + 2 OH− (aq) E° = +0.10 V
2 H2O(l) + 2 e− → H2(g) + 2 OH− (aq) E° = −0.83 V.
N2
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 22 基於毒性、氣味和對環境衝擊的考量,非常不適合在燃料電池中產生氨。 3.8 寫 出 聯 胺 在 鹼 性 條 件 下 分 解 產 生(i) 氨 和 氮 氣 (ii) 氮 氣 和 氫 氣 的 淨 反 應 , 並 分 別 計 算 其 在 T = 298.15 K 之平衡常數。需包括計算過程。 聯胺分解的反應式: Calculations: 聯胺在鹼性環境下分解為 NH3和 N2: K = 聯胺在鹼性環境下分解為 H2和 N2: K = 可充電的鋰離子電池可作為燃料電池的替代品。鋰離子電池通常用石墨作為其中一個電極,而鋰離 子可嵌入石墨的層狀結構中。另一電極,由鋰鈷氧化物(lithium cobalt oxide )製成;此電極在充放電 過程中,可以可逆性的吸收或放出在兩電極間移動的鋰離子。此系統之相關半反應如下:
3.9 根據前面敘述,寫出放電時電池的全反應,並寫出鈷原子的氧化態
(C)n + Li+ + e– → Li(C)n E° = – 3.05 V,
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 23 3.10 根據3.9 小題有關鋰離子電池之放電過程的描述,勾選正確的敘述。 Li(C)n電極為 陰極 因為鋰離子在此還原 陽極 因為鋰原子在此氧化 LiCoO2電極為 陰極 因為鈷離子在此還原 陽極 因為鈷離子在此氧化 3.11 假設在兩電極間轉移一個電子所需 C6(一單位)、CoO2(一單位)和鋰原子(一個)的質量總和稱為
有效電池質量。根據標準 EMF 及有效電池質量,計算此鋰離子電池之 theoretical specific
reversible charge capacity,即單位有效電池質量產生之最大電量(單位:mA·h g−1)和 energy
density,即單位有效電池質量產生之最大能量(單位:kW·h kg−1)。 需包括計算過程。
Calculations:
Charge capacity (cq,s) = mA·h g−1 Calculations:
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 24
Theoretical Problem 4
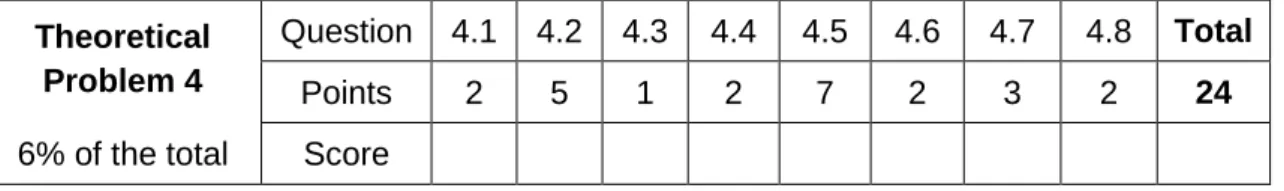
Question 4.1 4.2 4.3 4.4 4.5 4.6 4.7 4.8 Total
Points 2 5 1 2 7 2 3 2 24
6% of the total Score
第
4 題 放射銅的管柱層析
64 Cu 會放射正子(β+),可用於正子斷層攝影,而 64Cu 是利用氘轟擊鋅靶(後續稱為活化靶)來製備。 4.1 寫出用氘轟擊 64Zn 核,產生64Cu 的平衡核反應式,並填入所有元素的質子數和質量數。無需 考慮其電荷。 … + … → … + … 將活化靶溶解在濃鹽酸中,可得到 Cu2+離子和 Zn2+離子及這兩種離子之氯錯合物的混合物。 4.2 依 據 鋅 活 化 靶 製 備 所 得 的 銅 總 量 , 計 算 其 中 帶 負 電 之 含 銅 物 種 的 莫 耳 分 率 。 假 設 [Cl−] = 4 mol dm−3,總體錯合常數β,見表 1 在開始計算之前,將其電荷寫在右上方空格:Cu [CuCl] [CuCl
2] [CuCl
3] [CuCl
4]
表 1. Cu 物種的總體錯合常數β(化學式中已將電荷省略)。𝛽𝑖 = [CuCl𝑖]
[Cu]∙[Cl]𝑖
i in [CuCli]
1 2 3 4
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 25 Calculation: 莫耳分率= (回答至小數點後 2 位) 用陰離子交換樹脂分離含有 Cu2+和 Zn2+離子的混合物及其各自的氯錯合物。將 OH-形式的乾燥樹脂 分散在水中,並將懸浮液轉移到管柱中。為使 Cl−離子佔據其所有位置(即獲得 Cl−形態的樹脂), 用鹽酸洗滌樹脂,然後用去離子水洗滌所有未結合的 Cl-離子。 4.3 在使用鹽酸洗滌之前,所有化合物的最初溫度皆和實驗室溫度相同。當用鹽酸洗滌時,管柱溫 度是否會發生變化?
☐
不會☐
會,其溫度會下降。☐
會,其溫度會上升。THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 26 將 Cu2+ 與 Zn2+離子及其各自的氯錯合物的混合物轉移到填充樹脂的管柱上。使用鹽酸溶液作為沖提 液。 使用簡單的實驗公式,您可以計算層析管柱上銅和鋅兩類物種其平均沖提性質的數值。 滯留體積 VR(將 50%化合物從管柱中沖提出來所需的移動相體積)可以計算如下: VR = Dg × mresin,dry,OH form + V0 4.4 使用平均質量分佈係數 Dg (Dg(Cu 物種) = 17.4 cm3 g−1,Dg(Zn 物種) = 78.5 cm3 g−1),乾燥的 OH−型樹脂的質量= 3.72 g,及管柱的空腔體積 V0 = 4.93 cm3,分別計算銅物種和鋅物種的滯 留體積 VR(單位為 cm3)。 Calculation: VR(Cu species) = cm3 (回答至小數點後 1 位) VR(Zn species) = cm3 (回答至整數) . 如果無法求得答案,請使用 VR(Cu 物種) = 49.9 cm3和 VR(Zn 物種) = 324 cm3進行後續的計算。
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 27 使用簡單的實驗公式,若滿足下式,則兩種化合物 A 和 B 可視為完全分離 V0.001(A) – V0.999(B) > 10Vc V0.001 (A)是將 0.1%的化合物 A 從管柱中沖提出來的移動相體積;而 V0.999 (B)是將 99.9%的化合物 B 從 管柱中沖提出來的移動相體積。Vc為填充濕潤樹脂的管柱的體積。 V0.001(A) = VR(A) × (1 – 6.91√dp/Lc) V0.001(B) = VR(B) × (1 – 6.91√dp/Lc) V0.999(B) = 2VR(B) – V0.001(B) 4.5 根據計算,決定銅物種是否與鋅物種完全分離。填充濕潤樹脂的管柱的體積 Vc = 10.21 cm3, 樹脂粒徑 dp = 0.125 mm,管柱充填濕潤樹脂的高度 Lc = 13.0 cm。 V0.001(A) = cm3 V0.999(B) = cm3 是否可以將銅物種與鋅物種分離?
☐
True☐
False 4.6 計算問題中使用的乾燥樹脂之總離子交換質量容量的理論值 Qm,theor,單位為 mmol g−1。 將四 烷基銨基團視為是唯一進行樹脂離子交換的官能基團,沒有其他含氮基團存在。乾燥樹脂中氮 的質量分率為 4.83%。 Qm,theor = mmol g−1 (回答至小數點後 2 位) 如果無法求得答案,請使用 Qm,theor = 4.83 mmol g−1進行後續計算。THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 28 實際上,並非所有四烷基銨基團都參與離子交換。為了確定總離子交換體積容量 Qv,用過量的硫酸 鈉溶液洗滌一支填充 3.72g 已轉換為 Cl-型態乾燥樹脂的管柱。將沖提物收集在 500 cm3容量瓶中, 然後用水填充至刻度。取其中 100 cm3的試樣,使用 0.1027 mol dm−3硝酸銀溶液進行電位滴定。 達當量點時,使用的硝酸銀溶液體積為 22.20 cm3。填充有濕潤樹脂的管柱體積 V c, 為 10.21 cm3。 4.7 考量以每 cm3濕潤樹脂所含有的活性四烷基銨基團(單位 mmol),計算濕潤樹脂的 Qv (單位使用 mmol cm−3)。 Qv = mmol cm−3 (回答至小數點後 2 位) 如果無法求取答案,請使用 Qv = 1.00 mmol cm−3進行後續計算。 4.8 計算實際參與離子交換之四烷基銨基團的莫耳分率(x)。 x = (回答至小數點後 3 位)
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 29 Theoretical Problem 5 8% of the total Question 5.1 5.2 5.3 5.4 5.5 5.6 5.7 5.8 5.9 Points 3 3 1 5 3 2 4 1 2 Score Question 5.10 5.11 5.12 5.13 5.14 5.15 5.16 5.17 Total Points 5 7 3 2 6 1 1 1 50 Score
第
5 題 波西米亞石榴石
波西米亞石榴石 (Bohemian garnet),又稱為紅榴石(pyrope),是捷克一種著名血紅色的半寶石。天然石榴石的化學組成可用 A3B2(SiO4)3的通式來表示。其中,AII 為二價的陽離子,BIII 為三價的陽離
子。石榴石的晶體為立方體單位晶格(cubic unit cell),此每個立方體中共含有 8 個單位的通式。其中
石榴石晶格結構由三類多面體所組成,即: AII 陽離子佔據十二面體的中心位置,且被 8 個氧原子所 圍繞;BIII 陽離子佔據八面體的中心,且被 6 個氧原子所為圍繞;SiIV 陽離子則佔據四面體的中心位 置,且被 4 個氧原子所圍繞。 最常見的石榴石礦為鐵鋁榴石(almandine),它的化學組成為 Fe3Al2(SiO4)3,其單位晶格邊長(晶格常 數) a=11.50 Å 。 5.1 計算出鐵鋁榴石(almandine)的理論密度值。 = g cm−3 波西米亞石榴石的結構組成為 Mg3Al2(SiO4)3。其純物質呈現無色,而天然石榴石的顏色來自於結構 中的發色團(chromophores),即礦石材料中原先的陽離子被外來的過渡金屬陽離子取代。紅榴石的 顏色,源自於八面體及十二面體的中心離子,分別被微量的 CrIII 及 FeII 離子所取代。 5.2 試畫出 [CrIIIO6]oct 中 d-軌域於此配位晶場中的能階分裂圖,並依序填入電子。
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 30 5.3 找出第一列過渡金屬中,何者的三價陽離子(MIII)處於八面體中心,其低自旋電子組態呈現反磁 性(diamagnetic),其高自旋電子組態則呈現順磁性(paramagnetic)? 5.4 在十二面體晶體場中,d-軌域的能階分裂圖如下。依照發光團[FeIIO8]dod 可能具有的兩種電子 自旋組態,依序填入電子於其所對應的能階軌域中。 a)高自旋電子組態 b)低自旋電子組態 5.5 根據發生兩種不同自旋電子組態所需具備的能量條件,以不等式(例如 P > E1 + E2 + E3) 來表
示其電子成對能量 (P, pairing energy)和躍遷能量(E1、E2、E3)間的關係式。
a)高自旋電子組態: P b)低自旋電子組態: P
5.6 假設 P > E3,找出第一列過渡金屬中,有哪些二價的陽離子(MII)位於十二面體中,其低自旋電
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 31
四種具有顏色的礦石: 波西米亞石榴石 (Bohemian garnet)、綠色鈣鉻榴石(green uvarovite)、藍色藍 寶石(blue sapphire)、橘黃石英石(yellow-orange citrine),其簡化後的吸收光譜如下圖所示。
5.7 寫出下面四種礦石所對應之吸收光譜圖的代號。
波西米亞石榴石(Bohemian garnet): 藍寶石(Sapphire):
鈣鉻榴石(Uvarovite): 石英石(Citrine):
5.8 如果僅照射藍綠顏色的單色光,此波西米亞石榴石(Bohemian garnet)外觀呈現什麼顏色?
Red Blue Yellow-orange Black
Yellow Blue-green Violet White
鈣鐵榴石(Andradite)是另一種石榴石,其化學組成為 Ca3Fe2(SiO4)3。在兩種陽離子的雙取代效應
下,即鈦離子(TiIV )取代八面體中心的鐵離子(FeIII ),鐵離子(FeIII )則取代四面體中心的矽離子(SiIV ),
進而形成黑色的鈦榴石(Schorlomite),化學組成可表示為 Ca 3[Fe,Ti] oct 2 ([Si,Fe] tet O 4) 3。 Abso rb an ce λ (nm) 450 400 500 550 600 650 700 350 300 A b sor b an ce λ (nm) 450 400 500 550 600 650 700 350 300 λ (nm) 450 400 500 550 600 650 700 350 300 A b sorb an ce Abso rb an ce λ (nm) 450 400 500 550 600 650 700 350 300
A
B
C
D
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 32
5.9 若在已知樣品中,八面體中的鐵離子(FeIII)中有 5%被鈦離子(TiIV)所取代。試計算: 鈦榴石
(Schorlomite)中有多少(%)對應的矽離子(SiIV),必將被鐵離子(FeIII)所取代?
p = %
礦石的顏色是由兩種[FeIIIO
6]oct發色團及[FeIIIO4]tet發色團所決定。於此兩種發色團中,其中心離子具
有相同數目的未成對電子。
5.10 畫出兩種發色團(八面體及四面體),所對應的 d-軌域能階分裂圖,並分別填入電子。
八面體的[FeIIIO
6]oct: 四面體的[FeIIIO4]tet:
四面體晶體場造成的能量分裂,較八面體晶體場要小(∆tet = 49 ∆oct)。但令人訝異的是,對 FeIII離子
而言,光譜(雖然訊號強度非常微弱)所測得的第一的 d-d 電子躍遷能量,八面體發色團 (11,000 cm-1)
會較四面體發色團(22,000 cm-1)要小。
5.11 假設電子成對能量(P) 在兩種發色團中均相同。試計算: 電子成對能量(P, pairing energy)、八
面體 (Δoct) 和四面體晶體場中能階 (Δtet) 的分裂大小。
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 33
Δoct = cm−1
Δtet = cm−1
光電材料中所使用的人造石榴石(YAG, YttriumAluminiumGarnet) ,其化學組成為 Y3Al5O12。可視為
在 A3B2(SiO4)3石榴石的通用結構中,分別以 YIII 及 AlIII 來取代 A, B 及 Si 的位置。
5.12 根據你所認知離子半徑的相對大小,決定何種陽離子會取代 A、B 和 Si 位置上的離子?
A: B: Si:
5.13 摻雜有 CeIII 的 YAG,可應用在 LED 科技。若 YAG 中有 5% 的 YIII 被 CeIII所取代,並依此計
量比例,計算 CeIII取代後之化學組成中的 x 及 y 值。 YxCeyAl5O12 x = y = 若你沒有算出答案,以 x = 2.25,y =0.75 做為依據,繼續作答。 5.14 上述的材料可利用 Y2O3、Al2O3、 CeO2的混合物,於含氫氣(H2)的環境中加溫製備。根據 5.13 的化學組成,寫出此反應的平衡方程式,並以最小整數來平衡其係數。
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 34 摻雜稀土離子(rare-earth ions)的人造石榴石(YAG),可製造出不同放光波長的雷射,其放光範圍涵 蓋自紫外光至中紅外光。下圖為幾種稀土離子其簡化之 f-f 軌域間的能量躍遷圖。 5.15 下列何者陽離子,在電子躍遷過程中會放出藍光? Er3+ Sm3+ Tm3+ Pr3+ Yb3+ Nd3+ Tb3+ 5.16 依據上題所選定的陽離子,計算其藍光波長。 λ = nm 5.17 根據傳說,諾亞使用一枝鑲有石榴石的權杖放光照明,做為諾亞方舟航程的引導。假設只考慮 放光效應,若權杖的石榴石 (Bohemian garnet) 顏色為血紅色,則其放光的顏色為何?
Red Blue Yellow-orange Black
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 35
Theoretical Problem 6
Question 6.1 6.2 6.3 6.4 6.5 6.6 6.7 6.8 Total
Points 18 4 8 3 4 12 16 3 68
7% of the total Score
第
6 題 讓我們去玩蘑菇捉迷藏
在捷克和斯洛伐克雖然有一些蘑菇物種是可食用的,但也有一些是不可食用,甚至是有毒的。 墨帽菇(英文名稱為 Inky cap 或 Coprinopsis atramentaria)是一種可食用而且美味的蘑菇,因為它 含有一種稱為 coprine(E)的天然化合物。coprine(E)可以使用 3-氯丙酸乙酯(1)來合成。
6.1 清楚而精準地畫出化合物 A ~ E 的結構。
提示:第一步驟的反應是先產生有機金屬化合物後,再進行環化反應而產生環狀化合物 A。
A B C
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 36
在人體中,coprine 水解後會產生 L-谷氨酸(L-glutamic acid,3)和 C。C 會繼續水解產生化合物 4, 導致化合物 C 和 4 都會造成抑制乙醛脫氫酶參與酒精的代謝副作用。當乙醛脫氫酶被抑制時,酒精 脫氫後所形成的乙醛就會累積在體內,造成嚴重的宿醉(所謂的 antabuse effect)。而原因是乙醛脫 氫酶中的活化位置含有胱氨酸(cysteine)的 SH 官能基,會被化合物 C 或 4 阻斷。
Enzyme = acetaldehyde dehydrogenase
6.2 根據上述的反應圖,畫出乙醛脫氫酶被化合物 4 抑制後所生成的化合物 F 的結構。
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 37 這種宿醉(antabuse effect)的副作用,是因服用戒酒藥 antabuse(5) (antabuse 名叫戒酒硫)後 所出現的現象。戒酒硫 antabuse(5)是一種古老的戒酒藥物,可用來治療酒精成癮。這種藥可經 由下列的反應途徑來製備: 6.3 畫出化合物 G 和 H 的結構。 提示:化合物 H 含有五個碳原子。 G H 6.4 挑選出所有可能作為試劑 I 的選項。
☐ m-chloroperbenzoic acid (mCPBA) ☐ diluted H2O2
☐ Zn/CH3COOH ☐ NaBH4
☐ I2 ☐ hot concentrated H2SO4
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 38 戒酒硫 antabuse(5)抑制乙醛脫氫酶的方式類似化合物 C 和 4 的作用。
Enzyme = acetaldehyde dehydrogenase
6.5 根據上述的反應圖,畫出乙醛脫氫酶被戒酒硫 antabuse(5)抑制後所生成的化合物 J 的結構。 提示:J 的結構包含三個硫原子。 假羊肚菌(Gyromitra esculenta)是另一種有趣的蘑菇。過去雖然有人認為它可以食用(esculentus 拉丁文的意思為可食用),但已有證據明確的指出這種蘑菇由於含有 gyromitrin(M)而具有毒性。 這種有毒天然化合物(M)可以從使用 N-methylhydrazine (6) (N-甲基聯胺,化合物 6) 而製成,如 下圖: 6.6 清楚而精準地畫出化合物 K、L 和 M 的結構。 K L M J
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 39
在人體中,gyromitrin(M)會水解而產生具強烈肝毒性的 N-methylhydrazine (6) (N-甲基聯胺,化 合物 6)。gyromitrin(M)進入人體的胃後,因為胃是屬於酸性的環境,所以 gyromitrin(M)的醯 胺和亞胺官能基都被水解。
在此,讓我們只來探討 gyromitrin(M)分子中的醯胺官能基的水解。有關 C-N 鍵振動中的拉伸模式
的波數為 1293.0 cm-1;同時,觀察同位素效應(isotopes substitution effect)時,位能趨勢曲面
(potential energy surface)的形狀並沒有顯著改變。
6.7 在人體溫度為 37℃的條件下,詳細列出每一個計算步驟並清楚地註明單位,以求得同位素效
應的最大理論值。
假設水解反應時,所有化合物中和反應相關的氮和碳原子均被同位素所取代,亦即,14
N 被
15N 所取代且12C被13C 所取代。且假設只有零點振動能(zero point vibrational energy)會影響
速率常數。計算時,所有元素及其同位素的莫耳質量均以整數代入,且所有的計算步驟內的每 個數值都要包含 5 位有效數字。
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 40
6.8 在觀察這些用同位素來取代的化合物的反應後,發現水解速率沒有顯著的差異,根據上述結果,
以下哪一項最有可能是速率決定步驟?
☐ 水分子對已質子化的 gyromitrin 分子(protonated gyromitrin molecule)進行親核性的攻 擊反應
☐ C-N 鍵的斷裂反應 ☐ 分子進行質子化的反應
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 41
Theoretical Problem 7
Question 7.1 7.2 7.3 7.4 7.5 7.6 Total
Points 10 6 15 9 11 6 57
7% of the total Score
Problem 7. Cidofovir 第 7 題 Cidofovir
由前 Caechoskovakia 的 Holy 教授及其小組所設計和製備的 Cidofovir (1) 是具有抗病毒活性的核苷酸 類似物。它可用於治療 AIDS 患者的病毒感染。
在合成 Cidofovir (1)的過程中,關鍵的中間體為單一鏡像選擇性的二醇類(diol) 2,它可由 L
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 42
7.1 清楚而精準地畫出化合物 A–D 的結構,包含其立體化學。反應過程中,1 莫耳的 A 可以產生 2 莫耳的 B。
A C12H22O6 B
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 43
7.2 清楚而精準地畫出所有其他可替代化合物 3 的立體異構物。當使用這些可替代的化合物時,經 由一樣的反應步驟亦可得到相同的產物 2。
如下圖,二醇類(diol) 2 可經由一系列反應而得到化合物 I。而圖中可將化合物 F 轉變成 G 時,所需 要的磷酸酯 (phosphonate 4)的合成反應,將於後面探討。
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 44 7.3 畫出化合物 E – I 的結構,包含其立體化學。 可用縮寫的 MMT 來表示(4-methoxyphenyl)diphenylmethyl group。 為方便作答,可參考這張與前頁相同的反應流程 圖。 E C30H30O4 F G H I C16H27O8PS
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 45 前述 7.2 中的反應試劑磷酸酯 (phosphonate 4)可以經由下列的步驟來製備
7.4 清楚而精準地畫出化合物 J – L 的結構。
J K
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 46 化合物 I (參考前述 7.3)和胞嘧啶 (cytosine) 5 反應後可得到比例為 3:1 的 M 和 N,而化合物 M 和 N
彼此為同分異構物。M 與 1,4-環己二烯(cyclohexa-1,4-diene)及 Pd(OH)2/C 反應後可得到化合物 O。O
再加入(CH3)3SiBr 即可得到 cidofovir (1)。
7.5 清楚而精準地畫出 M 和 N 兩個同分異構物和化合物 O 的結構,包含它們的立體化學。同時畫 出 P 的結構,此時 P 是胞嘧啶 (cytosine) 5 的另一個具有芳香性的互變異構體(aromatic tautomer)。
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 47
O P
7.6 在將化合物 M 轉變成 O 的過程中,會出現兩個結構比較簡單的有機副產物 Q 和 R。畫出化合 物 Q 和 R 的結構。
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 48
Theoretical Problem 8
Question 8.1 8.2 8.3 8.4 8.5 8.6 8.7 8.8 Total
Points 14 14 2 16 6 8 9 6 75
9% of the total Score
第
8 題 石竹烯
-石竹烯(-caryophyllene) 3 是一種存在於丁香樹的自然界的倍半萜類化合物。它亦存在於某些捷克 和斯洛伐克的植物中,如啤酒花植物或小樹林。
有關-石竹烯(-caryophyllene) 3 的合成,可以從使用單一掌性異構物二烯酮的化合物 A 開始,如 下列反應圖。首先 A 與 silyl ketene acetal 1 反應後,接著進行還原反應並在水溶液中處理而得到酮 類化合物 2。接著中間產物 2 再和甲苯磺醯氯 TsCl (tosyl chloride)反應而得到中間產物 B。產物 B 可在鹼性物質 t-BuOK 的條件下進行環化得到產物 C。最後,產物 C 與葉立德 D (ylide D)反應而生 成最終產物-石竹烯(-caryophyllene) 3。
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 49
8.1 清楚而精準地畫出化合物 A – D 的結構,必要時,包含立體化學。
提示:在 A → 2 的轉化中,silyl ketene acetal 作為親核試劑用。
A C10H14O B
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 50 由於環夠大,化合物 2 和 3 中均可存在一個穩定的反式的雙鍵。在各種環化物中,反式環辛烯(4) (trans-Cyclooctene,4)是允許具有反式雙鍵結構的最小環化物,它可以經由下列反應途徑來合成: 8.2 清楚而精準地畫出反應物 E 和中間產物 F、G 的結構。對於化合物 F 和 G,你一定要清楚地 畫出它們的立體結構,同時挑選出格子內關於立體化學最正確的描述。 E F ☐ achiral ☐ single enantiomer ☐ racemic mixture ☐ mixture of diastereoisomers G ☐ achiral ☐ single enantiomer ☐ racemic mixture ☐ mixture of diastereoisomers
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 51 8.3 畫出反式-環烯烴 4 (cycloalkene 4)的掌性異構物。 -石竹烯(-caryophyllene) 3 中的兩個雙鍵的活性明顯不同。在大部分的案例中,屬於環內 (endocyclic)的雙鍵往往比環外(exocyclic)的雙鍵來的活潑。 8.4 清楚而精準地畫出化合物 Ha + Hb、I 和 Ja + Jb 的立體化學結構。 提示:Ha + Hb 屬於非掌性異構物,同理 Ja + Jb 也是屬於非掌性異構物。
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 52
Ha + Hb
I
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 53
非常有趣的現象是異石竹烯 5 (isocaryophyllene,5) 中的雙鍵的活性和 -石竹烯(-caryophyllene) 3 則完全相反,也就是環外的雙鍵比較活潑。
8.5 清楚而精準地畫出化合物 Ka 和 Kb 的化學結構。提示:Ka 和 Kb 彼此屬於非掌性異構物。
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 54
同位素標記法是一種非常珍貴的工具,可用來研究有關反應機構、決定結構、和質譜或核磁共振光 譜學的資訊。在此,讓我們來觀察以下使用-石竹烯(-caryophyllene) 3 來進行同位素標記的反應。
8.6 清楚而精準地畫出化合物 L 和 M 的結構,包含適當的立體化學。
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 55 -石竹烯(-caryophyllene) 3 在酸的催化下可以進行環化反應而產生一系列複雜的產物,如下圖。化 合物中的 Na 和 Nb 彼此為非掌性異構物,7a 和 7b 彼此也屬於非掌性異構物,而它們是含量最多的 產物。首先反應是從該比較活潑的環內的雙鍵先和質子反應,而生成陽離子的中間產物 O。接下來 的環化反應是不會斷裂任何一個碳-碳單鍵的反應,而且可生成具有三環結構的陽離子中間產物 Pa 和 Pb,同時,Pa 和 Pb 彼此屬於非掌性異構物。接著,Pa 和 Pb 可以和水反應,而生成醇類 Na 和 Nb。另一種可能是 Pa 和 Pb 可以經由斷裂某一個碳-碳單鍵,再次重組而生成具陽離子的 Qa 和 Qb, 接著,再脫去質子而生成 7a 和 7b。 8.7 清楚而精準地畫出最後生成非掌性異構物 7a 的三種中間體 O、Pa 和 Qa 的結構,包含適當的 立體化學。 O Pa Qa
THEORETICAL PROBLEMS, OFFICIAL ENGLISH VERSION 56 8.8 清楚而精準地畫出彼此屬於非掌性異構物 Na 和 Nb 的結構。