N-(羥基苯)多羥基苯醯胺化合物在抑制過氧化氫及酪胺酸酶活性能力之研究
張嘉苓1、楊朝成2 1敏惠醫護管理專科學校 美容保健科 2嘉南藥理科技大學 化粧品應用與管理系 Email:[email protected]摘 要
本實驗透過簡單的合成步驟合成一系列多酚醯胺類化合物(1~40),將不穩定的亞胺類結構,改為較具穩定 性、極性、高化性、且不受pH 值影響的醯胺類結構,再將所合成出來的多酚醯胺化合物透過抑制酪胺酸酶酵 素活性及過氧化氫的活性測試,進而篩選出具有抗氧化功效的多酚醯胺類化合物。其抗氧化能力以超微弱冷 光技術BJL 評估,藉以測試清除過氧化氫活性能力,並與 Trolox(水溶性維他命 E)做比較;而對於抑制黑色素 生成之效果,透過抑制酪胺酸酶活性的測試,並與L-Ascorbic acid(維生素 C)和 Kojic Acid(麴酸)做比較。研 究結果發現,多酚醯胺化合物的抑制能力好壞主要取決於苯環上羥基的取代數目,羥基數越多其抑制過氧化 氫及酪胺酸酶酵素的能力越好。
關鍵詞:多酚醯胺、過氧化氫、酪胺酸酶酵素、活性
1. 前 言
人體在代謝過程中,往往需要靠著氧的參與來維持生物體內的正常運作,在這過程當中,就會產生許多 的活性氧物質ROS (Reactive oxygen species),也就是所謂的自由基。而造成人體老化的成因非常之多,其中 又分為外在因素及內在因素,而這些因素都跟自由基有關[1]。過量的過氧自由基會阻礙人體酵素活性的下降、 DNA 退化、細胞膜受損及多醣類的代謝異常等傷害與光老化現象[2],進而破壞免疫系統的正常運作,導致各 種細胞的病變。雖然生物體內本身就存在著保護系統以維護體內各部位之正常運作,如人體本身存在一套可 消除過量自由基的酵素型抗氧化保護系統,以避免人體過量產生自由基現象,如過氧化物歧化酵素(Superoxide dismutase,簡稱為 SOD)、過氧化氫酵素(Catalase)、穀胱甘汰過氧化酵素(Glutathione peroxidase)、過氧化酵 素(Peroxidase)等,讓體內的自由基維持在一種動態的平衡中來達到對細胞 DNA 的保護作用[3],以及非酵素 型抗氧化保護系統如藉由外界補充具有抗氧化物質如:glutathione、Vitamin A、Vitamin C、Vitamin E、 flavonoids、Zn、及輔酶 Q10 等物質,以輔助體內抗氧化系統,來避免這些氧化所帶來的病變產生。 此外,皮膚是人體的最大器官,也是與外界接觸的部位,然而長期暴露在自由基中,皮膚上的脂質就會 與氧反應,而產生脂質氧化的現象,當過量脂質氧化,就會累積在我們皮膚中,而導致皮膚脂質過氧化而產 生變化,雖然皮膚也存在著抗氧化酵素系統,來幫助我們消除體內過量的活性氧自由基,並且也可以同時對 抗紫外線及污染所帶來的氧化壓力,然而也可以透過飲食方式來攝取抗氧化物質,但由於從飲食方面攝取抗 氧化量有限,經常因為消化吸收後,運送到皮膚的含量非常微弱,因此為了增加皮膚的抗氧化量,添加抗氧 化劑成分在化粧品中還是對皮膚有幫助的。 目前開發抗氧化原料的研究走向,多數從天然植物中萃取出多酚類(PolyPhenols)化合物為主,而存在植物 和蔬菜中的天然抗氧化成分種類繁多如:類胡蘿蔔素(carotenoids)、硫醇(thiols)、兒茶素(Catechins)、類黃酮 (flavonoids)、多酚類(polyphenols)、維生素(Vitamins):ascorbic acid、tocopherols 等,都具有其抗氧化效果[4-5], 目前在天然的抗氧化物中,具有較低毒性的優點,但因為來源取得不易、成本昂貴、不易純化,後製處理較 ©2010 National Kaohsiung University of Applied Sciences, ISSN 1813-3851
為複雜且費時加上成分相當不穩定等缺點。因此,利用合成技術製造之抗氧化劑依然佔有市場的重要一席之 地,過去已證實了複合式的飲食中具抗氧化活性,另外,在各種化學、生物、和電化學的評估方式下,也已 經證實多酚類的化合物具有很強的抗氧化與清除自由基的活性[6],而對於從天然的實材中去找尋其有效成 分,由於取得不易加上品質又難控管,所以利用合成方法生產之原料,透過合成技術普遍運用在工業上當作 抗氧化添加物[7],因此,本研究希望透過有機合成製備一系列多酚類化合物,探討其在抗氧化及抑制黑色素 生成能力,進而研發出抗氧化原料。
2. 實驗方法
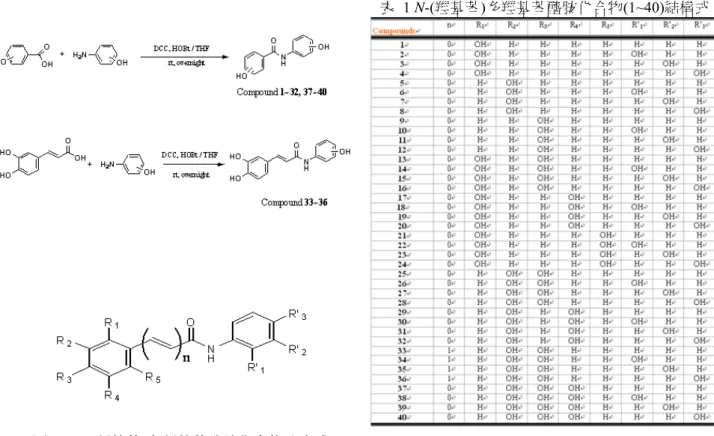
2.1 N-(羥基苯)-多羥基苯醯胺化合物製備 分別取原兒茶酸、胺基苯酚、HOBt (1-hydroxybenzotriazole),加入無水四氫呋喃(THF)於室溫下攪拌,最 後再加入DCC (N, N’-dicyclohexylcarbodiimide)於四氫呋喃(THF)中溶解,攪拌反應過夜。隔天再加入原來胺 基苯酚三分之一量於反應瓶中,置放過夜。用TLC 檢視反應結果(以 50% EtOAc/n-Hexane 為展開劑),確定產 物反應完成後,先將固體濾掉,濾液用減壓濃縮機濃縮,並加入蒸餾水再用乙酸乙酯萃取,合併有機層加入 飽和食鹽水(brine)處理,再以無水硫酸鈉進行乾燥,過濾,減壓濃縮後,經 60 M 的 silical gel 進行管柱層析 純化(以 50 % EtOAc/n-Hexane 為沖提劑),再以1H 及13C NMR 鑑定結構,得到一系列高產率之多酚醯胺化產物(1~40),其反應如圖 1 以及與各結構式如表 1 所示。
表 1 N-(羥基苯)多羥基苯醯胺化合物(1~40)結構式
2.2 抑制過氧化氫活性測試 本測試套組系列,包含過氧化氫啟動試劑,以及冷光產生之特異探針。當過氧化氫與探針作用後,產生 之超微弱冷光,以超微弱冷光儀偵測過氧化氫。當超微弱冷光儀之計數達平衡時(約 10-15 分鐘後),加入欲測 試樣品溶液,若該樣品有清除過氧化氫的能力,則冷光之計數會急速下降。藉由添加不同劑量測試樣品對產 生冷光值之變化來計算抑制過氧化氫能力及計算其IC50值,以評估樣品的抑制過氧化氫能力。 首先將已配置好的過氧化氫第Ⅰ劑(Luminol)、第Ⅱ劑(pH 7.3 PBS)、第Ⅲ劑(1.2 % H2O2),分別加入於 BJL 超微弱冷光儀之石英測量杯內充份混合均勻,放入儀器測定冷光值(約 600 秒),當冷光值達平衡後,再取 5mg 樣品與去離子水配製成濃度10 μg/ml,將 10 μg/ml 樣品中取 10 μl 加入試劑中,觀看冷光值的變化,等冷光再 達平衡後,記錄其冷光值,分次再加入10 μl 相同劑量之樣品,觀察再度下降之冷光值,並記錄之,測試步驟 重覆四次,求出四次的抑制率(百分比%),再分別計算出其抑制過氧化氫能力之 IC50值。並且以水溶性維他命 E(Trolox)為正相(+)作對照,觀察多酚醯胺化合物彼此間抑制過氧化氫活性能力的差異性。抑制過氧化氫能力 之計算方法如公式(1)所示。 過氧化氫抑制能力
(%)
=
−
1×
100
%
initial initialA
A
A
(1) 2.3 抑制酪胺酸酶活性活性測試 首先取多酚醯胺化合物(1~40)與 DMSO 溶液,加入酪胺酸酶酵素(Enzyme)PBS 溶液,配製成總體積 1000 μl;最終濃度分別為 10、20、60、150、200 μg/ml 之 DMSO 溶液的測試濃度,分別測試其不同濃度下樣品對 抑制制酪胺酸酶活性。扣色組含樣品及 PBS 磷酸緩衝液,但不加酪胺酸溶液,其餘步驟相同。在控制組(+) 方面則不加待測樣品;空白組(-)則不加酪胺酸酶酵素(Enzyme) PBS 溶液,另外以維生素 C(Vit.C)和麴酸(Kojic acid)作為本實驗對照組。溶液配製完成後,量測在 540 nm 之吸光值,每次測試皆重覆三次。再算出抑制率, 將求出多酚醯胺化合物抑制制酪胺酸酶活性之IC50濃度。酪胺酸酶抑制活性之計算方法如公式(2)所示。 Tyrosinase 抑制活性(%)
(
)
(
)
100
%
2 1 4 3 2 1×
−
−
−
−
=
A
A
A
A
A
A
(2) A1:控制組540 nm 之吸光值 A2:空白組540 nm 之吸光值 A3:樣品540 nm 之吸光值 A4:扣色組540 nm 之吸光值3. 結果與討論
3.1 抑制過氧化氫活性測試 如圖2 所示,以多酚醯胺化合物 8 為例將其置於石英量測杯中,在超微弱冷光儀中與過氧化氫共存下所 得之冷光值變化圖,圖中可見冷光值在三劑過氧化氫混合加入後,當達到穩定時的冷光值為25264(約 538 秒), 在加入多酚醯胺化合物 8 後,急速下降至 21893,待冷光值趨向穩定時(約 60 秒),再次加入 10 μl 相同濃度的 樣品待測物,其抑制過氧化氫活性能力之冷光值再度下降為 19654,待冷光值趨向穩定時,第三次以同樣方 式加入樣品待測物,其抑制過氧化氫活性能力之冷光值逐步下降為 18035,待冷光值趨向穩定時,第四次加 入10 μl 的樣品待測物時,其冷光值再度下降為 17221;利用公式(1)求出其抑制過氧化氫活性之抑制率,並算 出其IC50值。圖3 多酚醯胺化合物(1~40)抑制過氧化氫 活性能力之IC50 圖2 利用 BJL 超微弱冷光儀器測試多酚醯胺化合 物 8 抑制過氧化氫活性能力之冷光變化光譜 表2 多酚醯胺化合物抑制過氧化氫活性能力測試 其多酚醯胺化合物(1~40)抑制過氧化氫活性能力之 IC50,如圖3 所示(Compound 2 之 IC50 :365.4、Compound 5 之 IC50為負值表示無抑制過氧化氫活性能力) 。為明顯觀察其冷光值變化以求得其抑制過氧化氫之活性,實 驗中,每種多酚醯胺化合物若以相同濃度(1 mg/ml)加入 10μl 時,其冷光值變化將不固定,因此將多酚醯胺化 合物與過氧化氫作用下其冷光值變化相當的化合物分類在一起,並調整其適當濃度以方便觀察,再依相同步 驟,測試其抑制過氧化氫之活性能力,其結果如表一所示。多酚醯胺化合物抑制過氧化氫活性評估,從結果 顯示大部分皆有良好抑制效果且明顯與羥基取代數量有關;當羧酸苯環上具有三羥基或二羥基取代之醯胺化 合物其抗氧化力較單羥基(IC50 = 0.18~17.02 g/ml)取代時好,甚至可以比 Trlox(IC50 = 12.06 g/ml)之抑制過 氧化氫活性能力強。
3.2 抑制酪胺酸酶活性測試
抑制酪胺酸酶活性評估結果,以咖啡酸、沒食子酸及2, 5-二羥基苯甲酸之醯胺衍生物(Compound 33~40、
17~20)效果最為顯著(IC50 = 62.41~130.28 g/ml),但也有少許之化合物顯示出明顯抑制酪胺酸酶活性能力,
如(Compound 12 之 IC50 = 71.70 g/ml、Compound 24 之 IC50 = 57.26 g/ml 及 Compound 36 之 IC50 = 71.03
g/ml)也出現較強之抑制酪胺酸酶活性能力,與對照組維生素 C (IC50 = 107.26 g/ml)及麴酸(IC50 = 80.11 g/ml)之抑制酪胺酸酶活性能力比較不相上下;而其中以 Compounds 12、24、36、39 效果最佳,比麴酸強, 但其他測試樣品對抑制酪胺酸酶活性能力就沒有明顯之效果,如表 2。而圖 3 所示為多酚醯胺化合物(1~40) 抑制酪胺酸酶活性能力之 IC50,由圖中值得注意的是,多酚醯胺化合物 37~40 皆為具有較佳之抑制酪胺酸酶 活性能力,且羧酸苯環上剛好具有三個羥基。另外,多酚醯胺化合物1~11 羧酸苯環的羥基數只有一個,其 IC50 數值偏高,而這也說明羥基數目可以影響活性抑制率。 表 3 多酚醯胺化合物抑制酪胺酸酶活性能力測試 圖4 多酚醯胺化合物(1~40)抑制酪胺酸酶活性能 力之IC50圖
4. 結 論
多酚醯胺化合物抑制過氧化氫活性評估結果,皆有良好抑制效果,明顯與羥基取代數量有關;當羧酸苯 環上具有三羥基或二羥基取代之醯胺化合物(IC50 = 0.18~17.02 g/ml)普遍其抗氧化力較單羥基取代時好,甚 至比Trlox(IC50 = 12.06 g/ml)之抑制過氧化氫活性能力強,但也有少許例外如(Compounds 25 之 IC50 = 53.96 g/ml、28 之 IC50 = 45.77 g/ml 及 33 之 IC50 = 30.56 g/ml)。 美白活性測試:抑制酪胺酸酶活性評估結果,以咖啡酸、沒食子酸及2, 5-二羥基苯甲酸之醯胺衍生物效 果最為顯著(IC50 = 62.41~130.28 g/ml),但也有少許之化合物顯示出明顯抑制酪胺酸酶活性能力,如 (Compounds 12 之 IC50 = 71.70 g/ml、24 之 IC50 = 57.26 g/ml 及 36 之 IC50 = 71.03 g/ml)也出現強之抑制 酪胺酸酶活性能力,總結多酚醯胺化合物以 20、24、34、37、39 及 40 同時在抑制過氧化氫及抑制酪胺酸酶 活性上具有極強之能力。參考文獻
[1] Kohen, R., Kakundas, A., and Rubinstein, A., “The Role of Cationized Catalase and Cationized Glucose OxidainseMucosal Oxidative Damage Induced in the Rat Jejunum.”, The Journaolf biologicachle Mistry, Vol. 267, pp. 21349-21354, 1992. [2] Jia, Z., Tang, M.,and Wu, J., “The determination of flavonoid content in mulberry and their scavenging effects on superoxide
radicals”, Food Chemistry,Vol. 64, pp. 555-559, 1999.
[3] Kohen,S. R., Kakundas, A and Rubinstein, A., “The Role of Cationized Catalase and Cationized Glucose Oxidainse Mucosal Oxidative Damage Induced in the Rat Jejunum”, J Biol Chem ,Vol.267,pp.21349-21354, 1992.
[4] Argolo, A. C. C. G., Sant A. E., Ana M., Pletsch, Coelho, L. C . B. B., “Antioxidant activity of leaf extracts from Bauhinia monandra”, Bioresource Technology ,Vol.95, pp. 229-233, 2004.
[5] Rangkadilok N., Sitthimonchai S., Worasuttayangkurn L., Mahidol C., Ruchirawat M., Satayavivad J., “Evaluation of free radical scavenging and antityrosinase activities of standardized longan fruit extract”, Food and Chemical Toxicology, Vol.45, pp. 328-336, 2007.
[6] Luque-Rodr guez J. M., Luque de Castro M. D.,and Perez-Juan P., “Dynamic superheated liquid extraction of anthocyanins and other phenolics from red grape skins of winemaking residues”,Bioresource Technology, Vol.98 ,pp. 2705-2713 ,2007. [7] Rosemayre S., Freire, Selene M., Morais, Francisco E. A., Catunda- Junior and Diana C. S. N., Pinheiro., “Synthesis and
antioxidant, anti- inflammatoryand gastroprotector activities activities of anethole and related compounds”, Bioorg. Med. Chem ,Vol .13, pp. 4353-4358, 2005.