國立高雄大學化學工程及材料工程學系
碩士論文
以原子轉移自由基聚合法合成聚甲基丙烯酸二甲胺基乙酯及其幾
丁聚醣接枝共聚物作為二氧化碳可切換表面活性劑用於甲基丙烯
酸甲酯懸浮聚合之研究
Atom transfer radical polymerizations of (2-dimethylamino) ethyl
methacrylate and its grafting copolymerizations with chitosan used as
a CO
2-switchable surfactant for suspension polymerizations of methyl
methacrylate
研究生:胡芳滋 撰
指導教授:謝永堂 教授
謝誌
每個碩士生都非常盼望這個時刻,這代表我們即將為碩士做個完美的結果紀 錄。光陰似箭,碩班兩年生活至今仍歷歷在目,從剛大學畢業進入碩班的懵懵懂 懂,到現在懂得思考人生規劃,忽然發現我好像成長很多。這兩年碩士時期,學 到的不光只是專業知識,更重要的是與人之間的相處,以及自我的責任感。 首先,感謝我的指導老師謝永堂老師,帶領我進入環境很棒的實驗室,謝謝 老師在研究上的細心教導與生活上的關心,除了讓我在學業上得到更多知識,對 於待人處事也有更深的體會。此外,也要感謝鄭智嘉老師,熱心的協助後續實驗 並解釋其現象,謝謝鄭老師的鼓勵與支持,讓我得到的不光只是實驗部分,更多 的是對研究的熱忱與態度,在此對兩位老師獻上最大的敬意。最後還要謝謝林榮 顯老師及鄭智嘉老師在百忙之中特地抽空,參與學生的口試並給予指導,使論文 更加完整。 在碩士班這兩年中認識了很多一起並肩作戰的夥伴們,首先感謝系辦的亞貞 姊,總是很親切地笑臉迎人,幫我處理任何的瑣碎事;還有謝謝怡雅姊管理學校 的貴重儀器,讓我能如期的生出數據。再來謝謝妍慈與凱筑,在我剛進碩班時, 帶我熟悉實驗室及儀器,並在我對實驗方向迷惘時給我許多建議。接下來這一群 人要狠狠地感謝,當我實驗上遇到困難時,總提供與協助我以及給我建議,並陪 我一起面對困難、度過難關的同學們 (子豪、維庭、肯尼、政憲、丁丁、絹如、 昱嘉…等人),除了開心能認識你們,也很高興我們一起擁有那些時光。尤其是 維庭、政憲和丁丁,常在我面臨挫折時,給予我相當大的安慰,我衷心的感恩。 此外,也謝謝可愛的學弟妹 (珮羽、曜銓),你們幫了我不少的忙,除此之外,也 謝謝其他幫助我的同學以及學弟妹,雖然沒有一一提名,但我依然感謝。 最重要的是感謝我的家人,你們無疑是最大的功臣,毫無保留的提供讓我安 心求學的環境,默默地在身邊陪伴我,給予我最大的支持及鼓勵,讓我順利完成 學業。最後,謝謝所有幫助過我的人和使我成長的人,因為有你們,使我更加茁 壯,在此獻上我最真誠的謝意。I
目錄
目錄 ... i 表目錄 ... v 圖目錄 ... VII 摘要 ... 1 Abstract ... 2 第一章 前言 ... 4 1-1 刺激應答型高分子 ... 4 1-2 幾丁聚醣之簡介 ... 5 1-2-1 幾丁聚醣的性質與應用 ... 6 1-3 聚甲基丙烯酸二甲胺基乙酯之簡介 ... 7 1-4 較低臨界溶解溫度(LCST)簡介 ... 8 1-4-1 較低臨界溶解溫度(LCST)之測定 ... 9 1-5 超臨界流體 ... 10 1-5-1 超臨界流體之特性 ... 11 1-5-2 選擇超臨界二氧化碳流體的原因 ... 12 1-5-3 超臨界流體之應用 ... 12 1-6 界面活性劑 ... 12 第二章 文獻回顧 ... 14 2-1 原子轉移自由基聚合(ATRP)之簡介 ... 14 2-1-1 原子轉移自由基聚合之原理 ... 14 2-1-2 原子轉移自由基聚合優缺點 ... 15 2-2 利用 ATRP 接枝共聚物 ... 16II 2-3 CO2 刺激應答的官能基團 ... 20 2-4 CO2可切換的界面活性劑 ... 23 2-5 懸浮聚合(Suspension polymerization)之簡介 ... 24 2-5-1 懸浮聚合之原理 ... 25 2-5-2 影響懸浮顆粒的因素 ... 26 2-6 使用具有 CO2響應的起始劑進行乳化聚合反應 ... 27 2-7 研究動機 ... 31 第三章 實驗步驟及方法 ... 32 3-1 實驗藥品 ... 32 3-2 實驗設備 ... 34 3-3 實驗步驟 ... 38 3-3-1 以 ATRP 聚合 PDMAEMA ... 38 3-3-1-1 PDMAEMA 之純化 ... 39 3-3-2 CS-g-PDMAEMA 之合成及純化... 41 3-3-3 在 scCO2下合成 CS-g-PDMAEMA ... 43 3-3-4 在 CO2 下,以 PDMAEMA 作為懸浮安定劑,進行 MMA 的懸浮聚合45 3-3-5 以1H-NMR 鑑定分析材料之組成 ... 46 3-3-6 以 FT-IR 鑑定分析材料官能基... 47 3-3-7 以 GPC 測定材料之分子量 ... 47 3-3-8 以懸滴法測定水溶液之表面張力 ... 47 3-3-9 以 DSC 量測材料之 Tg點 ... 47 3-3-10 以 TGA 量測材料之熱裂解溫度 ... 47 3-3-11 以 UV-Vis 光譜儀測量水溶液之相轉變(LCST) ... 47 3-3-12 以粒徑分析儀量測水溶液之粒徑 ... 48
III 3-3-13 以 SEM 觀察材料之表面形貌 ... 48 3-3-14 以 Zeta potential 量測水溶液之界面電位 ... 48 3-3-15 以數位攝影觀察懸浮聚合溶液之 pH 應答行為... 48 3-3-16 以數位攝影觀察懸浮聚合溶液對 CO2之應答行為 ... 48 第四章 結果與討論 ... 49 4-1 以 PDMAEMA 為懸浮安定劑,懸浮聚合 MMA ... 49 4-1-1 以 1H-NMR 鑑定材料結構... 49 4-1-2 以 FTIR 鑑定材料結構... 54 4-1-3 以 GPC 測量材料之分子量及分子量分佈 ... 58 4-1-4 以懸滴法測量懸浮安定劑之表面張力 ... 61 4-1-5 以 DSC 測量材料之玻璃轉換溫度(Tg) ... 62 4-1-6 以 TGA 測量材料之熱裂解溫度 ... 63 4-1-7 以 SEM 觀察懸浮顆粒表面之形貌 ... 66 4-1-8 以 Zeta potential 測量懸浮安定劑及懸浮溶液之界面電位 ... 71 4-1-9 以粒徑分析儀測量懸浮安定劑 PDMAEMA 與其懸浮顆粒之粒徑... 72 4-1-10 以數位攝影觀察懸浮聚合顆粒溶液之 pH 應答行為 ... 75 4-1-11 以數位攝影觀察懸浮聚合顆粒溶液對 CO2之應答行為 ... 76 4-2 CS-g-PDMAEMA 之合成 ... 79 4-2-1 以 1H-NMR 鑑定材料結構... 79 4-2-2 以 GPC 測量 PDMAEMA 與 CS-g-PDMAEMA 之分子量 ... 83 4-2-3 以懸滴法測量 CS-g-PDMAEMA 水溶液之表面張力 ... 84 4-2-4 PDMAEMA 與 CS-g-PDMAEMA 之 pH 值與溫度應答行為分析 ... 85
4-2-5 以 Zeta potential 測量 PDMAEMA 與 CS-g-PDMAEMA 之界面電位 94 4-2-6 以粒徑分析儀測量 CS-g-PDMAEMA 之粒徑 ... 96
IV
第五章 結論 ... 98
5-1 以 PDMAEMA 為懸浮安定劑,懸浮聚合 MMA ... 98
5-2 CS-g-PDMAEMA 之合成 ... 99
V
表目錄
表 1-1 氣體、液體及超臨界流體之物理性質。 ... 11 表 2-1 ATRP 合成 PDMAEMA 之參數表 ... 16 表 3-1 聚合高分子量 PDMAEMA ( h-PDMAEMA ) 反應條件及反應結果表 ... 40 表 3-2 聚合中分子量 PDMAEMA ( m-PDMAEMA ) 反應條件及反應結果表 ... 40 表 3-3 聚合低分子量 PDMAEMA ( l-PDMAEMA ) 反應條件及反應結果表... 40 表 3-4 聚合 CS-g-PDMAEMA( low MW CS, HCl )之反應條件 ... 42表 3-5 聚合 CS-g-PDMAEMA( low MW CS, CH3COOH )之反應條件... 43
表 3-6 聚合 CS-g-PDMAEMA( high MW CS, HCl )之反應條件 ... 43
表 3-7 聚合 CS-g-PDMAEMA( high MW CS, CH3COOH )之反應條件 ... 43
表 3-8 聚合 CS-g-PDMAEMA ( ScCO2, no catalyst ) 之反應條件 ... 44
表 3-9 聚合 CS-g-PDMAEMA ( ScCO2, HCl ) 之反應條件 ... 44
表 3-10 聚合 CS-g-PDMAEMA ( ScCO2, CH3COOH ) 之反應條件 ... 45
表 3-11 在 CO2 下,以 PDMAEMA 作為懸浮安定劑,進行 MMA 的懸浮聚合之 反應條件 ... 46 表 4-1 懸浮顆粒 PDMAEMA 和 PMMA 組成比例... 50 表 4-2 PMMA 與 PDMAEMA 溶於 CDCl3氫譜圖之化學位移 ... 50 表 4-3 PMMA 與 PDMAEMA 之官能基波數 ... 55 表 4-4 h-PDMAEMA、m-PDMAEMA 與 l-PDMAEMA 之分子量 ... 59 表 4-5 懸浮顆粒 h-PDMAEMA/PMMA、m-PDMAEMA/PMMA 與 l-PDMAEMA/PMMA 之分子量比較 ... 61 表 4-6 懸浮安定劑 PDMAEMA 與其懸浮顆粒 h-PDMAEMA/PMMA、 m-PDMAEMA/PMMA 與 l-PDMAEMA/PMMA 之 Zeta potential ... 72
VI
表 4-8 1 wt% PDMAEMA 及 1 wt% CS-g-PDMAEMA 水溶液之 LCST (℃) ... 94 表 4-9 PDMAEMA 及 CS-g-PDMAEMA 水溶液分別使用不同酸類催化劑進行反 應之界面電位比較 ... 95 表 4-10 前驅物 CS 與 PDMAEMA 分別使用不同酸類催化劑進行界面電位量測95
VII
圖目錄
圖 1-1 Chitin 之結構圖 ... 5 圖 1-2 Chitosan 之結構圖 ... 6 圖 1-3 質子化 Chitosan 之結構圖。 ... 6 圖 1-4 PDMAEMA 之結構圖 ... 7 圖 1-5 PDMAEMA 水溶液之 LCST 示意圖。 ... 8 圖 1-6 質子化 DMAEMA 結構圖。 ... 8 圖 1-7 高分子溶液的相示意圖,溫度對高分子體積分率 Ф 作圖,(a)較低臨界溶 液溫度(LCST)的行為,(b)較高臨界溶液溫度(UCST)行為。 ... 9 圖 1-8 不同升溫速率下 PNIPAAm 之 UV-vis 圖。 ... 10 圖 1-9 物質之相圖。 ... 11 圖 1-10 表面張力與濃度作圖,進一步得知臨界微胞濃度。 ... 13 圖 2-1 ATRP 反應機制示意圖 ... 14圖 2-2 (A) grafting to、(B) grafting from 接枝方法之示意圖 ... 17
圖 2-3 0.05 wt % PDMAEMA-g-CS 水溶液在 (a) pH 4,(b) pH 5 及 (c) pH 7 下之 TEM 圖。 ... 18 圖 2-4 在室溫下 PDMAEMA-g-CS 水溶液於不同 pH 值下之結構示意圖 ... 18 圖 2-5 在 20°C 以定波長 500 nm 測量不同 pH 值對 CS-g-PDMAEMA 水溶液之光 穿透率圖 ... 19 圖 2-6 以定波長 500 nm 測量溫度對 pH 7 之 CS-g-PDMAEMA 水溶液之光穿透 率圖 ... 19 圖 2-7 CO2-switchable hydrophilicity 示意圖 ... 20
圖 2-8 ABA 三嵌段共聚物 CO2-induced gel-to-sol 和相反的 sol-to-gel transition 示 意圖。 ... 21
圖 2-9 CO2-switchable LCST 及其應用。 ... 22
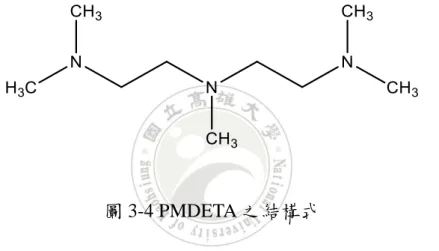
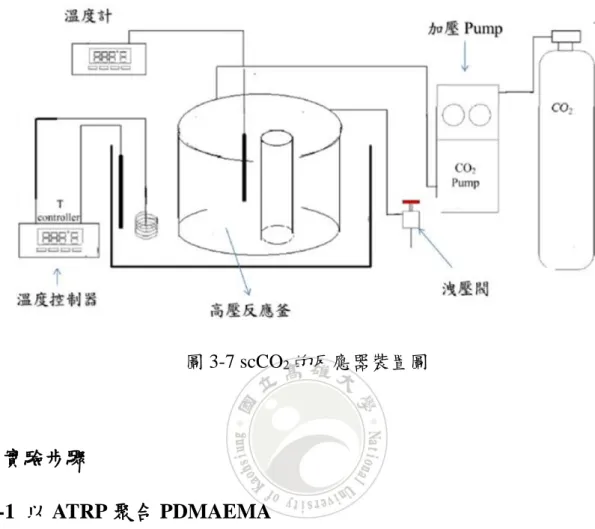
VIII 圖 2-11 十六烷/水(2 : 1)混合物中含有 1a,通 CO2 (左)或 Ar (右)後晃動 10 分鐘, 靜置(A) 5 分鐘,(B) 30 分鐘和(C) 24 小時。(D)在 65℃至 70℃下通入 Ar 兩小時。 ... 24 圖 2-12 不同聚合方法合成高分子之步驟示意圖。 ... 25 圖 2-13 懸浮聚合之示意圖。 ... 26 圖 2-14 PVA 結構式。 ... 27 圖 2-15 使用具有 CO2 響應的起始劑 VA-061 製備 CO2可轉換的苯乙烯膠乳 .... 27 圖 2-16 使用具有 CO2 響應的 DEAEMA 作為共聚單體以製備 CO2可切換的 Polystyrene。 ... 28 圖 2-17 使用 RAFT 的溶液聚合,兩步驟得到 PDMAEMA-b-PMMA。... 29 圖 2-18 以 PDMAEMA-b-PMMA 製備的 PMMA 凝聚/再分散示意圖 ... 29 圖 2-19 膠乳的凝聚/再分散示意圖。 ... 30 圖 3-1 Chitosan 之結構式 ... 32 圖 3-2 DMAEMA 之結構式 ... 32 圖 3-3 MBIB 之結構式 ... 33 圖 3-4 PMDETA 之結構式 ... 33 圖 3-5 MMA 之結構式 ... 33 圖 3-6 GPC 層析管截面示意圖... 36 圖 3-7 scCO2的反應器裝置圖 ... 38 圖 3-8 以 ATRP 合成 PDMAEMA 之反應流程圖 ... 39
圖 3-9 以 MBIB 為起始劑,利用 ATRP 合成 PDMAEMA 之結構反應式 ... 39
圖 3-10 以醯化反應合成 CS-g-PDMAEMA 之反應流程圖 ... 41
圖 3-11 以醋酸/鹽酸當催化劑,醯化反應接枝 CS-g-PDMAEMA ... 42
圖 3-12 在 ScCO2下合成 CS-g-PDMAEMA 之反應流程圖 ... 44
圖 3-13 在 CO2 下,以 PDMAEMA 作為懸浮安定劑,進行 MMA 的懸浮聚合示 意圖 ... 45
IX
圖 3-14 在 CO2下,以 PDMAEMA 作為懸浮安定劑,進行 MMA 的懸浮聚合 . 46 圖 4-1 在 CDCl3中之(A) PMMA 與 (B) PDMAEMA 之 NMR 氫譜圖 ... 51 圖 4-2 在 CDCl3中懸浮顆粒 (A) l-PDMAEMA/PMMA 與 (B)
m-PDMAEMA/PMMANMR (C) h-PDMAEMA/PMMA 之氫譜圖 ... 52
圖 4-3 在 CDCl3中之 (A) PMMA、(B) l-PDMAEMA/PMMA、(C)
m-PDMAEMA/PMMANMR、(D) h-PDMAEMA/PMMA 與 (E) PDMAEMA 之氫
譜疊圖 ... 53 圖 4-4 (A) PMMA、(B) PDMAEMA 之 FTIR 光譜圖 ... 56 圖 4-5 (a) h-PDMAEMA/PMMA、(b) m-PDMAEMA/PMMA 與(c)
l-PDMAEMA/PMMA 之 FTIR 光譜圖 ... 57
圖 4-6 (a) PDMAEMA、(b) h-PDMAEMA/PMMA、(c) m-PDMAEMA/PMMA、(d)
l-PDMAEMA/PMMA 與 (e) PMMA 之 FTIR 疊圖 ... 57
圖 4-7 h-P DMAEMA、m-PDMAEMA 與 l-PDMAEMA 之 GPC 疊圖 ... 59 圖 4-8(A)低分子量系統(B)中分子量系統(C)高分子量系統之懸浮安定劑 與其懸浮顆粒之 GPC 圖譜 ... 60 圖 4-9 懸浮安定劑 PDMAEMA(aq)之表面張力測量圖... 62 圖 4-10 (a) PMMA、(b) h-PDMAEMA/PMMA、(c) m-PDMAEMA/PMMA、(d)
l-PDMAEMA/PMMA、(e) h-PDMAEMA、(f) m-PDMAEMA 與 (g) l-PDMAEMA
之 Tg疊圖 ... 63
圖 4-11(A)低分子量系統(B)中分子量系統(C)高分子量系統之懸浮安定劑 與其懸浮顆粒之 TGA 圖譜 ... 65 圖 4-12 懸浮顆粒 h-PDMAEMA/PMMA 在 pH 7 之 SEM 圖,(a)放大倍率 30k,(b) 放大倍率 100k,(c)放大倍率 200k。 ... 67 圖 4-13 懸浮顆粒 h-PDMAEMA/PMMA 在 pH 2 之 SEM 圖,(a)放大倍率 30k,(b) 放大倍率 100k,(c)放大倍率 200k。 ... 67 圖 4-14 懸浮顆粒 h-PDMAEMA/PMMA 在 pH 12 之 SEM 圖,(a)放大倍率 30k, (b)放大倍率 100k,(c)放大倍率 200k。 ... 68 圖 4-15 懸浮顆粒 m-PDMAEMA/PMMA 在 pH 7 之 SEM 圖,(a)放大倍率 30k, (b)放大倍率 100k,(c)放大倍率 200k。 ... 68
X
圖 4-16 懸浮顆粒 m-PDMAEMA/PMMA 在 pH 2 之 SEM 圖,(a)放大倍率 30k,
(b)放大倍率 100k,(c)放大倍率 200k。 ... 69
圖 4-17 懸浮顆粒 m-PDMAEMA/PMMA 在 pH 12 之 SEM 圖,(a)放大倍率 30k, (b)放大倍率 100k,(c)放大倍率 200k。 ... 69
圖 4-18 懸浮顆粒 l-PDMAEMA/PMMA 在 pH 7 之 SEM 圖,(a)放大倍率 30k,(b) 放大倍率 100k,(c)放大倍率 200k。 ... 70
圖 4-19 懸浮顆粒 l-PDMAEMA/PMMA 在 pH 2 之 SEM 圖,(a)放大倍率 30k,(b) 放大倍率 100k,(c)放大倍率 200k。 ... 70
圖 4-20 懸浮顆粒 l-PDMAEMA/PMMA 在 pH 12 之 SEM 圖,(a)放大倍率 30k, (b)放大倍率 100k,(c)放大倍率 200k。 ... 71
圖 4-21 三者系統之懸浮溶液在 pH 7、25 ̊C 下之可見光穿透粒徑所滯留之時間曲 線圖 ... 73
圖 4-22 (A) h-PDMAEMA/PMMA、(B) m-PDMAEMA/PMMA、(C) l-PDMAEMA/PMMA 懸浮溶液在 pH 7、25 ̊C 下之粒徑分析 ... 74
圖 4-23 懸浮溶液 h-PDMAEMA/PMMA(aq)之 pH 應答行為,並搭配 SEM 對照圖 ... 75 圖 4-24 PDMAEMA 質子化結構示意圖 ... 76 圖 4-25 懸浮顆粒溶液對 pH 之沉澱或分散應答之示意圖 ... 76 圖 4-26 低分子量懸浮溶液 l-PDMAEMA/PMMA(aq) 對 CO2之應答行為 ... 77 圖 4-27 中分子量懸浮溶液 m-PDMAEMA/PMMA(aq) 對 CO2之應答行為 ... 78 圖 4-28 高分子量懸浮溶液 h-PDMAEMA/PMMA(aq) 對 CO2之應答行為 ... 78 圖 4-29 懸浮溶液對 CO2應答行為示意圖 ... 79
圖 4-30 在 D2O 中之 (A) Chitosan 與 (B) PDMAEMA 之 NMR 氫譜圖 ... 80
圖 4-31 在 D2O 中之 (a) Chitosan、(b) CS-g-PDMAEMA(scCO2, HCl)、(c) CS-g-PDMAEMA(scCO2, CH3COOH)與(d) PDMAEMA 之 NMR 氫譜疊圖 ... 81
圖 4-32 在 D2O 中之 (a) Chitosan、(b) CS-g-PDMAEMA (high MW CS,CH3COOH)、(c) CS-g-PDMAEMA (high MW CS, HCl)與(d) PDMAEMA 之 NMR 氫譜疊圖 ... 82
XI
圖 4-34 1wt% PDMAEMA 水溶液在不同 pH 值下之穿透度隨溫度之變化 ... 87 圖 4-35 (A) 1 wt% CS-g-PDMAEMA ( high MW CS, HCl )、(B) 1 wt%
CS-g-PDMAEMA ( high MW CS, CH3COOH ) 水溶液在不同 pH 值下之穿透度隨 溫度之變化 ... 89 圖 4-36 (A) 1 wt% CS-g-PDMAEMA ( low MW CS, HCl )、(B) 1 wt%
CS-g-PDMAEMA (low MW CS, CH3COOH ) 水溶液在不同 pH 值下之穿透度隨溫 度之變化 ... 90 圖 4-37 1wt% PDMAEMA 水溶液及 1wt% CS-g-PDMAEMA 水溶液在不同 pH 值 之穿透度隨溫度變化曲線,其 為 PDMAEMA、 為 CS-g-PDMAEMA ( high
MW CS, HCl )、 為 CS-g-PDMAEMA (low MW CS, HCl )、 為
CS-g-PDMAEMA ( high MW CS, CH3COOH ),而 為 CS-g-PDMAEMA (low MW CS, CH3COOH) ... 92 圖 4-38 1 wt% PDMAEMA 水溶液及 1 wt% CS-g-PDMAEMA 水溶液隨 pH 值變 化之 LCST,其 為 PDMAEMA、 為 CS-g-PDMAEMA ( high MW CS, HCl )、
為 CS-g-PDMAEMA (low MW CS, HCl )、 為 CS-g-PDMAEMA ( high MW CS, CH3COOH ),而 為 CS-g-PDMAEMA (low MW CS, CH3COOH) ... 93 圖 4-39 CS-g-PDMAEMA (cat. CH3COOH) 在 pH 7、25 ̊C 下之粒徑分析 ... 96 圖 4-40 CS-g-PDMAEMA (cat. HCl) 在 pH 7、25 ̊C 下之粒徑分析 ... 97
1 以原子轉移自由基聚合法合成聚甲基丙烯酸二甲胺基乙酯及其幾丁聚醣接枝共 聚物作為二氧化碳可切換表面活性劑用於甲基丙烯酸甲酯懸浮聚合之研究 指導教授:謝永堂 教授 國立高雄大學 化學工程與材料工程學系 學生:胡芳滋 國立高雄大學 化學工程與材料工程學系 碩士班
摘要
本研究先以原子轉移自由基聚合反應 ( atom transfer radical polymerization, ATRP ) 聚 合 特 定 分 子 量 且 分 佈 窄 的 聚 甲 基 丙 烯 酸 二 甲 胺 基 乙 酯 ( poly(2-dimethylamino) ethyl methacrylate, PDMAEMA),並將此高分子作為 CO2 可切換(CO2 switchable)的懸浮安定劑,用於(methyl methacrylate, MMA)的懸浮聚 合,以製備 CO2可切換的 PMMA。實驗中以質子核磁共振光譜儀 ( 1H-NMR )、 傅立葉轉換紅外線光譜儀 ( FT-IR )、凝膠滲透層析儀 ( GPC )、熱重分析儀 ( TGA )、示差掃描熱卡分析儀 ( DSC )、掃描式電子顯微鏡 ( SEM ) 、粒徑分析 儀與 Zeta potential 鑑定分析 PDMAEMA 懸浮安定劑及 PDMAEMA/PMMA 懸浮 顆粒等樣品之組成、分子量、熱性質、顆粒粒徑及水溶液相關性質。結果顯示我 們成功以 PDMAEMA 作為懸浮安定劑聚合 PMMA,顆粒粒徑約為 125 nm。觀 察懸浮溶液對 CO2之應答行為,發現懸浮溶液因 PDMAEMA 結構中的三級胺對 CO2有可切換性,在 CO2環境下,三級胺會質子化而變為親水,使得懸浮顆粒彼 此產生斥力而穩定分散於水中;當通入惰性氣體趕走 CO2後,此時三級胺會去質 子化,使得懸浮顆粒沉澱下來,溶液變為兩相。 此外,我們以 ATRP 合成 PDMAEMA 後 , 再 以 醯 化 反 應 接 枝 合 成 CS-g-PDMAEMA , 以 懸 滴 法 量 測 CS-g-PDMAEMA 水溶液之表面張力,調查 pH 值與 CS-g-PDMAEMA 之親疏水 性及界面活性之相依性,由測量結果可得知,pH 6 以下,CS-g-PDMAEMA 水溶 液表面張力皆無明顯下降;在 pH 6 至 pH 8.5 區間時,表面張力急速下降,此時 具有界面活性之效果;在 pH 9 以上時,表面張力及界面活性不再明顯變化,但 因 PDMAEMA 與 CS 皆去質子化,缺乏足夠的靜電排斥力而不溶於水中。 CS-g-PDMAEMA 接枝反應若在 scCO2 (25 oC, 4000 psi)中進行,接枝反應時間可 大幅縮短,從在一大氣壓下需 3 天的接枝時間,大幅縮短為 4 小時,這部份之研 究我們也分析酸催化劑、CS 分子量對接枝反應之影響。
關鍵字:幾丁聚醣、聚甲基丙烯酸二甲胺基乙酯、原子轉移自由基聚合、二氧化 碳可切換表面活性劑、懸浮聚合
2
Atom transfer radical polymerizations of (2-dimethylamino) ethyl
methacrylate and its grafting copolymerizations with chitosan used as a
CO
2-switchable surfactant for suspension polymerizations of methyl
methacrylate
Yeong-Tarng Shieh, Fang-Zi Hu
Department of Chemical Engineering and Materials Engineering, National University of Kaohsiung
Abstract
In this study, poly(2-dimethylamino) ethyl methacrylate (PDMAEMA) of certain molecular weights with narrow distributions were prepared by atom transfer radical polymerizations and used as a CO2-switchable stabilizer for suspension polymerizations of methyl methacrylate. PDMAEMA and PDMAEMA/PMMA suspension particles were characterized by proton NMR, FTIR, GPC, TGA, DSC, SEM, particle size analysis and Zeta potential analyzer. Experimental results found that PMMA suspension particles of about 125 nm in diameter were successfully synthesized and exhibited CO2-switchable behavior in aqueous solutions. The CO2-switchable behavior can be associated with the tertiary amine groups of PDMAEMA. Upon bubbling CO2, the tertiary amine groups were protonated by the formed H2CO3 and resulted in hydrophilic and thus water-soluble PMMA suspension particles. Upon bubbling N2, CO2 was removed and the water-soluble particles reverted to water-insoluble particles. In addition, the PDMAEMA was grafted to chitosan to obtain CS-g-PDMAEMA. Pendant drop method was used to measure surface tensions of aqueous solutions of CS-g-PDMAEMA and their pH dependencies. Below pH 6, surface tensions of CS-g-PDMAEMA aqueous solutions were found to insignificantly change with pH. Between pH 6 and 8.5, the surface tensions decreased dramatically with pH, indicating that CS-g-PDMAEMA were surface active in this pH range. Above pH 9, the surface tensions and thus the surface activities of CS-g-PDMAEMA decreased insignificantly with pH and phase separation was found due to deprotonations of PDMAEMA and CS. The grafting
3
reactions of CS-g-PDMAEMA in scCO2 at 25 ℃ and 4000 psi took 4 hours which was much shorter than 3 days which was needed for the same reactions under atmosphere pressure. Effects of acid catalysts and molecular weights of CS on the grafting reactions were also investigated in this study.
Keywords: Chitosan, poly(2-dimethylamino) ethyl methacrylate, atom transfer
radical polymerization, CO2-switchable suspension stabilizer, suspension polymerizations.
4
第一章 前言
近幾年來,很多研究對刺激應答型材料很感興趣,這些刺激應答型高分子能夠對 外部環境變化做出反應,使結構或物理及化學性質改變,做出響應的現象。其中以溫 度和 pH 值敏感的高分子為最廣泛的研究,常應用在藥物輸送系統、溫度敏感塗料等。 二十一世紀以來,科技與能源邁入永續經營及環境保護的新代,許多產業朝向低 汙染及高效率發展,若能尋求一個創新且環保的材料與技術,這勢必是一個重要的 研究發展趨勢,Dehui Han 團隊[1][2]利用簡單的概念:CO2在水中會形成碳酸,將 含特殊結構(如:三級胺)的高分子,在水中通入 CO2,藉由 CO2在水中會形成碳 酸,使高分子官能基被質子化,改變親疏水性,之後再通入惰性氣體,就會恢復原本 的結構,而這些高分子又可稱為 CO2-responsive polymer。CO2-responsive polymer 為可切換材料(Switchable materials)的一種,其性質可 隨觸發行為不同而有所改變,因為其可切換性,能使材料有更多潛在的應用,提高能 源效率、減少材料消耗以降低成本,使過程更加環保。近年來,許多研究以二氧化碳 可切換材料(CO2-switchable materials)為最廣泛的研究,因為 CO2是良性的,並且 有化性穩定、便宜,且易取得等特點,許多不同的 CO2響應材料包括聚合物、膠乳、 凝膠、表面活性劑等,陸續被研究開發出,在本研究中,我們使用了 CO2-responsive 的 DMAEMA 作為二氧化碳可切換的懸浮安定劑,成功進行 MMA 的懸浮聚合。
1-1 刺激應答型高分子
天然環保且具有環境敏感的高分子材料在科學領域上引起廣大的興趣。早在 20 世紀,美國及日本科學家首先提出了智能結構這個概念,當時將它稱為自適 應系統。而 20 世紀末,美國 Claus 等人將光纖埋入碳纖維以增強其複合材料,使 之具有感知應力和斷裂損傷的能力,這是智能材料的首次實驗。1989 年日本高木 俊宜教授[3]將智能材料明確的定義,定義智能材料是指對環境具有感知、響應, 並具備功能性的新型材料。 這類高分子材料能夠對外部環境的變化(如:溫度[4]、pH 值[5]、磁場及離子 等)做出反應,大部分的材料只能對一種刺激做出應答,但有些材料能同時對兩 種以上的刺激做出響應。這些環境刺激物會改變高分子鏈間的相互作用力或改變 高分子鏈間與溶劑間的作用力,通常環境中的細微變化就足以誘導這類高分子引 起大變化。 最常見的刺激應答型高分子為溫度和 pH 值應答型。溫度應答型高分子是指 材料可隨溫度變化而做出應答的行為,可導致材料結構外觀的性質改變。通常具5
有較低臨界溶解溫度(Lower critical solution temperature, LCST),此類常見的高 分子有聚氮-異丙基丙烯醯胺 ( PNIPAAm )、聚乙烯吡咯烷酮 ( P4VP )、聚氧化 乙烯醚 ( PEO )等。而 pH 值應答型高分子則是材料對於 pH 值的變化而產生體積 或型態的改變,此種材料通常具有可離子化的官能基團,不管是溫度或 pH 應 答型,其轉變皆具有可逆性,而常見的 pH 值應答型高分子有幾丁聚醣 ( Chitosan )、聚丙烯酸(PAA)及聚甲基丙烯酸二甲胺基乙酯(PDMAEMA)等。
1-2 幾丁聚醣之簡介
幾丁質俗稱甲殼素,是世界上第二個重要的天然聚合物,地球上含量最豐富 的胺基酸型式的多醣體,其含量僅次於纖維素,以β-1,4 鍵 結 的 天 然 直 鏈 型 多 糖 、 N-醯 葡 萄 胺 糖 ( 2-acet-amido-2-deoxy-β-D-glucose,N-acetyl-D-glucosamine, NAG ) 為結 構 組 成 (圖 1-1) [6]。主要含於蝦蟹外骨骼、昆蟲及水生甲殼類等無 脊椎動物的外殼上,和真菌的細胞壁上[7]。 幾丁聚醣 ( Chitosan, CS ) 是幾丁質去乙醯化去除部份或大部份的乙醯基 而 得 的 產 物 , 由 N-乙 醯 葡 萄 胺 糖 ( N-acetyl glucosaminee ) 與 葡 萄 胺 糖 ( glucosamine ) 所組成,其結構與纖維素不同於纖維素在 C-2 的位置上所接的是 -OH 基,而幾丁質或幾丁聚醣在 C-2 位置上所接的是乙醯胺基 (-NHCOCH3 ) 或胺 基 ( -NH2 ),如圖 1-2 之結構式。且當 N-葡萄胺糖含量大於 50 %,即可稱之為 幾丁聚醣 [8]。由於幾丁聚醣分子鏈具有氫氧基與胺基,本身即具有很強的分子 間氫鍵,因此無法溶解於中性水中。但在酸性的水溶液下,胺基 -NH2 會形成帶 正電的 -NH3+,降低幾丁聚醣分子間的氫鍵強度,使得分子鏈展開而溶解於酸性 水溶液中,為天然多醣中唯一的鹼性多醣體。其具有特殊的物理化學和生理功 能,是由天然物質中製得的生物高分子 ( biopolymer ),與生物體細胞有良好的 生物相容性,不具毒性且可被生物分解,被視為最具有生物潛力的生物高分子 [9]。 圖 1-1 Chitin 之結構圖6 圖 1-2 Chitosan 之結構圖
1-2-1 幾丁聚醣的性質與應用
一般市面上的幾丁聚醣為白色帶淡黃色粉末狀的固體,分子鏈中氫氧基與胺基 會產生很強的分子內氫鍵,使幾丁聚醣無法溶於中性水中。當幾丁聚醣溶於弱酸溶 液中,其分子鏈上 -NH2 基團會質子化形成 NH3+,如圖 1-3,使分子間產生靜電 排斥力,使分子鏈得以展開,並溶於弱酸性溶液中。 圖 1-3 質子化 Chitosan 之結構圖。 幾丁聚醣可溶解在稀鹽酸、硝酸、磷酸等無機酸及甲酸、醋酸、乳酸、蘋果酸及 檸檬酸等有機酸中。甲酸為幾丁聚醣的最佳溶劑,醋酸則為最常使用的標準溶劑, 其溶解度主要取決於乙醯化程度和溶液的 pH 值。幾丁聚醣上的胺基孤對電子已 被證實可與過渡金屬產生配位共價鍵,可用來吸附廢水中的有毒金屬,但對鹼金屬和 鹼土金屬離子效果較差。而不同去乙醯程度、水溶液 pH 值、添加濃度與離子強 度皆為影響幾丁聚醣溶解於水溶液中之分子構型變數,但以去乙醯度與溶液 pH 值影響最大。 幾丁聚醣屬於生物聚合物 ( biopolymer ) 一類,包含許多特性,如生物相容 性、生物可降解性、無毒性、再生性、保水性、傷口癒合、發泡成膠性及抗菌等, 並且胺基與羥基容易與其他基團發生反應產生其衍生物,應用更加寬廣 [10]。7
1-3 聚甲基丙烯酸二甲胺基乙酯之簡介
聚甲基丙烯酸二甲胺基乙酯 ( poly (2-dimethylaminoethyl methacrylate ), PDMAEMA ) 為一種新型的刺激應答型高分子,屬於陽離子聚合物[11]。具有 溫度和 pH 雙重敏感性,具有一定的強度和良好的黏彈性。PDMAEMA 分子結 構單元中具有親水性的三級胺、羰基和疏水性的烷基基團,如圖 1-4 所示。當環 境溫度改變時,當環境溫度改變時,會造成氫鍵的形成與破壞,使高分子在水中的溶 解性隨溫度的升高而降低。當所受的溫度高達某一臨界點時,即稱為較低臨界溶液溫度 ( LCST ),高分子在水溶液中,會由相對舒展狀態轉變為團聚狀態,出現相分離,使溶 液產生混濁現象,如圖 1-5 為 PDMAEMA 在水溶液中的 LCST 轉變現象。 PDMAEMA 之三級胺在不同 pH 條件下質子化程度會有所不同,導致親疏水平衡 及相轉變溫度隨 pH 改變而有所不同:在低 pH 值時為親水,而高 pH 值則是相對疏水 的。這種質子化和去質子化行為,可以藉由通入及去除 CO2可逆地進行,為一種 二氧化碳可切換的單體,如圖 1-6 所示。 由許多文獻得知,在共聚物中摻入 DMAEMA 單體,可以誘導共聚物之 CO2 可切換行為[2],當聚合物結構中,原本為不帶電的官能基,會因環境中 pH 值變化而 發生質子化,聚合物鏈會從原先的折疊狀態變為擴展狀態,而此轉變是可逆的。 圖 1-4 PDMAEMA 之結構圖
8 圖 1-5 PDMAEMA 水溶液之 LCST 示意圖。 圖 1-6 質子化 DMAEMA 結構圖。
1-4 較低臨界溶解溫度(LCST)簡介
溫度應答型高分子是因受到一個外部刺激(溫度),會做出不同的行為反應 而加以研究並探討。利用材料對溫度敏感的特性,溫度敏感聚合物可著重於和生 物學相關的應用;藥物輸送、基因遞送和組織工程等。溫度應答型高分子主要有 兩種基本術語,分別為較低臨界溶解溫度(Lower critical solution temperature, LCST),和較高臨界溶液溫度(Upper critical solution temperature,UCST)。LCST 與 UCST 為高分子和溶劑完全混溶時,會低於或高於臨界溫度點,如圖 1-7 所 示,例如,在均勻的溶液中溫度低於 LCST 的聚合物溶液是澄清透明的,而溫度 大於 LCST 以上時,聚合物溶液會出現白色混濁 (也因此 LCST 也被稱為濁點)。 會發生 LCST 和 UCST 這些情況,可以使用吉布斯自由能的方程式ΔG =Δ H-TΔS(G: Gibbs free energy,H:焓,S:熵)來解釋相分離的原因。而特 別的是水的主驅動力是熵,當高分子不是在水溶液中,會有較高的熵。這也被稱9 為疏水性效果 [12]。並且在高分子水溶液的情況下,LCST 還會受高分子的聚合 度、分子量分佈等影響。PDMAEMA 水溶液具有 LCST (約 40℃),但 LCST 也 會受聚合物製備、共聚物中單體比例還有其共聚物親疏水性的情況影響。 圖 1-7 高分子溶液的相示意圖,溫度對高分子體積分率 Ф 作圖,(a)較低臨界溶 液溫度(LCST)的行為,(b)較高臨界溶液溫度(UCST)行為。
1-4-1 較低臨界溶解溫度(LCST)之測定
1999 年,Lin 團隊 [13] 以 ATR/FTIR 對 PNIPAAm 做測試。內容提到在 ATR/FTIR 光譜中,PINPAAm 異丙基訊號(3000cm-1~2835cm-1),在 LCST 以上, 會隨溫度上升而增強;而以下則反之。這顯示異丙基的疏水性質在 LCST 以上 時會較 LCST 以下的情形更加明顯,造成異丙基誘發 PNIPAAm 聚集而析出。 1997 年 C. Kiparissides 團隊 [14],配置 9 wt%的 PNIPAAm 水溶液,利用可 變溫的紫外光-可見光光譜儀(UV-vis)以穿透度的方法量測 LCST,使用不同的升 溫速率,並定義穿透度減少 10%時為 PNIPAAm 水溶液之 LCST (圖 1-8)。他們 發現以同樣的冷卻速率降溫至起始溫度,穿透度會較未量測前高,此歸因於部分 尺寸較使用波長小而造成的偏差,這也顯示 UV-vis 潛在的問題。
10 圖 1-8 不同升溫速率下 PNIPAAm 之 UV-vis 圖。
1-5 超臨界流體
任一物質都有固、液、氣三相存在,物質在臨界點以下,藉由改變溫度或壓 力,會使物質產生相變化,由圖 1-9 所示。當液態物質被放置在密閉容器中,會 和氣態物質之間有兩相分離之界面,此界面產生的原因是由於兩相密度不同,於 特定情形下,加熱加壓可使兩相共存。物質受熱至臨界溫度以上時,無法以壓力 的改變來使之液化,此時氣態和液態的密度相同,為均勻狀態,稱為臨界點,此 點的溫度和壓力即臨界溫度和臨界壓力,超過此點的勻相流體就是超臨界流體。11 圖 1-9 物質之相圖。
1-5-1 超臨界流體之特性
超臨界流體之物理化學性質是介於液體與氣體之間,即是超臨界流體有兼具 液體與氣體之特性。其擴散性質和氣體相似,此液體可如氣體般迅速擴散充滿整 個空間;又超臨界流體的密度及分子間距離類似液體,因此也具有類似液體分子 間的引力,所以超臨界流體對物質的溶解能力近似液體,從表 1-1 可知,超臨界 流體的擴散係數為液體的百倍以上,而密度則為氣體的千倍以上,表示其溶解能 力較氣體佳;黏度接近氣體,有良好的流動性;且擴散係數介於氣體和液體之間, 有良好的質傳性質,因此超臨界流體為優良的溶劑。 表 1-1 氣體、液體及超臨界流體之物理性質。 相 密度 ρ (g/cm3) 黏度 (Pa‧s) 擴散係數 (cm2/s) 氣體 10-3 10-4 10-1 超臨界流體 0.1~0.5 10-4~10-5 10-3 液體 1 10-3 10-512
1-5-2 選擇超臨界二氧化碳流體的原因
一般使用超臨界流體作為溶劑時,需要考慮臨界點是否適當,是否易 達到 臨界點狀態,化學性質是否安定而不與目標物反應,是否不具毒性且來源取得容 易等。二氧化碳的臨界溫度 ( Tc ) 為 31.2℃ 和臨界壓力 ( Pc ) 約 73 bar,並且 具有惰性、無毒性、非燃性、無腐蝕性、價格低及易取得高純度等優點,除此之 外,又因為二氧化碳在常溫常壓下為氣態,使用完二氧化碳會逸失到大氣中,所 以只需要洩壓即可獲得產物,但二氧化碳容易殘留在產物內,所以利用超臨界二 氧化碳流體所得之產物,均需經過真空抽氣的清潔製程除去殘餘之二氧化碳。1-5-3 超臨界流體之應用
超臨界流體目前主要用於以下幾個領域:(a) 石油化學工業方面:許多學者在石化方面的研究,如 Scholskyet al. [15]曾利 用超臨界流體來萃取聚合物中殘留的揮發性溶劑。 (b) 製藥工業方面:製藥程序中常有異構物的出現,但並不容易分離,目前許多 的研究針對 scCO2對異構物溶解度進行測定。此外,對於中藥材或植物中具有 藥效的成份,以 scCO2 進行萃取及溶解度相平衡的研究也是極具前景的領域。 (c) 環境工程方面:超臨界流體對於有機分子的高溶解度,可用在環境工程上, 分離廢水及土壤中具毒性的有機污染物。Hunter [16]以超臨界二氧化碳萃取受污 染土壤之中的農藥成份。 (d) 食品工業方面:由於傳統去除咖啡豆中咖啡因的方法,是使用三氯乙烯等含 氯的有機溶劑為萃取溶劑,但其被懷疑具有致癌性,因此需有替代的溶劑。曾經 有研究以超臨界二氧化碳萃取生咖啡豆之咖啡因,並且這個分離技術經過改良, 在 1979 年於美國建立了第一座商業化運轉的工廠。
1-6 界面活性劑
表面活性劑(又稱界面活性劑)一般具有親水與疏水基團的有機兩性分子, 可溶於有機溶液和水溶液。須具備下列基本性質:(a) 界面吸附性、(b) 界面膜 形成性及排列性、(c) 界面張力降低性、(d) 微胞形成性。最典型的例子是肥皂, 加入少許,便能使目標溶液表面張力有顯著下降,可降低兩種液體或液體-固體 間的表面張力。13
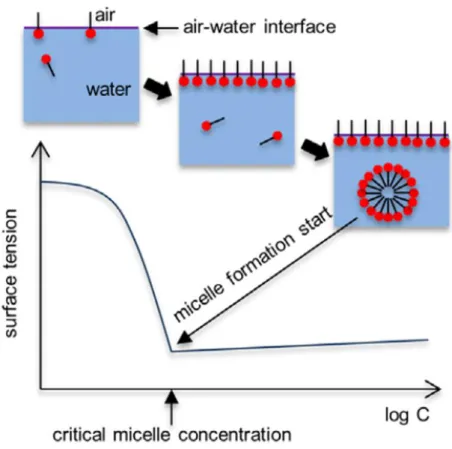
界面活性劑極性部分為親水性,非極性部分為親油性,藉著極性基,能使界 面活性劑溶於水中。當界面活性劑溶於溶劑中時,因其特殊構造,能夠減少與溶 劑之間的表面張力及在溶劑中產生微胞 ( micelle )。當微胞開始明顯形成時,此 時濃度稱為臨界微胞濃度 ( critical micelle concentration, CMC),是表面活性劑的 重要參數。當微胞生成後,再加入界面活性劑,只會增加微胞數量,而在界面增 加甚少,故表面張力幾乎不變,由圖 1-10 所示[17]。
14
第二章 文獻回顧
2-1 原子轉移自由基聚合(ATRP)之簡介
2-1-1 原子轉移自由基聚合之原理
1995 年 Matyjaszewski [18] 發現以過渡金屬作為催化劑之原子轉移自由基聚 合 ( ATRP )。 圖 2-1 ATRP 反應機制示意圖 起始劑 ( R-X ) 上的鹵素原子轉移至過渡金屬錯化物 ( Mtn/Ligand ),使金屬 氧化而產生具有活性的自由基,且活性自由基的失活 ( deactivation ) 反應速率大 於休眠種 ( dormant species ) 的活化 ( activation ) 反應速率,因此系統中的自由 基濃度極低,抑制自由基鏈間的終止反應,進一步有效的控制所需要的分子量及 分子量分佈(PDI)狹窄的聚合物,如圖 2-1 所示。ATRP 關鍵在於使主鏈在低濃度 的自由基環境中成長,能夠有效控制自由基聚合。在此反應中必須趨於休眠反應 而降低活化自由基反應速率,使反應中的自由基濃度保持在極低狀態,因此不可 逆的終止反應相對地變慢而可被忽略。分子量增加是由單體加成而得,不需考慮 控制鏈終止反應、鏈轉移反應及其他副反應。休眠反應與活化反應的交換速率必 須大於鏈成長反應,方可確保每一條高分子鏈與單體反應具有相同的反應性,則 可利用活性自由基聚合法製備分子量分佈窄的高分子。 由此得知 ATRP 的基本原理其實是通過一個交替的“活化-失活”可逆反 應,使反應中的游離基濃度處於極低,迫使不可逆終止反應被降到最低程度,可 稱活性/可控自由基聚合。15
2-1-2 原子轉移自由基聚合優缺點
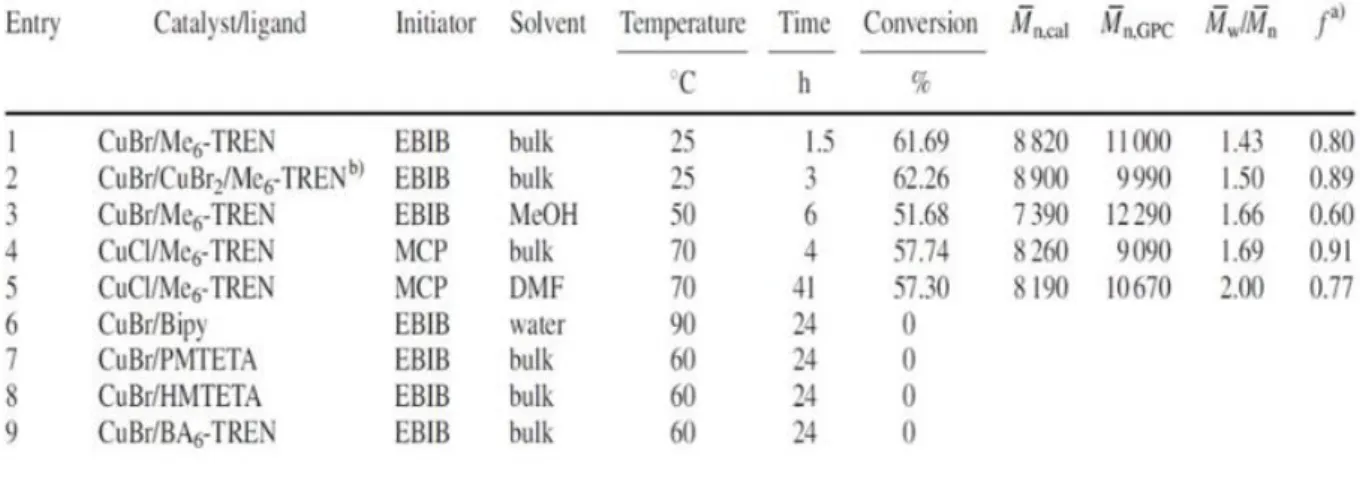
ATRP 的優點 [19] 有下列主要兩點分別為:(a) 適用此聚合的單體種類較 多:大多數單體如甲基丙烯酸酯、丙烯酸酯、苯乙烯和電荷轉移化合物等均可順 利的進行 ATRP。(b) 可以聚合梯度共聚物:例如 Greszta [20] 團隊曾用活性差 別較大的苯乙烯和丙烯腈,以混合法進行 ATRP,在聚合初期,活性較大的單體 進入聚合物,隨著反應時間進行,活性較大的單體濃度下降而更多活性較低的單 體進入聚合物鏈,形成了共聚單體隨時間的延長而呈梯度變化的梯度共聚物。而 需注意且避免影響反應結果之 ATRP 缺點,主要為下列幾點:(a) 催化劑中的還 原態過渡金屬離子易被空氣中的氧氣氧化,不易保存及操作。(b) 過渡金屬化合 物的用量大,且在聚合過程中不消耗,殘留在聚合物中容易導致聚合物老化。(c) 活性自由基的濃度很低(為避免偶合終止),因而聚合速度慢。 因此 ATRP 具有四個明顯區別於傳統自由基聚合之反應特徵:(a) 引發反應 速率大於成長反應速率,所以幾乎不存在鏈終止鏈轉移反應,表示所有聚合物鏈 同時成長、且成長數目不變,因此分子量分佈(PDI)可達到很窄。(b) 聚合物分子 量正比於消耗單體濃度/起始劑初始濃度比。(c) 聚合物分子量隨轉化率成線性增 長,可透過控制單體及起始劑進料比以控制高分子聚合度。(d) 在第一單體之轉 化率達 100%時再加入其他單體,可合成具有特定結構之團聚共聚物、或新型高 分子材料。2002 年,Zhu 團隊 [21] 透過 ATRP 合成 PDMAEMA,探討過渡金屬與 ligand 之配對最佳條件,可在表 2-1 得知以 CuBr 或 CuCl 搭配 Me6-TREN ( ligand ) 能有效的控制其分子量。而其他的 ligand 顯示出對單體沒有活性,以 至於無法聚合成高分子。
16
表 2-1 ATRP 合成 PDMAEMA 之參數表
2-2 利用 ATRP 接枝共聚物
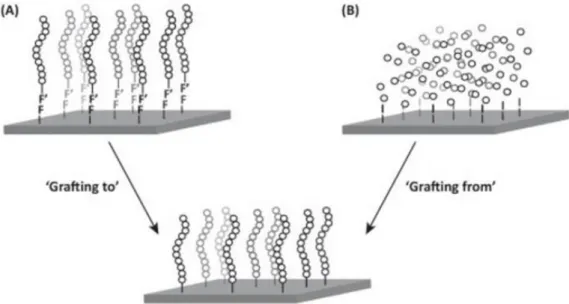
利用 ATRP 接枝共聚物大多以 grafting from 方法接枝,其次也有以 grafting to 方法接枝。grafting from 的接枝原理主要是使主鏈功能化,使其帶有引發單元, 這些引發單元能夠引發單體聚合形成接枝鏈。這項技術主要可用來合成梳型的聚 合物,這種聚合物在每一個重複單元上都含有一個接枝鏈,有關的重要應用是兩 性的殼核狀分層的梳狀聚合物的合成。grafting to [22] 的接枝原理主要是指將具 末端官能化的聚合物鏈接枝到主鏈上,如圖 2-2 所示。這種情況能使梳狀聚合物 形成在固體表面上,並且此梳狀聚合物決定了表面性質。此外,聚合含混刷層的 聚合物,能提供開關和自適應表面特性,且表面粗糙度與混刷層的組合,可以提 供可切換的超疏水表面。 grafting to [23] 方法比起其它聚合物的接枝技術,主要優勢為聚合物可以是 通過各種化學和物理方法來鑑定分析。grafting to 方法被定義可合成良好聚合 物,其特性具有窄分子重量分佈。此外,接枝的方法從化學觀點來看具有較低的 挑戰性,因為它不涉及複雜的合成方法。然而,該技術的主要缺點是所得到的接 枝密度較低,以至於文獻常搭配 Click chemistry 穩定其接枝密度。
17
圖 2-2 (A) grafting to、(B) grafting from 接枝方法之示意圖
2009 年,Lin Li 團隊 [24] 利用 ATRP 及酯化反應,成功接枝梳狀並具有 pH 敏感性之 PDMAEMA-g-CS,並探討其水溶液 pH 敏感性。由圖 2-3 所示,在 pH 4 時,因 CS 和 PDMAEMA 段幾乎質子化,而在強烈的正電荷排斥力呈現鏈展開 型態。在 pH 5-6 時形成自組裝核殼結構之膠束,因大多數 CS 去質子化且疏水 性增加,減小正電荷排斥力同時也促進自身氫鍵與 CS 之作用力,產生以 CS 作 為核且部分去質子化之 PDMAEMA 為殼之膠束型態。當 pH 值達 pH 7 時,核 殼結構進一步折疊成雙層的球狀,是因為大多數 PDMAEMA 和 CS 幾乎被去 質子化而形成雙層硬球,而在 pH 8 時膠束聚集並沉澱,因為 PDMAEMA 和 CS 皆去質子化,而缺乏足夠的靜電排斥力,使 PDMAEMA-g-CS 膠束聚集和 沉澱,如圖 2-4 示意圖所示。
18
圖 2-3 0.05 wt % PDMAEMA-g-CS 水溶液在 (a) pH 4,(b) pH 5 及 (c) pH 7 下之 TEM 圖。
圖 2-4 在室溫下 PDMAEMA-g-CS 水溶液於不同 pH 值下之結構示意圖
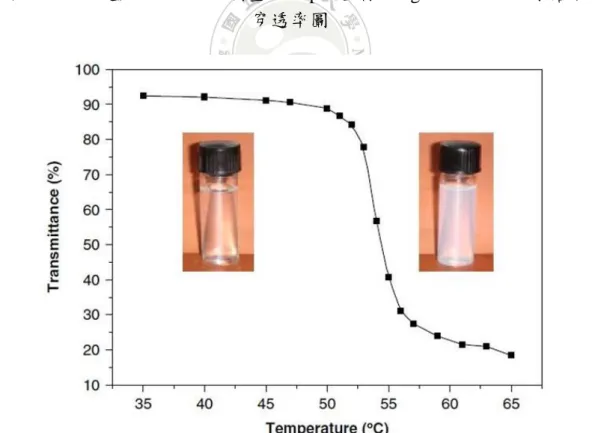
2010 年,Weizhong Yuan 團隊 [25] 利用 ATRP 以 grafting from 方式接枝 CS-g-PDMAEMA,合成方式是將 Chitosan 的 NH2 基團保護住不參與反應,接 著加入溴化物與 OH 基團反應接上形成溴的大分子引發劑,再與 DMAEMA 反 應,成功接枝 CS-g-PDMAEMA。並進行接枝物鑑定分析、測定 pH 值及溫度 應答性質,結果以圖 2-5 所示,以 UV-Vis 量測水溶液之穿透度,發現 pH 值超 過 8 時發現其光穿透率下降,是因為 PDMAEMA 失去正電荷,所以水溶液形成 團聚而沉澱,使穿透率下降。由圖 2-6 所示,原本透明之 CS-g-PDMAEMA 水 溶液升溫至約 53°C 時,其穿透率開始下降,表示其溫度過 LCST 使 CS-g-PDMAEMA 因與水分子的氫鍵作用減弱所以開始團聚沉澱。
19
圖 2-5 在 20°C 以定波長 500 nm 測量不同 pH 值對 CS-g-PDMAEMA 水溶液之光 穿透率圖
圖 2-6 以定波長 500 nm 測量溫度對 pH 7 之 CS-g-PDMAEMA 水溶液之光穿透 率圖
20
2-3 CO
2刺激應答的官能基團
2010 年,Jessop 團隊 [26] 發現具有 amidines 和 guanidines 官能基之高分子 溶液可作為可切換的親水性溶劑,[eq.1]。這意味著此溶劑可以使原先兩者不相 溶的兩相溶液中,藉由通過在大氣壓力下的 CO2,高分子溶液中的官能基可逆 地切換形成親水端的官能基,使得溶劑被切換至其親水形式,在通空氣或加熱趕 走 CO2 可使其切換回來,此時高分子溶液會失去乳化功能,使溶液恢復為原先 的兩相。如圖 2-7 所示。 圖 2-7 CO2-switchable hydrophilicity 示意圖 2012 年,Dehui Han 團隊 [27] 研究合成出兩種三嵌段共聚物分別為 P(MEO2MA-co-DMAEMA)-b-PEO-b-(P-(MEO2MA-co-DMAEMA) 以及
P(MEO2MA-co-MAA)-b-PEO-b-P(MEO2MA-co-MAA),其中,PDMAEMA 及 PMAA 在水溶液中會對 CO2響應,通入 CO2或惰性氣體時,可以使 LCST 可逆 的轉換,分為 CO2-induced gel-to-sol transition 或相反的 sol-to-gel transition,如圖 2-8。
P(MEO2MA-co-DMAEMA)-b-PEO-b-(P-(MEO2MA-co-DMAEMA)嵌段共聚 物中,PDMAEMA 含有三級胺基團 (tertiary amine group)且具有熱感應型的高分 子,當在水中通入 CO2 時,三級胺基團會被質子化,增加極性,使 PDMAEMA 變得可溶,導致 LCST-1 增加變成 LCST-2;之後再通入惰性氣體 (如氬氣 Ar),
21
隨著 LCST-2 恢復到 LCST-1,gelation 再次出現,這個稱為 CO2-induced gel-to-sol transition。
P(MEO2MA-co-MAA)-b-PEO-b-P(MEO2MA-co-MAA)嵌段共聚物中,PMAA 是含羰酸(carboxylic acid)的 pH 敏感型高分子,當在水中通入 CO2時,會降低離 子化程度,使得嵌段共聚物從可溶變為不可溶,即 CO2-induced gelation,使得 LCST-1 降低成 LCST-3,此轉換稱為 CO2-induced sol-to-gel transition。
圖 2-8 ABA 三嵌段共聚物 CO2-induced gel-to-sol 和相反的 sol-to-gel transition 示 意圖。
同一團隊 [2] 的另一篇文獻指出,PDMAEMA 在水中會和 CO2 反應,增加 其 LCST,從 hydrated 變成 dehydrated,這是因為 PDMAEMA 側鏈 amine group 和 CO2 作用,此轉變可藉由通入氬氣(Ar)使其恢復原本的 LCST。後來將 PDMAEMA 當作 CO2-sensitive 引發劑,分別與 PNIPAAm 或 PMEO2MA 共聚
22 合,可以使共聚物也具有二氧化碳應答行為,通入 CO2 或 Ar 可以可逆改變共 聚物的 LCST,如圖 2-9 所示。 圖 2-9 CO2-switchable LCST 及其應用。 二氧化碳應答型的高分子較少報導,主要是因為高分子具有 CO2可響應的官 能基團不多見,在 2014 年,Zhao 團隊調查 CO2可響應的官能基團,根據文獻 [28],主要有這四種官能基團具有 CO2響應行為,如圖 2-10。響應之原理為 CO2 在水中會使水形成碳酸水,而碳酸水會解離出質子將這些基團質子化,質子化的 程度視 pka 值而定,由圖中可得知三級胺的 pka 是四個中最小的,因此質子化速 度最慢,而去質子化就變得較容易,可以經由通入惰性氣體去除 CO2,恢復原先 不帶電的形貌。當 pka 值大到某個程度時,如 quanidine 和 imidazole 鹼性很強, 質子化行為變得很容易,卻不能夠藉由通惰性氣體去除 CO2 ,甚至要輔以加熱 才能恢復原本不帶電的結構。
23
圖 2-10 CO2響應的官能基團。
2-4 CO
2可切換的界面活性劑
一般我們維持乳化的常規方法通常都是加入鹽,但這樣往往會導致系統中鹽 的積累,為了解決這個問題,近年來許多文獻報導了有關 CO2可切換的表面活性 劑 (CO2-switchable surfactants),CO2-switchable surfactants 已經被用於乳液聚合 以穩定原始乳液,又做為乳化劑。乳化劑在乳化聚合中,結構以一端疏水,而一 端為親水的相貌存在,當通入 CO2時,藉由 CO2在水中形成碳酸,高分子官能 基會被質子化,狀態類似表面活性劑,具有帶電荷的親水頭部和疏水尾部,之後 再通入惰性氣體,就會恢復原本的結構。 2006 年,Jessop 團隊 [29] 使用長鏈具有 amidine 官能基的高分子聚合物, 在苯乙烯的乳化聚合裡,作為可切換 CO2的表面活性劑,[Eq. (1)],藉由將 CO2 通入水溶液中使官能基質子化,再通入氬氣去除 CO2,使含有 amidine 之碳酸氫 鹽溶液在 65℃時,引發聚苯乙烯膠乳的凝結。由圖 2-11 所示,搖動含 1a 之十六 烷和水的混合物之溶液進行觀察,可發現一開始乳化現象發生,並清楚地在停止 搖晃後的 5 分鐘之內溶液分成兩層。若溶液在搖動前一小時用 CO2處理,能使乳 化現象更為穩定。而乳液在 65℃通入氬氣,可使十六烷和水的完全分離,使高 分子失去劑面活性劑功能,形成兩相溶液。
24
圖 2-11 十六烷/水(2 : 1)混合物中含有 1a,通 CO2 (左)或 Ar (右)後晃動 10 分鐘, 靜置(A) 5 分鐘,(B) 30 分鐘和(C) 24 小時。(D)在 65℃至 70℃下通入 Ar 兩小時。
2-5 懸浮聚合(Suspension polymerization)之簡介
高分子的聚合方法分為五種,分別為:(a) 總體聚合 ( bulk polymerization)、 (b) 懸浮聚合 ( suspension polymerization )、(c) 沉澱聚合 (precipitation
polymerization )、(d) 二步驟溶脹聚合 ( two-step swelling polymerization )。由圖 2-12 為不同聚合方法合成高分子之步驟示意圖。[30]
25 圖 2-12 不同聚合方法合成高分子之步驟示意圖。
2-5-1 懸浮聚合之原理
如圖 2-13 所示,懸浮聚合是將溶有起始劑的單體以強烈攪拌,變成液滴狀, 在懸浮安定劑的保護下分散於水(介質)中,並使溶於液滴中的起始劑受熱分解, 產生自由基以引發單體的聚合方法,每一液滴就相當於本體聚合的一個小單元, 因此懸浮聚合的機理與本體聚合相同。一般懸浮聚合反應大部分是指 O/W ( oil/water ) 系統的懸浮聚合反應,以水為媒介,不溶於水的單體、能溶於單體 的起始劑以及懸浮安定劑,經由混合後,給予適當的攪拌及溫度,進行聚合反應。 由於是在大量水中進行聚合,優點是散熱好,反應平穩,與本體聚合相比,得到 的聚合物的分子量分布比較均勻。此外,分散劑附著在聚合物小顆粒的表面,容 易分離與洗滌,所以產品純度比乳液聚合高;缺點是聚合過程中聚合物容易黏結 在釜壁上,必須定期清理,因此不能連續生產。而攪拌對懸浮聚合物的粒徑有決 定性作用,攪拌速率越快,粒徑越小,當單體在水中被攪拌時,會形成不穩定的 分散液,液滴經過連續不斷地破裂、分散、集結和合併的過程,會達到最小的平 均粒徑,也由於聚合釜內各點受力的強度不一,各處形成的粒徑也不相同,因此26 有一定的粒度分布。在工業上採用懸浮聚合生產的聚合物主要有聚氯乙烯、聚苯 乙烯、聚甲基丙烯酸甲酯、聚偏二氯乙烯、聚四氟乙烯等。 圖 2-13 懸浮聚合之示意圖。
2-5-2 影響懸浮顆粒的因素
在文獻 [31] 提到在懸浮聚合的反應過程中,為了防止早期液滴與液滴之間 和後期聚合的顆粒間的凝聚,會在反應過程中加入懸浮安定劑。而懸浮安定劑和 攪拌速率是影響懸浮顆粒粒徑、粒徑分佈、顆粒型態等特性的重要因素。在固定 攪拌速率下,懸浮安定劑的用量、種類、性質,是控制顆粒的關鍵因素,當顆粒 分散在介質中,會有布朗運動或重力影響,引起粒子間的碰撞而發生凝絮 ( flocculation ) 或凝集 ( coagulation ) 現象。為了避免這些現象發生,會在反應 過程中加入懸浮安定劑,使粒子之間存在斥力或立體障礙,讓粒子之間無法因相 互接觸而沉澱下來。 懸浮安定劑是能提高固體或液體物料分散性能的助劑。當固體染料研磨時, 加入懸浮安定劑,有助於顆粒粉碎並阻止已碎顆粒凝聚而保持分散體穩定;當不 溶於水的油性液體在高剪切力攪拌下,可分散成很小的液滴,但停止攪拌後,在 界面張力的作用下很快就會分層,然而當溶液中有懸浮安定劑的加入,則能形成 穩定的乳液態,使顆粒穩定的分散於液體中。其主要作用是懸浮安定劑降低了液 -液和固-液間的界面張力,因此懸浮安定劑也是表面活性劑的一種。 在 2012 年,Das 團隊 [32] 使用 PVA 作為懸浮安定劑,利用懸浮聚合法共 聚 VAc–MMA,PVA 為界面活性劑的一種,PVA 有著疏水的主幹,及親水的 OH-基,如圖 2-14,因此具有界面活性的效果,而成功進行懸浮聚合。27 圖 2-14 PVA 結構式。
2-6 使用具有 CO
2響應的起始劑進行乳化聚合反應
2012 年,Cunningham 團隊 [33] 於 CO2氣氛下,使用具有 CO2 響應的起始 劑 VA-061 進行苯乙烯乳化聚合,發現所獲得的膠乳顆粒可以經由除去 CO2而凝 聚,並且在通入 CO2時分散,由圖 2-15 所示。 圖 2-15 使用具有 CO2 響應的起始劑 VA-061 製備 CO2可轉換的苯乙烯膠乳28
同一年底,Jessop 團隊 [34] 進行 surfactant-free emulsion polymerization ( SFEP ),在 CO2氣氛下,使用 VA-061 作為起始劑、DEAEMA 作為 CO2可轉換 的共聚單體,製備 CO2可轉換的 Polystyrene 乳膠,為了增加固體含量,實驗在 65℃下聚合,並發現加入少量莫耳百分比的 MMA 可以顯著增加轉化率,因為 MMA 比 styrene 更親水,並且在水相中可產生更多的疏水性低聚物。之後在破壞 穩定和真空乾燥後可以得粉末固體,再經由加水並通入 CO2鼓泡處理可以再分散 膠乳,如圖 2-16 所示。 圖 2-16 使用具有 CO2 響應的 DEAEMA 作為共聚單體以製備 CO2可切換的 Polystyrene。 2012 年,Zhang 團隊 [35] 使用 RAFT 兩步驟溶液聚合,合成出乳化劑 PDMAEMA-b-PMMA,在 pH 值為 3 的環境下,進行 PMMA 的乳化聚合,反應 式如圖 2-17。在酸性環境下,DMAEMA 的三級胺會發生質子化,以質子化的方 式,作為 CO2可轉換的表面活性劑,再透過起始劑引發聚合,其示意圖由圖 2-18 所示。
29 圖 2-17 使用 RAFT 的溶液聚合,兩步驟得到 PDMAEMA-b-PMMA。 圖 2-18 以 PDMAEMA-b-PMMA 製備的 PMMA 凝聚/再分散示意圖 2013 年,同個團隊 [36] 對同個材料 PDMAEMA-b-PMMA 進行更深入的探 討,其膠乳的穩定性,取決於兩嵌段共聚物的組成比例,發現當 MMA 的重量百 分比 ( FMMA ) 小於 58.5% 時,膠乳保持穩定,而膠乳顆粒尺寸會隨著 FMMA的 增加而降低。 乳化聚合後的膠乳,須先經由添加少量苛性鈉使凝聚,再以去離子水洗滌至 中性,獲得的膠乳才可進一步用於 N2-coagulatable and CO2-redispersible 的可切換 性研究,如圖 2-19 顯示。
30
31
2-7 研究動機
刺激應答型高分子是指高分子材料會因環境的改變或受到刺激,使得材料本 身的結構之物理及化學性質會產生改變,做出響應的行為,此種高分子材料在環 境和生物醫學領域之應用,有無可限量的潛力,因其最容易操控的環境刺激因素 為溫度和 pH 值,所以常見的刺激應答型高分子以溫度和 pH 應答型高分子居多。 幾丁聚醣 ( chitosan ) 為 pH 應答型高分子,有著天然、良好生物相容性及 抗菌除臭等優點;而聚甲基丙烯酸二甲胺基乙酯 ( PDMAEMA ) 是溫度與 pH 值 皆有應答的高分子,當環境溫度超過較低臨界溶液溫度( LCST ) 時,PDMAEMA 在水溶液中,會由澄清透明、鏈展開狀態轉變為非水溶性顆粒,出現混濁現象; 其結構中的三級胺,可藉由通入 CO2,使官能基被質子化,改變結構親疏水性; 如再通入惰性氣體,就能恢復原本的結構,在理論上,因其性質會隨 CO2之有無 而有所改變,因此又稱為 CO2響應高分子,也因為對 CO2有切換性,使材料有 更多潛在的應用,能提高能源效率、減少材料消耗以降低成本,使反應過程更加 環保。 在本研究中,我們以對 CO2具有響應的 DMAEMA 作為 CO2可切換的高分 子材料,進行原子轉移自由基聚合(ATRP),合成不同分子量且分子量分佈(PDI) 窄的高分子聚合物,而 PDMAEMA 本身即具有親水性的三級胺、和疏水性的烷 基基團,具有界面活性的效果,因此我們將此高分子進一步作為 CO2可切換的懸 浮安定劑,利用懸滴法測出 PDMAEMA(aq)之臨界微胞濃度後,進行 MMA 的懸 浮聚合。也因 PDMAEMA 結構中的三級胺對 CO2具可切換性,在 CO2環境下, 三級胺會發生質子化而變為親水,使得懸浮顆粒彼此產生斥力而穩定分散於水 中;當通入惰性氣體趕走 CO2後,此時三級胺會去質子化,而失去懸浮安定劑效 果,使得懸浮顆粒沉澱下來,溶液變為兩相。此外,我們以 ATRP 方法,選擇起始劑 MBIB,使高分子末端有酯基團 (COOCH3),經醯化反應能與 chitosan 之 NH2 形成鍵結,以 grafting to 方法接 枝合成 CS-g- PDMAEMA,藉由搭配不同 pH 值,製備具有不同親疏水鏈端的兩 親性高分子 CS-g-PDMAEMA,然而 chitosan 結構中的一級胺對常壓 CO2的應答 並不明顯,因此我們將接枝反應在 scCO2中進行,接枝反應時間可大幅縮短,從 在一大氣壓下 3 天的接枝時間,大幅縮短為 4 小時,這部份之研究我們也分析酸 催化劑、CS 分子量對接枝反應之影響。
32
第三章 實驗步驟及方法
3-1 實驗藥品
1. 幾丁聚醣 ( Chitosan, CS ),誠麗實業股份有限公司,DD 97%,分子量 350000 Da,將 CS 溶於 HCl 水溶液,加少量 NaOH 使之沉澱,抽氣過濾後,再用去 離子水洗至中性,真空乾燥後使用,結構式如圖 3-1 所示。 2. 幾丁聚醣 ( Chitosan, CS ),Sigma-Aldrich,DD 75~85%,分子量 50000~190000 Da。 圖 3-1 Chitosan 之結構式 3. 甲基丙烯酸二甲胺基乙酯 ( 2- dimethylaminoethyl methacrylate, DMAEMA),Sigma-Aldrich,98%,減壓蒸餾後使用,如圖 3-2 結構式所示。 圖 3-2 DMAEMA 之結構式4. 甲基-α 溴異丁酸乙酯 ( Methyl α-bromoisobutyrate, MBIB), Sigma-Aldrich, ≥99.0%,直接使用,如圖 3-3 結構式所示。
33
圖 3-3 MBIB 之結構式
5. 五甲基二乙烯三胺 ( N,N,N′,N′′,N′′- Pentamethyldiethylenetriamine,
PMDETA),Sigma-Aldrich,≥99%,直接使用,如圖 3-4 結構式所示。
圖 3-4 PMDETA 之結構式
6. 甲基丙烯酸甲酯 ( methyl methacrylate, MMA),SHOWA,≥99%,直接使用, 如圖 3-5 結構式所示。
34
7. 偶氮二異丁腈 ( 2,2-azodiisobutyronitrile, AIBN ),UniRegion,直接使用。 8. 溴化亞銅 ( copper (I) bromide, CuBr),Sigma-Aldrich,直接使用。
9. 乙醇 ( Ethanol, EtOH ),ACS,≥99.5%,直接使用。 10. 甲醇 ( Methanol, MeOH ),ACS,99%,直接使用。
11. 氧化鋁粉 ( Aluminum oxide ),Sigma-Aldrich,直接使用。 12. 正己烷 ( n-Hexane ),ACS,直接使用,直接使用。
13. 鹽酸 ( Hydrochloric acid, HCl ),日本試藥 Japan,37%,直接使用。 14. 氫氧化鈉 ( Sodium hydroxide, NaOH ),ACS,95%,直接使用。 15. 丙酮 ( Acetone, CH3COCH3 ),工業用溶劑,直接使用。 16. 二氧化碳氣瓶,精上氣體公司,直接使用。 17. 氮氣氣瓶,精上氣體公司,直接使用。
3-2 實驗設備
1. 超音波震盪器 ( Ultrasonic Cleaner ) 型號:DC-80 代理商:明昱科技儀器有限公司 2. 真空烘箱 ( Vacuum oven ) 型號:DOV-30 代理商:明昱科技儀器有限公司 3. pH meter 型號:P25 代理商:明昱科技儀器有限公司 4. 離心機 型號: DC-400 代理商:明昱科技儀器有限公司35
5. 質子核磁共振光譜儀 ( Proton nuclear Magnetic Resonance,1H-NMR ) 型號: Varian® Unity Inova-500
儀器操作原理:核磁共振分析儀必須要將樣品放在強磁場下,某些特定 原子 核具自旋角動量造成的磁矩,磁場內的磁矩會選擇特定量化方向, 每方向皆 對應到特定能階,若磁矩和磁場反向對應能量較高,反之亦然。 當無線電波 頻率為能量差時,位於低能階的原子核會吸收能量,進到高能階,此改變自 旋方式現象稱核磁共振。
6. 紫外光/可見光光譜儀 ( Ultraviolet/visible spectroscopy, UV/Vis ) 廠商:Perkin Elmer
型號:Lambda-35
儀器操作原理:利用可見光及紫外光之燈管(Lamp)作為光源,將特定波 長之 光線射入樣品管,最後射入光電管中將光能轉換為電器訊號,藉由樣本及空 白水樣本間所吸收之光能量差,與標準液之能量吸收值比較。
7. 凝膠滲透層析儀 ( Gel Permeation Chromatography, GPC ) 廠商:Young Lin 型號:Acme 9000 儀器操作原理:GPC 的工作原理是利用固體粒子在流體內的擴散行為作為分 離的基礎,具有良好解析能力 ( High resolution ) 與高理論板數的分離管是構 成 GPC 良好分析能力 ( High performance ) 的要件。GPC 的分離管為 Polystyrene 和 divinylbenzene 共聚物膠體所填充而成,GPC 是利用它們的 「Effective size」來分離溶液中的分子。將溶解後的待測物注入流動相 ( mobile phase ),在流動相的推動下,待測物流經緊密填充在層析管柱裡數以 百萬計的大小孔洞,其中小分子的單元由於在孔洞內滯留時間較長,因此較 大分子的單元先流出層析管,由於這種時間差的產生,便形成分離的效果, 圖 3-6 所示。GPC 其定量方法是利用多種已知絕對分子量的聚苯乙烯標準品, 由分子量取對數與時間作圖,在已知待測物沖提時間的情形下,便可計算出 其對應分子量。
36 圖 3-6 GPC 層析管截面示意圖 8. 接觸角測量儀 ( contact angle )-表面張力測量(懸滴法) 廠商:欣創達科技有限公司 型號:Model 100SL 儀器操作原理:當液體自管口滴落時,液體的大小與液體的密度和表面張力 有關;落滴重量與管口半徑與液體表面張力有關。因此當界面兩相的密度差 已知時,可經由測量一懸滴的輪廓來獲得液體的表面張力。
9. 示差掃描熱卡分析儀 ( Differential Scanning Calorimeter, DSC ) 廠商:TA Instruments 型號:DSC-Q100 儀器操作原理:以量測樣品在特定的溫度及條件下,其吸熱及放熱情形,藉此可判 定材料的玻璃轉移溫度 ( Tg )、熔點 ( Tm )、結晶溫度、反應熱及比熱等,也 可進行動力學分析。當有 peak 產生時表示樣品具有吸熱或放熱情形,若是一 轉折代表為 Tg,表示比熱發生變化。
10. 熱重分析儀 ( Thermogravimetric analyzer, TGA ) 廠商:TA Instruments
型號:SDT-Q600
37
化,主要被用於測量材料熱穩定性及其組成。 11. 粒徑分析儀 (Particle Size Analyzer)
廠商:Brookhaven Instruments 型號:NanoBrook 90 Plus PALS
儀器操作原理:雷射光源照射於奈米粒子溶液時,粒子會使雷射光散射,藉 由觀察不同尺寸奈米粒子之布朗運動程度不同,其影響雷射光散射之程度不 同,計算出集體性的奈米尺寸與尺寸分布。
12. 界面電位分析儀 (Zeta Potential Analyzer) 廠商:Brookhaven Instruments
型號:NanoBrook 90Plus PALS
儀器操作原理:在毛細管兩側加一電場,帶電顆粒會往相反電極移動測量粒 子移動速度,藉由 Henry Equation 計算界面電位。當粒子平衡後,分散液與 分散粒子間電位差,其電位差越大越容易維持穩定懸浮狀態,電位差絕對值 『>30 mV 穩定分散;< 30 mV 系統不穩定,容易聚集;=0 等電位點(IEP) 』。 13. 冷場發射掃描式電子顯微鏡 ( Field emission scanning electron microscopy,
FE-SEM ) 廠商:HITACHI 型號:S-4800 儀器操作原理:電子鎗透過熱游離或是場發射原理產生高能電子束,經過電 磁透鏡組後,可以將電子束聚焦至試片上,利用掃瞄線圈偏折電子束,在試 片表面上做二度空間的掃描。 14. 定壓輸送幫浦及烘箱型高壓反應槽 廠商:玖容有限公司 儀器操作原理:先利用定壓輸送幫浦將二氧化碳自鋼瓶吸出,後將二氧化碳 打入反應釜內,似針筒的概念,重複動作可將壓力達到反應所需的壓力,輸 送二氧化碳的管線均含有逆止閥,可避免二氧化碳倒流回去。超臨界流體使 用的鋼瓶為液態二氧化碳氣瓶,因為內部有插管,因此可使氣瓶下方液態的 二氧化碳先出來,壓力夠容易加壓到指定壓力。
38
圖 3-7 scCO2的反應器裝置圖
3-3 實驗步驟
3-3-1 以 ATRP 聚合 PDMAEMA
由流程圖 3-8 所示,量取 CuBr ( catalyst )置入裝有 EtOH/H2O (1/1, V/V) 共 36 ml 溶劑之反應容器中,以磁石攪拌,在於反應容器外架設降溫裝置,降溫裝 置是使用液態氮使整個容器降溫,待反應容器內部溶劑完全結凍產生晶格排列, 排出溶劑中之氧氣。再以抽真空方式確定去除反應容器中多餘的氧氣後,通以氮 氣破真空解凍讓反應容器內的溶劑回到液體狀態,並重複冷凍-抽真空-解凍步驟 2 次。接著由血清塞處注入 PMDETA ( ligand ),並以磁石均勻攪拌。再重複冷凍 -抽真空-解凍循環 2 次,目的是為了確保反應容器內無任何的氧氣阻礙反應。再 由血清塞處注入 DMAEMA ( monomer ),並以磁石均勻攪拌,重複冷凍-抽真空-解凍循環 2 次。持續以磁石攪拌,將反應容器維持在低溫約 10 分鐘,避免開始 反應時速率太快。最後由血清塞處注入起始劑 MBIB 待溫度回到室溫開始反應 72 小時,聚合反應式如圖 3-9 所示。
39
3-3-1-1 PDMAEMA 之純化
將反應暴露於空氣中終止反應,接著利用氧化鋁粉過濾去除 Cu+ 與 PMDETA,過濾一次後,換新的氧化鋁粉並重複上述的步驟 1 次。再以迴旋濃縮 機去除大部分的溶劑後,倒入 150mL 正己烷純化去除未反應之 DMAEMA,以 傾析方式留下層高分子溶液,再倒入新的正己烷重複上述的步驟 2 次。最後收 集不溶物真空乾燥後取得產物,反應條件與結果顯示於表 3-1、表 3-2、表 3-3。 圖 3-8 以 ATRP 合成 PDMAEMA 之反應流程圖40 表 3-1 聚合高分子量 PDMAEMA ( h-PDMAEMA ) 反應條件及反應結果表 DMAEMA (monomer) MBIB (Initiator) CuBr (catalyst) PMDETA (Ligand) 莫耳比 100 0.5 1 2 實際進料量 (g) 14 0.08 0.13 0.31 產量 (g) 10.3 產率 (%) 73.5 表 3-2 聚合中分子量 PDMAEMA ( m-PDMAEMA ) 反應條件及反應結果表 DMAEMA (monomer) MBIB (Initiator) CuBr (catalyst) PMDETA (Ligand) 莫耳比 100 1 1 2 實際進料量 (g) 14 0.16 0.13 0.31 產量 (g) 10.5 產率 (%) 75 表 3-3 聚合低分子量 PDMAEMA ( l-PDMAEMA ) 反應條件及反應結果表 DMAEMA (monomer) MBIB (Initiator) CuBr (catalyst) PMDETA (Ligand) 莫耳比 100 2 1 2 實際進料量 (g) 14 0.32 0.13 0.31 產量 (g) 11.2 產率 (%) 80 產率% = (反應生成物之重量/反應前之反應物重量) x 100%
41
3-3-2 CS-g-PDMAEMA 之合成及純化
由流程圖 3-10 所示,取定量 CS (分別有低分子量、高分子量) 與 PDMAEMA 置入反應容器中,溶劑為去離子水,以兩種不同催化劑(分別是醋酸、鹽酸) 調整 其 pH 值 ( 醋酸為 pH 4、鹽酸為 pH 2 ) 使 CS 全溶,油浴控溫 55℃以磁石攪拌 反應 3 天,聚合反應式如圖 3-11 所示。 以降溫方式終止反應,再以離心機離心使未反應之 CS 沉澱,取其澄清液, 再以透析法透析 2 天,分離未反應之 PDMAEMA 與產物 CS-g-PDMAEMA,最 後經過真空乾燥取得最終產物,反應條件與結果顯示於表 3-4、3-5、3-6、3-7。 圖 3-10 以醯化反應合成 CS-g-PDMAEMA 之反應流程圖42 圖 3-11 以醋酸/鹽酸當催化劑,醯化反應接枝 CS-g-PDMAEMA 表 3-4 聚合 CS-g-PDMAEMA( low MW CS, HCl )之反應條件 一個 CS 重複單位 PDMAEMA 分子量 (g/mol) 161.2 14600 莫耳比 1 1 實際進料量 (g) 0.013 1 產量 (g) 0.18 產率 (%) 19
43
表 3-5 聚合 CS-g-PDMAEMA( low MW CS, CH3COOH )之反應條件 一個 CS 重複單位 PDMAEMA 分子量 (g/mol) 161.2 14600 莫耳比 1 1 實際進料量 (g) 0.013 1 產量 (g) 0.17 產率 (%) 18 表 3-6 聚合 CS-g-PDMAEMA( high MW CS, HCl )之反應條件 一個 CS 重複單位 PDMAEMA 分子量 (g/mol) 161.2 14600 莫耳比 1 1 實際進料量 (g) 0.01 1 產量 (g) 0.3 產率 (%) 30
表 3-7 聚合 CS-g-PDMAEMA( high MW CS, CH3COOH )之反應條件 一個 CS 重複單位 PDMAEMA 分子量 (g/mol) 161.2 14600 莫耳比 1 1 實際進料量 (g) 0.01 1 產量 (g) 0.4 產率 (%) 40
3-3-3 在 scCO
2下合成 CS-g-PDMAEMA
由流程圖 3-12 所示,取定量 CS、PDMAEMA 置於瘦高型反應瓶 ( 內徑 14 mm × 高度 52 mm,容積 7mL ),溶劑為去離子水,以兩種不同催化劑 ( 醋酸、 鹽酸 ) 調整其 pH 值 ( 醋酸為 pH 4、鹽酸為 pH 2 ),以超音波震盪形成均一相 後,將反應瓶放入高壓反應釜,25℃、4000 psi 反應 4 小時,其反應條件與結果 顯示於表 3-8、3-9、3-10。待反應結束,數分鐘內洩壓完成,反應即告終止。將44
產物純化,再進行真空乾燥後,得到產物 CS-g-PDMAEMA。
圖 3-12 在 ScCO2下合成 CS-g-PDMAEMA 之反應流程圖
表 3-8 聚合 CS-g-PDMAEMA ( ScCO2, no catalyst ) 之反應條件 一個 CS 重複單位 PDMAEMA 分子量 (g/mol) 161.2 21500 莫耳比 1 1 實際進料量 (g) 0.005 0.5 產量 (g) 0.03 產率 (%) 6 表 3-9 聚合 CS-g-PDMAEMA ( ScCO2, HCl ) 之反應條件 一個 CS 重複單位 PDMAEMA 分子量 (g/mol) 161.2 21500 莫耳比 1 1 實際進料量 (g) 0.005 0.5 產量 (g) 0.11 產率 (%) 21.7