國立高雄大學化學工程及材料工程學系
碩士論文
奈米碳管作為聚氯乙烯熱安定劑之研究
Carbon nanotubes used as a thermal stabilizer for
poly(vinyl chloride)
研究生:謝凱筑 撰
指導教授:謝永堂 教授
謝誌
在這碩士生涯的兩年,對於研究的努力與辛酸歷歷在目,從失敗與錯誤中 不斷的學習,成長了許多,也有很深刻的體會。首先,要感謝我的指導教授謝 永堂教授,在教學及實驗研究上對我的幫助及教導,還有對生活上的關心,讓 我在待人處事及研究思考方面等等都成長許多,衷心感謝謝永堂教授對我的指 導與勉勵,以及給予學習上寶貴的建議和解惑,在此深表感謝。 感謝在這兩年中許多人的照顧和幫助,謝謝亞貞姐和怡雅姐在行政事務上 的所有幫助,非常感謝我的好朋友妍慈,不管是生活或學業上對我一切的關心、 支持和幫助,成為我碩士生涯中的精神支柱,分享我所有的心情,也很開心一 起面對了許多難關,一同努力直到畢業,也謝謝子豪在實驗上所有的幫助和支 持,還有在烈日中幫忙跑腿買點心等等,還有感謝學姐江昀真給予我生活和實 驗上的許多建議和鼓勵,且安撫我的情緒,也謝謝芳滋和佩儀對我的鼓勵和幫 忙,謝謝周廷宇和陳彥橋在我碩一的實驗室生活中增添許多歡笑,使實驗室氣 氛更加的融洽,也謝謝珮羽和曜銓在實驗室事務上的幫忙,由衷感謝實驗室所 有成員和我在實驗室一起分擔所有大小事,且暢所欲言盡情歡笑,讓我在實驗 室的生活有許多快樂時光。最後,感謝一同努力奮鬥的碩士班同學們,在撰寫 論文及實驗的過程中互相加油打氣與扶持,也很開心與大家一起出去聚餐、唱 歌和出遊的日子,其中,感謝龔恩正在實驗及論文上給予我許多建議和幫助, 也謝謝謝泓諭、吳逸莒、范逸昇、郭家佑和吳孟諺在實驗上的幫忙和生活上帶 來的歡樂。 最重要的是感謝我的家人,默默給我支持與鼓勵,也謝謝他們對我的包容, 甚至勉勵我增加我的信心,讓我能夠順利完成學業。最後,謝謝所有幫助過我 的人,替我的碩士生活增添許多色彩,增加許多笑與淚。 謝凱筑 謹致於國立高雄大學 中華民國 105 年 7 月目錄
第一章 前言 ... 1 1.1 聚氯乙烯 ... 1 1.1.1 聚氯乙烯結構與性質 ... 1 1.1.2 聚氯乙烯的聚合方法 ... 2 1.1.3 聚氯乙烯之熱裂解 ... 3 1.1.4 聚氯乙烯之裂解形式 ... 5 1.2 塑化劑 ... 7 1.3 熱安定劑 ... 8 1.3.1 熱安定劑之作用機制 ... 9 1.3.2 熱安定劑的種類 ... 9 1.4 自由基(free radicals) ... 12 1.5 奈米碳管 ... 13 1.5.1 奈米碳管之結構 ... 13 1.5.2 奈米碳管之特性 ... 14 1.5.3 奈米碳管吸收自由基之特性 ... 16 1.6 奈米碳管之製備 ... 16 1.6.1 奈米碳管之官能基化改質 ... 17 1.6.2 奈米碳管之酸處理改質 ... 18 第二章 文獻回顧 ... 19 2.1 奈米碳管吸收自由基之性質 ... 19 2.2 聚氯乙烯之熱安定化 ... 27 2.3 研究動機 ... 38 第三章 實驗內容 ... 39 3.1 實驗藥品 ... 39 3.2 實驗設備 ... 40 3.3 實驗材料與樣品之製備 ... 41 3.4 實驗步驟及流程 ... 44 3.4.1 純 PVC 和添加各種類碳管之 PVC 薄膜之加熱加速老化試驗 ... 44 3.4.2 以 FE-SEM 鑑定碳管表面形貌 ... 45 3.4.3 以 DSC 測定 PVC 玻璃轉移溫度 ... 45 3.4.4 以 TGA 測定 PVC 熱裂解溫度 ... 45 3.4.5 以 UV 測定 PVC 共軛雙鍵之生成 ... 46 3.4.6 以 FTIR 測定 PVC 熱裂解之官能基 ... 463.4.7 以 Congo Red Test 測量 PVC 熱安定化時間 ... 46
3.4.8 以 pH meter 測量 pH 值(PVC dehydrochlorination test) ... 47
3.4.9 以 GPC 測定分子量 ... 47 第四章 結果與討論 ... 48 4.1 材料之鑑定分析 ... 48 4.1.1 奈米碳管 ... 48 4.1.1.1 SEM ... 48 4.1.1.2 Raman ... 51 4.1.2 聚氯乙烯 ... 53 4.1.2.1 FTIR ... 53 4.1.2.2 DSC ... 55 4.1.2.3 TGA ... 56 4.2 奈米碳管對聚氯乙烯熱老化所生成雙鍵之影響 ... 57 4.2.1 FTIR 光譜分析 ... 57 4.2.2 以數位影像方式紀錄聚氯乙烯之顏色變化 ... 65 4.2.3 UV-vis 光譜分析 ... 68 4.2.3.1 CNT 添加量對抗老化程度之比較 ... 69 4.2.3.2 bmCNT 添加量對抗老化程度之比較 ... 72 4.2.3.3 CNT-COOH 添加量對抗老化程度之比較 ... 75 4.2.3.4 碳管種類對聚氯乙烯抗老化程度之比較 ... 77 4.3 奈米碳管對聚氯乙烯熱老化之脫氯化氫的影響 ... 80
4.3.1 Congo Red Test(剛果紅試驗) ... 80
4.3.2 Dehydrochlorination test (去氯化氫試驗) ... 83
4.4 GPC ... 86
4.5 TGA ... 91
第五章 結論 ... 94
表目錄
表 2-1 ID/IG ratios obtained from Raman spectra and atomic compositions(%) of C and obtained from EDS for various modified CNT ... 25 表 2-2 UV/Vis absorbance of DPPH at λmax 517 nm at day10 in MeOH solutions
containing various modified CNT ... 27 表 2-3 Comparison of effects of different LTSs on thermal stability of PVC
compounds. ... 36 表 4-1 PVC 之 peak 分析 ... 54 表 4-2 GPC 測定純 PVC、1 phr CNT/PVC、1 phr bmCNT/PVC 和 1 phr CNT-COOH/PVC 經 180 ℃不同加熱老化時間(0, 30, 60, 120, 180 min)後 之 Mw、Mn 和 PDI ... 89 表 4-3 TGA 測定純 PVC、1 phr CNT/PVC、1 phr bmCNT/PVC 和 1 phr CNT-COOH/PVC 薄膜之兩階段重量損失(%)和 700 ℃殘存量(%) ... 93 表 4-4 TGA 測定純 PVC、1 phr CNT/PVC、1 phr bmCNT/PVC 和 1 phr CNT-COOH/PVC 薄膜之兩階段熱裂解溫度(T1, T2 (℃))和熱裂解速率 (DR1, DR2 (%/℃)) ... 93
圖目錄
圖 1-1 PVC 的合成 ... 1
圖 1-2 各類型氯結構 ... 3
圖 1-3 PVC 鏈段間 Diels Alder condensation ... 4
圖 1-4 PVC 內部苯的產生 ... 4 圖 1-5 PVC 之自由基裂解機制 ... 5 圖 1-6 PVC 之離子型裂解機制 ... 6 圖 1-7 PVC 之自動氧化機制 ... 6 圖 1-8 鄰苯二甲酸酯之結構 ... 8 圖 1-9 有機錫與氯化氫反應 ... 10 圖 1-10 有機錫取代不穩定氯 ... 11 圖 1-11 硫基化合物與 PVC 作用 ... 11 圖 1-12 環氧基團與氯化氫反應 ... 12 圖 1-13 環氧基團與 PVC 鍵結 ... 12 圖 1-14 (a)單層奈米碳管, (b)多層奈米碳管 ... 14 圖 1-15 因不同捲曲方式所造成的碳管螺旋性 ... 15 圖 1-16 化學氣相沉積法製備奈米碳管示意圖 ... 16 圖 1-17 奈米碳管典型的表面缺陷位置 ... 18
圖 2-1 Temperature ramped chemiluminescence curves in O2 for pure PS and PS-nanotube composites ... 20
圖 2-2 Thermogravimetric analysis of pure PVDF and PVDF-BCNT composites . 20 圖 2-3 Evaluation of OIT by DSC ... 21
圖 2-4 Evaluation of OIt at required temperature by DSC (a) 180 ℃, (b) 190 ℃, (c) 200 ℃ ... 22
圖 2-5 Dependence of OIt on MWCNT-OH concentration at 180 ℃ ... 22
圖 2-6 Generation of hydroxyl radicals by the Fenton reaction in the presence of different kinds of CNTs (a) Blank, (b) SWCNTs, (c) MWCNTs, (d) MWCNTs-OH. ... 23
圖 2-7 General scheme of polyolefin thermal oxidation in the presence of CNTs .. 24
圖 2-8 EPR spectra of OH· radicals in (a) DMPO/OH·, (b) DMPO/OH·/CNT, (c) DMPO/OH·/bmCNT, (d) DMPO/OH·/mw10CNT, (e) DMPO/OH·/mw20CNT, (f) DMPO/OH·/mw30CNT, (g) DMPO/OH·/bpoCNT, (h) DMPO/OH·/CNT-COOH... 26
圖 2-9 UV/Vis spectra taken at day 10 for DPPH in MeOH solutions containing 4 mg of nanotubes for (a) DPPH/MeOH, (b) DPPH/MeOH/CNT, (c)
DPPH/MeOH/mw30CNT, (d) DPPH/MeOH/mw20CNT, (e) DPPH/MeOH/bpoCNT, (f) DPPH/MeOH/bmCNT, (g)
DPPH/MeOH/mw10CNT, (h) DPPH/MeOH/CNT-COOH ... 26
圖 2-10 Schematic of the device for Congo red test ... 28
圖 2-11 Congo red tests of PVC samples in the presence of various stabilizers ... 28
圖 2-12 Discoloration of PVC samples as a function of degradation time, heated at 185 ℃. ... 29
圖 2-13 UV spectra of PVC samples. Formulation a: PVC 100 phr, CaSt2/ZnSt2 2.5 phr; Formulation b: PVC 100 phr, CaSt2/ZnSt2 2.5 phr, organic tin 0.2 phr.30 圖 2-14 FTIR spectra of neat PVC during the whole accelerated weathering test. . 31
圖 2-15 FTIR spectra of neat PVC and stabilizer-doped PVC after 50 days’ accelerated weathering test. ... 32
圖 2-16 Thermal stability time of PVC, PVC/LDH, PVC/BP and PVC/LDH-BP measured by Congo Red test. ... 32
圖 2-17 Color evolution, as a function of time, of PVC samples heated at 180 ℃. 34 圖 2-18 UV-VIS spectra of PVC samples stabilized with different thermal stabilizers heated at 180 ℃ for 0 min. (a) La-PE/ZnSt2 ... 34
圖 2-19 UV-VIS spectra of PVC samples stabilized with different thermal stabilizers heated at 180 ℃for 120 min. (a) La-PE/ZnSt2 ... 35
圖 2-20 DHC of PVC compounds stabilized with different LTSs. ... 36
圖 2-21 TGA traces in air for the PVC-LDH composites. ... 37
圖 3-1 酸處理改質奈米碳管之流程圖 ... 42
圖 3-2 試片製備之流程圖 ... 43
圖 3-3 本實驗所使用之分析方法 ... 44
圖 3-4 樣品加熱老化試驗之示意圖 ... 45
圖 3-5 Congo Red Test 裝置之示意圖 ... 46
圖 3-6 PVC 加熱去氯化氫試驗之裝置示意圖 ... 47
圖 4-1 CNT 在不同放大倍率下之 SEM 顯微圖(a) 20 k, (b) 50 k, (c) 100 k ... 49
圖 4-2 bmCNT 在不同放大倍率下之 SEM 顯微圖(a) 20 k, (b) 50 k, (c) 100 k ... 49
圖 4-3 CNT-COOH 在不同放大倍率下之 SEM 顯微圖(a) 20 k, (b) 50 k, (c) 100 k50 圖 4-4 各種表面改質之奈米碳管(a) CNT, (b) bmCNT, (c) CNT-COOH 在 100 k 倍率下之 SEM 顯微圖 ... 50
圖 4-5 各種類碳管之 Raman 光譜圖(A) CNT, (B) bmCNT, (C) CNT-COOH,所計 算之(D) ID/IG值 ... 52 圖 4-6 純 PVC 之 FTIR 光譜圖 ... 54 圖 4-7 純 PVC 之 DSC 第二次升溫曲線圖 ... 55 圖 4-8 純 PVC 之 TGA 升溫(20 ℃/min)曲線圖 ... 56 圖 4-9 (a) 純 PVC, (b) 0.1 phr CNT/PVC, (c) 0.1 phr bmCNT/PVC, (d) 0.1 phr CNT-COOH/PVC 之薄膜於 180 ℃加熱老化試驗前之 FTIR 光譜圖 .... 59 圖 4-10 純 PVC 薄膜經 180 ℃加熱老化(a) 0 h, (b) 8 h, (c) 24 h 後之 FTIR 光譜 圖 ... 60 圖 4-11 0.1 phr CNT/PVC 薄膜經 180 ℃加熱老化(a) 0 h, (b) 8 h, (c) 24 h, (d) 48 h 後之 FTIR 光譜圖 ... 61 圖 4-12 0.1 phr bmCNT/PVC 薄膜經 180 ℃加熱老化(a) 0 h, (b) 8 h, (c) 24 h, (d) 48 h, (e) 72 h 後之 FTIR 光譜圖 ... 62 圖 4-13 0.1 phr CNT-COOH/PVC 薄膜經 180 ℃加熱老化(a) 0 h, (b) 8 h, (c) 24 h 後之 FTIR 光譜圖 ... 63 圖 4-14 (a) 純 PVC, (b) 0.1 phr CNT/PVC, (c) 0.1 phr bmCNT/PVC, (d) 0.1 phr CNT-COOH/PVC 薄膜經 180 ℃不同加熱老化時間後出現烯類結構特 徵峰(3017 cm-1 )之 FTIR 光譜圖 ... 64 圖 4-15 純 PVC、0.1 phr CNT/PVC、0.1 phr bmCNT/PVC 和 0.1 phr CNT-COOH/PVC 薄膜於 180 ℃不同加熱老化時間(0, 10, 30, 60, 90, 120 min)後溶於 THF(40 mg/15 mL)之溶液之數位影像 ... 66 圖 4-16 純 PVC、0.3 phr CNT/PVC、0.3 phr bmCNT/PVC 和 0.3 phr CNT-COOH/PVC 薄膜於 180 ℃不同加熱老化時間(0, 10, 30, 60, 90, 120 min)後溶於 THF(40 mg/50 mL)之溶液之數位影像 ... 67
圖 4-17 純 PVC 經 180 ℃加熱老化(a) 0 min, (b) 10 min, (c) 30 min, (d) 60 min, (e) 90 min, (f) 120 min 後溶於 THF(40 mg/15 mL)之溶液之 UV-vis 光譜圖69 圖 4-18 (A) 0.1 phr CNT/PVC,(B) 0.3 phr CNT/PVC 經 180 ℃加熱老化(a) 0 min, (b) 10 min, (c) 30 min, (d) 60 min, (e) 90 min, (f) 120 min 後溶於 THF(40 mg/15 mL)之溶液之 UV-vis 光譜圖 ... 70
圖 4-19 經 180 ℃加熱老化(A) 30 min, (B) 60 min, (C) 90 min, (D) 120 min 後之 (a) 純 PVC, (b) 0.1 phr CNT/PVC, (c) 0.3 phr CNT/PVC 溶於 THF(40 mg/15 mL)之溶液之 UV-vis 光譜圖 ... 71
圖 4-20 (A) 0.1 phr bmCNT/PVC, (B) 0.3 phr bmCNT/PVC 經 180 ℃加熱老化(a) 0 min, (b) 10 min, (c) 30 min, (d) 60 min, (e) 90min, (f) 120 min 後溶於 THF(40 mg/15 mL)之溶液之 UV-vis 光譜圖... 73 圖 4-21 經 180 ℃加熱老化(A) 30 min, (B) 60 min, (C) 90 min, (D) 120 min 之(a) 純 PVC, (b) 0.1 phr bmCNT/PVC, (c) 0.3 phr bmCNT/PVC 溶於 THF(40 mg/15 mL)之溶液之 UV-vis 光譜圖 ... 74 圖 4-22 (A) 0.1 phr CNT-COOH/PVC, (B) 0.3 phr CNT-COOH/PVC 經 180 ℃加
熱老化(a) 0 min, (b) 10 min, (c) 30 min, (d) 60 min, (e) 90min, (f) 120 min 後溶於 THF(40 mg/15 mL)之溶液之 UV-vis 光譜圖 ... 75 圖 4-23 經 180 ℃加熱老化(A) 30 min, (B) 60 min, (C) 90 min, (D) 120 min 之(a) 純 PVC, (b) 0.1 phr CNT-COOH/PVC, (c) 0.3 phr CNT-COOH/PVC 溶於 THF(40 mg/15 mL)之溶液之 UV-vis 光譜圖... 76 圖 4-24 (a) 純 PVC, (b) 0.1 phr CNT-COOH/PVC, (c) 0.1 phr CNT/PVC, (d) 0.1
phr bmCNT/PVC 於 180 ℃加熱老化(A) 60 min, (B) 90 min, (C) 120 min 後溶於 THF(40 mg/15 mL)之溶液之 UV-vis 光譜圖 ... 78 圖 4-25 (a) 純 PVC, (b) 0.3 phr CNT-COOH/PVC, (c) 0.3 phr CNT/PVC, (d) 0.3
phr bmCNT/PVC 於 180 ℃加熱老化(A) 60 min, (B) 90 min, (C) 120 min 後溶於 THF(40 mg/15 mL)之溶液之 UV-vis 光譜圖 ... 79 圖 4-26 添加不同劑量(A) CNT, (B) bmCNT, (C) CNT-COOH, (D)各種碳管於
PVC 進行剛果紅試驗之測定結果 ... 82 圖 4-27 純 PVC 和不同比例之 CNT/PVC、bmCNT/PVC 和 CNT-COOH/PVC 經
180℃加熱老化(A) 30 min, (B) 60 min, (C) 90 min, (D) 120 min 之
Dehydrochlorination test 測定結果 ... 85 圖 4-28 (A) 純 PVC, (B) 1 phr CNT/PVC, (C) 1 phr bmCNT/PVC, (D) 1 phr
CNT-COOH/PVC 經 180 ℃加熱老化(a) 0 min, (b) 30 min, (c) 60 min, (d) 120 min, (e) 180 min 後之 GPC 測定 ... 88 圖 4-29 GPC 測定純 PVC、1 phr CNT/PVC、1 phr bmCNT/PVC 和 1 phr
CNT-COOH/PVC 經 180 ℃不同加熱老化時間(0, 30, 60, 120, 180 min) 後之(A) Log Mw, (B) Log Mn, (C) PDI ... 90 圖 4-30 (a) 純 PVC, (b) 1 phr CNT/PVC, (c) 1 phr CNT-COOH/PVC, (d) 1 phr
奈米碳管作為聚氯乙烯熱安定劑之研究
指導教授:謝永堂 教授 國立高雄大學 化學工程及材料工程學系 碩士班 學生:謝凱筑摘要
本研究以 solvent-casting 法製備 PVC 及添加不同劑量之奈米碳管(CNT)、 球磨奈米碳管(bmCNT)、酸處理奈米碳管(CNT-COOH)於 PVC 之薄膜中,在 氮氣下以 180 ℃油浴恆溫,對薄膜進行加熱加速老化試驗。以 FTIR、數位影 像(樣品顏色變化)和 UV-vis 進行薄膜加熱老化前後之測定分析,調查奈米碳管 種類及添加量對 PVC 熱安定性之影響。實驗結果發現添加適量(0.1 phr 或 0.3 phr)奈米碳管能抑制 PVC 熱裂解,延緩 PVC 形成共軛多烯結構(CH=CH)n之速 度,因而達到抗老化效果;碳管表面缺陷含量與 COOH 基團對 PVC 之抗老化 程度有不同的表現,當缺陷含量增加時,因其清除自由基能力增加,有較佳的 抗老化效果,而酸處理奈米碳管因有 COOH 基團之酸催化作用,則有促進 PVC 熱裂解之效果。本研究也利用剛果紅試驗(Congo Red test)和去氯化氫試驗 (Dehydrochlorination test)調查 PVC 熱裂解脫去氯化氫與碳管種類及添加量之 相依性,發現各種奈米碳管在 PVC 短期加熱(30 min)下皆有催化 PVC 脫氯化 氫之效果,但在長期加熱(120 min)下則有抑制 PVC 釋放氯化氫之效果,而 bmCNT 及 CNT-COOH 對 PVC 熱安定性最佳化(氯化氫釋放量最少)之添加量 為 1 phr。本研究也由 TGA 之動態升溫過程,發現添加 1 phr 各種奈米碳管具 有安定 PVC 第一階段熱裂解之情形。最後,以 GPC 測定分析調查各種奈米碳 管於添加 1 phr 時,對 PVC 熱安定性之影響,可知短期加熱(1 h)下皆有催化 PVC 熱裂解,降低分子量的效果,但在長期加熱(2 h)下則有熱安定化 PVC 上 之自由基,促進交聯反應,分子量上升之效果。 關鍵字:奈米碳管、自由基、聚氯乙烯、熱安定性、安定劑Carbon nanotubes used as a thermal stabilizer for
poly(vinyl chloride)
Yeong-Tarng Shieh, Kai-Chu Hsieh
Department of Chemical and Materials Engineering, National University of Kaohsiung
ABSTRACT
The as-prepared multiwalled carbon nanotubes (CNT), ball-milled CNT (bmCNT), and acid-treated CNT (CNT-COOH) were comparatively investigated on their use as a thermal stabilizer in poly(vinyl chloride)(PVC) in this study. Films of pure PVC and CNT/PVC composites that were cast from THF were subjected to thermal aging in N2 in a test tube in an oil bath controlled at 180 oC for a certain time. FTIR, UV-vis, discoloration of aged PVC samples containing different types of CNT of different amounts were measured as a function of aging time to investigate stabilizing effects of nanotubes. Experimental results revealed that the addition of nanotubes of a small amount (0.1 phr or 0.3 phr) could effectively stabilize the PVC thermal degradation because the formation rate of conjugated polyene structure was clearly lowered. Surface defects on nanotubes and COOH groups on CNT-COOH appeared to give different effects on PVC thermal stabilization which was found to increase with contents of the defects but decrease with contents of COOH groups. Moreover, Congo red test and dehydrochlorination test were also performed to investigate the dependency of the HCl removal during thermal aging on the type and content of nanotubes. It was found that all three types of nanotubes could catalyze the thermal degradation of PVC in an initial 30 min of thermal aging but stabilize the degradation in a long time (120 min) of aging. The optimal amount of bmCNT and CNT-COOH that exhibited stabilizing effects was 1 phr which was consistent with TGA data. GPC data found that the nanotubes of 1 phr addition could catalyze PVC thermal degradation in the first hour resulting in a decrease in molecular weight of PVC but could stabilize the degradation in the second hour resulting in an increase in molecular weight of PVC.
Keywords: Carbon nanotubes, free radicals, poly(vinyl chloride), thermal stability,
第一章
前言
1.1 聚氯乙烯
聚氯乙烯在 1835 年和 1872 年分別被 Henri Victor Regnault 及 Eugen Baumann 發現,他們觀察到在陽光照射下燒杯中的白色固體為氯乙烯。1912 年德國化學家 Fritz Klatte 及 1926 年 Waldo Semon 皆合成了聚氯乙烯,1926 年 Waldo Semon 及 B. F. Goodric 公司開發出利用加入塑化劑,使聚氯乙烯達到塑 化之方法,因此使得聚氯乙烯更柔韌有利於加工,並且具有商業價值而得到廣 泛的應用。1930 年起,使用鄰苯二甲酸酯使聚氯乙烯塑化,並於德國和美國 商業化生產聚氯乙烯。
1.1.1 聚氯乙烯結構與性質
聚氯乙烯(poly(vinyl chloride),PVC),是一種使用一個氯原子來取代聚乙 烯中的一個氫原子的高分子材料,經由氯乙烯單體(vinyl chloride monomer,
VCM)自由基聚合而成,也可以藉由乙炔與氯化氫反應而得,如圖 1-1 所示。 就 結 構 上 而 言 , PVC 其 分 子 鏈 上 的 排 列 方 式 大 部 分 都 是 以 頭 尾 相 接 (-CH2-CHCl-CH2-CHCl-),在每條分子鏈上大約有 15~20 個左右的支鏈,PVC 立體結構是屬於無規則型立體結構,但因為分子鏈上的氯、氫原子的空間排列 為基本無序,因此使得 PVC 結晶度低,一般只有 5~15%。[1]
PVC 為世界上產量第三大的塑料品種,僅次於聚乙烯與聚丙烯,相較於傳 統材料像是銅、鐵或是木製管材和型材的應用,PVC 在建築上的應用較為多功 能性且具有成本效益,因為 PVC 本身為硬質塑料,可藉由塑化劑的添加使材 料更加柔軟且具有彈性,塑化劑中最廣泛應用的就是鄰苯二甲酸酯(phthalates), 常用於服飾、室內裝潢、電線絕緣材料和充氣產品,以及可以取代橡膠的其他 應用。 純 PVC 是一種白色脆性固體,不溶於醇類,微溶於四氫呋喃。PVC 可以 抵抗水與火這兩種性質完全不同的物質,由於具有防水性,因此可以製成雨衣、 浴簾及水管等產品;就其阻燃性而言,PVC 結構中含有氯,故在燃燒時氯原子 會被釋放,抑制燃燒。[1] 數以千計以 PVC 為基礎的硬質、半硬質和軟質的材料已長時間持續地廣 泛應用於全世界,在 2000 年因為開發了新的用途與市場,就產量估計而言, 全世界所生產的 PVC 從幾百億英鎊增長至 440 億英鎊,然而,由於 PVC 的熱 穩定性差,在升溫過程中因熱裂解釋放出氯化氫而加速了裂解的過程,形成具 有共軛雙鍵的多烯結構,而共軛雙鍵數目的多寡造成 PVC 發生顏色變化,由 黃、橘、咖啡最後甚至是黑色。從 PVC 主幹所斷裂的氯化氫會影響高分子的 物理、化學和機械性質,直到熱安定劑被發現以前,PVC 在工業上並不是常用 的聚合物,因為它不能在高溫下進行加工製造程序,然而,隨著安定劑和潤滑 劑技術有重大的進步,使得壓製和注塑成型機械及壓製印模設計也有一定程度 的進展,因而提高了 PVC 噸位的生產與使用率。[2]
1.1.2 聚氯乙烯的聚合方法
生產聚氯乙烯的聚合方法通常有四種,分別是懸浮聚合、本體聚合、乳液 聚合、與溶液聚合,其中以懸浮聚合為主。 1.懸浮聚合(Suspension Polymerization):在攪拌和分散劑的作用下,單體會分 散成液滴狀懸浮在水中聚合,聚合結束後經汽提脫除殘留單體而得到成品。聚 合時為了保證得到所需要的分子量和分子量分布範圍並防止爆聚,必須控制溫 度和壓力。由於此種聚合方法是以水作為分散介質,可有效的控制反應熱的導 出,但因為可變因素很多,包括溫度、催化劑、分散劑、表面活性劑的用量、 攪拌速率和冷卻速率,因此需要控制自動化的設備來生產,才能有效控制品 質。 2.本體聚合(Bulk Polymerization):一般採用兩段法生產,第一階段使用少量 高活性引發劑使聚合進行到 7~9%轉化率,此階段形成一定形狀的顆粒骨架, 並保留活性中心,第二階段再加入與預聚物等量的單體,繼續進行聚合,聚合 結束後再脫去殘留單體即可獲得成品。此種方法聚合而成的聚氯乙烯純度比較 高,質量也比較優,透明性高,熱安定性佳,結構規則均勻,顆粒大小均一,加工的性能良好,而且在過程中不需要用到水,因此省去乾燥的步驟降低了加 工成本。 3.乳液聚合(Emulsion Polymerization):氯乙烯單體在乳化劑作用下,使單體 分散於水中形成乳液狀,乳化劑通常為陰離子或是非陰離子型的界面活性劑, 再利用水溶性的誘發劑來引發產生聚合,聚合結束後脫除單體後經乾燥可得粉 狀成品。此種聚合法所生產的聚氯乙烯表面殘留的界面活性劑較多,所以電絕 緣性較差。 4.溶液聚合(Solution Polymerization):將氯乙烯單體加入溶劑中進行聚合,但 因溶液中的聚氯乙烯不溶於溶劑,所以會不斷地析出。此種聚合方法聚氯乙烯 所含的雜質較少,分子量較低,由於反應過程中會使用大量溶劑,使得生產成 本較高。[3][4]
1.1.3 聚氯乙烯之熱裂解
聚氯乙烯相較於其他聚合物而言,其熱穩定性較差,因為 PVC 結構中的 C-Cl 鍵鍵能弱,容易受熱發生斷鍵因而產生自由基,Cl 自由基會抓走相鄰碳 上之氫原子,因而脫去氯化氫,造成 PVC 熱裂解,然而,PVC 在製造的過程 中會產生一些結構上的缺陷,生成不穩定的氯結構,如圖 1-2 所示,其內部烯 丙基氯的結構最不穩定,其次是三級碳氯,接著是末端的烯丙基氯,最穩定的 是氯乙烯結構,由於這些缺陷結構的存在誘導了 PVC 的分解溫度降低,加速 引發 PVC 之熱裂解。 圖 1-2 各類型氯結構Nandini Chatterjee 等人[5]利用 DTA、DSC、TG 對 PVC 進行熱裂解分析, 將聚氯乙烯熱裂解分為以下四個階段:
(2)第二階段:在 185~375 ℃,此為 PVC 裂解的主要階段,大量的含氯鏈段在 吸收充足的能量後會開始脫去氯化氫,並且在主鏈上生成一些多烯烴鏈段 (polyene sequence),隨著加熱時間越久,多烯烴的含量也越來越多,Troitskii 等人[6]利用動力學計算發現,氯化氫的濃度會影響整個降解動力學,當氯化氫 濃度越高,聚氯乙烯降解速率就越快,而氯化氫的濃度主要是取決與在 PVC 之中的溶解度以及從 PVC 遷移的速率。 (3)第三階段:在 375~500 ℃,此階段的多烯烴達到一定的含量,因此產生了 一些交聯或芳香族的反應,如圖 1-3 Diels Alder condensation,反應產生了環狀 烯烴,如圖 1-4 所示,產生苯且主鏈會逐漸變小。
圖 1-3 PVC 鏈段間 Diels Alder condensation[1]
圖 1-4 PVC 內部苯的產生[1]
(4)第四階段:在 500 ℃以上,在此階段 PVC 失去了原先的物理性質,化學結 構也大不相同,機械性能完全下降,原因是在加熱時使得 PVC 的主鏈斷裂, 導致整個分子結構的崩解。
1.1.4 聚氯乙烯之裂解形式
聚氯乙烯的裂解形式可大致分為下列三種: 1.脫氯化氫:此部分可分為自由基型與離子型。 (1)自由基型:Winkler 等人[7]提出自由基型機制,如圖 1-5 所示,PVC 在加熱 過程中產生的活性自由基攻擊亞甲基,使得主鏈產生自由基結構,進而脫去氯 離子,在主鏈上形成雙鍵,氯離子在捕捉主鏈上的氫,主鏈上再度帶有自由基 結構,使得反應持續進行,形成一種自由基連鎖反應。 圖 1-5 PVC 之自由基裂解機制[7] (2)離子型:如圖 1-6 所示,首先 C-Cl 鍵先斷鍵,形成氯離子以及碳陽離子, 氯離子會抓住碳陽離子旁的氫形成氯化氫,同時在主鏈上形成雙鍵,而主鏈上 的 C-Cl 會不斷的重複此步驟,產生更多的雙鍵,也就是連鎖反應。[8]圖 1-6 PVC 之離子型裂解機制[8] 2.自動氧化:如圖 1-7 所示,由 Gupta 等人[9]提出。
3.剪切力作用:PVC 在加工過程中會受到壓延、擠出等影響,承受相當大的剪 切力作用,使得 PVC 中的反應基團碰撞機率增加,因而導致裂解,而且受到 剪切力作用會使 PVC 之 C-C 鍵產生斷裂生成自由基,加速熱裂解反應。
1.2 塑化劑
塑化劑是一種低分子量非揮發性化合物,廣泛應用於高分子工業中做為添 加劑,其扮演的主要角色為藉由降低二級轉移溫度、玻璃轉移溫度(Tg)和彈性 模量,進而改善高分子的可塑性、柔韌性和加工性。IUPAC (International Union of Pure and Applied Chemistry) 將塑化劑定義為加入一材料(通常是塑料或彈性 體)中會增加材料之彈性、加工性或擴張性的一種物質,這種物質能減少聚合 物之變形、硬度、密度、黏度和靜電荷的張力,同時增加聚合物鏈的靈活性、 抗斷裂及介電常數,其他性質像是結晶度、光學透明度、導電性和耐生物降解 等等也受到影響。 塑化劑的種類多達百餘種,PVC 在未加入塑化劑之前材質堅硬,再加入大 量塑化劑後使其材質變得柔軟,增加其黏度以利於加工性,因此一般依 PVC 的柔軟度,將 PVC 區分成軟質 PVC 與硬質 PVC。硬質 PVC 相較於軟質 PVC 而言,具有柔韌性好、易成型、不容易脆化且保存時間長等特性,故佔有較多 的市場;軟質 PVC 一般用於天花板、皮革表層或地板等應用。由於 PVC 軟硬 度的差異,大幅降低了產品的生產成本,利於生產者製造軟硬度不同的各種產 品。[10] 塑化劑加入塑料、混凝土、牆板、水泥和石膏等產品中,可以增加材料的 彈性或流動性,塑化劑的種類有很多種,鄰苯二甲酸酯是最廣泛使用的塑化劑, 其結構如圖 1-8 所示,包括 di-(2-ethylhexyl) phthalate (DEHP)、di-isononyl phthalate (DINP)、di-isodecyl phthalate (DIDP)、 butyl benzyl phthalate (BBP)、 di-n-butyl phthalate (DBP)和 diethyl phthalate (DEP),其中 DEHP 和 DINP 經常 被添加到 PVC 中來創造範圍廣泛的產品,例如地板、裝潢、食品包裝和醫療 設備,而 DEP 和 DBP 則常用於化妝品中作為香料溶劑和固色劑,然而,使用 塑化劑作為食品添加劑是不被允許的! 鄰苯二甲酸酯因揮發性低且穩定性高,容易溶於大多數有機溶劑中,常添 加到塑膠中增強彈性,但其極易釋放到環境中,隨著塑膠的老化和分解,使其 釋放速度加快,為普遍存在於食品、室內空氣、土壤和沉積物中的污染物,人 體能經由排尿迅速排出 DEHP,然而,有些種類之鄰苯二甲酸鹽會干擾內分泌, 例如 DEHP、DBH 及 BBP,這些物質已經被證實是有毒性的,會對動物發育 和繁殖造成影響。[11]圖 1-8 鄰苯二甲酸酯之結構 塑化劑依作用方式可區分為外部塑化劑與內部塑化劑兩大類,外部塑化劑 是添加到聚合物中的低揮發性物質,在這種情況下塑化劑分子與聚合物鏈相互 作用,但未被化學附著於聚合物的主鍵上,因此經由蒸發、遷移或萃取而使塑 化劑消失。內部塑化劑是聚合物分子的固有部分,可以共聚合到聚合物結構, 或是與聚合物本身反應而成為產物,內部塑化劑通常具有龐大的結構,提供聚 合物有更多空間可以移動,避免聚合物靠得太緊密。因此,塑化劑透過軟化聚 合物,降低聚合物的玻璃轉移溫度和彈性模量,就上述兩種類型的塑化劑而言, 內部塑化劑容易生產但使用溫度範圍窄,而使用外部塑化劑的益處是有機會選 擇其合適的物質,這種合適的物質取決於所期望的產品性質。[10]
1.3 熱安定劑
熱安定劑是指能改善聚合物的熱穩定性所添加的助劑,由於大部分高分子 加工製程反應都在高溫環境中進行,因此需要藉由添加熱安定劑來提高材料的 熱裂解溫度,阻止或延緩高分子的老化,提高其使用性能以利於後續的加工程 序,然而,聚氯乙烯相較於其他高分子而言,其熱安定性較差,因此大部分熱 安定劑通常都使用於 PVC。常見的熱安定劑依化學成分組成來分類,大致上分 為有機錫類、金屬皂類、環氧類、鉛鹽類、稀土類等等,例如金屬皂類和環氧 類的熱安定劑一起使用,會有協同效果更能提高熱安定性。1.3.1 熱安定劑之作用機制
聚氯乙烯受熱降解時會脫去氯化氫,並且生成共軛多烯結構導致材料變色, 且氯化氫有催化效果會加速熱裂解的進行,因此熱安定劑分為以下兩種類型: 1.預防型:這種熱安定劑可以阻止脫氯化氫反應,或是能夠減緩氯化氫反應的 速度。 (1)吸收氯化氫,直接阻斷氯化氫對聚氯乙烯的催化作用。 (2)取代聚氯乙烯中不穩定的氯原子,防止產生脫氯化氫反應。 (3)捕捉碳自由基或氯自由基,防止自由基反應導致脫氯化氫。 2.修補型:這類型的熱安定劑主要是針對多烯類結構,藉由化學反應縮短共軛 多烯的結構。[12]1.3.2 熱安定劑的種類
以下列出較常見四種類型的熱安定劑來介紹:[12] 1.金屬皂類(Metal soap): 金屬皂類指的是帶有鉀、鈉、鎂、鈣等金屬的有機羧酸鹽,有機酸的部分 常見的有:硬脂酸、異辛酸、環烷酸等,因為具有良好的熱安定性且帶有潤滑 性,因此也可以作為 PVC 樹脂的潤滑劑。一般來說金屬皂合併使用會有協同 效果,因此通常是合併兩種金屬皂類一起使用,以下是它的作用機制: 化學式(1.1)為金屬皂與 PVC 釋出的氯化氫反應的第一步驟,金屬離子會 和氯離子結合,酸根則捕捉氫離子,此步驟的目的是要快速地吸收氯化氫,避 免 PVC 在加工初期產生變色,因此在金屬的部分傾向於選擇電負度強的金屬 離子,可以快速吸收掉氯離子,例如鋅、鎘、鋁,不過這些金屬氯化物本身帶 有酸性,當累積至一定量時仍然會催化 PVC 的分解,所以化學式(1.2) M2 金材料的裂化,M2 金屬的選擇則傾向於和 M1 金屬氯化物反應性高的金屬,例 如鈣和鋇。 2.有機錫類: 市面上所使用的有機錫熱安定劑一般皆為四價的錫,又可以分為含硫有機 錫及無硫有機錫。 無硫有機錫結構如下: 含硫有機錫結構如下: 有機錫熱安定劑優點在於長期熱安定性好,所製造的產品透明。 以下列出有機錫熱安定劑的三種作用機制: (1) 中和掉加熱過程中 PVC 所產生的 HCl 圖 1-9 有機錫與氯化氫反應[13]
(2) 取代掉不穩定的烯丙基氯 圖 1-10 有機錫取代不穩定氯[13] (3) 硫醇有機錫和 HCl 反應後所產生的硫基化合物會繼續與 PVC 鏈段中不飽和 部分進行反應,反應後 PVC 鏈段的共軛雙鍵減少,使得 PVC 顏色變淺。 圖 1-11 硫基化合物與 PVC 作用 3.鉛鹽類(Lead salt): 鉛鹽類優點是有很好的穩定性,具有強吸收氯化氫之能力,反應後會形成 PbCl2,價格低廉且加工性好,因此適合各類產品的製作,不過缺點是有毒性, 所以許多國家禁止使用。 4.環氧類(epoxides): 環氧類指的是在分子結構中帶有環氧基團,其環氧基團對於 PVC 不但有
以下為環氧大豆油與 PVC 的作用機制: (1) 吸收氯化氫:利用環氧基團的環氧基捕捉氫離子,而碳陽離子和氯離子形 成鍵結。 圖 1-12 環氧基團與氯化氫反應[14] (2) 取代不穩定的氯離子:烯丙基氯是不穩定的結構,捕捉掉氯離子後,氧基 和 PVC 碳鏈上的碳陽離子鍵結,藉此隔離掉不穩定的氯結構。 圖 1-13 環氧基團與 PVC 鍵結[15]
1.4 自由基(free radicals)
自由基(free radicals)為帶有一個不成對電子的原子、分子、或離子。一 般穩定的化學分子都有成雙成對的電子,化學鍵結也都以成對的電子排成,故 自由基會與其他分子作用,搶奪其他分子的電子,使本身原本不成對之電子變 成對而成為較穩定的分子,然而失去電子的分子會因此成為另一個不穩定的分 子,再去搶奪其他分子的電子,於是產生一連串的連鎖反應,換言之,一個自 由基可以帶動一連串的分子參與化學作用,這就是自由基會造成鏈鎖反應的原 因[16]。許多塑膠的聚合程序就是利用自由基的鏈鎖反應來達成的。自由基常是瞬間產生的過渡中間產物,壽命極短,但有些自由基,在低溫 的環境下能保持不配對電子的狀態長達幾十年。自由基本身的穩定性由化學結 構形態和靜電作用來決定,而分子量較大的自由基通常不活躍,例如維生素 C、 維生素 E 自由基,他們可以利用自身結構的特性來穩定不成對的自由基電子, 且不太會攻擊其他物質[17]。
生物體內常見的自由基為含氧的自由基(oxygen-containing free radicals), 包括過氧化物或超氧化物的分子,例如過氧化物(superoxide;O2-·)、過氧化氫 (hydrogen peroxide;H2O2)和反應性極強之羥基自由基(hydroxyl radicals;OH·) 等,此類帶有不穩定電子的含氧的自由基,又稱為活性氧(Reactive oxygen species; ROS)。 因自由基是一種極活潑、不穩定、生命週期短的化合物,因為不穩定,所 以易和體內的細胞組織產生化學反應,這個化學反應可統稱為氧化,會使組織 細胞失去正常功能,甚至破壞 DNA,造成損害或突變,引起癌症。近來許多 文獻都指出,人類有 8 成以上的慢性疾病,都是因為自由基損害而造成的,因 為身體要運作,在進行新陳代謝時,就需藉氧化產生能量,此時就有氧化活性 的自由基產生。當不穩定的自由基產生後,就會開始攻擊正常的分子,輕則造 成皮膚老化,比如說產生皺紋,或是出現黑、白斑點或粉刺等,嚴重一點則導 致身體的免疫力下降,心臟血管疾病,高血壓,糖尿病等代謝症候群[18]。
1.5 奈米碳管
1991 年,Iijima 等人利用電弧放電法(arc discharge method)合成 C60時,在 陰極處發現針狀物,經由高解析度穿透式電子顯微鏡分析其針狀物結構,發現 這些針狀物是碳原子所構成的中空管柱狀,型態為多層壁的碳管,稱其為多層 奈 米 碳 管 (multi-walled carbon nanotubes, MWNTs)[19] 。 而 單 層 奈 米 碳 管 (single-walled carbon nanotubes, SWNTs)則於 1993 年同時被 Iijima 等人及 Bethone 等人所發現。
1.5.1 奈米碳管之結構
奈米碳管(carbon nanotube, CNT)之管壁是以 sp2的方式鍵結而成,與蜂巢 狀結構以及石墨相似,由石墨捲曲形成中空管柱的結構,其捲曲方向及寬度會 使奈米碳管呈現不同特性,依層數的不同可概分為多層及單層石墨捲曲的多層 奈 米 碳 管 (multi-walled carbon nanotube, MWCNT) 及 單 層 奈 米 碳 管 (single-walled carbon nanotube, SWCNT)。由於奈米碳管的直徑約為數奈米至數
度、導電性特異等等,因此也就衍生了許多新的應用。
圖 1-14 (a)單層奈米碳管(single-walled carbon nanotubes), (b)多層奈米碳管 (multi-walled carbon nanotubes)
單層奈米碳管為一層石墨層所構成,而多層奈米碳管則是由二至數十層同 心軸之石墨層所構成,其管壁間的石墨間距為 0.3354 nm,與平面石墨層的間 距一樣,而每層石磨管壁的結構與一般片狀石墨的結構也相同[20]。單層奈米 碳管的直徑範圍為 0.4~3 nm,多層奈米碳管直徑範圍為 1.4~100 nm,其中多層 奈米碳管各層的螺旋度與直徑的不同會造成每層的電性都不一樣,不像單層奈 米碳管能以結構來定義,石墨的層狀結構因層末端的空懸鍵比例增大,並非為 最穩定的結構,所以會捲曲成圓狀管柱降低空懸鍵的數目,已達到較穩定的結 構狀態。 奈米碳管依其石墨層之捲曲方式的不同可分為三大類:扶椅式(arm-chair)、 鋸齒狀(zigzag)和螺旋型(chiral),因不同捲曲方式造成碳管不同的螺旋性,會 使管壁上的六圓環有不同的捲曲程度,而造成六圓環上未飽和雙鍵間電子傳導 的阻力,不同的螺旋性會造成奈米碳管間傳導性的差異,因此奈米碳管的特性 決定於石墨層的寬度和捲曲方向,不同的捲曲方向可呈現出奈米碳管的金屬、 辦金屬及半導體的特性。[21]
1.5.2 奈米碳管之特性
1.機械性質:奈米碳管側面是由六邊形碳環組成,而在管身彎曲和兩端半球帽 部分則含有一些五邊形及七邊形的碳環結構。因為構成這些不同碳環結構的碳 -碳共價鍵是自然界中最穩定的化學鍵,所以奈米碳管具有相當好的力學性能。 [22]2.熱性質:由於奈米碳管主要由碳原子以 sp2混成碳-碳雙鍵結,並形成為六圓 環,其碳管表面沒有未鍵結電子,因此具有高度化學穩定性。奈米碳管本身結 晶性佳,因此具有相當大的晶格振動自由路徑(phonon mean free path),熱可藉 由 晶 格 的 振 動 有 效 傳 遞 , 所 以 碳 管 之 熱 傳 導 性 優 於 熱 裂 解 石 墨 (pyrolytic graphite)及鑽石。[22] 3.電性質:奈米碳管具有獨特的電學性質,由於奈米碳管內流動的電子受到量 子限域(quantum confinement)所致,電子在碳管中通常只能在同一層的石墨片 上沿碳管的軸向運動,沿徑向的運動將受到很大的限制。理論計算和實驗研究 都表明,不同類型的奈米碳管,可得到不同的電性,如金屬、半金屬或半導體 之性質,甚至在同一根奈米碳管的不同位置,由於結構上的變化,也可以呈現 出不同的導電性[22]。因不同捲曲方式所造成的碳管螺旋性,會使管壁上的六 圓環有不同的扭曲程度,而造成六圓環上未飽和雙鍵間電子傳導的阻力,因此 不同的螺旋性造成了奈米碳管間導電性質的差異,它可以是導電性(扶手型)或 是半導體(螺旋型或鋸齒型)的特性,如圖 1-15。[23][24] 圖 1-15 因不同捲曲方式所造成的碳管螺旋性
1.5.3 奈米碳管吸收自由基之特性
由於奈米碳管結構類似於 C60,C60是由 60 個碳原子形成的籠狀結構,分 子高度對稱,每個碳原子都是等價的,分子結構含有 30 個π鍵,可引發加成 反應,故被稱為「自由基海綿」(free radical sponges)。六元環之間的碳-碳雙鍵 (C=C)為反應活性部位,由於反應活性部位對稱地分布在球面上,故其加成反 應的選擇性不高,在許多研究報告相繼提出之後,目前可觀測到的反應性質有: 環加成反應(親電子性、親核性、自由基)、氧化反應、還原反應、鹵化反應、 重氮化反應以其聚合反應等。
1.6 奈米碳管之製備
奈米碳管自 1991 年開始發展至今,已經發展出許多不同的製備方法,其 中較為廣泛使用的製備方法,包括電弧放電法(arc discharge method)、雷射汽化 法(laser ablation method)、化學氣相沉積法(chemical vapor deposition method, CVD)、太陽能法及微波輔助化學氣相沉積法等等。使用不同方法製備奈米碳 管造成結構上會有些許不同,如改變使用的觸媒、反應氣體與反應溫度等條件, 除了可獲得單層奈米碳管或多層奈米碳管外,還可以決定所生成奈米碳管的管 徑與長度。由於化學氣相沉積法的製程簡易且產能大,故被廣泛的使用,因此 本實驗採用化學氣相沉積法來製備奈米碳管,製備的條件與文獻[25]相同。 化學氣相沉積法在早期已被用於合成氣相中成長碳纖維(VGCF),其反應 原理簡單且製程容易,在適當的合成條件下可控制奈米碳管之長度。如圖 1-16 所示,化學氣相沉積法主要是在高溫環境下將含碳氣體通入反應腔體中,藉著 催化劑的幫助使含碳氣體釋放出碳原子,合成奈米碳管,依反應物及催化劑的 型態大致可分為化學氣相沉積法、熱分解法、CO disproportion 法。 圖 1-16 化學氣相沉積法製備奈米碳管示意圖在化學氣相沉積法中,影響奈米碳管生長的因素包括含碳氣體(碳源)、催 化劑以及基板。催化劑需經過前處理成適當大小,以利於奈米碳管之成核,觸 媒的活性與成長的溫度會直接影響到碳源的裂解及碳原子在催化劑表面的擴 散速度,太高的裂解速率會導致催化劑被石墨層包覆而失去其裂解的功能,使 反應最後無法獲得奈米碳管結構的產物,因此可藉由適當的加入具有腐蝕非晶 質碳能力的氣體,如 H2、NH3及 O2等,改善奈米碳管成長並提高奈米碳管的 品質。
1.6.1 奈米碳管之官能基化改質
由於奈米碳管具有非常優異的機械、導電、導熱性質,加上本身具有低密 度(質輕)和高長徑比等特性,因此為極佳的補強材料,然而奈米碳管間具有很 強的凡德瓦力,容易團聚,造成其不易分散在水及大部分的有機溶劑中,而限 制了它的應用性。 為了提升碳管的應用性,改善碳管在目標溶劑中的溶解度是必要的,若能 成功地將奈米碳管表面作適當之官能基化或接枝修飾改質,提升其溶解性質, 更進一步將有特殊功能的官能基接枝於碳管表面,賦予它除了能在溶劑及基材 中均勻分散之外的功能,目前許多文獻[26][27]皆指向將奈米碳管作有效地改 質來發揮碳管在各領域之應用性。 官能基化奈米碳管的方法主要有兩種,非共價鍵改質與共價鍵改質。 非 共價鍵改質主要是藉由靜電作用力、凡得瓦爾力及親疏水性作用力等這些次要 鍵結把分散劑吸附在碳管上,進而使碳管能溶解在溶液中。另外,利用高分子 的纏繞的方法來也能改質碳管表面,例如使用界面活性劑當作分散劑(如: SDS) [28],主要是將奈米碳管以超音波震盪破壞碳管間的凡德瓦爾力,界面活性劑 的疏水端將碳管包覆形成微胞,而親水端可與溶液形成穩定的分散。 常見的共價鍵改質奈米碳管的方式可分為兩大類: (1)酸處理改質:活化碳管,在管壁及末端產生含氧官能基之活性端點。 (2)接枝改質:藉由 Grafting from 或 Grafting to 方式接上具特殊官能基的分子 片段。1.6.2 奈米碳管之酸處理改質
由於酸處理改質是一種傳統且有效的改質方法,因此本實驗選擇官能化改 質之奈米碳管以酸處理為主,製備酸處理改質奈米碳管之條件與文獻[29]相 同。 酸處理改質主要是使用強酸作為氧化劑,將奈米碳管的管壁或末端反應成 帶有含氧的官能基 (-COOH、-OH、C=O),因奈米碳管的末端是由碳的五圓環 和六圓環組成的半球形,強氧化劑可將末端打開氧化成羧基,進而與其它的化 學試劑反應,改質成所需求之目標官能基。而在管壁上奈米碳管本身就含有一 些缺陷位置,如圖 1-17 所示,有五圓環與七圓環之位置缺陷、sp3位置缺陷及 晶格空位缺陷,這些缺陷點因強酸對管壁的氧化破壞作用而留下空洞,進而連 接上所需之官能基團,同時,將奈米碳管切短成達數百奈米的短碳管,因此經 過官能基化的奈米碳管可以有效的分散於水溶液及不同的有機溶劑中,或進行 更進一步之反應。 圖 1-17 奈米碳管典型的表面缺陷位置(A)碳架構上的五圓環及七圓環取代六圓 環而導致奈米碳管彎曲, (B) sp3缺陷(R = H, OH), (C)氧化作用在碳管表面結構 上產生的連接-COOH 的小空洞, (D)奈米碳管開口及末端位置連接-COOH 官 能基團。第二章
文獻回顧
2.1 奈米碳管吸收自由基之性質
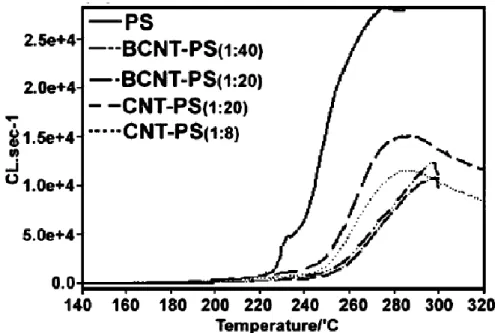
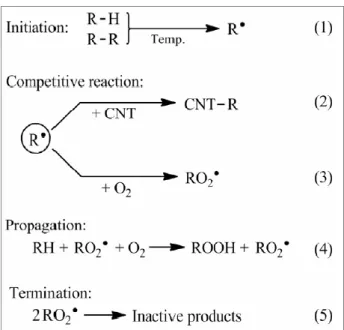
2002 年,P.C.P. Watts et al.[30]研究奈米碳管與硼摻雜之碳管在 polystyrene、 polyethylene、polypropylene 和 poly(vinylidene fluoride)中之抗氧化現象,由於 奈米碳管結構類似於 C60,具有很高的電子親和力(electron affinities) (C60約 2.65 eV),所以亦能夠吸收高分子老化時所產生之自由基,打斷自由基反應之 chain propagation 階段,因而在材料中發揮抗氧化的效果。典型的老化反應中,一個 碳自由基與氧氣反應,產生 alkylperoxyl radicals: 此自由基在與高分子鏈上之氫原子反應,產生一新的碳自由基,放出一個光 子: 此實驗藉由觀察化學發光(Chemiluminescence, CL)之多寡來判斷材料老化 的情形,將 CL 測定儀加裝在 DSC 儀器當中,當 DSC 對材料做恆溫(測定 oxidation induction temperature, OIT)及動態掃描時,詳細記錄 CL 之變化,CL 儀測得光子表示高分子老化的發生,光子數量越多表示材料老化的情況越嚴重, 如圖 2-1,無添加碳管之 PS 在 225 ℃開始產生高分子老化,但有加入碳管之 PS 其材料老化現象往後延遲至約 250 ℃才發生,證明碳管具有吸收自由基、 使材料抗氧化之效果。在 TGA 之測定中,如圖 2-2,加入不同比例碳管之 PVDF, 其失重起始溫度隨著碳管添加量的上升逐漸延後,說明碳管抗氧化之效果。
圖 2-1 Temperature ramped chemiluminescence curves in O2 for pure PS and PS-nanotube composites
2012 年 Xiaomei Shi et al.[31]利用 DSC (Differential scanning calorimetry)測 定 HDPE/CNT 複合材料之氧化誘導溫度(oxidation induction temperature, OIT) 及氧化誘導時間(oxidation induce time, OIt),研究單壁奈米碳管(SWCNT)、多 壁奈米碳管(MWCNT)及 OH 官能基之改質多壁奈米碳管(MWCNT-OH)三者各 自在 HDPE 中之抗氧化能力。 在 HDPE 中各類碳管添加量為 5 wt%時(依序為加入 SWCNT、MWCNT、 MWCNT-OH),HDPE/CNT 複合材料之氧化誘導溫度(OIT)增加了 16 ℃、23 ℃ 和 28 ℃,表示含有碳管之 HDPE 在高溫時更具抗氧化能力,如圖 2-3 所示。 在氧化誘導時間(OIt)測定結果中,可看到未添加碳管之 HDPE 在開始通入氧氣 後便開始產生氧化之放熱峰,而含有各種碳管之 HDPE 大幅延長了 OIt,如圖 2-4,且在 180 ℃、190 ℃、200 ℃測定之結果皆有一致性。針對 MWCNT-OH 之添加濃度為 0.5 wt%、2.5 wt%、5 wt%時測試複合材料 OIt 之變化,如圖 2-5, 發現碳管添加量和抗氧化能力(延長 OIt 之效果)成正比關係,在碳管添加量為 0.5~5 wt% 之 區 間 內 近 乎 呈 現 線 性 關 係 。 由 拉 曼 光 譜 及 ESR(electron spin resonance)推估其吸收自由基之機制,三者的抗氧化能力排序為:MWCNT-OH > MWCNT > SWCNT,發現當各種碳管之缺陷濃度上升,其自由基清除效率也 會提升。 圖 2-3 Evaluation of OIT by DSC
圖 2-4 Evaluation of OIt at required temperature by DSC (a) 180 ℃, (b) 190 ℃, (c) 200 ℃
利用 Fenton reaction (Fe2+
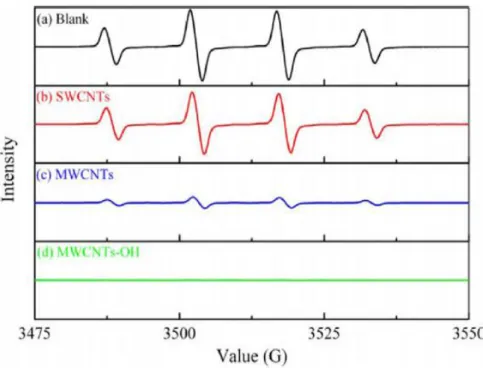
+ H2O2 → Fe3++ HO·+ HO-) 來研究碳管對 OH· 自由基之吸收特性,但由於 OH·自由基具高反應性而使半生期極短,故須利用 spin trap 的方式以 DMPO 來與 OH·形成較穩定之 DMPO/HO·,以便能用 ESR 來測得自由基之訊號,典型之 DMPO/HO·如圖 2-6,將其與添加 1 mg 之各種 碳管加入 Fenton 試劑後之 ESR 圖譜比較,SWCNT 加入能抑制 13%之 OH·自 由基,MWCNT 能抑制 84%,而 MWCNT-OH 則完全澆熄 OH·自由基。而 MWCNT 需加入 1.6 mg 才會與 1 mg 之 MWCNT-OH 之自由基清除效率相同, 而 SWCNT 則需要至少 5 mg 才能達到 MWCNT-OH 之自由基清除效率。另外, 多壁奈米碳管之管壁數量越多,或是 OH 基改質量較高之多壁奈米碳管具有更 好的抗氧化能力。碳管在清除自由基時能提供或接收電子來穩定自由基,典型 之機構如圖 2-7。[32]
圖 2-6 Generation of hydroxyl radicals by the Fenton reaction in the presence of different kinds of CNTs (a) Blank, (b) SWCNTs, (c) MWCNTs, (d) MWCNTs-OH. The number of generated radicals is proportional to the intensity of the ESR signal.
圖 2-7 General scheme of polyolefin thermal oxidation in the presence of CNTs
2014 年,Y.T Shieh et al.研究改質和微波處理多層奈米碳管之自由基清除 能力[29],此實驗利用多種改質碳管來進行自由基吸收能力之比較,包括奈米 碳管(CNT)、球磨奈米碳管(bmCNT)、bpo 改質奈米碳管(bpoCNT)、酸處理改 質碳管(CNT-COOH)和不同微波時間改質奈米碳管(mw10CNT、mw20CNT、 mw30CNT)。
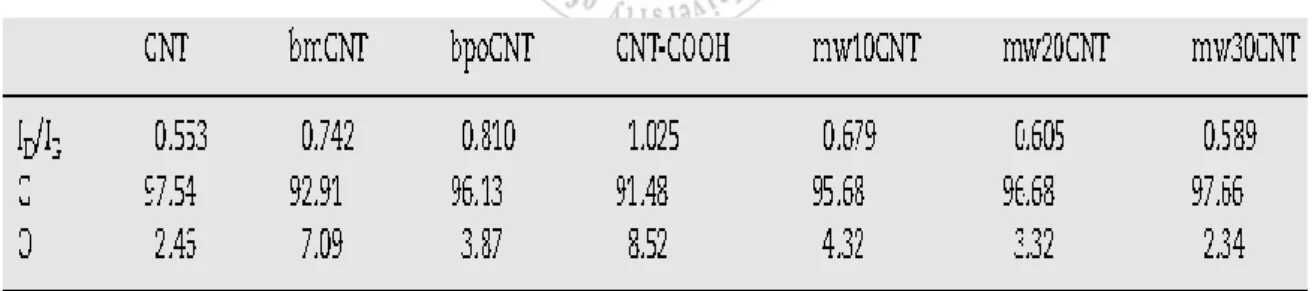
Raman 光譜之鑑定主要是測試各種碳管之 D-band 與 G-band 的訊號,其中 D-band 與 G-band 訊號強度的比值為 ID/IG,ID/IG值的增加表示缺陷點含量增加,
其缺陷點如無序碳之 sp3混成結構或是非石墨的 sp2混成結構,而 ID/IG值越低 表示碳管管壁上石墨碳含量越高,即碳管純度越高,表 2-1 為 Raman 光譜測得 各種改質奈米碳管之 ID/IG 值,顯示出各種奈米碳管缺陷點的含量,測定結果 可知 CNT-COOH 的 ID/IG值最高,表示 CNT-COOH 相較於其他改質碳管之缺 陷點含量為最高,而改質碳管相較於未改質碳管而言,改質碳管因結構受到破 壞產生更多缺陷,其 ID/IG 值較未改質碳管高,表示改質碳管的缺陷濃度皆比 未改質碳管的缺陷濃度高。
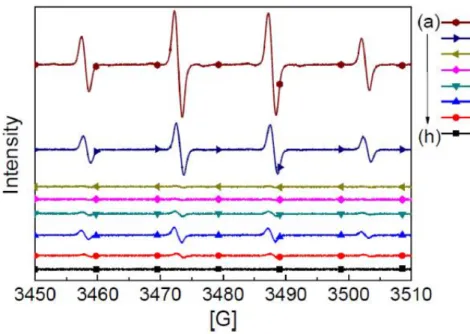
EPR 鑑定各種碳管的自由基清除效應,先利用 Fenton reaction 產生 OH· 自由基,再利用 spin-trap 法,使 DMPO (5,5-dimethyl-pyrroline N-oxide)與 OH· 反應形成較穩定之錯合物 DMPO/OH·,DMPO/OH·在 3450 至 3510G 有明顯波 峰訊號,訊號強度正比於 DMPO/OH·濃度,而波峰訊號的消失表示自由基完 全被清除,圖 2-8 為測試各種碳管吸收 DMPO/OH·自由基能力之結果,各種碳 管加入 DMPO/OH·中可觀察到訊號強度皆下降許多,表示不論是改質或未改 質碳管對 DMPO/OH·都有明顯吸收自由基能力,其中 CNT 對 OH·自由基之吸
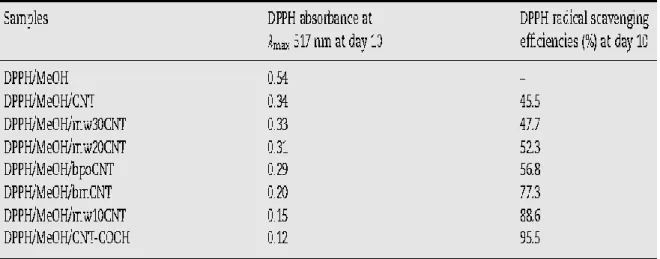
收率只有 51%,改質碳管對 OH·自由基之吸收率大幅提升,高達 85%以上, 表示改質碳管相較於未改質碳管而言,其自由基吸收能力更強,就 CNT、 bmCNT、bpoCNT 及 CNT-COOH 四者而言,其 EPR 測試結果與上述 Raman 鑑定分析之結果一致,隨著 ID/IG值增加,自由基清除效應也提升,而 bpoCNT 對 OH·自由基清除效率比 bmCNT 差,是因為 bpoCNT 所接枝上的苯基可能在 OH·自由基反應過程中形成立體障礙,使 bpoCNT 吸收自由基能力略微下降, CNT-COOH 之自由基吸收能力在各種碳管中為最強,清除率高達 99.5%。 DPPH 自由基在甲醇溶液中為深紫色,此溶液在 UV/Vis 光譜中波長 517 nm 有明顯波峰,隨著 DPPH 自由基的消失,其顏色會由深紫色逐漸轉為淡黃色, 因此利用 UV/Vis 來鑑定分析各種碳管吸收 DPPH 自由基之能力,如圖 2-9 與 表 2-2 所示,可觀察到加入碳管後在波長 517 nm 位置的吸收度明顯減少,表 示加入各種碳管後溶液顏色明顯改變,具有清除 DPPH 自由基之能力,其中 CNT 對 DPPH 自由基清除效率 45.5%為最低,而 bpoCNT 受到接枝苯基所形成 立體障礙的影響,因此對 DPPH 自由基清除效率較 bmCNT 差,CNT-COOH 相 較於其他改質碳管而言,其清除 DPPH 自由基之效率為最高。由此文獻可知, 碳管缺陷對其自由基吸收能力有重大的影響,當未改質或改質之奈米碳管的缺 陷濃度增加,其自由基清除效應也會提升。
表 2-1 ID/IG ratios obtained from Raman spectra and atomic compositions(%) of C and obtained from EDS for various modified CNT
圖 2-8 EPR spectra of OH· radicals in (a) DMPO/OH·, (b) DMPO/OH·/CNT, (c) DMPO/OH·/bmCNT, (d) DMPO/OH·/mw10CNT, (e) DMPO/OH·/mw20CNT, (f) DMPO/OH·/mw30CNT, (g) DMPO/OH·/bpoCNT, (h) DMPO/OH·/CNT-COOH
圖 2-9 UV/Vis spectra taken at day 10 for DPPH in MeOH solutions containing 4 mg of nanotubes for (a) DPPH/MeOH, (b) DPPH/MeOH/CNT, (c)
DPPH/MeOH/mw30CNT, (d) DPPH/MeOH/mw20CNT, (e)
DPPH/MeOH/bpoCNT, (f) DPPH/MeOH/bmCNT, (g) DPPH/MeOH/mw10CNT, (h) DPPH/MeOH/CNT-COOH
表 2-2 UV/Vis absorbance of DPPH at λmax 517 nm at day10 in MeOH solutions containing various modified CNT (4 mg each)
2.2 聚氯乙烯之熱安定化
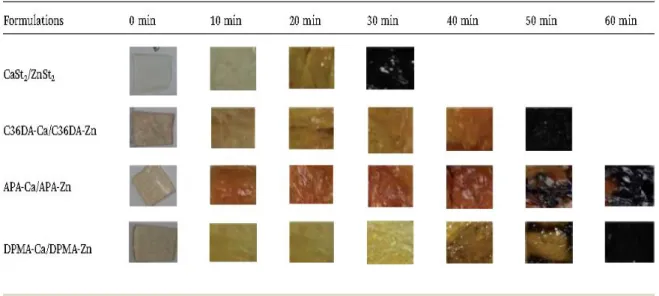
由於 PVC 熱穩定性差的緣故,故通常需添加安定劑以利於加工製造和使 用,關於研究 PVC 熱穩定性之文獻不計其數,因此參考以下六篇文獻來了解 關於 PVC 熱安定化的分析方法,以利於進行本實驗進行研究分析。 2014 年,Mei Li et al.研究由松香和雙戊烯所獲得之雙羧酸混合鈣和鋅鹽之 製備與其對聚氯乙烯之熱穩定性[33],文獻中提到 PVC 的加工穩定化之測試可 分為短期穩定性(或是 early color)和長期穩定性(通常稱為 point-to-black),其中 定義短期穩定性為 off-the-mill 顏色,長期穩定性是指裂解後使化合物無法再 回收利用或是開始危害加工設備,此實驗製備多種熱安定劑來進行其對 PVC 穩定化程度之比較,包括 CaSt2/ZnSt2、C36DA-Ca/C36DA-Zn、APA-Ca/APA-Zn 和 DMPA-Ca/DMPA-Zn。靜態熱穩定性分析藉由剛果紅(Congo Red, CR)試驗, 如圖 2-10 所示,厚度約 1 mm 的 PVC 薄膜裁切成長度為 15 mm 的正方形置於 封閉的管子內,將管子浸入溫度控制在 185 ℃的油浴中,直到管子上方的 CR 試紙變色,由紅色轉為藍色,其 CR 試紙顏色轉變所需時間代表 PVC 穩定化 的時間。圖 2-11 為剛果紅試驗所測得之 PVC 不同安定劑的靜態熱穩定時間(Tss), 測試結果可知 DMPA-Ca/DMPA-Zn 具有較高的長期熱穩定性,四者的 Tss排序 為 : DMPA-Ca/DMPA-Zn (48 min) > C36DA-Ca/C36DA-Zn (31 min) > APA-Ca/APA-Zn (29 min 25 s) > CaSt2/ZnSt2 (20 min 55 s)。圖 2-12 為 PVC 在 含有各種熱安定劑之 CR 測試下的變色結果,CaSt2/ZnSt2在 10 min 內呈現出極 好的保色度,但在 30 min 內會完全轉為黑色,相反地,APA-Ca/APA-Zn 相對 於 C36DA-Ca/C36DA-Zn 和 CaSt2/ZnSt2而言,雖然沒有良好的持色度,但導致 其較長的穩定化時間,可能是因為松香酸的羧酸根陰離子反應性比脂肪酸取代此在特定的裂解時間內更能有效得減少氯化氫的釋放, APA-Ca/APA-Zn 雖然 在 PVC 加工初期階段並不是一個好的氯化氫清除劑,但卻提供了良好的長期 穩定性,另外,DMPA-Ca/DMPA-Zn 金屬離子含量和羧酸根陰離子反應性都比 APA-Ca/APA-Zn 高,所以 DMPA-Ca/DMPA-Zn 對 PVC 穩定性為最高,可以觀 察到含有 DMPA-Ca/DMPA-Zn 的 PVC 薄膜在 30 min 後所呈現的顏色最淺,需 要在長時間(60 min)下才會完全變成黑色。
圖 2-10 Schematic of the device for Congo red test
圖 2-12 Discoloration of PVC samples as a function of degradation time, heated at 185 ℃.
2006 年,Ming Wang et al. 研究含鈣/鋅 硬酯酸鹽(calcium/zinc stearates) 的有機錫和季戊四醇(pentaerythritol)對聚氯乙烯穩定化的效果[34],添加不同 劑量之 PeE (pentaerythritol)及有機錫作為 PVC 穩定劑是否與 CaSt2/ZnSt2 有協 同作用,並了解其對 PVC 穩定化之效果。利用 UV/Vis 光譜儀及 X 光能量散 佈分析儀來鑑定分析有機錫之作用機制,圖 2-13 為(PVC+CaSt2/ZnSt2)與 (PVC+CaSt2/ZnSt2+有機錫)之 UV-Vis 光譜圖,發現曲線 b 往短波長方向移動, 表示由於有機錫的摻入明顯的導致 PVC 共軛雙鍵含量減少,其意旨有機錫會 與 PVC 降解過程所產生之雙鍵反應。在 X 光能量散佈分析儀測試結果指出, 摻入有機錫之 PVC 在加熱後存在 6.66%錫和 9.33%硫元素,而摻入有機錫之 PVC 在未加熱前其錫與硫元素比例分別為 9.57%和 5.87%,表示 PVC 和有機 錫之間的作用力是因為硫元素含量的增加,作者觀點是在 PVC 加工過程中因 為有機錫的添加使 C-S 鍵形成,有機錫會以更穩定的硫醇基(mercaptide groups) 取代 PVC 鏈中不穩定的氯原子,並且和 HCl 產生其他反應產生硫醇(mercaptan), 硫醇與 PVC 降解過程中所生成之雙鍵產生加成反應。
圖 2-13 UV spectra of PVC samples. Formulation a: PVC 100 phr, CaSt2/ZnSt2 2.5 phr; Formulation b: PVC 100 phr, CaSt2/ZnSt2 2.5 phr, organic tin 0.2 phr.
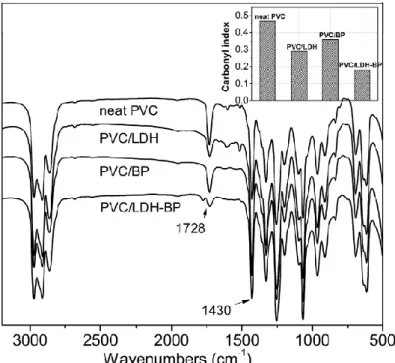
2014 年,Xiaofei Zhang et al. 研究雙氫氧化物插層在 UV 穩定劑中對 PVC 加速候化與穩定化之效果[35],此實驗使用 LDH(Layered double hydroxides)、 BP(2-hydroxy-4-methoxybenzophenone-5-sulfonic acid)及 LDP-BP 來測試三者對 PVC 的耐候性及穩定性。圖 2-14 為純 PVC 在不同時間下經加速候化試驗之 IR 光譜圖,經曝光五天之 PVC 有明顯的變化,其在位置 1728 cm-1之特徵波峰為 羰基(carbonyl group),隨著曝光時間變長,其相對的波峰強度增加,從羰基指 數(carbonyl index)的變化中也能明顯觀察,光譜中所觀察到的羰基是由於 PVC 鏈的光氧化作用,這表示硬質 PVC 在整個加速候化試驗中以氧化反應為主導, 添加穩定劑會阻礙 PVC 的氧化反應,由圖 2-15 可以觀察到 PVC/BP 及 PVC/LDH 的氧化程度較 PVC/LDH-BP 高,並藉由圖 2-15 右上圖之羰基指數來 解釋各種 PVC 穩定劑的氧化行為,可以發現 PVC/LDH-BP 相對 PVC/BP 和 PVC/LDH 而言,其羰基指數較低,表示 LDH-BP 會阻礙 PVC 的光氧化,此行 為歸因於差層後結構的穩定化和 LDH-BP 對 UV 之吸收能力。 剛果紅(Congo Red)試驗主要是測試材料之穩定化能力,在 PVC 摻雜熱安 定劑的系統中,PVC 所釋放之 HCl 與安定劑反應,延緩自動催化效應,可觀 察到長時間的靜態熱穩定化,PVC 之靜態熱安定性藉由量測 HCl 的濃度來分 析。圖 2-16 是藉由剛果紅試驗量測 PVC 去氯化氫的過程,來了解 LDH、BP 及 LDH-BP 對 PVC 靜態熱穩定性之影響,純 PVC 的靜態穩定化時間為 97 min, 添加 BP 後靜態穩定化時間下降到 50 min 以內,原因為 BP 結構中的磺酸基 (sulfonic acid group)造成 BP 之 pH 值低於 2,且強酸會催化 PVC 的熱穩定性; 當 LDH 與其他主要熱安定劑混合使用時,藉由吸收 HCl 來延長 PVC 降解,並
改善顏色穩定性,此實驗加入 0.5 phr 及 1 phr LDH 增長 PVC 的靜態穩定化時 間,然而,添加 3 phr LDH 會加速 PVC 降解,使穩定化時間降至 50 min 以內, 原因為 LDH 呈微鹼性無法中和 HCl,因此加入過量 LDH 會引發 PVC 降解。 另外,添加 LDH-BP 與添加 BP 或 LDH 對 PVC 熱穩定性之差異為,隨著 LDH-BP 含量的增加,其熱穩定化時間也隨之增加,添加 3 phr LDH-BP 其穩定化時間 高達 160 min,超過純 PVC 穩定化時間的 1.6 倍,此結果指出在 PVC 去氯化氫 過程中,LDH-BP 的添加會促進 HCl 的吸收,而由於插層的關係,使 LDH-BP 的酸鹼催化消失,因此添加過量 LDH-BP 更能增強 PVC 的穩定性。
圖 2-15 FTIR spectra of neat PVC and stabilizer-doped PVC after 50 days’ accelerated weathering test.
圖 2-16 Thermal stability time of PVC, PVC/LDH, PVC/BP and PVC/LDH-BP measured by Congo Red test.
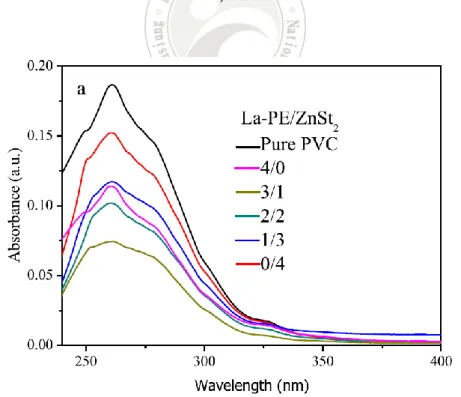
2015 年,Degang Li et al. 研究鑭-季戊四醇醇鹽(lanthanum-pentaerythritol alkoxide)與硬脂酸鋅(zinc stearates)和β-二酮(β -diketone)的協同效應對聚氯乙 烯的熱安定性[36]。PVC 含不同熱安定劑的熱老化試驗結果如圖 2-17,可觀察 到純 PVC 一開始的顏色為淺灰色,設 180 ℃為起始溫度開始加熱,隨著加熱 時間變長,純 PVC 的顏色變化從淺棕色到黑色,含有 4 phr La-PE 有良好的起 始顏色且其顏色在 120 min 之後都不會轉為黑色,這證明了 La-PE 具有延長 PVC 的顏色穩定性的能力,當 3 phr La-PE+1 phr ZnSt2一同作為 PVC 穩定劑時, 展現其優異的起始顏色且在 90 min 才轉為黑色,隨著 ZnSt2劑量的增加其顏色 穩定性隨之下降,而含有 4 phr ZnSt2之 PVC 在 10 min 內則完全變成黑色,表 示 La-PE 與 ZnSt2對 PVC 顏色穩定性有協同效應。 圖 2-18 為不同熱安定劑添加於 PVC 試片在 180 ℃下加熱 0 min 之 UV-vis 光譜圖,可以觀察到最大吸收波峰位置在 261 nm,為 PVC 去氯化氫過程中所 形成之三烯(trienes),純 PVC 呈現出最高濃度的雙鍵(Cdb),表示 La-PE 與 ZnSt2 有效的增強 PVC 的熱穩定性,ZnSt2/PVC 證明了其熱穩定性優於純 PVC,但 劣於 La-PE/PVC 及 La-PE+ZnSt2/PVC 的熱穩定性,而 3 phr La-PE+1 phr ZnSt2/PVC 其 Cdb為最低,表示其組成比例在 PVC 熱穩定性中達到最優異的協 同效應。圖 2-19 為 PVC 添加不同熱安定劑於 180 ℃加熱 120 min 之 UV-VIS 光譜圖,可觀察到最高波峰位置位移至 280 nm,此吸收波長為試片加熱 120 min 後所形成的四烯(tetraenes),然而,六者之 Cdb皆提高,而含純 ZnSt2之 PVC 其 Cdb 卻超過純 PVC,意味著 ZnSt2/PVC 發生鋅燃燒(zinc-burning)現象。3 phr La-PE+1 phr ZnSt2/PVC 其 Cdb在六者中為最低,可知 3 phr La-PE+1 phr ZnSt2 的配比為 PVC 帶來最優異的熱安定性。
圖 2-17 Color evolution, as a function of time, of PVC samples heated at 180 ℃. (For interpretation of the references to colour in this figure legend, the reader is referred to the web version of this article.)
圖 2-18 UV-VIS spectra of PVC samples stabilized with different thermal stabilizersheated at 180 ℃ for 0 min. (a) La-PE/ZnSt2
圖 2-19 UV-VIS spectra of PVC samples stabilized with different thermal stabilizers heated at 180 ℃ for 120 min. (a) La-PE/ZnSt2
2014 年, Mei Li et al.發表了從松香(rosin)和脂肪酸中製備一種新型液態熱 穩定劑(LTS)及 PVC 穩定化性質之研究[37],文獻中分別以 180 ℃和 190 ℃對 聚氯乙烯試片進行去氯化氫試驗(Dehydrochlorination test),0.5 g 的 PVC 薄膜 被裁為邊長 0.5 cm 的正方形,將其放進反應器中,DHC 試驗所建立之玻璃反 應器帶有可拆卸的蓋子,從蓋子口通入氮氣(流量 20 ml/min),且有一彎曲管可 將氣體排出,將反應器浸置於溫度控制於±1 ℃以內的矽油浴中,從反應器中 排出的氣體被收集在裝有 pH 電極的滴定池中,滴定池內含有 NaOH 水溶液(pH 10),NaOH 溶液能快速封存由氮氣牽引而來的 HCl 氣體,當反應器浸置於油 浴中即開始記錄時間。圖 2-20 為在 180 ℃和 190 ℃加熱之 PVC 試片之去氯 化氫(DHC)曲線,DHC 曲線可以被分為兩部分:初始區及線性區,當 pH 開始 增加的這段時間為視覺誘導時間(Ti),由 X 軸上線性區之切線的截距來決定, 而在△pH=2.2 的時間定義為穩定時間(Ts),在 pH 曲線中,初始區的低斜率被 解釋為添加劑的存在導致 HCl 氣體釋放較慢,而線性區的高斜率是因為 HCl 氣體釋放速率較快。 表 2-3 為含有不同安定劑之 PVC 試片的誘導時間(Ti)和穩定時間(Ts),在 190 ℃去氯化氫試驗結果中,Ts 的排序為 RODA-Ca/RODA-Zn (98.6 min) > JRH-LTS-Ca/JRH-LTS-Zn (86.2 min) > M509-LTS-Ca/Zn (64.6 min) , 含 RODA-LTS 之 PVC 其 Ts 也最大,此外,以 JRH-LTS-Ca/JRH-LTS-Zn 來穩定
圖 2-20 DHC of PVC compounds stabilized with different LTSs.
表 2-3 Comparison of effects of different LTSs on thermal stability of PVC compounds.
2015 年,F.J.W.J. Labuschagne et al. 發表了以層狀雙氫氧化衍生物來熱穩 定彈性聚氯乙烯之研究[38],利用 TGA(熱重分析儀)來了解純 PVC 及 PVC 化 合物之固有的熱穩定性,將試片置於熱重分析儀中,通入氮氣流速為每分鐘 50 mL,升溫速率為每分鐘 10 ℃,由 25 ℃加熱至 900 ℃,進行 TGA 測定, 測得之 PVC 及各種類 PVC-LDH 化合物之熱重分析圖,如圖 2-21 所示,彈性 PVC 熱重損失主要分為兩個階段,第一階段的熱重損失的起始溫度在 340 ℃, 熱重損失之最大速率在 315 ℃,最終溫度於 370 ℃,此溫度點之重量百分率 為 20.7%;而第二階段熱重損失的起始溫度在 420 ℃,熱重損失之最大速率在 467 ℃,最終溫度於 510 ℃, 殘餘之重量百分率為 7%。在第一階段造成 PVC 熱重損失是由於 PVC 脫去氯化氫及塑化劑的揮發,第二階段重量損失是因為 PVC 主鏈斷裂所造成之熱裂解,最終的殘餘物為碳焦。LDH-PVC 化合物之熱 重損失曲線與純 PVC 相互對照,可以發現在第一階段它們的重量損失之起始 溫度幾乎相同,然而,相較於純 PVC 而言,各種類 LDH-PVC 化合物每一階 段的殘餘物較多,因此對於各種類 LDH-PVC 其熱重損失速率由快到慢之排序, 依 序 為 MgZnAl-LDH >> MgFeAl-LDH > MgCuAl-LDH > CaAl-LDH ≈ MgAl-LDH,其中 MgZnAl-LDH 明顯的在第一階段加速重量損失,根據 Levchik and Weil 所提出的機制[39],ZnCl2會自催化加速脫去氯化氫反應,在工業中被 稱為鋅中毒,較高的殘餘碳焦率被歸因於催化效應,此催化效應有利於交聯反 應和芳香族之環化反應。
圖 2-21 TGA traces in air for the PVC-LDH composites. Temperature was scanned -1
2.3 研究動機
聚氯乙烯為一種最常被使用的熱塑性高分子材料,且被廣泛的應用於軟性 及硬性的塑膠產品,由於聚氯乙烯是一種熱穩定性差的高分子,因此在遇到光、 高溫或高能量時容易受到熱降解,聚氯乙烯在熱裂解後會釋放出氯化氫(HCl), 隨著熱裂解過程逐漸加快,其氯化氫所釋放的量也會逐漸增加,因此為了抵抗 聚氯乙烯老化之現象,需添加熱安定劑來延緩或阻礙其熱裂解情形,提高聚氯 乙烯的使用性能與壽命。 C60結構中其分子內含有 30 個π鍵,可引發自由基加成反應,故被稱為自 由基海綿(free radical sponge),其具有良好的電子親和力,且有能力扮演自由 基清除劑的角色,例如濃度為 1.5×10-5mol/L 的 C 60會阻礙 AIBN 引發苯乙烯 (styrene)和甲基丙烯酸甲酯(methyl methacrylate)。由於高分子的氧化裂解是自 由基之鏈反應,包括烷基自由基和過氧烷基自由基,因此容易受到自由基捕捉 劑的抑制。由於奈米碳管其結構類似於 C60,具備良好的電子親和力,在自由 基之鏈反應中可被視為自由基捕捉劑,是因為奈米碳管打斷自由基反應之 chain propagation 階段,進而在高分子材料中形成抗氧化效應,由此可知,奈 米碳管也具有良好的吸收自由基能力。[30] 本研究是利用奈米碳管具有吸收自由基之特性來研究不同劑量及種類之 奈米碳管對聚氯乙烯其熱穩定性之影響,來了解奈米碳管是否能作為聚氯乙烯 之有效熱安定劑,藉由將不同劑量與種類之奈米碳管添加於聚氯乙烯進行加熱 老化試驗,在固定 180 ℃加熱溫度但改變時間參數的條件下,以 UV-vis 和 FTIR 測定來分析添加微量未改質與改質之奈米碳管對聚氯乙烯裂解後所生成之碳 碳雙鍵的影響,且觀察聚氯乙烯其顏色變化。另外,藉由聚氯乙烯之靜態熱穩 定性試驗來研究添加不同比例及種類之奈米碳管對聚氯乙烯受熱後所釋放 HCl 之程度,以 TGA 熱重分析來觀測添加不同種類奈米碳管對聚氯乙烯的重 量損失及熱裂解溫度之變化,並透過 GPC 分析來了解不同加熱老化時間下各 種奈米碳管對聚氯乙烯分子量的影響。第三章
實驗內容
3.1 實驗藥品
1.聚氯乙烯(Poly(vinyl chloride),PVC),型號:S-80,K 值:79.4~81.1,平均 聚合度:1800±50,台灣塑膠工業股份有限公司。
結構:
2.四氫呋喃(Tetrahydrofuran,THF),純度:99.5%,AVANTOR PERF MAT-JT BAKER LAB。
結構:
3.二茂鐵(Ferroncene,C10H10Fe),純度:98%,Sigma-Aldrich。 結構:
5.硫酸(Sulfuric acid,H2SO4),純度:95~97%,Sigma-Aldrich。
6.硝酸(Nitric acid,HNO3),純度:69~70%,AVANTOR PERF MAT-JT BAKER LAB。
3.2 實驗設備
1.熱重分析儀(Thermogravimetry analyzer, TGA) 廠牌:TA Instruments
型號:SDT-Q600
2.傅立葉轉換紅外線光譜儀(Fourier transfer infrared spectrometer, FT-IR) 廠牌︰Perkin-Elmer
型號︰Spectrum Two
3.紫外光/可見光譜儀(Ultraviolet/visible spectroscopy, UV/vis) 廠牌︰Perkin Elmer
型號︰Lambda-35
4.微差掃描熱卡儀 (Differential scanning calorimeter, DSC) 廠牌:TA Instruments
型號:DSC-Q100
5.FE-SEM (Field emission scanning electron microscopy) 廠牌︰HITACHI 型號︰S-4800 6.恆溫油浴槽 廠牌︰DENGYNG 型號︰DOB-10 代理商: 明昱科技儀器有限公司 7.超音波震盪器(ultrasonic cleaner) 型號:DC-80
![圖 1-6 PVC 之離子型裂解機制[8]](https://thumb-ap.123doks.com/thumbv2/9libinfo/8793006.220812/18.892.144.770.127.290/圖16PVC之離子型裂解機制8.webp)