國立宜蘭大學生物技術研究所 碩士論文
Institute of Biotechnology National Ilan University
Master Thesis
利用微奈米免疫脂球建立一免疫吸附法以檢測仙人掌桿菌 An assay development for the detection of Bacillus cereus with
the use of immunoliposomal micro/nano vesicles
指導教授:陳威戎博士
Wei-Jung Chen, Ph. D.
溫曉薇博士
Hsiao-Wei Wen, Ph. D.
研究生:梁譽耀
Yu-Yao Liang
中華民國九十七年八月
謝誌
回想起這兩年的時間,來回宜蘭與台中,一路上跌跌撞撞,但也使我深深
感受到友情和親情的扶持與鼓勵。現在,終於到了可以感謝各位的時候。
常笑著自己當初進入生物技術研究所的時候就像文盲一樣,還好遇見我的指 導教授 溫曉薇老師,用盡耐心與關心教導學生,使學生獲得此生受用不盡的知 識與觀念,使學生在研究的領域上獲得啟發與指引。同時也感謝為了學生的口 試,百忙之中從宜蘭遠到台中來的陳威戎老師在這兩年間的關心、鼓勵與指導,
使學生備感溫暖。感謝周志輝老師平時在生活上給予學生創新的想法及口試中給 予學生寶貴的意見。
感謝清大周鳳英老師及筱萍、雅亭學姐在學生的實驗技術上奠定良好的基礎 與觀念。使學生在之後的實驗進展上勇敢邁進而不擔心受怕。
在草創時期的實驗室中,感謝有元氣指導力的俐儀學姊、活潑的琇惠、可愛 的心怡與雅琪,使我在生活上得到歡樂,給予我全方位的支持而不覺寂寞。當實 驗室來到中興大學食生所之初,感謝希銀同學助我一臂之力讓我順利完成搬遷,
隨之而來的陌生與孤單感,則要感謝生技所的薇頻、生物晶片研究室的佳緯學 姊、瑋育、幸蓉、吟曲及宗聖的熱情與誠懇引領我進入這個大家庭,深深的感受 到人情味。食品微奈米科技實驗室隨著學期的開始,在新生的加入後,漸漸熱鬧 了起來。實驗室中,很感謝敬業樂群的明強在每個日子的義氣相挺、夢中情人的 霈慈默默支持、低調俏皮的心怡安慰鼓勵、活潑聰明的琇惠快樂分享、正義直言 的旃暥互助合作、單純愛笑的翊婷認真聆聽、快樂愛家的雅芳單純志氣、機智聰 明的汶哲默默耕耘、國際觀寬廣的婉甄、活力滿檔的雅芬及認真的傑鴻,伴我在 實驗室奇妙的每一天。感謝周老師實驗室的宗翰給我的資源與努力的標竿。感謝 生物資源加工實驗室的珮堯學姊、振能、千琇、例雅、宜欣、鈺惠及怡菁給我一 個積極、正面的避風港,使我能沉澱、冷靜的思考。謝謝你們在 506 實驗室及食 生所的大家。
感謝在生技所的同學,雖然相處的時間不多,但足智多謀的春榮、可靠實在 的明傑、趣味豪氣的彥均、溫文搞笑的紹凱、安靜沉著的卓臻、溫柔自信的楹涵 與耐心包容的賴技士葉卿在我每次回到宜蘭時你們給予我的熱情跟關心我都一 直銘記在心。感謝佳煒、子甯、殿強、耀文、彥閔、本強同學們的陪伴與談心。
最後的感謝將留給我的家人,感謝我的父母與兄弟在這兩年當中對我持續的 支持與鼓勵,讓我無後顧之憂的進行研究,讓我知道所有的難關都須忍耐且努力 前進,以得到最後甜美的結果。沒有你們就沒有我今天的成果,我在此謹以最感 恩的心,獻上此論文,與你們共同分享我的喜悅與成果。
2008 年 9 月 3 日 梁譽耀 於 中興大學 食品微奈米科技實驗室 506
I
中文摘要
仙人掌桿菌為台灣食品病原菌之一,而此株菌以傳統的微生物檢測方 式既耗時且費力。故此研究的目的在於發展以免疫微脂體搭配96孔平盤的 檢測系統-「免疫微脂體-螢光免疫吸附法」,對於仙人掌桿菌進行檢測。實 驗將先探討仙人掌桿菌生長的最適化條件,包含培養基種類 (TSB、NB及 PCB)及溫度 (30、35、40及45℃),以尋找出可以產生最短世代時間的培養 條件。繼之,「免疫微脂體-螢光免疫吸附法」的建立將分別對於96孔微量 盤及免疫微脂體做適當的參數調整以達到最佳的偵測靈敏度。在對96孔微 量盤做最適化的調整中,包含(1)捕獲抗體在不同pH值與鹽濃度的塗佈環 境、(2)捕獲抗體的濃度及(3)阻礙 (blocking)溶液的種類及濃度。在免疫微 脂體的最適化的調整中,將探討其(1)抗體活性的篩選、(2)免疫微脂體的粒 徑大小、(3)表面抗體佔總脂質莫耳數的修飾百分比及(4)免疫微脂體的濃度 對靈敏度的影響;繼之,將最適化的免疫微脂體-螢光免疫吸附法應用於仙 人掌桿菌存在於緩衝溶液中的專一性、靈敏度及偵測極限進行測試。
仙人掌桿菌在生長的最適化研究方面得到;當菌體培養在40℃的TSB 中將會有最短的生長世代及最高的菌體濃度。而在96孔微量盤的製備中;
抗體需以0.1 M PBS (pH 9.6)稀釋至5 μg/mL以進行捕獲抗體的塗佈(4℃、12 hr),再以0.05% casein阻絕溶液進行作用後 (37℃、2 hr),最後以含0.01%
casein與0.05% Tween-20的0.01 M PBS清洗溶液清洗後即完成微量盤的製 備。而最適化免疫微脂體為粒徑287 nm、表面抗體為總脂質0.05 mol%的修 飾比例的免疫微脂體,並以250 nmole/mL的濃度進行檢測。樣品未經大量 培養(enrichment)時,其檢測靈敏度達到105 CFU/mL。專一性方面,9個菌 種當中具有78%專一性與產生22%的偽陽性。而當樣品在TSB培養基增殖 14小時後,其偵測極限可達到0.083 CFU/mL。
關鍵字:仙人掌桿菌、免疫吸附法、微脂體、免疫微脂體
II
Abstract
Bacillus cereus, a major foodborne pathogen in Taiwan since the conventional plate culture techniques are time-consuming and laborious, the goal of this study is to develop the immunoliposomal nanovesicle sandwich fluorescence (ILN/SF) assay to detect B. cereus, with the use of microtiter plate reader to automatize the process and to simultaneously evaluate a large amount of samples. First, in order to find the optimal enrichment condition for B.
cereus, we used combinations of different medium (TSB, NB and PCB) and temperatures (30, 35, 40 and 45℃). Then, in finding the optimal condition for producing microtiter plate, different coating buffers, blocking buffer and antibody (Ab) coating density have been applied. Moreover, the optimization of immunoliposome (IM) was processed by studying different sizes, Ab mol%, and IM concentrations. Finally, the established assay was applied to determine the specificity, sensitivity and limit of detection (LOD).
The optimal condition of preparing microtiter plate is coated with 5 μg/mL of antibody dissolved in 0.1 M PBS (pH 9.6) and blocked with 0.05% casein dissolved in 0.01 M PBS (pH 7.2). The optimal condition of immunoliposome was 287 nm with 0.05 mol% of antibody and concentration as 250 nmole/mL.
Without enrichment, the LOD was 1 x 105 CFU/mL. In the analysis with 9 different bacteria, the specificity was 78% and the false positive value is 22%.
After a 14 h-enrichment, the LOD could be as low as 0.083 CFU/mL in TSB.
Therefore, this developed assay was able to provide a novel protocol for the rapid detection of B. cereus with a high sensitivity.
Keyword: Bacillus cereus, immunoassay, liposome, and immunoliposome
III
目錄
中文摘要...I 英文摘要...II 目錄...III 表目錄...V 圖目錄...VI 縮寫表...VII
第一章、文獻回顧...1
1-1、食物中毒 ...1
1-1-1、細菌性食物中毒(感染型及毒素型) ...1
1-1-2、台灣區歷年食物中毒案件...3
1-2、仙人掌桿菌 ...3
1-2-1、特性 ...3
1-2-2、感染源與汙染途徑...5
1-2-3、致病機制及中毒症狀...6
1-2-4、仙人掌桿菌檢測法...7
1-3、微脂體 ...12
1-3-1、組成、結構及分類...12
1-3-2、微脂體之製備...15
1-3-3、免疫微脂體之製備...17
1-4、免疫分析技術 ...19
1-4-1、免疫微脂體分析...21
第二章、仙人掌桿菌之免疫螢光分析技術...25
2-1、摘要 ...25
2-2、實驗流程圖 ...26
2-3、藥品與材料 ...27
2-4、方法 ...29
2-4-1、仙人掌桿菌之最適化培養...29
2-4-2、抗體活性分析...29
IV
2-4-3、免疫微脂體之製備...30
2-4-4、微脂體之磷濃度測定-磷酸含量測定法 ...32
2-4-5、粒徑分析...32
2-4-6、免疫微脂體-螢光免疫吸附法之建立 ...33
2-4-7、靈敏度分析...34
2-4-8;專一性分析...34
2-4-9、仙人掌桿菌在培養基中的檢測極限...34
第三章、結果與討論...35
3-1、仙人掌桿菌之最適化培養 ...35
3-2、抗體活性分析 ...36
3-3、含 SRB 螢光染劑之免疫微脂體之製備...36
3-4、96 孔微量盤的最適化環境 ...37
3-4-1、阻礙溶液的種類與濃度最適化...37
3-4-2、捕獲抗體的塗佈環境最適化...38
3-4-3、捕獲抗體濃度的最適化...39
3-5、免疫微脂體最適化 ...39
3-5-1、免疫微脂體的尺寸對於檢測的影響...40
3-5-2、免疫微脂體表面修飾比例對檢測檢測的影響...40
3-5-3、免疫微脂體濃度對檢測的影響...40
3-6、靈敏度分析 ...41
3-7、專一性分析 ...41
3-8、仙人掌桿菌在培養基中的檢測極限 ...42
第四章、結論與未來展望...43
第五章、參考文獻...63
V
表目錄
表1-1、仙人掌桿菌聚合酶鏈鎖反應所使用之引子及其對應之毒素基因與
片段大小...9
表1-2、仙人掌桿菌在不同檢測法之比較 ...10
表1-3、仙人掌桿菌於商業檢測法之比較 ...11
表1-4、常用的微脂體組成成分 ...13
表1-5、架橋分子的結構與官能基 ...18
表1-6、微脂體在 96 孔平盤的應用 ...24
表3-1、仙人掌桿菌對於不同培養條件下的生長結果之比較 ...47
表3-2、仙人掌桿菌對於不同培養條件下的繼代時間 ...48
VI
圖目錄
圖1-1、2003~2006 年細菌性食物中毒統計圖 ...3
圖1-2、仙人掌桿菌孢子囊的外層結構圖 ...4
圖1-3、仙人掌桿菌的薄切片孢子 ...5
圖1-4、磷脂質結構 ...12
圖1-5、磷脂質的極性頭端種類 ...13
圖1-6、微脂體種類 ...14
圖1-7、單層微脂體的粒徑大小比較 ...15
圖1-8、抗體及 PEG 進行表面修飾的微脂體...17
圖1-9、此研究所使用的免疫微脂體製備 ...19
圖1-10、此研究所使用的檢測分析方式 ...24
圖2-1、實驗流程圖 ...26
圖3-1、仙人掌桿菌 F4810 以不同培養條件培養的生長曲線...44
圖3-2、仙人掌桿菌 4552 以不同培養條件培養的生長曲線 ...45
圖3-3、仙人掌桿菌 11778 以不同培養條件培養的生長曲線 ...46
圖3-4、抗仙人掌桿菌膜蛋白抗體之活性分析 ...49
圖3-5、微脂體的粒徑分析 ...50
圖3-6、SMCC 修飾後的抗體之管柱層析 ...51
圖3-7、免疫微脂體-抗體混合物之管柱層析...52
圖3-8、抗體與微脂體之接合率 ...53
圖3-9、阻礙溶液對於檢測之影響 ...54
圖3-10、捕獲抗體在不同塗佈條件之下的表現能力 ...55
圖3-11、不同濃度的捕獲抗體對於檢測之影響 ...56
圖3-12、不同粒徑的免疫微脂體對於檢測之影響 ...57
圖3-13、不同修飾抗體比例的免疫微脂體對於檢測的影響 ...58
圖3-14、不同濃度的免疫微脂體對於檢測的影響 ...59
圖3-15、最適化免疫微脂體檢測的靈敏度試驗 ...60
圖3-16、最適化免疫微脂體檢測的專一性試驗 ...61
圖3-17、仙人掌桿菌接種於 TSB 培養基中的檢測極限...62
VII
縮寫表
Abbreviation Full text
AP alkaline phosphatase
BCET-RPLA kit B. cereus enterotoxin-reversed passive latex agglutination kit BDE-VIA Bacillus diarrheal enterotoxin visual immunoassay
CF carboxyfluirescein
CIA colony immunoassay
CMC critical micelle concentration
competitive ELISAs competitive Enzyme-linked sorbent assays DCT direct-charge transfer
DPPC dipalmitoylphophatidyl choline DPPE dipalmitoylphophatidyl ethanolamine DPPG dipalmitoylphophatidyl glycerol
EDC 1-ethyl-3-(3-dimethylaminopropyl)carbodiimide ELISA enzyme-linked immunosorbent assay
EMIT enzyme-multiplied immunoassay technique FPIA fluorescence polarization immunoassay
f-PSA free prostate specific antigen
HBL hemolysin BL
HBV hepatitis B virus
HRP horsedish peroxidase IL-2 interferon-2
ILSF immunoliposomes sandwich fluorometric assay immuno-FRET immunofluorescence resonance energry transfer IUVs intermidium unilamellar vesicles
LIA liposome immunoaggregation assay
LIC liposome immunocompetition LUVs large unilamellar vesicles
MCC-PE maleimidomethyl cyclohexane-carboximide-PE
VIII
MEIA microparticle enzyme immunoassay MLVs multi-lamellar vesicles
MPB N-4-(p-maleimidophenyl)butyrate MPB-PE maleimidophenyl butyramide-PE MYP mannitol-egg yolk-polymyxin NHE non-hemolytic enterotoxin OG-514 oregon green-514
PA phosphatidyl acid
PCBs polychloride benzenes PCR polymerase chain reaction
PDP-PE pyridyldithiopropionate-PE PE phosphatidylethanolamine PEG polyethylene glycol
PG phosphatidylglycerol PI phosphatidylinositol PI-PLC phosphatidylinositol phospholipase C PS phosphatidylserine QCM quartz crystal microbalance
SATA N-succinimidyl S-acetylthilacetate
SMCC succinimidyl-4-(N-maleididomethyl)-cyclohexane-1-carboxylate SPDP N-succinimyidyl-3-(2-pyridyldithio)propionate
SPR surface plasma resonance
SRB sulforhodamine B
SUVs small unilamellar vesicles
UVs unilamellar vesicles VEGF-C vascular endothelial growth factor-C
X-IP 5-bromo-4-chloro-3-indoxyl-myo-inositol-1-phosphate OSM osmotility
1
第一章、文獻回顧 1-1、食物中毒
依流行病學及美國疾病防治中心採用之定義,食物中毒為攝取到病 毒、細菌、寄生蟲、重金屬、環境及食物本身產生的毒素汙染的食物,而 造成兩人或兩人以上發生噁心、腹痛、嘔吐及腹瀉的中毒症狀。並且自可 疑的食餘檢體及患者糞便、嘔吐物、血液等人體檢體,或者其他有關環境 檢體 (如空氣、水、土壤) 中分離出相同類型 (如血清型、噬菌體型) 的致 病原因,則稱為一件「食物中毒」,但如因攝食肉毒桿菌或急性化學性中 毒時,就算只有一人,也可視為一件「食物中毒」1。而病原菌引發的食品 中毒可分為兩型,一為攝取大量的菌體進入腸胃道,再增殖菌體而導致的 病徵稱作「感染型」。另一型則是因為攝取到菌體在繁殖期間產生的有毒 物質而導致的「毒素型」食物中毒2。
1-1-1、細菌型食物中毒(感染型及毒素型)
毒素型
肉毒桿菌 (Clostridium botulinum),屬革蘭氏陽性,厭氣性桿菌,周邊 有鞭毛,具運動性,多分布於土壤、海、湖、川之沙泥中,在缺氧狀態下 易培養且產生毒素3。毒素產生於營養態菌體生長與孢子轉換成營養態菌體 時。毒素阻斷神經與肌肉的突觸,導致神經傳導中斷。或是與神經細胞作 用而抑制神經傳導物質 (例如:乙醯膽鹼)釋放4,主要症狀為神經麻痺。中 毒潛伏期約12-30小時,發病期3-7天,特異症狀有視力減退、複視、瞳孔 散大、眼皮下垂等眼部症狀及言語障礙、吞嚥困難、唾液分泌障礙、口渴 等3。此類中毒致命率占所有細菌性食品中毒的第一位。食品加工過程中,
混入菌體或芽胞,且滅菌不完全,造成此菌將生長於食品中,通常以罐頭 食品、香腸等加工品為主要原因食品。食品原料應充分洗淨,香腸、火腿 類應注意亞硝酸鹽的添加量是否均勻,則可預防此菌感染。
金黃色葡萄球菌 (Staphylococcus aureus),為革蘭氏陽性,兼性厭氧
2
菌,可在高滲透壓與低濕度的環境下生長 (例如鼻腔或皮膚),最適生長溫 度為37℃。其產生的毒素具有很高的熱穩定性,即使存在沸水中30分鐘,
也還能保持活性4。主要症狀為嘔吐、腹痛及腹瀉4。常存於人體皮膚、毛 髮及鼻腔、咽喉等黏膜2, 4,因此極易經由人體而污染食品。主要中毒原因 食品為受污染的火腿等肉製品、乳製品、魚貝類、便當或生菜沙拉等1。 感染型
腸炎弧菌 (Vibrio parahaemolyticus),為革蘭氏陰性菌,兼性厭氧菌,
菌體略呈彎曲,有單極鞭毛,活動性強,主要分布於近海河囗及海底泥沙 的含鹽水體中,因此主要引起中毒之原因食品為海產類或受到間接污染的 食品4。潛伏期約為2-48小時,平均為10-18小時,主要症狀是下痢、激烈 腹痛、噁心、嘔吐、頭痛、發燒、寒顫等。但此菌對低溫極敏感,可用冷 藏或加熱 (60℃,l5分鐘)方式避免此菌種汙染2。
沙門氏菌 (Salmonella spp.),是因幾乎所有沙門屬的菌種皆可能致 病。革蘭氏陰性桿菌,無芽胞,貝有鞭毛,好氣性或兼性厭氧菌。主要存 在溫體動物的腸道中4,容易汙染肉品、鮮蛋、乳品等動物性食品或蛋白質 含量較高的植物性食品。中毒的潛伏期平均為18-36小時,主要症狀為下 痢、腹痛、寒顫、發燒 、噁心、嘔吐等2。
仙人掌桿菌 (Bacillus cereus),革蘭氏陽性,兼性厭氧菌,可產孢子,
生長溫度為l0-45℃,可耐熱 (於100℃下經1-7.5分鐘僅可殺滅90%)。廣泛 分布於自然界,可由細菌本身或其產生之毒素致病。中毒症狀可分為由兩 種,一為具熱穩定性的小分子胜肽所造成的嘔吐症狀,潛伏期約1-6小時,
及另一種為大分子蛋白質毒素所造成的下痢症狀,潛伏期約8-16小時5。而 高澱粉食物易導致嘔吐症狀的發生,如米飯、馬鈴薯及義大利麵等。腹瀉 型症狀主要由高蛋白含量的食物所導致,例如肉類製品與乳類製品等5。 病原性大腸桿菌 (Enteropathogenic Escherichia coli),革蘭氏陰性菌,
兼性厭氧菌,其最適生長的pH值為6-72。感染後的潛伏期平均為5-48小時。
3
中毒症狀主要為菌體侵入人體之腸管而引起類似志賀氏桿菌毒素 (例如:
verotoxin) 的中毒症狀造成水樣便、血便及脫水等症狀5。若症狀持續發生 有可能導致電解質不平衡而死亡。生的牛肉或雞肉為感染的食品,常針對 嬰兒、衛生環境不良的地區或是第三世界國家造成流行性的感染6。 1-1-2、台灣區歷年食物中毒案件
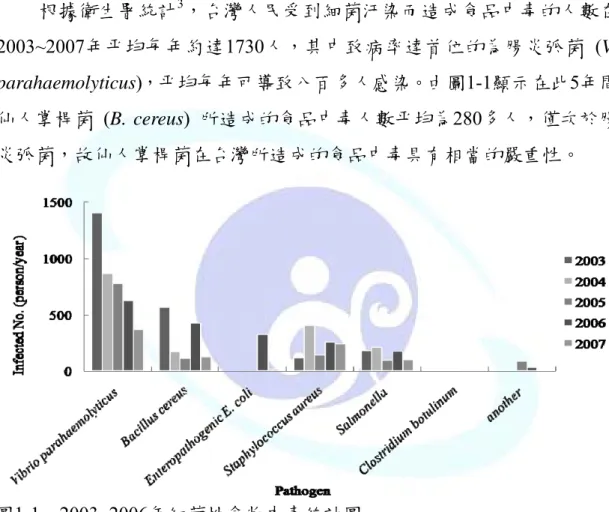
根據衛生署統計3,台灣人民受到細菌汙染而造成食品中毒的人數在 2003~2007年平均每年約達1730人,其中致病率達首位的為腸炎弧菌 (V.
parahaemolyticus),平均每年可導致八百多人感染。由圖1-1顯示在此5年間 仙人掌桿菌 (B. cereus) 所造成的食品中毒人數平均為280多人,僅次於腸 炎弧菌,故仙人掌桿菌在台灣所造成的食品中毒具有相當的嚴重性。
1-2、仙人掌桿菌
1-2-1、特性
仙人掌桿菌 (B. cereus) 為食品病原菌,其菌體的長寬分別為5-10 μm 與1 μm,革蘭氏陽性,具有好氧或是兼性厭氧的能量代謝模式,並且能在 有氧環境下產生內孢子。也因為其生長環境無特別的營養需求,使得此菌 圖1-1、2003~2006年細菌性食物中毒統計圖。
Figure 1-1. The statictics of bacterial food poinsoning in 2003-2006.
4
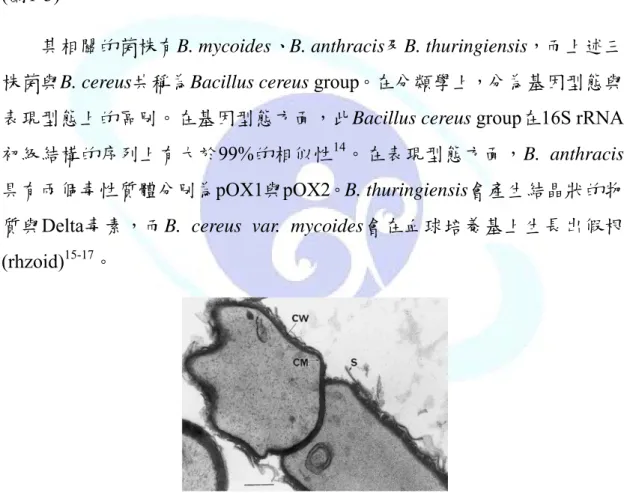
株能夠廣泛存在於自然界中的土壤與植被中7-12。營養態的菌株經過穿透式 電子顯微鏡的圖1-2顯示,其細胞壁表面被大量S-層蛋白所覆蓋,此蛋白用 以穩定其他細胞壁結構13。最適合的生長溫度範圍從攝氏25度到37度,其 分裂的時間為20-30分鐘,是生長相當快速的菌種。仙人掌桿菌的孢子態並 沒有代謝的活性,但可承受極端的外在環境,例如:耐低溫、耐熱、耐乾 旱與輻射傷害等13。此孢子和其他仙人掌桿菌屬的孢子相似,並不會膨脹 其 孢 子 囊 , 而 從 孢 子 的 核 心 (core) 向外層層依序圍繞著內膜 (inner membrane)、皮質 (cortex)、內夾膜 (inner coat) 與外夾膜 (outer membrane) (圖1-3) 13。
其相關的菌株有B. mycoides、B. anthracis及B. thuringiensis,而上述三 株菌與B. cereus共稱為Bacillus cereus group。在分類學上,分為基因型態與 表現型態上的區別。在基因型態方面,此Bacillus cereus group在16S rRNA 初級結構的序列上有大於99%的相似性14。在表現型態方面,B. anthracis 具有兩個毒性質體分別為pOX1與pOX2。B. thuringiensis會產生結晶狀的物 質與Delta毒素,而B. cereus var. mycoides會在血球培養基上生長出假根 (rhzoid)15-17。
圖1-2、仙人掌桿菌孢子囊的外層結構圖。CM;細胞膜,CW;細胞壁,S;
表面層 13。
Figure 1-2. Ultrastructure of B. cereus sporangium. CM: cytoplasmic membrane;
CW: cell wall; and S: surface layer 13.
5
1-2-2、感染源與汙染途徑
有許多種食物可以被仙人掌桿菌或其孢子所汙染,如:義大利麵、通心 麵、米飯、鮮奶或乳製品、香料與乾燥的肉類、雞肉、海鮮、穀類、蔬菜
水果等10, 12-23。造成腹瀉症狀的食物大致可歸類為蛋白質含量較高的食
物,例如奶類製品等。而造成嘔吐症狀的食物則為澱粉含量較多的食物,
例如米飯、麵食等24。在過去1991-1994年間,全球飛機上3%的肉類餐點遭 受仙人掌桿菌的汙染25。另外在醫院供應的膳食與嬰兒食品若遭受到汙 染,也會對於免疫功能低下的病人或是新生兒造成感染26, 27。
因為仙人掌桿菌廣泛存在於自然界當中,不論是空氣、水中、土壤等 環境皆能發現其蹤跡而且具有容易從孢子體轉換成營養態的特性。就食品 的汙染而言,從食物的原產地、運輸、加工過程或是最後的食用與保存等 皆有可能發生汙染的情形,最後引發腸胃道感染。以牛乳為例,仙人掌桿 菌容易存在於乳牛的乳腺內而造成牛乳受到汙染27。另外,Ro¨nner的研究 團隊也發現此株菌容易與疏水性的牛乳加工設備產生黏附作用28。另外,
已知某些菌株的孢子會黏附於人類的上皮細胞,故孢子也是仙人掌桿菌傳 播的重要的媒介29。
圖1-3、仙人掌桿菌的薄切片孢子,IM;內膜,C;皮質,IC;內夾膜,OC;
外夾膜13。
Figure 1-3. A thin sectioned spore of B. cereus. IM: immer memebrane; C:
cortex; IC: immer coat, and OC: outer coat 13.
6
1-2-3、致病機制及中毒症狀
仙人掌桿菌主要會分泌外毒素造成宿主產生病徵並且引發免疫反 應,依菌體的分佈而會使得人體出現不同的疾病。依其分佈主要區分成腸 胃道感染及非腸胃道感染。
腸胃道感染亦稱為食物中毒,其中毒的症狀主要分為兩種型態,其中 一種為嘔吐型 (emetic syndrome),另一種為腹瀉型 (diarrheal syndrome)。
嘔吐症狀的發生主要起因於攝取到嘔吐毒素 (emetic toxin-cereulide),其結 構為類似纈氨黴素 (valinomysin) 的dodecadepsipeptide30, 31。具有耐高溫 (121℃)及耐酸鹼 (pH 2-11) 的特性,並且不受pepsin及trypsin的影響31。其 致病機制尚未被完全瞭解,根據過去的報告知道其作用機制是在細胞膜上 形成離子通透的孔洞,進而使得粒線體的氧化磷酸化失去功能,造成脹大 的粒線體,導致細胞死亡32。Hughes等研究者發現HEp-2細胞培養在含有嘔 吐型毒素的培養液會誘導HEp-2細胞的液胞形成33。另外,此毒素會經由細 胞膜上的5-HT3 受器而刺激迷走神經的傳導31,也會對於肝臟細胞中粒線 體 的 脂 肪 酸 氧 化 作 用 抑 制 進 而 導 致 肝 功 能 喪 失22。 腹 瀉 型(diarrheal enterotoxin) 的 致 病 毒 素 主 要 分 為 非 溶 血 型 毒 素 (non-hemolytic enterotoxin;NHE) 與溶血型毒素 (hemolysin BL;HBL)。NHE分別由三個 分子量為39、45與105 kDa的次單元蛋白所組成34,其基因分別為nheA、nheB 與nheC。在NHE的各個次單位的研究如下。在動物實驗中,Shinagawa等 人進行其腸胃道毒素的生物活性特徵評估得到,NHE的45 kDa次單位具有 提高血管通透性、小鼠致死毒性及在連結小鼠腸道後所造成的液體累積等 影響35。而在細胞研究中發現,NHE會在上皮細胞的脂雙層平面上形成孔 洞36。當細胞與NHE混合之後的滲透性的試驗中,以細胞直徑的增加可以 了解NHE會形成穿越膜的孔洞而使得滲透性不同而導致細胞破裂,最後使 細胞死亡37。另外,HBL毒素分別由B、L1及L2三種次單位蛋白所組成,基 因分別為hblA、hblC與hblD;而其蛋白質分子量分別為35、36與45 kDa。
HBL的組成蛋白B、L1與L2的功能過去區分成:B為結合用分子,L1與L2為 溶解用分子38。從含血球培養基的孔洞中加入HBL毒素可以觀察到毒素從
7
孔洞內擴散出去而形成很清楚的溶血環39。但在1997年,Beecher與Wong 的研究中發現HBL的機制是三種次單位會各自與紅血球的膜結合,之後再 聚集成為有功能的複合物,此複合物將會形成穿透膜的孔洞而導致細胞質 滲透的破裂機制40。
仙人掌桿菌亦會因其他途徑的汙染而造成非腸胃道系統及傷口的感 染,例如:靜脈注射或接觸等。而其感染的對象主要為免疫功能低下的患 者、嬰兒、藥物成癮的人、創傷、手術傷口、使用導尿管的病患及眼部的
感染13, 16, 40, 41。以皮膚的創傷而言,如:手術後的傷口、創傷等,皆會受到
仙人掌桿菌所分泌的HBL所影響42, 43。而大部分的感染皆是輕微的,但也 有發生過嚴重的皮膚壞死及化膿等感染症狀。仙人掌桿菌亦是造成眼部感 染重要的病原菌之一,其常見的症狀有角膜炎、眼內炎與眼球炎13, 43。 Beecher與Alfaro各自的團隊也發現HBL毒素會導致視網膜剝離及壞死而造
成失明43, 44。組織系統的感染雖然不常見,但是有可能會因為人工心臟瓣
膜、風濕性心臟病或是毒品的注射而造成心內膜炎15, 45。過去也有文獻記 載其他受仙人掌桿菌影響的疾病如腦膜炎、致命性腦膜炎、肺炎、尿道炎、
猛爆性肝炎等非腸胃道疾病15, 21, 46-48
。另外在口腔的感染方面,也有文獻 曾指出與青少年齒齦炎有關49。
1-2-4、仙人掌桿菌檢測法
傳統的仙人掌桿菌檢測方法概略先以選擇性培養基檢測卵磷脂酶的 產生、甘露糖 (mannitol) 的發酵作用50,並且從選擇性甘露糖-蛋黃-多黏 桿菌素 (mannitol-egg yolk-polymyxin B;MYP) 培養基中選出可疑菌落 後,再搭配此株菌體不具有假根生長及蛋白質毒素晶體,但具有泳動性的 菌落外觀形態來大致區別。而在生化試驗當中,會在觸酶試驗(catalase test) 中會產生氣泡、能分解酪胺酸、能在無氧環境中利用葡萄糖產生酸、使硝 酸鹽 (nitrate) 的還原、在歐普氏 (VP test) 試驗中能產生粉紅色、具有β- 溶血作用 (β-hemolysis)、能耐受溶菌酶(lysozyme)等反應51。以MYP培 養基為例,因為仙人掌桿菌無法利用甘露糖作為醣類的來源,故無法產酸
8
使培養基呈現粉紅色。仙人掌桿菌可產生卵磷脂酶以分解培養基所含有的 卵磷脂而造成菌落周圍產生環狀的乳白色沉澱。最後,因為仙人掌桿菌是 革蘭氏陽性菌,培養基內所含的多黏桿菌素B能抑制革蘭氏陰性菌的生長 而篩選出革蘭氏陽性菌50。硝酸鹽 (nitrate) 還原成亞硝酸鹽 (nitrite) 的生 化分析方面,是將菌落培養在5 mL並含有0.1%硝酸鹽的培養基 (0.3% beef extract,0.5% peptone) 中24小時 (35℃),之後分別加入0.25 mL的A及B試 劑 (A:0.8% sulfanilic acid的5 N醋酸溶液。B:0.5% α-naphthol的5N醋酸溶 液),反應在10分鐘之內完成,硝酸鹽會被仙人掌桿菌還原成橘紅色的亞硝 酸鹽51。但是因為仙人掌桿菌存在著非典型菌株,造成傳統及後續的生化 檢測方式無法提供絕對的專一性,故對於食品中毒的機會相對的提供了不 確定性。
Shelef的研究團隊在2001年發展出一種利用顏色來區分仙人掌桿菌屬 的選擇性培養基,其原理為在培養基中加入5-bromo-4-chloro-3-indoxyl- myo-inositol-1-phosphate (X-IP),此物質會經由仙人掌桿菌屬的菌體所產生 的phosphatidylinositol phospholipase C (PI-PLC)分解而在菌落四周產生藍 色區域,但此種培養基不能分辨同屬的B. cereus與B. thuriugiesis菌株,且 須 耗 時39 小 時 才 能 觀 察 結 果50。 繼 之 ,Moravek 等 人 發 展 出 colony immunoassay (CIA)檢測法,將仙人掌桿菌的毒素蛋白質吸附在硝化纖維膜 上,再利用兩種單株抗體分別針對HBL的B次單元及NHE的nhe A次單元進 行偵測,共需花費22.5小時52。另外,Bruno等人利用免疫螢光能量轉移分 析法 (immunofluorescence resonance energry transfer;immuno-FRET) 檢測 仙人掌桿菌孢子。利用Oregon Green-514 (OG-514)標定在抗仙人掌桿菌孢 子的抗體被激發,以進行同質競爭性 (homogeneous competitive assay)螢光 檢測。在加入孢子檢測物之前,OG-514是被原存在的孢子上另一個QSY-7 螢光分子消光 (qenuch) 而無法被激發,當分析物存在之後會與QSY-7孢子 競爭抗體而遠離QSY-7產生螢光。其檢測時間需要15分鐘,而其檢測極限 達 到1.0 x 105- 2.5 x 105 spore/mL53。 另 外 在 搭 配 電 化 學 檢 測 法 的 direct-charge transfer (DCT)分析中,Sudeshna等人將抗仙人掌桿菌抗體鍵結
9
上polyaniline,再與仙人掌桿菌樣本混合後,利用固定有抗仙人掌桿菌抗 體的硝化纖維膜與抗體-菌混合液進行側流分析,而使polyaniline-antibody- 仙人掌桿菌留存於膜上,再利用因polyaniline而形成的電流通路而進行檢 測54, 其 檢 測 時 間 只 需6分鐘,在緩衝溶液中的檢測極限可達101-102 CFU/mL。在生物分析模式上,當仙人掌桿菌嘔吐型毒素的含量達到1.5 ng/mL以上時,也可利用牛精蟲 (含2.7 x 107 cells) 的泳動性下降進行半定 量評估55。另外,也發展出利用Ped-2E9細胞對於仙人掌桿菌胃腸道毒素進 行檢測,對於毒素的靈敏度可達0.3-0.4 μg/mL,但其所有的檢測需費時19 個小時以上56。
在DNA檢測法中則是應用蝦子中分離出來仙人掌桿菌BIS59的質體,
以限制脢Bgl II切割而得到的3kb片段並以α-32P-dCTP放射性標定後可作為 偵測仙人掌桿菌的DNA探針,所檢測時間為124小時57。聚合脢鏈鎖反應 (polymerase chain reaction;PCR)是目前廣泛被應用於分子檢測的工具,利 用能合成毒性基因的引子 (表1-1) 與待測菌體的DNA混合後進行毒基因 的合成與分析,其所耗費時間約3-4小時52,對於被仙人掌桿菌所汙染的脫 脂奶粉試驗中,靈敏度可達到25-46 CFU/g58。但是PCR技術反應的是基因 體的資訊,並不代表菌體在真實情況的表現。過去文獻也指出,即使以PCR 方式檢測出仙人掌桿菌的毒素基因片段,但是利用其他的溶血性試驗或是 傳統的卵磷脂脢檢測皆無法提供相同的印證59。以上所介紹的仙人掌桿菌 檢測法整理於表1-2。
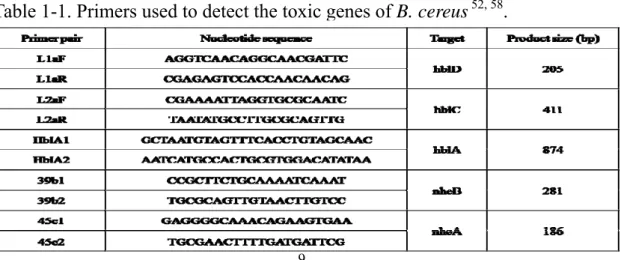
表1-1、仙人掌桿菌聚合酶鏈鎖反應所使用之引子及其對應之毒素基因與片段 大小52, 58。
Table 1-1. Primers used to detect the toxic genes of B. cereus 52, 58.
10
表1-2、仙人掌桿菌在不同檢測法之比較。
Table 1-2. Comparison of different methods for the detection of B. cereus.
11
目前有三組商業化的仙人掌桿菌腸胃道毒素檢測套件 (表1-3),其中 一 種 為 仙 人 掌 桿 菌 腸 胃 道 毒 素 逆 向 式 被 動 膠 體 凝 集 試 劑 (B. cereus enterotoxin reversed passive latex agglutination kit;BCET-RPLA kit)是用來檢 測HBL毒素中的L2次單元。其原理是將抗體與聚苯乙烯乳膠顆粒結合再加 入至96孔盤中。若樣品含有L2次單元,則會導致接合抗體的聚苯乙烯乳膠 顆粒形成網狀結構的膠體而懸浮於微量孔中。相反的,若不含有L2次單元,
則乳膠顆粒會產生沉澱,故可用肉眼觀察結果,靈敏度為2 ng/mL 60。此法 雖然簡單,但首先必須將菌體活化6-18個小時;另外,在試劑與樣本作用 時,必須震盪20-24小時61, 62,相對耗時。第二種為偵測NHE毒素中的Nhe A 次 單 元 蛋 白 的 仙 人 掌 桿 菌 腹 瀉 型 腸 胃 道 毒 素 免 疫 分 析 試 劑 (Bacillus diarrheal enterotoxin visual immunoassay;BDE-VIA),其作用原理與ELISA 相同,偵測極限達1 ng/mL,可在4小時之內檢測出毒素的存在,但須將菌 體活化20小時以產生毒素34, 60, 63。最後一種是可同時偵測NHE與HBL的側 流分析試劑 (lateral flow assay Doupath® Cereus Enteroto),使用前不論是從 選擇性培養基取得的菌落或是食物樣本,都需先以CGY培養基培養以活化 菌體產生大量毒素。此產品可分為培養18-24小時的快速檢測與培養26~30 小時的精準檢測,其偵測極限分別達100 CFU/g及1 CFU/g。而對於純的 NHE與HBL毒素而言,檢測時間只需30分鐘,而靈敏度分別為6 ng/mL及 20 ng/mL64。以上三種試劑 (表1-3)的檢測對象皆為毒素,若食物中只含有 營養態或是孢子態的菌體則對食品安全的檢測上依然存在著隱憂。
表1-3、仙人掌桿菌於商業檢測法之比較。
Table 1-3. Comparison of commercial detection kits of B. cereus.
12
1-3、微脂體
微脂體是英國學者Alec Bangham在1965年所發現的。其大致的結構類 似於細胞,外圍具有磷脂雙層膜、中心含有液體的結構,並且能懸浮於水 相中。也因其似細胞的結構,可易於研究膜與膜之間磷脂質的交互作用、
離子的通透性、藥物、闡述殺蟲劑與抗生素對於目標微生物的作用機制
65-72。以下將介紹微脂體的組成、結構與分類、製備方法及目前的應用。
1-3-1、組成、結構與分類
微脂體的主要組成分子為磷脂質及膽固醇,將前述兩種物質混合並溶 於水相液體中會自然的組成仿細胞態的球型複合物。磷脂質的分子結構主 要是由甘油為骨幹,接著在甘油的一及二號碳接上脂肪酸鏈,在第三號碳 接上磷酸根分子 (圖1-4)。磷脂質的命名是根據分別接上的脂肪酸及磷酸 官能基而命名,常見的脂肪酸為:棕梠酸 (phosphatidic acid)、硬脂酸 (stearic acid)等;而在磷酸基上也分別接上不同的官能基,如:膽鹼 (choline)、乙醇胺 (ethanolamine)、甘油 (glycerol)、酸基 (acid)、絲胺酸基 (serine)及肌醇 (inositol)等。分別形成磷脂基膽鹼 (phosphatidylcholine:
PC) 、 磷 脂 基 乙 醇 胺 (phosphatidylethanolamine, PE) 、 磷 脂 基 甘 油 (phosphatidylglycerol:PG)、磷脂基酸 (phosphatidylacid:PA)、磷脂基絲 胺酸 (phosphatidylserine:PS)、磷脂基肌醇 (phosphatidylinosito:PI),如 圖1-5。而膽固醇的存在能夠穩定磷脂雙層膜的結構,降低膜的通透性,因 為其頭端會與磷脂基膽鹼產生氫鍵以穩定膜結構72。而為本研究所使用的 磷脂質成分如表1-4。
圖1-4、磷脂質結構。
Figure 1-4. The structure of phospholipid.
13
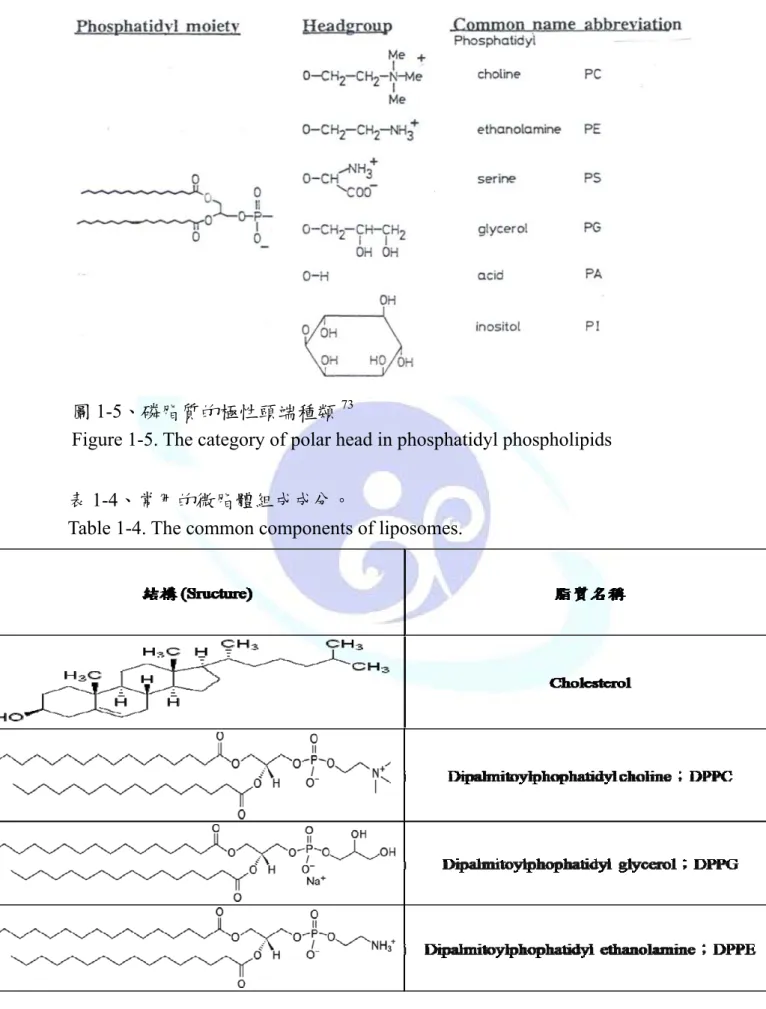
圖1-5、磷脂質的極性頭端種類73
Figure 1-5. The category of polar head in phosphatidyl phospholipids
表1-4、常用的微脂體組成成分。
Table 1-4. The common components of liposomes.
14
根據上述的組成成分,兩個磷脂質分子的脂肪酸長鏈將會因非極性作 用而形成疏水性區域,同時兩個親水性頭端將朝向水溶液而形成一個雙分 子複合體,在大量的雙分子複合體排列後,將形成一個封閉的脂雙層膜結 構如圖1-6,即所謂的微脂體。其結構近似於細胞膜,此種仿細胞膜的球型 複合體內部將形成一個含有水溶液的空腔,並且膜外部也將被水溶液所包 圍,脂雙層結構將隔絕內外溶液的流通,形成一個獨立的區域。
根 據 微 脂 體 的 構 造 如 圖1-6 , 主 要 可 以 分 為 同 心 圓 多 層 微 脂 體 (multi-lamellar vesicles;MLVs)、多液胞微脂體 (multi-vesicular liposomes;
MVLs)與單層膜微脂體 (unilamellar vesicles;UV)。同心圓多層微脂體,
粒徑分佈在0.4-3.5 μm,其特色是每顆微脂體內部再由多層磷脂雙層以同心 圓方式層層包裹。多液胞微脂體,粒徑約1-2 μm,每一大顆微脂體內部會 同時分佈多顆獨立存在之小微脂體。單層膜微脂體可再依粒徑大小細分為 三 種 ( 圖 1-7) , 由 小 至 大 分 別 為 小 單 層 膜 微 脂 體 (small unilamellar vesicles;SUVs),粒徑分佈在0.025 μm左右,其內腔包裹的水溶液非常小 量。中單層膜微脂體 (intermidium unilamellar vesicles;IUVs),粒徑分佈 在0.25 μm左右,內腔包含的水溶液量較SUVs多。大單層膜微脂體 (large unilamellar vesicles;LUVs),粒徑分佈在2.5 μm左右,可包覆較高比例的 水相。
圖1-6、微脂體種類73。
Figure 1-6. The categories of liposomes.
15
1-3-2、微脂體之製備
I. 機械性分散法 (Mechanical dispersion)
秤取不同種類的脂質,依比例均勻溶解於有機溶劑當中,再以減壓濃 縮機去除有機溶劑後,將可發現脂質混合物將在瓶壁上形成薄膜,最後再 加入欲包裹的水溶液物質進行脂質的震盪水合作用而形成大小不一的同 心圓多層微脂體 (MLVs)。同心圓多層微脂體 (MVLs)再經過不同的機械 分散的製備過程後,將形成不同類型的微脂體73。
A. 超音波震盪 (sonication)是廣泛使用於製備小粒徑微脂體的方法,其原 理是利用超音波震盪的外力使得原本的MLVs破裂後重新組合74,最後成為 小單層微脂體 (SUVs)。而此法分為探針式 (probe type)及水浴式 (bath type)超音波震盪,探針式主要針對於小體積且需要高能量的脂質混合物,
而水浴式超音波震盪主要是適合大量的樣本體積。探針式超音波機因功率 較強,易生熱而使脂質氧化降解,且有可能造成探針上金屬掉落而汙染樣 品的問題。
圖1-7、單層微脂體的粒徑大小比較73。
Figure 1-7. The comparative sizes of unilarmellar vesicles.
16
B. 膜 擠 壓 式 (membrane exclusion) 是 利 用 固 定 孔 徑 的 聚 碳 酸 酯 濾 膜 (polycarbonate filter)來過濾MLVs是更容易控制得到小粒徑的微脂體的方 式。此種濾膜並不會造成複雜且扭曲的三度空間而是單純的擠壓到膜的另 一端。膜擠壓式的優點為不論MLVs的原始粒徑是否等於孔徑,皆可經擠 壓而導致磷脂膜的重組,最後通過濾膜。也因為孔徑的固定將使得原先大 粒徑的微脂體變小,而最終形成粒徑平均的微脂體74。
C. 高壓均質法 (homogenization)則以法式高壓均質器 (French pressure cell)為例,其機心為不鏽鋼所組成的機體,可承受20000-40000 psi.的壓力。
將樣本置入裝置當中,經設定後,啟動裝置使活塞作動而蓄積壓力,直到 壓力強度達到閥門設定的抗壓極限時,原本儲存在裝置內的脂質混合物將 流出機心本體,因壓力使微脂體重組以達到包覆物被包裹的目的。此外,
提高操作的次數可使微脂體的粒徑大小達到一均勻度。其優點是可以大量 製造出粒徑平均的微脂體,縮短生產微脂體的時間75, 76。
D. 凍融法 (freeze and thaw)其原理是將水合後形成的MLVs微脂體,利用 極低溫的環境產生的水分子冰晶破裂微脂體,再利用微脂體轉變液晶態的 溫度環境下,重組微脂體的型態,在反覆的冷熱環境交替之下,最後將形 成單層微脂體77。
II. 乙醚注射法 (Ether injection)
將脂質溶於乙醚中,以針筒吸取乙醚脂質液後,將脂質混合物注射於 正在攪拌且溫度在60℃的水溶液中,藉由乙醚的快速蒸散,使得磷脂質形 成密閉LUV脂體,而粒徑大小會因脂質濃度及注射速率而改變78, 79。 III. 逆向蒸散法 (Reverse phase evaporation)
將小量的水溶液注射到大量且含有脂質的有機溶劑當中,再以震盪方 式將溶液變成小液滴。利用此方式形成微脂體分為兩個步驟,首先脂質會 先包圍水溶液 (water-in-oil)形成單層膜的形式,再利用第二次乳化或是有 機溶劑蒸散後,移除干擾膜形成的有機溶劑之後,即形成微脂體80。
17
IV. 界面活性劑溶解法 (Detergent solubilization)
界 面 活 性 劑 開 始 形 成 乳 糜 微 粒 時 的 最 低 濃 度 稱 為 臨 界 微 胞 濃 度 (critical micelle concentration;CMC)。將磷脂質與界面活性劑同時溶於水 溶液中,在達到CMC時將形成含有磷脂質與界面活性劑的乳糜微粒,此時 經過透析或膠體層析方式移除界面活性劑,而使乳糜微粒因為界面活性劑 的移除,最後達到只含有磷脂質的單層脂雙層膜的微脂體構造73。
1-3-3、免疫微脂體之製備
免疫微脂體主要是在微脂體的外圍接上生物辨識分子,如:抗體、抗 原、配體等。微脂體球體表面可含有胺基 (amine group)、羧基 (carboxyl group)、馬來亞醯胺基 (maleimide group)、雙硫基 (disulfide group)或氫氧 基 (hydroxyl group)。具有以上官能基的磷脂質可做為典型的接合分子,分 別 如 phosphatidylethanolamine (PE) 、 maleimidomethyl-cyclohexane- carboximide-PE (MCC-PE)、N-glutary-PE或maleimidophenyl butyramide- PE (MPB-PE)、pyridyldithiopropionate -PE (PDP-PE)81-87。另外還有使用膽固醇 及聚乙二醇 (polyethylene glycol;PEG)的氫氧基 (圖1-8)。
圖1-8、抗體及 PEG 進行表面修飾的微脂體
Figure 1-8 The liposome were modified with antibody by PEG linker.
http://www.science-art.com/gallery/127/127 831200535020 small.jpg
18
而提供專一性辨認功能的生物分子也必須經由化學分子的修飾而在生 物分子上提供特殊官能基,使其有效接合在微脂體的球體表面。目前常用 來提供接合的架橋分子主要特性是必須具有異質雙功能的特性,使得生物 辨識分子能有效的與微脂體結合形成免疫微脂體,例如:一端具有與生物 辨認分子的胺基接合功能,另一端具有提供生物分子與微脂體球體形成雙 硫鍵結的功能基團。目前常見的架橋化學分子將以下列四種物質為範例:
succinimidyl-4-(N-maleididomethyl)-cyclohexane-1-carboxylate (SMCC) 、 N-succinimyidyl-3-(2-pyridyldithio) propionate (SPDP) 、 1-ethyl-3-(3- dimethylaminopropyl) carbodiimide (EDC) 與 N-4-(p-maleimidophenyl) butyrate (MPB) 84-90,如表1-4。除了上述的化學架橋之外,可以提供高結合 力的生物分子亦可作為架橋,例如biotin-streptavidin交互作用、Protein A/G 與 抗 體 的 結 合 能 力 等80, 91-93。 而 在 本 研 究 中 , 首 先 以N-succinimidyl S-acetylthilacetate (SATA) 與 DPPE 作 用 , 形 成 能 產 生 硫 醇 基 (SH-) 的 DPPE-ATA分子,再與其餘的磷脂質合成出能形成架橋的ATA-liposome。
另 外 , 在 合 成 免 疫 微 脂 體 前 , 須 先 將 抗 體 與4-(N-maleimidomethyl) cyclohexane-1-carboxylic acid 3-N-hydroxysuccinimide ester (SMCC)進行衍 生化作用,使抗體帶有能與SATA鍵結的馬來亞醯胺基後,與ATA-Liposome 混合作用,即形成此研究所使用的免疫微脂體試劑 (圖1-9)。
表1-5 架橋分子的結構與官能基。
Table 1-5 The structure and functional groups of cross-linking agents.
19
1-4、免疫分析技術
免疫分析技術的特點在於抗體可專一的辨認抗原,因而此技術常用於 癌症的診斷或特定蛋白質的定量等。以抗體的專一性為基礎,再利用追蹤 劑接合定量技術分析其檢測結果以進行定量分析。目前有各式各樣的追蹤 劑被使用,如:放射性同位素、酵素、螢光劑/冷光及微脂體免疫分析技術。
就免疫檢測的形式主要可分為兩種,分別為同質式 (homogeneous)及異質 式 (heterogeneous),同質式的檢測方式是將所有的檢測物及檢測環境建立 在同一個容器之內,而且不需經過其他的分離步驟就可提供檢測資訊。而 異質式相較於同質式的檢測是在於檢測過程當中需要分離步驟以移除游 離且會影響檢測的物質,才能得到精確的檢測結果94。在同質性檢測模式 方面,其原理是藉由物質的結合改變定量分子的性質。而常見的例子有兩 種 , 分 別 為 酵 素 多 重 免 疫 分 析 法 (enzyme-multiplied immunoassay technique ; EMIT) 與 螢 光 偏 振 免 疫 技 術 (fluorescence polarization immunoassay;FPIA)兩種。在EMIT技術中,被分析物標籤後的酵素與正常 的分析物共同競爭會抑制酵素活性的抗體,若樣品中分析物含量較高,則 酵素活性越高,所導致的訊號值將與分析物的濃度成正比95。在FPIA技術 中,其原理是利用螢光標識後的分析物與正常分析物競爭其專一性抗體,
圖1-9、此研究所使用的免疫微脂體製備。
Figure 1-9. The flow chart of manufacting immunoliposome.
20
藉由螢光標識分析物與抗體的結合,降低原本游離於環境中的旋轉速度,
才使得螢光可供偵測,反之則無法得到螢光值,所以樣品分析物的濃度將 與螢光強度成反比96。在異質性檢測方面,主要分為兩個檢測模式,一種 為三明治雜合直接檢測法(direct sandwich assay),另一種為競爭性結合間接 檢測法(indirect competitive assay)。常見的範例分別為微粒子酶免疫法 (microparticle enzyme immunoassay;MEIA)與競爭性酵素連結免疫吸附法 (competitive enzyme-linked sorbent assays;competitive ELISAs)。而MEIA 的檢測原理是分析物分別結合在已固定抗體的顆粒與標的螢光物質的抗 體之間,其偵測訊號將與分析物濃度成正比97。而competitive ELISAs的檢 測原理則是將螢光標的後的分析物與樣本分析物進行競爭,最終所得到的 螢光訊號值將與分析物濃度成反比72。目前所使用的定量的免疫分析技術 有放射性免疫技術、酵素免疫技術、電化學免疫技術、重量免疫分析及微 脂體免疫分析技術等。
將放射性同位素標籤於抗體上,利用抗體的辨識能力加上放射性同位 素的標籤,使得此種免疫分析方法可用於樣本的定量。而其缺點是必須操 作放射性同位素,故須具有專業技術與特殊的操作設備才能應用,也因這 些缺點而使得此種方式無法普遍應用。酵素免疫分析是將酵素做為標籤與 抗體連結,此酵素-抗體複合物將做為檢測工具。當抗體上酵素與受質反應 時會產生顏色,以作為檢測時的測量標的。常見的酵素為鹼性磷酸酵素 (alkaline phosphatase;AP)及辣根過氧化酶 (horsedish peroxidase;HRP)98。 另外,螢光/冷光免疫分析為直接在抗體上標的螢光/冷光物質如:acridinium ester與acridinium sulfonamide ester。在檢測上同樣利用抗體結合抗原的辨 識能力,移除未結合的抗體之後,加入過氧化物誘導冷光被激發或是直接 偵測螢光/冷光訊號的產生98。而電化學免疫分析是結合「抗體與抗原的結 合」與「電化學的測量方式」而形成的檢測系統。此領域的發展皆是因免 疫反應的結果而針對電流、電壓、電阻、電傳導與離子變化做為評估的依 據。在電壓及電流的檢測原理中,以測量免疫反應後所造成在偵測設備的 表面價數、電位的變化或是利用氧化還原反應所產生的電流變化來進行測
21
量。而在電傳導及獲能性 (capacitiy)的檢測中,以測量因免疫反應中,特 定產生或減少的離子所導致裝置中恆定的電傳導或電壓變化98。
重量免疫分析的應用上目前有兩種,一種為石英晶體微平衡 (quartz crystal microbalance;QCM)系統,其組成是在兩個金屬電極之間夾著一塊 壓電材料如:石英晶體,而壓電材料本身具有固定的振動頻率,若改變原本 的振動頻率將會有電流的產生,利用其電流作為訊號檢測的依據99。若應 用在生物檢測上,在壓電材料 (如石英)上塗佈抗體之後,再加入欲檢測的 抗原,此時因為抗原與系統中的抗體結合後將改變質量而使得石英原本的 頻率改變,而導致電流產生以獲得偵測訊號98。另一種為表面電漿共振法 (surface plasma resonance;SPR),其原理是利用位於金箔表面的抗體與抗 原的交互作用所產生的重量變化,而導致原本細微的光線經電漿表面後造 成反射角度不同而進行測量98。
1-4-1、免疫微脂體分析
微脂體具有相當大的內部空腔,且其脂雙層的表面能共價鍵結各式各 樣的生物辨識分子,使得微脂體可應用於藥物載體、基因治療、化妝品工 業與分析檢測等領域。在近年的研究中,有相當多的學者將微脂體大量的 應用於檢測上,原因是此種檢測工具可以提供一種穩定的、快速的、敏感 與低廉的檢測方式100。將微脂體工具再搭配上各種不同的檢測方式如:光 學、電化學的與流體注射分析系統等101-116,將更大幅的延伸出各式各樣的 檢測技術。
利用微脂體作為免疫分析可分為非破裂微脂體及破裂微脂體兩種型 式。在非破裂的微脂體檢測上,為應用免疫微脂體搭配硝化纖維膜試紙所 發展出的檢測平台是微脂體免疫競爭(liposome immunocompetition;LIC) 法。其原理是將biotin與分析物鍵結於微脂體膜表面成為免疫微脂體,當液 體樣品與免疫微脂體混合後,將試紙置入前述樣品液中,經由毛細現象使 液體上升。此時樣本內若含有分析物則會與免疫微脂體競爭試紙上已固定 的抗分析物抗體結合位。另外,在抗體結合位上方另有一個抗biotin抗體結
22
合位,用以捕捉未結合於抗分析物抗體結合位的免疫微脂體,在biotin 結 合位所表現的濃度將與樣品中分析物的濃度成正比。目前LIC可應用於 herbicide alachlor 117、biotin 118、aflatoxin B1 119、與polychloride benzenes (PCBs) 120等物質的檢測。另外,在異質式的直接檢測模式中,以三明治雜 合為基礎,表面接有抗體的微脂體與目標分子在溶液中作用,再置入表面 已固定抗分析物抗體的硝化纖維膜條,液體因毛細現象上升後,三明治複 合體 (immunoliposome-antigen-antibody)將在抗體結合位上被組成並呈色 在試紙上。此法目前被應用於霍亂毒素、大腸桿菌及臘腸毒素的檢測,其 偵測極限分別為10 fg/mL、104 CFU/mL與15 pg/mL121-123。而在競爭性的檢 測模式中,微脂體免疫凝集法 (liposome immunoaggregation assay;LIA) 的檢測模式亦被應用,其作用原理是將分析物鍵結的微脂體 (同時與biotin 鍵結)與分析物在水溶液中與抗體進行競爭性結合而產生凝集效應,再用原 先固定有streptavidin的硝化纖維膜以吸收未反應的微脂體。若分析物濃度 高,則硝化纖維膜上的螢光訊號與分析物濃度成正比。對於農藥殘留的檢 測 ,Chaniotakis 等 學 者 以 微 脂 體 產 生 適 合 酵 素 存 在 的 微 環 境 與 使 organophosphorus (OPs) pesticide分子經膜蛋白而進出微脂體而抑制其內部 的酵素活性的方式發展出OPs的檢測,靈敏度可達到10-10 M,分析時間為 15分鐘124。
在破裂的微脂體檢測方式上,為達到更高的靈敏度,可添加界面活性 劑使得微脂體破裂而釋放出所包裹的染劑釋放。目前已開發出利用微量盤 (microplate)、流體注射 (flow-injection)與微流道系統 (microfluid)為平台進 行多種物質檢測71。螢光染劑是普遍應用於微脂體包裹的染劑之一,某些 螢光物質如calcein、fluorescein、sulforhodamine與sulforhodamine B等103, 120,
125,在高濃度之下包裹在微脂體內會產生非螢光聚合、分子碰撞與能量從 螢光單體轉移至非螢光性雙聚體的自身閉鎖 (self-quenching)效應,導致螢 光訊號不明顯120, 125,而當其濃度被稀釋之後將會使得螢光訊號明顯提高。
另外可將酵素包裹於微脂體當中,當檢測時,在環境當中加入受質,產生 的訊號或化學反應將隨著微脂體破裂而與釋出的酵素數目成正比。而在誘
23
導微脂體破裂的機制可利用溶劑或清潔劑添加的化學方式126, 127、經由添加 phospholipase C或trypsin的酵素破裂法128, 129、加入天然的蛇毒 (mellitin)或 蜂毒破裂微脂體130或是使用補體系統與抗體結合在微脂體上導致其破裂
131。例如在微脂體內包裹glucose 6-phosphate dehydrogenase,當微脂體藉由 補體系統的啟動而破裂時將分解環境中的glucose將NAD+轉換為NADH,
而NADH可還原藍色染劑2,6-dichlorophenolindophenol成無色,此時藍色的 訊號隨樣本濃度增加而增加132。
過去將免疫微脂體應用在菌體檢測上的研究中,有學者研究以試紙條 對於造成咽喉炎的鏈球菌 (Streptococcal pharyngitis)進行檢測。使用表面修 飾抗體且內腔含有SRB染劑的免疫微脂體作為檢驗試劑以簡化先前須加入 酵素受質以產色的步驟。藉由免疫反應使得微脂體破裂而導致SRB釋放。
其檢測結果得到,其靈敏度達91%,專一性達83%,陽性預估值為88%,
陰性預估值為87%133。而另一種平台為利用96孔盤,因其具有多功能性、
簡單、高敏感性與可定量等特點134,而其搭配以顏色、螢光、冷光及膠體 凝集等方式來判定訊號進行定性或定量分析,已廣泛使用在游離前列腺專 一性抗原 (free prostate specific antigen;f-PSA)135、血管上皮生長因子 (vascular endothelial growth factor-C;VEGF-C)136、干擾素-2 (interferon-2;
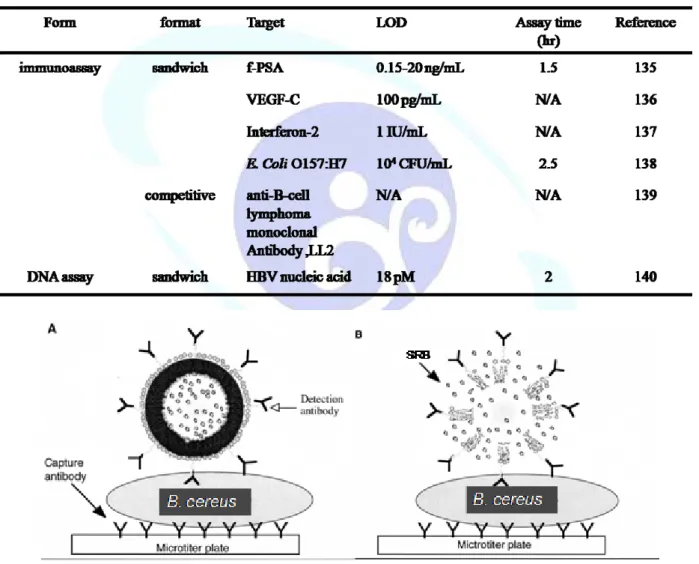
IL-2)137、大腸桿菌 (Escherichia coli O157:H7)138、抗B細胞微脂體139及B型 肝炎病毒 (hepatitis B virus;HBV)核酸140的檢測方面 (表1-6)。另外,在分 析時還可以大量處理樣本、減少樣本體積、快速與可自動化等優點,所以 是一種發展快速的檢測平台。
因為以上的優點,以96孔盤同時搭配具有生物辨識能力且包裹大量的 訊號分子的微脂體形成本論文的檢測系統。在過去的研究中,已發展針對 E. coli O157:H7的免疫微脂體三明治螢光 (immunoliposomes sandwich fluorometric assay;ILSF)檢測系統138,其原理是經由硫醇基衍生化的抗體 與帶有馬來亞醯胺基且內腔含有carboxyfluirescein (CF)螢光分子的微脂體 共價形成的免疫微脂體作為檢測試劑。當免疫微脂體辨認樣品內的E. coli O157:H7,分離未作用的免疫微脂體後,經過介面活性劑破壞與菌體結合
24
的微脂體結構而釋放出CF,經由螢光測定儀測定其螢光訊號而評估樣品中 菌體含量。根據研究結果指出,檢測緩衝溶液環境下的純菌株,其靈敏度 可達104 CFU/mL,而食物樣本的檢測極限可經菌體檢測前增殖培養而達到 0.8 CFU/mL138。在過去報告中皆指出以免疫微脂體作為檢測試劑可提高其 檢測的靈敏度,故此論文將以此系統建構出檢測仙人掌桿菌的方法,如圖 1-10。
圖1-10、此研究所使用的檢測分析方式。
Figure 1-10 The schematic diagram of detection principle in this study.
表1-6、微脂體在 96 孔平盤的應用。
Table 1-6. The applifiction of liposome with the use of microtiter plate.
25
第二章、仙人掌桿菌之免疫螢光分析技術 2-1、摘要
首先以不同溫度及培養基的環境下進行菌株生長速率的測定。將所欲 建立的「免疫微脂體-螢光免疫吸附法」最適化以進行菌體檢測極限的測 定。圖 2-1 為本論文的實驗流程圖。實驗將先探討仙人掌桿菌生長的最適 化條件,包含培養基種類 (TSB、NB 及 PCB)及溫度 (30、35、40 及 45℃),
以尋找出可以產生最短世代時間的培養條件。繼之將「免疫微脂體-螢光免 疫吸附法」最適化以達到最佳的偵測靈敏度,分別對 96 孔微量盤及免疫 微脂體做適當的參數調整。在對 96 孔微量盤做最適化的調整中,包含(1) 捕捉抗體的塗佈環境: 溶液的 pH 值與鹽濃度、(2)捕獲抗體的濃度及(3)阻 礙 (blocking)溶液的種類及濃度。在免疫微脂體的最適化的調整中,探討 其(1)抗體活性的篩選、(2)免疫微脂體的粒徑大小、(3)表面抗體佔總脂質 莫爾數的百分比及(4)免疫微脂體的濃度對靈敏度的影響;繼之,將最適化 後的免疫微脂體分析檢測技術平台進行仙人掌桿菌存在於緩衝溶液中的 專一性及靈敏度進行測試,另外以0.083 CFU/mL 的菌濃度進行 14 小時的 培養以分析其檢測極限。
26
2-2、實驗流程圖
圖2-1、實驗流程圖
Figure 2-1 The schematic flowchart of experiment
27
2-3、藥品與材料:
2-3-1、試驗菌株
B. cereus 11778/4552/F4810 由美國康乃爾大學食科系的 Dr. Randy Worobo 慷慨提供。 E. coli DH10β 由中興大學食生系黃文哲老師慷慨提供。B.
subti1is DB430、E. faecalcs 10789、Staphylococcus aureus 10781、Listeria monocytogenes 14845、Yersinia enterocolitica 13999、Vibro parahaemolyticus 10806 及 Pseudomonas aeruginosa 10944 由宜蘭大學食科系林世斌老師慷慨 提供。所有菌株皆於-20oC 下保存備用。
2-3-2、 抗體
Goat anti-Rabbit polyclonal antibody (AP132P) 購自 Chemicaon 公司,Rabbit anti-Bacillus cereus polyclonal antibody 由食品工業研究所陳紀樺研究員慷 慨提供。
2-3-3、 化學藥品
A. 以下藥品購自美國 Difco 公司
Nutrient Broth/Agar (BD 234000/ BD 213000)、Plate count Broth/Agar (BD 275120/ BD 247940) 及 Tryptic soy Broth/Agar (BD 211825/ BD 236950)。
B. 以下藥品購自美國 Sigma 公司
cholesterol (C8667)、sucrose (CALBIOCHEM 573113)、hydroxylamine-HCl (Aldrich 431362)、N-ethylamine (Aldrich E3876)、ammonium molybdate (Aldrich A1314)、sodium bisulfite (JT Baker 3556)、sodium sulfite (Aldrich S0505)、ammonium persulfate (A3678)、dimethyl sulfoxide (Aldrich 154938)、
Sephardex G-50 (G50150) 、Sephardex-G25 (G25150)、Sepharose CL-4B (CL4B200) 、 chloroform (C8667) 、 N,N,N,N-Tetramethyllethylenediamine (TEMED;T9281)、sulforhodamine B (SRB;S9012)、casein (C7078)、
N-succinimidyl S-acetylthioacetate (SATA;A9043)、4-(N-maleimidomethyl) cyclohexane-1-carboxylic acid 3-N-hydroxysuccinimide ester (SMCC ;
28
M5525)、Triton X-100 (T8787)、amino-2-naphthol-4-sulfonic acid hemihydrate (S440884)、octyl beta-D-glucopyranoside (n-OG;O8001)、sodium dodecyl sulfate (SDS;23771)及 30% hydrogen peroxide (Riedel-deHaen 31642)。
C. 以下藥品購自日本 NOF 公司
L-α-dipalmitoylphosphatidylethanolamine (DPPE;COATSOME® ME-6060)、
L-α-dipalmitoylphosphatidylcholine (DPPC ; COATSOME® MC-6060) 及 L-α-dipalmitoylphosphatidylglycerol , sodium salt (DPPG ; COATSOME®
MG-6060LS)。
D. 以下藥品購自德國 Merck 公司
Disodium hydrogen phosphate (106580)、acetic acid (1.00063.2500)、potassium dihydrogen phosphate (104873)、sodium chloride (106404)、sodium azide (NaN3;822335)、methanol (106009)、sulfuric acid (100731)、triethylamine (TEM808352) 、 Tween-20 (8.22184.0500) 、 ethylenedinitrilotetraacetic acid disodium salt dehydrate (EDTA-2Na;108418)、Tris-HCl (CALBIOCHEM 648313) 、 Tris-base (CALBIOCHEM 648311) 及 N-2-hydroxyethylpiperazine-N-2-ethanesulfonic acid (HEPES;CALBIOCHEM 391340)。
E. 以下藥品購自美國 Bio-Rad 公司
Glycine (161-0718)及 30% Acrylamide/Bis solution (BIO-RAD 161-0156)。
F. 以下物品購自當地超商 脫脂奶粉 (安佳)。
29
2-4、方法:
2-4-1、仙人掌桿菌之最適化培養
挑選單一菌落至10 mL 的培養基中,進行隔夜活化。再將活化的菌液 吸取1 mL 至含有 49 mL 的培養基中進行第二次隔夜培養,活化環境皆為 37℃及 150 r.p.m。生長曲線的製作是將二次活化後的菌液經過序列稀釋 後,取1 mL 加至 49 mL 的培養基中,使終濃度達到 102 CFU/mL 後進行培 養。藉由三種培養基 (NB、PCB 及 TSB)及四種溫度 (30、35、40 及 45℃) 的相互搭配之下,評估菌體在第 0、1、3、5、7、9、11、13 及 14 小時的 菌落數目。將菌液取出進行適當的序列稀釋及塗盤,經隔夜培養後,計算 菌落數並回推各時間點之原始菌液濃度。以菌體濃度及時間點作出生長曲 線,並在菌體的生長對數期中,依公式(1)(2)計算出世代時間。
2-4-2、抗體活性分析 A. 膜蛋白萃取
在經培養18 小時的仙人掌桿菌菌株固態培養基上加入 2 mL 的 0.01 M PBS (pH 7.2),將培養基上仙人掌桿菌菌株 (B. cereus 11778、4552 及 F4810) 刮起,再加入 1 mL 的 0.01 M PBS 以懸浮培養基上的菌體。將懸浮液離 (3000 r.p.m,15 min)去除上清液後,再重複上述步驟以去除菌體外圍的雜 質 。 菌 體 加 入 1 mL 的 0.01 M PBS pH 6.8 ( 含 1% SDS 與 0.2%
2-mercaptoethanol)再以 70℃水浴槽作用 20 分鐘後離心 (10000 r.p.m,10 min)。將 500 μL 上清液移至微量超過濾離心管 (Millipore,Cal No : 42409) 中以11000 r.p.m 離心 10 分鐘,重複步驟兩次。接著以 500 μL 的 0.01 M PBS 清洗留存於過濾膜上的蛋白三次後,加入100 μL 0.01 M PBS 並將上層裝置 倒置在新的微量離心管中,以3000 r.p.m 離心 10 分鐘回收膜上蛋白。
2
1 2
Log LogNt LogNt
n= −
n t T =t2− 1
………(1)
………(2)
N: 菌體濃度
t1: 前段時間菌體濃度 t2: 後段時間菌體濃度 n: 菌體生長代數
T: 生長速率( Doubling time )
30
B. 十 二 烷 基 硫 酸 鈉 -聚丙烯醯胺膠體電泳法 (sodium dodecyl sulfate- polyacrylamide gel electrophoresis: SDS-PAGE)
以3%上層膠及 12.5%下層膠的聚丙烯醯胺膠體進行仙人掌桿菌的膜蛋 白膠體電泳,將仙人掌桿菌的膜蛋白樣本以 1:1 的體積比例均勻混合於 sample buffer (含 10% SDS、20% glycerol、125 mM Tris-HCl、0.02%
bromophenol blue 與 2-mercaptoethanol)中,並在 95℃下加熱 1 分鐘。分別 在上層膠體中加入2 μL 蛋白質標準品與 15 μL 膜蛋白樣本溶液,以 Bio-Rad 迷你膠體電泳槽 (BIO-RAD 525BR 084091)進行電泳分析 (上層膠,100 mV;下層膠 150 mV,共 1.5 小時)。膠片取出後以染色液 (0.2% Commassie brilliant blue,45% methanol 及 10% acetic acid)作用 2 小時後,再以褪染劑 (25% methanol 及 10% acetic acid) 作用 3 小時以進行褪染。
C. 西方墨點法 Western Blot
將膠片移至經transfer buffer (25 mM Tris-Base,192 mM glycine 及 10%
methanol)浸泡兩分鐘的的 PVDF 膜 (Millipore IPVH 00010)上,分別在 PVDF 膜及膠片上覆蓋濾紙及泡棉後,形成轉印三明治,以 100 mA 進行轉 印作用,待 SDS-PAGE 上的膜蛋白轉印至 PVDF 膜上,再將膜取出以 5%
脫脂奶粉溶液 (溶於 0.01 M PBS, pH 7.2)在 4℃下作用 16 小時以將 PVDF 膜上的其他蛋白質結合位阻斷。移除奶粉液後以10 mL 的 0.01M TBST (含 0.15 M NaCl,0.5% Tween-20)清洗 PVDF 膜三次 (5 分鐘/次,100 r.p.m)。
清洗完成後,加入10 mL 的待測的抗體 (100 μg/mL),室溫下作用 1.5 小時。
再以30 mL 的 0.01M TBST 清洗 PVDF 膜(10 mL/次;15 分鐘/次,100 r.p.m)。
加入總體積10 mL,以 1:5000 稀釋的 goat anti-rabbit antibody conjugated alkaline phosphatase 在室溫下作用 1.5 小時,再以 TBST 清洗 PVDF 膜三次,
最後加入NBT 及 BCIP 反應,作用完成後將膜移至大量清水中以終止反應。
2-4-3、免疫微脂體之製備
秤取莫耳比例為1:2 的 DPPE 與 SATA 置入圓底燒瓶中,加入 2 mL 的氯仿(含有 0.7% triethylamine;v/v)溶解後,避光震盪 30 分鐘。以旋轉減 壓濃縮機 (rotary evaporator;Eyela N-1000)去除有機溶劑。再加入 2 mL 氯