第三章 實驗材料及方法
第一節 實驗材料
1.藥材
本實驗所使用之中藥材購自台中市欣隆藥材行
黃芩為唇形科植物 Scutellaria baicalensis GEORGY.的乾燥根 芍藥為毛茛科植物 Paeonia alctiflora PALL.的乾燥根
甘草為豆科植物 Glycyrrhiza uralensis FISCH.的乾燥根及根莖 大棗為鼠李科植物 Ziziphus jujuba MILL.的乾燥成熟果實
2.藥品及試劑
黃芩 (Baicalin) Aldrich Chemical Co.
芍藥 (Paeoniflorin) Yoneyama Chemical Co 甘草酸(Glycyrrhizic acid) TCI Chemical Co
對羥苯甲酸甲酯(Methylparaben) WAKO Chemical Co
肝素鈉(Heparin sodium) Novo Industrial Co.5000 I.U./ml 磷酸(Phosphoric acid) Merck Co.
甲醇(Methanol) Merck Co.
乙 (Acetonitrile) Merck Co.
氫氧化鈉(Sodium hydroxide) 德國 R.D.H. Co.
藥用酒精(Ethanol) 臺灣煙酒公賣局
生理食鹽水 信東化學工業公司
氮氣 吉源氮氣
* 使用於高效液相層析儀之試劑均為 HPLC 級
3.儀器及材料
A.高效液相層析儀之裝備
幫浦(Pump): Jasco Model PU-980
偵測器(Detector): Jasco Model UV-975 Intelligent UV/VIS 積分儀(Integrator): Scientific Information Service
Corporation Integrator 自動取樣機(Auto Sampler):
Jasco Model AS-851
印表機(Printer): Heweltt Packard Deskjet 695C 層析管(Column): Inertsil ODS-2 (5µm 4.6×250mm) 保護管柱(Guard-column): Inertsil ODS-2 (5µm 4.6×50mm) B.實驗室裝備
電子天平: Sartorius Type 1801
減壓抽氣機: Eyela, Aspirator A-2S, Tokyo, Rikak Co.
微量移液管: Socorex Transferpette:2 - 20 µl 20 - 200 µl 100 - 1000 µl 試管振盪器: Maxi Mix II Thermolyne Type 37600 Mixer 高速離心機: Hettich Zentrifugen D-7200 Tuttlingen,
Germany(5000 rpm)
酸鹼測定儀: Suntex Microprocessor pH meter Model-2200 純水製造裝置: RiOs,TK-5/ZROS6016Y, Millipore Co. and
Milli-Q, FM-12OD/ZMQS600, Millipore Co.
超音波振盪器: BRANSON 5510, BRANSON ULTRASONIC Co. , USA
吹氣濃縮裝置: Organomation Associates INC. Model No.112.
過濾膜: Millipore Type HV, 0.45µm, Millipore Co.
C.動物實驗所用器材
胃管(內徑 1.5 mm): 季勗儀器公司 針筒過濾器 0.22 µm: PRO-XTM(Lida)
注射針及針筒: Terumo Co.Tokyo, Japan
1 ml Syringe 25G× 5/8〞(0.5 × 16 mm) 2.5 ml Syringe 24G× 1〞(0.55× 25 mm) 10 ml Syringe 22G×1 1/2〞(0.70 × 38 mm) 靜脈置留針及針塞: Terumo Co.Tokyo, Japan
IV Catheter 22G× 1〞
Injection Plug, 0.2 ml
家兔固定器: 信德儀器公司
張口器、棉花、3M 膠帶、計時器
4.溶液製備
(1)黃芩 、芍藥 及甘草酸的標準溶液(Baicalin, Paeoniflorin and Glycyrrhizic acid stock standard solution)
精稱黃芩 、芍藥 及甘草酸標準品各 25.0 mg,分別置入 25 ml 的容量瓶中,添加甲醇至刻度,即得濃度為 1.0 mg/ml 的 黃芩 、芍藥 及甘草酸的標準溶液。使用時再以甲醇稀釋成所 需濃度之標準溶液。
(2)內部標準溶液(internal standard solution)
精稱對羥苯甲酸甲酯(methylparaben) 3 mg 置於 100 ml 定量瓶 中,先加入適量乙 (Acetonitrile)使之溶解,再加入乙 至刻度,
可得濃度為 30 µg/ml 對羥苯甲酸甲酯之儲備液;取 50 ml 之儲備液 置於 500 ml容量瓶,加入乙 至刻度並混合均勻,即得濃度 3 µg/ml 的內部標準溶液。
(3)肝素鈉溶液(Heparin sodium solution)
精取肝素鈉注射液(5,000 I.U./ml)2.5 ml 加於 500 ml 生理食鹽 水中,即得 25 I.U./ml 抗凝血肝素鈉溶液。
(4)黃芩 、芍藥 及甘草酸靜脈注射液(Baicalin, Paeoniflorin and Glycyrrhizic acid solution for intravenaous injection)
精稱所須的黃芩 、芍藥 及甘草酸加入注射用水混合,滴加 適量 1N NaOH 溶液調 pH 值 7.2-8.0 之間,再經 0.22 µm 過濾薄膜 過濾除菌即得。
(5)黃芩湯口服溶液(Huang-Ch′in-Tang oral solution)
依黃芩湯方中各藥材用量比例 3:2:2,秤取飲片黃芩 300 g、
芍藥 200 g、炙甘草 200 g 及大棗 24 枚,首先將芍藥、炙甘草及大 棗加入純水 1000 ml 浸濕後,煮沸後再加入已用溫水浸泡過之黃 芩,煎煮 1 小時,以紗布過濾,殘渣再加入 1000 ml 純水如此連續 煎煮 3 次,合併煎煮液約 1500 ml,過濾後,將濾液以減壓濃縮至 300 ml,取濾液 250 ml 為黃芩湯口服溶液,放冷後置於-30℃冷凍 櫃備用。
(6)黃芩湯靜脈注射液(Huang-Ch′in-Tang solution for intravenaous injection )
試驗用黃芩湯注射液之製備過程,如同上述口服溶液製備方 法,所得濾液 50 ml,放置於 8℃下冷藏過夜,隔天傾出上清液,
上清液用高速離心將沉澱物沉降之,取出澄明的上清液集中合併,
經濾紙過濾。濾液調 pH 值 7.2-8.0 之間,先經 0.45 µm 濾膜,再經 0.22 µm 濾膜過濾,即得黃芩湯注射液。
操作流程如下:
黃芩湯 ( 黃芩 300 g、芍藥 200 g、炙甘草 200 g 及大棗 24 枚 ) 芍藥、炙甘草及大棗加入純水 1000 ml 浸濕
煮沸後再加入已用溫水浸泡過之黃芩,煎煮 1 小時,以紗布過濾,殘渣再加 1000 ml 純水 如此連續煎煮 3 次,合併煎煮液,過濾。
藥渣 濾液 濃縮至 300 ml
濾液 250 ml 濾液 50 ml
黃芩湯口服溶液 8°C 下冷藏過夜 離心,過濾。
沉澱 濾液 調 pH 值至 7.2-8.0
先經 0.45µm 濾膜,
再經 0.22µm 濾膜過濾
黃芩湯注射液
第二節 實驗方法
1.黃芩湯製劑中指標成分之 HPLC 定量分析方法
A. HPLC 分析條件
層析管(Column) Inertsil ODS-2 ( 5 µm 4.6×250 mm ) 保護管柱(Guard-column) Inertsil ODS-2 ( 5 µm 4.6×50 mm ) 檢測波長 Time (min ) UV (nm)
0 230
13 230
13.1 280
28 280
28.1 248
40 248
40.1 230
47 230
移動相 A: Acetonitrile
B: Water (以 85% Phosphoric acid 調 pH 3.45-3.50) 以 A、B 兩種移動相依下列混合比例進行
Time(min) A B
0 15 85
13 34 66
25 34 66
28 60 40
40 60 40
42 15 85
47 15 85 流速 1.0 ml/min
注入量 20 µl
分析時間 40 min.
B.標準溶液檢量線之製作
精確量取不同濃度之黃芩 (Baicalin)、芍藥 (Paeoniflorin)、甘 草酸(Glycyrrhizic acid)標準溶液 180 µl,加入 20 µl 之內標乙 溶液 (Methylparaben, 30 µg/ml),取 20 µl 注入 HPLC 分析,所得之黃芩
、芍藥 、甘草酸與內標之面積比與各已知濃度作線性迴歸以製 作檢量線。
C.黃芩湯注射液中指標成分的定量
取黃芩湯注射液 1 ml 置於 100 ml 的容量瓶中,加入甲醇至刻 度,可得稀釋濃度 100 倍之黃芩湯注射液。再取稀釋 100 倍的黃芩 湯注射液 1 ml 置於 10 ml 的容量瓶中,加入甲醇至刻度,可得稀釋 濃度 1000 倍之黃芩湯注射液,用 0.45 µm 過濾膜過濾後,精取此稀 釋之黃芩湯注射液 180 µl,加入20 µl 之內標乙 溶液(Methylparaben, 30 µg/ml),取 20 µl 注入 HPLC 分析,代入標準溶液檢量線方程式,
結果本實驗用黃芩湯注射液中含黃芩 13.55 mg/ml、芍藥 3.65 mg/ml、甘草酸 6.45 mg/ml。
D.黃芩湯口服液中指標成分的定量
取黃芩湯口服液 1 ml 置於 100 ml 的容量瓶中,加入甲醇至刻 度,可得稀釋濃度 100 倍之黃芩湯口服液。再取稀釋 100 倍的黃芩 湯口服液 1 ml 置於 10 ml 的容量瓶中,加入甲醇至刻度,可得稀釋 濃度 1000 倍之黃芩湯口服液,用 0.45 µm 過濾膜過濾後,精取此稀 釋之黃芩湯注射液 180 µl,加入20 µl 之內標乙 溶液(Methylparaben, 30 µg/ml),取 20 µl 注入 HPLC 分析,代入標準溶液檢量線方程式,
結果本實驗用黃芩湯注射液中含黃芩 10.32 mg/ml、芍藥 4.39 mg/ml、甘草酸 7.86 mg/ml。
2 黃芩湯血漿檢品中指標成分之 HPLC 定量分析方法
A. HPLC 分析條件
如同上述黃芩湯製劑中指標成分之 HPLC 定量方法 B.血漿檢品之前處理
精確量取血漿檢品 200 µl 置入試管中,加入含 3 µg/ml 對羥苯甲 酸甲酯(Methylparaben)內標準品之乙 溶液 700 µl,並以振盪器振盪 20 秒,使蛋白沉澱。再以 5000 rpm 離心 20 分鐘。吸取上清液置於另 一試管中,以氮氣噴吹至乙 完全離逸後,以甲醇 200 µl 溶解之。接 著以 HPLC 分析。
C.檢量線之製作
精確量取家兔空白血漿 180 µl 加入 20.0 µl 含不同濃度之黃芩 (Baicalin)、芍藥 (Paeoniflorin)、甘草酸(Glycyrrhizic acid)標準溶液,
配製成濃度為 100.0 至 0.05 µg/ml 之標準血漿檢品液(Table 4)。再加 入含 3 µg/ml 對羥苯甲酸甲酯(Methylparaben)內標準品之乙 溶液 700 µl,以振盪器振盪 20 秒,使蛋白沉澱。再離心 20 分鐘,取上清 液。以氮氣噴吹至乙 完全逸離後,以甲醇 200 µl 溶解之。接著以 HPLC 分析,由所得之黃芩 、芍藥 、甘草酸與對羥苯甲酸甲酯之 面積比與校正液濃度作線性迴歸以製作檢量線。
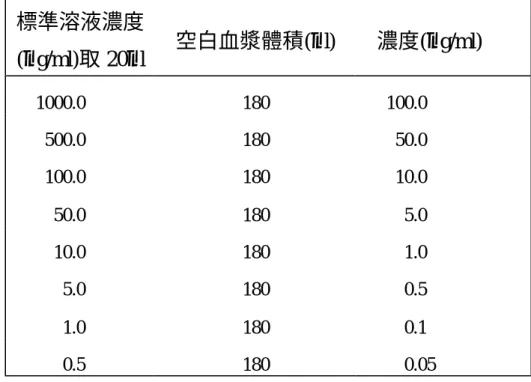
Table 4 Baicalin、Paeoniflorin、Glycyrrhizic acid 標準濃度血漿檢品 溶液之製備
標準溶液濃度
(µg/ml)取 20µl 空白血漿體積(µl) 濃度(µg/ml)
1000.0 180 100.0
500.0 180 50.0
100.0 180 10.0
50.0 180 5.0
10.0 180 1.0
5.0 180 0.5
1.0 180 0.1
0.5 180 0.05
D.回收率試驗
目的在比較添加黃芩 、芍藥 及甘草酸在空白血漿和空白甲醇 溶液中,經血漿檢品之前處理步驟處理後檢出量之差異。實驗步驟如 同校正曲線製作中對檢品的處理過程。回收率可從下式求得:
標準濃度在血漿中與內標積分面積比 Recovery (%) =
標準濃度在甲醇中與內標積分面積比 ×100%
E.精確性試驗
為 了 確 認 黃 芩 (Baicalin) 、 芍 藥 (Paeoniflorin) 及 甘 草 酸 (Glycyrrhizic acid)定量分析方法之精確性,因此做同日內(Intraday)及 異日內(Interday)的精確性比較。同日內試驗是以三種不同濃度之含黃 芩 、芍藥 及甘草酸標準濃度血漿檢品,分別於同一日的早上、中 午、晚上各分析兩次,計算各個校正液濃度之平均值(Mean)、標準偏 差(S.D.)及變異係數(C.V.)。若於不同天以同法操作則可得到異日內的 精確性比較。
F.靈敏度試驗
分析過程中,欲找出能被檢定出之最低濃度,但不需要能夠被定 量,故做偵測極限試驗(Limit of Detection, LOD),利用已知濃度的指 標成分予以分析,使指標成分之訊號對雜訊之比值(即 S/N ratio)為 3:
1,所建立該指標成分能可靠的被檢測出來的最低濃度,即為 LOD 值。而偵測極量(Limit of Quantitation, LOQ),將依前述「檢量線之製 作」,採標準濃度血漿檢品製備方法,取六次檢品分析決定之。
G.安定性試驗
(1) 黃芩 、芍藥 及甘草酸在家兔血漿中於-30℃下之安定性試驗 取適當之含黃芩 、芍藥 及甘草酸標準溶液加入空白血漿中,
振盪一分鐘以混合均勻,使濃度為 1.0, 5.0, 25.0 µg/ml 之血漿檢品,
將之置於-30℃的冷凍櫃中,於第 0, 1, 3, 6, 10, 15, 21 天分別取出一組 檢品(n=3)。解凍後,依血漿檢品之前處理方法處理後,以 HPLC 分 析,觀察黃芩 、芍藥 及甘草酸之濃度變化情形。
(2) 黃芩 、芍藥 及甘草酸在家兔血漿中於 37℃下之安定性試驗 取適當含黃芩 、芍藥 及甘草酸標準溶液加空白血漿中,振盪 一分鐘以混合均勻,使濃度為 1.0, 5.0, 25.0 µl/ml 之血漿檢品,將之 置於 37±2℃的恆溫箱中,於第 0, 1, 3, 6, 12, 24, 36, 48 小時,分別取 出一組檢品(n=3),依血漿檢品之前處理方法處理後,以 HPLC 分析,
觀察黃芩 、芍藥 及甘草酸之濃度變化情形。
3.黃芩湯指標成分在家兔體內之藥物動力學
A.實驗設計
取雄性家兔六隻,體重介於 1.8 至 3.0 公斤之間,進行指標成分 注射液靜脈注射(IVS)、黃芩湯靜脈注射(IVE)與黃芩湯口服(PO)給 藥,每次給藥後至下次給藥,時間須相隔一週以上。實驗家兔之重量 及給藥劑量示於 Table 5
Table 5 實驗家兔之重量及實際給藥劑量
Rabbit N.O 1 2 3 4 5 6 兔重(kg) 2.4 2.5 2.8 3.0 2.4 2.5
B(mg) 36.00 37.50 42.00 45.00 36.00 37.50 P 12.00 12.50 14.00 15.00 12.00 12.50 IVS 實
際
給G 24.00 25.00 28.00 30.00 24.00 25.00 兔重(kg) 2.2 2.7 2.2 2.2 2.9 2.2
B(mg) 29.81 36.59 29.81 29.81 39.30 29.81 P 8.03 9.86 8.03 8.03 10.59 8.03 IVE 實
際
給G 14.19 17.42 14.19 14.19 18.71 18.71 兔重(kg) 1.8 1.8 1.9 1.9 1.8 1.8
B(mg) 259.00 259.00 273.29 273.29 259.00 259.00 P 109.75 109.75 116.34 116.34 109.75 109.75 P.O 實
際
給G 199.00 199.00 210.94 210.94 199.00 199.00
*B: Baicalin; P: Paeoniflorin; G: Glycyrrhizic acid
(註)
靜脈注射黃芩湯標準品:Baicalin : 15 mg/kg Paeoniflorin : 5 mg/kg
Glycyrrhizic acid : 10 mg/kg 靜脈注射黃芩湯煎劑 :Baicalin : 13.55 mg/kg
Paeoniflorin : 3.65 mg/kg Glycyrrhizic acid : 6.45 mg/kg 口 服 黃 芩 湯 煎 劑 :Baicalin : 143.89 mg/kg
Paeoniflorin : 60.97 mg/kg
Glycyrrhizic acid : 110.55 mg/kg
B.給藥法及檢品處理
(1) 指標成分注射液靜脈注射給藥及血漿檢品之處理:
實驗前家兔至少禁食 24 小時,實驗時先稱重記錄實際體重以 便配製注射溶液。將兔子關入限制籠內兩耳之毛剃除乾淨,接著以 燈泡照射兔耳使其血管擴張,再以酒精棉消毒並助血管擴張,隨即 插入靜脈留置針,將針塞(Injection plug)注滿肝素鈉溶液後,固定 於靜脈留置針上。每次採血後均由針塞注入 25 I.U./ml 之肝素鈉溶 液約 0.2 ml,以防靜脈留置針管內之血液凝固。投藥前先抽取 1.5ml 之空白血液,由另一耳靜脈投藥後,分別於投藥後 2.5, 5, 10, l5, 20, 30, 45, 60, 90, 120, l50, l80, 210, 240, 300 及 360 分鐘由靜脈留置針 之針塞抽取 l.5 ml 血液,置於試管中,以 3000 rpm 轉速離心 15 分 鐘後,取出上層血漿,即保存於-30℃之冷凍櫃中。
血漿檢品之前處理、檢量線及分析條件均依前述方法操作,黃
芩 、芍藥 及甘草酸之濃度則由標準曲線經內插法推算而得。
(2)黃芩湯靜脈注射給藥及血漿檢品處理:
如同上述指標成分靜脈注射給藥方式。
(3).黃芩湯口服給藥及血漿檢品處理:
口服給藥實驗前家兔至少禁食 24 小時,實驗期間亦不進食。
實驗時家兔之處理如同上述靜脈注射給藥方式,惟口服給藥法是以 張口器將家兔之口張開後,再以胃管插入給藥。而其採血點為給藥 後之 10, 20, 30, 45, 60, 90, 120, 150, l80, 210, 240, 270, 300, 360, 420, 480, 540, 600, 660, 720 分鐘。
C.數據處理及統計方法
各種給藥法所取得之血漿檢品經使用前述 HPLC 法分析後,依標 準曲線內插法推算黃芩湯指標成分,黃芩 (Baicalin)、 芍 藥 (Paeoniflorin)及甘草酸(Glycyrrhizic acid)之血中濃度數據後,利用電 腦程式 JANA(79), WINNONLIN(80)及 LAGRAN-P 等,分別利用配適 後的分室及非分室理論,計算相關之藥物動力學參數。統計軟體 SPSS 之 Independent-Samples t-test 和 One-way ANOVA,分析不同製劑及 不同給藥方式之間的差異。
(1)一室體模式(One Compartment Model)
分析而得之各個指標成分血中濃度數據,經 JANA PROGRAM 作 Weighting 、 One Exponential Curve stripping 處 理 , 取 其 Volume/F、K01及 K10的數值。再用 WINNONLIN PROGRAM 作曲 線配適(Curve Fitting)取最適合的室體模式,求其相關藥動學參數。
(2)二室體模式(Two Compartment Model)
分析而得之各個指標成分血中濃度數據,經 JANA PROGRAM 作 Weighting 、Two Exponential Curve stripping 處理,取其 A、B、
α及β的數值。再用 WINNONLIN PROGRAM 作曲線配適(Curve Fitting)取最適合的室體模式,求其相關藥動學參數。
(3)非分室理論
以靜脈注射及口服給予家兔所得血漿檢品,由分析而得之各個 指標成分血中濃度數據,經 LAGRAN-P PROGRAM 處理,可由非 分室理論計算相關藥動學參數。
由上述所得之藥動學參數以統計學 t-test 比較 WINNONLIN 及 LAGRAN-P 處理後所得之藥物學參數(AUC, CL, T1/2 , VDSS)。另以 統計學 One Way ANOVA 處理,比較不同投藥間藥動學參數之差 異。