新穎稀土氟硫化物與氟硫氧化物螢光材料之製備、發光特性鑑定與其應用
全文
(2) 新穎稀土氟硫化物與氟硫氧化物螢光材料 之製備、發光特性鑑定與其應用 Synthesis, Luminescence Characterization and Potential Applications of Rare Earth Fluorosulfide and Fluorooxysulfide Phosphors. 研 究 生:黃云琪. Student:Yun-Chi Huang. 指導教授:陳登銘 博士. Advisor:Dr. Teng-Ming Chen. 國立交通大學 應用化學系碩士班 碩士論文. A Dissertation Submitted to M. S. Program, Department of Applied Chemistry National Chiao Tung University in Partial Fulfillment of the Requirements for the Degree of Master of Science in Applied Chemistry July 2013 Hsinchu, Taiwan, Republic of China 中華民國一佰零二年七月.
(3) 新穎稀土氟硫化物與氟硫氧化物螢光材料之 製備、發光特性鑑定與其應用 學生:黃云琪. 指導教授:陳登銘 博士 國立交通大學應用化學系碩士班 摘要. 利用藍光或近紫外光晶片搭配螢光粉以產生白光的方法是目前 白光發光二極體發展的主要課題之ㄧ。本論文主要以研發新型的氧氟 硫化物和氟硫化物系列螢光體並研究其發光特性與潛在應用為重 點。本研究利用固態反應於密閉石英管中,以 900 ~ 1000℃分別製備 CeSF:Lnn+ (Lnn+ =. Gd 3+ ,. Y 3+ ,. Tb 3+ ,. Mn2+ )、La3OF3S2:Ce3+ 氧氟. 硫化物螢光體與Ce2CaF4S2:Tb3+及(Ce1-xYx)2SrF4S2兩系列氟硫化物。粉 末X光繞射、螢光光譜和掃瞄式電子顯微鏡被用以探討合成條件、活 化劑摻雜濃度的最佳化,同時亦測量了激發與發光光譜、色度座標 圖、量子效率與熱消光光譜,並進一步評估其應用於白光LED之潛力。 本研究首先探討不同主體之最佳製程條件與粉末X光繞射晶相 之分析鑑定;第二部份則探討 La3OF3S2:Ce3+ 、CeSF、Ce2CaF4S2 與 Ce2SrF4S2之發光特性;第三部份則探討摻雜Mn2+ 摻雜氟硫氧化物之 發光特性;第四部份探討Ce3+/ Tb3+ 共摻氟硫化物螢光體之發光特 性;最後則探討所合成螢光材料之熱消光效應。 i.
(4) Synthesis, Luminescence Characterization and Potential Applications of Rare Earth Fluorosulfide and Fluorooxysulfide Phosphors Student:Yun-Chi Huang. Advisor:Dr. Teng-Ming Chen. M. S. Program, Department of Applied Chemistry National Chiao Tung University. Abstract White LEDs fabricated with blue or near-UV LED chips and compatible R/G/B phosphors is the main stream of current solid-state lighting device. This research is attempted to develop new fluorosulfide and oxyfluorosulfide phosphors undisclosed in the literature or patent application. We have prepared four series phosphors with compositions of CeSF:Lnn+. (Lnn+. =. Gd3+,. Y3+,. Tb3+,. Mn2+),. La3OF3S2:Ce3+,. Ce2CaF4S2:Tb3+ and (Ce1-xYx)2SrF4S2 by solid-state reactions in evacuated sealed quartz glass tubes at 900-1000℃, which were further characterized by powder X-ray diffraction, fluorescence spectroscopy, and electron microscopy. to. microstructures,. investigate chromaticity,. their. phase. quantum. identity, efficiency. luminescence, and. thermal. luminescence quenching behaviors. Based on the characterization results, we then evaluated their potential applications in fabrication of white light LEDs. This thesis first investigates the optimization of synthesis conditions and performs X-Ray diffraction characterization and phase identifications. The second part deals with the luminescence of La 3OF3S2:Ce3+ and the ii.
(5) third part investigates the luminescence of Mn2+-doped fluorosulfide and oxyfluorosulfide phosphors. Fourthly, this research investigates the luminescence of Ce3+/Tb3+-codoped fluorosulfides and studies the possibility of Ce3+ → Tb3+ energy transfer. Finally, we investigated the thermal luminescence quenching property of all synthesized phosphors and fabricated a white-light LED device using Ce2CaF4S2:Tb3+ and blue-emitting commodity phosphors in combination of a 365 nm near-UV LED chip.. iii.
(6) 誌謝 不知不覺來交大已經兩年了,這段時間似乎一瞬而過。這兩年的 時間說長不長、說短也不短,不過卻是影響我最多的一個時期。其中 特別感謝陳登銘老師,謝謝您對我的耐心教導,對於不懂的地方都能 夠仔細地解釋給我聽,讓我受益匪淺,您不時給予的關心以及建議, 讓我的研究成果更臻充實及完備。另外也要感謝口試委員劉偉仁老 師、裘性天老師以及李紫原老師特地來參加口試,所給予的建議使學 生論文更加完整。 感謝實驗室的學長姐教導許多儀器與實驗技巧,以及同學對我研 究上的幫助,讓我能順利地完成論文。還要感謝陪伴在我身邊的家人 及朋友,謝謝你們所給予的支持,是我心目中最大的支柱。另外還要 感謝我的男朋友,在我研究上遇到困難時所給予的幫助。 最後,再次感謝我的家人、師長對我的關心與幫助,以及所有幫 過我的學長姐、同學及朋友們,如今能順利地完成碩士學位,都是因 為你們對我無私的付出。謝謝大家成就今天的我!. iv.
(7) 總目錄 摘要................................................................i Abstract.............................................................ii 誌謝...............................................................iv 總目錄..............................................................v 表目錄............................................................viii 圖目錄.............................................................ix 第一章 1-1. 緒論.......................................................1 研究動機....................................................1. 1-2 研究背景....................................................5 1-2-1 螢光體發光原理…....................................... 5 1-2-2 稀土離子能階............................................11 1-2-3 主體晶格效應............................................17 1-2-4 濃度淬滅................................................20 1-2-5 能量轉移................................................20 1-2-6 固態合成法..............................................23 1-2-7 三基色原理和 C.I.E.色度座標圖.............................24 1-2-8 量子效率................................................26 1-3 文獻回顧.................................................. 28 1-4 螢光體設計原則............................................ 第二章 主體晶體結構簡介.......................................... 2-1 La3OF3S2 晶體結構簡介..................................... 2-2 CeSF 晶體結構簡介........................................ 2-3 第三章 3-1 3-2 3-3. 30 31 31 33. Ce2AF4S2 晶體結構簡介..................................... 35 實驗方法...................................................37 實驗藥品.................................................. 37 儀器設備.................................................. 38 實驗步驟.................................................. 41. 3-3-1 3-3-2 3-3-3. La3OF3S2:Ce3+ ( or Mn2+, Na+ )螢光材料之合成與特性鑑定.... 42 Ce1-xLnxSF ( Ln = Tb3+, Mn2+, Y3+, Gd3+ )螢光材料之合成與特性鑑 定................................................... 43 (Ce1-x Tb x)2CaF4S2 與 Ce2(Ca1-xMnx)F4S2 螢光材料之合成與特性 鑑定................................................. 44. 3-3-4 (Ce1-xYx)2SrF4S2 螢光材料之合成與特性鑑定............... 45 第四章 結果與討論....... ......................................... 46 v.
(8) 4-1 螢光體合成與 X 光繞射圖譜之分析............................46 4-1-1 La3OF3S2 X 光繞射圖譜之研究........................... 46 4-1-2 (La1-xCex)3OF3S2 X 光繞射圖譜與晶相鑑定之研究...........48 4-1-3 4-1-4 4-1-5 4-1-6. (La1-xMnx)3OF3S2 X 光繞射圖譜與晶相鑑定之研究........... 51 CeSF X 光繞射圖譜與晶相鑑定之研究.....................53 (Ce1-xGdx)SF 之 X 光繞射圖譜之研究...................... 55 (Ce1-xTbx)SF X光繞射圖譜之研究......................... 57. 4-1-7 4-1-8 4-1-9 4-1-10 4-1-11. (Ce1-xMnx)SF1-x X 光繞射圖譜與晶相鑑定之研究............ 60 (Ce1-xYx)SF X 光繞射圖譜與晶相鑑定之研究................62 Ce2CaF4S2 X 光繞射圖譜與晶相鑑定之研究.................64 (Ce1-xTbx)2CaF4S2 之 X 光繞射圖譜與晶相鑑定之研究....... 66 Ce2(Ca1-xMnx)F4S2 X 光繞射圖譜與晶相鑑定之研究......... 68. 4-1-12 Ce2SrF4S2 X 光繞射圖譜與晶相鑑定之研究................ 70 4-1-13 (Ce1-xYx)2SrF4S2 X 光繞射圖譜與晶相鑑定之研究............ 72 4-2 掃瞄式電子顯微鏡影像之分析................................ 75 4-2-1 La3OF3S2 掃描式電子顯微鏡之影像....................... 75 4-2-2 CeSF 掃描式電子顯微鏡之影像.......................... 76 4-2-3 4-2-4 4-3 Ce3+ 4-3-1 4-3-2. Ce2CaF4S2 掃描式電子顯微鏡之影像.......................77 Ce2SrF4S2 掃描式電子顯微鏡之影像....................... 78 活化螢光體螢光特性之研究.............................. 79 La3OF3S2:Ce3+ 放光特性之研究..........................79 CeSF 放光特性之研究.................................. 82. 4-3-2-1 Ce1-xGdxSF........................................ 86 4-3-2-2 Ce1-xYxSF......................................... 87 4-3-3 Ce2CaF4S2 放光特性之研究..............................90 4-3-4 Ce2SrF4S2 放光特性之研究.............................. 93 4-3-5 4-4 Mn2+ 4-4-1 4-4-2 4-4-3. 討論................................................. 98 活化螢光體之研究.................................... 101 La3OF3S2:Mn2+ , Na+ 放光特性之研究................... 101 CeSF:Mn2+ 放光特性之研究............................ 102 Ce2CaF4S2:Mn2+ 放光特性之研究....................... 104. 4-4-4 討論................................................ 105 3+ 4-5 Ce /Tb3+共摻螢光體之研究................................. 107 4-5-1 CeSF:Tb3+ 放光特性之研究............................ 107 4-5-2 Ce2CaF4S2:Tb3+ 放光特性之研究........................ 110 4-5-3 討論................................................ 113 4-6 氧氟硫化物與氟硫化物螢光粉之熱消光效應................... 116 4-6-1 La3OF3S2:Ce3+螢光體熱消光之研究...................... 116 ii.
(9) 4-6-2 4-6-3 4-6-4. CeSF:Ln3+ ( Ln3+ = Y3+, Tb3+ )螢光體熱消光之研究..........119 Ce2CaF4S2:Ln3+ ( Ln3+ = Tb3+ )螢光體熱消光之研究......... 123 Ce2SrF4S2:Ln3+ ( Ln3+ = Y3+ )螢光體熱消光之研究...........126. 4-6-5 討論................................................ 131 4-7 螢光粉之應用............................................. 133 第五章 結論......................................................135 第六章 未來展望..................................................137 參考文獻.......................................................... 138. iii.
(10) 表目錄 表1 表2 表3 表4 表5. La3OF3S2 晶格常數............................................. 31 CeSF 晶格常數.................................................33 Ce2SrF4S2 與Y2SrF4S2 晶格常數之比較............................. 35 本論文所合成四種螢光粉放光特性之比較.......................... 98 本論文所合成螢光粉與商品YAG之QE值與C.I.E.座標值比較.......... 99. 表6 表7 表8 表9 表10. CeSF與Ce2SrF4S2螢光粉摻雜Y3+離子後之QE值與C.I.E.座標值比較....100 本論文所合成螢光粉摻雜Mn2+後放光特性之比較...................105 CeSF與Ce2CaF4S2螢光粉摻雜Tb3+後放光特性與文獻之比較.......... 113 (Ce1-xTbx)SF 螢光體色度坐標之比較............................. 114 (Ce1-xTbx)2CaF4S2螢光體色度坐標之比較......................... 115. 表11 摻雜Ce3+螢光粉淬滅溫度之比較................................ 131 表12 摻雜Tb3+螢光粉淬滅溫度之比較................................ 132 表13. 本研究螢光體發光特性與量子效率之比較........................ 135. ii.
(11) 圖目錄 圖 圖 圖 圖 圖. 1-1 白光 LED 製作示意圖........................................... 3 1-1 敏化劑與活化劑能量轉移示意圖................................. 6 1-3 活化劑離子基態與激發態組態示意圖............................. 7 1-4 電子躍遷過程之呼吸模型....................................... 9 1-2 Stokes Shift 示意圖............................................ 10. 圖 圖 圖 圖 圖. 1-6 自由態三價鑭系離子的 4f n 能階示意圖......................... 13 1-7 晶場與自旋-軌域對 Ce3+ 能階分裂效應示意圖.....................14 1-8 Tb3+ 能階分裂示意圖.......................................... 15 1-9 結晶場效應對 Mn2+能階分裂示意圖............................. 16 1-10 d5 電子組態的 Tanabe-Sugano diagram........................... 17. 圖 1-11 共價性及結晶場效應造成 d 軌域能階分裂示意圖................. 19 圖 1-12 敏化劑 S 與活化中心 A 之間能量轉移示意圖..................... 22 圖 1-13 C.I.E.色度座標............................................... 26 圖 2-1 La3OF3S2 晶體結構示意圖...................................... 32 圖 圖 圖 圖 圖. 2-2 La3OF3S2 之 La3+ 配位環境示意圖............................... 32 2-3 CeSF 晶體結構示意圖......................................... 34 2-4 CeSF 之 Ce3+ 配位環境示意圖................................. 34 2-5 Ce2AF4S2 (A=Ca, Sr)晶體結構示意圖............................. 36 2-6 Ce2AF4S2 (A=Ca, Sr) 配位環境示意圖............................ 36. 圖 圖 圖 圖 圖. 4-1 不同燒結溫度所製備La3OF3S2 之X光繞射圖譜之比較.............. 47 4-2 Miller Index 標定 La3OF3S2 X 光繞射圖譜......................... 47 4-3 含不同 Ce3+濃度 (La1-xCex)3OF3S2 X 光繞射圖譜之比較..............48 4-4 (La1-xCex)3OF3S2 晶格常數/體積與Ce3+ 濃度之關係................. 50 4-5 不同濃度 Mn2+摻雜(La1-xMnxNax)3OF3S2 之 X 光繞射圖譜比較.........51. 圖 圖 圖 圖. 4-6 4-7 4-8 4-9. 圖 圖 圖 圖 圖. 4-10 Ce1-xGdxSF晶格常數/體積與Gd3+ 濃度之關係..................... 56 4-11 含不同Tb3+濃度 (Ce1-xTbx)SF X光繞射圖譜之比較................ 57 4-12 最高摻雜濃度Ce0.9Tb0.1SF與雜相來源之X光繞射圖譜比較......... 58 4-13 Ce1-xTbxSF晶格常數/體積與Tb3+ 濃度之關係......................59 4-14 含不同Mn2+濃度 (Ce1-xMnx)SF1-x X光繞射圖譜比較............... 60. (La1-xMnxNax)3OF3S2 晶格常數/體積與 Mn2+ 濃度之關係.............52 不同燒結溫度所製備CeSF之X光繞射圖譜之比較.................. 53 Miller Index 標定 CeSF 之 X 光繞射圖譜..........................54 含不同Gd3+濃度 (Ce1-xGdx)SF 之X光繞射圖譜比較................ 55. 圖 4-15 Ce1-xMnxSF1-x晶格常數/體積與Mn2+ 濃度之關係................... 61 圖 4-16 含不同 Y3+濃度 (Ce1-xYx)SF X 光繞射圖譜之比較.................62 圖 4-17 Ce1-xYxSF 晶格常數/體積與 Y3+ 濃度之關係......................63 ii.
(12) 圖 4-18 於不同溫度所製備Ce2CaF4S2 X光繞射圖譜之比較................ 64 圖 4-19 Miller Index 標定 Ce2CaF4S2 之 X 光繞射圖譜.................... 65 圖 4-20 不同濃度 (Ce1-xTbx)2CaF4S2 之X光繞射圖譜比較................. 66 圖 圖 圖 圖. 4-21 (Ce1-xTbx)2CaF4S2 晶格常數/體積與 Tb3+ 濃度之關係...............67 4-22 不同濃度 Ce2(Ca1-xMnx)F4S2 之X光繞射圖譜比較................ 68 4-23 Ce2Ca1-xMnxF4S2 晶格常數/體積與 Mn2+ 濃度之關係...............69 4-24 不同合成條件所製備 Ce2SrF4S2 之 X 光繞射圖譜之比較............ 71. 圖 圖 圖 圖 圖. 4-25 Miller Index 標定 Ce2SrF4S2 X 光繞射圖譜........................ 71 4-26 含不同 Y3+濃度 (Ce1-xYx)2SrF4S2 之 X 光繞射圖譜比較.............72 4-27 (Ce1-xYx)2SrF4S2 晶格常數/體積與 Y3+ 濃度之關係................. 74 4-28 La3OF3S2 之 SEM 影像........................................75 4-29 CeSF 之 SEM 影像............................................76. 圖 圖 圖 圖 圖. 4-30 Ce2CaF4S2 之 SEM 影像........................................77 4-31 Ce2SrF4S2 之 SEM 影像........................................78 4-32 (La1-xCex)3OF3S2 激發與放射光譜...............................80 4-33 (La1-xCex)3OF3S2 螢光粉發光強度與 Ce3+濃度之關係...............80 4-34 (La0.94Ce0.6)3OF3S2 放射光譜之解析..............................81. 圖 圖 圖 圖 圖. 4-35 La3OF3S2 與 La3OF3S2:Ce3+漫反射光譜之比較.....................82 4-36 CeSF 激發與放光光譜........................................ 83 4-37 CeSF激發與放射光譜隨著時間的變化........................... 84 4-38 CeSF放射光譜之解析......................................... 85 4-39 CeSF 漫反射光譜............................................ 86. 圖 圖 圖 圖. 4-40 (Ce1-xGdx)SF激發與放光光譜................................... 87 4-41不同Y3+濃度攙雜的(Ce1-xYx)SF激發與放光光譜................... 89 4-42 摻雜 Y3+的 Ce1-xYxSF 之能階示意圖............................. 90 4-43 Ce2CaF4S2 激發與放射光譜以及放光強度隨時間的變化.............91. 圖 圖 圖 圖 圖. 4-44 Ce2CaF4S2 之放射光譜解析.....................................92 4-45 Ce2CaF4S2 漫反射光譜.........................................93 4-46 不同合成條件所得 Ce2SrF4S2 之放射光譜........................ 94 4-47 (Ce1-xYx)2SrF4S2激發與放光光譜................................95 4-48 Ce2SrF4S2 放射光譜之解析..................................... 96. 圖 圖 圖 圖 圖. 4-49 Ce2SrF4S2 與(Ce0.9Y0.1)2SrF4S2漫反射光譜........................ 97 4-50 合成螢光粉與商品 YAG 色度座標之比較........................ 99 4-51 合成螢光粉與摻雜 Y3+離子後色度座標之比較...................100 4-52 La3OF3S2 與La3OF3S2: Mn2+, Na+漫反射光譜之比較............... 102 4-53 CeSF與CeSF:Mn2+ 漫反射光譜之比較.......................... 103. 圖 4-54 Ce2CaF4S2 與Ce2CaF4S2: Mn2+漫反射光譜之比較................. 104 圖 4-55 摻雜Mn2+離子色度座標之比較................................ 106 ii.
(13) 圖 4-56 Ce1-xTbxSF激發與放射光譜................................... 108 圖 4-57 Ce1-xTbxSF發光強度與Tb3+濃度之關係.......................... 108 圖 4-58 CeSF 與 CeSF:Tb3+ 漫反射光譜之比較.......................... 109 圖 圖 圖 圖. 4-59 (Ce1-xTbx)2CaF4S2激發與放射光譜..............................110 4-60 (Ce1-xTbx)2CaF4S2發光強度與Tb3+濃度之關係.................... 111 4-61 Ce2CaF4S2 與Ce2CaF4S2:Tb3+ 漫反射光譜之比較.................. 112 4-62 Ce1-xTbxSF 色度座標之變化趨勢.............................. 114. 圖 圖 圖 圖 圖. 4-63 (Ce1-xTbx)2CaF4S2色度座標之變化趨勢......................... 115 4-64 (La0.94Ce0.06)3OF3S2 熱消光光譜................................ 117 4-65 (La0.94Ce0.06)3OF3S2發光強度、最佳放光波長與溫度之關係......... 117 4-66 (La0.94Ce0.06)3OF3S2的ln[(I0/I)-1]與1/T之關聯..................... 118 4-67 CeSF 熱消光光譜............................................119. 圖 4-68 Ce0.85Y0.15SF熱消光光譜...................................... 120 圖 4-69 Ce0.94Tb0.06SF熱消光光譜..................................... 120 圖 4-70 CeSF 與 CeSF:Ln3+ ( Ln = Y3+ , Tb3+ )發光強度、最佳放光波長與溫度之關 係................................................................ 121 圖 4-71 CeSF 與 CeSF:Ln3+ ( Ln = Y3+ , Tb3+ )之 ln[(I0/I)-1]與 1/T 之關聯......122 圖 4-72 Ce2CaF4S2熱消光光譜........................................123 圖 4-73 (Ce0.97Tb0.03)2CaF4S2 熱消光光譜............................... 124 圖 4-74 Ce2CaF4S2 與(Ce0.97Tb0.03)2CaF4S2 發光強度、最佳放光波長與溫度之關 係................................................................ 125 圖 4-75 Ce2CaF4S2與(Ce0.97Tb0.03)2CaF4S2之ln[(I0/I)-1]與1/T之關聯.......... 126 圖 圖 圖 圖. 4-76 Ce2SrF4S2 熱消光光譜........................................ 127 4-77 (Ce0.98Y0.02)2SrF4S2 熱消光光譜.................................127 4-78 (Ce0.92Y0.08)2SrF4S2熱消光光譜................................. 128 4-79 Ce2SrF4S2 與 Ce2SrF4S2:Y3+發光強度、最佳放光波長與溫度之關係...129. 圖 4-80 Ce2SrF4S2與Ce2SrF4S2:Y3+之ln[(I0/I)-1]與1/T之關聯............... 130 圖 4-81 摻雜Ce3+螢光粉發光強度與溫度關係圖........................ 131 圖 4-82 摻雜Tb3+螢光粉發光強度與溫度關係圖........................ 132 圖 4-83 Ce2CaF4S2:Tb3+(green-yellow)與 BaMgAl10O17:Eu2+(blue)搭配 365 nm chip 之電致發光光譜....................................................134. iii.
(14) 第一章 緒論 1-1 研究動機 由於科技的進步,發光材料被廣泛地應用於人類的生活中,包括 從早期的日光燈、霓虹燈等照明設備,一直到現在備受矚目的電子顯 示器。而顯示器的種類繁多,有陰極射線管顯示器(CRT)、液晶顯示 器(LCD)、電漿顯示器(PDP)、有機發光二極體顯示器(OLED)以及發 光二極體(LED)等十多種不同的形式。從白光發光二極體問世以來, 就不斷的被研究開發,由於白光的應用廣泛,例如機車尾燈、汽車頭 燈、路燈、電腦指示燈、手電筒、LED背光源等,涉及生活中各個層 面,被視為未來最有發展潛力的照明光源。白光LED與市面上的白熾 鎢絲燈泡及日光燈相比,具有體積小、反應速度快、低耗電量、元件 壽命長、光指向性強、低熱輻射、高發光效率、可平面封裝、耐震以 及無汞污染等優點,且近年來成功發展出高功率與高亮度LED,被視 為下世代照明光源的主流。 1907 年美國無線電工程師Henry Joseph Round在 SiC 半導體材 料中觀察到電致發光的現象,之後俄國人O. W. Losseve將電流注入此 材料中而產生藍光,被認為是LED始祖。 1970 年代第一顆商用LED 出現,為J. I. Pankove 所製作的橘光LED以及美國GE、Monsanto 與 IBM 的 聯 合 實 驗 室 成 功 開 發 出 第 一 顆 磷 砷 化 鎵 (GsAsP) 的 紅 光 1.
(15) LED,其後各國的科學家都陸續進行各種發光半導體的研究,然而 1970~1980 年代開發出來的二元及三元LED因亮度偏低,且發光區域 集中在紅、黃、橙、綠等光,因此僅作為指示燈、數字顯示等用途, 為 傳 統 LED 時 代 。 1991 年 HP 與 東 芝 合 作 開 發 出 以 磷 化 鋁 鎵 銦 (InGaAlP)為材料的LED,可發出高亮度紅光與琥珀色光,被歸類為 高亮度LED,此後LED產業開始朝向高亮度發展。因高亮度LED的應 用廣泛,包括面板背光源、戶外顯示器、車用照明、室內外照明及交 通號誌等。由於磷化鋁鎵銦其四元組成元素的特性,包括磷化鎵、磷 化砷鎵、甚至磷化鋁鎵銦皆為紅、黃、橘、綠光,而無法得到藍、紫 光,因此一直無法使LED達到全彩化。直到 1993 年日亞化學(Nichia Chemicals) 的中村修二博士成功開發出以氮化鎵銦 (InGaN) 為材質 的藍光LED,配合MOCVD的磊晶技術可製成高亮度的純綠及藍光 LED,成為全球第一個能夠商業化量產的藍光LED產品。隨後 1996 年又發表以氮化物(GaN)系列的藍光LED(波長 460~470 nm),與鈰釔 鋁石榴石 (yttrium aluminum garnet ; YAG:Ce3+ )的黃光螢光粉(發光 波長為 550 nm)搭配而得白光發光二極體[1],此經混光作用而得的白 光光源,成為全球照明市場最矚目的新興光源。. 2.
(16) 圖 1-1[2]顯示目前白光LED的製作方式主要有以下四種: (1) 整合紅、綠、藍三LED晶片取得白光。 (2) 藍光LED晶片與黃光螢光粉搭配以產生白光。 (3) 藍光LED晶片與紅、綠螢光粉搭配以產生白光。 (4) 紫外光LED晶片與三原色螢光粉搭配以產生白光。 其中,利用紫外光晶片搭配三原色螢光粉所得到的光譜範圍廣、演色 性佳等優點,是目前較具發展潛力的白光光源。. 圖 1-1 白光 LED 製作示意圖[2] 目前以藍光晶片激發黃光螢光粉以獲得白光相關的技術具有專 利限制,例如:日亞化學公司的Y3Al5O12:Ce3+(YAG:Ce)螢光粉和歐斯 朗(Osram)公司的Tb3Al5O12:Ce3+(TAG:Ce)。因此開發新穎組成藍光激 發螢光粉或紫外光激發螢光粉,以迴避國外專利限制且可應用在LED 進行光轉換的螢光材料為當前首要目標。 本論文研究動機為尋找目前尚未被國內外專利涵蓋的LED螢光 材料及組成配方,並對不同的稀土離子、過渡元素發光特性進行探 3.
(17) 討。我們在設計螢光粉時需考慮主體與活化離子,為得到激發波長較 長之螢光體,而挑選主體為共價性較強之氟硫氧化物與氟硫化物,並 搭配可激發寬帶的稀土離子作為活化劑,為本研究的重點。由於常用 的活化離子很多,而以稀土離子作為發光中心可大致分為 f→f 與 f→ d 兩種躍遷:(1) f→ f 躍遷受到外層5s與5p軌域的遮蔽,其激發波 長與發光波長的變化較小;(2) f→ d 躍遷受晶場影響大,其激發波長 與發光波長呈現明顯變化。而本研究除了摻雜發光特性具明顯變化之 Ce3+的 f→ d 躍遷外,亦探討摻雜發光特性較不受主體影響之Tb3+的 f→ f 躍遷,並搭配主體設計之規則以篩選主體,希望能得到寬帶激 發的新穎螢光材料。而寬帶激發具有多波段選擇之特性,利用價值較 高,故為本研究之方向。. 4.
(18) 研究背景. 1-2 1-2-1. 螢光體發光原理. 螢光材料泛指在接受紫外光、X光或電子等高能粒子照射後,材 料內部發生能量的吸收、轉換與緩解過程,最後以光輻射的方式輸出 能量。而激發螢光體的激發源有很多種,如:紫外光、陰極射線、電 壓、熱、摩擦、化學、X光,本研究著重於光致發光材料發光原理的 探討。 螢光粉主要由主體(Host)與活化劑(activator)組成,有時還需要敏 化劑(sensitizer)作為能量傳遞的媒介,化學式通常以H: A或H: S, A來 表示。主體在光的激發過程中傳送能量,活化劑則激發活化主晶格, 吸收激發光後產生可見光輻射,故活化劑是扮演發光中心的角色。而 添加敏化劑是為了能夠更有效地吸收激發的能量,並將能量傳遞給活 化劑,以達到提升放光效率的效果 。此外還可再加入助激活劑 (coactivator)作為電荷補償劑,而提升放光強度。 下圖為敏化劑將吸收的部分能量轉移給活化劑,活化劑被激發後 放光的機制示意圖:. 5.
(19) 圖 1-1 螢光體中敏化劑與活化劑能量轉移示意圖[3] 若以能階(energy level)及電子躍遷(electronic transition)的觀點來 解釋螢光體的發光過程。當活化劑離子吸收外部光源的能量後,位於 基態的電子躍遷至激發態,這時若直接由這能態迅速緩解至激發態中 的最低振動能態,再以放光形式回到基態,就稱為螢光 (fluorescence);若是經由系統間跨越(intersystem crossing)轉移至電子 自旋三重態的能態,再緩解至最低振動能態,然後以放光的形式釋放 能量回至基態,則稱為磷光(phosphorescence),兩者皆屬於自發性的 發光。基本上,電子的躍遷具有某些特性,這些特性稱為選擇律 (selection rule),若在基態與激發態間的躍遷具有這些特性,則此躍遷 稱為允許的(allowed);反之則稱為禁止的(forbidden)。 根據自旋選擇律(spin selection rule)和Laporte’s rule,躍遷僅於相 同自旋多重態S(spin multiplicity)之間發生,即總自旋量子數不變 (ΔS=0),和不同的反轉對稱(Inverse symmetry)即g→u或u→g,例如 6.
(20) s→p、p→d或d→f 軌域之間的躍遷為允許的;而d→d或f→f 軌域之 間的躍遷為禁止的。螢光因為遵守選擇律,電子能量的轉移不涉及電 子自旋態的改變(△S=0),發生的機率較高、發光強度較強、衰減期 也較短暫(約10-9-10-3秒);而磷光因牽涉到多重態的電子能量轉移,不 遵守選擇律,發生的機率較低、衰減期較長(約10-3-10秒)。 螢光粉的活化劑為稀土離子(rare earth ions)和過渡金屬離子 (transition metal ions),造成放射光譜呈現線狀或是寬帶狀,其放光機 制可藉由圖 1-3[4]組態座標圖(configurational coordinate diagram)的觀 念加以解釋。圖 1-3[4]中,橫座標為晶格中陽離子與陰離子團間的平 衡距離(r),縱軸為能量E,其間的關係可用振子(oscillator)中能量與位 1 2. 移的關係式 E kr 2 來描述,其中k為力常數,而r為位移。. 圖 1-3 活化劑離子基態與激發態組態示意圖[4]. 7.
(21) 當活化劑吸收外部光源的能量後,被激發到激發態而導致活化劑 離子附近的晶格發生膨脹。激發跟放光的過程在圖 1-3[4] 中以垂直箭 頭表示,是代表活化劑的原子核在這些過程中仍然停留在大約相同的 位置。而根據 Franck-Condon 原理,由於原子核的重量是電子的 103-105倍,電子的移動速度遠比原子核快很多,電子的振動頻率也較 原子核快,因此在電子由基態躍升至激發態時,可以假設晶體中原子 核間的相對位置(r)和振動頻率大約不變。而躍遷產生時,以基態的電 子發生機率最高,如圖中的r0位置處。以△r=r1-r0 來表示電子與發光 中心之振動交互作用的程度;當該躍遷的△r=0時,由於無振動過程 牽涉其中,其電子與發光中心振動偶合極弱(vibronic coupling),稱之 為零點躍遷(zero-transition)或非聲子躍遷(non-phonon transition),此一 情況所展現的吸收或放射光譜的波峰皆為陡峭的波峰(sharp peak)。 當 主 體 晶 格 與 活 化 中 心 產 生 聲 子 波 傳 遞 (phonon wave propagation),而引起電子與晶格振動偶合(vibronic-coupling),使得△r 不等於零,造成激發態的化學鍵長與基態的化學鍵長不同,因基態能 階不再與激發態能階平行,會產生一明顯的距離改變(△r ≠ 0),此時 所展現的光譜為寬帶(broad band)。當 △r >>0時,電子遷移與聲子 (phonon)或晶格振動偶合作用最強,而螢光體放光的過程中通常會伴 隨一些非輻射或熱緩解的行為在內,使得吸收與放射的能量有所差. 8.
(22) 異,兩者相對應的波長位置當然也產生明顯的位移而有差距存在,這 個差距即稱之為Stokes shift。另外,當螢光體的溫度超過一定值時, 振動能有足夠的能量去激發活化劑的電子到激發態的Q點,然後經由 振動耗損能量而回到基態,造成激發能量耗損於晶格中且不貢獻於發 光,此現象稱之為溫度淬滅效應[4]。 在圖 1-4[5] 中,同樣以模型解釋電子躍遷過程。當電子處於基態 時,中心陽離子與周圍陰離子皆處於一平衡狀態,受外加能量激發 時,陽離子運動軌域變大,此時周圍的陰離子依然保持不動。接著經 由晶格緩解,陰離子移動至另一平衡位置,而後經由放光過程之輻射 緩解回至基態時,陽離子軌域回復原本大小,陰離子再收縮回至基態 之平衡位置。因此在電子吸收能量與放射能量時,會有兩次的晶格緩 解而發射聲子,即以熱振動的方式失去能量,導致放射的能量比吸收 的能量低,此即為史托克位移(Stokes shift)產生之原因。. 圖 1-4 電子躍遷過程之呼吸模型[5]. 9.
(23) Stokes shift 可以由下方程式表示: Stokes shift = 2Shν 其中S為Huang-Rhys偶合常數,通常為一整數,代表電子-晶格振動偶 合之積分因子;ν為兩振動能階間的能量差;h為普朗克常數。當S<1 時稱之為弱偶合,也就是電子與聲子的作用弱;1<S<5時,稱為中度 偶合;S>5時則為強度偶合,表示電子與聲子的作用強。由於Stokes shift與(△r)2成正比,因此△r越大,Stokes shift也越大,在光譜上所顯 示的放射峰也就越寬廣。. 圖 1-2 Stokes Shift 示意圖[6]. 10.
(24) 1-2-2 稀土離子能階 稀土元素(rare-earth elements)包含元素周期表中從鑭(Lanthanum; La)到鎦(Lutetium; Lu)的15個鑭系元素及同族(ⅢB)的鈧(Scandium; Sc) 和釔(Yttrium; Y),總共17個元素。由於稀土元素的最外兩層軌域(5d6s) 電子組態相同,在化學反應中容易在4f、5d或6s軌域中失去3個電子 而成+3價態離子。根據Hund’s rule,在同一殼層中的電子若為全填 滿、半填滿或全空時,電子雲的分布呈球型,此時的原子或離子比較 穩定。因此在三價稀土離子中,Y3+ (4f 0)、La3+ (4f 0)、Gd3+ (4f 7)和Lu3+ (4f 14)比較穩定,激發能階均較高,在可見光區沒有發射和吸收躍遷, 而具有很強傳遞輻射能量能力,故適合做為發光材料的主體元素。 稀土元素具有未填滿的 4f 5d 電子組態,可以[Xe]4f n5dm6s2 (n = 1~14, m = 0 或 1)通式表示,其表現豐富的可躍遷的電子能階和長壽 命的激發態能階(10-2 ~10-6 秒),可能的能階躍遷多達 20 萬種,因此 可以產生紫外-可見-紅外光譜範圍內的躍遷吸收和放射,具有作為各 種發光材料的活化劑之潛力。 所有正三價態鑭系離子其電子組態通式為 [Xe]4f n5s25p6 (n =1~ 14),除La3+ 和Lu3+ (4f 殼層為全空和全滿)外,其它鑭系元素的4f 電 子可以在4f 及5d6s6p各軌道之間分布。但能階之間的躍遷會受到光 譜選擇律的限制,且有些能階的能量很高而超出紫外光的範圍,所以. 11.
(25) 在近紫外到近紅外光學範圍內,能觀測到的譜線所對應的能階數仍有 一定的限制。 此外,4f 電子受到外層 5s25p6 軌域上電子的屏蔽作用(shielding effect),故晶場作用對鑭系離子 4f n 電子的影響相當地小,產生的能 階分裂(splitting)僅幾百個波數,因此晶體中鑭系元素離子的光譜和自 由離子的光譜都是線狀光譜,其發射特性與主體結構無關。然而部份 稀土離子的 5d 電子因處於外層,易受晶場作用而產生能階分裂,例 如 Eu2+、Ce3+等離子由於 5d-4f 躍遷(△l =1,在光譜選擇律是允許 的躍遷),其光譜呈現寬帶放射,且強度也較高(參考圖 1-6. [3,8]. )。這. 類離子因結晶場以及晶體中格位的對稱性對於其能階會產生影響,而 可能造成發光離子基態(ground state)與激發態(excited state)能階的分 裂,另外還有光譜選擇律的限制,而影響到放射光譜的強度以及分 裂,且最終影響到放光波長與色度[7]。. 12.
(26) 圖 1-6 自由態三價鑭系離子的 4f n 能階示意圖[8]. 在了解相關基礎理論後,以下將逐步介紹幾種在本研究中所探討 的稀土離子(Ce3+, Tb3+)及過渡元素(Mn2+):. 13.
(27) (1). Ce3+( [Xe]4f 1 ): Ce3+的4f 1電子基態能階在自旋軌道偶合的作用下,分裂成 2F7/2. 和2F5/2二個能階,差距約 2000 cm-1 。最鄰近的激發態為 5d 能階, 易受到結晶場的影響分裂為 2 ~ 5 個能階,而激發態的電子可能緩解 到兩種基態,所以會產生兩個放射的寬帶(圖 1-7)[3],故 Ce3+放光 具有典型雙峰特徵,且發射的波長一般位於紫外光和藍光區域。但在 釔鋁石榴石 Y3Al5O12 中 Ce3+ 因受結晶場影響( crystal field effect ),使 得放射波長位於綠光及紅光區域。而在CaS: Ce3+中Ce3+受到共價效應 ( covalency effect )影響而發紅光。此乃因Ce3+ 的5d電子處於外層,使 其發光受主體環境的影響十分明顯,因此在不同主體中而有不同的放 光波長。特別的是,Ce3+有一個寬而強的 4f-5d 吸收帶,不僅可有 效地吸收能量使本身發光,還可將能量傳遞給其它離子而起敏化作 用。另外,因 4f-5d 間的能階躍遷遵守選擇律,所以Ce3+ 的5d激 發態的平均壽命很短,在 10-7 ~ 10-8 s 之間,而適合用作超短餘輝發 光材料。. 圖 1-7 晶場與自旋-軌域對Ce3+ 能階分裂效應示意圖[3] 14.
(28) (2). Tb3+( [Xe]4f 8 ): Tb3+的4f 殼層具有8個電子,根據Russell-Saunders Coupling(或稱. L-S coupling)[5],其基態能階在自旋軌道偶合的作用下,分裂成七重 態,而放光主要來自於第一激發態5D4→7FJ (J=0~6)的電子躍遷,波長 範圍為 460 ~ 660 nm(綠光區)。但也有5D3→7FJ 較高能量的藍光和紫 外範圍的放射(圖 1-8[7])。由於Tb3+ 和大多數的三價稀土離子一樣, 在吸收外界的能量後,電子從基態躍遷至激發態為 f-f 能級躍遷( f-f transition),屬於4f 內部殼層發生的躍遷機制,在受到外層電子( 5s25p6 ) 的遮蔽下,產生的光譜不受主體環境影響、對於激發能量的吸收小、 放光較弱、半衰期長( >1 ms ),且光譜為線狀光譜。. 圖 1-8 Tb3+ 能階分裂示意圖[7] 15.
(29) (3) Mn2+( [Ar]3d5 )[5,9,10]: Mn2+ 於 d 軌域外層具有 5 個電子,由於 d 軌域價電子在空間中 三個方向的分佈不一,若周圍環境的配位方式不同(常見配位數為 4 或 6),就會使原本相同能階的五個 d 軌域分裂成兩組不同的軌域, 圖 1-9 即為軌域與能階關係圖。. 圖 1-9 結晶場效應對Mn2+能階分裂示意圖[9] Mn2+的電子基態能階為6A1,其能階因受到強自旋軌域偶合的影 響,而分裂成多個光譜項,如圖1-10。在受到外界能量的激發下,電 子從基態躍遷至激發態為 d-d 能級躍遷( d-d transition),屬於外殼層 發生的躍遷機制,故易受晶場作用的影響,放射光譜會產生紅位移或 藍位移的變化。且 d-d 能級躍遷在光譜選擇律中屬於宇稱及自旋禁 制,所以在紫外光或可見光的激發下,其發光訊號很微弱。其放射光 譜為一寬帶波形,從Mn2+ 的Tanabe-Sugano diagram,可看出此寬帶即 為4T1(4G)6A1(6S) 躍遷。一般來說,若Mn2+ 填在四面體格位中屬於 弱結晶場,放射綠光,若Mn2+ 填在八面體格位中(強結晶場) ,則放 16.
(30) 射橘光或紅光。. 圖 1-10 d5 電子組態的Tanabe-Sugano diagram[5]. 1-2-3. 主體晶格效應. 在不同主體晶格中,活化劑離子因配位數和結晶場不同,所表現 出的發光特性也有所差異。若能夠掌握主體晶格對發光特性的影響因 子,就能預測螢光發光材料的性質。在主體晶格中有兩個影響光譜特 性的因素:一為主體共價效應(covalency effect);另一則是主體結晶 場效應(crystal field effect)。 17.
(31) 主 體 共 價 效 應 就 是 所 謂 的 電 子 雲 擴 散 效 應 (Nephelauxetic Effect),即是當陰離子配位基軌域與中心金屬原子鍵結形成分子軌域 時,中心金屬原子配位之陰離子種類不同而影響其共價性。在不同能 階間,電子躍遷的能量取決於電子間的作用力,當配位陰離子的電負 度越小時,因為陰陽離子間的陰電性差異變小,主體晶格具有較高的 共價性,而導致電子雲擴張、電子密度更分散於軌域中,電子間排斥 減小,使得中心金屬之電子處於更穩定的狀態,所對應的電荷轉移 (charge transfer) 躍遷能量降低。對同一金屬離子,不同配位基對電子 雲擴張效應的影響強弱趨勢如下[11]:. F - < H2O < NH3 <. 1 Ox2- < NCS - < Cl - < CN - < Br - < N3 - < I - < S 22. 當共價性增加時,電子雲擴散效應增加,使得不同能階間對應的 電子躍遷能量減小,故螢光體的發光波長產生紅位移。 結晶場理論主要是考量靜電作用力,以點電荷模型處理金屬離子 於錯合物及晶體化合物中能階分裂之情形。將金屬離子的配位基及周 圍環境均視為不具結構、無電子軌域之點電荷,由此建立一靜電場, 而主體結晶場理論即在處理此靜電場對於金屬離子d軌域上電子的作 用。由於電子帶有負電荷,周圍配位基就其電性而言亦屬於帶負電, 因此對於軌域上的電子而言,兩者間的作用力屬於靜電排斥力。由於. 18.
(32) d軌域共分成dxz、dyz、dxy、dx2-y2 和 dz2 五種軌域,當電子在 dx2-y2 和 dz2 軌域時會正對配位基,此時所受的靜電排斥力較大,而能階較高;若 電子為 dxz、dyz、dxy 軌域時,因位於兩配位基之間,受靜電力的影響 較小,而能階較低。如此受到 d 軌域的影響,總共會分裂成兩種不 同的能階。 圖 1-11[12] 說明電子雲膨脹效應和主體結晶場效應對於 4f-5d 能階躍遷之影響。電子雲擴散效應導致能量降低,而結晶場之作用則 導致能階分裂。故考慮 4f→5d 之能階躍遷,電子雲擴散效應使發光 波長產生紅位移,於結晶場作用5d能階將產生分裂;而 f→f 能階躍 遷之稀土離子,因 4f 殼層受到外層電子的遮蔽,較不受結晶場作用 之影響;但 d→d 能階躍遷之發光離子,結晶場的作用會導致發光波 長產生藍位移。. 圖 1-11 共價性及結晶場效應造成d軌域能階分裂示意圖[12]. 19.
(33) 1-2-4. 濃度淬滅. 一般活化劑(activator)的添加達到適當的比例時,螢光體會得到 最高的發光強度,隨後隨著添加量的增加,發光效率將不再提高反而 開始下降,此現象稱為濃度淬滅(concentration quenching)[3]。發生的 原因主要有以下兩種:一為發光中心在發光前產生能量轉移,而能量 於活化劑間轉移的機率會隨著活化劑增加而提升,同時能量傳遞至淬 滅劑或缺陷中心的機率也隨之增加,使能量以非輻射放光釋出;另一 原因為活化劑濃度升高時,活化中心之間的距離變短,使得能量在晶 格中持續轉移至其他活化劑離子的機率提高,以非輻射緩解 (non-radiative cross-relaxation)形式散失所致。. 1-2-5. 能量轉移. 螢光粉之活化中心之間的能量轉移 (energy transfer)[13]機制,主 要可分為輻射(radiative)與非輻射(nonradiative)兩大類: (1) 輻射轉移通常發生於鄰近且共振頻率相同的活化中心,當活化中 心 A1 吸收足夠能量,其基態電子被激發到激發態後,緩解並釋放出 光子,此光子被鄰近的活化中心 A2 捕捉,轉而激發 A2 的基態電子 至激發態,所以輻射能量轉移可視為活化中心之間實質的光子交換 (virtual photon exchange)。. 20.
(34) (2) 非輻射能量轉移過程中離子間並無帶電粒子轉移發生,其中最常 見的機制為共振(resonance)能量轉移。而共振能量轉移的發生必須滿 足以下條件:敏化劑與活化劑兩者之激發態與基態能量差相同,即為 共振狀態(resonance condition),以及兩中心之間存在適當的相互作 用 , 例 如 交 換 作 用 (exchange interaction) 、 輻 射 再 吸 收 (radiation reabsorption)或多偶極作用(multipolar-multipolar interaction)。 由於此一共振狀態可視為敏化劑的放射光譜與活化劑的吸收光 譜之相互重疊。由Dexter之推論可得以下關係式[14]:. PSA . 2π | S, A * | H SA | S*, A |2 g S E g A E dE . 其中,積分部分表示光譜重疊面積;gS(E) 和 gA(E)分別代表標準化的 敏化劑放射譜線與活化劑激發譜線;HSA 代表相互作用的哈密爾敦函 數(Hamiltonian);矩陣部分表示起始狀態| S*, A>與最終狀態<S, A* | 之間的交互作用;PSA 則為能量轉移機率,因此當光譜無重疊時,共 振能量轉移的現象也不會存在,如圖 1-12 所示。. 21.
(35) Energy transfer. 圖 1-12 敏化劑 S 與活化中心 A 之間能量轉移示意圖 當螢光體中的活化劑達到一定的離子濃度,且彼此間的距離夠近 而足以發生交互作用,其中之一即為能量轉移。Dexter提出固體材料 中的敏化發光(sensitized luminescence)的能量傳遞過程是由以下步驟 所組成[15]: (1) 敏化劑吸收一個光子的能量E0 ; (2) 敏化劑將其在輻射躍遷中可用之電子能量E1 緩解至周圍晶格, E1<E0 ; (3) E1轉移至活化劑; (4) 可被用作活化劑輻射 躍遷之電子能 量 E2 在活化劑周圍緩解 , E2<E1;或者能量在敏化劑周圍緩解使其回到類似(但不需要完全 一樣)原本未被激發前的狀態;. 22.
(36) (5) 放出能量為E2的光。. 1-2-6. 固態合成法. 在反應燒結中伴隨著化學反應的進行,稱之為固態反應法(solid state reaction)。此法是以金屬氧化物(metal oxides)或金屬鹽類(metal salts)作為起始物,依照適當的化學計量比例配製,經均勻混合研磨 後,再進行熱處理與燒結,並透過熱擴散的原理反應長成晶相。此為 一種簡單且被廣泛採用的技術,優點為成本較低、產物結晶性高以及 可大量生產,但有粉體均勻度(homogeneity)不佳、粒徑大小不均以及 合成顆粒較粗等問題。常用的改善方法如:研磨時利用球磨法 (ballmilling)使反應物混合均勻;但因各金屬鹽類在空氣中潮解的程度 不同,可能造成金屬離子不同比例的流失;而使用溶劑的濕式混合研 磨(wet mixing and milling),則因各金屬鹽溶解度不同,混合效率不 佳,故其效果有限。本研究使用固態合成法,是主要因為其合成步驟 簡單,儘管仍有顆粒大小不均,易導致螢光粉在塗佈上發生困難,但 本研究著重在找尋新穎的螢光材料,而非將螢光粉的發光效率最佳 化,所以固態法可以說是最好的選擇。. 23.
(37) 1-2-7. 三基色原理和C.I.E.色度座標圖[7]. 人眼可感受顏色的三種不同屬性:色調(hue)、彩度(chroma)與亮 度(brightness)。其中,色調為不同波長之色彩區隔,如紅、綠、藍等; 彩度指色彩之純度,描述顏色中純光譜色所佔之比例;亮度則為光強 度或物體明暗之程度。就人類的視覺觀點,感覺上同樣的色彩但實際 上卻可能是由不同波長的色光所混合而產生的效果,而紅、藍、綠三 原色光以不同的比例搭配,對人類的眼睛可以形成與各種頻率的可見 光等效的色覺,此乃光三原色原理。 1931 年 國 際 照 明 委 員 會 (CIE, Commission Internationale de I’Eclairage) 規定一套標準色度系統,以700nm、546.1nm與435.8nm 之標準紅(R)、綠(G)、藍(B)三原色,以數學線型操作變換之,並考慮 光源發射強度與人眼對於三原色之敏感變化,而確定了原色當量單 位。標準的白光光通量比為︰ Φr︰Φg︰Φb=1︰4.5907︰0.0601 原色光單位確定後,白光[W]的配色關係為︰ [W]=1[R]+1[G]+1[B] 其中 R 代表紅光,G 代表綠光,B 代表藍光。 對任意一彩色光 F 而言,其配色方程式為: F=r[R]+g[G]+b[B]. 24.
(38) 其中r、g、b. 為紅、藍、綠三色係數﹙可由配色實驗測得﹚ ,其對應. 的光通量(單位Φ,指光源的輻射通量對人眼引起的視覺強度),其單 位為流明(lumen簡稱lm,為照度單位)︰ Φ=680(R+4.5907G+0.0601B) 其中 r、g、b 的比例關係決定了所配色的光之色彩度(色彩飽和程 度),而其數值則決定了所配成彩色光的亮度。r[R]、g[G]、b[B]通稱 為物理三原色,三色係數之間的關係,可以利用矩陣加以表示,歸一 化(normalization)之後可以寫成︰ F=X[X]+Y[Y]+Z[Z]=m{x[X]+y[Y]+z[Z]} 其中m=X+Y+Z. 且x=(X/m)、 y=(Y/m)、z=(Z/m). 每一個發光波長都有特定的r、g、b值,將可見光區範圍的r值相 加總合為X,g值相加總合為Y,b值相加總合為Z,因此我們可以使用 x、y直角座標來表示螢光體發光的色度,此即所謂 C.I.E. 1931標準色 度學系統,簡稱 C.I.E.色度座標。圖 1-13[14] 中的黑色曲線,稱微光 譜軌跡,即所有譜色光都在線上面,自然界中的色彩皆能使用整個閉 合曲線及其內部所對應點的座標來表達。當座標點的位置越靠近譜色 軌跡,其所對應的色彩越純,代表色彩飽和度越高。當量測光譜後, 計算各個波長光線對光譜的貢獻,找出x、y值後,在色度座標圖上標 定出所對應的座標位置,我們就可以定義出螢光體所發光之色彩度。. 25.
(39) 圖 1-13 C.I.E.色度座標[14] 另外,以對應的黑體溫度值來描述光源的顏色稱之為色溫。不同 色溫的光源給予人不同氣氛的感覺,例如光源色溫大於5000K之晝光 色日光燈,因光色略藍具寒冷氣氛,適合熱帶地區使用;而低於3000K 之白熾燈因光色略紅,給予人溫暖的感覺,故適合寒冷地區使用。而 光源品質主要由光源對色彩之演繹表現所決定,即光源呈現物體真實 色彩之能力,稱為演色性,最小值為0,最大值為100,單位為Ra。因 此演色性越高的光源對顏色的表現較逼真,眼睛所呈現的物體會愈接 近原來的真實顏色。 1-2-8. 量子效率. 螢光體的量子效率QE (quantum efficiency, η),即為放射的光子數 與所吸收的光子數之比值,可由以下方程式來定義:. QE . No. of Photons Emitted No. of Photons Absorbed 26.
(40) 若以能量的觀點而言,則為放射能量總合與吸收能量總合的比值。此 時 QE 可以表示為: QE . (Id ) emission (1 - R) emission (Id ) absorption (1 - R) absorption. 其中I為強度、λ為波長、R為反射率,可由比對吸收光譜中得出反射 能量大小得知。所謂優良的螢光體,其QE值一般約為80%或更高。 若定義S為標準樣品,U為未知樣品,則未知樣品的量子效率為: (QE) U (QE)S . ( Edexc )S ( Edem ) U (1 - R) S ( Edexc ) U ( Edem )S (1 - R) U. 其中E為能量, λex 與 λem 分別代表激發與發射波長,Ed λex 則用吸 收值代表。 量子效率的量測方法如下: (1) 測量空積分球的背景值: 將未裝入待測樣品之石英片(holder)放入積分球中,使用樣品的 最佳激發波長,在不使用濾光片的情況下,激發空白之石英片 做空白實驗。並且把光譜上激發光源(±10 nm)的面積積分可得 值 Lb ,而此時在放光波段的面積積分值為 E b 。 (2) 將樣品置於積分球中入射光的路徑上: 將裝入待測樣品之石英片放入積分球中,使用樣品的最佳激發 波長,在不使用濾光片的情況激發樣品。並且把光譜上激發光. 27.
(41) 源(±10 nm)的面積積分而得到 Lc 值,將發光波段的面積積分得 到 Ec 。之後利用L b 與L c 依下式計算吸收係數A: A. Lb - Lc Lc. 最後以A、Eb 與Ec 依下列計算求得量子效率Φ:. Φ 1-3. E c - (1 - A)Eb A Lb. 文獻回顧 迄今在文獻中已有眾多有關摻雜稀土離子之螢光粉,本研究的鈰. 氟硫化物在摻雜 Tb3+ 離子後可明顯增加其量子效率,故著重於 Ce3+ 與 Tb3+ 共摻雜螢光粉的研究。文獻提到以三基色螢光粉(Y2O3:Eu3+、 MgAl11O19: Ce3+, Tb3+ 、BaMg2Al16O27:Eu2+)中,綠色螢光粉對燈的光 通量最大,一般均以 Tb3+ 作為活化劑,且以 Ce3+ 作為敏化劑。由於 Ce3+ 在紫外波段有一個寬而強的 4f-5d 吸收帶,其放光波段剛好與 Tb3+ 的吸收峰有部份的重疊,因此能將吸收的能量傳遞給Tb3+ 而起 敏化作用。如:1974年J. M. P. J. Verstegen等人所提出的MgAl11O19: Ce3+, Tb3+ (CAT)是目前最廣為使用的綠色螢光粉。CAT為六方晶系, 最強發射峰位於543nm,量子效率可達80%,是化學穩定性和熱穩定 性相當高的螢光粉。在CAT中,不存在Ce3+ → Ce3+的能量傳遞,且 Ce3+ → Tb3+ 的能量傳遞屬於多偶極作用,而Ce3+ 放光約在330nm,. 28.
(42) 與Tb3+ 的 7F6 → 5G2, 5D1, 5H1 吸收譜線之間有良好的重疊,因此Ce3+ → Tb3+ 為高效的能量傳遞,能使Tb3+ 的放光達到最高效率[7]。 目前稀土磷酸鹽為發光效率最高的螢光材料之ㄧ,而單斜晶系的 LaPO4: Ce3+, Tb3+ (LAP),具有比CAT更高的量子效率(高3%左右)、合 成溫度較低等優點而受到重視。LAP與CAP的放射光譜相似,色座標 也相近,而以LAP色座標的x值較高,能節省三基色螢光粉中昂貴的 紅粉比例。但化學穩定性不如CAT,溫度淬滅相當地嚴重,另外還有 製備工藝與生產成本等等考量,因此用量受到限制[16]。 活化劑Ce3+ 容易受到晶場的影響,在不同的配位環境中會有不一 樣的激發與放射光譜。例如在具有扭曲八配位 Y3+ 的 Y3Al5O12 呈現 黃光放射,而在具有八配位Y3+ 的YPO4中發藍光[17]。由此可知當 Ce3+ 進入高對稱性的格位中會導致較短波長的藍光放射,反之則會使放光 波長產生紅位移而有綠光至黃光的放射。而Tb3+ 因受到外層電子的遮 蔽,不太會受到晶場作用的影響,在不同的主體中皆具有相似的放射 光譜。 由於 Ce3+ 離子的 4f →5d 能階間之電偶極躍遷為選擇律所允 許,故其為寬帶的吸收與放射,迄今文獻上有許多利用 Ce3+ 扮演敏 化劑角色,將其部份能量傳遞給 Eu2+, Mn2+ 或 Tb3+ 等活化劑以提升 放光效率之相關研究。因此本論文以尚未發表且較易合成的氟硫化物. 29.
(43) 與氟氧硫化物為主體,進行 Ce3+ 與Tb3+ 的摻雜,並研究Ce3+ - Tb3+ 之間能量轉移的機制。 許多以氧化物為主體的螢光粉,普遍激發波長偏短,不適於以藍 光LED晶片激發製做白光LED。而以硫化物(等電子結構)為主體的螢 光粉因共價性較強,能使激發與放光波長紅位移,更符合白光LED的 需求[18]。例如以鈰離子激活氟硫化物螢光粉:Y2AF4S2:Ce3+ (A = Ca, Sr)[19]、α-YSF:Ce3+[20]、β-YSF:Ce3+[21]之製備及發光特性,以及其在白 光LED上面的應用,可以近紫外光或藍光激發,放射出藍光至紅光。 1-4. 螢光體設計原則 本論文選用氟硫化物及氟硫氧化物為主體有以下原因:(1)兩者. 皆為雲散效應強烈之共價化合物,適用於近紫外或藍光波段激發的 LED。(2)與一般氧化物相比,氟硫化物及氟硫氧化物皆具有較低的合 成溫度且容易製備。(3)比一般硫化物具有較高的化學穩定性與熱穩 定性。另外挑選 Ce3+ 或 Tb3+ 為主要活化中心,因 Ce3+ 具有寬廣的 激發與放光譜帶,通常位於近紫外光到藍光區域,符合本篇論文的要 求。另外,由於 Ce3+ 易受主體晶格環境而影響,當以 Ce3+ 為主體 基質或少量摻雜時,是否會因組成的不同而影響其發光及其與 Tb3+ 之間的相容性是否相當高而形成良好的固溶液。這些問題皆是目前在 文獻中甚少探討,是相當有趣的問題。. 30.
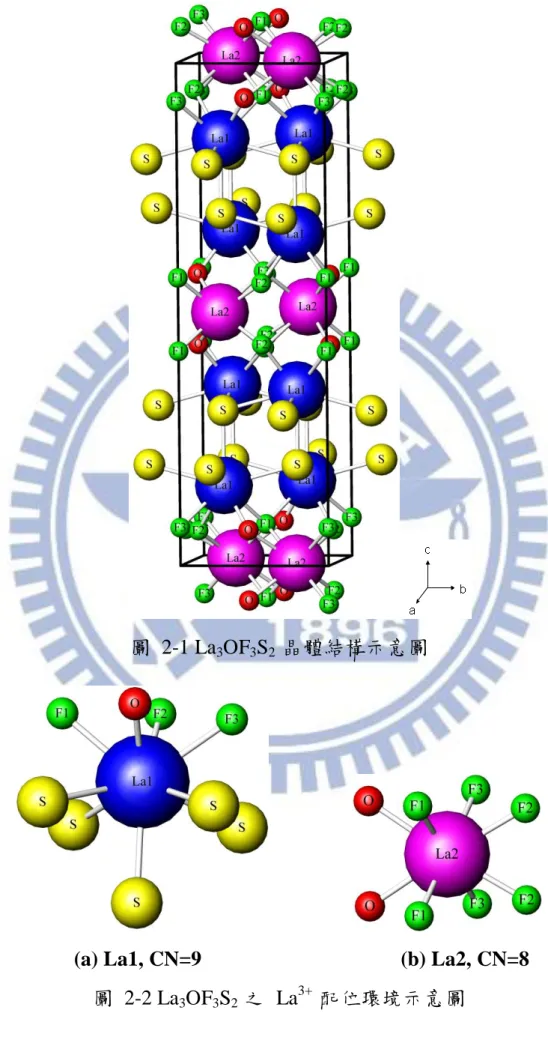
(44) 第二章 2-1. 主體晶體結構簡介. La3OF3S2 晶體結構簡介[22] Ln3OF3S2 ( Ln= La, Ce ) 與La2O1.5FS 晶體結構由Damien Pauwels. 等人於2002年所報導,此類化合物分別涉及到 α-LnSF 的 PbFCl 型 結構和 Ln2O2S 的 La2O3 型結構,陽離子的電荷可為+2價或+4價。 由於為層狀結構,層與層間由單層或雙層硫原子所區隔,稀土離子周 圍的配位環境(例如周圍的原子數量、鍵角以及鍵長)會因硫層的數目 而不同。表1為 La3OF3S2 之晶系與相關結晶學常數。. 表1. La3OF3S2 結晶學常數一覽. Crystal System Formula units Space group Lattice parameter (Å ) Lattice parameter (Å ) Lattice parameter (Å ) Lattice parameter (Å ) Lattice parameter (Å ) Lattice parameter (Å ) Voluma (Å 3 ). Orthorhombic Z=4 Pnnm 5.804 5.784 19.482 90° 90° 90° 654.02. a b c α β γ. La3OF3S2 為斜方晶系( orthorhombic ),其單位晶格如圖 2-1 所 示。在單位晶格中,陽離子 La3+ 有兩種不同的格位,La1佔據空間群 Pnnm中4g的格位為九配位,而La2佔據8h的格位為八配位,如圖 2-2 所示。 31.
(45) 圖 2-1 La3OF3S2 晶體結構示意圖. (a) La1, CN=9. (b) La2, CN=8. 圖 2-2 La3OF3S2 之 La3+ 配位環境示意圖. 32.
(46) 2-2. CeSF 晶體結構簡介. [23-26]. A. Demourgues與A. Tressaud等人於2001年報導了稀土氟硫化物 LnSF與 Ln2AF4S2 ( Ln=Sm, Ce; A=Ca, Sr )的晶體結構,由於具有鮮豔 顏色,被作為色料( pigment )使用。LnSF(有α、β兩種相位)的結構可 視為 [Ln2F2]4+ 與雙硫層 [S2]4+ 延著c軸所堆疊而成,而氟離子具有高 電負度以及高反應性等特點,可極化陽離子使得此類化合物的結構特 性和電荷密度得到一定程度的改善。表2為 CeSF 之晶系與相關結晶 學常數。. 表2 CeSF 結晶學常數一覽 Crystal System Formula units Space group Lattice parameter (Å ) Lattice parameter (Å ) Lattice parameter (Å ) Lattice parameter (Å ) Lattice parameter (Å ) Voluma (Å 3 ). Tetragonal Z=2 P4/nmm 3.9917 6.9473 90° 90° 90° 110.7. a c α β γ. CeSF為高對稱性的四方晶系結構,其單位晶格結構如圖 2-3 所 示。在此結構中,稀土原子 Ce 與硫原子填佔在空間群P4/nmm之2c 的格位,而氟原子佔據 2a 的格位,而 Ce3+ 周圍被五個硫原子與四 個氟原子所圍繞,形成九配位的結構,如圖 2-4 所示。 33.
(47) 圖 2-3 CeSF 晶體結構示意圖. CN=9 圖 2-4 CeSF 之 Ce3+ 配位環境示意圖. 34.
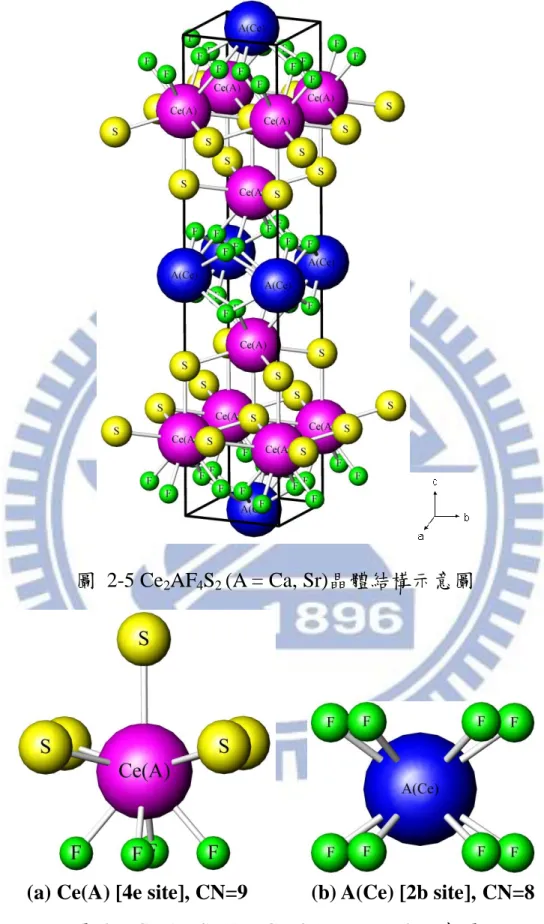
(48) 2-3. Ce2AF4S2 晶體結構簡介[19, 25-26] Ln2AF4S2 ( Ln=Sm, Ce; A=Ca, Sr ) 和LnSF屬於同一晶系,其結構. 可視為 [Ln2AF4]4+ 與雙硫層 [S2]4+ 延著c軸所堆疊而成。由於在ICSD 資料庫只有Ce2SrF4S2 的資料而沒有 Ce2CaF4S2 的相關訊息,且 Sr2+ 離子比 Ca2+ 大很多,在XRD圖譜繞射峰有明顯的偏移,因此本篇論 文便與同結構的Y2SrF4S2 標準XRD圖譜作比較,表3為 Ce2SrF4S2 與 Y2SrF4S2 之晶體相關結晶學參數之比較。 表3. Ce2SrF4S2 與Y2SrF4S2 結晶學常數之比較 Y2SrF4S2[19]. Crystal System Formula units Space group Lattice parameter (Å ) Lattice parameter (Å ) Lattice parameter (Å ) Lattice parameter (Å ) Lattice parameter (Å ) Voluma (Å 3 ). a c α β γ. Ce2SrF4S2. Tetragonal Z=2 I4/mmm 3.9345 4.0782 19.0722 19.637 90° 90° 90° 295.24 326.6. Y2SrF4S2與Ce2SrF4S2同樣為高對稱性的四方晶系結構,Ce2AF4S2 ( A = Ca, Sr) 之晶體結構如圖 2-5 所示。在此結構中,部分的陽離子 Ce3+、A2+與S2-同樣填佔在空間群I4/mmm的4e格位,其餘的陽離子則 填佔在2b格位,故化學式可寫 [Ce1.6A0.4](4e)[A0.6Ce0.4](2b)F4S2,其配 位環境如圖 2-6 所示。 35.
(49) 圖 2-5 Ce2AF4S2 (A = Ca, Sr)晶體結構示意圖. (a) Ce(A) [4e site], CN=9. (b) A(Ce) [2b site], CN=8. 圖 2-6 Ce2AF4S2 (A = Ca, Sr) 配位環境示意圖. 36.
(50) 第三章. 實驗方法. 3-1. 實驗藥品. (1). 氟化鈣 CaF2 ( Calcium Fluoride ) Strem Chemicals, Inc., 99.95%. (2). 氟化鈰 CeF3 ( Cerium(III) Fluoride ) Alfa Aesar Co., 99.9%. (3). 硫化鈰 Ce2S3 ( Cerium Sulfide ) Alfa Aesar Co., 99.9%. (4). 氟化鑭 LaF3 ( Lanthanum Fluoride ) Prochem, 99.9%. (5). 氧化鑭 La2O3 ( Lanthanum Oxide ) Sigma-Aldrich Co. LLC., 99.99%. (6). 硫化鑭 La2S3 ( Lanthanum Sulfide ) Alfa Aesar Co., 99%. (7). 氟化錳 MnF2 ( Manganese(II) Fluoride ) Strem Chemicals, Inc., 99%. (8). 氟化鈉 NaF ( Sodium Fluoride ) Sigma-Aldrich Co. LLC., 99.9%. (9). 氟化鍶 SrF2 ( Strontium Fluoride ) Sigma-Aldrich Co. LLC., 99.99%. (10) 硫粉 S ( Sulfur ) Acros Organics Co., 99.99% (11) 氟化鋱 TbF3 ( Terbium Fluoride ) Sigma-Aldrich Co. LLC., 99.99%. 37.
(51) (12) 氟化釔 YF3 ( Yttrium Fluoride ) Sigma-Aldrich Co. LLC., 99.99% (13) 氫氣 H2 ( Hydrogen ) 洽隆企業有限公司,99.9% (14) 氧氣 O2 ( Oxygen ) 洽隆企業有限公司,99.9% (15) 石英管 ( Quartz Tubes ) GM Associates, Inc. ID/9 mm, OD/11 mm, LG/4 ft 3-2. 儀器設備. (1). 手套箱( Glovebox ) 德國 MBraun 公司生產之手套箱,型號為 Labstar 50。內 部填充氣體為洽隆企業有限公司生產之高純度氮氣(99.995%)。. (2). 箱型高溫爐組( High Temperature Furnaces ) 新店市陵勝企業有限公司生產之高溫爐,爐體內加熱空間 約為7,056 cm3,配備 Eurotherm 818P 型溫控器及矽化鉬加熱 元件,最高溫度可達1,700 ℃。. (3). 紫外-可見光光譜儀( UV-Visible Spectrophotometer ) 本研究所合成固態樣品的全反射光譜量測使用日本 Hitachi 公司所製型號 U-3010 紫外-可見光光譜儀,掃描波長 範圍為 190 至 1,000 nm。 38.
(52) (4). X光繞射儀 ( X-ray diffractometer ) X光繞射儀為 Bruker AXS D8 advance 機型,其光源為銅 靶,功率為2.2 KW。X光源產生之原理為利用40 kV的操作電 壓,加速電子撞擊銅靶以激發銅原子,經單光晶體分光,使之 產生波長為 1.5405Å 的 Kα X 射線,量測時之操作電流為40 mA。掃瞄範圍之2θ值為10至80度,掃瞄模式為2θ/θ,掃瞄速率 為每分鐘5度。量測前先將分析樣品研磨成均勻細粉,固定在樣 品槽上以進行量測;必要時以矽粉做內標,以校正繞射峰之2θ 值。最後利用 DIFFRAC PLUS Evaluation軟體處理數據及圖像。. (5). 螢光光譜儀 ( Spectrofluorometer ) 使用美國 Jobin Yvon-Spex Instruments S. A. Inc.公司所製 Spex Fluorolog-3 螢 光 光 譜 儀 , 搭 備 450 W 氙 氣 燈 與 Hamamatsu Photornics 所製造 R928 型光電倍增管為偵測器, 掃描波長範圍為 200 nm至1,000 nm,並附有低溫光譜系統的杜 瓦瓶( Dewar )以及量測量子效率的積分球。. 39.
(53) (6). 色彩分析儀 (Color Analyzer) 為日本 LAIKO 所製 DT-100 Color Analyzer,搭配螢光光 譜儀即可測得輝度、對比度、閃爍以及色度。另以工業技術研 究院量測技術研究中心葉迎春博士所撰寫之色度座標分析軟 體,將樣品量測所得之放光光譜圖中強度與波長之關係,利用 該軟體計算出各螢光體的色度座標(x, y)值。. 40.
(54) 3-3. 實驗步驟 本研究所有螢光粉皆利用固態燒結法製備,由於所使用之部分反. 應物(例如金屬硫化物)對空氣中的氧氣與水氣極具敏感性,為將氧氣 與水氣的影響降至最低,因此所使用之藥品皆放置在手套箱中保存, 以隔絕氧氣與水氣而避免被氧化或潮解。本實驗需在手套箱內完成藥 品的秤量與研磨,之後封入與玻璃真空裝置搭配之石英玻璃管中,才 離開手套箱。接著利用真空系統抽走石英玻璃管中的大部分氣體,使 管內壓力達到 10-3 torr 左右,再用氫氧焰於動態真空下完成封管。 最後將石英玻璃管送入高溫爐中進行高溫燒結以得到產物,此流程稱 為石英玻璃管封管法。 藉由 X-ray 繞射儀檢測晶相後,再利用紫外-可見光譜儀、螢 光光譜儀與色彩分析儀等,進行螢光體發光光譜與特性之研究。以下 為樣品固態合成之流程圖:. 41.
(55) 3-3-1. La3OF3S2:Ce3+ ( or Mn2+, Na+ )螢光材料之合成與特性鑑定. 於手套箱中,依化學計量秤取所需反應物進行以下反應: (1) 2 La2S3 + (3-9x)LaF3 + La2O3 + 9x CeF3 → 3(La1-xCex)3OF3S2 (2) 2 La2S3 + (3-9x)LaF3 + La2O3 + 9x (MnF2, NaF) → 3(La1-2xMnxNax)3OF3S2 以上反應物置入瑪瑙研缽均勻混合後並經手研磨 10 分鐘,然後 置於石英玻璃管中。. 利用真空系統將石英玻璃管內壓力抽至 10-3 torr 左右,接著將石 英玻璃管在動態真空下以氫氧焰密封,然後置於高溫爐內於 900℃燒結 10 小時,待自然冷卻至室溫後取出。. 將燒結後所得的粉末經手研磨 10 分鐘後,對其進行 X-ray 繞射 晶相鑑定、螢光光譜與 C.I.E. 色度座標、漫反射光譜、熱消光螢 光光譜與量子效率等測量。. 42.
(56) 3-3-2. Ce1-xLnxSF ( Ln = Tb3+, Mn2+, Y3+, Gd3+ )螢光材料之合成與特. 性鑑定. 於手套箱中,依化學計量秤取所需反應物進行以下反應: Ce2S3 + (1-3x)CeF3 + 3x GdF3 ( or YF3 , TbF3 , MnF2 ) → 3(Ce1-xLnx)SF (Ln = Gd3+, Y3+, Tb3+, Mn2+) 以上反應物置入瑪瑙研缽均勻混合後並經手研磨 10 分鐘,然後 置於石英玻璃管中。. 利用真空系統將石英玻璃管內壓力抽至 10-3 torr 左右,接著將石 英玻璃管在動態真空下以氫氧焰密封,然後置於高溫爐內於 950℃燒結 6 小時,待自然冷卻至室溫後取出。. 將燒結後所得的粉末經手研磨 10 分鐘後,對其進行 X-ray 繞射 晶相鑑定、螢光光譜與 C.I.E. 色度座標、漫反射光譜、熱消光螢 光光譜與量子效率等測量。. 43.
(57) (Ce1-x Tb x)2CaF4S2 與Ce2(Ca1-xMnx)F4S2 螢光材料之合成與特. 3-3-3 性鑑定. 於手套箱中,依化學計量秤取所需反應物進行以下反應: 2 3. 2 - 6x CeF3 + CaF2 + 2x TbF3 → (Ce1-xTbx)2CaF4S2 3. 2 3. 2 - 6x CeF3 + CaF2 + 2x MnF2 → Ce2(Ca1-xMnx)F4S2 ) 3. (1) Ce2S3 + (2) Ce2S3 +. 以上反應物置入瑪瑙研缽均勻混合後並經手研磨 10 分鐘,然後 置於石英玻璃管中。. 利用真空系統將石英玻璃管內壓力抽至 10-3 torr 左右,接著將石 英玻璃管在動態真空下以氫氧焰密封,然後置於高溫爐內於 1000℃燒結 8 小時,待自然冷卻至室溫後取出。. 將燒結後所得的粉末經手研磨 10 分鐘後,對其進行 X-ray 繞射 晶相鑑定、螢光光譜與 C.I.E. 色度座標、漫反射光譜、熱消光螢 光光譜與量子效率等測量。. 44.
(58) 3-3-4. (Ce1-xYx)2SrF4S2 螢光材料之合成與特性鑑定. 於手套箱中,依化學計量秤取所需反應物進行以下反應: 2 - 6x 2 Ce2S3 + CeF3 + CaF2 + 2x YF3 + 10% excess S 3 3. →(Ce1-xYx)2SrF4S2 + excess S 以上反應物置入瑪瑙研缽均勻混合後並經手研磨 10 分鐘,然後 置於石英玻璃管中。. 利用真空系統將石英玻璃管內壓力抽至 10-3 torr 左右,接著將石 英玻璃管在動態真空下以氫氧焰密封,然後置於高溫爐內於 1000℃燒結 10 小時,待自然冷卻至室溫後取出。. 將燒結後所得的粉末經手研磨 10 分鐘後,對其進行 X-ray 繞射 晶相鑑定、螢光光譜與 C.I.E. 色度座標、漫反射光譜、熱消光螢 光光譜與量子效率等測量。. 45.
(59) 第四章. 結果與討論. 螢光體合成與X光繞射圖譜之分析. 4-1. 本節中依序討論本論文所合成的La3OF3S2:Ce3+ ( or Mn2+ )、 CeSF:Tb3+ ( or Mn2+ , Y3+, Gd3+ )、 Ce2CaF4S2:Tb3+ ( or Mn2+ )與 Ce2SrF4S2:Y3+ 四系列氟氧硫化物及氟硫化物螢光材料,在不同的製程 條件下(如:燒結溫度、時間、活化劑摻雜比例等),所得產物之X光 繞射圖譜晶相分析與晶格參數之變化。 4-1-1. La3OF3S2 X光繞射圖譜之研究. 本研究依化學計量秤取La2S3、LaF3 與 La2O3 為起始物,於 700 ~ 900℃溫度下合成La3OF3S2。圖 4-1 為不同溫度所合成樣品測得X 光粉末繞射圖譜之比較,可發現在低溫時( 700~800℃)仍有部份氟化 物未反應完全,當合成溫度提升至900℃可促進純La3OF3S2 之生成, 然而在此溫度下若將燒結時間增加至10小時,則可使氟化物的雜相強 度降低而得純相。 綜合以上數據,最佳反應條件為La2S3、LaF3 與 La2O3依照化學 計量比例秤取後,於900℃下燒結10小時即可合成La3OF3S2 。圖 4-2 為 Miller Index 標定La3OF3S2 之X光粉末繞射圖譜與 ICSD-95692 所載圖譜之比較。. 46.
(60) 圖 4-1 不同燒結溫度所製備La3OF3S2 之X光繞射圖譜之比較. 圖 4-2 Miller Index 標定La3OF3S2 X光繞射圖譜 47.
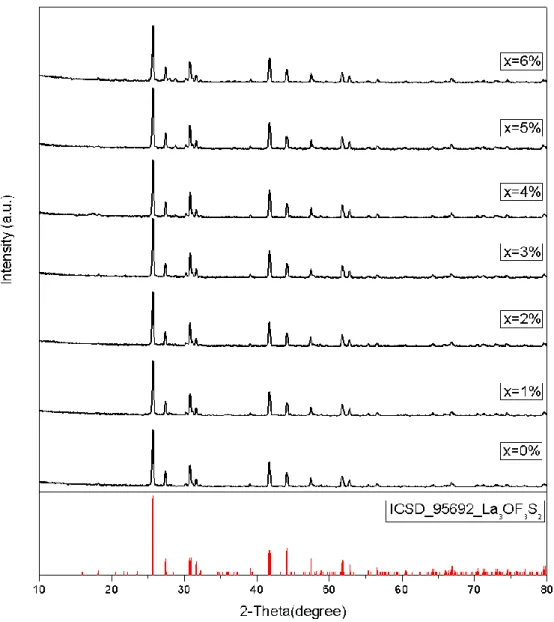
(61) 4-1-2. (La1-xCex)3OF3S2 X光繞射圖譜與晶相鑑定之研究. 如圖 4-3 所示,當主體摻雜活化劑後,由於La3+(1.06Å )只略大 於Ce3+(1.034Å ),即使摻雜的濃度高達6%,X-ray繞射圖譜並未呈現 明顯的2θ角偏移,故整體結構不受影響。. 圖 4-3 含不同Ce3+濃度 (La1-xCex)3OF3S2 X光繞射圖譜之比較. 48.
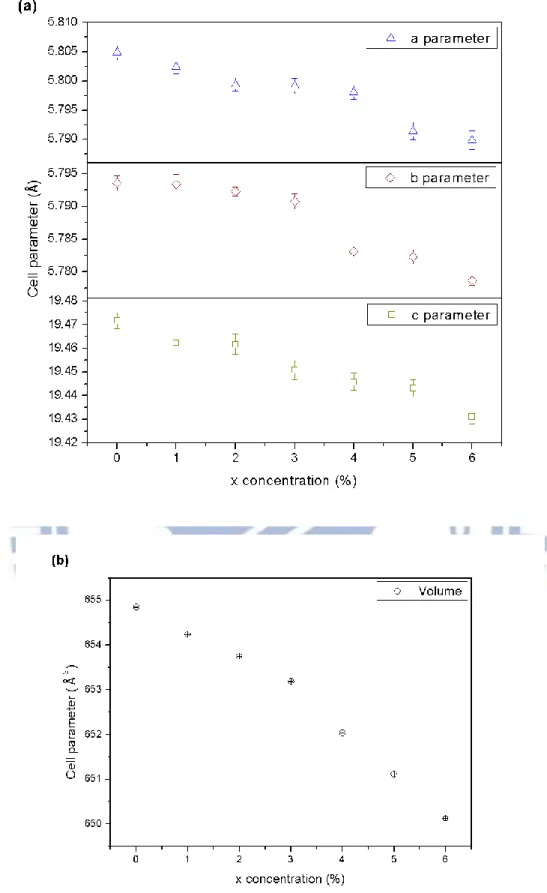
(62) 雖然在XRD圖譜中並未發現明顯的角度偏移,在此可藉由晶格常 數精算軟體 Cell refinement 來精算晶格常數與晶格體積變化,以確 認Ce3+ 是否進入晶體格位中並形成良好固溶液。 考慮陽離子配位數與有效半徑,於主體晶格中所摻入Ce3+(1.034Å ) 較原本陽離子La3+(1.06Å )之離子半徑為小,兩者半徑之差異造成晶格 的大小改變,晶格常數數值亦隨之改變。隨著Ce3+ 摻雜濃度的提升, 晶格常數與體積呈現逐漸縮小的趨勢,證實Ce3+ 有進入晶格中。如圖 4-4 所示,顯示其可形成良好的固溶液。. 49.
(63) 圖 4-4 (a) (La1-xCex)3OF3S2 晶格常數與Ce3+ 濃度之關係 (b) (La1-xCex)3OF3S2 單位晶格體積與Ce3+ 濃度之關係. 50.
(64) 4-1-3. (La1-xMnx)3OF3S2 X光繞射圖譜與晶相鑑定之研究. 如圖 4-5 所示,由於 La3OF3S2 中含有氧離子,因此當主體摻雜 較高濃度的過渡金屬離子Mn2+與電荷補償劑(NaF)後,容易生成LaOF 而造成主體的雜相。. 圖 4-5 不同濃度Mn2+摻雜(La1-xMnxNax)3OF3S2之X光繞射圖譜比較 當 La3OF3S2 摻雜Mn2+後,所摻入的Mn2+(0.67Å )較原本陽離子 La3+(1.06Å )之離子半徑為小,兩者的離子半徑差異過大,易造成晶格 中有殘留應力(residual)的產生造成不易取代。如圖 4-6 所示,隨著 Mn2+ 摻雜濃度的提升,晶格常數與體積有逐漸縮小的趨勢,而推測 Mn2+ 應進入晶格中。 51.
(65) 圖 4-6 (a) (La1-xMnxNax)3OF3S2 晶格常數與Mn2+ 濃度之關係 (b) (La1-xMnxNax)3OF3S2 單位晶格體積與Mn2+ 濃度之關係 52.
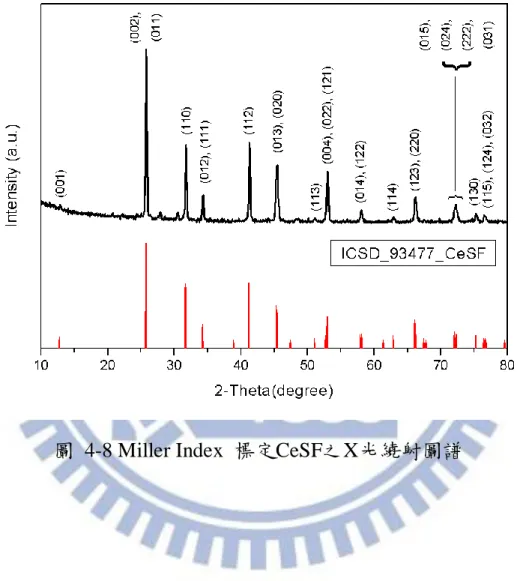
(66) 4-1-4. CeSF X光繞射圖譜與晶相鑑定之研究. 本研究依化學計量秤取Ce2S3與CeF3為起始物,於 800 ~ 1000℃ 的溫度下合成CeSF。圖 4-7 為所測得不同的溫度下產物X光粉末繞 射圖譜之比較,可看出當合成溫度為950℃以上可得較純之CeSF。而 在950℃下燒結6小時與8小時所得產物一樣,在此研究中便考慮以6 小時為燒結時間。. 圖 4-7 不同燒結溫度所製備CeSF之X光繞射圖譜之比較. 53.
(67) 綜合以上數據,合成CeSF最佳反應條件為起始物依照化學計量 於950℃下燒結6小時即可獲得純相。圖 4-8為此反應條件下以 Miller Index 標定之X光粉末繞射圖譜與 ICSD-93477 所載圖譜之比較。. 圖 4-8 Miller Index 標定CeSF之X光繞射圖譜. 54.
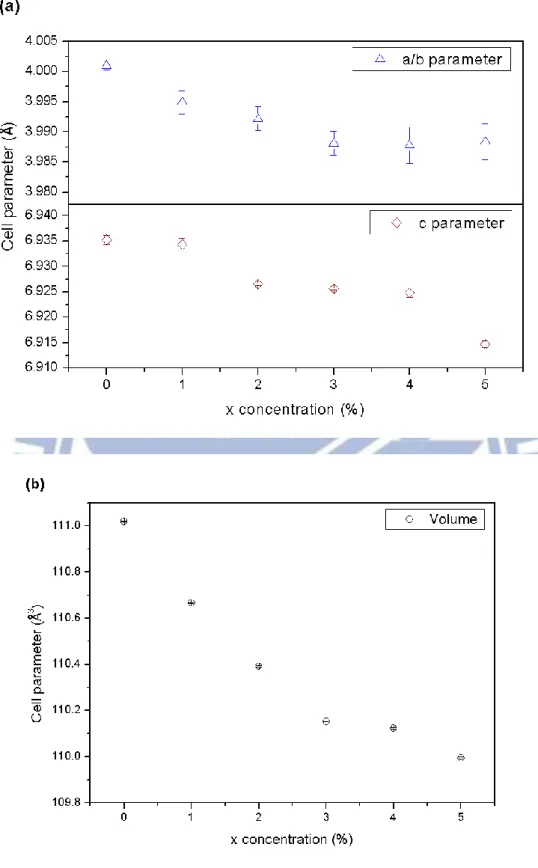
(68) 4-1-5. (Ce1-xGdx)SF 之X光繞射圖譜之研究. 秤取計量Ce2S3、CeF3與GdF3起始物於950℃下燒結6小時進行合 成。其產物XRD圖譜如圖 4-9 所示,當主體摻雜活化劑後,由於 Ce3+(1.034Å )略大於Gd3+(0.938Å ),即使摻雜的濃度高達5%,X-ray繞 射圖譜並未呈現明顯的2θ角偏移,故不影響整體結構。. 圖 4-9 含不同Gd3+濃度 (Ce1-xGdx)SF 之X光繞射圖譜比較 在(Ce1-xGdx)SF螢光材料中,由於所摻入的Gd3+(0.938Å )離子較原 本陽離子Ce3+(1.034Å )之離子半徑為小,造成晶格的縮小,晶格常數 數值亦隨之改變。如圖 4-10 所示,隨著Gd3+摻雜濃度的提升,晶格 常數與單位晶格體積有逐漸縮小的趨勢,推測Gd3+有進入晶格中。 55.
(69) 圖 4-10 (a) (Ce1-xGdx)SF晶格常數與Gd3+ 濃度之關係 (b) (Ce1-xGdx)SF單位晶格體積與Gd3+ 濃度之關係. 56.
(70) 4-1-6. (Ce1-xTbx)SF X光繞射圖譜之研究 秤 取 計 量 之 CeF3 、 Ce2S3 與 TbF3 後 , 於 950 ℃ 燒 結 6 小 時 合 成. (Ce1-xTbx)SF。圖 4-11 顯示,由於Ce3+離子半徑略大於Tb3+ (1.034Å > 0.923Å ),即使摻雜的濃度高達10%,X光繞射圖譜並未呈現明顯的2θ 角偏移。而摻雜濃度高達7%後,逐漸有 TbSF 的雜相出現,直到摻 雜濃度9%以上有明顯的 TbSF 的雜相,顯示 CeSF 摻雜 Tb3+ 的相 容性可達8%。. 圖 4-11 含不同Tb3+濃度 (Ce1-xTbx)SF X光繞射圖譜之比較 57.
(71) CeSF與TbSF皆為四方晶系,空間群也同為P4/nmm,唯其X光繞 射圖譜不同,如下圖 4-12 所示。當CeSF摻雜Tb3+高達9%以上時, XRD圖譜逐漸有TbSF雜相出現。另外,在2θ值≒27°處有來自於sample holder的繞射峰。. 圖 4-12 最高摻雜濃度Ce0.9Tb0.1SF與雜相來源之X光繞射圖譜比較 (Ce1-xTbx)SF 摻 入 的 Tb3+ 離 子 半 徑 較 Ce3+ 離 子 小 ( 0.923Å < 1.034Å ),此造成單位晶格體積縮小且導致晶格常數變小,如圖 4-13 所示。當摻雜濃度高於8%即達飽和,且有TbSF的雜相出現。. 58.
(72) 圖 4-13 (a) (Ce1-xTbx)SF晶格常數與Tb3+ 濃度之關係 (b) (Ce1-xTbx)SF單位晶格體積與Tb3+ 濃度之關係 59.
(73) 4-1-7. (Ce1-xMnx)SF1-x X光繞射圖譜與晶相鑑定之研究. 當主體摻入活化劑Mn2+後,由於Mn2+與Ce3+為不等價取代,而 Mn2+(0.67Å )明顯小於Ce3+(1.034Å ),圖 4-14 所示為進行微量取代(≦ 1%)的狀況下,其X光繞射圖譜並未呈現雜相與明顯的2θ角偏移,顯 示主體微量的摻雜Mn2+,依然可形成良好的固溶液,且整體結構不受 影響。. 圖 4-14 含不同Mn2+濃度 (Ce1-xMnx)SF1-x X光繞射圖譜比較 在(Ce1-xMnx)SF1-x 螢光體中,晶格體積的縮小源自於所摻入的 Mn2+ (0.67Å )離子半徑較原本陽離子Ce3+(1.034Å )之為小,且晶格常數 數值亦改變。圖 4-15 顯示隨著Mn2+摻雜濃度的提升,晶格常數與單 位晶格體積有逐漸縮小的趨勢,推論Mn2+有進入格位中。. 60.
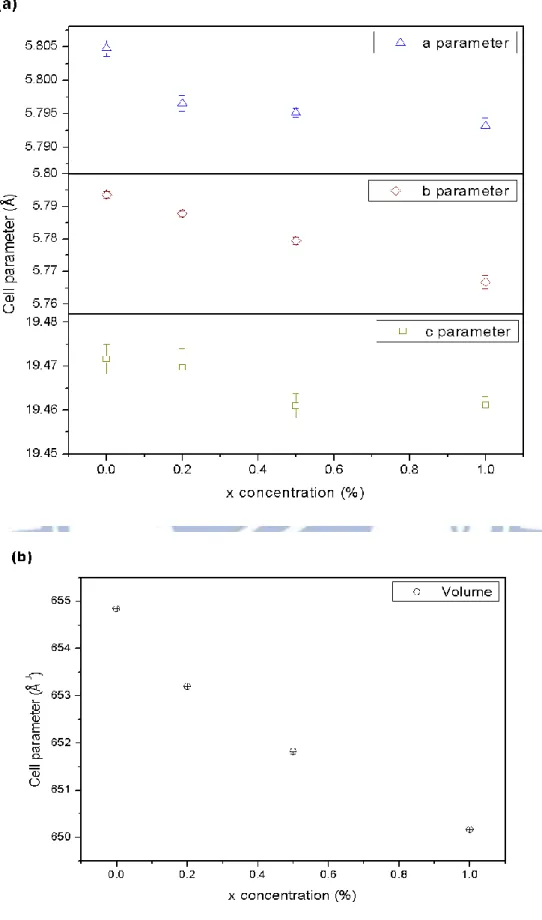
(74) 圖 4-15 (a) (Ce1-xMnx)SF1-x晶格常數與Mn2+ 濃度之關係 (b) (Ce1-xMnx)SF1-x單位晶格體積與Mn2+ 濃度之關係. 61.
(75) 4-1-8. (Ce1-xYx)SF X光繞射圖譜與晶相鑑定之研究. 依計量秤取CeF3、Ce2S3與YF3後,以950℃燒結6小時合成。主體 摻雜離子半徑相對較小之Y3+(0.90Å )後,當(Ce1-xYx)SF中Y3+摻雜的濃 度高達15%時,X-ray繞射圖譜出現雜相,顯示其相容性最多只能摻 雜至10%。. 圖 4-16 含不同Y3+濃度 (Ce1-xYx)SF X光繞射圖譜之比較 由於(Ce1-xYx)SF所摻入的 Y3+ 離子半徑較 Ce3+ 離子( 0.90Å < 1.034Å )小,造成晶格常數數值改變。如圖 4-17 所示,當Y3+摻雜的 濃度到6%以上,可能已生成雜相而導致晶格常數出現不規律的變化。 62.
(76) 圖 4-17 (a) (Ce1-xYx)SF晶格常數與Y3+ 濃度之關係 (b) (Ce1-xYx)SF晶格體積與Y3+ 濃度之關係. 63.
數據
![圖 1-1 螢光體中敏化劑與活化劑能量轉移示意圖 [3]](https://thumb-ap.123doks.com/thumbv2/9libinfo/8512882.185961/19.892.139.764.102.916/圖11螢光體中敏化劑與活化劑能量轉移示意圖3.webp)
![圖 1-2 Stokes Shift 示意圖 [6]](https://thumb-ap.123doks.com/thumbv2/9libinfo/8512882.185961/23.892.136.751.358.915/圖12StokesShift示意圖6.webp)
![圖 1-6 自由態三價鑭系離子的 4f n 能階示意圖 [8]](https://thumb-ap.123doks.com/thumbv2/9libinfo/8512882.185961/26.892.191.723.116.885/圖16自由態三價鑭系離子的4fn能階示意圖8.webp)
相關文件
展生物医学、生物育种等产业。新材料领域重点发展新型电子
而在後續甲烷化反應試驗方面,以前段經厭氧醱酵產氫後之出流水為進流基 質。在厭氧光合產氫微生物方面,以光合作用產氫細菌中產氫能力最好的菌株 Rhodopseudomonas palustris
其他光學儀器及設備製造業 從事 2771 細類以外光學儀器及設 備製造之行業,如望遠鏡、顯微
The prepared nanostructured titania were applied for the photoanodes of dye-sensitized solar cell.. The photoanodes were prepared by the doctor blade technique and the area
The research proposes a data oriented approach for choosing the type of clustering algorithms and a new cluster validity index for choosing their input parameters.. The
In this paper, we build a new class of neural networks based on the smoothing method for NCP introduced by Haddou and Maheux [18] using some family F of smoothing functions.
dimensional nanomaterials for photodetectors with ultrahigh gain and wide spectral response. II. Photon down conversion and light trapping in hybrid ZnS nanopartcles/Si
4634 potassium hydrogen fluoride 氟化氫鉀,氫氟化鉀. 4635 potassium