固定化電子媒介體結合零價金屬去除水中含氯有機物質之應用
146
0
0
全文
(2) 致謝 在研究所兩年的過程中,我學習了許多新知識,感謝土環系老師 們的教導,讓我對於環工領域有更多的了解。其中特別感謝連興隆 老 師,對於課業和研究上都能耐心的教導,也幫助我許多。另外也感謝 袁菁 口試委員和孫元邦 口試委員在論文方面給予寶貴的意見。 還有感謝書丞學長和岱霖學姐在研究上的帶領,以及學弟方大哥、昌 翰和順景對我的協助,除此還要感謝齡仟、世鴻、嘉仁、惟翔、文躍、 子彬、坤楠和明君能給予支持與協助。 除此之外還要感謝許多親朋好友給予我的支持與鼓勵,最終感謝我的 父母親,讓我有這個就讀機會,完成碩士學位。.
(3) 目錄 圖目錄 .........................................................................................................VI 表目錄 .......................................................................................................... X 摘要 .............................................................................................................XI ABSTRACT ............................................................................................. XII 第一章 前言 ................................................................................................. 1 1.1 研究緣起 ............................................................................................ 1 1.2 研究目的 ............................................................................................ 4 第二章 文獻回顧 ......................................................................................... 5 2.1 含氯有機物 ........................................................................................ 5 2.1.1 四氯化碳 ....................................................................................... 5 2.1.2 二氯甲烷 ...................................................................................... 7 2.2 廢水與地下水中污染物的去除 ........................................................ 9 2.2.1 廢水中含氯有機物之去除 ........................................................... 9 2.2.2 地下水的污染與整治 ................................................................ 12 2.2.2.1 透水性反應牆 ......................................................................... 14 2.3.零價金屬的應用 ............................................................................... 16 2.3.1 零價鐵 ......................................................................................... 16 2.3.2 零價鋁 ........................................................................................ 18 2.3.3 零價銅 ........................................................................................ 18. I.
(4) 2.3.4 其他零價金屬的應用 ................................................................ 19 2.3.4.1 零價鎳 ..................................................................................... 19 2.3.4.2 零價鈀 ..................................................................................... 20 2.4 複合金屬的運用 .............................................................................. 21 2.4.1 Fe/Al 複合金屬 ........................................................................... 21 2.4.2 Cu/Fe 複合金屬 ......................................................................... 24 2.4.3 Cu/Al 複合金屬 .......................................................................... 26 2.4.4 鈀鐵複合金屬 ............................................................................ 27 2.4.5 複合金屬之比較 ......................................................................... 28 2.5 電子媒介體 ...................................................................................... 29 2.5.1 維生素 B12 基本特性 ................................................................. 29 2.5.2 維生素 B12 之運用 ..................................................................... 31 2.5.3 TPPS(tetraphenylporphinesulfonate) .......................................... 33 2.5.4 磷鎢酸鈉 .................................................................................... 35 2.6 電子媒介體固定方式 ....................................................................... 37 第三章 材料與研究方法 ........................................................................... 41 3.1 研究架構 .......................................................................................... 41 3.2 實驗材料 .......................................................................................... 43 3.3 儲備溶液配製 .................................................................................. 44 3.3.1 四氯化碳儲備溶液 .................................................................... 44 3.3.2 二氯甲烷儲備溶液 ..................................................................... 44. II.
(5) 3.3.3 維生素 B12 儲備溶液 ................................................................. 44 3.3.4 TPPS 儲備溶液 ........................................................................... 44 3.4 複合金屬合成技術 ........................................................................... 45 3.4.1 Fe/Al 複合金屬 .......................................................................... 45 3.4.2 Cu/Al 複合金屬 .......................................................................... 45 3.4.3 Cu/Fe/Al 複合金屬 ..................................................................... 45 3.5 電子媒介體固定方法 ...................................................................... 46 3.5.1 直接與矽膠混合 (F) .................................................................. 46 3.5.2 合成過程升溫 (FH) ................................................................... 47 3.5.3 複合金屬合成過程中添加 (FI)................................................. 49 3.5.4 B12 結合活性碳 (FAC) ............................................................... 49 3.6 材料表面特性分析 .......................................................................... 52 3.6.1 掃描式電子顯微鏡 (SEM) ........................................................ 52 3.6.2 X 光粉末繞射儀 (XRD) ............................................................ 52 3.6.3 比表面積分析儀 (BET)............................................................ 52 3.6.4 傅利葉轉換紅外線光譜儀 (FTIR) .......................................... 52 3.7 污染物分析方法 .............................................................................. 53 3.7.1 氣相層析儀分析技術 ................................................................ 53 3.7.2 金屬離子之測量 ........................................................................ 53 3.8 批次實驗 .......................................................................................... 54 3.9 管柱實驗 .......................................................................................... 55 3.9.1 四氯化碳 .................................................................................... 56. III.
(6) 3.9.2 二氯甲烷 .................................................................................... 57 3.10 反應動力學分析 ............................................................................ 58 3.11 實驗之品保品管 ............................................................................. 59 3.11.1 精密度 ...................................................................................... 59 3.11.2 準確度 ...................................................................................... 59 3.11.3 檢量線 ...................................................................................... 59 第四章 結果與討論 ................................................................................... 60 4.1 複合金屬材料特性分析 ................................................................... 60 4.1.1 金屬的組成分析 ......................................................................... 60 4.1.2 電子顯微鏡 (SEM) 分析 ......................................................... 62 4.1.3 X 光粉末繞射儀 (XRD) 分析 .................................................. 64 4.1.4 比表面積分析儀 (BET) 分析.................................................. 66 4.2 批次實驗 .......................................................................................... 68 4.2.1 Fe/Al 複合金屬 ........................................................................... 69 4.2.2 Cu/Fe/Al 複合金屬 ..................................................................... 71 4.2.3 Fe/Al 和 Cu/Fe/Al 之比較 .......................................................... 76 4.3 管柱實驗 ........................................................................................... 78 4.3.1 去除四氯化碳之管柱實驗 ......................................................... 79 4.3.2 去除二氯甲烷之管柱實驗 ......................................................... 82 4.4 電子媒介體與複合金屬之應用 ....................................................... 84 4.4.1 直接與矽膠混合(F) .................................................................... 87. IV.
(7) 4.4.2 合成過程升溫(FH) ..................................................................... 92 4.4.3 複合金屬合成過程中添加 (FI)................................................. 99 4.4.4 B12 結合活性碳 (FAC) .......................................................... 101 4.4.4.1 四氯化碳的重複添加 ........................................................... 103 4.4.4.2 二氯甲烷的重複添加 ........................................................... 104 4.5 固定化電子媒介體總比較 ............................................................. 108 第五章結論 ............................................................................................... 109 第六章 建議 ............................................................................................. 111 參考文獻 ................................................................................................... 112 附錄一 實驗數據 ..................................................................................... 123 附錄二 口試委員意見回覆 ..................................................................... 129. V.
(8) 圖目錄 圖 1-1. 地下水整治技術與人體醫療間之關連性 ..................................... 2 圖 2-1. DNAPL 物質於地下水中分佈圖 .................................................. 13 圖 2-2. 透水性反應牆示意圖 ................................................................... 15 圖 2-3. 鐵鋁複合金屬示意圖 ................................................................... 21 圖 2-4. 四氯化碳經由 Fe/Al 複合金屬降解處理 .................................... 22 圖 2-5. 鐵鋁的鐵含量對四氯化碳脫氯之有效性 ................................... 23 圖 2-6. (a) 鐵鋁複合金屬 SEM 圖,(b) (c) 分別為鐵鋁元素 mapping 圖 .............................................................................................................. 24 圖 2-7. Cu/Fe 複合金屬去除 1, 2, 4-trichlorobenzene .............................. 25 圖 2-8. 銅鐵複合金屬還原 NO3−-N 之概念模型..................................... 26 圖 2-9. 維生素 B12 之結構......................................................................... 30 圖 2-10. 維生素 B12 於 1 g/L 硼氫化鈉還原系統中隨時間之變化 ....... 31 圖 2-11. 維生素 B12 參與反應示意圖,Red 表還原劑,Ox 表氧化劑 .............................................................................................................. 32 圖 2-13 溶質在活性碳表面擴散吸附路徑 .............................................. 39 圖 3-1. 研究架構圖.................................................................................... 42 圖 3-2. 本研究固定電子媒介體於複合材料表面之方法 ....................... 51 圖 3-2. 空白管柱實驗示意圖 ................................................................... 55 圖 3-3. Cu/Fe/Al 管柱實驗......................................................................... 56 圖 4-1. 不同銅含量之 Cu/Fe/Al 實際金屬含量配比 .............................. 61 圖 4-2. 鐵鋁複合金屬(0.5% Cu)之 SEM 分析 (a)SEM 分析 (b)EDX VI.
(9) (c)Fe 的 Mapping 圖 (d)Al 的 Mapping 圖 ........................................ 63 圖 4-3. 鐵鋁複合金屬(1% Cu)之 SEM 分析 (a)SEM 分析 (b)EDX (c)Fe 的 Mapping 圖 (d)Al 的 Mapping 圖 ................................................. 63 圖 4-4. 鐵鋁複合金屬(10% Cu)之 SEM 分析 (a)SEM 分析 (b)EDX (c)Cu 的 Mapping 圖 (d)Fe 的 Mapping 圖 (e)Al 的 Mapping 圖 ... 64 圖 4-5. 不同比例銅鐵鋁之 XRD 分析圖譜 ............................................. 65 圖 4-6. 銅之 XRD 標準圖譜 ..................................................................... 65 圖 4-7. 鐵之 XRD 標準圖譜 ..................................................................... 66 圖 4-8. 鋁之 XRD 標準圖譜 ..................................................................... 66 圖 4-9. 四氯化碳還原脫氯示意圖 ........................................................... 68 圖 4-10. 四氯化碳降解之中間代謝產物 ................................................. 69 圖 4-11. Fe/Al 在不同 pH 對去除四氯化碳之影響 ................................. 70 圖 4-12. 不同 pH 值對於 Fe/Al 去除四氯化碳之反應速率 ................... 71 圖 4-13. 銅鐵鋁的銅含量對四氯化碳脫氯之情形 ................................. 73 圖 4-14. 不同銅含量之銅鐵鋁複合金屬 (a) 0.5% (b) 1% (C) 10% ....... 73 圖 4-15. 不同劑量的 Cu/Fe/Al 降解四氯化碳 ........................................ 74 圖 4-16. Cu/Fe/Al 在不同 pH 對去除四氯化碳之影響 ........................... 75 圖 4-17. 不同 pH 值對於 Cu/Fe/Al 去除四氯化碳之反應速率 ............. 76 圖 4-18. Fe/Al 和 Cu/Fe/Al 在不同 pH 值降解四氯化碳之比較 ............ 77 圖 4-19. 四氯化碳通過石英砂填充管柱之貫穿曲線 ............................. 78 圖 4-20. Cu/Fe/Al 之材料管柱對四氯化碳的去除曲線 .......................... 80 圖 4-21. 管柱實驗採樣後之樣品 ............................................................. 81. VII.
(10) 圖 4-22. 管柱實驗後之金屬濃度分析 ..................................................... 81 圖 4-23. Cu/Fe/Al 之材料管柱對二氯甲烷的去除曲線 .......................... 83 圖 4-24. 維生素 B12 於 60 g/L 銅鋁複合金屬(20%)還原系統中隨時間之 變化 ...................................................................................................... 84 圖 4-25. B12 溶液與 Cu/Al 結合的實際情況 ............................................. 85 圖 4-26. 未固定化之 B12 和 TPPS 分別結合 Cu/Al 去除二氯甲烷 ....... 86 圖 4-27. Cu/Fe/Al 與 TPPS- Cu/Fe/Al 降解二氯甲烷之比較 .................. 86 圖 4-28.經由 F1 方式合成的 B12-Cu/Fe/Al ............................................... 88 圖 4-29. Fe/Al、Cu/Fe/Al 和經由 F1 固定方式的 B12 去除四氯化碳之比 較 .......................................................................................................... 88 圖 4-30. B12 經 F2 方式固定後之粉末 ...................................................... 89 圖 4-31. Cu/Fe/Al 與經 F2 方式固定後之材料去除四氯化碳之比較 .... 90 圖 4-32.經 F4 固定化之 TPPS ................................................................... 91 圖 4-33. Cu/Fe/Al 與經 F4 方式固定之材料降解四氯化碳之比較 ........ 92 圖 4-34. 經 FH2 方式固定後之 B12-Cu/Al ............................................... 93 圖 4-35. Cu /Al 與經 FH2 方式固定後之 B12-Cu/Al 去除四氯化碳之比較 .............................................................................................................. 93 圖 4-36. 經 FH3 固定過程中的微生素 B12 .............................................. 94 圖 4-37. 經 FH3 方法固定後之 B12-Cu/Al ............................................... 95 圖 4-38. Cu/Al 與經 FH3 固定的 B12-Cu/Al 去除四氯化碳之比較 ........ 95 圖 4-39. 經 FH5 方式固定之批次實驗過程 (左圖為 Cu/Al,右圖為 B12-Cu/Al) ............................................................................................ 96. VIII.
(11) 圖 4-40. Cu /Al 與經 FH5 方式固定之 B12-Cu/Al 去除四氯化碳比較圖 .............................................................................................................. 97 圖 4-41. 經過 FH5 固定方式之 FTIR 分析圖.......................................... 98 圖 4-42. Cu/Al 與經 FH6 固定之材料去除四氯化碳之比較 .................. 99 圖 4-43. 經 FI2 方法固定的材料降解四氯化碳之批次反應 (左圖為 Cu/Al,右圖為 B12-Cu/Al) ............................................................... 100 圖 4-44. Cu/Al 與經 FI2 方法固定的 B12-Cu/Al 降解四氯化碳之比較 100 圖 4-45. 經 FAC1 固定之 FTIR 分析圖 ................................................. 101 圖 4-46. PAC 與經 FAC1 固定方式之材料去除二氯甲烷比較圖 ........ 102 圖 4-47. Cu/Al 與經 FAC1 固定方式之材料降解二氯甲烷之產物分析 ............................................................................................................ 102 圖 4-48. PAC-Cu/Al 與經 FAC1 固定之材料降解四氯化碳之產物分析 ............................................................................................................ 103 圖 4-49. 利用二氯甲烷確認系統的再利用性 ....................................... 104 圖 4-50.PAC 結合 B12 之系統測定 .......................................................... 105 圖 4-51.甲烷產量分析圖.......................................................................... 105 圖 4-52.不同濃度 B12 去除二氯甲烷之比較 .......................................... 106 圖 4-53. 不同濃度 B12 去除二氯甲烷後之甲烷產生量 ........................ 107. IX.
(12) 表目錄 表 2-1 氧化劑之相對氧化力 .................................................................... 10 表 2-2. 地下水中污染物之管制標準 ....................................................... 13 表 2-3.奈米零價鐵去除含氯有機物比較表 ............................................. 17 表 3-1. 本研究批次實驗的操作條件規劃 ............................................... 54 表 4-1. 銅鐵鋁複合金屬之比表面積 (單位:m2/g) ............................... 67 表 4-2. Fe/Al 去除四氯化碳初始和最終 pH 值 ....................................... 70 表 4-3. 去除四氯化碳及二氯甲烷之甲烷濃度 (mg/L) ........................ 104 表 4-4. 固定化電子媒介體結合複合金屬去除污染物總表 ................. 108. X.
(13) 固定化電子媒介體結合零價金屬 去除水中含氯有機物質之應用 指導教授:連興隆 博士 國立高雄大學土木與環境工程學系. 學生:蘇蓮香 國立高雄大學土木與環境工程學系. 摘要 本研究利用四大類共計 13 種方法固定電子媒介體(維生素 B12、TPPS 和磷鎢 酸鈉),結合複合金屬(Cu/Al、Fe/Al 和 Cu/Fe/Al)在不同條件下去除污染物(四氯化 碳和二氯甲烷),經由結果探討固定化的有效性以及其優缺點。結果顯示當探討複 合金屬於批次實驗在不同條件下去除四氯化碳,Fe/Al 在 pH=4 的效果最佳,4 小 時之內,去除率達 76%,而 Cu/Fe/Al 在 pH=10 的效果最佳,0.5 小時之內,去除 率可達 80%,兩種複合金屬的比較,是以三層複合金屬為最佳。而兩者對於二氯 甲烷效果就顯得不佳,24 小時去除效率約為 50%,說明單以複合金屬去除效果不 彰。管柱實驗以銅鐵鋁複合金屬進行反應,其與批次實驗有相同趨勢,當去除四 氯化碳時,經過使用 7 天,去除效率仍維持約 98%,但是降解二氯甲烷約 2 天就 達貫穿,失去去除功效。電子媒介體的固定方式,在四大類中以直接與矽膠混合 的方式或結合活性碳的固定方式較為有效。直接與矽膠混合的方式則以 TMOS: 甲醇:TPPS 為 1:6:0.33 為最佳。活性碳的固定方式能有效的應用於四氯化碳和 二氯甲烷,尤其以達飽和的方式最有效。而比較三種電子媒介體,則是以維生素 B12 最佳,TPPS 次之,磷鎢酸鈉為最差。. 關鍵字:固定化、電子媒介體、鐵鋁複合金屬、銅鐵鋁複合金屬、含氯有機物. XI.
(14) The Application of Immobilized Electron Mediators Combined with Zero-Valent Metals for Treatment of Chlorinated Organics in Water Advisor: Dr. Hsing-Lung Lien Department of Civil and Environmental Engineering National University of Kaohsiung. Student: Lien-Hsiang Su Department of Civil and Environmental Engineering National University of Kaohsiung. ABSTRACT The research use four major class that total of 13 kinds of methods to immobilized electron mediators.(vitamin B12, TPPS and sodium phosphotungstic) combined with bimetal and trimetal ( Cu/Al、Fe/Al and Cu/Fe/Al) in different condition to removal pollution (CT and DCM). To discuss the effectiveness, advantages and disadvantages of the immobilization by results. The results showed discuss bimetal and trimetal of batch experience to removal CT in different condition. The results show to removal CT in batch experiment that bimetallic iron-aluminum the best condition in pH=4. The removal efficiency reach 76% in 4 hr. And trimetallic copper-iron-aluminum the best condition in pH=10. The removal efficiency reach 80% in 0.5 hr. Compaired with them that trimetall was the best. But trimetallic copper-iron-aluminum had poor results to removal DCM. The removal efficiency only 50% in 24 hr. Explanation the poor results with only trimetall. The column tests use trimetallic copper-iron-aluminum. It had same trend with batch experiment. The removal efficiency keep 98% in 7d with CT. But only 2d was though by DCM that was lose efficacy. The methods to immobilized electron mediators were best ways for mixing directly with silicone and combining PAC in four. XII.
(15) category. The best methods to mix directly with silicone that ratio of TMOS : methanol:TPPS was 1:6:0.33. The immobilized method of PAC could effective applied for CT and DCM. In particular reach saturation was the most effective. Compared the three electron mediators, the best of the three was vitamin B12, the second was TPPS, the worst was sodium phosphotungstic.. Keywords: Immobilized, Electron mediator, Bimetallic iron-aluminum, Trimetallic copper-iron-aluminum, Chlorinated organic. XIII.
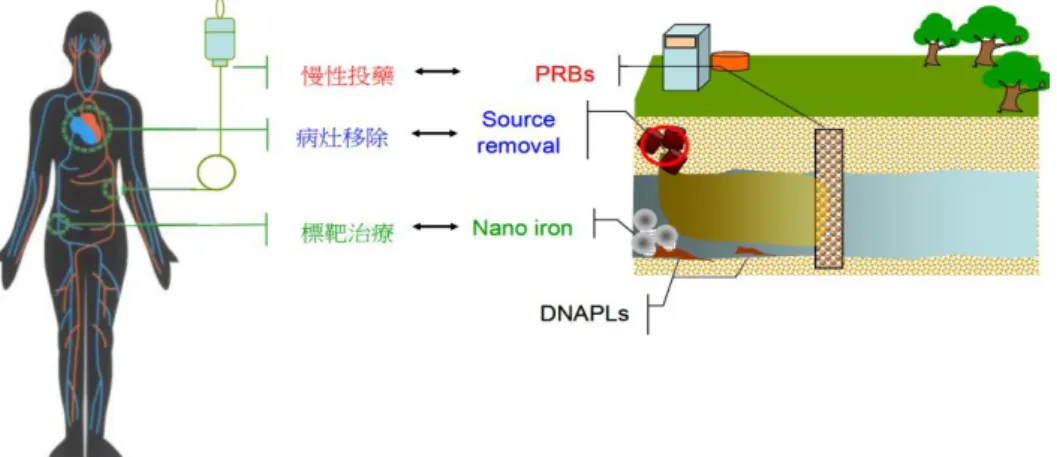
(16) 第一章 前言 1.1 研究緣起 隨著科技日益的進步,環境污染的問題也日趨嚴重,水是很重要的 資源,當水受到污染,對環境也是一大破壞,甚至影響人體的健康。在 水體有分為地面水以及地下水,地面水包含河川、湖泊等。通常地面水 的污染來源可能來自工廠的排放,其受到污染比較容易察覺,因為可能 發生變色或生物死亡等。而地下水污染有可能是經由土壤污染滲透到地 下水或管線破裂所造成,其污染較不易被察覺,一但受到污染,影響是 相當廣泛。. 對於含氯有機物去除的方式相當多,一般工業廢水以高級氧化處理 方式去除,而對於地下水的整治就如同醫師對病人的治病一般(圖 1-1)。 醫師發現病人的病灶,例如腫瘤等,對病患開刀移除病灶避免其繼續擴 大危害病患健康,此為第一要務。之後,針對病患的狀況擬定治療之療 程,例如持續的投藥與定期的回診追蹤,以確保病患術後之復原良好, 如果病灶位置無法開刀,標靶治療成了少數可以選擇的療法。地下水污 染的整治也是如此,如果能夠針對污染源進行移除(source removal),則可 以有效的解決地下水污染的絕大部分問題,然而,常常由於無法找出污 染源的位置(例如:DNAPLs)或已知的污染源無法移除(例如:工廠搬遷問 題),以致於只能針對地下水的污染進行持續性的整治。在歐美各國,充 填零價鐵金屬之透水性反應牆(permeable reactive barrier, PRB)為近 20 年 來最成功的地下水復育技術之一(Flury et al., 2009; Phillips et al., 2010;. 1.
(17) Higgins et al., 2009; Zolla et al., 2009 ),但實場的長期操作經驗顯示,透水 性反應牆之處理效果,由於受限於水中 pH 的影響,造成鐵金屬表面氧化 物 的 生 成 導 致 處 理 效 果 有 隨 時 間 遞 減 的 趨 勢 (Phillips et al., 2010; O’Hannesin et al., 1998; Puls et al., 1999)。PRB 為被動式整治技術,但具 有長效性,一般操作年限至少有 5 年的時間,可視為慢性投藥技術。奈 米零價鐵金屬則是地下水整治技術的另一種代表,奈米零價鐵金屬粒徑 大小約 10-100 nm,比表面積約 35 m2/g,具有殼核結構(core-shell)(Li and Zhang, 2007)。其外殼為具吸附能力之氧化鐵(FeOOH),內層為具還原 能力之零價鐵,不但保留所有一般鐵金屬的優點,更由於比表面積的顯 著增加(30~300 倍) ,其處理效率遠高於一般的鐵金屬,降低中間產物的 生成,同時,可藉由直接注入地下水的方式,提供了更多的機動性與便 利性(USEPA, 2008; Wei et al., 2010; Kirschling et al., 2010)。由於奈米鐵的 時效性較 PRB 短,但操作彈性高,處理效率佳,可提供類似標靶治療的 概念,針對急迫性的地下水污染進行快速的處理。. 圖 1-1. 地下水整治技術與人體醫療間之關連性. 2.
(18) 在地下水的物化整治技術上,PRB 仍被視為是最有效的技術之一, 其原因是在污染源無法移除的前提下,長期的處理能力成為成本考量的 核心關鍵因素。與醫師治病的藥物一般,越多的藥物提供醫師選擇,對 病因複雜度高的病患治療的彈性越高,透水性反應牆的填充材料越多 元,面對複雜的地下水污染問題的處理成功的機會越大。傳統的零價鐵 透水性反應牆對含氯有機污染物與重金屬的去除皆有良好之功效,除了 重金屬的吸附作用外,對還原性含氯有機物污染物而言,主要是透過氧 化還原反應,也就是零價鐵做為還原劑,將含氯有機污染物經由還原脫 氯反應(Reductive dechlorination) 達到去除之目的(Matheson and Tratnyek, 1994): Fe0 Fe2+ + 2e-(鐵腐蝕作用). (1-1). CxHyClz + zH+ + zFe0 CxHy+z + zFe2+ + zCl-. (1-2). 然而,仍有一些環境中不易分解之還原性污染物是零價鐵金屬無法 處理的,例如:二氯甲烷(Lien and Zhang, 1999)、二氯乙烷(Lien and Zhang, 2005),這些不易分解之含氯污染物,有些是其他污染物降解之產物,且 毒性比原污染物更強,如二氯甲烷是四氯化碳的還原脫氯產物。因此, 研究著重於二氯甲烷的去除。而針對二氯甲烷的去除,在過去的研究曾 利用 Cu/Al 結合 B12 的方式達到有效去除,且能加速其反應速率,因此作 為研究中去除二氯甲烷的添加物(黃,2008)。但是過去研究中的電子媒介 體是液相的,不但參與反應的時間較為短暫,也易隨著水流而帶走,因 此需探討其固定化方式,以及將其固定化之後對二氯甲烷的去除情況。. 3.
(19) 1.2 研究目的 利用複合金屬(Fe/Al、Cu/ Fe/Al)與電子媒介體去除難分解之二氯甲 烷。 電子媒介體的固定化以及測試固定之後去除污染物之情況,從中評估 最適合的固定方式。 藉由反應速率評估降解的效率以了解不同材料之間對於污染物的去 除速率。. 4.
(20) 第二章 文獻回顧 2.1 含氯有機物 氯是鹵素的一種元素,含氯有機物廣泛的應用於農業與工業,農業 中的含氯有機物應用於農藥、除草劑或殺蟲劑,而工業的運用包含冷凍 劑、金屬去油劑、半導體製造或是溶劑。農藥、除草劑以及殺蟲劑容易 透過噴灑的過程,經由土壤滲入地下水,或者隨水流入河川中;而工業 製程的有機溶劑可能因輸送的管線破裂,進而入滲至地下水,亦或蓄意 的傾倒造成水的污染。一般常見的含氯有機污染物包含 DDT、六氯苯、 五氯酚、四氯化碳、四氯乙烯、三氯乙烯、氯仿、二氯甲烷等。大部份 的含氯有機物低溶水性、高親脂性且密度比水大,因此易下沉至水底部, 如果進到地下水層將累積於不透水層底部,並使污染範圍逐漸擴大,造 成整治工作的困難。因此研究以含氯有機物為主,然而二氯甲烷是很難 整治的污染物,故以二氯甲烷為主軸,另外二氯甲烷為四氯化碳的代謝 產物,相較之下四氯化碳較容易處理,所以利用四氯化碳作為材料測試 的有效性,以下針對四氯化碳和二氯甲烷作為探討。. 2.1.1 四氯化碳 四氯化碳(Carbon tetrachloride, CT),具氯仿的微甜氣味,化學分子式 是 CCl4,分子量為 153.84,為無色、容易揮發,揮發速率:12.8 (乙酸丁 酯=1)、不易燃的液體,沸點 76.8℃,蒸氣壓 15.26 kPa (25℃),蒸氣密度 5.3 g/L,熔點-22.6℃。微溶於水,水溶性:0.8 g/L,辛醇/水分配係數(log Kow):2.83,可與乙醇、乙醚、氯仿及石油醚等混溶。相對密度(水=1):. 5.
(21) 1.60,易沉於水底部 (物質安全資料表)。曾廣泛作為滅火器、有機物的 氯化劑、香料的浸出劑、纖維的脫脂劑、藥物的萃取劑、乾洗劑、冷凍 劑、金屬去油劑、農業用的消毒劑、氯化有機化合物、半導體製造以及 溶劑 (脂肪、油、橡膠等)。其對環境的影響深遠,當釋放至大氣中非常 安定,可存在 30-50 年。對於健康危害則是會抑制中樞神經系統,為疑 似致癌物質,引起動物肝腫瘤,但有關人的資料有限。當重覆暴露可能 造成嚴重的腎 、肝損害及心、肺衰弱。(物質安全資料表). 四氯化碳在地下水中的管制標準依據環保法規地下水污染管制標準 第四條之規定在飲用水水源水質保護區內之地下水(第一類)為 0.005 mg/L,而第一類以外之地下水為 0.05 mg/L。去除四氯化碳的方式有很 多,像是 FeS + Cu, Co, Ni、Fe/Al、ZVI 以及 Ultrasonic 等方式(Choi et al., 2009; Chen et al., 2008; Jiao et al., 2009; Lee and Oh, 2010)。由 FeS +過渡 金屬(Cu, Co, Ni)的結果顯示 1mM 的 Cu、Ni 加上 33 g/L FeS,去除效率 達 90%以上,顯示過渡金屬的添加能增加去除效率,另外添加 Cu 的反應 效率優於添加 Ni,所以 Cu 較 Ni 適合(Choi et al., 2009)。Fe/Al 去除四氯 化碳的結果顯示其能有效還原脫氯,產生 9%的三氯甲烷、17%的二氯甲 烷和 38%的甲烷,一方面說明四氯化碳的產物,另一方面證明 Fe/Al 能 有效還原脫氯(Chen et al., 2008)。使用零價鐵在不同 pH 值下去除四氯化 碳會強烈影響去除效率,愈酸的情況下去除效率較高,最高可達 79.2% (pH=0.4 與 0.62V,30 min),在鹼性情況下較差,於 pH=12 的情況下,去 除率僅有 2~5% (Jiao et al., 2009)。而超音波在同時去除三氯乙烯和四氯. 6.
(22) 化碳時,超音波能提升三氯乙烯去除效率,但是對於四氯化碳則沒有顯 著影響(Lee and Oh, 2010)。由以上結果可得幾個結論: 一、 四氯化碳以還原脫氯方式處理其會降解成三氯甲烷、二氯甲烷以及 甲烷,因此以其代謝產物可以觀察出是否為還原脫氯。 二、 零價鐵 pH 值在酸性為最佳,在鹼性條件較差。 三、 銅的添加能幫助去除四氯化碳。 四、 比較幾種去除方式說明 Fe/Al 能有效降解四氯化碳。 以上結論作為後續研究參考要件。. 2.1.2 二氯甲烷 二氯甲烷(Dichloromethane, DCM),為無色透明易揮發液體,化學分 子式是 CH2Cl2,分子量為 84.93,為四氯化碳的代謝產物,是一種無色、 揮發性及不燃性的液體,具有類似於醚類的刺激性味道,人體嗅覺對空 氣中二氯甲烷的察覺極限約為 1000 mg/m3,密度為 1.33,溶解度為 2 g/100 mL,溶於約 50 倍的水,溶於酚、醛、酮、冰醋酸、磷酸三乙酯、乙醯 乙酸乙酯、環己胺。與其他氯代烴溶劑乙醇、乙醚和 N,N-二甲基甲醯 胺混溶。熔點-95.1°C,沸點 40°C,自燃點 640°C,臨界溫度 237°C,臨 界壓力 6.0795 MPa (物質安全資料表)。. 溶劑是二氯甲烷的最主要用途,二氯甲烷具有廣大的溶解力、低沸 點以及相對而言最低的毒性和相對而言最好的反應惰性,使其成為有機 合成中使用頻率位居第一的有機溶劑。另外作為有機合成原料,像是油 漆、殺蟲藥、油污去除劑、清潔劑和其他產品中。 二氯甲烷可經由吸入、 7.
(23) 口服或皮膚接觸而中毒。急性接觸可導致黏膜、呼吸道剌激、頭痛。較 高濃度可抑制中樞神經糸統及導致呼吸衰竭。皮膚接觸可致刺激感或灼 傷,若濃度超過 50000 ppm 可致對生命產生立即危險。重複性地接觸二 氯甲烷可導致皮膚發炎,液體和蒸氣會刺激眼睛、皮膚及上呼吸道。暴 露的症狀包括頭痛、昏睡、嘔吐、眼花、恍惚、暴躁、麻痺和四肢疼痛 等(勞工安全衛生研究所)。. 二氯甲烷在地下水中的管制標準依據環保法規地下水污染管制標準 第四條之規定在飲用水水源水質保護區內之地下水(第一類)為 0.005 mg/L,而第一類以外之地下水為 0.05 mg/L。去除二氯甲烷的方式包含 Fe/TiO2、Cu0+B12、GAC、Fenton (傅,2003; Huang, et al., 2013; Khan et al., 2010; Michael et al., 2013)。Fe/TiO2 去除二氯甲烷主要以光催化的方式去 除,其結果顯示隨著 Fe:Ti 比例的增加,光催化活性有下降趨勢,當 Fe/Ti=0.005 mol%時光觸媒對於二氯甲烷有最佳的催化能力。Cu0+B12 則 是利用被還原的 B12 進行催化的功能,結果顯示於 2 hr 去除二氯甲烷的去 除效率可達 99%,另外在鹼性的條件下(pH=9.6)有最佳的去除效率。GAC 的應用在許多類別的活性碳和去除條件中以椰子製造的活性碳在 pH 6-8 吸附能力最高,吸附量達 45.5 mg/g。另外亦有利用 Fenton 的方式去除二 氯甲烷。根據這幾種去除二氯甲烷的方式主要以氧化還原的方式去除, 如 Fe/TiO2、Cu/Al+B12 和 Fenton,也有利用吸附的方式達到去除,如 GAC 的運用,與四氯化碳的去除方式都一樣具有複合金屬的運用,或是 Fenton 的方式且能有效去除,因此複合金屬將會是後續研究的主軸。. 8.
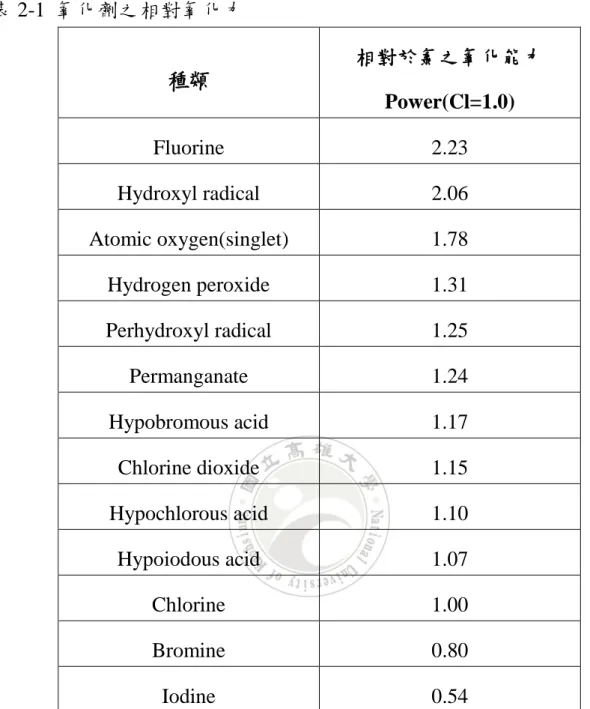
(24) 2.2 廢水與地下水中污染物的去除 去除水中含氯有機污染物分為工廠所排放的廢水和進入地下水體的 地下水污染,其去除的方式也會有所不同,先後分別敘述一般廢水的處 理方式以及地下水的整治方法。. 2.2.1 廢水中含氯有機物之去除 一般廢水處理的方式分為物理、化學和生物,對於生物技術的處理 方式而言,其成本較低廉,且適合用於不同種類的污染物,雖然使用上 相當普遍,但是卻只適用於生物易分解無毒的物質與有機廢水,且處理 時間長。對於含氯有機物之廢水可能因其毒性或濃度太高,而使生物生 長受到抑制,進而無法有效的發揮其效果。而以物理方式處理的混凝與 吸附,其沉澱物或吸附物需要再做另外的處理,因此以化學方式的處理 較為適當(劉,2002)。. 為了對於毒性高且較難處理之含氯有機物採以高級氧化處理程序 (advanced oxidation processes,AOPs),高級氧化程序例如 Fenton 氧化法 (Fe2++H2O2)、光催化氧化法(UV+TiO2)和臭氧法(O3)等技術普遍用於處理 廢水中的有機物,如 Fe2++H2O2 (Fenton)、H2O2+UV、O3+OH-、O3+ H2O2、 O3+ UV、O3+UV+H2O2、O3+TiO2、UV+TiO2 等的應用。這些方法主要的 反應機制就是在過程中生成具高反應性的氫氧自由基(hydroxyl radical), 氫氧自由基具有相當高的氧化電位,如表 2-1,其可將有機物完全礦化或 轉化為較無害的物質(蘇,2009)。. 9.
(25) 表 2-1 氧化劑之相對氧化力 相對於氯之氧化能力 種類 Power(Cl=1.0) Fluorine. 2.23. Hydroxyl radical. 2.06. Atomic oxygen(singlet). 1.78. Hydrogen peroxide. 1.31. Perhydroxyl radical. 1.25. Permanganate. 1.24. Hypobromous acid. 1.17. Chlorine dioxide. 1.15. Hypochlorous acid. 1.10. Hypoiodous acid. 1.07. Chlorine. 1.00. Bromine. 0.80. Iodine. 0.54. 光催化氧化法應用於廢水中,很常用來處理藥物,像是抗生素藥物 環丙沙星(ciprofloxacin) (An et al., 2010)或是磺胺類藥物(Yang et al., 2010) 等。在光催化的過程會產生氫氧自由基,而氫氧自由基可以加速其反應, 在降解環丙沙星的過程,發現氫氧自由基能有效的增加反應速率,在對 磺胺類的藥物處理,也有很好的去除效率,尤其在 pH=3 的情況下(An et. 10.
(26) al., 2010; Yang et al., 2010)。光催化除了處理藥物外,也被用來去除含氯 有機物質,在廖 (2007)的研究利用光催化去除二氯乙烷和氯乙烯,結果 顯示有相當好的去除效率,不過其去除的方式不盡然以還原脫氯的方式 進行,一部分會吸附於觸媒的表面,而致使最終活化效率變差。雖然光 催化產生的氫氧自由基能有效加速其去除效率,但是其需要光源,面對 光照不到之處則不適用,因此以其他產生自由基的方式去除。. 臭氧在不同 pH 值產生自由基去除污染物的情況則與光催化和 Fenton 反應很不一樣,在 Gharbani et al., (2010)的研究去除 4-氯-2-硝基苯 酚,pH=3 的情況下降解效果最差,幾乎無自由基的產生,pH=7 則有自 由基的產生,達到完全去除的時間減少 5 分鐘,pH=9 一開始就有氫氧自 由基的產生,促使其反應加速。由此一方面可以得知臭氧能有效快速的 降解污染物,另一方面 pH 值會影響氫氧自由基的產生,進而影響其去除 效率,可見氫氧自由基在反應中佔很重要的位子,後續再對 Fenton 反應 進一步討論。臭氧雖然能快速有效的降解,但是其半衰期短,約 20 分鐘, 因此接下來要再針對 Fenton 反應作討論。. Fenton 反應為 Fe2++H2O2,通常可能將 Fe2+置換成 Fe3+或 Fe0,稱之 為 Fenton-like , Fenton 反 應 亦 會 與 光 能 或 電 能 結 合 , 分 別 稱 之 為 photo-Fenton 和 electro-Fenton,每個反應機制略有不同,但是都會產生 OH‧,由前面的回顧可知氫氧自由基能有效幫助反應的去除,因此選擇 類似 Fenton 反應的材料進行去除,在林 (2012c)的研究指出 Fe/Al 複合金. 11.
(27) 屬可產生二種自由基,在儀器測定下,分別是氫氧自由基與甲基自由基, 且都能維持長效性的自由基產生,除此之外傳統 Fenton 反應容易有混凝 的產生,而 Fe/Al 複合金屬則不會有混凝的憂慮,因此後續以 Fe/Al 複合 金屬作為討論的主軸。. 2.2.2 地下水的污染與整治 地下水的運用相當廣泛,通常會用來作為農田灌溉、魚塭用水、工 業用水甚至是民生用水,因此地下水是扮演著相當重要的角色,一旦地 下水遭到污染,相對所產生的危害性以及衝擊性就相當的大。一般在農 業上的施肥、噴灑農藥,會經由土壤滲透至地下水,在工業上許多工廠 或者一些科技產業會使用相當大量的有機溶劑來作為清潔劑或是溶劑等 用途,當儲槽或管線的洩漏,或者工廠廢水的排放,這些都是會造成污 染的原由,而這些污染物則會危害環境同時也影響人體的健康。. 地下水的污染包含芳香族碳氫化合物、氯化碳氫化合物、農藥、重 金屬等。在地下污染物質目前較受重視的為,重金屬、非混合性污染物。 以液態存在的,一般稱為 NAPL(Non Aqueous Phase Liquid,非水相液 體) 。其中 NAPL 與水接觸後,形成與水壁壘分明的獨立體,故 NAPL 與 水呈不可混合的情況。NAPL 又可分為比水輕之不含水液態物質 (Less Dense Non-Aqueous Phase Liquid,LNAPL,如石油碳氫化合物等)及比水 重之不含水液態物質(Dense Non-Aqueous Phase Liquid, DNAPL,如三 氯乙烯等)。常見的 LNAPL 為汽油、煤油、柴油等燃油類,所以 LNAPL 污染通常發生於石油煉製、加油站、儲油槽等地。常見的 DNAPL 為三 12.
(28) 氯乙烯(TCE)、四氯乙烯(PCE)等含氯有機溶劑 (圖 2-1)。另外由於 DNAPL 難予以清除且易形成永久性污染之特性,對環境的影響非常大, 因此著重於含氯有機物質作為探討(鄭,2006)。. 圖 2-1. DNAPL 物質於地下水中分佈圖 (資料來源:http://oceanworld.tamu.edu/resources/environment-book/groundwaterremediation.html). 針對這些污染物的整治,先了解台灣對這些污染物的管制標準,以 下是台灣法規,對於地下水四氯化碳、三氯甲烷、二氯甲烷,訂定的法 規標準。(地下水污染管制標準第四條) 表 2-2. 地下水中污染物之管制標準 (地下水污染管制標準第四條) 污染物. 四氯化碳 三氯甲烷. 二氯甲烷. 管制. 第一類. 0.005. 0.1. 0.005. 標準. 第二類. 0.05. 1.0. 0.05. *濃度單位:mg/L *第一類:飲用水水源水質保護區內之地下水。 *第二類:第一類以外之地下水。. 13.
(29) 地下水整治可分為控制及處理兩個部分。地下水控制的目的包括: (1)遏止或限制污染團的移動、(2)阻止污染源繼續產生污染、(3)避免乾淨 的地下水流經污染源、(4)避免受污染的地下水流經飲用水源、(5)降低污 染源下方的地下水位以免形成滲漏。地下水處理的目的則是:(1)能永久 去除或減低污染物之毒性、(2)降低污染團之移動性、(3)降低污染體積。. 地下水處理方法大致可概分為:(1)抽取處理法、(2) 循環井處理法、 (3) 水力破裂處理法、(4)生物處理法、(5)自然衰減法、(6)現地透水性反 應牆 (環保署土污基管會)。如前面所提,含氯有機物屬於DNAPLs較不 易去除,且毒性高不適用於生物處理,另外對於找不到或無法移除之污 染源,以透水性反應牆較佳,因此後續著重於透水性反應牆的論述。. 2.2.2.1 透水性反應牆 透水性反應牆是在概念上發展比較完整的整治技術,其對於含鹵素 的有機污染物具有相當好的處理效果(Puls et al., 1998; Liang et al., 2000)。其原理為,將透水性反應牆設置於受污染地下水之前緣,待地下 水通過反應牆時,其內部填充之污染物清潔劑與污染物反應,以達去除 污染物之目的(Beitinger, 1998)。. 去除地下水中的含氯有機物很常運用的方式是利用透水性反應牆, 如圖2-2所示,其主要先評估污染區以及地下水流,然後開挖一條深溝, 在溝內建一面透水性的牆,使地下水流經這面牆,牆內的物質會與污染 物產生反應,當其穿透之後,會轉變為較乾淨的地下水,達到去除效果。 14.
(30) 而在透水性反應牆設置之前會經過幾項程序,包括:初步場址評估、場 址特徵調查、選用反應材料、處理能力試驗、模式用工程設計及施工方 法等(Gavaskar, 1998)。圖2-2為透水性反應牆示意圖。其優點為,可以在 不改變地下水流狀態下,以較低的操作及維護成本去除地下水之污染 物,且對於難確定之 DNAPL 污染源位置 (hot spot)之污染團仍能有效去 除。另外透水性反應牆是一種被動式的的反應介質,運用於地下水的整 治技術,傳統的反應牆運用的是100% 的顆粒狀零價鐵用來去除水中的 重金屬,像是鉻金屬,另外也用來移除地下水中的有機污染物,像是三 氯乙烯(Puls et al., 1999)。. 圖2-2. 透水性反應牆示意圖 (資料來源:http://oceanworld.tamu.edu/resources/environment-book/groundwaterremediation.html). 15.
(31) 2.3.零價金屬的應用 以下分為兩大類,一大類是由金屬自己提供電子,像是零價鐵、零價 鋁、零價銅等。另一大類是由氫氣為電子供應者,如零價鎳、零價鈀等。 以下針對這兩大類分別介紹。. 2.3.1 零價鐵 零價鐵是很廣泛運用的零價金屬,因為其對環境具有友善性,可以 減少毒性副產物的生成,另外其能夠廣泛的去除含鹵素有機化合物, Gvaskar 等人指出,在 1972 年 Weeney and Fiscer 發現零價金屬可在室溫 下破壞含氯有機物(Gvaskar et al., 1998),由以下方程式為零價鐵去除含氯 有機物之作用情形。零價鐵提供電子給含氯有機物,以達到還原脫氯 (Reductive dechlorination)之目的(Matheson et al., 1994)。. Fe0 Fe2+ + 2e-(鐵腐蝕作用). (2-1). CxHyClz + zH+ + zFe0 CxHy+z + zFe2+ + zCl-. (2-2). 然而零價鐵金屬去除含氯有機物為一種氧化還原作用,因此在反應 的過程中會造成零價鐵表面形成沉澱物如氫氧化鐵或氧化鐵的生成,使 其反應下降,也會使水中 pH 值增高(Matheson et al., 1994) (方程式 2-3、 2-4、2-5)。 4Fe0 + 3O2 2Fe2O3. (2-3). Fe0 + 2H2O Fe2+ + H2 + 2OH-. (2-4). Fe2+ + 3OH- Fe(OH)3↓. (2-5) 16.
(32) 因此改使用奈米零價鐵,其效果則較傳統的零價鐵好,除了接觸的 表面積較大之外,奈米零價鐵會形成殼核結構(core-shell) 。其外殼為具吸 附能力之氧化鐵(FeOOH) ,內層為具還原能力之零價鐵,不但保留所有 一般鐵金屬的優點,更由於比表面積的顯著增加(30~300 倍) ,其處理效 率遠高於一般的鐵金屬,降低中間產物的生成,同時,可藉由直接注入 地下水的方式,提供了更多的機動性與便利性(USEPA, 2008; Wei et al., 2010; Kirschling et al., 2010)。 另外其針對不同含氯有機物之去除效率的比較,如表 2-3。由表 2-3 的結果可以發現去除某些含氯數較低的物質,像是氯乙烯,去除效率較 不佳。另外單一零價鐵對於某些含氯有機物的去除效率較不好,例如單 一零價鐵去除四氯化碳的效率僅有 16.3%,因此後續再對其他零價金屬 進一步探討。 表 2-3.奈米零價鐵去除含氯有機物比較表 反應材料. 污染物. 去除效率. 參考文獻. NZVI. 氯乙烯. 50-99%. Wei et al., 2010. NZVI. 三氯乙烯. 84%. Teerakun et al., 2011. NZVI +電力. 三氯乙烯. 100%. 劉,2006. Fe/Pd-alginate. 三氯乙烯. >99.8%. Kim et al., 2010. NZVI. 16.3% 四氯化碳. Zhang et al., 2011. NZVI +EDTA. 89.1%. NZVI. 六氯苯. 隨變數不一. Shih et al., 2011. NZVI. 六氯苯. 95%. Elliott et al., 2008. 17.
(33) 2.3.2 零價鋁 零價鐵在高 pH 值的情況降解效果較不佳,相對地零價鋁在高 pH 值 的條件下能夠成為更好的反應試劑,因為零價鋁在有 OH- 的情況下比較 不會產生氧化物沉澱,所以在鹼性的情況下零價鋁會較零價鐵佳 (Lien and Zhang, 1999; Lien and Zhang, 2005)。零價鋁提供的標準還原電位為 -1.662V,然而在中性的情況下三氧化二鋁會快速的形成,限制它作為反 應介質的應用程序,所以使用複合金屬來彌補其缺陷(Lien and Zhang, 2002; Lee et al., 2006)。. 零價鋁除了以還原脫氯的方式去除污染物之外,還有可能以吸附的 方式去除污染物,在 Lien et al., (2010)的研究去除過氯酸鹽就是以吸附的 方式進行,說明鋁不一定以還原脫氯的方式去除,當其轉換為氫氧化鋁 時會以吸附的方式進行。因為除了還原的去除方式外,還可能以吸附的 方式進行,因此進行產物分析很重要,以確保還原降解而非單純吸附。. 2.3.3 零價銅 奈米銅大部分的成分是零價銅(Cu0),少部分以氧化銅(Cu2O)的方式 存在,零價銅是很好的催化劑,有助於去除較難處理之含氯有機物質, 像是 1,2-二氯乙烷,雖然零價鐵能夠降解各種高度氯化的污染物,但是 對 1,2-二氯乙烷的反應性是非常低的,去除效率相對較差,因此改以奈 米銅取代奈米鐵。文獻回顧利用奈米零價銅結合硼氫化鈉去除 1,2-二氯 乙烷,在 2 小時內去除效率達 80%以上,降解過程產生 79%的乙烷和 1.5% 的乙烯,說明其以還原脫氯的方式進行以及大部分轉變為乙烷(Huang et. 18.
(34) al., 2011)。. 除了 1,2-二氯乙烷之外,二氯甲烷也是很難去除的物質,Huang et al., (2013)利用零價銅結合維生素 B12,2 hr 內去除效率達 99%,另外利用鐵 提供電子,形成銅鐵複合金屬的方式去除,也能有效去除,因此後續會 以銅的複合金屬與維生素 B12 探討去除二氯甲烷之情形。. 以銅為材料釋出在水中的銅濃度也是需注意的,於放流水中和地下 水污染管制標準有所不同,於放流水的管制標準為 3.0 mg/L(放流水標 準,2012),而在地下水第一類(飲用水水源水質保護區內之地下水)的管 制標準為 1.0 mg/L,第二類(第一類以外之地下水)的管制標準為 10 mg/L(地下水污染管制標準,2011),因此視用於何種環境,管制標準也有 所不同。. 2.3.4 其他零價金屬的應用 與前面所提的零價金屬不同之處,在於其藉由氫氣來提供電子,以 下所提的零價鎳與零價鈀皆藉由氫氣提供電子。. 2.3.4.1 零價鎳 零價鎳與其他物質結合能有效的去除含氯有機物,像是與氫自營菌 的結合,去除三氯乙烯能完全轉換為烷類,其中鎳金屬所產生的氯乙烯 再經生物脫氯,達到良好去除效氯(杜,2005)。除此之外鎳也會與鐵形成 鎳鐵複合金屬,鎳鐵複合金屬能有效的去除三氯乙烯和五氯酚,Schrick et 19.
(35) al., (2002)的研究指出當其去除三氯乙烯時主要產物為丁烷、己烷與辛烷 等,而毒性副產物例如氯乙烯、 1,1-二氯乙烯、順-二氯乙烯與反-二氯乙 烯等只偵測到微量且不持續累積,說明鎳鐵複合金屬有著高處理效果與 幾乎不產生有毒產物的特性。而去除五氯酚則是經十六烷基三甲基溴化 銨 (cetyl trimethylammonium bromide, CTAB)修飾鎳鐵雙金屬以吸附的方 式進行,藉由反應動力學可發現 CTAB 修飾之鎳鐵雙金屬可較未修飾之 鎳鐵雙金屬快速吸附五氯酚,並較快還原脫氯產生氯離子(林,2012b)。 雖然鎳鐵複合金屬有著高處理效果與幾乎不產生有毒產物的特性,但是 由於鎳金屬在水中會釋出鎳離子而對環境造成二次危害,因此較不適合 用於地下水污染之現地復育。. 2.3.4.2 零價鈀 Pd 為有效的催化劑,利用 Pd 與 H2 能有效降解氯乙烯、四氯化碳、 過氯酸鹽、硝酸根和偶氮染料。對於這些污染物探討其去除的途徑,例 如對於氯乙烯或四氯化碳是以還原脫氯方式,對於過氯酸鹽和硝酸根則 是脫氧,而對於偶氮染料則是以脫氮的方式去除。對於不同污染物,適 合與 Pd 所結合的金屬也有所不同,如對於去除含氯有機物則是以 Pd/γAl2O3 或 Pd/Fe 較為適合(Chaplin et al., 2012)。. 單純零價金屬較難以有很好的去除功效,通常會加其他添加物增加 其去除效率,或者以複合金屬的型態,利用內部不斷的提供電能,使得 材料可反應的時間增加,同時增加去除效率,因此後續對於一些複合金 屬進行回顧。 20.
(36) 2.4 複合金屬的運用 有一些環境中不易分解之還原性污染物是零價鐵金屬無法處理的, 例如:二氯甲烷(Lien and Zhang, 1999)、二氯乙烷(Lien and Zhang, 2005), 這些不易分解之含氯污染物,有些是其他污染物降解之產物,且毒性比 原污染物更強,如二氯甲烷是四氯化碳的還原脫氯產物,因此改使用複 合材料來取代單純零價鐵。. 2.4.1 Fe/Al 複合金屬 Fe/Al 複合金屬是以中心為鋁,外層為鐵所組成,其主要就是應用鋁 不斷的提供鐵電子,讓鐵能維持元素狀態,以達到去除的效用,如圖 2-3 顯示之作用情形,其不但保有零價鐵的優點外,也同時能夠克服表面生 成沉澱物之缺點,除此之外還可以達到更佳的去除效率(謝等,2005)。另 外其中心為鐵而外層為鋁的原因是因鋁金屬具有高還原位(1.66V),相較 之下鐵的電位能為(0.44V),所以中心的鋁才能不斷地提供鐵電能。. 圖 2-3. 鐵鋁複合金屬示意圖. 從以上論述可以得知鐵鋁複合金屬乃是由鋁提供電子給鐵,由以下 的反應式可以更明確看出其電子傳遞之情形。零價鋁金屬氧化成三價鋁. 21.
(37) 金屬,然後釋出電子,而亞鐵離子接受電子之後會還原成零價鐵。. Al0. → Al3+ +3 e-. ΔE = +1.66V. (2-6). Fe3+ + 3e- → Fe0. ΔE = + 0.33V. (2-7). Al0 +Fe3+ → Al3+ + Fe0 ↓. ΔE = +1.99V. (2-8). 一般鐵鋁的運用可以用來還原脫氯,像是對四氯化碳降解。圖 2-4 為 Chen 等學者運用 Fe/Al 複合金屬降解四氯化碳之概念圖,四氯化碳在 零價鐵表面進行還原脫氯,導致零價鐵氧化成亞鐵離子,使得水中的亞 鐵離子濃度增加。但在鐵鋁複合金屬內部的零價鋁會提供電子給亞鐵離 子,還原成零價鐵,得以再降解四氯化碳。而零價鋁被氧化成三價鋁離 子,隨後形成氫氧化鋁而沉澱(Chen et al., 2008)。. 圖 2-4. 四氯化碳經由 Fe/Al 複合金屬降解處理 (Chen et al., 2008). 而針對鐵鋁複合金屬探討鐵金屬的含量對於四氯化碳之降解情形 (圖 2-5),其分別用 5、15、25、35、45 wt%作為探討,測定其表面積反. 22.
(38) 應速率常數(kSA),從中可發現在 15%有最佳效率,因此在研究中鐵含量 設定為 15%作為探討。. 圖2-5. 鐵鋁的鐵含量對四氯化碳脫氯之有效性(Lee et al., 2006). 另 外 由電子顯微鏡 (SEM)分析鐵鋁複合金屬 (理論配比 15%)(圖 2-6a),可發現複合金屬表面為顆粒狀結構,附著於鋁載體上。而元素 mapping 分析可看到顆粒狀為鐵金屬(圖 2-6c),載體為鋁金屬(圖 2-6b)。 而由 SEM-EDX 分析結果亦證實複合金屬組成包含鋁元素與鐵元素(Chen et al., 2008)。. 23.
(39) 圖 2-6. (a) 鐵鋁複合金屬 SEM 圖,(b) (c) 分別為鐵鋁元素 mapping 圖 (Chen et al., 2008). Fe/Al 複合金屬在不同 pH 值的情況下以酸性為最佳,鹼性較差,Lee et al., (2006)中提到將 pH 值分別調整為 2.3、6.3 和 11.8 的條件下去除四 氯化碳,於 pH=2.3 的去除效率最高,而 pH=11.8 的去除效率最差,說明 在酸性的情況下去除效率較鹼性條件佳。除此之外 pH 值與不同金屬配比 比較,在研究中分別比較 pH 4.2-4.8 和 pH 5.5-6.7 在 5%-45%之間的配比, 都以 15%的去除速率最高,呼應前面所提的 15%為最佳(Lee et al., 2008)。. 2.4.2 Cu/Fe 複合金屬 Cu/Fe 複合金屬是一個內層為鐵,外層為銅的複合金屬,鐵的電位能 為-0.44V 而銅的電位能為 0.337V,其反應的方式為 2-9 式到 2-11 式。其 一開始是零價鐵氧化成二價鐵並釋出電子,當二價銅接受電子之後會還 原成零價銅。 24.
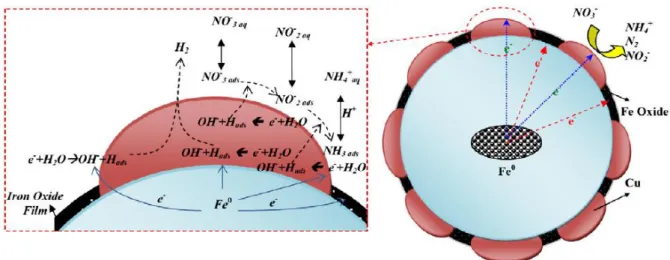
(40) Fe0. → Fe2+ + 2e-. ΔE = + 0.44V. (2-9). Cu2+ + 2e- → Cu0↓. ΔE = +0.34V. (2-10). Fe0 + Cu2+ → Fe2+ + Cu0↓. ΔE = +0.77V. (2-11). Cao 等人的研究中提到銅扮演著催化劑的角色,雖然說鈀的效果更 勝於銅,但是相較之下銅卻比鈀便宜很多,而在圖 2-7 展現了銅鐵複合 金屬降解 1,2,4-三氯苯之情形。鐵將電子傳遞給銅之後,在結合水中 H+, 其會使苯環上與氯產生斷鍵,而達到去除氯的效果(Cao et al., 2011)。. 圖 2-7. Cu/Fe 複合金屬去除 1, 2, 4-trichlorobenzene (Cao et al., 2011). 銅鐵的運用除了去除含氯有機物質,像是三氯乙烯和 1,2,4-三氯苯, 還有去除硝基苯以及硝酸鹽,由圖 2-8 的結果可以更清楚的了解銅鐵複 合金屬的作用機制,其中有氫氧自由基的產生而幫助硝酸根離子轉換成 氨根離子、氮及亞硝酸根離子,因此它是協助降解的因子之ㄧ(Hosseini et al., 2011)。另外在反應中可發現有氫離子的協助,因此它在酸性的情況下 會較其他條件下的去除效率還高。根據 Wenying 等人的研究證實在酸性 的條件下會優於鹼性,而在中性的情況下則屬最差(Wenying et al., 2008)。 25.
(41) 圖 2-8. 銅鐵複合金屬還原 NO3−-N 之概念模型 (Hosseini et al., 2011). 2.4.3 Cu/Al 複合金屬 銅為一惰性金屬,相對於鋁的電位(+1.66V),銅具有較低的還原電位 (+0.34V),因此將銅覆蓋於鋁的表面,以保護內層的零價鋁金屬,使鋁金 屬表面不易生成氧化鋁殼,並且鋁會不斷的提供銅電子,以增加其反應, 此外銅也為是一種具備催化功能之金屬,因此銅鋁複合金屬可能藉由銅 的催化能力以還原分解各種含氯污染物 (Yang et al., 1997; Lien and Zhang, 2002)。. 銅鋁複合金屬是以鋁的還原能力將銅離子還原並附著於鋁之表面, 一開始零價鋁金屬放出電子,並形成三價鋁離子釋出水中(式 2-12), 之後二價銅離子經接受電子後還原形成零價銅金屬(式 2-13),而三價鋁 離子在鹼性條件下又會形成氫氧化鋁(Al(OH3)),因此總反應如式 2-14。 另外文獻中提及銅鋁複合金屬無法在酸性條件下配製,其產物形成單獨. 26.
(42) 分散的零價銅金屬 (Lien and Zhang, 2002),可能是因為在酸性條件下, 氫離子會加速銅在鋁表面的結晶析出(黃,2008)。. 2Al0. → 2Al3+ + 6e-. ΔE = +1.66V. (2-12). 3Cu2+ + 6e- → 3Cu0. ΔE = +0.34V. (2-13). 3Cu2+ + 2Al0 → 3Cu0 + 2Al3+. ΔE = +2.00V. (2-14). 目前已證實銅鋁複合金屬可以去除數種含氯有機物如四氯化碳、三 氯甲烷、三溴甲烷 (CHBr3)以及二氯甲烷等含氯有機污染物(Lien and Zhang, 2002)。其中二氯甲烷是一種難以被零價鐵或鈀鐵複合金屬所分解 (Lien and Zhang, 1999)。根據黃(2008)的研究以維生素 B12 結合銅鋁複合 金屬能有效的去除二氯甲烷,當添加了維生素 B12 之後反應速率常數可從 0.11 增至 1.51 hr-1,顯示這兩種物質合在一起時能有效的去除二氯甲烷, 此為後續研究重要的參考資訊。. 2.4.4 鈀鐵複合金屬 鈀 (Pd)金屬為常用之催化劑(通常可催化涉及氫氣的化學反應) ,將 之附著於零價鐵表面即為鈀鐵複合金屬,經實驗證實鈀可降低表面沈澱 物的產生,並且有效強化零價鐵的能力,使其反應速度加快 (Grittini et al., 1995; Muftikian et al., 1996; Zhang et al., 1998; Lien and Zhang, 2005)。文獻 中指出鈀鐵複合金屬去除四氯化碳之比表面積標準化反應速率常數由 5.3×10-4 提昇為 9.0×10-3 L/hr/m2,增加約 17 倍,而去除三氯甲烷之速率 也由 8.4×10-5 提昇為 6.5×10-3 L/hr/m2,增加多達 77 倍 (Lien and Zhang, 27.
(43) 1999)。 鈀鐵複合金屬之配製是將零價鐵顆粒置入含鈀金屬離子之溶液中, 利用氧化還原作用將鈀金屬附著於零價鐵顆粒表面以形成複合金屬(方 程式 2-15、2-16、2-17)。鈀溶液可用乙醇溶解醋酸鈀 (Pb(C2H3O2)2) (Znang et al., 1998; Lien and Zhang, 1999; Lien and Zhang, 2005),或以純水 溶解六氯鈀酸鉀 (K2PdCl6) (黃與連,2007)皆可用以配製鈀鐵複合金屬。. Fe0. → Fe2+ + 2e-. (2-15). Pd2+ + 2e- →Pd0 ↓. (2-16). Fe0 + Pd2+ → Fe2+ + Pd0 ↓. (2-17). 雖然鈀鐵複合金屬被證實可去除多種含氯有機物,但對於二氯甲烷 等不易分解之含氯污染物效果較不彰,且鈀的價格相對較貴,因此對於 二氯甲烷的去除則不考慮運用。. 2.4.5 複合金屬之比較 根據以上各種複合金屬的回顧,為了去除難以分解之二氯甲烷,同 時考慮環境影響以及成本問題,故選用 Fe/Al 與 Cu/Al 複合金屬,但在過 去的研究證明單純以 Cu/Al 複合金屬處理的效果不彰,因此電子媒介體 也會一併加入反應,而關於電子媒介體會在下一章節中介紹。除了電子 媒介體之外,還合併 Fe/Al、Cu/Al 和 Cu/Fe,依其電位能的高低,形成 最內層為 Al 而最外層為 Cu 的 Cu/Fe/Al 三層複合金屬,使其同時兼具 3 種複合金屬的特性,因此除了 Cu/Al 結合 B12 之外,研究中還會使用 Fe/Al 和 Cu/Fe/Al 作為去除污染物之材料。 28.
(44) 2.5 電子媒介體 單獨的複合金屬去除二氯甲烷的效果可能不佳,因此再另外添加電 子媒介體作為催化劑,以加速其反應。而在連 (1994)的研究說明在還原 條件下,添加電子媒介體 (Electron Mediators, EM),可作為加速反應之 催化劑。根據目前已知的電子攜帶者包括微生物、維生素 B12 (Vitamin B12) 及其衍生物、Corrinoid、TPPS(tetraphenylporphinesulfonate)、胞色素、黃 素、黃素蛋白、葉綠素、血質蛋白、輔酶 F430 (Coenzyme F430)、磷鎢酸鈉 (POMs)等。除了微生物外,皆被視為具催化劑的功能。其中維生素 B12 、 TPPS 和磷鎢酸鈉很常被使用於環境中幫助去除含氯有機物,因此特別這 三種物質進行回顧、探討。. 2.5.1 維生素 B12 基本特性 維生素 B12,化學簡式為 C63H88O14N14PCo,分子量為 1355.38。其結 構如圖 2-9 所示,其分子中心部份之結構由平面大環分子所組成,此結 構稱為 Corrin Ring,中心為一個鈷原子,因此維生素 B12 亦稱為鈷胺素 (Cobalamin) 。 其 軸 向 配 位 基 為 氰 基 (CN) , 因 此 又 稱 為 氰 鈷 胺 素 (Cyanocobalamin)。此軸向配位基(氰基)可被其他配位基取代,例如與 水 形 成 Acquacobalamin (B12a) , 或 被 甲 基 取 代 形 成 甲 基 維 生 素 B12 (Methylcobalamin)等維生素 B12 之衍生物 (連,1994)。. 維生素 B12 依其中心金屬離子鈷的價電子數,可分成三種不同之氧 化還原型態之維生素 B12,分別為三價的維生素 B12、二價還原態的維生 素 B12r 、 一 價 超 還 原 態 的 維 生 素 B12s , 這 三 者 存 在 一 關 聯 式 29.
(45) (Disproportionation)如式 2-18,其平衡常數在酸性及中性條件時,約為 10-14,當 pH 大於 12 時也僅約 10-10 (Blaser and Halpern, 1979; Lexa and Saveant, 1983)。. 2 B12r = B12+B12s. (2-18). 圖 2-9. 維生素 B12 之結構. 維生素 B12 溶解於水中,會呈現紅色透明狀。而當以檸檬酸鈦或硼 氫化鈉等還原劑加以還原為還原態之 B12,則會轉為琥珀色之液體,根據 黃 (2008)的研究以色度圖譜證實其確實會轉換為琥珀色,結果如圖 2-10 所示,其是以 UV 進行全波長掃描,可以發現在操作時間 20 min 內, 隨著時間增加,三價維生素 B12 (波長 361 及 550 nm 處)之特徵波峰 逐漸下降,而波長 390 nm 處則快速增加,而在此過程中顏色會因此轉 30.
(46) 變,所以可由顏色來簡單判斷維生素 B12 之還原態。. 圖 2-10. 維生素 B12 於 1 g/L 硼氫化鈉還原系統中隨時間之變化 (黃,2008). 2.5.2 維生素 B12 之運用 連 (1994)的研究顯示,單獨的檸檬酸鈦在還原系統中,四氯化碳並未 發生轉換,但加入電子攜帶者後反應則明顯的進行。這可說明加入的電 子攜帶者促進了反應的發生,並進一步使四氯化碳發生轉換。就理論與 實驗上的結果,暗示了四氯化碳轉換過程中,存在一個能量障礙,經由 電子攜帶者的作用,降低了能障,達到催化四氯化碳轉換的效果(連, 1994)。其反應如圖 2-11 所示。另外 Wood 等人使用維生素 B12 降解含氯 烷類,發現維生素 B12 與四氯化碳反應生成 Co-CCl3,與氯仿反應生成. 31.
(47) Co-CHCl2,與二氯甲烷反應生成 Co-CH2Cl (Wood et al., 1968)。. 圖 2-11. 維生素 B12 參與反應示意圖,Red 表還原劑,Ox 表氧化劑 (黃, 2009). 除四氯化碳,文獻中也指出四氯乙烯經由檸檬酸鈦-B12 系統,可被還 原為三氯乙烯,並進一步還原降解為二氯乙烯、氯乙烯及乙炔等產物 (McCauley et al., 2005)。還有 Hisaeda et al., (2003)的研究是利用維生素 B12 來處理 DDT 等含氯有機物,請作用的情形則在圖 2-12 顯示。以上皆證 明了維生素 B12 在有還原劑的情況下能還原降解含氯有機物 (RCl)。此 外,除了以還原劑作為電子提供者得以還原電子媒介體外,也可以電化 學的方式進行維生素 B12 之還原 (Ahuja et al., 2004)。. 圖 2-12. B12 用來當作去除含氯有機物之催化劑 (Hisaeda et al., 2003). 32.
(48) 另外在黃(2008)的研究利用 Cu/Al 結合維生素 B12 的方式,利用 Al 提供電子還原維生素 B12,結果能有效的增加去除二氯甲烷的效率,因 此研究以複合金屬結合維生素 B12,讓維生素 B12 達到還原並同時增加去 除效率。雖然維生素 B12 能有效的增加去除效率,但是在傳統中其為溶於 水的狀態,易隨著水流流動而帶走,需要長期的,因此將 B12 固定可以延 長他的使用時間,故經由文獻回顧的結果可以瞭解如何達到固定,Dror et al., (2005)則利用 tetramethyl orthosilicate (TMOS)作為固定劑,因此作為 B12 固定的參考來源。. 2.5.3 TPPS(tetraphenylporphinesulfonate) 吡喀紫質(Porphyrins)是天然產生的、有機的四吡喀大環(tetrapyrrole macrocycles),四吡喀大環是由四吡喀環(four pyrrole-type rings)和次甲基 橋(methine bridges)所組成。吡喀紫質是芳香環含 22 個共軛π電子,其中 18 個有遵守 Huckel’s rule 裡芳香族的規則 4N+2 (n=4),因此有 1 至 2 個 吡喀紫質外圍的雙鍵可以經過添加的過程形成吡喀紫質衍生物,像是 corrins 和 chlorins。吡喀紫質和其衍生物存在於許多生化環境,包含活 細胞、土壤、沉積物、煤、油頁岩、石油等,一般來說在原油或瀝青中 主要和吡喀紫質錯合的金屬為鎳和釩,也有微量的鐵、鈷、鋅、鈦、銅 (Dror and Schlautman, 2003)。. 一般常見脫氯的吡喀紫質為維生素 B12,其他吡喀紫質和衍生物當電 子傳輸介質包含 tetrakis (N-methyl-4-4 pyridiniumyl)porphyrin (TMPyP)、 輔酶素 F430、血紅素、protoporphyrin、uroporphyrin、coproporphyrin 和 33.
(49) hematoporphyrin。此外各種金屬核像是鈷、鐵、鎳、鎂、鉬作為中心離 子的反應金屬吡喀紫質,TPP(Tetraphenyl porphine) 隨著架構中所含的金 屬不同而代表不同的物質,如 Co-TPP、Ni-TPP 和 Fe-TPP 等。吡喀紫質 的類別有以下幾種 TPP、TP-OHP、T(methoxy)P、T(p-toly)P、T(benzoic)P、 TMPyP 和 T(pyridyl)P,其結構式如表 2-3 所示。. 表 2-3 吡喀紫質的資訊 (Dror and Schlautman, 2003). 在 Dror et al., (2005)等人的研究中發現 T(benzoic)P-Co 經過 6 天去除 四氯化碳、三氯乙烯和四氯乙烯有很好的效果,去除效率皆達 99.5%以. 34.
(50) 上,因此研究以 T(benzoic)P 為主之後再結合其他複合金屬去除四氯化碳 和 二 氯 甲 烷 。 T(benzoic)P 為 人 工 合 成 之 異 環 化 合 物 (heterocyclic compound),屬吡喀紫質(porphyrins)之一種,為親水性之電子媒介體 (Kalyanasundaram and Neumann-Spallart, 1982). 2.5.4 磷鎢酸鈉 Polyoxometalates (POMs)被認為是氧化還原的催化劑,在水溶液狀態 需依賴 pH 平衡(Kozhevnikov, 1998),POM 的運用主要會與其他物金屬結 合,金屬的結合包含結合 TiO2,運用於光催化的氧化還原,扮演著催化 劑的角色,由於單純 POM 電子媒介體對於四氯化碳和三氯乙酸的光還原 脫氯是微不足道的,需要與 TiO2 的結合才可提升去除效率,因此在此與 TiO2 作結合,而 POM 在研究中使用的藥品為 HNa2PW12O40 (Kim et al., 2004)。另外還曾利用其膠化包覆零價鐵,達到零價鐵的抗氧化及催化並 加速氧化的反應 (Lee et al., 2008; Keenan and Sedlak, 2008)。. POMs 是一聚合金屬陰離子,其具有催化能力,在 UV 光照射之催化 系統中,能同時降解有機污染物並還原重金屬,但在無光照之環境下, 也能由溶液中之電子捐贈者 (如零價鐵)上攫取電子,生成還原態之 POMs(e-)。而這些 POMs(e-)會進一步與溶氧反應生成 H2O2,使鐵離子與 H2O2 進行 Fenton 作用生成 OH.,讓系統維持氧化能力,其反應方程式 如 2-19 到 2-22(林,2009c)。. 35.
(51) Fe0(s) + 2POM → Fe(II) + 2POM-. (2-19). POM- + O2 → POM + O2-.. (2-20). POM- + O2-. → POM + H2O2. (2-21). Fe(II) + H2O2 → Fe(III) + OH.+ OH-. (2-22). 36.
(52) 2.6 電子媒介體固定方式 過去的研究證實維生素 B12、TPPS 和磷鎢酸鈉等電子媒介體能有效 的幫助含氯有機物的去除,但是由於溶於水,可提供催化的時間較為短 暫,且易被水流帶走,因此將電子媒介體進行固定,而固定的方式有許 多種,主要分成兩大類,一類是利用矽膠固定,例如四甲氧矽(TMOS)或 矽烷胺基(ATPS),而另一類則是將其附著於另一個物體的表面,例如活 性碳、沸石等。以下就針對這兩大類再分成幾個小類,利用矽膠固定的 方式有分為自然乾燥以及加溫進行合成。. 採用自然乾燥的合成方式就是先利用溶膠-凝膠法進行固定,合成方 法以 TMOS、甲醇和電子媒介體的莫爾比為為 1:5:8 進行合成,再放 置 hood 乾燥,達到固定。結果顯示在 6 天的反應之後,去除四氯化碳的 效率是最高的,而三種污染物去除效率最高都可達 99%以上,顯示固定 之後也能發揮很好的去除效率(Dror et al., 2005)。. 經過加熱的合成方式則是在合成過程中除了添加矽膠、酒精和電子 媒介體外還以升高溫度的方式進行合成。Yue et al., (2002) 的研究則是利 用矽膠固定 POM,形成 SiO2-POM,POM 包含 W7O246-、W10O324-、PW12O403和 P2W18O626-,合成過程分別添加混合水 0.2 mol、乙醇 0.02 mol、POM (Na6W7O24 (SW7)、H4W10O32 (SW10)、H3PW12O40 (SPW12)和 H6P2W18O62 (SP2W18)) 1.0×10-4 mol 和四甲氧矽 0.02 mol,經過 80℃攪伴 3 hr,最終 達成固定。固定之後結合 TiO2 和紫外光去除四氯酚,結果顯示 SW10 的. 37.
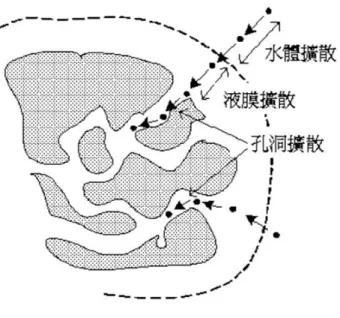
(53) 產氯量和產 CO2 的量都較高,其次是 SP2W18,再次之是 SPW12,SW7 最低,產氯量和產 CO2 的量說明污染物產生脫氯以及用氧化的方式去 除,而產量愈高則是去除效率愈高(Yue et al., 2002)。另外林 (2012a)在修 飾奈米顆粒的過程也是種固定的方式,其利用 2.5 g 的 MNP 粉末置於平 底燒瓶後加入 200 mL 的乙醇以及 10 mL 的矽烷胺基(ATPS),利用冷凝迴 流裝置搭配水浴,定溫 60℃攪拌 7 hr,使其完全分散於乙醇中,達到合 成。. 將電子媒介體吸附於活性碳也是一種固定方式,活性碳是一種多孔 性的含碳物質,其組成物質除了碳元素外,尚含有少量的氫、氮、氧及 灰份,其結構則為碳形成的六環物堆積而成。由於六環碳的不規則排列, 造成了活性碳多微孔體積及高表面積的特性。它具有高度發展的孔隙構 造,是一種極優良的吸附劑,每克活性碳的吸附面積更相當於八個網球 場之多,而其吸附作用是藉由物理性吸附力與化學性吸附力達成。其用 途相當廣泛,因高吸附能力,因此很常用來作為吸附劑,其主要用於去 除水中/空氣中有機或非極性物質,一般其去除污染物的路徑如圖 2-13 所 示。會先經由水體擴散後液膜擴散,再經由孔洞擴散,最終以表面吸附。 而污染物在液膜中之移動及由活性碳表面傳送至孔隙內部為吸附速度的 限制因子,其中粉狀活性碳因粒徑小,內部況散限制則較小。. 38.
(54) 圖 2-13 溶質在活性碳表面擴散吸附路徑. 活性碳除了當吸附劑,亦會用來作為載體,當運用於污水中的生物 處理,會將活性碳作為載體,讓生物膜生長於表面,達到去除的效果, 將此稱之為生物活性碳,生物活性碳(BAC)技術乃是結合活性碳吸附、生 物膜處理及活性碳生物再生等三重作用優點的廢水處理技術。採用與廢 水吸附特性相符的活性碳,利用活性碳吸附功能,增加污染物質於反應 槽的停留時間,同時促進微生物於活性碳表面形成生物膜,進一步將廢 水中吸附於活性碳顆粒上之殘留污染物質加以分解與再生,達到提升處 理水質與延長活性碳使用時間之目的。生物活性碳可延長原活性碳吸附 飽和時間 10 倍以上,大幅降低操作成本與廢棄活性碳的處理負擔(工業 技術研究院)。另外活性碳也用來結合其他金屬作為固定的催化劑,在丁 (2009)的研究則是利用椰殼含浸氯化銅/硫酸鋅製備成活性碳金屬觸媒以 連續流的方式氧化降解酚,而在 Yuan et al., (2005)的研究則是將 TiO2 固. 39.
(55) 定於活性碳,說明活性碳適合作為載體,能將物質附著於表面,而達到 催化等功能,因此運用活性碳固定電子媒介體是可行的,後續將運用活 性碳固定電子媒介體的方式探討。. 40.
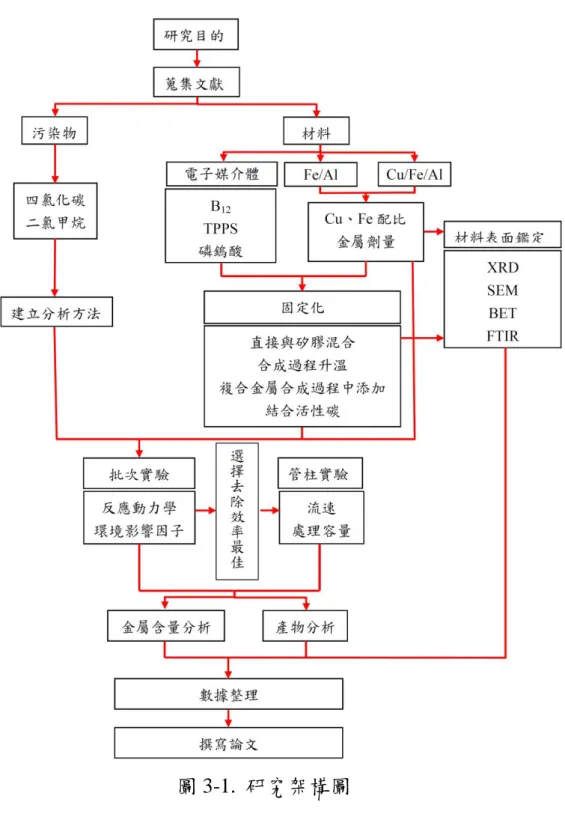
(56) 第三章 材料與研究方法 3.1 研究架構 研究架構如圖 3-1 所示,一開始架構主要分兩大類,分成污染物和 材料,污染物包含四氯化碳和二氯甲烷,經過建立分析方法後與材料反 應,材料部分複合金屬採用 Fe/Al 和 Cu/Fe/Al,複合金屬會確定 Cu、Fe 比例和金屬含量,以及進行材料表面鑑定,另外電子媒介體的部分包含 維生素 B12、TPPS 和磷鎢酸鈉,這些電子媒介體會與複合金屬結合進行 固定化,之後再以批次實驗去除污染物,批次實驗後會再進行管柱實驗, 而測定的項目主要是產物分析,一部分會進行金屬含量分析,最後進行 數據彙整以及討論研究數據。. 41.
(57) 圖 3-1. 研究架構圖. 42.
數據


+7
相關文件
– 有些化合物的電子為奇數個,像NO及NO 2 ,其中N 原子 只有7個電子 ( 含共用 ),稱為自由基 (free radical)。由 於具有未成對電子 (unpaired
要得到真正的分子式,除了需要知道實驗式 之外,還要知道化合物的莫耳質量,化合物
是由兩個相等的碳原子均等地共用兩個鍵結電子 然而 有很多化學鍵結不是完全的離子鍵,也不是完全的共價 鍵,而是介於這兩種極端之間,這種鍵結稱為極性共價 鍵(polar
雖然水是電中性分子,然其具正極區域(氫 原子)和負極區域(氧原子),因此 水是一種極 性溶劑
使金屬離子均勻分散在纖維中而具有抗菌作用。抗菌
六、進口人申請核發「聯合國禁止化學武器公約列管化學物質最終用途保 證書」 ,除繕打「聯合國禁止化學武器公約列管化學物質最終用途保證 書 申 請 書 (APPLICATION FOR END-USE
式中 、 、 為隨物質而定的常數﹐表面張力隨液體性質不同可有很大差別。例 如 20 C 時有機液體苯的表面張力是 28.88
C.轄屬各樂齡學習中心 數超過 25 所者,103 年 度於平面媒體(含報 紙、雜誌)刊出達 12 則 以上,並結合廣播電